Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКОГО ПРЕПАРАТА И БИОЛОГИЧЕСКИ АКТИВНАЯ ДОБАВКА
Вид РИД
Изобретение
Изобретение относится к пищевой промышленности, медицине и может быть использовано в производстве добавки к пище, обладающей профилактическими свойствами при желудочно-кишечных заболеваниях и дисбиотических состояниях, благодаря чему обеспечивается становление экосистемы пищеварительного тракта человека.
Известен способ получения биологически активной добавки (БАД) на основе биомассы Saccharomycetaceae по патенту №2233320 (опубл. 27.07.2004), состоящий в том, что готовят питательную среду, культивируют посевной материал в питательной среде с получением посевной массы, размещают посевную массу на отрубях зерновых культур (пшеничные, ржаные, гречишные) и культивируют до требуемой концентрации клеток Saccharomycetaeceae, получая целевой продукт после инактивации биомассы и высушивания.
Известна биологически активная добавка (БАД) к пище пребиотического действия, по патенту №2233320 (опубл. 27.07.2004), приводящая к коррекции метаболического синдрома, состоящая из биомассы Saccharomyces иммобилизованных на отрубях зерновых культур, содержащей биотрансформированные органические вещества, представленные углеводами, белками, жирами, витаминами, пищевые волокна и неорганические вещества, содержащая отруби зерновых культур, часть которых представляют собой остатки цитоскелета клеточных мембран зерновых культур, образованных в результате дезинтеграции клеточных мембран во время, например, экструдирования, и имеют ячеистую, пористую поверхность не менее 2,0 м2/г, и содержание растворимой клетчатки увеличено больше чем на 1,0 об. %, а нерастворимой клетчатки уменьшено более чем на 3,0 об. % за счет уменьшения гемицеллюлозы на 3,0 об. % и целлюлозы на 1,9 об. %, причем БАД имеет структуру мелкодисперсных частиц размером не более 2-х мм, а биомасса представляет собой цитоскелет Saccharomyces с концентрацией не менее 109-1012 клеток / 1 г, причем биотрансформированные органические вещества составляют не менее 80-90 мас. % от массы отрубей зерновых культур, остальное составляют биотрансформированные неорганические вещества.
Недостатком данного технического решения является то, что данный препарат, полученный способом по патенту №2233320, не стимулирует антагонистическую активность нормофлоры в отношении патогенных и условно-патогенных микроорганизмов. Для его производства применяются микроорганизмы семейства Saccharomycetaceae, которые не свойственны нормальной микрофлоре человека. Способ их получения сложен, т.к. предполагает специальную подготовку питательного субстрата, включающую предварительное увлажнение, стерилизацию или пастеризацию, а также особых условий культивирования - создание анаэробной среды или аэрация стерильным воздухом среды культивирования.
Известен способ получения пищевой добавки по патенту №2136175 (опубл. 10.09.1999), для получения которой используют морковь и капусту, взятые дополнительно к пшеничным отрубям в соотношении 2:1:1. Смесь гомогенизируют, проводят пастеризацию и ферментируют Bifidobacterium adolescentis МС-42, Propionibacterium schermanii Э6, Lactobacillus acidophilus, Lactobacillus plantarum 31, взятыми в отдельности или в смеси в равных количествах.
Известна биологически активная добавка (БАД), полученная по способу получения пищевой добавки по патенту №2136175 (опубл. 10.09.1999).
Недостатком данного технического решения является то, что данный препарат не стимулирует антагонистическую активность нормофлоры в отношении патогенных и условно-патогенных микроорганизмов, не обладает необходимой стандартностью как по составу используемого сырья, так и по совокупности бактериальных компонентов для ферментации субстрата.
Наиболее близким аналогом по составу являются БАД по патенту №2048123 «Способ производства продукта для диетического питания» (опубл. 20.11.1995), включающий обработку растительного сырья биологически активным веществом, в качестве растительного сырья используют активированные пищевые волокна, выделенные путем кислотного гидролиза из отрубей, а в качестве биологически активного вещества препарат, полученный из культуры молочнокислых бактерий Lactobacillus acidophilus, обработку осуществляют при соотношении активированных пищевых волокон и препарата 1:(3-10) мас. ч., препарат получают путем заквашивания обезжиренного молока и/или молочной сыворотки.
Наиболее близким аналогом является биологически активная добавка (БАД), полученная по способу производства продукта для диетического питания» (опубл. 20.11.1995), по патенту №2048123 «Способ производства продукта для диетического питания».
Недостатком данного технического решения является то, что способ получения сложен и не технологичен, т.к. предполагает специальное активирование пищевых волокон, а также то, что данный препарат не стимулирует антагонистическую активность нормофлоры в отношении патогенных и условно-патогенных микроорганизмов.
Предлагаемым изобретением решается задача стимуляции антагонистической активности нормофлоры в отношении патогенных и условно-патогенных микроорганизмов, создания натурального пищевого комплекса на основе растительных компонентов, сочетающих в себе естественные факторы, способствующие деятельности ферментных систем физиологичных штаммов молочнокислых микроорганизмов, обладающего про- и пребиотической, бактериостатической и сорбционной активностью, профилактическими свойствами при желудочно-кишечных заболеваниях, благодаря чему обеспечивается становление экосистемы пищеварительного тракта человека.
Техническим результатом изобретения является получение БАД, являющейся синбиотиком сложного состава - содержащей в качестве компонентов, определяющих основные заявленные свойства, пребиотический (ферментированные отруби) и пробиотический комплекс (клетки, компоненты клеток и активные метаболитные комплексы лактобактерий). Данный технический результат обеспечивает увеличение биомассы за счет увеличения количества лактобактерий на единицу объема целевого продукта с заданными свойствами, позволяет достичь увеличения сорбционной поверхности носителя микроорганизмов, причем процесс идет ускоренно. Данный технический результат обеспечивает быстрое увеличение максимального количества микробных клеток лактобактерий, увеличение микробной массы и качественные изменения в составе целевого продукта, выражаемые в увеличении адсорбционной способности, улучшении биоусвояемости и стимуляции антагонистической активности нормофлоры в отношении патогенных и условно-патогенных микроорганизмов.
Для достижения указанного технического результата в способе, включающем обработку растительного сырья культурой бактерий рода Lactobacillus, инокулят готовят получением взвеси лактобактерий штаммов Lactobacillus plantarum 8Р-А3 и/или Lactobacillus fermentum 90Т-С4 с содержанием клеток не менее 1×108 КОЕ/мл, смешивание инокулята и растительного сырья (субстрат) проводят в объемном соотношении от 1:1 до 1:1,5, инкубирование смеси проводят в течение 15-24 ч при температуре 36-38°С до рН 3,5-5,2, инактивацию ферментирующей массы клеток с одновременным высушиванием ферментированного субстрата проводят при температуре 100°С и атмосферном давлении в течение 1,5-2,0 ч с последующим досушиванием продукта до остаточной влажности 10-15% при температуре 55-70°С. Биологически активная добавка получена по вышеописанному способу.
Отличительными признаками предлагаемого способа от указанного выше известного, наиболее близкого к нему, является то, что инокулят готовят получением взвеси лактобактерий Lactobacillus plantarum 8Р-А3 и/или Lactobacillus fermentum 90Т-С4 с содержанием клеток не менее 1×108 КОЕ/мл, смешивание инокулята и растительного сырья (субстрат) проводят в объемном соотношении от 1:1 до 1:1,5, инкубирование смеси проводят в течение 15-24 ч при температуре 36-38 С до рН 3,5-5,2, инактивацию ферментирующей массы клеток с одновременным высушиванием ферментированного субстрата проводят при температуре 100°С и атмосферном давлении в течение 1,5-2,0 ч с последующим досушиванием продукта до остаточной влажности 10-15% при температуре 55-70°С.
В таблицах, представленных в графической части, поясняющих сущность изобретения, показано следующее:
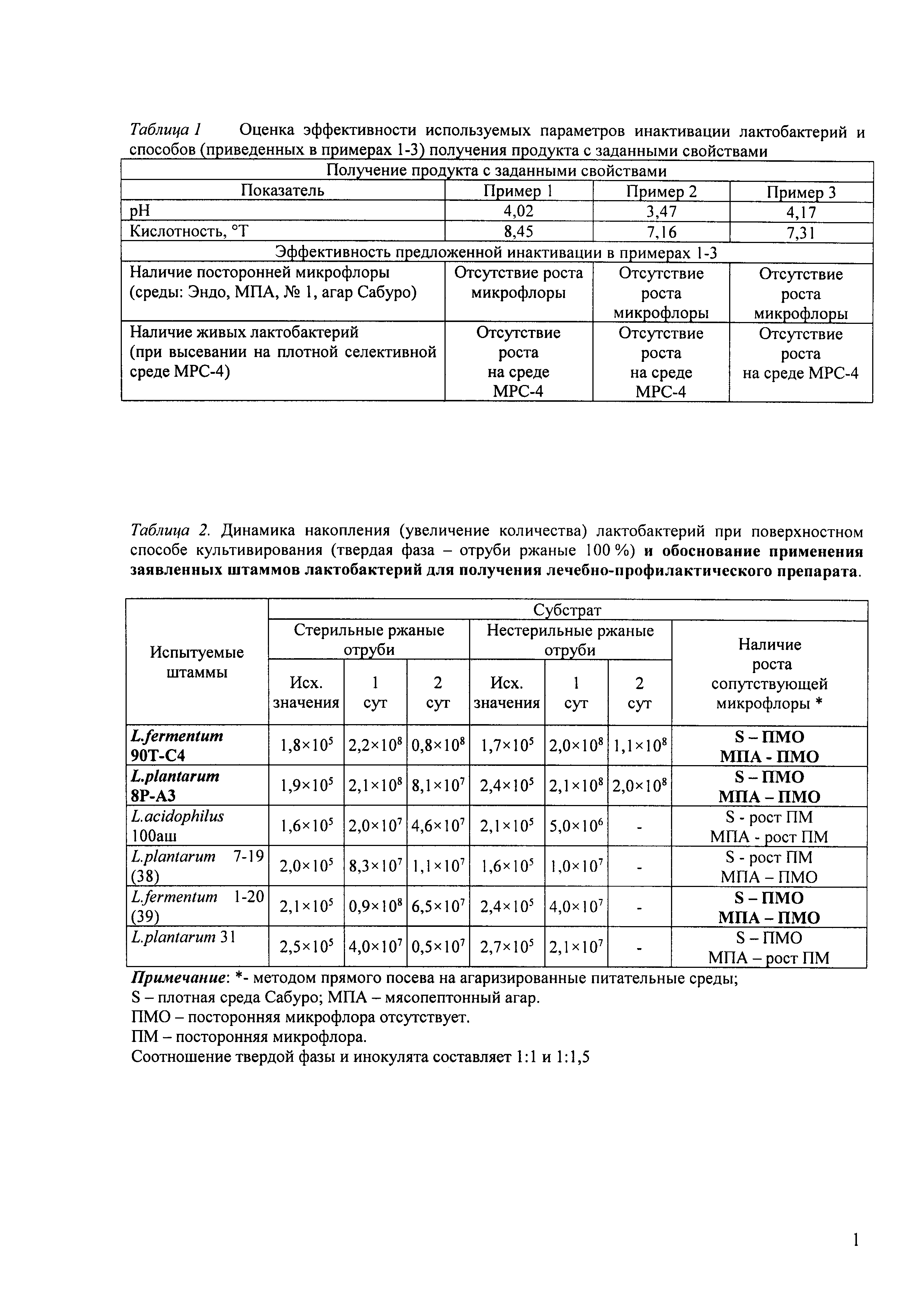
Таблица 1. Оценка эффективности используемых параметров инактивации лактобактерий и способов (приведенных в примерах 1-3) получения продукта с заданными свойствами.
Таблица 2. Динамика накопления (увеличение количества) лактобактерий при поверхностном способе культивирования (твердая фаза - отруби ржаные 100%) и обоснование применения заявленных штаммов лактобактерий для получения профилактического препарата.
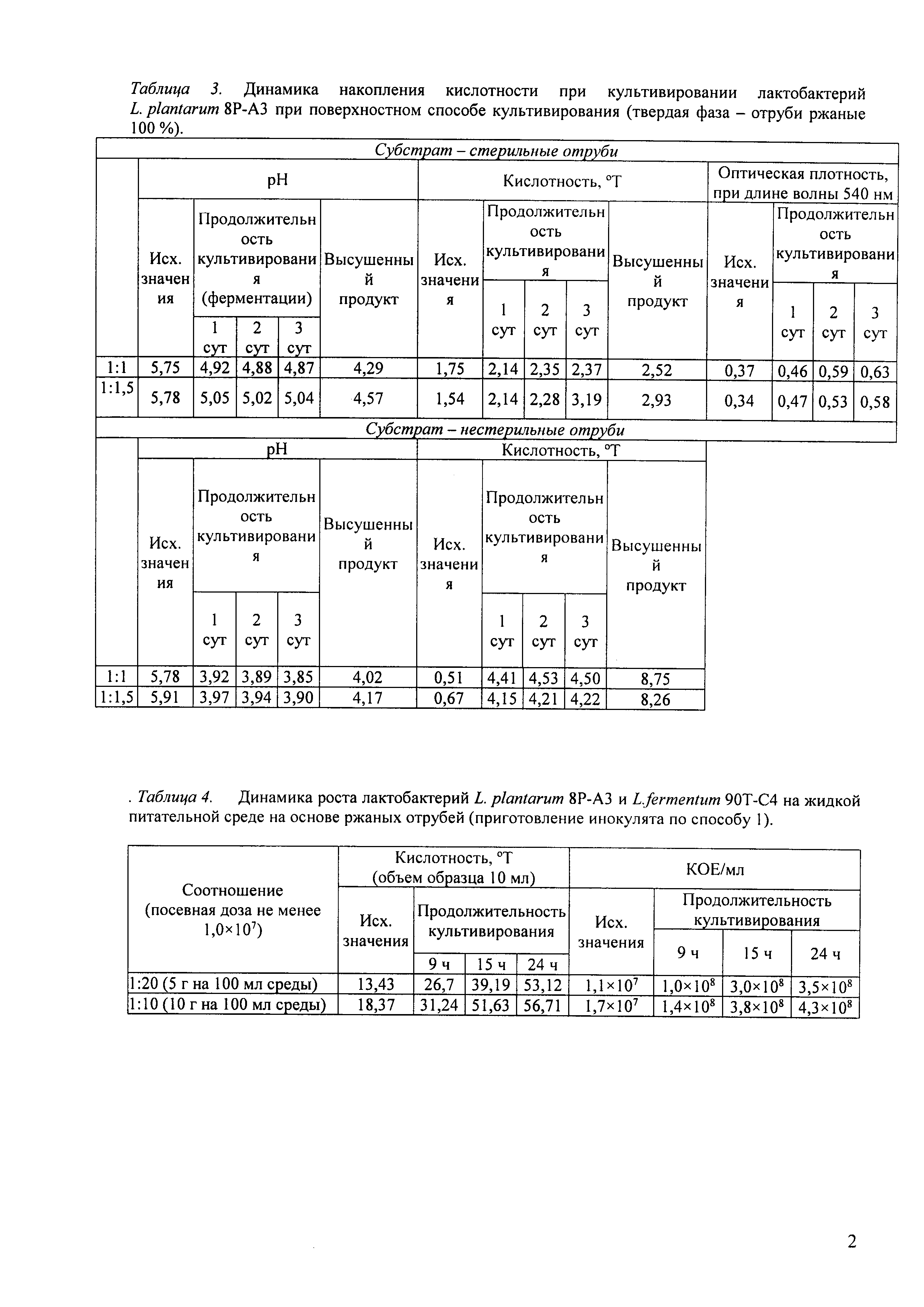
Таблица 3. Динамика накопления кислотности при культивировании лактобактерий L. plantarum 8Р-А3 при поверхностном способе культивирования (твердая фаза - отруби ржаные 100%).
Таблица 4. Динамика роста лактобактерий L. plantarum 8Р-А3 и L. fermentum 90Т-С4 на жидкой питательной среде на основе ржаных отрубей (приготовление инокулята по способу 1).
Таблица 5. Показатели прямой бактериостатической активности в отношении патогенных и условно-патогенных микроорганизмов.
Таблица 6. Показатели стимуляции гетероантагонизма на примере пробиотического штамма L. plantarum 8Р-А3 в отношении патогенных и условно-патогенных микроорганизмов.
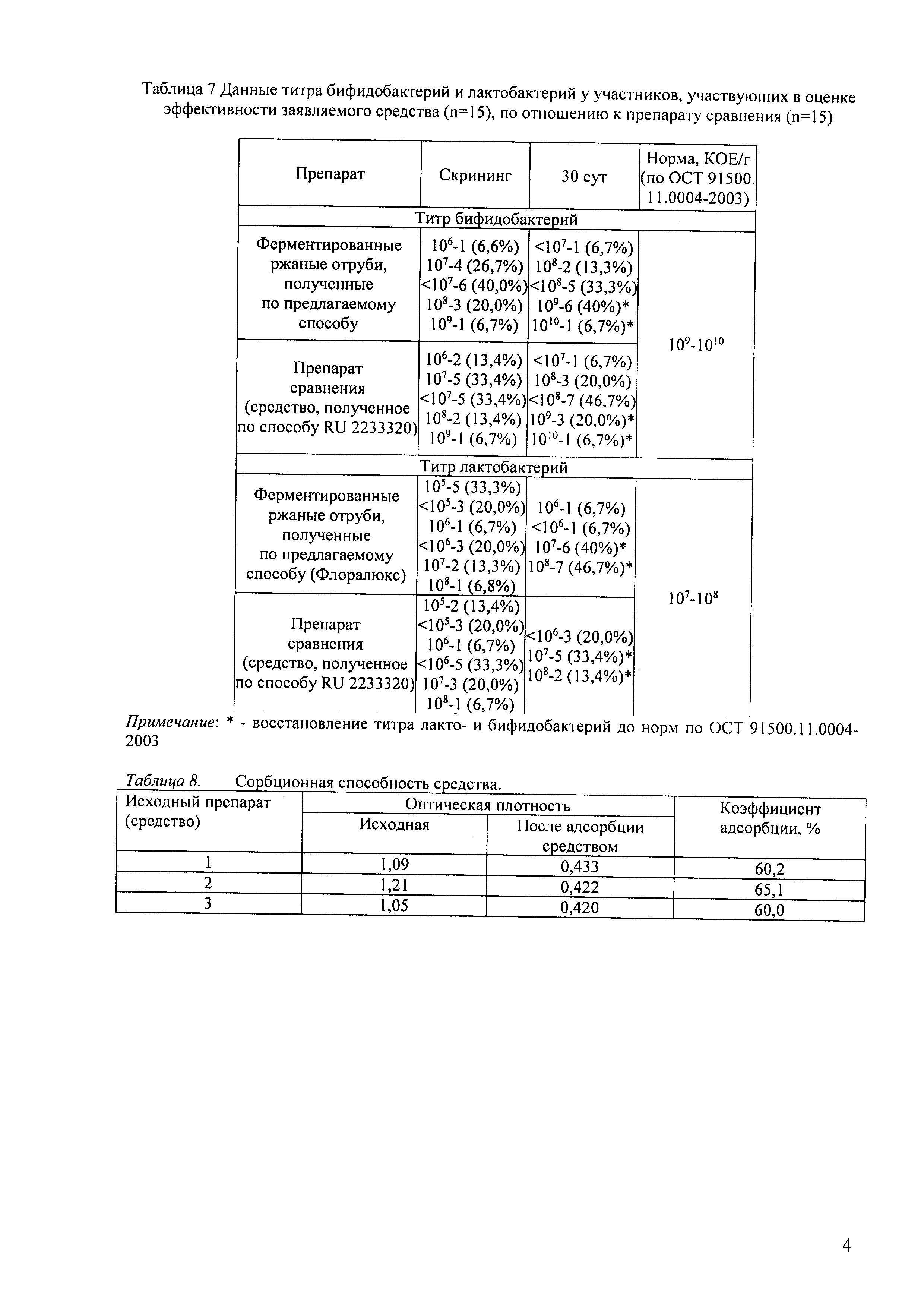
Таблица 7. Данные титра бифидо- и лактобактерий у участников, участвующих в оценке эффективности заявляемого средства (n=15), по отношению к препарату сравнения(n=15).
Таблица 8. Сорбционная способность средства.
Таблица 9. Проведены химические исследования заявляемой биологически-активной добавки на наличие пищевых волокон (в т.ч. растворимых и не растворимых), содержания молочной кислоты и витаминов группы В (B1, В3) (Протокол испытаний №280905/16, Испытательные лаборатории ООО «Лаборатории Весселинг», аттестат аккредитации № RA.RU.021АИ88 от 08.06.2016).
Способ получения - БАД осуществляют следующим образом.
Посевной материал культивируют в жидкой питательной среде (в один этап), в которую вносят посевную массу с общим конечным содержания клеток от 1×106 до 1×107 КОЕ/мл. Среду готовят путем смешивания отрубей с очищенной или питьевой водой в пропорции от 1:10 до 1:20 с последующей пастеризацией (для извлечения питательных компонентов отрубей в объем среды) или без нее. Инкубирование полученной смеси проводят от 15 до 24 ч при температуре от 36 до 38°С. После накопления клеток в посевном материале до концентрации не менее 1×108 КОЕ/мл его смешивают со стерильными или нестерильными ржаными отрубями в соотношении от 1:1 до 1:1,5 и инкубируют в течение от 20 до 24 ч при температуре от 36 до 38°С в закрытых емкостях или иным способом, обеспечивающим влажность ферментируемой массы на уровне 90-100%, до рН 3,5-5,2. Инактивацию лактобактерий проводят термическим способом, включающим нагревание ферментирующей биомассы при (100±1)°С в течение 1,5 ч при атмосферном давлении, насыщенным паром при температуре (121±1)°С - не менее 15 мин, или при температуре (111±1)°С - не менее 30 мин, или инфракрасным излучением (например, при плотности не более 2,0 Вт/см2 с длиной волны 4,3-8,2 мкм). При термической обработке происходит кислотный гидролиз клеток за счет накопленных продуктов обмена, что приводит к положительным изменениям в продукте - накоплению продуктов гидролиза, увеличению аминного азота.
Далее продукт подвергается досушиванию до остаточной влажности 10-15% при температуре 55-70°С. Возможно высушивание массы в конвективных сушилках при температуре 55-70°С в качестве отдельной операции.
В способе также возможно использовать экструдированные ржаные отруби. При этом основным отличием является обеспечение степени пропитывания субстрата посевным материалом на стадии внесения инокулята.
Для получения посевного материала сразу в стерильную очищенную воду или стерильный физиологический раствор 0,9% натрия хлорида возможно добавлять чистую культуру штамма лактобактерий до общего количества клеток не менее 1×108 КОЕ/мл.
В целях получения максимального количества микробных тел в биомассе целевого продукта может применяться подготовленный посевной материал от 1 до 1,5 л на 1 кг экструдированных или нативных нестерильных ржаных отрубей. Полученную смесь перемешивают для однородного распределения и сорбции лактобактерий на поверхности отрубей, культивируют в течение 15-24 ч при температуре от 36 до 38°С в закрытых емкостях, или иным способом, обеспечивающим влажность ферментируемой массы на уровне 90-100%, до достижения рН 3,5-5,2, а инактивацию лактобактерий проводят термическим способом, включающим нагревание ферментированной массы при (100±1)°С в течение 1,5 ч при атмосферном давлении, насыщенным паром при температуре (121±1)°С - не менее 15° мин, или при температуре (111±1)°С - не менее 30 мин, или инфракрасным излучением (например, плотность излучения 0,1-2,0 Вт/см2 с длиной волны 4,3-8,2 мкм). Высушивание возможно проводить одновременно с термической инактивацией, которую производят при температуре 100°С в течение 30 мин с последующим досушиванием до достаточной влажности 10-15% при температуре 55-60°С. Высушивание массы возможно проводить отдельно от стадии инактивации в конвективных сушилках различного типа при температуре 55-70°С.
Кроме того, в качестве исходного сырья (носителя лактобактерий при поверхностном культивировании) можно использовать смесь стерильных или нестерильных ржаных отрубей с пшеничными или гречневыми отрубями от 15 до 50 мас. %. Подготовленные смеси увлажняют посевным материалом (инокулятом) от 1 до 1,5 л на 1 кг смеси отрубей.
Способы подготовки инокулята:
Способ 1. В качестве исходного сырья берут сухие нативные ржаные отруби и питьевую или очищенную воду, подготавливают смесь в соотношении от 1:20 до 1:10 (от 5 г до 10 г на 100 мл воды) отрубей и воды, проводят пастеризацию полученной смеси (нагреванием при 70-100°С в течение 1,5 ч) в полученную среду вносят посевную массу лактобактерий до общего содержания клеток от 1×106 до 1×107 КОЕ/мл, далее проводят культивирование течение 15-24 ч при температуре от 36 до 38°С с получением инокулята, содержащего необходимую концентрацию клеток (не менее 1×108 КОЕ/мл).
Способ 2. В стерильную питьевую или очищенную воду, или стерильный физиологический раствор 0,9% натрия хлорида добавляют чистую культуру L. plantarum 8Р-А3 или L. fermentum 90Т-С4 до общего количества клеток не менее 1×108 КОЕ/мл. В качестве чистой культуры можно использовать лекарственное средство Лактобактерий (ЛС 002098-010714).
Способ 3. Сухие нативные ржаные отруби и питьевую или очищенную воду смешивают в соотношении от 1:20 до 1:10 (от 5 г до 10 г на 100 мл воды) отрубей и воды, в полученную среду вносят посевную массу лактобактерий до общего содержания клеток от 1×106 до 1×107 КОЕ/мл, далее проводят культивирование от 15 до 24 ч при температуре от 36 до 38°С с получением инокулята, содержащего необходимый уровень клеток (не менее 1×108 КОЕ/мл).
Примеры получения средства заявленного состава
Пример 1.
Ржаные отруби (или их смесь с пшеничными или гречневыми отрубями от 15 до 50 мас. %) стерилизуют в автоклаве 30 мин при (111±1)°С, охлаждают до 30-35°С, смешивают с посевным материалом в количестве от 1 до 1,5 л на 1 кг отрубей. Посевная доза - не менее 1×108 КОЕ/мл во всем объеме инокулята. Полученную смесь перемешивают для однородного увлажнения всей массы, инкубирование проводят в течение 24-48 ч при температуре от 36 до 38°С в закрытых емкостях, или иным способом, обеспечивающим влажность ферментируемой массы на уровне 90-100% до достижения рН 3,5-5,2. Ферментированную массу нагревают при (100±1)°С в течение 1,5 ч при атмосферном давлении, при давлении насыщенного пара при температуре (121±1)°С - не менее 15 мин, или при температуре (111±1)°С - не менее 30 мин, или инфракрасным излучением для инактивации бактерий в качестве отдельной операции. Инактивированную массу высушивают при температуре 55-70°С в конвективных сушилках различного типа
Представленные в табл. 2 и 3 данные показывают, что оптимальная продолжительность твердофазного культивирования (ферментации) лежит в интервале от 24 до 48 ч.
Пример 2.
Используют ржаные нестерильные отруби (или их смесь с пшеничными или гречневыми отрубями от 15 до 50 мас. %). Посевной материал готовят по способу 1 или 3 и вносят аналогично примеру 1 и проводят культивирование (ферментацию) в течение 15-36 ч при температуре от 36 до 38°С. Данные табл. 2 и 3 свидетельствуют, что процесс культивирования (ферментация) сопровождается интенсивным закислением среды, а количество клеток лактобактерий в культурах не значительно превышает количества в засеваемой дозе или происходит снижение их количества. Кроме того, достаточно четко видна высокая питательная ценность нестерильных отрубей, на которых активность лактобактерий превышает активность по примеру 1. Инактивация лактобактерий и высушивание продукта - аналогичны примеру 1.
Пример 3.
Используют ржаные стерильные и нестерильные отруби (или их смесь с пшеничными или гречневыми отрубями от 15 до 50 мас. %) ферментированные по примеру 1 или 2, при этом инактивацию бактерий проводят одновременно с высушиванием инактивированной массы при условиях, приведенных в примере 1.
Все приведенные способы получения (изложенных в примерах 1-3) и способы инактивации лактобактерий позволяют получить продукт с заявленными свойствами, с полным отсутствием лактобактерий (продуцентов органических кислот), посторонней микрофлоры и необходимым уровнем биогенных органических кислот (таблица 1).
Сравнительная оценка возможности использования заявленных штаммов лактобактерий, а также данные, показывающие динамику роста лактобактерий и изменение функциональных показателей, представлены в таблицах 2-4.
Данные таблицы 2 показывают, что исходное сырье (стерильные отруби зерновых культур, например ржаные, или их смеси с пшеничными или гречневыми отрубями от 15 до 50 мас. %) является ценным питательным субстратом для лактобактерий. Показана возможность использования стерильных и нестерильных отрубей при использовании штаммов L. fermentum 90Т-С4 или L. plantarum 8Р-А3, которые выгодно отличаются от остальных штаммов и позволяют в значительной степени накапливать достаточное количество клеток и их естественные метаболиты необходимые для получения заявляемого средства. Использование нестерильных отрубей приводит к значительному увеличению активности лактобактерий, что связано с сохранением нативных ростовых свойств питательного субстрата из-за исключения стадии термической обработки, конкуренции лактобактерий за питательный субстрат и стимуляции выработки бактериоцинов.
Оптимальным является соотношение от 1 до 1,5 л инокулята на 1 кг смеси отрубей с влажностью не более 15%, при этом данное соотношение примерно одинаково для нативных или экструдированных отрубей.
В таблице 3 показана закономерности культивирования лактобактерий штамма L. plantarum 8Р-А3 и накопление необходимого количества кислотности при соотношении твердой фазы и инокулята составляет 1:1 и 1:1,5, оптимальная продолжительность ферментации для отрубей с использованием инокулята полученного способом 1 и 3 составляет не более 24 ч, при использовании инокулята, приготовленного по способу 2 - не более 48 ч и позволяет получать продукт с заданными свойствами.
В таблице 4 показана возможность культивирования лактобактерий штаммов L. plantarum 8Р-А3 и L. fermentum 90Т-С4 и накопления необходимой посевной дозы и кислотности для возможности засева и подавления сопутствующей микрофлоры при получении средства. Установлена продолжительность культивирования составляет не более 15-24 ч при температуре от 36 до 38°С, более длительное культивирование посевного материала приводит к снижению количества клеток и их ферментативной активности.
Данные таблиц 2-4 свидетельствуют, что процесс культивирования (ферментации) сопровождается интенсивным закислением среды (накоплением органических кислот, в частности молочной), а количество клеток лактобактерий в культурах, в случае использования стерильных отрубей, не значительно превышает количества в засеваемой дозе или происходит снижение их количества. Кроме того, достаточно четко видна высокая питательная ценность применяемых стерильных и нестерильных отрубей, на которых активность и уровень накопления биомассы заявляемых штаммов лактобактерий L. plantarum 8Р-А3 и L. fermentum 90Т-С4 значительно превышает активность других штаммов, в том числе используемого в способе получения пищевой добавки по RU 2136175. Заявляемые штаммы обладают высокой активностью роста и биохимической активностью при культивировании с применением сред на основе отрубей, что способствует подавлению посторонней микрофлоры и позволяет использовать нестерильный субстрат. В случаях сравниваемых штаммов (L. acidophilus 100 аш, L. plantarum 7-19 (38), L. fermentum 1-20 (39), L. plantarum 31), используемых в таких же условиях и широко применяемых в пищевой и фармацевтической промышленности, не происходит накопление биомассы и органических кислот до необходимого уровня, что приводит к активации посторонней микрофлоры и контаминации среды культивирования и не возможности их применения для получения БАД с заявленными свойствами (сорбционной, антагонистической и пробиотической активностью).
Культуры штаммов L. plantarum 8Р-А3 и L. fermentum 90Т-С4 могут быть получены из ВКПМ или Государственной коллекции промышленных микроорганизмов ФГБУ «НЦЭСМП» Минздрава России или может быть использован препарат Лактобактерий (ЛС 002098-010714).
Внесение инокулята изготовленного по способу 1 и 3 в массу отрубей с последующим однородным перемешиванием, существенно снижает время ферментации (культивирования) за счет обеспечения адекватного питания лактобактерий и их предварительной активации, тогда как инокулят, приготовленный внесением лактобактерий в количестве не менее 1×108 КОЕ/мл в стерильную очищенную воду или физиологический раствор натрия хлорида (способ 2), требует более длительной экспозиции при твердофазном культивировании на отрубях, что связано с адаптацией лактобактерий, регидратированием после лиофильного высушивания. Питательная среда на основе отрубей, применяемая для изготовления инокулята по способу 1 и 3, является оптимальной средой подращивания и активации лактобактерий, что дает возможность использовать в качестве субстрата нестерильные отруби. За счет активного роста клеток и выделения значительного количества метаболитов (как фактора колонизационной резистентности) подавляется контаминантная микрофлора нестерильных отрубей, которая в дальнейшем инактивируется (обезвреживаются) термической стерилизацией вместе с лактобактериями.
Накопление достаточного количества лактобактерий (не менее 1×108 КОЕ/мл) при использовании жидкой питательной среды на основе ржаных отрубей (изготовление инокулята по способу 1 и 3) подтверждают данные табл. 4, применение инокулята, изготовленного по способу 1-3 позволяет получать средство с заявляемыми свойствами.
Заявляемая биологически активная добавка получена на основе растительного сырья, ферментированного молочнокислыми микроорганизмами с образующимися в результате ферментации сырья метаболитами и органическими кислотами, причем, продукты клеточного метаболизма дополнительно обогащают получаемый продукт и в итоге повышают его биологическую ценность.
Предлагаемый способ позволяет получить средство, обладающее следующими свойствами:
1. Бактериостатическая активность средства
Сравнительная оценка показателя прямой бактериостатической активности в отношении патогенных и условно-патогенных микроорганизмов полученного средства в сравнении с препаратом полученным по способу RU 2233320 (таблица 5), была выявлена с помощью метода диффузии в агар (метод колодцев) и свидетельствует об относительно высокой бактериостатической активности полученного препарата превышающей препарат сравнения в среднем на 96,6%.
2. Стимуляция антагонистической активности нормофлоры
Показатель стимуляции антагонистической активности нормофлоры заявляемым средством оценен на примере пробиотического штамма L. plantarum 8Р-А3 в отношении патогенных и условно-патогенных микроорганизмов (таблица 6). Приведенные данные свидетельствуют о стимуляции антагонизма и подавлении роста тест-штаммов, относящихся к патогенным и условно-патогенным бактериям и возможности использования средства для коррекции дисбактериозов, вызванных усиленным ростом патогенной или условно-патогенной флоры.
Представленные данные подтверждают методом «in vitro» наличия у заявляемого препарата пробиотической активности выражаемого в стимуляции роста нормофлоры.
Высокая антагонистическая активность объясняется стимуляцией биохимической активности нормофлоры и наличием бактериоцинов и органических кислот в средстве, накапливающихся в процессе его получения.
3. Пробиотическая активность
Пробиотическая активность изучалась с привлечением добровольцев с дисбактериозом кишечника различной этиологии и степени выраженности возрастом от 14 до 60 лет, участвующих в определении эффективности.
При оценке критериев эффективности установлено, что участники отмечали купирование или уменьшение жалоб, характерных для дисбактериоза кишечника: исчезновение отрыжки, метеоризма, урчания и/или вздутия живота, нормализацию и улучшение стула. Наблюдалась достоверное увеличение скорости восстановления титра лакто- и бифидобактерий до нормального уровня (таблица 7), в случае наличия в рандомизированной группе участников в анализе условно-патогенных микроорганизмов в группе принимающих средство, полученное по предлагаемому способу, наблюдалось достоверное снижение их количества вплоть до отсутствия обнаружения в последующих бактериологических анализах, что подтверждает данные о наличии прямого противомикробного действия и высокой стимуляции антагонистической активности в отношении условно-патогенных микроорганизмов. Клинические наблюдения:
Участник №05
На начало приема препарата беспокоил метеоризм средней степени выраженности, на 5-й день после приема выраженность симптома уменьшилась, на 7-й работа ЖКТ нормализовалась.
Участник №06
В бактериологическом анализе кала на этапе скрининга была обнаружена гемолитическая Е. coli 108 КОЕ/г при начале приема средства самочувствие было прежнее без отрицательной динамики по завершении 7 дней приема средства в бактериологическом анализе кала гемолитическая Е. coli. не обнаружена.
Участник №09
В бактериологическом анализе кала было обнаружено повышенное содержание типичных кишечных палочек 1010 КОЕ/г в бактериологическом анализе кала через 7 дней применения обнаружены типичные кишечные палочки не 104 КОЕ/г, на 14 день приема в анализе не обнаружены.
Участник №11
До приема препарата на этапе скрининга беспокоил жидкий стул, без патологических примесей, до 3 раз в день, без болей в животе. Самостоятельно не лечился, за медицинской помощью не обращался. Симптом прошел поле приема средства в течение 7 дней, стул нормализовался, без патологических примесей.
Участник №14
В бактериологическом анализе кала на этапе скрининга был обнаружен St. aureus 104 КОЕ/г после 7 дней применения средства в бактериологическом анализе кала не обнаружен St. aureus.
Участник №13
В бактериологическом анализе кала на начало приема средства было обнаружено повышенное содержание условно-патогенных энтеробактерий (Klebsiella oxytoca 107 КОЕ\г). После 7 дней применения средства в бактериологическом анализе кала условно-патогенные энтеробактерий не обнаружены.
Таким образом, полученные данные свидетельствуют об эффективности препарата показатели которого превышает препарат сравнения (средство, полученное по способу RU 2233320) в предписанной методике приема, что свидетельствует о возможности применения его в качестве синбиотика (метабиотика), который оказывает благоприятное действие на организм человека за счет прямого подавления условно-патогенной микрофлоры, опосредованной нормализации нарушений микрофлоры и ее функций.
4. Сорбционная активность
Сорбционная активность заявленного препарата изучена на модели 0,15% раствора метиленового синего, который использовался в качестве маркера по химическому строению и молекулярной массе близкому к средне молекулярным токсикантам (билирубин, желчные кислоты, холестерин, мочевина, меркаптен, индол и др.). Установлено, что способ получения средства, а именно использование ферментации заявленными штаммами L. fermentum 90Т-С4 и L. plantarum 8Р-А3 происходит изменение субстрата (обрабатываемых отрубей) под действием ферментов лактобактерий и активных метаболитов, накапливающихся в процессе их жизнедеятельности. Изменяется сама структура отрубей, увеличивается их пористость (активация поверхности) и приводит к увеличению адсорбционной способности готового продукта, что наглядно показано в таблице 8.
Ферментация отрубей в процессе культивирования лактобактериями заявленных штаммов с последующей инактивацией, высушиванием и измельчением, позволяет получить продукт с высокой сорбционной способностью по отношению к низкомолекулярным токсикантам эндогенного и бактериального происхождения и дает возможность использовать средство в качестве энтеросорбента.
5. Влияние на рост перевиваемой прогностически значимой опухоли
На базе лаборатории комбинированной терапии опухолей НИИ «Экспериментальной диагностики и терапии опухолей» ФГБУ «РОНЦ им. Н.Н. Блохина» Минздрава России проведено исследование заявляемого средства по программе для потенциальных модификаторов биологических реакций в онкологии.
Определено влияние при пероральном многократном введении на рост подкожно трансплантированного лимфолейкоза Р388 у мышей и выявлено достоверное торможение роста опухоли на разных сроках наблюдения от 29 до 54% (р<0,05), при этом общее состояние и поведение мышей на фоне и после применения было удовлетворительным без патологических изменений, гибели мышей не отмечено. Установлено отсутствие риска стимуляции роста опухоли при рекомендованной схеме приема в качестве БАД.
Дано заключение в отчете от 20 июля 2016 г. о перспективности изучения препарата в качестве симптоматического средства для коррекции паранеопластического синдрома или токсичности химиотерапии у онкологических пациентов.
Таким образом, вышеуказанные способы, за счет подобранной композиции (используемых отрубей зерновых культур, штаммов лактобактерий и их метаболитов) позволяют получить средство, стимулирующее антагонистическую активность нормофлоры, обладающее про- и пребиотической, бактериостатической и сорбционной активностью, что позволяет его использовать в качестве энтеросорбента при дисбактериозах различной этиологии и устранения интоксикации организма. Наличие сочетанных свойств и особенность оригинального состава позволяет использовать препарат, получаемый по заявленным способам в качестве симптоматического средства для коррекции паранеопластического синдрома или токсичности химиотерапии у онкологических пациентов.
На сегодняшний день отсутствуют препараты, содержащие отруби зерновых культур, биогенную молочную кислоту и инактивированные клетки лактобактерий заявляемых штаммов и обладающих описанными свойствами.
Проведены химические исследования заявляемой биологически активной добавки на наличие пищевых волокон (в т.ч. растворимых и не растворимых), содержания молочной кислоты, витаминов группы В (В1, В3) и свободных незаменимых аминокислот (Протокол испытаний №280905/16, Испытательные лаборатории ООО «Лаборатории Весселинг», аттестат аккредитации № RA.RU.021АИ88 от 08.06.2016 (таблица 9).
Таким образом, заявляемую биологически активную добавку можно считать нутрицевтиком - источником пищевых веществ, применяемых для коррекции химического состава пищи человека. Доказан ее безопасность -отсутствие токсичных элементов, пестицидов, проведены микробиологические исследования, показывающие эффективность применяемых способов инактивации и подавление сопутствующей микрофлоры в процессе ферментации заявленными штаммами лактобактерий (Протокол лабораторных испытаний №15897, ФБУЗ «Центр гигиены и эпидемиологии Пермского края», аттестат аккредитации №RA.RU510375).
На основании полученных данных заявляемая БАД, полученная вышеуказанным способом, была зарегистрирована Роспотребнадзором в качестве биологически активной добавки к пище «Флоралюкс» свидетельство государственной регистрации RU.77.99.11.003.Е.005301.11.16 от 15.11.2016, в качестве источника пищевых волокон и содержащую органические кислоты (биогенную молочную кислоту).