Результат интеллектуальной деятельности: ПРИМЕНЕНИЕ ПРОИЗВОДНОЙ ПИРАЗОЛА В ЛЕЧЕНИИ ОСТРЫХ ПРИСТУПОВ ХРОНИЧЕСКОЙ ОБСТРУКТИВНОЙ БОЛЕЗНИ ЛЕГКИХ
Вид РИД
Изобретение
ОБЛАСТЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Данное изобретение относится к органическим соединениям и их применению в качестве лекарственных средств, конкретнее, к инновационному применению 3-[5-амино-4-(3-цианобензоил) пиразол-1-ил]-N-циклопропил-4-метилбензамида или его фармацевтически приемлемого производного, именно в лечении острых приступов хронической обструктивной болезни легких.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
В патентной заявке WO 2005/009973 описаны различные соединения на основе пиразола и имидазола или их фармацевтически приемлемых производных, имеющие цитокин ингибирующую активность. В заявке раскрыты соединения, которые можно применять для лечения состояний, связанных с p38 киназой, особенно P38α и β киназой, включающих среди прочего астму, аллергические реакции, респираторный дистресс-синдром взрослых и хроническую обструктивную болезнь легких.
В заявке WO 2005/009973 раскрыт 3-[5-амино-4-(3-цианобензоил)-пиразол-1-ил]-N-циклопропил-4-метилбензамид, как пример инновационного ингибитора р38-киназы на основе пиразола, и описаны способы его получения.
В настоящее время обнаружено, что 3-[5-амино-4-(3-цианобензоил)-пиразол-1-ил]-N-циклопропил-4-метилбензамид и его фармацевтически приемлемые производные являются эффективными в лечении острых приступов хронической обструктивной болезни легких.
На удивление, разовая доза, например при пероральном введении, ускоряет восстановление состояния стабилизации заболевания. По существу, данное лечение представляет новый и инновационный тип симптом-модифицирующей терапии, по меньшей мере, в ближайшей перспективе, и при этом обеспечивает значительные преимущества перед существующими поддерживающей терапией и спасательной терапией.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В первом аспекте настоящее изобретение относится к применению 3-[5-амино-4-(3-цианобензоил)-пиразол-1-ил]-N-циклопропил-4-метилбензамида в производстве лекарственных средств для лечения острых приступов хронической обструктивной болезни легких.
Во втором аспекте настоящее изобретение относится к 3-[5-амино-4-(3-цианобензоил)-пиразол-1-ил]-N-циклопропил-4-метилбензамиду или его фармацевтически приемлемому производному для применения в лечении острых приступов хронической обструктивной болезни легких.
В третьем аспекте настоящее изобретение относится к способу лечения острых приступов хронической обструктивной болезни легких, который содержит введение пациенту, нуждающемуся в этом, эффективного количества 3 [5-амино-4-(3-цианобензоил) пиразол-1-ил]-N-циклопропил-4-метилбензамида или его фармацевтически приемлемого производного.
В четвертом аспекте настоящее изобретение относится к лекарственному препарату для перорального введения, который содержит 3-[5-амино-4-(3-цианобензоил)-пиразол-1-ил]-N-циклопропил-4-метилбензамид или его фармацевтически приемлемое производное.
ТЕРМИНЫ
Если не указано иное, все технические и научные термины, использованные в данном документе имеют обычное значение, понятное специалисту в области техники, к которой принадлежит изобретение (изобретения).
Термины, использованные в подробном описании, имеют следующие значения:
Термин "хроническая обструктивная болезнь легких" или "ХОБЛ", использованный в данном документе, является общим термином для поддающейся лечению болезни и характеризуется стойкой бронхиальной обструкцией, которая прогрессирует и связана с развитием хронической воспалительной реакции в дыхательных путях и легких на вредные частицы газов. Характерные симптомы заболевания включают в себя одышку, хронический кашель и хроническое отхождение мокроты.
Термин "острые приступы хронической обструктивной болезни легких" или "ОХОБЛ", использованный в данном документе, означает резкое ухудшение любого из симптомов хронической обструктивной болезни легких, обычно включающий уменьшение воздушного потока и увеличение гиперинфляции легких в сравнении со стабильной ХОБЛ. Обострения в общем оказывают существенное негативное влияние на состояние здоровья пациентов и часто требуют оказания пациенту срочной медицинской помощи в больнице в попытке вернуть пациента в предшествующую стабильную стадию заболевания.
Термин "фармацевтически приемлемое производное", использованный в данном документе, означает производное рассматриваемого терапевтически активного соединения, которое подходит для использования в качестве активного ингредиента лекарственного препарата.
Термин "объем форсированного выдоха за одну секунду" или "ОФВ1", использованный в данном документе, обозначает объем воздуха, выдуваемый с усилием за одну секунду после полного вдоха, который измеряется спирометром. Указанное является способом измерения функции легких или показателем их работы. Средние значения ОФВ1 у здоровых людей зависят в основном от пола и возраста. Значения между 80% и 120% от среднего значения считаются нормальными.
Термин "индекс Борга", использованный в данном документе относится к измерению одышки согласно шкале Борга. 0 по шкале обозначает отсутствие одышки и 10 обозначает максимальную одышку.
Термин "EXACT PRO", использованный в данном документе, относится к качественному способу, используемому для разработки механизма обострения хронического заболевания легких (EXACT), нового инструмента прибора для оценки частоты, тяжести и продолжительности острых приступов хронической обструктивной болезни легких по представленным пациентом результатам (PRO). Метод и его особенности описаны в Leidy et al. in International Society for Pharmacoeconomics and Outcomes Research, vol. 13, no. 8, 2010, pages 965-975. Способ и его разработка описаны в Leidy et al., Am. J. Respir. Crit. Care Med. vol. 183, 2011, pages 323-329, Celli and Vestbo, Am. J. Respir. Crit. Care Med. vol. 183, 2011, pages 287-291, и Jones et al., Chest vol. 139, no. 6, 2011, pages 1388-1394.
Термин "P38β", использованный в данном документе, относится к ферменту, описанному в Han et al. (1995) Biochim. Biopbys. Acta 1265(2-3): 224-7.
Термин "P38β", использованный в данном документе, относится к ферменту, описанному в Jiang et al. (1996) J. Biol. Chem. 271 (30): 17920-6.
В данном описании и в последующей формуле изобретения, если не требуется иного по контексту, слово «содержать», «содержит» или «содержащий», следует понимать означающим включение указанного целого или шагов или группы целых или шагов, но не исключение любого другого целого или шага или группы целых или шагов.
Патент США и патентная заявка, упомянутые в данной патентной заявке, полностью включены в виде ссылки в данном документе для всех целей.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к инновационному применению 3-[5-амино-4-(3-цианобензоил)-пиразол-1-ил]-N-циклопропил-4-метилбензамида или его фармацевтически приемлемого производного, а именно, в лечении острых приступов хронической обструктивной болезни легких.
Вышеизложенное может также быть выражено как: (а) применение 3-[5-амино-4-(3-цианобензоилхлорида) пиразол-1-ил]-N-циклопропил-4-метилбензамида или его фармацевтически приемлемого производного в производстве лекарственного средства для лечения острых приступов хронической обструктивной болезни легких; (b) применение 3-[5-амино-4-(3-циано-бензоил)-пиразол-1-ил]-N-циклопропил-4-метилбензамида или его фармацевтически приемлемого производного в лечении острых приступов хронической обструктивной болезни легких; или (c) способ лечения острых приступов хронической обструктивной болезни легких, который включает введение пациенту, нуждающемуся в лечении, эффективного количества 3-[5-амино-4-(3-цианобензоилхлорида) пиразол-1-ил]-N-циклопропил-4-метилбензамида или его фармацевтически приемлемого производного.
3-[5-амино-4-(3-цианобензоил)-пиразол-1-ил]-N-циклопропил-4-метилбензамид (в данном документе "Соединение А") имеет следующую химическую структуру:
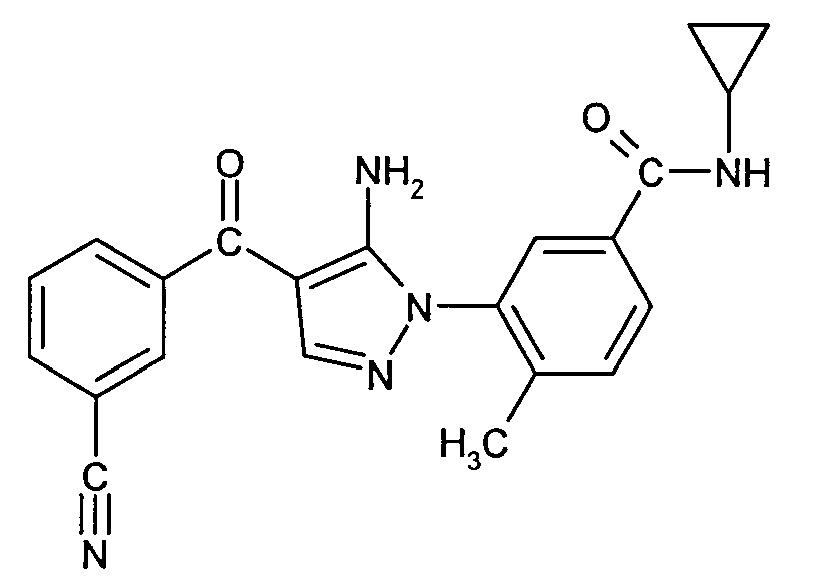
В патентной заявке WO 2005/009973 раскрыты различные соединения на основе пиразола и имидазола или их фармацевтически приемлемых производных, имеющих цитокин ингибирующую активность. Данные соединения включают в себя 3-[5-амино-4-(3-цианобензоил)-пиразол-1-ил]-N-циклопропил-4-метилбензамид.
В заявке WO 2005/009973 раскрыты соединения на основе пиразола и имидазола или фармацевтически приемлемых производных, которые можно использовать для лечения состояний, связанных с P38α и β киназой и для лечения состояний, связанных с р38-киназой, включающих панкреатит (острый или хронический), астму, аллергии, респираторный дистресс-синдром взрослых, хроническую обструктивную болезнь легких, гломерулонефрит, ревматоидный артрит, системную красную волчанку, склеродермию, хронический тиреоидит, болезнь Грейвса, аутоиммунный гастрит, диабет, аутоиммунную гемолитическую анемию, аутоиммунную нейтропению, тромбоцитопению, атопический дерматит, активную форму хронического гепатита, миастению, рассеянный склероз, воспалительное заболевание кишечника, неспецифический язвенный колит, болезнь Крона, псориаз, реакцию ТПХ, воспалительную реакцию, индуцированную эндотоксином, туберкулез, атеросклероз, мышечную дистрофию, кахексию, псориатический артрит, синдром Рейтера, подагру, травматический артрит, краснушный артрит, острый синовит, заболевания поджелудочной железы β-клеток; заболевания, характеризующиеся массивной инфильтрацией нейтрофилов; ревматоидный спондилит, подагрический артрит и другие артриты, церебральную малярию, хроническое воспаление легких, силикоз, легочный саркоидоз, костную резорбцию, отторжение аллотрансплантата, лихорадку и миалгии вследствие инфекции, кахексию на фоне инфекции, миелоидное огрубление, огрубление рубцовой ткани, язвенный колит, пирез, грипп, остеопороз, остеоартрит и множественное повреждение кости, связанное с миеломой, острый миелобластный лейкоз, хронический миелолейкоз, метастатическую меланому, саркому Капоши, множественную миелому, сепсис, септический шок и шигеллез; Болезнь Альцгеймера, болезнь Паркинсона, церебральную ишемию или нейродегенеративные заболевания, вызванные травматическим повреждением; ангиогенные нарушения, включающие в себя твердые опухоли, глазные неоваскулиты и инфантильные гемангиомы; вирусные заболевания, включающие в себя инфекции острого гепатита (включающие в себя гепатит А, гепатит В и гепатит С), ВИЧ-инфекцию и ЦМВ ретинит, СПИД, атипичную пневмонию, ARC или злокачественное развитие и герпес; инсульт, ишемию миокарда, ишемию инсульта сердечных приступов, гипоксию органов, сосудистую гиперплазию, сердечное и почечное реперфузионное повреждение, тромбоз, гипертрофию сердца, тромбин индуцированную агрегацию тромбоцитов, эндотоксемию и/или токсический шоковый синдром, и состояния, связанные с простагландина эндопероксидаза синтазой-2.
Хроническая обструктивная болезнь легких (ХОБЛ) и острые приступы хронической обструктивной болезни легких (ОХОБЛ) являются отличающимися индикаторами или, по меньшей мере, касаются различных состояний заболевания, требующих различного лечения.
ХОБЛ является предотвратимым и поддающимся лечению заболеванием, характеризующимся устойчивым снижением поступления воздуха, которое обычно прогрессирует и связано с повышенной хронической воспалительной реакцией на вредные частицы газов в дыхательных путях и легких. ХОБЛ страдают более 80 миллионов человек во всем мире. В настоящее время болезнь занимает четвертое место в мире среди причин смерти и по прогнозам может занять третье место среди причин смерти к 2030 году. Характерные симптомы заболевания включают в себя одышку, хронический кашель и хроническое отхождение мокроты. Из перечисленных симптомов, одышка обычно является самым заметным и тревожным симптом. Основными патофизиологическими признаками ХОБЛ являются ограничение скорости воздушного потока на выдохе и пузырьки воздуха, которые проявляются как гиперинфляция легких и динамическая гиперинфляция легких во время увеличения вентиляции. Данная гиперинфляция легких влияет на одышку и результирующие ограничения деятельности во время стабилизации заболевания. По мере прогрессирования болезни, тяжесть одышки и других симптомов увеличивается, а качество жизни пациентов снижается.
Лечение ХОБЛ в состоянии стойкого хронического заболевания обычно включает введение пациентом бронходилататора длительного действия, например, β2-агониста длительного действия (LABA) или мускаринового антагониста длительного действия (LAMA) отдельно, или в комбинации с кортикостероидами (ICS). Данные соединения в общем разработаны для ингаляционного введения до четырех раз в день с использованием одного или нескольких ингаляционных устройств. Такое лечение предназначено для поддерживающей терапии, облегчения симптомов и помогает предотвратить острые приступы.
Пациенты с ХОБЛ, особенно ХОБЛ в тяжелой форме, могут испытывать острый приступ болезни, т.е. внезапное и серьезное ухудшение состояния, что требует госпитализации для возврата пациента к стабильному состоянию. Врачи обычно лечат пациентов с острым приступом болезни пероральными стероидами (например, преднизоном) и/или антибиотиками и/или кислородом, но клиническая эффективность, особенно оральных стероидов, в лучшем случае маргинальна. В среднем пациент проводит 8,4 дней в больнице, для восстановления до прежнего стабильного состояния заболевания, хотя данные различны для разных стран вследствие различий в клинической практике и стоимости госпитализации. Иногда восстановление является неполным. Некоторые острые приступы болезни могут оказаться летальными.
В настоящее время обнаружено, что лечение пациентов с ХОБЛ, испытывающих острый приступ болезни, однократной дозой соединения А ускоряет время восстановления. При этом уменьшается время, проведенное в больнице, таким образом уменьшается стресс у пациента и уменьшаются затраты на госпитализацию для пациента, страховщика, системы национального здравоохранения или другого соответствующего плательщика. Кроме того, данное лечение может уменьшить число случаев неэффективного лечения, увеличить вероятность возврата к исходному состоянию, уменьшить или потенциально устранить лечение стероидами и возможно отсрочить наступление следующего острого приступа болезни. По существу, данное лечение представляет новый и инновационный тип терапии, являющейся симптом-модифицирующей, по меньшей мере в ближайшей перспективе, и при этом обеспечивает значительные преимущества перед существующими поддерживающей терапией и экстренной спасательной терапией.
Препарат A можно получать с помощью способов, описанных в заявке WO 2005/009973, содержание которой включено в данном документе в виде ссылки. Конкретно, Препарат А можно получить способами, описанными в примере 52 или примере 161 заявки WO 2005/009973.
Все стереоизомеры Препарата А рассматриваются либо в примеси или в чистой или практически чистой форме. Препарат А в данном документе охватывает все возможные стереоизомеры и их смеси. Препарат охватывает рацемические формы и разрозненные оптические изомеры, имеющие определенную активность. Рацемические формы могут разлагаться физическими способами, например, фракционной кристаллизацией, разделением или кристаллизацией диастереомерных производных или разделением с помощью хиральной колоночной хроматографии. Отдельные оптические изомеры можно получать из рацематов обычными способами, такими как, образование соли с оптически активной кислотой с последующей кристаллизацией. Препарат A может также иметь пролекарственные формы. Любой препарат, который преобразуют в естественных условиях для создания биоактивного агента, представляет собой пролекарство. Различные формы пролекарств являются хорошо известными.
Фармацевтически приемлемые производные Препарата А включают в себя соли, сложные эфиры, енольные эфиры, енольные сложные эфиры, ацетали, кетали, ортоэфиры, гемиацетали, гемикетали, кислоты, основания, сольваты, гидраты или пролекарства. Такие производные может легко получить специалист в данной области известными способами. Полученные соединения могут вводиться животным или людям без существенных токсических эффектов и являются либо фармацевтически активными или пролекарствами. Фармацевтически приемлемые соли включают, кроме прочего, соли аминов, такие как N,N'-дибензилэтилендиамин, хлорпрокаин, холин, аммиак, диэтаноламин и другие гидроксиалкиламины, этилендиамин, N-метилглюкамин, прокаин, N-бензилфенетиламин, I-пара-хлорбензил-2-пирролидин-1'илметил-бензимидазол, диэтиламин и другие алкиламины, пиперазин и трис (гидроксиметил)аминометан; соли щелочных металлов, таких как, без ограничения этим, литий, калий, натрий; соли щелочноземельных металлов, таких как, без ограничения этим, барий, кальций и магний; соли переходных металлов, таких как, без ограничения этим, цинк; и другие соли металлов, такие как, без ограничения этим, фосфаты и динатрийфосфаты; а также включают, без ограничения этим, нитраты, бораты, метансульфонаты, бензолсульфонаты, толуолсульфонаты, соли минеральных кислот, такие как, без ограничения этим, гидрохлориды, гидробромиды, гидроиодиды и сульфаты; и соли органических кислот, такие как, в частности, ацетаты, трифторацетаты, оксалаты, бензоаты, салицилаты, малеаты, лактаты, малаты, тартраты, цитраты, аскорбаты, сукцинаты, бутираты, валераты и фумараты. Кроме того, можно формировать цвиттер-ионы ("внутренние соли"). В некоторых вариантах осуществления солевые формы препаратов улучшают скорость растворения препарата и биодоступность при пероральном введении. Фармацевтически приемлемые эфиры включают в себя, кроме прочего, алкил, алкенил, алкинил, арил, гетероарил, аралкил, гетероаралкил, циклоалкил и гетероциклические эфиры кислотных групп, включающие, в частности, карбоновые кислоты, фосфорные кислоты, фосфиновые кислоты, сульфоновые кислоты, сульфиновые кислоты и бороновые кислоты. Фармацевтически приемлемые енольные эфиры, включают в себя, кроме прочего, производные формулы C=C(OR) где R представляет собой водород, алкил, алкенил, алкинил, арил, гетероарил, аралкил, гетероаралкил, циклоалкил или гетероциклил. Фармацевтически приемлемые енольные сложные эфиры включают в себя, кроме прочего, производные формулы C=C(OC(O)R), где R представляет собой водород, алкил, алкенил, алкинил, арил, гетероарил, аралкил, гетероаралкил, циклоалкил или гетероциклил.
Фармацевтически приемлемые сольваты и гидраты представляют собой комплексы соединения с одной или несколькими молекулами растворителя или воды, или от 1 до около 100, или от 1 до около 10, или от одной до около 2, 3 или 4, молекул растворителя или воды.
Препарат А можно изготавливать с возможностью введения любым подходящим способом, например, перорально, например, в форме таблетки или капсулы; парентерально, например, внутривенно; местно на кожу, например, при лечении псориаза; интраназально, например, при лечении сенной лихорадки; или с помощью ингаляции. Такие композиции можно получать с использованием обычных разбавителей или наполнителей и способами, используемыми в галеновых препаратах. Таким образом, пероральные лекарственные формы могут включать в себя таблетки и капсулы. Композиции для местного введения могут принимать форму кремов, мазей, гелей или трансдермальных систем, например пластырей. Композиции для ингаляции могут содержать аэрозольные или другие распыляемые лекарственные формы, а также сухие порошки.
В некоторых предпочтительных вариантах осуществления изобретения, предложен лекарственный препарат для перорального введения, содержащий 3-[5-амино-4-(3-цианобензоил)-пиразол-1-ил]-N-циклопропил-4-метилбензамид или его фармацевтически приемлемое производное.
Дозировки, использованные в практическом применении изобретения должны изменяться, в зависимости, например, от способа введения. В некоторых предпочтительных вариантах осуществления изобретения предложен фармацевтический состав для перорального введения, содержащий от 50 до 100 мг, например от 60 до 90 мг, в том числе 75 мг 3-[5-амино-4-(3-цианобензоил)-пиразол-1-ил]-N-циклопропил-4-метилбензамида или его фармацевтически приемлемого производного.
Дополнительные варианты и признаки изложены частично в приведенном ниже описании, и в частности становятся понятным специалистам в данной области техники при рассмотрении подробного описания, или могут быть изучены при практическом осуществлении изобретения.
Данное изобретение дополнительно иллюстрирует следующий пример, который не должен рассматриваться как ограничение.
ПРИМЕРЫ
ПРИМЕР 1
Диагностическое, рандомизированное, двойным слепым методом, плацебо-контролируемое, многоцентровое исследование для оценки эффективности, безопасности и переносимости однократной дозы 75 мг 3-[5-амино-4-(3-циано-бензоил)-пиразол-1-ил]-N-циклопропил-4-метилбензамида при пероральном введении пациентам, с острым приступом ХОБЛ.
Эффективность, безопасность и переносимость однократной дозы 75 мг 3-[5-амино-4-(3-циано-бензоил)-пиразол-1-ил]-N-циклопропил-4-метилбензамида (препарат А), введенной перорально пациентам с острым приступом ХОБЛ.
Цели исследования были следующими:
Главная цель: оценка эффективности однократной дозы 75 мг препарата А у больных с обострением ХОБЛ, измеряемая по улучшению в ОФВ1 через первые 5 дней лечения по сравнению с плацебо.
Дополнительные задачи: безопасность и переносимость, результаты по сообщению пациентов и время до очередного обострения.
План исследования:
90 пациентов были рандомизированы 1:1:1 на три группы лечения.
Лечение А (n=15)
= Разовая доза 75 мг препарата А в 1-й день + преднизон плацебо Ч 10 дней
Лечение В (n=15)
= Разовая доза плацебо препарата А в 1-й день + преднизон плацебо Ч 10 дней
Лечение С (n=15)
= Разовая доза плацебо препарата А в 1-й день + 40 мг преднизона плацебо Ч 10 дней
Все группы
= Доксициклин 100 мг Ч 10 дней или немакролидный антибиотик в сочетании с назначением антибиотиков местного действия.
Посещение на 3, 5 и 14-й дни и последующие посещения на 30 и 90-й дни. Конец контрольного посещения через 6 месяцев.
Первый промежуточный анализ взят у 45 пациентов в день 5.
Представление данных (во второй промежуточный период) включает всего 91 рандомизированного пациента за 30 дней наблюдения.
Критериями отбора для исследуемой группы были:
- Мужчины/женщины ≤40 до ≤80 лет
- этапы GOLD (глобальная инициатива по хронической обструктивной болезни легких) от 2 до 4
- Курение в анамнезе, по меньшей мере 10 лет по пачке в день
- Исследователь зафиксировал острый приступ ХОБЛ
Критериями исключения для исследуемой группы были:
- рН артериальной крови <7,26 при рандомизации
- История или наличие клинически неконтролируемой недостаточности левых отделов сердца
- Клинические или рентгенологические признаки пневмонии
- Длительная кислородная терапия >15 часов в сутки
- История клинически значительных изменений на ЭКГ
- История или наличие ухудшения функции почек
- Использование макролидных антибиотиков в течение 48 часов рандомизации
Ключевые критерии эффективности:
- Улучшение ОФВ1 по сравнению с начальным в день 5
- Индексы Борга
- EXACT PRO:
Восстановление определяется как снижение индекса EXACT ≥9 баллов по сравнению с максимальным наблюдаемым баллом (MOV: высокий индекс EXACT используя трехдневное скользящее среднее) за 14-дневный период от начала.
Время восстановления
Степень тяжести
Максимальная степень тяжести - самая высокая точная оценка более 30 дней
Общая степень тяжести - площадь под кривой от начала (т.е. день 1) до восстановления/день 30 в зависимости от того, что наступит раньше в пересчете на общий точный индекс.
Длительность обострения (в днях от начала до восстановления/30-й день)
Количество выздоровевших пациентов в день 30
- Неэффективность лечения:
Пациентам, которых лечили кортикостероидами, и которые поступили в больницу с симптомами ХОБЛ, изменили антибиотикотерапию относительно ХОБЛ, или которым, по мнению лечащего врача, необходимо лечение дальнейшего обострения.
Определения:
Исходным является стабильное состояние, устанавливаемое каждые 4 недели, и последние 7 дней 4-й недели используют для установки исходного значения.
Наступление события определяется либо увеличением индекса EXACT на ≥12 точек выше средних точек исходных индексов для 2 последовательных дат, где день 1 из 2 дней служит днем 1 (наступления события), либо увеличением ≥9 точек выше средней базовой линии в течение 3 следующих друг за другом дней, день 1 из 3 дней служит днем 1 (наступления события).
Восстановление определяется как улучшение или уменьшение индекса EXACT по меньшей мере на 9 пунктов от максимального наблюдаемого значения за 14 дней с момента события, что сохраняется в течение 7 дней, используя 3-дневного скользящего среднего.
Продолжительность события определяют: наступление, трехдневное скользящее среднее, максимальное наблюдаемое значение, порог для улучшения и восстановления.
Трехдневное скользящее среднее используется для подсчета суточных колебаний индекса EXACT, которые могут происходить во время обострения (инициируется в день 1 наступления события и заканчивается на день 1 восстановления).
Результаты исследования обобщены в следующих таблицах:
|
Данные результаты показывают, что пациенты, получавшие лечение препаратом А не чаще, чем пациенты из группы, получавшей плацебо или преднизон (пероральный стероид) прекращали участие в исследовании.
|
Данные результаты не показывают различия в демографии между группами
(Группа с преднизоном ОФВ1 р>0,05 по сравнению с группами с препаратом А и плацебо).
|
Данные результаты показывают у пациентов, получавших лечение препаратом А, больше улучшений в ОФВ1 по сравнению с плацебо и преднизоном в День 3.
Изменение ОФВ1 от исходного состояния проанализированы с помощью модели ANCOVA (дисперсионный анализ) для повторных измерений. Расчетное стандартное отклонение между пациентами ~200 мл.
60% пациентов, получавших лечение препаратом А, отреагировали с >100 мл улучшением в День, 3,27% пациентов, получавших лечение с плацебо, отреагировали с >100 мл улучшением в День 3.
|
Данные результаты показывают, что пациенты, получавшие лечение препаратом А, задыхались в среднем меньше, в течение 14 дней, чем пациенты, получавшие лечение преднизоном.
НК является аббревиатурой для метода наименьших квадратов.
Комбинированная конечная точка неэффективности лечения была определена как повторное лечение антибиотиками, пероральными стероидами, смертью, госпитализацией, или лечением, по мнению исследователя, устанавливающим новое обострение. Неэффективность лечения для каждой терапии была следующей:
- Препарат A=0 пациентов
- Плацебо (стандарт медицинской помощи + один антибиотик) = 5 пациентов
- Преднизон = 5 пациентов
Результаты по безопасности приведены в следующей таблице:
|
Данные результаты показали, что введение Препарата А в виде разовой дозы было безопасным и хорошо переносилось. Никаких нежелательных явлений ХОБЛ от Препарата А не наблюдались.
Первичная госпитализация при обострении ХОБЛ на исходном состоянии отмечена в качестве серьезного нежелательного явления (СНЯ). Записаны только последующие поступления на госпитализацию. Таблица 5 показывает только нежелательные явления, испытываемые, по меньшей мере, 2 пациентами в исследовании. Появления сыпи не отмечено. Не отмечено никаких необычных событий или дисбаланса между группами лечения.
Различные признаки и варианты осуществления настоящего изобретения, указанные выше в одних разделах, являются применимыми в других разделах с соответствующими изменениями. Следовательно, признаки, указанные в одном разделе можно комбинировать надлежащим образом с признаками, указанными в других разделах.
Специалисты в данной области техники знают или могут установить, используя стандартные исследования, множество эквивалентов конкретных вариантов изобретения, описанных в данном документе. Такие эквиваленты относятся к объему, определенному прилагаемой формулой изобретения.

