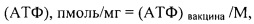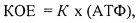Результат интеллектуальной деятельности: СПОСОБ БЫСТРОГО КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СПЕЦИФИЧЕСКОЙ АКТИВНОСТИ ЛИОФИЛИЗИРОВАННОЙ ВАКЦИНЫ БЦЖ
Вид РИД
Изобретение
Настоящее изобретение относится к области биотехнологии, в частности к способам определения специфической активности лиофилизированной вакцины БЦЖ.
Вакцина на основе ослабленного штамма живых лиофилизированных бактерий Mycobacterum bovis (БЦЖ-вакцина) используется для вакцинации против туберкулеза и как иммунотерапевтический агент против рака мочевого пузыря. Одной из ключевых характеристик БЦЖ-вакцины является специфическая активность (жизнеспособность) лиофилизированных бактерий М. bovis BCG, которая характеризуется количеством колониеобразующих единиц в расчете на 1 мл суспензии вакцины (КОЕ/мл) или на 1 мг сухой биомассы (КОЕ/мг). Для характеризации специфической активности используют метод посева разведений суспензии вакцины на плотную питательную среду с последующей инкубацией клеток до образования видимых глазом колоний. Клетки микобактерий, в том числе и бактерий М. bovis BCG, растут медленно, длительность инкубации составляет 3-5 недель, после чего становится возможным завершение испытаний образцов вакцины. Кроме того, КОЕ-тест плохо воспроизводим не только из-за трудностей, связанных с культивированием микобактерий и сложным составом используемой для их роста питательной среды, но и из-за склонности этих организмов к агрегации.
В последнее десятилетие получил распространение альтернативный метод быстрого определения жизнеспособности клеток в БЦЖ-вакцине, основанный на биолюминесцентном измерении содержания внутриклеточного аденозин-5'-трифосфата (АТФ). Содержание внутриклеточного АТФ является основным индикатором жизнеспособности клеток. Биолюминесцентный метод позволяет измерять количество внутриклеточного АТФ в короткие сроки. За счет сокращения времени анализа данный метод позволяет существенно упростить процедуру определения специфической активности готового препарата, а также проводить контроль специфической активности полупродукта на разных этапах производственного цикла.
Известен способ быстрого обнаружения жизнеспособных бактерий в БЦЖ-вакцине [CN 101793832 (A)], включающий следующие этапы: построение градуировочной зависимости в виде уравнения линейной регрессии зависимости сигнала биолюминесценции от концентрации АТФ с использованием стандартных растворов АТФ и биолюминесцентного реагента; растворение лиофилизированной БЦЖ-вакцины в буферном растворе для получения суспензии клеток; проведение экстракции внутриклеточного АТФ путем нагревания суспензии вакцины в буферном растворе, содержащем лизирующие добавки; измерение сигнала биолюминесценции для лизата вакцины с использованием биолюминесцентного реагента; определение концентрации АТФ в суспензии вакцины с использованием уравнения линейной регрессии; подсчет содержания жизнеспособных бактерий в образце БЦЖ-вакцины с использованием ранее полученных данных о содержании АТФ в одной клетке анализируемой вакцины.
Известный способ имеет ряд существенных недостатков. Одним из наиболее существенных является отсутствие стадии удаления внеклеточного АТФ, что ставит под сомнение достоверность получаемых по заявленному методу результатов.
Более близким к заявляемому является АТФ-способ быстрой оценки жизнеспособности препаратов лиофилизированной БЦЖ-вакцины, описанный в статье [Jensen S.E., Hubrechts P., Klein B.M., Haslow K.R. ((Development and validation of an ATP method for rapid estimation of viable units in lyophilized BCG Danish 1331 vaccine», Biologicals, 2008, том 36, c. 308-314]. Ключевой стадией известного способа, которая обеспечивает достижение хорошей корреляции между содержанием внутриклеточного АТФ и КОЕ, является предварительная инкубация реконструированной вакцины в питательной среде в течение 24 ч при 37°C. Затем экстрагируют внутриклеточный АТФ путем нагревания суспензии вакцины в буферном растворе, содержащем лизирующие добавки; измеряют сигнал биолюминесценции полученного экстракта с использованием биолюминесцентного реагента. Концентрацию внутриклеточного АТФ в суспензии вакцины рассчитывают с использованием градуировочной зависимости, полученной при использовании разбавлений АТФ-стандарта с известным содержанием АТФ и биолюминесцентного реагента. Содержание жизнеспособных клеток в вакцине рассчитывают по построенной заранее зависимости содержания внутриклеточного АТФ от величины КОЕ/мл, определенной методом посевов. Общая длительность анализа составляет 36-48 часов.
Известный АТФ-способ имеет ряд недостатков: длительная инкубация в питательной среде сложного состава, экстракция АТФ из клеток вакцины путем инкубирования пробы образца в горячем буферном растворе, содержащем лизирующие добавки, сложная методика расчета содержания внутриклеточного АТФ.
Ближайшим аналогом предлагаемому способу является способ быстрого обнаружения жизнеспособных клеток БЦЖ-вакцины [Kristopher Kolibab, Steven С. Derrick, William R. Jacobs, Sheldon L. Morris. Characterization of an intracellular ATP assay for evaluating the viability of live attenuated mycobacterial vaccine preparations. // Journal of Microbiological Methods, 2012. 90 p. 245-249], включающий реконструкцию лиофилизированной вакцины в растворе Саутона, содержащем сложную композицию минеральный солей, органических добавок и апиразы, с последующей инкубацией в течение 0,5-15 часов при комнатной температуре без перемешивания, в процессе которой происходит удаление внеклеточного АТФ. Далее путем обработки реконструированной вакцины кипящим Tris-ЭДТА буфером высвобождают внутриклеточный АТФ и измеряют его концентрацию с помощью биолюминесцентного реагента. Параллельно определяют количество КОЕ методом посевов разведений и строят зависимость содержания АТФ от величины КОЕ.
Недостатки ближайшего аналога: использование при реконструкции лиофилизированной вакцины сложной смеси растворов Саутона и апиразы может приводить к неполному разрушению внеклеточного АТФ за счет снижения активности апиразы компонентами раствора Саутона, температурный режим и оптимальная длительность стадии реконструкции не установлены, что снижает точность метода, при том что поддержание постоянной температуры является одним из важнейших параметров, определяющих правильное значение содержания внутриклеточного АТФ; использование кипящего Tris-ЭДТА буферного раствора усложняет и удлиняет проведение определения внутриклеточного АТФ.
В изобретении решается задача оптимизации биолюминесцентного метода количественного определения специфической активности лиофилизированной вакцины БЦЖ.
Техническим результатом, достигаемым при использовании изобретения, является сокращение длительности и упрощение процедуры определения специфической активности БЦЖ-вакцины, что способствует снижению трудоемкости и стоимости контроля специфической активности лиофилизированной БЦЖ-вакцины.
Технический результат достигается тем, что в способе быстрого количественного определения специфической активности лиофилизированной БЦЖ-вакцины, включающего реконструкцию лиофилизированной вакцины, удаление внеклеточного АТФ с использованием апиразы, экстракцию внутриклеточного АТФ, определение содержания внутриклеточного АТФ биолюминесцентным методом и расчет специфической активности, реконструкцию лиофилизированной вакцины проводят в физиологическом растворе в течение 15 минут при комнатной температуре без перемешивания, а затем в течение 60 минут при 37°C при перемешивании, удаление внеклеточного АТФ проводят путем инкубации реконструированной вакцины в течение 10 минут с апиразой при конечной концентрации апиразы 0,5-1 ед/мл, экстракцию внутриклеточного АТФ проводят путем добавления 100%-ного ДМСО до конечной его концентрации не менее 80 об. % и инкубации полученного экстракта в течение 1 минуты при комнатной температуре, определение содержания АТФ в полученном экстракте проводят по интенсивности сигнала биолюминесцении для смеси, включающей экстракт реконструированной БЦЖ-вакцины в ДМСО и раствора АТФ-реагента на основе люциферин-люциферазы при их объемном соотношении 1:5, расчет содержания внутриклеточного АТФ в образце реконструированной вакцины проводят, используя значение интенсивности биолюминесцентного сигнала для АТФ-контроля, представляющего собой лиофилизированный препарат с известным содержанием АТФ, по формуле:
 ,
,
где - содержание АТФ в анализируемом образце БЦЖ-вакцины, пмоль;
- содержание АТФ в анализируемом образце БЦЖ-вакцины, пмоль;
 - содержание АТФ в АТФ-контроле, пмоль;
- содержание АТФ в АТФ-контроле, пмоль;
 и
и  - значения интенсивностей сигналов биолюминесценции для экстракта вакцины и АТФ-контроля в ДМСО, расчет удельного содержания внутриклеточного АТФ в анализируемом образце (АТФ, пмоль/мг) проводят с учетом массы лиофилизированной вакцины в анализируемом образце по формуле:
- значения интенсивностей сигналов биолюминесценции для экстракта вакцины и АТФ-контроля в ДМСО, расчет удельного содержания внутриклеточного АТФ в анализируемом образце (АТФ, пмоль/мг) проводят с учетом массы лиофилизированной вакцины в анализируемом образце по формуле:
 ,
,
где M - масса лиофилизированной вакцины,
а расчет специфической активности проводят по формуле:
 ,
,
где КОЕ - специфическая активность вакцины, млн КОЕ/мг;
(АТФ) - удельное содержание АТФ в вакцине, пмоль/мг;
 - предварительно определенный для данного штамма БЦЖ-вакцины коэффициент пропорциональности между удельным содержанием АТФ и специфической активностью, измеренной методом посевов.
- предварительно определенный для данного штамма БЦЖ-вакцины коэффициент пропорциональности между удельным содержанием АТФ и специфической активностью, измеренной методом посевов.
Предлагаемый способ осуществляют следующим образом.
Предлагаемый способ быстрого количественного определения специфической активности лиофилизированной БЦЖ-вакцины включает несколько стадий: реконструкцию лиофилизированной вакцины, удаление внеклеточного АТФ с использованием апиразы, экстракцию внутриклеточного АТФ, определение содержания внутриклеточного АТФ биолюминесцентным методом и расчет специфической активности.
Для осуществления предлагаемого способа используют флаконы с лиофилизированными биопрепаратами (АТФ-реагент, АТФ-контроль и апиразу) и флаконы с жидкими стерильными препаратами (деионизированной водой, физиологическим раствором (9%-ный водный раствор хлорида натрия, далее, физраствор) и диметилсульфоксидом). Использование реагентов, не требующих длительного приготовления и стерилизации, существенно сокращает длительность и трудоемкость анализа.
Приготовление раствора АТФ-реагента. Во флакон с лиофилизированным АТФ-реагентом медленно вводят 2 мл стерильной воды, выдерживают раствор в течение 10-15 минут без перемешивания, а затем содержимое флакона аккуратно перемешивают до однородности и инкубируют при комнатной температуре в течение 30 мин перед использованием. Получают раствор АТФ-реагента на основе люциферин-люциферазы.
Приготовление раствора АТФ-контроля. Раствор АТФ-контроля готовят непосредственно перед проведением измерения биолюминесценции. Для этого во флакон с лиофилизированным АТФ-контролем вводят 1 мл физраствора, чтобы получить раствор, содержащий ~10 пмоль АТФ (точное содержание АТФ указывается в паспорте АТФ-контроля). Для измерения биолюминесценции АТФ-контроля в две пробирки вносят по 100 мкл раствора АТФ-контроля в физрастворе, в каждую пробирку добавляют по 20 мкл физраствора и по 1 мл ДМСО и перемешивают. Полученные две пробы раствора АТФ-контроля в ДМСО можно хранить не более 4 часов при комнатной температуре.
Приготовление раствора апиразы. Во флакон с лиофилизированной апиразой вносят 130 мкл физраствора и получают раствор апиразы с концентрацией 5 ед/мл.
Для проведения реконструкции ампулу с сухой лиофилизированной БЦЖ-вакциной вскрывают, вводят в нее 1 мл физраствора, выдерживают в течение 15 мин при комнатной температуре без перемешивания, затем в течение 60 мин при 37°C в термостатируемой качалке при перемешивании, после чего охлаждают полученную суспензию вакцины до комнатной температуры в течение 3-5 минут.
Из каждой ампулы с суспензией реконструированной вакцины отбирают по две пробы объемом 100 мкл и вносят в две пробирки, содержащие по 20 мкл раствора апиразы. Пробы инкубируют в течение 10 мин при конечной концентрации апиразы 0,5-1 ед./мл при комнатной температуре для разрушения апиразой внеклеточного АТФ.
Для экстракции внутриклеточного АТФ к одной пробе с суспензией реконструированной вакцины добавляют 1 мл ДМСО, перемешивают, через минуту отбирают 20 мкл экстракта вакцины в ДМСО, помещают в кювету люминометра, добавляют 100 мкл раствора АТФ-реагента, быстро перемешивают и измеряют сигнал биолюминесценции на люминометре. Те же процедуры экстракции и измерения сигнала биолюминесценции повторяют для второй пробы и рассчитывают среднее арифметическое для двух проб одного и того же образца вакцины,  .
.
АТФ-контроль, как и вакцину, реконструируют в 1 мл физиологического раствора. В две пробирки отбирают по 100 мкл раствора АТФ-контроля, добавляют по 20 мкл физиологического раствора (вместо апиразы) и по 1 мл ДМСО, перемешивают и определяют сигнал биолюминесценции для АТФ-контроля аналогично определению сигнала биолюминесценции для суспензии реконструированной вакцины. Среднее арифметическое значение сигналов биолюминесценции для двух проб АТФ-контроля  используют для расчета содержания внутриклеточного АТФ в образце лиофилизированной вакцины по формуле (1).
используют для расчета содержания внутриклеточного АТФ в образце лиофилизированной вакцины по формуле (1).

где  - содержание АТФ в вакцине, пмоль;
- содержание АТФ в вакцине, пмоль;
 - содержание АТФ в АТФ-контроле, пмоль;
- содержание АТФ в АТФ-контроле, пмоль;
 - среднее значение интенсивности сигнала биолюминесценции для вакцины (усл.ед.);
- среднее значение интенсивности сигнала биолюминесценции для вакцины (усл.ед.);
 - среднее значение интенсивности сигнала биолюминесценции для АТФ-контроля (усл.ед.).
- среднее значение интенсивности сигнала биолюминесценции для АТФ-контроля (усл.ед.).
Значение  , пмоль, характеризует содержание АТФ в одной проанализированной ампуле вакцины. Используя известное значение массы вакцины в ампуле, рассчитывают удельное содержание АТФ в 1 мг массы вакцины по формуле (2)
, пмоль, характеризует содержание АТФ в одной проанализированной ампуле вакцины. Используя известное значение массы вакцины в ампуле, рассчитывают удельное содержание АТФ в 1 мг массы вакцины по формуле (2)
 ,
,
где (АТФ), пикомоль/мг - содержание АТФ на 1 мг вакцины;
 - содержание АТФ в вакцине, пмоль (в одной ампуле);
- содержание АТФ в вакцине, пмоль (в одной ампуле);
M - масса вакцины, мг (в одной ампуле).
Расчет специфической активности лиофилизированной вакцины проводят по формуле (3):

где КОЕ - специфическая активность вакцины, млн КОЕ/мг;
(АТФ) - содержание АТФ в вакцине, пмоль/мг;
 - предварительно определенный для данного штамма БЦЖ-вакцины коэффициент пропорциональности между содержанием внутриклеточного АТФ и его специфической активностью, измеренной методом посевов.
- предварительно определенный для данного штамма БЦЖ-вакцины коэффициент пропорциональности между содержанием внутриклеточного АТФ и его специфической активностью, измеренной методом посевов.
Коэффициент пропорциональности  получают предварительно при сопоставлении экспериментально полученных данных по специфической активности (млн КОЕ/мг), измеренных методом посевов, и данных по содержанию внутриклеточного АТФ (пмоль/мг), измеренных биолюминесцентным методом, для стандартных образцов анализируемой лиофилизированной БЦЖ-вакцины.
получают предварительно при сопоставлении экспериментально полученных данных по специфической активности (млн КОЕ/мг), измеренных методом посевов, и данных по содержанию внутриклеточного АТФ (пмоль/мг), измеренных биолюминесцентным методом, для стандартных образцов анализируемой лиофилизированной БЦЖ-вакцины.
Ниже приведены конкретные примеры выполнения предлагаемого способа.
Пример 1. Определение специфической активности лиофилизированной вакцины по содержанию внутриклеточного АТФ
Приготовление раствора АТФ-реагента. Во флакон с лиофилизированным АТФ-реагентом (ТУ 2639-001-72144176-2010) медленно вводят 2 мл стерильной воды, выдерживают раствор в течение 10-15 минут без перемешивания, а затем содержимое флакона аккуратно перемешивают до однородности и инкубируют при комнатной температуре в течение 30 мин перед использованием. В процессе работы флакон с раствором АТФ-реагента хранят при комнатной температуре в течение рабочего дня.
Приготовление раствора АТФ-контроля. Во флакон с лиофилизированным АТФ-контролем (ТУ 2639-002-72144176-2010) вводят 1 мл физраствора, получают раствор, содержащий 7,5 пмоль АТФ (содержание АТФ, указанное в паспорте АТФ-контроля). В две пробирки вносят по 100 мкл раствора АТФ-контроля в физиологическом растворе, в каждую пробирку добавляют по 20 мкл физиологического раствора и по 1 мл ДМСО и перемешивают. Полученные две пробы раствора АТФ-контроля в ДМСО хранят не более 4 часов при комнатной температуре.
Приготовление раствора апиразы. Во флакон с лиофилизированной апиразой вносят 130 мкл физиологического раствора и получают раствор апиразы с концентрацией 5 ед./мл. Раствор апиразы хранят при комнатной температуре не более 4 часов.
Измерение сигнала биолюминесценции для АТФ-контроля  . В кювету люминометра вносят 20 мкл раствора АТФ-контроля в ДМСО из первой пробы, добавляют 100 мкл раствора АТФ-реагента, быстро перемешивают и регистрируют сигнал биолюминесценции на люминометре, заносят в таблицу (повтор 1). Повторяют тот же эксперимент еще с одной порцией раствора АТФ-контроля из пробы №1 (повтор 2). Находят среднее арифметическое значение сигнала биолюминесценции для двух повторов. Находят среднее значение сигнала биолюминесценции для пробы №1, заносят в таблицу 1. Проводят аналогичные измерения с пробой №2 АТФ-контроля, находят среднее значение сигнала биолюминесценции для пробы №2. Среднее значение для двух проб используют как
. В кювету люминометра вносят 20 мкл раствора АТФ-контроля в ДМСО из первой пробы, добавляют 100 мкл раствора АТФ-реагента, быстро перемешивают и регистрируют сигнал биолюминесценции на люминометре, заносят в таблицу (повтор 1). Повторяют тот же эксперимент еще с одной порцией раствора АТФ-контроля из пробы №1 (повтор 2). Находят среднее арифметическое значение сигнала биолюминесценции для двух повторов. Находят среднее значение сигнала биолюминесценции для пробы №1, заносят в таблицу 1. Проводят аналогичные измерения с пробой №2 АТФ-контроля, находят среднее значение сигнала биолюминесценции для пробы №2. Среднее значение для двух проб используют как  при расчете концентрации внутриклеточного АТФ в образце вакцины.
при расчете концентрации внутриклеточного АТФ в образце вакцины.

Проведение испытаний вакцины. Отбирают для анализа три ампулы из одной и той же партии лиофилизированной БЦЖ-вакцины, маркируют их (ампулы №1-3). Ампулы вскрывают, не допуская попадания стекла внутрь, добавляют в них по 1 мл стерильного физраствора, закрывают сверху фольгой, предварительно протертой спиртом, инкубируют 15 мин при комнатной температуре без перемешивания, затем в течение одного часа при 37°C в термостатируемой качалке при перемешивании (250 об/мин). Через 1 час инкубации ампулы извлекают из качалки, охлаждают на воздухе до комнатной температуры в течение 3-5 минут. В шесть пробирок вносят по 20 мкл раствора апиразы (активность 5 ед./мл). Из каждой ампулы с суспензией реконструированной вакцины отбирают по две пробы объемом 100 мкл и добавляют их в две пробирки с апиразой, аккуратно перемешивают и инкубируют при комнатной температуре в течение 10 мин без перемешивания.
В первую пробирку (проба №1) с суспензией вакцины, обработанной апиразой, добавляют 1 мл ДМСО, перемешивают, инкубируют в течение 1 минуты, отбирают 20 мкл полученного экстракта вакцины в ДМСО, помещают в кювету люминометра, добавляют 100 мкл раствора АТФ-реагента, быстро перемешивают, измеряют сигнал биолюминесценции и вносят его величину в таблицу 2. Повторяют измерения с новой порцией экстракта из той же пробы №1 и находят среднее арифметическое для пробы №1. Аналогичным образом последовательно проводят измерения для пробы №2 из той же ампулы вакцины. Полученные результаты измерений вносят в таблицу 2 в колонки для пробы 2.

Затем находят среднее арифметическое для ампулы 1 и вносят в таблицу 3.
Выполняют аналогичные измерения для ампул №2 и №3.
Средние значения сигнала биолюминесценции для каждой ампулы вносят в таблицу 3

Рассчитывают содержание внутриклеточного АТФ в каждой ампуле по формуле (1):
 ,
,
где 7,5 - содержание АТФ-контроля в исходном образце АТФ-контроля (по паспорту);
 - сигнал биолюминесценции для АТФ контроля, усл.ед. (см. Таблицу 1);
- сигнал биолюминесценции для АТФ контроля, усл.ед. (см. Таблицу 1);
 - сигнал биолюминесценции для анализируемой ампулы, усл.ед. (см. Таблицы 2 и 3).
- сигнал биолюминесценции для анализируемой ампулы, усл.ед. (см. Таблицы 2 и 3).
Результаты вносят в Таблицу 3, колонка 4.
Рассчитывают содержание АТФ в 1 мг вакцины по формуле (2), используя известную величину массы вакцины в ампуле (0,5 мг):

M - масса вакцины, мг.
Результаты вносят в Таблицу 3, колонка 6.
Для проанализированного образца вакцины (трех проанализированных ампул) среднее значение содержания внутриклеточного АТФ составляет 40,6 пмоль/мг (Таблица 3, колонка 6, строка 6).
Рассчитывают специфическую активность данного образца вакцины по формуле (3):

Используя раннее полученный коэффициент K=0.36±0,02, имеем
Млн КОЕ/мг = (0,36 ± 0,02) × 40,6, пмоль/мг = (14,6±0,9) млн КОЕ/мг.
Величина специфической активности, определенной экспериментально методом посевов, для данной партии вакцины составляет (14,0±2,1) млн КОЕ/мг.
Сравнение величины специфической активности, полученной экспериментально и рассчитанной по результатам предлагаемого способа, показывает, что эти данные находятся в допустимом интервале определения величины КОЕ.
Пример 2. Определение коэффициента пропорциональности К между содержанием внутриклеточного АТФ (пмоль/мг), измеренным биолюминесцентным методом, и специфической активностью (млн КОЕ/мг), измеренной методом посевов, для анализируемого штамма лиофилизированной БЦЖ-вакцины
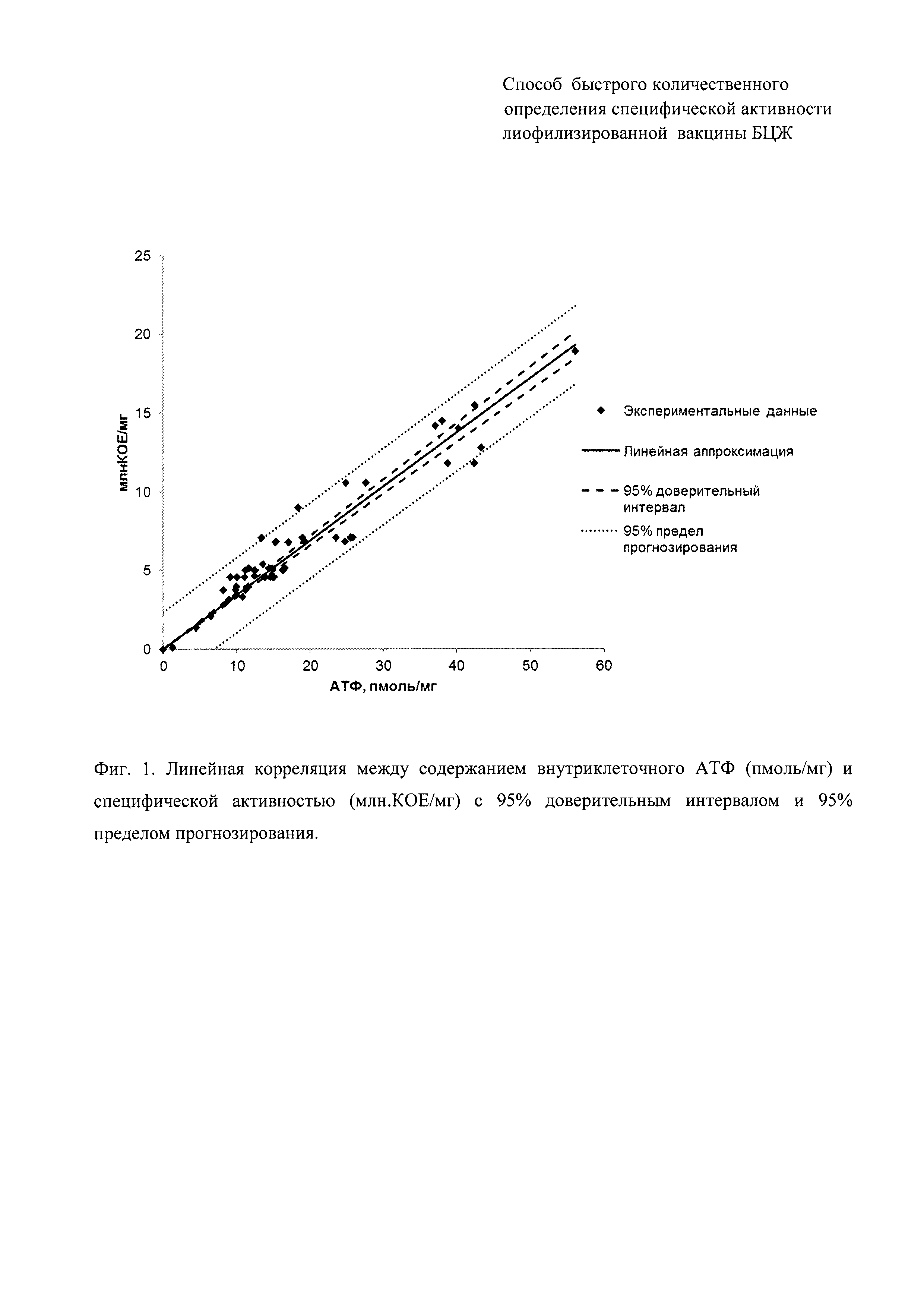
Для 48 образцов лиофилизированной БЦЖ-вакцины были определены специфические активности (млн КОЕ/мг) методом посева и содержание внутриклеточного АТФ (пмоль/мг) - биолюминесцентным методом. В качестве образцов БЦЖ-вакцины с активностью, соответствующей техническим требованиям на продукцию, были использованы препараты БЦЖ-вакцины, изготовленные в 2016 году, а в качестве образцов вакцины с низкой активностью были использованы препараты вакцины, хранившиеся длительное время по окончании срока их годности. На Фиг. 1 показано, что существует линейная зависимость между содержанием внутриклеточного АТФ (пмоль/мг) и специфической активностью (млн КОЕ, мг) с коэффициентом корреляции (R=0.95). Каждая точка соответствует экспериментальным данным для отдельных образцов вакцины и является усредненным результатом 2-3 независимых измерений. Наклон этой зависимости, коэффициент 

На основании существования линейной зависимости в широком интервале специфической активности БЦЖ-вакцины, простое линейное соотношение (формула 3) может быть использовано для расчета специфической активности (млн КОЕ/мг) по экспериментально измеренному значению содержания внутриклеточного АТФ (пмоль/мг):

Предлагаемый способ быстрого количественного определения специфической активности лиофилизированной БЦЖ-вакцины по сравнению с известными позволяет сократить длительность анализа до 2-х часов, упростить и стандартизировать процедуру реконструкции лиофилизированной БЦЖ-вакцины, сократить длительность и трудоемкость метода экстракции внутриклеточного АТФ и метода измерения сигнала биолюминесценции, унифицировать состав реагентов, используемых в анализе.