Результат интеллектуальной деятельности: Способ оценки гиперчувствительности по высвобождению гистамина из лейкоцитов цельной крови
Вид РИД
Изобретение
Изобретение относится к медицине, а именно к аллергологии-иммунологии, патофизиологии, фармакологии и токсикологии, и может быть использовано для определения реактивности лейкоцитов в цельной крови путем определения гистамина, высвобождающегося после ее инкубации со специфическими и неспецифическими высвободителями гистамина, включая лекарственные средства и пищевые продукты.
Методология определения гистамина in vitro после специфической стимуляции позволяет использовать как стандартные, так и лабораторно приготовленные аллергены. Для анализа высвобождения гистамина из базофилов можно использовать также экстракты из пищевых продуктов, лекарств, любых других материалов, подозрительных в отношении их причастности к причинно-значимым агентам, вызывающим гистаминолиберацию.
Методология определения гистамина ценна не только для целей диагностики сенсибилизации к тому или иному аллергену (или выявления прямого токсического действия какой-либо субстанции), но также и для мониторинга эффективности антиаллергического лечения при использовании как фармакологических препаратов, так и аллерген-специфической иммунотерапии. Определение гистамина сегодня является одним из инструментов диагностики аллергических состояний у человека. Существуют несколько методов определения гистамина: радиоизотопный, флуорометрический, иммуноферментный, с помощью газовой и жидкостной масс-спектрометрии. Последние два метода являются наиболее чувствительными и точными. Доступность в последнее время высокоэффективных жидкостных хроматографов (HPLC) с масс-спектрометрическими детекторами позволяет использовать этот высокоточный и высокочувствительный метод для целей аллергодиагностики, оценки функции тучных клеток и базофилов при изучении гиперчувствительности, мониторинга лечения аллергических состояний, включая лечение лекарственной и пищевой аллергии.
Наиболее близким аналогом данного изобретения (прототипом) является способ определения гистамина, высвобождающегося из лейкоцитов крови, так называемым, «фиброглассовым» методом (Glass-microfiber based histamine analysis) [Skov P.S., Mosbech H., Norn S., Weeke В. Sensitive glass microfiber-based histamine analysis for allergy testing in washed blood sells. Allergy, 1985; 40:213-218]. Отличительной особенностью данного способа является использование стекловолоконного матрикса, который помещается (закрепляется) на дно пластикового 96-луночного плейта и который избирательно сорбирует гистамин. Кратко: гепаринизированную кровь в определенном объеме от пациентов с сенсибилизацией к различным аллергенам или от здоровых доноров помещают в лунки 96-луночных «фиброглассовых» плейтов (производства Reference Laboratory, Дания), куда предварительно в дубликатах вносят, согласно выбранной конфигурации, определенный объем разведений аллергенов или других субстанций, положительного (анти-IgE) и отрицательного (только PIPES-буфер) контролей. Также, в зависимости от задач исследования, можно использовать разведения кальциевого ионофора А23187 или вещества 48/80. Далее плейты инкубируют в течение 1 часа при 37°С и после отмывки дистиллированной водой дополнительно инкубируют в течение 30 мин при 37°C с раствором SDS (Sodium Dodecyl Sulfate). После отмывки дистиллированной водой в каждую лунку плейтов добавляют определенное количество раствора орто-фталиевого диальдегида для перевода гистамина, сорбированного на стекловолоконном матриксе, в раствор с последующей его конденсацией. Реакцию останавливают через определенное время добавлением раствора HClO4. Результаты, полученные путем автоматизированного спектрофлуорометрического анализа на приборе "Histareader 501", выражаются в нанограммах гистамина в 1 мл крови (нг/мл). Чувствительность метода составляет 8-10 нг гистамина в мл крови (нг/мл).
Недостатками данного способа определения гистамина, высвобождающегося из лейкоцитов цельной крови и сорбирующегося на стекловолоконном матриксе с последующей его конденсацией для флуорометрического анализа, являются трудоемкость, связанная с многостадийностью и рядом последовательно проводимых химических реакций и физико-химических определений, а также высокая стоимость применяемых химических реактивов. Кроме того, являясь монополистом производства "фиброглассовых" плейтов и прибора для регистрации содержания гистамина (Histareader 501), фирма-производитель (Reference Laboratory, Дания) за последние годы многократно поднимала цены, как на сами "фиброглассовые" плейты, так и на прибор для регистрации, что приводило к существенному удорожанию анализа.
Поэтому задачей данного изобретения являлось создание простого и доступного метода определения реактивности (гиперчувствительности) лейкоцитов периферической крови в ответ на специфические и неспецифические стимуляторы с использованием новейших технологий определения гистамина, таких как высокоэффективная жидкостная хроматография с масс-спектрометрией.
Для решения данной задачи была предложена концепция прямого определения гистамина в надосадке цельной крови после ее инкубации со специфическими и неспецифическими субстанциями.
Техническим результатом данного изобретения является упрощение и удешевление процедуры специфической и неспецифической стимуляции лейкоцитов крови и повышение точности оценки гиперчувствительности за счет прямого количественного определения гистамина, высвобождающегося из лейкоцитов крови.
Представленный технический результат достигается тем, что с помощью способа оценки гиперчувствительности по высвобождению гистамина из лейкоцитов цельной крови, включающего забор в пробирки с гепарином венозной крови у обследуемого человека, центрифугирование крови, замену плазмы буфером, дальнейшую инкубацию аликвот ресуспендированных клеток крови с тестируемыми субстанциями в микроплейте, а также с анти-IgE в качестве положительного контроля и с буфером - отрицательного контроля, с последующим центрифугированием микроплейта, прямым количественным определением гистамина в надосадочной жидкости лунок микроплейта методом обращенно-фазной высокоэффективной жидкостной хроматографии в сочетании с тандемным масс-спектрометрическим детектором и сравнение уровней гистамина, полученных для каждой из тестируемых субстанций, с положительным и отрицательным контролями, и при повышении уровня содержания гистамина в опытном образце по сравнению с отрицательным контролем при наличии реакции в положительном контроле выявляют гиперчувствительность к тестируемой субстанции.
Способ осуществляется поэтапно следующим образом:
1. Венозная кровь от здоровых доноров или от больных аллергией забирается в пробирки с гепарином в необходимом объеме (из расчета 150 мкл крови на один образец для анализа), желательно натощак (кровь может храниться до использования в пробирках с гепарином в горизонтальном положении при комнатной температуре оптимально не более 24 часов).
2. После центрифугирования крови в течение 10 мин при 150 g из пробирки отбирают плазму, замещая ее тем же объемом PIPES буфера, после чего ресуспендируют клетки крови.
3. Пробирку с ресуспендированной кровью и 96-луночный плейт, в каждую лунку которого согласно выбранной конфигурации внесены в объеме 50 мкл разведения аллергенов или испытуемых субстанций, стандарт гистамина, разведения анти-IgE, ионофора А23187 и просто PIPES буфер, преинкубируют, помещают в термостат при 37°С на 15 мин для предварительного нагревания
4. После окончания преинкубации аликвоты ресуспендированной крови в объеме 150 мкл вносят в каждую лунку 96-луночного плейта, где уже содержатся вышеперечисленные ингредиенты, после чего плейт помещают в термостат при 37°С на 1 час.
5. По истечении срока инкубации плейты центрифугируют при 150 g 15 мин, и надосадочную жидкость из каждой лунки напрямую анализируют на содержание гистамина.
6. Анализ образцов надосадочной жидкости на содержание гистамина проводят методом обращенно-фазной высокоэффективной жидкостной хроматографии (HPLC) в сочетании с тандемным масс-спектрометрическим детектором. Объем забираемой пробы (образца для анализа) - 10 мкл. Колонка - Agilent Eclipse XDB-С18 (4,6×150 mm; 5 μm) с предколонкой Agilent Zorbax Eclipse Plus C18 (4,6×50 mm, 5 μm). Температура колонки: 40°С. Предварительно прибор калибруется по различным концентрациям гистамина от 10 до 1000 нг в мл. После калибрования проводится анализ образцов надосадочной жидкости в каждой лунке плейта на содержание гистамина. Примерное время получения результата по содержанию гистамина в образце - 5,1 мин. Результаты выражаются в нанограммах гистамина в 1 мл крови (нг/мл). Предел количественного определения гистамина составляет 10 нг/мл, что сравнимо с ближайшим прототипом - «фиброглассовым» методом. Чувствительность «фиброглассового» метода определения гистамина в цельной крови, основанного на детекции гистамина по его флуоресценции, составляет 8-10 нг/мл. Оценка и сравнение уровней гистамина, полученных для каждого из разведений аллергенов или тестируемых субстанций, проводится после математической обработки на основании значений «площади под кривой» или прямого сравнения количества гистамина при определенных концентрациях тестируемых субстанций.
7. При повышении уровня содержания гистамина в опытном образце по сравнению с отрицательным контролем при наличии реакции в положительном контроле выявляют наличие гиперчувствительности.
Заявленный способ представляет собой новый современный подход для быстрой оценки гиперчувствительности по высвобождению гистамина из лейкоцитов цельной крови, основанный на принципе высокоэффективной жидкостной хроматографии и масс-спектрометрического анализа. Использование стандартных 96-луночных плейтов позволяет анализировать гистамин-высвобождающую активность значительного количества субстанций (аллергенов, лекарственных препаратов, пищевых продуктов, профессиональных вредностей и др.) за счет инкубации с малым количеством крови. Результаты анализа высвобождения гистамина из лейкоцитов периферической крови могут быть использованы для in vitro аллерго-диагностики при оценке степени сенсибилизации к клинически-значимым аллергенам, особенно у детей младшего возраста (в том числе лекарственным препаратам, пищевым аллергенам, профессиональным вредностям), для изучения псевдоаллергических реакций, а также для мониторинга эффективности антиаллергического лечения, включая аллерген-специфическую иммунотерапию.
Краткое описание чертежей
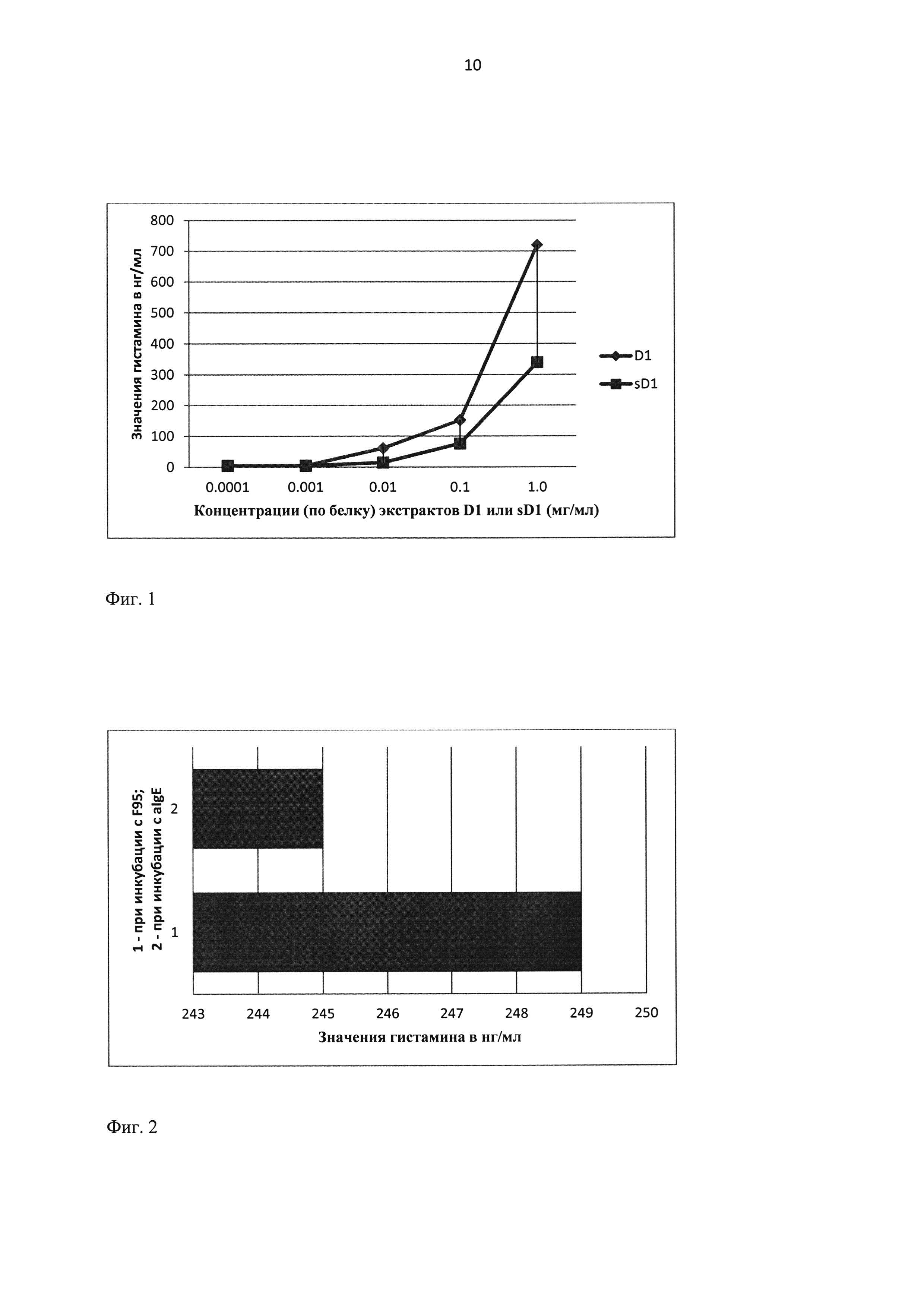
На Фиг. 1 показаны уровни гистамина после инкубации с различными концентрациями (по белку) модифицированного (sD1) и немодифицированного (D1) экстрактов из клещей домашней пыли Dermatophagoides pteronyssinus.
На Фиг. 2 показаны уровни гистамина по показателю ППК (площадь под кривой), высвобождающегося из лейкоцитов крови больного при инкубации с различными концентрациями (по белку) экстракта персика (F95 - Lofarma, Italy) и с разведениями анти-IgE (aIgE - Dako, Denmark).
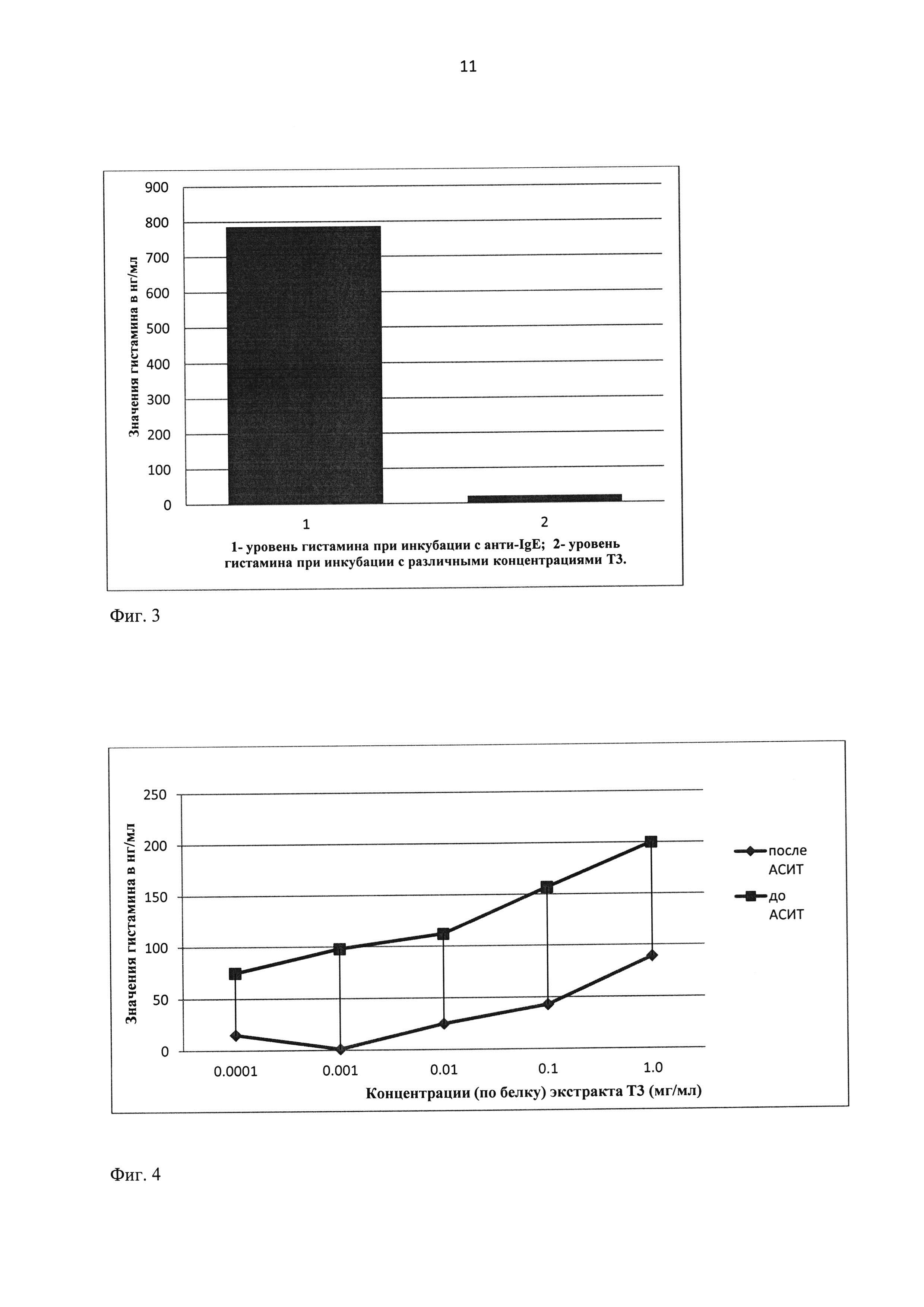
На Фиг. 3 показаны уровни гистамина по показателю ППК (площадь под кривой) у здорового донора (отсутствие сенсибилизации к пыльце березы) при инкубации его крови с разведениями анти-IgE (Dako, Denmark) и с различными концентрациями (по белку) экстракта пыльцы березы (Т3).
На Фиг. 4 показаны уровни гистамина, высвобождающегося из лейкоцитов крови больного А при инкубации с различными концентрациями (по белку) экстракта пыльцы березы (Т3) до и после аллерген-специфической иммунотерапии.
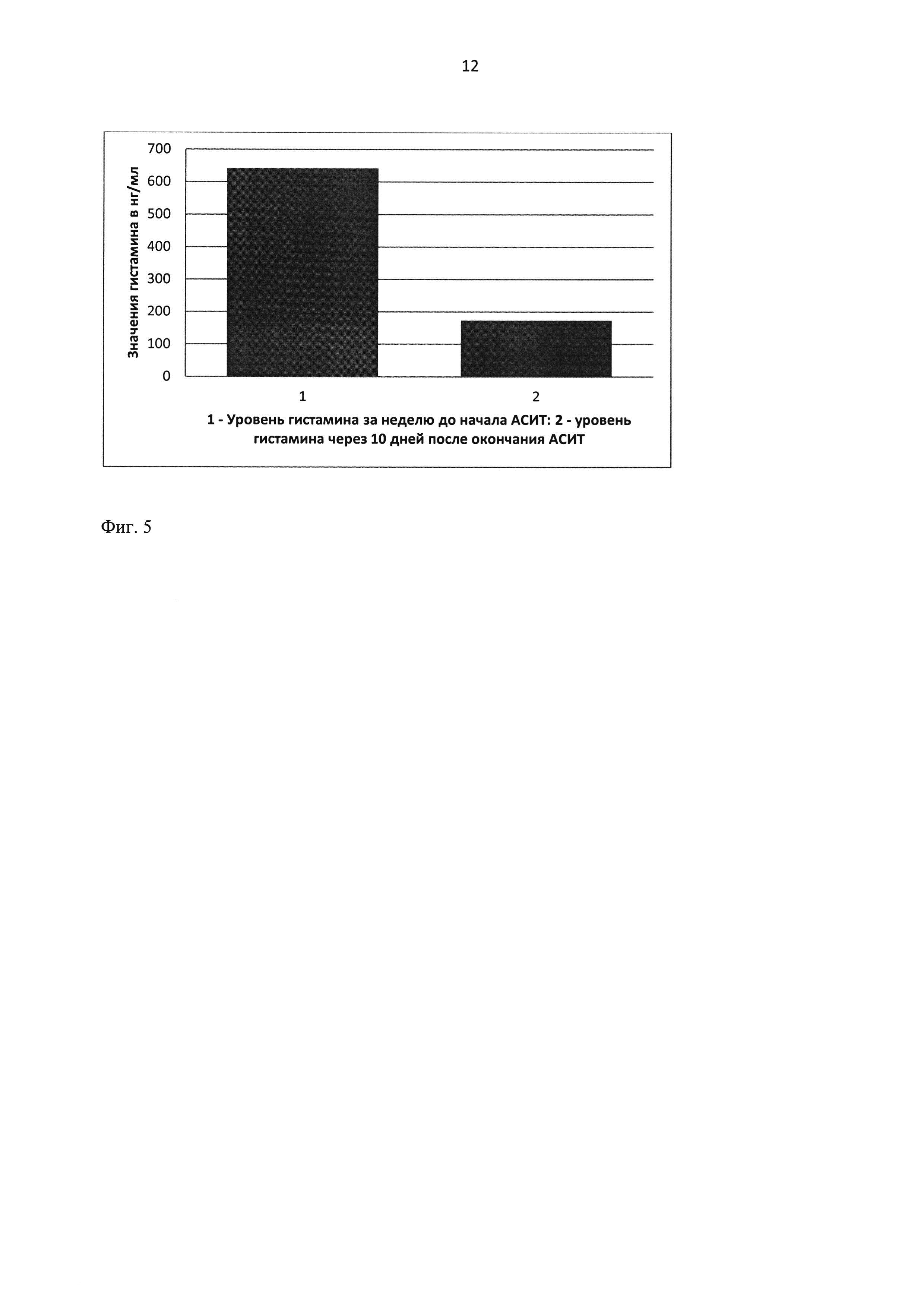
На Фиг. 5 показаны уровни гистамина (по показателю ППК - площади под кривой), высвобождающегося из лейкоцитов крови больного Б до и после аллерген-специфической иммунотерапии.
Пример 1
Экстракт из клещей домашней пыли Dermatophagoides pteronyssinus (D1) был химически модифицирован методом сукцинилирования, в результате чего получен мономерный аллергоид (sD1). Для сравнительной оценки аллергенности модифицированного экстракта sD1 кровь от больного с сенсибилизацией к Dermatophagoides pteronyssinus (Der р) инкубировали с различными концентрациями (по белку) модифицированного (sD1) и немодифицированного (D1) экстрактов.
Показано значительное снижение уровня гистамина, высвобождающегося из лейкоцитов крови сенсибилизированного больного, при ее инкубации с модифицированным экстрактом sD1 в сравнении с немодифицированным D1 (Фиг. 1), что свидетельствует о существенном снижении аллергенности аллергоида sD1.
Пример 2
Больной Р.С.А. - диагноз: оральный аллергический синдром. Уровни аллерген-специфического IgE (Pharmacia UniCap 100, Швеция) к аллергенам: береза (Т3) - >100 кЕдА/л (6 класс); вишня (F242) - 1,62 кЕдА/л (2 класс); персик (Pru р) (F95) - 4,41 кЕдА/л (3 класс).
Проведен анализ высвобождения гистамина из лейкоцитов цельной крови (данные представлены по показателю ППК - "площади под кривой") при ее инкубации с разведениями анти-IgE (aIgE - Dako, Denmark) и с различными концентрациями (по белку) экстракта персика (F95 - Lofarma, Italy). Полученные данные свидетельствуют о наличии корреляции между уровнем гистамина, высвобождающегося из лейкоцитов крови больного при ее инкубации с экстрактом F95, и уровнем анти-Pru p IgE, что является ценным показателем, демонстрирующим возможность диагностики гиперчувствительности к аллергенам (в данном случае к аллергенам персика - Pru р) путем анализа высвобождения гистамиина из лейкоцитов крови (Фиг. 2)
Пример 3
Б.Е.Н. - здоровый донор. Аллергологический анамнез - отрицательный. Сенсибилизация к пыльце деревьев отсутствует. Кожные пробы: береза - (-), ольха - (-), орешник - (-).
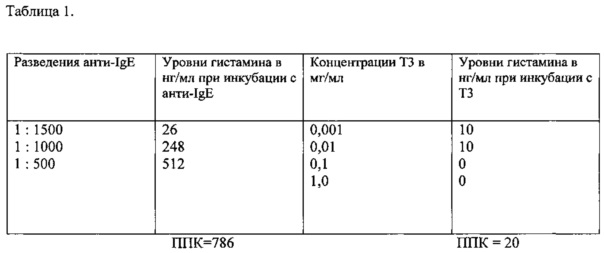
Проведен анализ высвобождения гистамина из лейкоцитов цельной крови (данные представлены по показателю ППК - "площади под кривой") при ее инкубации с разведениями анти-IgE (Dako, Denmark) и с различными концентрациями (по белку) экстракта пыльцы березы (Т3). Полученные данные свидетельствуют о высокой специфичности анализа высвобождения гистамина из лейкоцитов крови (Таблица 1, Фиг. 3).
Пример 4
Больной Т.В.В. - диагноз: бронхиальная астма, атопическая форма, легкое интермиттирующее течение; сенсибилизация к пыльце деревьев и трав. Кожные пробы до проведения аллерген-специфической иммунотерапии (АСИТ): береза ++, ольха +++, орешник +++.
Проведена инъекционная АСИТ смесью водно-солевых экстрактов аллергенов: береза (40%), ольха (30%), орешник (30%). Больной получил 30 инъекций (по одной инъекции ежедневно). Суммарная доза по трем аллергенам, полученная в ходе АСИТ, составила 5976 PNU. Для аллергена березы суммарная доза составила 2390,4 PNU.
Проведен анализ высвобождения гистамина из лейкоцитов цельной крови при ее инкубации с различными концентрациями (по белку) экстракта пыльцы березы (Т3) за неделю до начала АСИТ и через 10 дней после ее окончания (Фиг. 4 и Фиг. 5)
Полученные данные свидетельствуют о том, что анализ гиперчувствительности по высвобождению гистамина из лейкоцитов крови при ее стимуляции специфическим аллергеном может служить ценным показателем эффективности АСИТ.
Способ оценки гиперчувствительности по высвобождению гистамина из лейкоцитов цельной крови, включающий забор в пробирки с гепарином венозной крови у обследуемого человека, центрифугирование крови, замену плазмы буфером, дальнейшую инкубацию аликвот ресуспендированных клеток крови с тестируемыми субстанциями в микроплейте, а также с анти-IgE в качестве положительного контроля и с буфером - отрицательного контроля, с последующим центрифугированием микроплейта, прямым количественным определением гистамина в надосадочной жидкости лунок микроплейта методом обращенно-фазной высокоэффективной жидкостной хроматографии в сочетании с тандемным масс-спектрометрическим детектором и сравнение уровней гистамина, полученных для каждой из тестируемых субстанций, с положительным и отрицательным контролями, и при повышении уровня содержания гистамина в опытном образце по сравнению с отрицательным контролем при наличии реакции в положительном контроле выявляют гиперчувствительность к тестируемой субстанции.