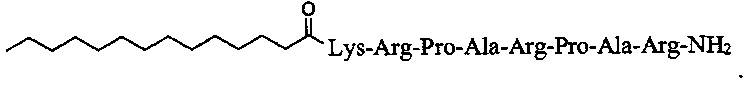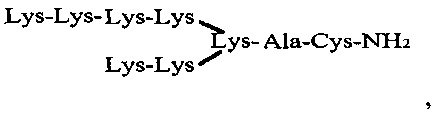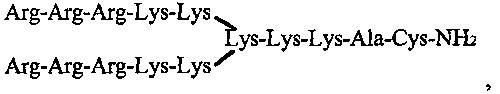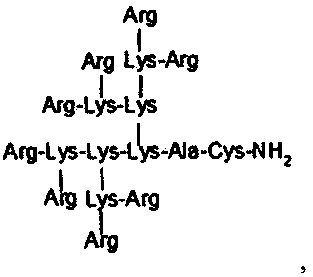Результат интеллектуальной деятельности: Применение катионных пептидов для индукции гибели клеток меланомы кожи человека
Вид РИД
Изобретение
Изобретение относится к медицине, а именно к экспериментальной онкологии, и касается применения катионных пептидов для индукции гибели клеток меланомы кожи человека.
Меланома кожи человека является неоднородным по молекулярно-генетическим характеристикам и клиническому течению онкологическим заболеванием. Для меланомы кожи человека характерна низкая чувствительность к различным видам терапии [Вишневская Я.В., Машенкина Я.А., Сендерович А.И., Строганова A.M., Полуэктова Ю.В. Современная морфологическая, иммуногистохимическая и молекулярно-генетическая диагностика меланомы кожи. Сибирский онкологический журнал; 2012. №4, с. 74-75]. Высокие дозы таргетных препаратов могут приводить к значительному нарастанию побочных эффектов и к отмене терапии.
Несмотря на достижения в области изучения и клинического применения противоопухолевых препаратов при лечении меланомы поиск нетоксичных молекулярно-направленных средств является актуальной проблемой онкологии.
Пептиды широкого спектра действия применяются как цитостатики, таргетные средства, агонисты гормонов, а также компоненты аптамеров и противоопухолевых вакцин [Thundimadathi J. Cancer treatment using peptides: Current therapies and future prospects. J. Amino Acids, 2012, doi: 1155/2012/967347; Zhao J., Zhou R., Fu X., Ren W, Ma L, Li R, Zhao Y, Guo L. Cell-penetrable lysine dendrimers for anti-cancer drug delivery: synthesis and preliminary biological evaluation. Arch. Pharm., 2014, 347(7): 469-477].
Известны низкомолекулярные катионные пептиды, молекулы которых несут высокий положительный заряд и обладают гидрофобными свойствами, благодаря значительному содержанию алифатических аминокислот. Катионные пептиды включают группу пептидов с поликатионной регулярной разветвленной структурой - дендритных пептидов, которые могут служить внутриклеточными переносчиками биологически активных веществ, в том числе и генетического материала: молекул ДНК, РНК, олигонуклеотидов [Патент РФ 2127125].
Основу сердцевины и ответвлений синтетических дендритных пептидов составляет полиамидоамин, сконструированный из метилакрилата и этилендиамина. Эти вещества не являются биогенными, поэтому возникает проблема их биологической деградации. Кроме того, синтетические полимеры не являются строго монодисперсными, поэтому вопрос о стандартизации таких препаратов не решен. Другая важная проблема - достижение специфичности и избирательной токсичности дендритных пептидов в отношении опухолевых клеток, поскольку они являются транспортерами молекул для любого типа клеток.
Данные проблемы решаются путем применения катионных пептидов со специфической дендритной структурой, обладающих значительно меньшей токсичностью по сравнению с линейными пептидами аналогичного аминокислотного состава; высокой проницаемостью клеточных мембран, благодаря амфифильным свойствам молекул; способностью взаимодействовать как с поверхностными, так и с внутриклеточными мишенями в опухолевых клетках.
Известно, что катионные пептиды синтезированы твердофазным методом с использованием стратегии Fmoc-защитных групп для внутриклеточной доставки нуклеиновых кислот [Патент 2572575].
Задачей изобретения является применение катионных пептидов для индукции гибели клеток меланомы кожи человека.
Поставленная задача решается тем, что для индукции гибели клеток меланомы кожи человека применяют малотоксичные для нормальных клеток катионные пептиды, включающие:
пептид с дендритной структурой и формулой R8K4K2KAC-NH2, содержащий в молекуле 8 остатков аргинина, 7 - лизина, 1 - аланина и 1 - цистеина
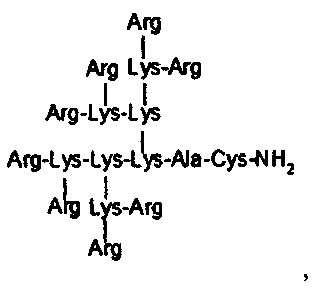
пептид с дендритной структурой и формулой K8K4K2KAC-NH2, содержащий в молекуле 15 остатков лизина, 1 - аланина и 1 - цистеина
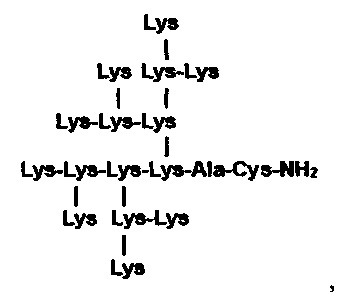
пептид с дендритной структурой и формулой (RRRKK)2KKKAC-NH2, содержащий в молекуле 7 остатков лизина, 6-аргинина, 1-аланина и 1-цистеина
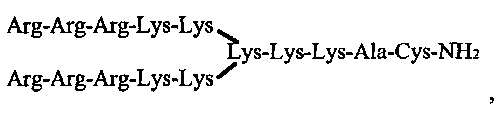
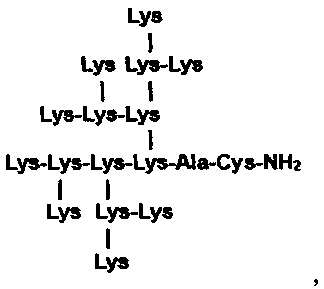
пептид с дендритной структурой и формулой (K)4(K)2KAC-NH2, содержащий в молекуле 7 остатков лизина, 1 - аланина, и 1 - цистеина
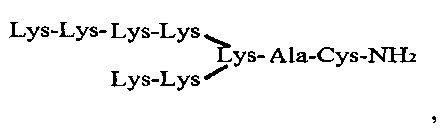
липопептид с линейной структурой и формулой Mir-KRPARPAR-NH2, содержащий миристоил на N-конце пептида, 3 остатка аргинина, 2 - пролина, 2 - аланина и 1 - лизина
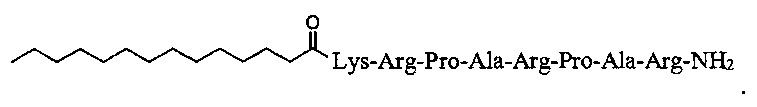
Технический результат изобретения состоит в том, что применение заявленных катионных пептидов в низких концентрациях (0,5-4,0 мкг/мл) позволяет индуцировать гибель клеток меланомы кожи человека, а также позволяет снизить побочные эффекты на нормальные клетки.
Краткое описание чертежей.
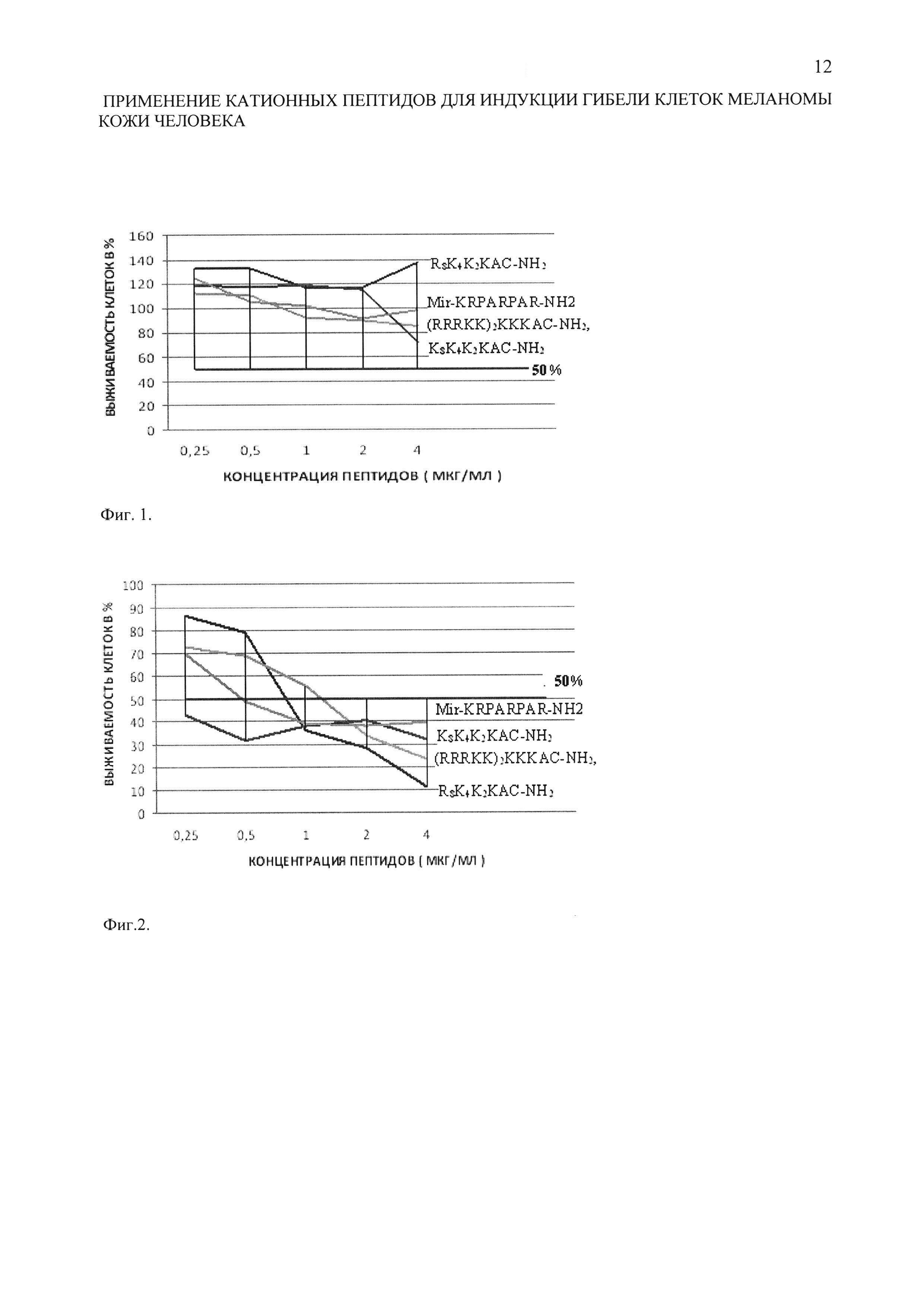
Фиг. 1. Выживаемость нормальных клеток (фибробластов линии H1036) через 3 суток инкубации клеток с катионными пептидами. За 100% принята выживаемость клеток без добавления раствора катионного пептида.
Фиг. 2. Выживаемость клеток меланомы линии mel IS223 через 3 суток инкубации с катионными пептидами. За 100% принята выживаемость клеток без добавления пептида.
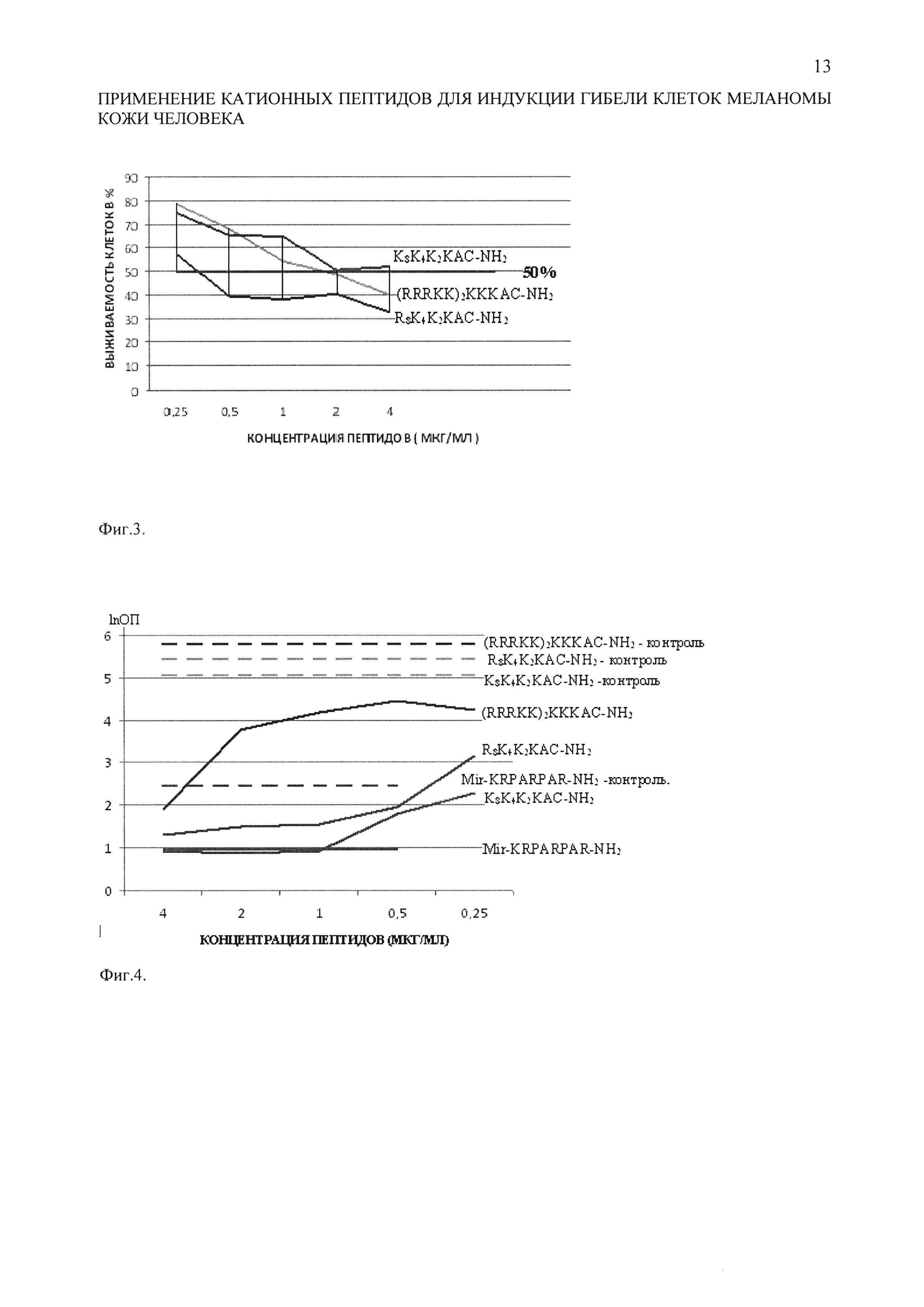
Фиг. 3. Выживаемость клеток линии mel IS223 через 2 суток инкубации клеток в экспоненциальной фазе роста с катионными пептидами.
Фиг. 4. Средняя оптическая плотность раствора формазана в клетках меланомы линии mel IS223. На оси Y - десятичный логарифм оптической плотности (lnОП). На оси X - концентрация пептидов в мкг/мл, в порядке ее уменьшения. Представлены средние величины оптической плотности формазана по трем повторам.
Пример 1. Изучение цитотоксической активности катионных пептидов
Объектами исследования служили перевиваемые клеточные линии меланомы кожи человека mel IS223 и mel Н275, полученные и охарактеризованные в ФГБУ «РОНЦ им. Н.Н. Блохина» Минздрава России, а также нетрансформированные фибробласты кожи человека линии H1036. Клеточную суспензию в полной питательной среде RPMI-1640 с 10% - эмбриональной телячьей сывороткой культивировали в 96-луночных планшетах по 180 мкл среды и от 7 до 10 тыс. клеток в лунке. После 24-часовой инкубации в лунки, за исключением контрольных, вносили по 20 мкл водного раствора каждого из катионных пептидов в конечной концентрации от 0,25 мкг/мл до 4,0 мкг/мл, в трехкратных повторах. Через 2-3 суток культивирования в каждую лунку добавляли по 10 мкл раствора 5 мМ раствора МТТ - бромида 3-(4,5-диметилтриазол-2ил)-2,5 дифенилтетразолия). Далее клетки инкубировали 2 часа до кристаллизации в них формазана, удаляли питательную среду и для растворения кристаллов добавляли в каждую лунку по 200 мкл ДМСО. Оптическую плотность раствора формазана измеряли спектрофотометрически. Зависимость выживаемости клеток от концентрации катионного пептида определяли по величине оптической плотности. Контролем служили лунки с клетками без добавления пептида. Показателем токсичности пептида служила разница значений оптической плотности в лунках с клетками меланомы кожи фибробластами после добавления МТТ. Параллельная инкубация опухолевых и нормальных клеток позволила определить пролиферативную активность и выживаемость клеток в ответ на внесение пептида. Клетки культивировали в течение 3 суток, для мониторинга выживших клеток использовали стандартный МТТ-тест. Максимальную цитотоксичность катионных пептидов наблюдали на 2-3 сутки культивирования клеток меланомы кожи.
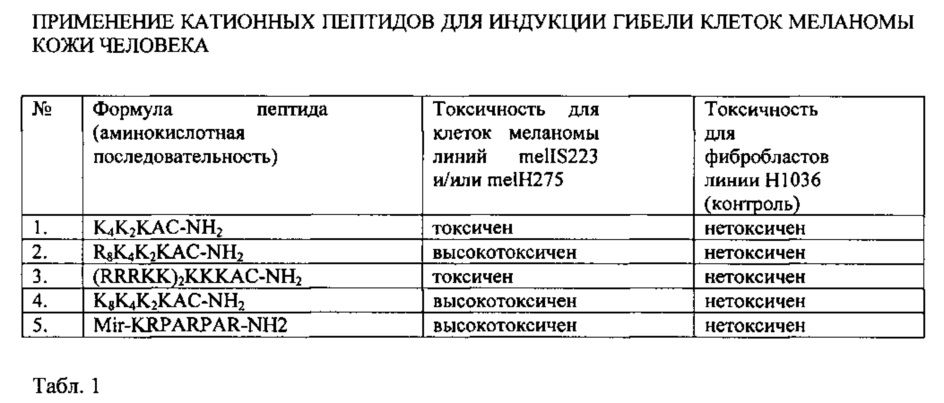
В табл. 1 представлена цитотоксическая активность примененных катионных пептидов (С-концевая амидная форма) в концентрации от 0,5 до 4,0 мкг/мл для нормальных клеток и клеток меланомы кожи человека.
Стандартом цитотоксичности пептидов является гибель не менее 60-70% опухолевых клеток. Высокотоксичные пептиды индуцируют до 90% опухолевых клеток, нетоксичные - не проявляют противоопухолевой активности.
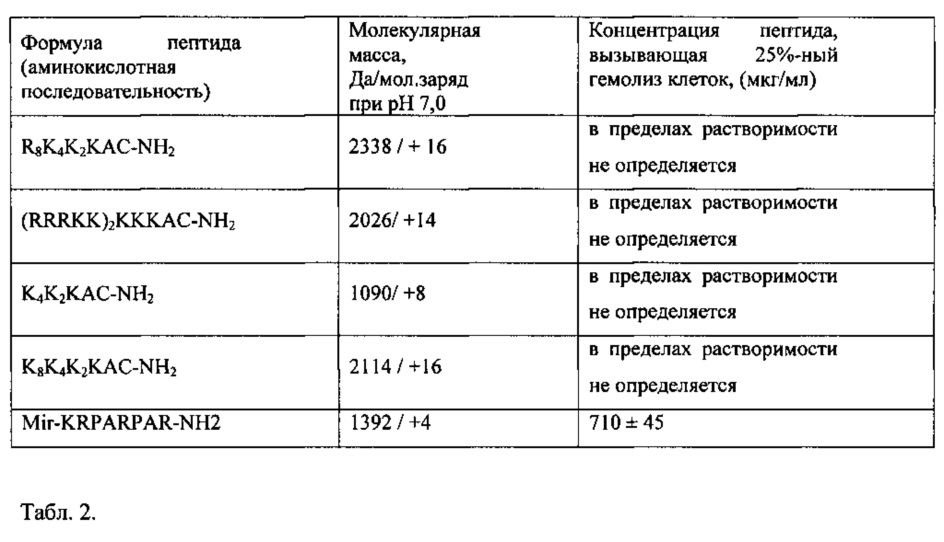
В табл. 2 приведены формулы катионных пептидов, использованы следующие обозначения: С - цистеин, К - лизин, R - аргинин, А - аланин, Р - пролин, Mir -миристоил. Применяемые катионные пептиды положительно заряжены, имеют молекулярную массу ~ от 1090 до 2338 Дальтон (Да) и различную геометрию ветвления молекулы. Токсичный для клеток меланомы кожи катионный пептид Mir-KRPARPAR-NH2 по своей структуре является липопептидом. Катионные пептиды K4K2KAC-NH2, R8K4K2KAC-NH2, (RRRKK)2KKKAC-NH2, K8K4K2KAC-NH2 по своей структуре являются дендритными пептидами.
Фиг. 1-4 иллюстрируют зависимость выживаемости клеток от концентрации различных катионных пептидов.
На фиг. 1 показана выживаемость нормальных клеток (фибробластов линии H1036) через 3 суток инкубации клеток с катионными пептидами. За 100% принята выживаемость клеток без добавления раствора катионного пептида. Выживаемость фибробластов при добавлении в культуру катионных пептидов была выше 50% (горизонтальная линия на графике). При малых концентрациях катионного пептида с формулой R8K4K2KAC-NH2 выживаемость нормальных клеток была выше, чем в контроле.
На фиг. 2 показана выживаемость клеток меланомы линии mel IS223 через 3 суток инкубации с катионными пептидами. За 100% принята выживаемость клеток без добавления пептида. Выживаемость менее 50% обусловлена высокой токсичностью пептидов. С увеличением концентрации пептидов от 0,25 мкг/мл до 4,0 мкг/мл токсичность нарастает, за исключением катионного липопептида с формулой Mir-KRPARPAR-NH2.
На фиг. 3 показана выживаемость клеток линии mel IS223 через 2 суток инкубации клеток в экспоненциальной фазе роста с катионными пептидами. Наиболее низкая выживаемость клеток меланомы кожи наблюдалась при применении катионных пептидов с формулой (RRRKK)2KKKAC-NH2 и R8K4K2KAC-NH2.
На фиг. 4 показана средняя оптическая плотность раствора формазана в клетках меланомы линии mel IS223. На оси Y - десятичный логарифм оптической плотности (lnОП). На оси X - концентрация пептидов в мкг/мл, в порядке ее уменьшения. Представлены средние величины оптической плотности формазана по трем повторам. Показано, что оптическая плотность с ростом концентрации катионных пептидов снижалась, что указывает на их токсичность. В контроле оптическая плотность не изменялась.
Применение катионных пептидов с формулами R8K4K2KAC-NH2, K8K4K2KAC-NH2, (RRRKK)2KKKAC-NH2 и Mir-KRPARPAR-NH2 выявило наиболее высокую токсичность для клеток меланомы кожи и низкую - для нормальных клеток кожи.
Пример 2. Изучение гемолитической активности катионных пептидов
Известно, что пептиды могут вызывать лизис клеток крови. В связи с этим была изучена гемолитическая активность катионных пептидов с использованием модифицированной методики [Duguid, J.G. et al. A physicochemical approach for predicting the effectiveness of peptide-based gene delivery systems for use in plasmid-based gene therapy. Biophys. J., 1998, 74(6): 2802-2814].
Кровь с добавлением гепарина была получена от доноров. Эритроциты осаждали центрифугированием при 300g в течение 15 мин в стерильном цитратном буфере следующего состава: 20 мМ цитрата натрия, 150 мМ хлорида натрия с рН=7,4. Далее эритрициты суспендировали до оптической плотности, равной единице, и плотности клеток около 3×107 кл/мл. В пробирки с данной суспензией эритроцитов добавляли катионные пептиды до конечной концентрации от 0,25 мкг/мл до 8 мкг/мл и инкубировали в течение часа при комнатной температуре 24°С. Отрицательным контролем служила проба с суспензией эритроцитов без добавления пептидов, положительным контролем - проба со стерильной дистиллированной водой. Оптическую плотность проб определяли спектрофотометрически при длине волны 540 нм. Для каждого из катионных пептидов эксперимент повторяли трижды.
В табл. 2 представлены индексы гемолитической активности, т.е. концентрации (мкг/мл) четырех катионных пептидов, вызывающие гемолиз 25% клеток в суспензии. Гемолитическая активность катионных пептидов в данных концентрациях не обнаружена.
Таким образом, катионные пептиды с формулами R8K4K2KAC-NH2, (RRRKK)2KKKAC-NH2 и K8K4K2KAC-NH2 в концентрациях от 0,5 до 4,0 мкг/мл показали высокую токсичность для клеток меланомы кожи и низкую - для нормальных клеток и отсутствие гемолитической активности. Катионный пептид с формулой K4K2KAC-NH2 в концентрациях от 1 до 2 мкг/мл был также токсичен для клеток меланомы кожи и малотоксичен - для нормальных клеток. Катионный пептид с формулой Mir-KRPARPAR-NH2 в концентрациях от 1 до 4 мкг/мл токсичен для клеток меланомы кожи и нетоксичен - для нормальных клеток.