Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ ЭКЗОСОМ ИЗ КРОВИ
Вид РИД
Изобретение
Область техники, к которой относится изобретение
Изобретение относится к области биотехнологии, в частности к способу получения экзосом из крови, и может быть использовано для изоляции и исследования микровезикул крови в диагностических целях.
Уровень техники
Известен способ выделения микровезикул эритроцитов из надосадочной жидкости, который включает забор крови, промывание эритроцитов, инкубацию отмытых клеток в присутствии кальция и ионофора А 23187, центрифугирование при 1000 g в течение 10 минут для получения супернатанта, ультрацентрифугирование супернатанта при 100000 g в течение 60 минут, получение осадка, содержащего микровезикулы (см. Allan D., Thomas P., Limbrick AR: The isolation and characterization of 60 nm vesicles (nanovesiclts) produced during ionophore A 23187 - induced budding of human erythrocytes. Biochem J 1980, 188 881-887).
Недостатком данного способа является длительность и трудоемкость выделения экзосом, низкий выход микровезикул, выделенных из крови.
Известен способ получения экзосом из плазмы крови, заключающийся в следующем. Образцы плазмы фильтруют через фильтры с диаметром пор 0,220 мкм для удаления клеточного дебриса и более крупных частиц и разделяют компоненты плазмы при помощи белковой жидкостной хроматографии, фракции объединяют и концентрируют путем центрифугирования с помощью 3 кДа-отсекающих фильтров (Millipore), затем сконцентрированный препарат наносят на сахарозный градиент 0,2-0,5 M в 20 мМ трис, pH 8,0 и ультрацентрифугируют при 175000 g в течение 16 часов. Частицы, находящиеся в диапазоне концентрации сахарозы 1,08-1,15 г/мл, объединяют, отмывают раствором PBS (10 мМ фосфатный буфер, 0,15 M NaCl, pH 7,5) и осаждают при помощи ультрацентрифугирования при 175000 g в течение 2 часов (см. Looze С, Yui D., Leung L., Ingham M., Yao X., Wu W.W., Shen R.-F., Daniels M.P., Levine S.J. Proteomic profiling of human plasma exosomes identifies PPAR as an exosome - associated protein // Biochem. Biophys. Res. Commun. 2009. V. 378. P. 433-438).
Недостатками данного способа являются недостаточная чистота целевого продукта, наличие примеси микрочастиц диаметром 100-220 нм, трудоемкость и длительность, более 23 часов, выделения экзосом, ограниченное количество экзосом, выделенных из плазмы крови.
Известен способ получения экзосом из плазмы крови, заключающийся в следующем. Клетки и дебрис удаляют путем последовательного центрифугирования периферической крови, супернатант фильтруют через фильтры с диаметром пор 0,2 мкм. Экзосомы плазмы крови выделяют с помощью коммерческого набора ExoQuick™ Exosome Precipitation Solution (см. System Biosciences Inc., Mountain View, CA, USA) (Ge Q., Zhou Y., Lu J., Bai Y., Xie X., Lu Z., miRNA in plasma exosome is stable under different storage conditions // Molecules. 2014. V. 19. P. 1568-1575).
Недостатками данного способа являются его недостаточная чистота целевого продукта, наличие примеси микрочастиц диаметром 100-220 нм, трудоемкость и длительность, более 10 часов, выделения экзосом, высокая стоимость коммерческого набора для выделения экзосом, ограниченное количество экзосом, выделенных из плазмы крови.
Наиболее близким по технической сущности и достигаемому положительному эффекту и принятый авторами за прототип является способ получения экзосом из крови, включающий разделение крови на бесклеточную и клеточную фракции с помощью центрифугирования с последующим получением экзосом путем ультрацентрифугирования, при этом кровь разделяют на плазму и клеточную фракцию, затем клетки крови последовательно, в две стадии, обрабатывают сначала буферным раствором PBS, содержащим 5 мМ ЭДТА, затем равным объемом 0,15-0,35% раствора трипсина в PBS, далее плазму и полученные супернатанты объединяют, удаляют клеточный дебрис и примеси неэкзосомального происхождения путем центрифугирования при 15000-20000 g в течение 10-20 минут и фильтрации через фильтры с диаметром пор 0,1 мкм, а суммарный пул экзосом осаждают ультрацентрифугированием при 100000-160000 g в течение 60-120 минут.
В способе, обработку буферным раствором PBS, содержащим 5 мМ ЭДТА, осуществляют в течение 5 минут с последующим центрифугированием в течение 20 минут при 300 g и сбором супернатанта.
В способе, обработку 0,15-0,35% раствором трипсина в PBS, осуществляют в течение 5 минут с последующим добавлением ингибитора фермента, перемешиванием, осаждением клеток крови центрифугированием в течение 20 минут при 300 g и сбором супернатанта (см. пат. RU №2556825, МПК C12N 5/00, опубл. 20.07.2015 г.).
Недостатком данного способа является длительность и сложность получения экзосом из крови в широкой лабораторно-диагностической практике.
Раскрытие изобретения
Задачей предлагаемого изобретения является разработка способа получения экзосом из крови, обладающего сокращением длительности и снижением трудоемкости способа изоляции экзосом из крови, а также увеличением выхода экзосом, повышением чистоты целевого продукта.
Технический результат, который может быть получен с помощью предлагаемого изобретения, сводится к сокращению длительности и снижению трудоемкости способа изоляции экзосом из крови.
Технический результат достигается с помощью способа получения экзосом из крови, включающего разделение крови на бесклеточную и клеточную фракции с помощью центрифугирования с последующим получением экзосом путем ультрацентрифугирования, причем разделение крови на плазму и клеточную фракции проводят с помощью центрифугирования, затем клеточную фракцию подвергают последовательной обработке буферным раствором PBS, в качестве которого используют 10 мМ фосфатного буфера, 0,15 М NaCl, содержащим 5 мМ ЭДТА, производят сбор первого супернатанта, центрифугирование и сбор второго супернатанта, затем плазму и полученные супернатанты объединяют, для получения суммарного пула экзосом крови, удаляют клеточный дебрис и примеси неэкзосомального происхождения путем центрифугирования, проводят фильтрацию через фильтры с диаметром пор 0,1 мкм, а суммарный пул экзосом осаждают ультрацентрифугированием при 100000 g в течение 60 минут, при этом фильтрацию и ультрацентрифугирование проводят одновременно с помощью ультрацентрифужных фильтровальных пробирок, причем разделение крови на плазму и клеточную фракции проводят с помощью центрифугирования, при 400-600 g в течение 10-20 минут, а клеточную фракцию подвергают последовательной обработке буферным раствором PBS, при pH 7,4, проводят инкубацию в течение 5-15 минут с последующим центрифугированием в течение 15-25 минут при 400-600 g и сбором первого супернатанта, затем проводят резкое встряхивание с последующим центрифугированием в течение 10 минут при 500 g и сбор второго супернатанта.
Сущность способа получения экзосом из крови заключается в следующем.
Проводят сбор периферической крови в вакутейнер или другие пробирки для сбора и консервирования крови. Кровь разделяют на плазму и клеточную фракцию путем центрифугирования при 400-600 g в течение 10-20 мин. Клеточную фракцию крови подвергают последовательной обработке буферным раствором PBS, в качестве которого используют 10 мМ фосфатного буфера, 0,15 М NaCl, при pH 7,4, содержащим 5 мМ ЭДТА, проводят инкубацию в течение 5-15 мин с последующим центрифугированием в течение 15-25 минут при 400-600 g, сбором первого супернатанта, затем проводят резкое встряхивание пробирки с последующим центрифугированием в течение 10 минут при 500 g и сбор второго супернатанта. Плазму и полученные супернатанты из клеточной фракции, содержащие экзосомы, связанные с поверхностью форменных элементов, объединяют и используют в качестве исходного материала для получения суммарного пула экзосом крови, для этого из объединенного образца удаляют клеточный дебрис центрифугированием при 25000-35000 g в течение 5-15 минут, экзосомы осаждают ультрацентрифугированием в ульрацентрифужных фильтровальных пробирках с диаметром пор 0,1 мкм при 100000 g в течение 60 минут.
В результате получают суммарный пул экзосом крови, который включает экзосомы плазмы и экзосомы, связанные с поверхностью клеток крови, что позволяет повысить выход целевого продукта и в последующем повысить чувствительность диагностических систем путем увеличения количества диагностического материала в анализе.
Таким образом, экзосомы представляют собой микровезикулы размером 20-100 нм, активно секретируемые через каскад экзоцитоза, при этом экзосомы секретируются в определенных физиологических условиях из различных типов клеток организма и предназначены для межклеточных взаимодействий (см. Гусаченко О.Н., Зенкова М.А., Власов В.В. «Нуклеиновые кислоты экзосом: маркеры заболеваний и молекулы межклеточной коммуникации // Биохимия. 2013. Т. 78. №1, с. 5-13), экзосомы переносят биомаркеры состояния продуцирующих их клеток, служат для ранней диагностики, определения стадии и факта прогрессии различных заболеваний, в том числе онкологической патологии, что поможет оказать своевременное лечение и оценить его эффективность (см. Medvedeva N.V., Nanobiotechnology and nanomedicine /N.V. Medvedeva, О.M. Ipatova, D. IvanovIu // Biomed Khim - 2006. – T. 52 - №6. - С. 529-546), а выполнение способа изоляции экзосом из крови путем разделения исходного образца крови на плазму и клеточную фракцию, проведения центрифугирования при 400-600 g в течение 10-20 мин, при этом клеточную фракцию крови подвергают последовательной обработке буферным раствором PBS рН 7,4, с последующей инкубацией 5-15 мин, с центрифугированием в течение 15-25 минут при 400-600 g, проведением встряхивания пробирки с последующим центрифугированием в течение 10 минут при 500 g, удаление клеточного дебриса центрифугированием при 25000-35000 g в течение 5-15 минут, одновременное проведение фильтрации и ультрацентрифугирования в ульрацентрифужных фильтровальных пробирках с диаметром пор 0,1 мкм при 100000 g в течение 60 минут позволяет снизить трудозатраты, связанные с изоляцией экзосом из крови, и уменьшить длительность способа с 4,0 до 2,3 часов.
Краткое описание чертежей и иных материалов
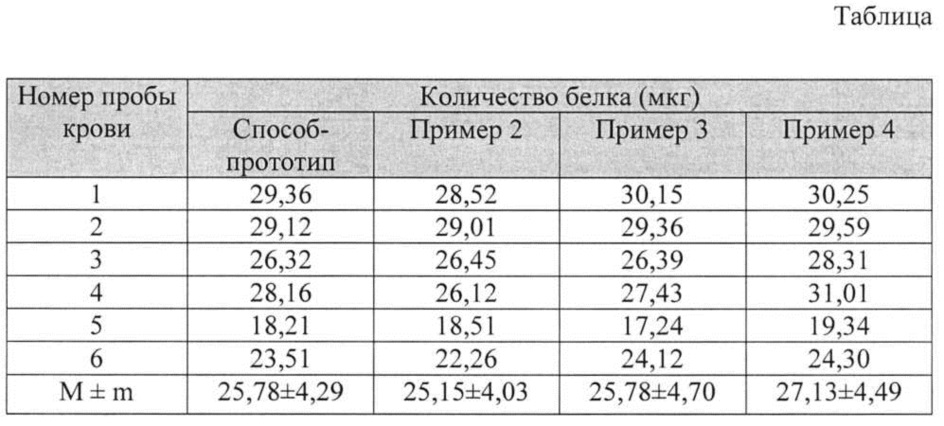
В таблице дан способ изоляции экзосом из крови, концентрация белка в пробе.
Осуществление изобретения
Примеры конкретного выполнения способа изоляции экзосом из крови.
Пример 1. Проводят сбор периферической крови в вакутейнер или другие пробирки для сбора и консервирования крови. Кровь разделяют на плазму и клеточную фракцию путем центрифугирования при 300 g в течение 8 мин.
Клеточную фракцию крови подвергают последовательной обработке буферным раствором PBS в количестве 10 мМ фосфатного буфера, 0,15 М NaCl, при рН 7,4, содержащим 5 мМ ЭДТА, проводят инкубацию в течение 4 мин с последующим центрифугированием 10 минут при 300 g, сбор первого супернатанта, затем проводят встряхивание пробирки с последующим центрифугированием в течение 8 минут при 400 g, сбор второго супернатанта.
Плазму и полученные супернатанты из клеточной фракции, содержащие экзосомы, связанные с поверхностью форменных элементов, объединяют и используют в качестве исходного материала для получения суммарного пула экзосом крови. Для этого из объединенного образца удаляют клеточный дебрис центрифугированием при 20000 g в течение 10 минут, экзосомы осаждают ультрацентрифугированием в ульрацентрифужных фильтровальных пробирках с диаметром пор 0,1 мкм при 100000 g в течение 50 минут.
Для оценки количества выделенных экзосом с использованием способа-прототипа и предлагаемого способа была измерена концентрация белка в 1 мл анализируемого вещества с использованием коммерческого набора NanoOrange Quantification Kit (Invitrogen, США) по протоколу, рекомендованному производителем.
В примере 1 получают невысокий суммарный пул экзосом крови, который включает экзосомы плазмы и экзосомы, связанные с поверхностью клеток крови, что не позволяет сохранить выход целевого продукта.
Пример 2. Проводят аналогично примеру 1, но кровь разделяют на плазму и клеточную фракцию путем центрифугирования при 400 g в течение 10 мин. Клеточную фракцию крови подвергают последовательной обработке буферным раствором PBS (10 мМ фосфатный буфер, 0,15 М NaCl, рН 7,4), содержащим 5 мМ ЭДТА (5 мин инкубация с последующим центрифугированием 15 минут при 400 g, сбор первого супернатанта); затем проводят встряхивание пробирки с последующим центрифугированием 10 минут при 500 g и сбор второго супернатанта. Плазму и полученные супернатанты из клеточной фракции, содержащие экзосомы, связанные с поверхностью форменных элементов, объединяют и используют в качестве исходного материала для получения суммарного пула экзосом крови. Для этого из объединенного образца удаляют клеточный дебрис центрифугированием при 25000 g в течение 15 минут, экзосомы осаждают ультрацентрифугированием в ульрацентрифужных фильтровальных пробирках с диаметром пор 0,1 мкм при 100000 g в течение 60 минут.
Для оценки количества выделенных экзосом с использованием способа-прототипа и предлагаемого способа была измерена концентрация белка в 1 мл анализируемого вещества с использованием коммерческого набора NanoOrange Quantification Kit (Invitrogen, США) по протоколу, рекомендованному производителем. Результаты исследования (см. пример 2 таблицы) концентрации белка представлены в таблице.
В результате получают высокий суммарный пул экзосом крови, который включает экзосомы плазмы и экзосомы, связанные с поверхностью клеток крови, что позволяет сохранить выход целевого продукта, а также сократить трудовые и финансовые затраты.
Пример 3. Проводят аналогично примеру 1, но кровь разделяют на плазму и клеточную фракцию путем центрифугирования при 500 g в течение 15 мин. Клеточную фракцию крови подвергают последовательной обработке буферным раствором PBS (10 мМ фосфатный буфер, 0,15 М NaCl, рН 7,4), содержащим 5 мМ ЭДТА (10 мин инкубация с последующим центрифугированием 20 минут при 500 g, сбор первого супернатанта), затем проводят встряхивание пробирки с последующим центрифугированием 10 минут при 500 g и сбор второго супернатанта. Плазму и полученные супернатанты из клеточной фракции, содержащие экзосомы, связанные с поверхностью форменных элементов, объединяют и используют в качестве исходного материала для получения суммарного пула экзосом крови, для этого из объединенного образца удаляют клеточный дебрис центрифугированием при 30000 g в течение 10 минут, экзосомы осаждают ультрацентрифугированием в ульрацентрифужных фильтровальных пробирках с диаметром пор 0,1 мкм при 100000 g в течение 60 минут.
Для оценки количества выделенных экзосом с использованием способа-прототипа и предлагаемого способа была измерена концентрация белка в 1 мл анализируемого вещества с использованием коммерческого набора NanoOrange Quantification Kit (Invitrogen, США) по протоколу, рекомендованному производителем. Результаты исследования (см. пример 3 таблицы) представлены в таблице.
В результате получают высокий суммарный пул экзосом крови, который включает экзосомы плазмы и экзосомы, связанные с поверхностью клеток крови, что позволяет сохранить выход целевого продукта, а также сократить трудовые и финансовые затраты.
Пример 4. Проводят аналогично примеру 1, но кровь разделяют на плазму и клеточную фракцию путем центрифугирования при 600 g в течение 20 мин.
Клеточную фракцию крови подвергают последовательной обработке буферным раствором PBS (10 мМ фосфатный буфер, 0,15 М NaCl, рН 7,4), содержащим 5 мМ ЭДТА (15 мин инкубация с последующим центрифугированием 25 минут при 600 g, сбор первого супернатанта); затем резким встряхиванием пробирки с последующим центрифугированием 10 минут при 500 g, сбор второго супернатанта.
Плазму и полученные супернатанты из клеточной фракции, содержащие экзосомы, связанные с поверхностью форменных элементов, объединяют и используют в качестве исходного материала для получения суммарного пула экзосом крови. Для этого из объединенного образца удаляют клеточный дебрис центрифугированием при 35000 g в течение 5 минут, экзосомы осаждают ультрацентрифугированием в ульрацентрифужных фильтровальных пробирках с диаметром пор 0,1 мкм при 100000 g в течение 60 минут. Для оценки количества выделенных экзосом с использованием способа-прототипа и предлагаемого способа была измерена концентрация белка в 1 мл анализируемого вещества с использованием коммерческого набора NanoOrange Quantification Kit (Invitrogen, США) по протоколу, рекомендованному производителем. Результаты исследования (см. пример 4 таблицы) представлены в таблице.
В результате получают высокий суммарный пул экзосом крови, который включает экзосомы плазмы и экзосомы, связанные с поверхностью клеток крови, что позволяет сохранить выход целевого продукта, а также сократить трудовые и финансовые затраты.
Пример 5. Проводят аналогично примеру 1, но кровь разделяют на плазму и клеточную фракцию путем центрифугирования при 700 g в течение 25 мин.
Клеточную фракцию крови подвергают последовательной обработке буферным раствором PBS (10 мМ фосфатный буфер, 0,15 М NaCl, рН 7,4), содержащим 5 мМ ЭДТА (20 мин инкубация с последующим центрифугированием 30 минут при 700 g, сбор первого супернатанта); затем резким встряхиванием пробирки с последующим центрифугированием 15 минут при 600 g, сбор второго супернатанта.
Плазму и полученные супернатанты из клеточной фракции, содержащие экзосомы, связанные с поверхностью форменных элементов, объединяют и используют в качестве исходного материала для получения суммарного пула экзосом крови. Для этого из объединенного образца удаляют клеточный дебрис центрифугированием при 37000 g в течение 8 минут, экзосомы осаждают ультрацентрифугированием в ульрацентрифужных фильтровальных пробирках с диаметром пор 0,1 мкм при 100000 g в течение 65 минут.
Для оценки количества выделенных экзосом с использованием способа-прототипа и предлагаемого способа была измерена концентрация белка в 1 мл анализируемого вещества с использованием коммерческого набора NanoOrange Quantification Kit (Invitrogen, США) по протоколу, рекомендованному производителем.
В результате, получают суммарный пул экзосом крови, который включает экзосомы плазмы и экзосомы, связанные с поверхностью клеток крови, при этом при измерении концентрации белка выявлено, что его значения практически не отличаются от значений концентрации белка по примеру 3, однако значительно увеличилось количество затрачиваемого времени (2,7 часа).
Таким образом, наиболее оптимальными являются примеры 2, 3 и 4, причем реализация предлагаемого способа позволяет сохранить эффективность изоляции экзосом из крови (см. табл.), при этом сокращается трудоемкость и длительность проведения способа с 4,0 до 2,3 часов.
Предлагаемое изобретение по сравнению с прототипом и другими известными техническими решениями имеет следующие преимущества:
- упрощение и сокращение длительности способа с 4,0 до 2,3 часов их изоляции из крови;
- позволяет снизить трудозатраты, связанные с изоляцией экзосом из крови.