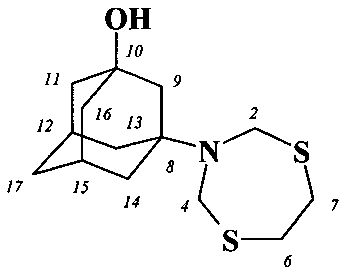
Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ N-АДАМАНТИЛ-1,5,3-ДИТИАЗЕПАНОВ
Вид РИД
Изобретение
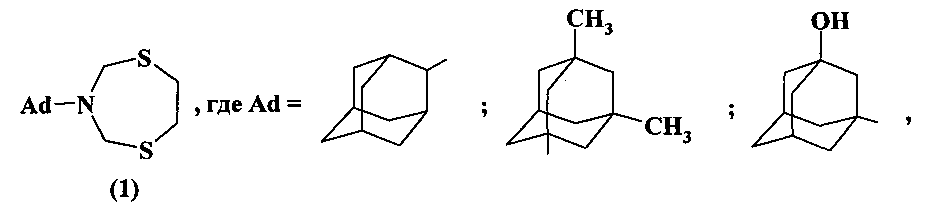
Предлагаемое изобретение относится к области органической химии, в частности к способу получения N-адамантил-1,5,3-дитиазепанов общей формулы (1)
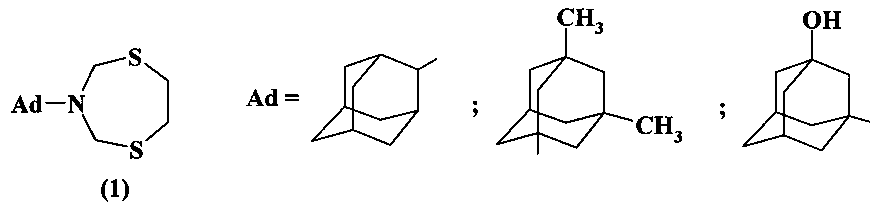
S,N-Содержащие гетероциклы известны как антиоксидантные (А.С. Березин, Е.А. Ломкова, Ю.А. Скорик, Изв. АН. Сер. хим., 778, 2012), фунгицидные (V. Ambrogi, G. Grandolini, L. Perioli, M. Ricci, С. Rossi, L. Tuttobello, European Journal of Medicinal Chemistry, 25, 403, 1990), противомикробные агенты (A.A. Bialy Serry, A.M. Abdelal, A.El-Shorbagi, M.M. Kheira Samy, Archiv der Pharmazie, 338, 38, 2005).
Известен способ (Е.Б. Рахимова, И.В. Васильева, Л.М. Халилов, А.Г. Ибрагимов, У.М. Джемилев. ХГС, 2012, 7, 1132) получения 2- и 4-(1,5,3-дитиазепан-3-ил)фенолов (2) реакцией каталитического переаминирования N-трет-бутил-1,5,3-дитиазепана с помощью о- и n-аминофенолов под действием Sm(NO3)3·6H2O.
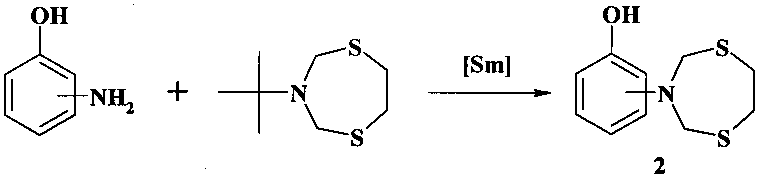
Известным способом не могут быть получены N-адамантил-1,5,3-дитиазепаны общей формулы (1).
Известен способ (Е.Б. Рахимова, Р.А. Исмагилов, Е.С. Мещерякова, Р.А. Зайнуллин, Л.М. Халилов, А.Г. Ибрагимов, У.М. Джемилев. ХГС, 2014, 5, 782) получения N-гидроксиалкил-1,5,3-дитиазепанов (3) межмолекулярной циклизацией 1,2-этандитиола с метоксиметиламиноспиртами под действием SmCl3·6H2O.
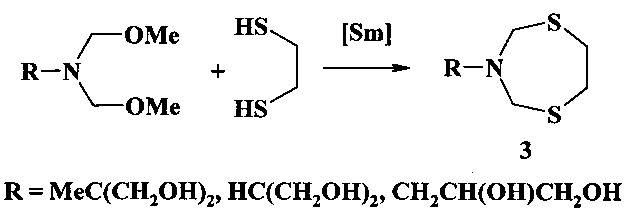
Известным способом не могут быть получены N-адамантил-1,5,3-дитиазепаны общей формулы (1).
Таким образом, в литературе отсутствуют сведения по получению N-адамантил-1,5,3-дитиазепанов общей формулы (1).
Предлагается новый способ получения N-адамантил-1,5,3-дитиазепанов общей формулы (1).
Сущность способа заключается во взаимодействии адамантиламина (2-аминоадамантан, или 1,3-диметил-5-аминоадамантан, или 1-гидрокси-3-аминоадамантан) с 1-окса-3,6-дитиациклогептаном в присутствии катализатора SmCl3·6H2O, взятыми в мольном соотношении адамантиламин:1-окса-3,6-дитиациклогептан:SmCl3·6H2O)=1:1:(0.03-0.07), предпочтительно 1:1: 0.05, при комнатной температуре (~20°С) и атмосферном давлении в среде растворителей этанол-хлороформ (1:1, объемное соотношение) в течение 2.5-3.5 ч. Выход N-адамантил-1,5,3-дитиазепанов (1) составляет 88-95%. Реакция протекает по схеме
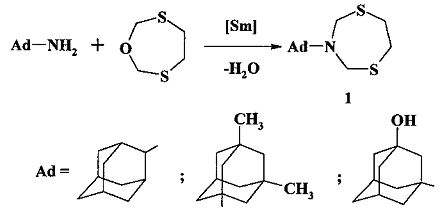
N-Адамантил-1,5,3-дитиазепаны общей формулы (1) образуются только лишь с участием адамантиламина и 1-окса-3,6-дитиациклогептана, взятых в стехиометрических количествах. При другом соотношении исходных реагентов снижается селективность реакции. Без катализатора SmCl3·6H2O реакция идет с выходом, не превышающим 35%. Проведение реакции в присутствии катализатора SmCl3·6H2O больше 7 мол.% по отношению к адамантиламину не приводит к существенному увеличению выхода целевого продукта (1). Использование в реакции катализатора SmCl3·6H2O менее 3 мол.% снижает выход (1), что связано с уменьшением каталитически активных центров в реакционной массе. Реакции проводили при комнатной температуре ~20°С. При более высокой температуре (например, 60°С) увеличиваются энергозатраты, при меньшей температуре (например, 0°С) снижается скорость реакции. Опыты проводили в среде растворителей этанол-хлороформ (1:1, объемное соотношение), т.к. в них хорошо растворяются исходные реагенты и целевые продукты.
Существенные отличия предлагаемого способа
В известном способе реакция идет с участием в качестве исходных реагентов 1,2-этандитиола и метоксиметиламиноспиртов с образованием N-гидроксиалкил-1,5,3-дитиазепанов (3). Известный способ не позволяет получать N-адамантил-1,5,3-дитиазепаны общей формулы (1).
В предлагаемом способе в качестве исходных реагентов применяются адамантиламин (2-аминоадамантан, 1,3-диметил-5-аминоадамантан, 1-гидрокси-3-аминоадамантан) и 1-окса-3,6-дитиациклогептан.
Предлагаемый способ обладает следующими преимуществами
Способ позволяет получать с высокой селективностью индивидуальные N-адамантил-1,5,3-дитиазепаны общей формулы (1), синтез которых в литературе не описан.
Способ поясняется следующими примерами
ПРИМЕР 1. В сосуд Шленка, установленный на магнитной мешалке, помещают 151 мг (1 ммоль) 2-аминоадамантана в 5 мл этанола, 18 мг (0.05 ммоль) SmCl3·6Н2О и 136 мг (1 ммоль) 1-окса-3,6-дитиациклогептана в 5 мл хлороформа. Реакционную смесь перемешивают при температуре -20°С в течение 3 ч, колоночной хроматографией на SiO2 выделяют N-(2-адамантил)-1,5,3-дитиазепан с выходом 93%.
Другие примеры, подтверждающие способ, приведены в таблице 1.
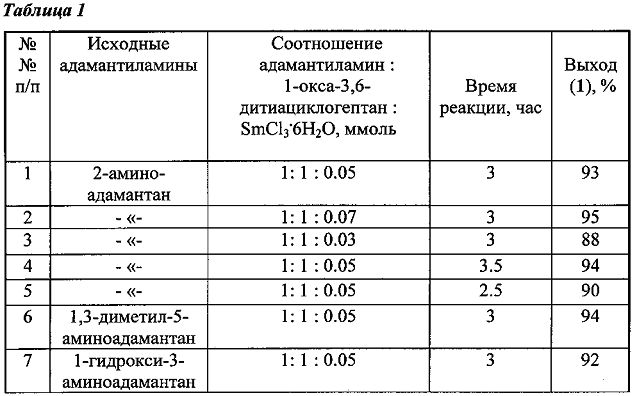
Все опыты проводили при комнатной температуре (-20°С) в среде растворителей этанол-хлороформ (1:1, объемное соотношение), т.к. в них растворяются исходные и целевые продукты.
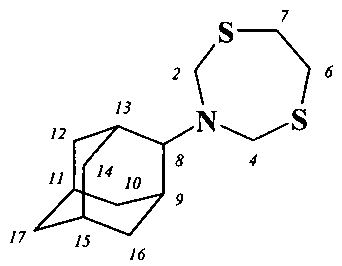
Спектральные характеристики N-(2-адамантил)-1,5,3-дитиазепана1 (1 Контроль реакции осуществляли методом ТСХ на пластинах Sorbfil (ПТСХ-АФ-В) проявляли парами I2. Для колоночной хроматографии использовали силикагель КСК (100-200 мкм). Спектры ЯМР 1D (1Н, 13С) и 2D (COSY, HSQC, НМВС) сняты на спектрометре Bruker Avance 400 (100.62 МГц для 13С и 400.13 МГц для 1Н) по стандартным методикам фирмы Bruker, внутренний стандарт Me4Si, растворитель - CDCl3. Масс-спектры получены на приборе MALDI TOF/TOF AUTOFLEX III фирмы Bruker.
Спектр ЯМР 1Н, δ, м.д.: 1.49 уш.с (2Н, СН2, На-12,16); 1.72 уш.с (2Н, СН2, Н-17); 1.82 уш.с (2Н, СН2, На-10,14; 1Н, СН, Н-15); 1.87 уш.с (4Н, СН2, Hb-10,12,14,16; 1Н, СН, Н-11); 2.00 уш.с (2Н, СН, Н-9,13); 3.17 уш.с (4Н, СН2, Н-6,7); 3.20 уш.с (1Н, СН, Н-8); 4.24 уш.с (4Н, СН2, Н-2,4).
Спектр ЯМР 13С, δ, м.д.: 27.1 (С-11), 27.3 (С-15), 28.3 (С-9, С-13), 31.5 (С-12, С-16), 35.5 (С-6, С-7), 36.9 (С-10, С-14), 37.5 (С-17), 56.8 (С-2, С-4), 58.3 (С-8).
MALDITOF, m/z: 268 [М-Н]+ (100%), 270 [М+Н]+ (46%). C14H23NS2. М269.
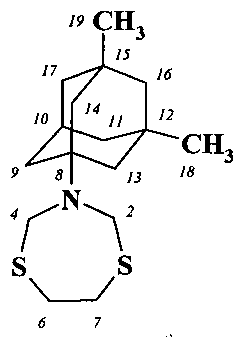
Спектральные характеристики N-(1,3-диметил-5-адамантил)-1,5,3-дитиазепана
Спектр ЯМР 1Н, δ, м.д.: 0.87 уш.с (6Н, СН3, Н-18,19); 1.12 д (2Н, СН2, Н-16, J 8 Гц); 1.30 уш.с (4Н, СН2, Н-11,17); 1.44 дд (4Н, СН2, Н-13,14, J32 и 14 Гц); 1.67 уш.с (2Н, СН2, Н-9); 2.16-2.18 м (1Н, СН, Н-10); 2.99 уш.с (4Н, СН2, Н-6,7); 4.49 уш.с (4Н, СН2, Н-2,4).
Спектр ЯМР 13С, δ, м.д.: 30.2 (С-10), 30.5 (С-18, С-19), 32.4 (С-12, С-15), 37.0 (С-6, С-7), 38.9 (С-9), 42.7 (С-11, 17), 46.7 (С-13, 14), 50.6 (С-16), 52.9 (С-2, С-4), 57.6 (С-8).
MALDI TOF, m/z: 163 [M-CH2NCH2S(CH2)2S]+(100%), 296 [М-Н]+ (15%), 298 [М+Н]+ (14%). C16H27NS2. М297.
Спектральные характеристики N-(1-гидрокси-3-адамантил)-1,5,3-дитиазепана
Спектр ЯМР 1H, δ, м.д.: 1.52уш.с (2Н, СН2, Н-17); 1.66 уш.с (4Н, СН2, Н-11,16); 1.7 6уш.с (4Н, СН2, Н-13,14); 1.80 уш.с (2Н, СН2, Н-9); 2.31 уш.с (2Н, СН, Н-12,15); 3.01 уш.с (4Н, СН2, Н-6,7); 4.47 уш.с (4Н, СН2, Н-2,4).
Спектр ЯМР 13С, δ, м.д.: 30.7 (С-12, С-15), 34.9 (С-17), 36.9 (С-6, С-7), 39.1 (С-13, С-14), 44.2 (С-11, С-16), 48.4 (С-9), 52.9 (С-2, С-4), 58.7 (С-8), 69.7 (С-10).
MALDI TOF, m/z: 284[М-H]+ (100%), 286 [М+Н]+ (45%). C14H23NOS2. М285.