Результат интеллектуальной деятельности: КАТАЛИЗАТОР, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И СПОСОБ ФОТОКАТАЛИТИЧЕСКОГО ПОЛУЧЕНИЯ ВОДОРОДА
Вид РИД
Изобретение
Изобретение относится к области фотокатализа и может найти применение в процессах фотокаталитического выделения водорода из водных растворов неорганических веществ под действием видимого излучения.
Использование в качестве доноров электронов растворов неорганических веществ, таких как Na2S/Na2SO3 [Li Q., Meng H., Zhou P., Zheng Y., Wang J., Yu J., Gong J.R. // ACS Catal. 2013. V. 3. №5. P. 882] или Na2S/K2SO3 [Chen J., Lin Sh., Yan G., Yang L., Chen X. // Catal. Commun. 2008. V. 9. №1. P. 65], является выгодным с практической точки зрения, поскольку для получения таких растворов необходим сероводород, являющийся побочным продуктом переработки нефти, производства стали, дубления кож и отходом целлюлозно-бумажной промышленности. Кроме этого, совмещение процессов очистки растворов от сероводорода и получение водорода при освещении видимым светом экологически выгодно.
Наиболее активными фотокатализаторами выделения водорода из водных растворов Na2S/Na2SO3 являются твердые растворы сульфидов кадмия и цинка состава Cd0.3Zn0.7S [Козлова Е.А, Любина Т.П. // Кин. Кат. 2012. Т. 53. №2. С. 188]. Основным недостатком таких фотокатализаторов являются низкие каталитическая активность и фотостабильность. Для того чтобы повысить эти параметры, необходимо модифицировать методы приготовления катализаторов и вводить сокатализаторы.
Наиболее активные сокатализаторы - благородные металлы: платина, палладий, рутений, золото [Sathish M., Viswanathan В., Viswanath R.P. // Int. J. Hydrogen Energy. 2006. V. 31. №7. P. 891], однако их высокая стоимость ограничивает практическое применение.
Известны фотокатализаторы состава Cd1-xZnxS с добавками сульфидов Me, где Me - Mo, V, Al, Cs, Ti, Μn, Fe, Pd, Pt, P, Cu, Ag, Ir, Sb, Pb, Ga, и нанесенными благородными металлами, такими как Pt, Ru, Ir, Со, Rh, Cu, Pd, Ni, и нанесенными оксидами этих металлов [RU 2199390, B01J 27/04, C01B 3/06, 27.02.2001; RU 2238145, B01J 27/04, C01B 3/06, 20.06.2003; RU 2175888, B01J 27/04, C01B 3/06, 20.11.2001; CA 2332544, B01J 23/06, 22.02.2000], Cd1-xHgxS, Cd1-xZnxS с нанесенными металлами - Pt, Ni, Ru, Os [ЕР 0100299B1, C01B 3/04, B01J 27/02]. Получение фотокатализаторов в приведенных выше случаях происходит путем осаждения сульфидов из смеси растворов солей цинка, кадмия и Me, где Me - Mo, V, Al, Cs, Ti, Μn, Fe, Pd, Pt, P, Cu, Ag, Ir, Sb, Pb, Ga, водным раствором сульфида натрия или газообразным H2S с дальнейшей сушкой и нанесением благородных металлов.
Известны способы получения фотокатализаторов, не содержащих благородных металлов, состава CuS (у) - Zn1-xCdxS, где x - содержание кадмия в твердом растворе (0.3<x<0.8), у - мольная доля меди (0%<у<15.8%) [Zhang W., Rong Χ. // Int. J. Hydrogen Energy. 2009. V. 34. №20. P. 8495], и yCuS/Cd0.3Zn0.7S, где у - мольная доля меди (0<у<0.1) [Markovskaya D.V., Cherepanova S.V., Saraev Α.Α., Gerasimov Ε. Yu., Kozlova Ε.Α. // Chem. Eng. J. 2015. P. 146]. Однако сравнительные эксперименты показали, что фотокатализаторы 0.1% NiS/Cd0.4Zn0.6S являются более активными, чем 0.1% CoS/Cd0.4Zn0.6S и 0.1% CuS/Cd0.4Zn0.6S, следовательно, применение никелевых сокатализаторов более выгодно для практических целей [Wang J., Li В., Chen J., Li Ν., Zheng J., Zhao J., Zhu Ζ. // Appl. Surf. Sci. 2012. V. 259. P. 118].
В литературе описаны сокатализаторы на основе гидроксидов переходных металлов (меди, никеля, железа и кобальта), при этом наибольшую активность показали фотокатализаторы Ni(OH)2/TiO2 и Cu(ОН)2/TiO2 [Υan Ζ., Yu X., Zhang Y., Jia H., Sun Ζ., Du P. // Appl. Cat. В. 2014. V. 160-161. P. 173].
Известно применение гидроксида никеля в качестве сокатализаторов для сульфидных композитных систем [Ran J., Yu J., Jaroniec M. // Green Chem. 2011. V. 13. №10. P. 2708]. Комплексный анализ различных сокатализаторов на основе соединений никеля (Ni, NiO, Ni(OH)2, NiS) также описан в литературе, причем каталитическая активность выделения водорода из водного раствора триэтаноламина снижалась в ряду 0.6% Ni(OH)2/Zn0.8Cd0.2S>0.6% Ni/Zn0.8Cd0.2S>0.6% NiS/Zn0.8Cd0.2S>0.6% NiO/Zn0.8Cd0.2S>Zn0.8Cd0.2S [Ran J., Zhang J., Yu J., Qiao S.Ζ. // Chemsuschem. 2014. V. 7. №12. P. 3426].
Наиболее близкими к данному изобретению являются фотокатализаторы 0.6% Ni(OH)2/Zn0.8Cd0.2S и 0.6% NiO/Zn0.8Cd0.2S [Ran J., Zhang J., Yu J., Qiao S.Ζ. // Chemsuschem. 2014. V. 7. №12. P. 3426]. Основным недостатком последних фотокатализаторов является исследование их активности только в органических средах, соответственно, остаются невыясненными возможность переноса этой зависимости на неорганическую донорную систему Na2S/Na2SO3 и максимально достигаемая каталитическая активность в такой системе. Существенным недостатком известных катализаторов является также сложный метод синтеза с применением автоклавирования и термопрограммируемого нагрева.
Изобретение решает задачу повышения эффективности работы катализатора и упрощения методики его приготовления.
Технический результат - высокая активность в процессе фотокаталитеского получения водорода из водного раствора Na2S/Na2SO3 под действием видимого излучения.
Задача решается катализатором для процесса фотокаталитического получения водорода из водных растворов неорганических веществ под действием видимого излучения следующего состава: x%MO/M(OH)2/Cd0.3Zn0.7S, где M=Cu, Ni, x - массовая доля нанесенного сокатализатора, равная 0,06-1,0.
Задача решается также способом приготовления этого катализатора, заключающимся в том, что на поверхность твердого раствора сульфидов кадмия и цинка состава Cd0.3Zn0.7S наносят гидроксид никеля или меди путем осаждения растворимой соли гидроксидом натрия. Сушка при 80°С позволяет получить смесь МО/М(ОН)2 (М=Cu, Ni) на поверхности твердого раствора сульфида кадмия и цинка.
Задача решается также способом получения водорода из водного раствора Na2S/Na2SO3 под действием видимого излучения, который осуществляют в присутствии фотокатализатора следующего состава: x%MO/M(OH)2/Cd0.3Zn0.7S, где M=Cu, Ni, x - массовая доля нанесенного сокатализатора, равная 0,06-1,0.
Оксиды меди и никеля являются полупроводниками, поэтому в изучаемых системах возможны гетеропереходы, увеличивающие скорость фотокаталитического процесса [Helaili Ν., Bessekhouad Y., Bouguelia Α., Trari M. // J. Hazard. Mat. 2009. V. 168. №1. P. 484; Ji Z., Natu G., Wu Y. // ACS Appl. Mater. Inter. 2013. V. 5. №17. P. 8641; Reguig Β.Α., Khelil A., Cattin L., Morsli M., Bernede J.С. // Appl. Sur. Sci. 2007. V. 253. №9. P. 4330].
Гидроксиды никеля и меди вовлекают фотогенерированные заряды в химические превращения, повышая разделение зарядов и время их жизни [Не Н., Xiao P., Zhou M., Zhang Y., Lou Q., Dong Χ. II Int. J. Hydrogen Energy. 2012. V. 37. №6. P. 4967; Kaluta S., Abe T. // Electrochemical and Solid State Letters. 2009. V. 12. №3. P. Р1]. К тому же, одновременное присутствие в системе оксидов и гидроксидов переходных металлов может приводить к синергетическому эффекту, как в случае многокомпонентных фотокатализаторов Pt/Cd1-xZnxS/ZnO/ε-Zn(OH)2/2D β-Ζn(ΟΗ)2 [Kozlova Ε.Α., Markovskaya D.V., Cherepanova S.V., Saraev Α.Α., Gerasimov Ε. Yu., Perevalov T.V., Kaichev V.V., Parmon V.N. // Int. J. Hydrogen Energy. 2014. V. 39. №33. P. 18758]. Перечисленные выше эффекты позволяют достичь образцам состава NiO/Ni(OH)2/Cd0.3Zn0.7S и CuO/Cu(OH)2/Cd0.3Zn0.7S высокой каталитической активности.
Сущность изобретения иллюстрируется следующими примерами.
Примеры 1-4 (сравнительные)
Пример 1
Готовят растворы Zn(NO3)2, CdCl2, NaOH, Na2S с концентраций 0.1 моль/л. В коническую колбу объемом 500 мл помещают 30 мл раствора хлорида кадмия и 70 мл раствора нитрата цинка, перемешивают в течение 5 мин. Затем добавляют в колбу 100 мл раствора гидроксида натрия, полученную суспензию перемешивают 20 мин, после чего добавляют 150 мл сульфида натрия. Процесс перемешивания продолжают в течение 1 ч, после чего осадок промывают несколько раз дистиллированной водой и сушат при температуре 80°С на воздухе.
Получают катализатор состава: Cd0.3Zn0.7S.
Пример 2
Аналогичен примеру 1, кроме того, что на полученный высушенный осадок наносят металлическую медь по следующей методике: 0.4 г Cd0.3Zn0.7S суспендируют в 10 мл воды, после чего по каплям добавляют 63 мкл раствора нитрата меди с концентрацией 0.1 моль/л, смесь перемешивают 5 мин и добавляют избыток боргидрида натрия (2.5 по молям). Перемешивание продолжают в течение 0.5 ч, после чего осадок промывают дистиллированной водой и сушат при температуре 80°С на воздухе.
Получают катализатор состава 0.1% CuZCd0.3Zn0.7S.
Пример 3
Аналогичен примеру 2, кроме того, что вместо раствора нитрата меди добавляют 832 мкл раствора хлорида никеля, а вместо боргидрида натрия используют раствор сульфида натрия с концентрацией 0.1 моль/л.
Получают катализатор состава: 1% NiS/Cd0.3Zn0.7S.
Примеры 4-6 иллюстрируют предлагаемое техническое решение.
Пример 4
Готовят растворы Zn(NO3)2, CdCl2, NaOH, Na2S с концентраций 0.1 моль/л. В коническую колбу объемом 500 мл помещают 30 мл раствора хлорида кадмия и 70 мл раствора нитрата цинка, перемешивают в течение 5 мин. Затем добавляют в колбу 100 мл раствора гидроксида натрия, полученную суспензию перемешивают 20 мин, после чего добавляют 150 мл сульфида натрия. Процесс перемешивания продолжают в течение 1 ч, после чего осадок промывают несколько раз дистиллированной водой и сушат при температуре 80°С на воздухе.
На полученный высушенный осадок наносят металлическую смесь оксида и гидроксида никеля по следующей методике: 0.4 г Cd0.3Zn0.7S суспендируют в 10 мл воды, после чего по каплям добавляют 300 мкл раствора хлорида никеля с концентрацией 0.1 моль/л, смесь перемешивают 5 мин и добавляют трехкратный избыток NaOH с концентрацией 0.1 моль/л. Перемешивание продолжают в течение 0.5 ч, после чего осадок промывают дистиллированной водой и сушат при температуре 80°С на воздухе.
Получают катализатор состава: 0.06% NiO/Ni(OH)2/Cd0.3Zn0.7S.
Пример 5
Аналогичен примеру 4, кроме того, что вместо хлорида никеля добавляют 63 мкл нитрата меди с концентрацией 0.1 моль/л.
Получают катализатор состава: 0.1% CuO/Cu(OH)2/Cd0.3Zn0.7S.
Пример 6
Аналогичен примеру 4, кроме того, что объем раствора хлорида никеля равен 5 мл.
Получают катализатор состава: 1.0% NiO/Ni(OH)2/Cd0.3Zn0.7S.
Каталитические свойства катализаторов приведены в таблице.
Способ получения водорода из водного раствора Na2S/Na2SO3 под действием видимого излучения проводят при следующих условиях: C(Na2S)=0.1 М, C(Na2SO3)=0.1 М, Скат=0.5 г/л, Vсуспензия=0.1 л, Т=20°С, источник освещения - светодиод 450 LED (30 Вт, 32.7 мВт/см2), один цикл освещения длился 1.5 ч.
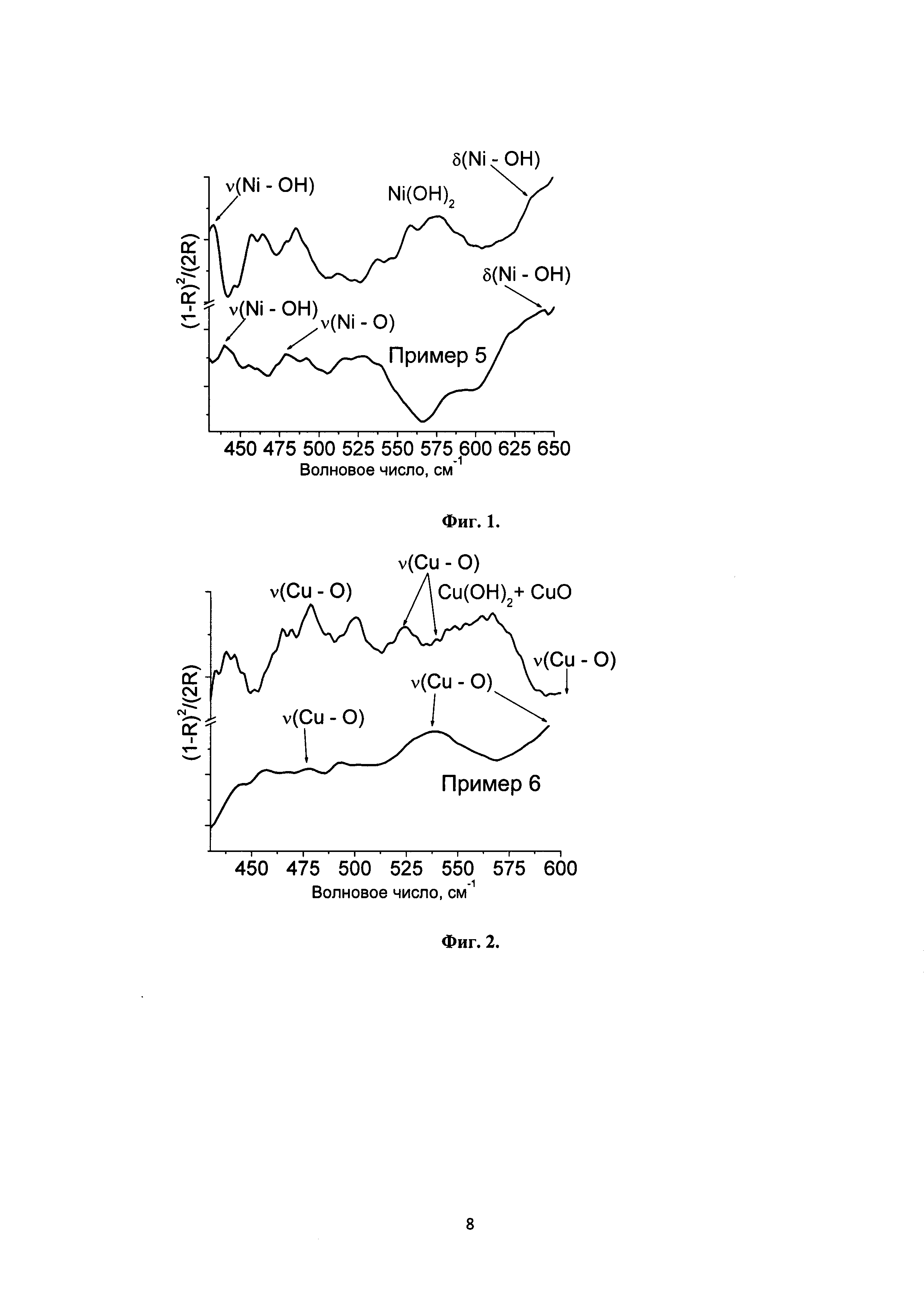
Данные ИК-спектроскопии, подтверждающие фазовый состав нанесенных компонентов, показаны на Фиг. 1 (ИК-спектр Ni(OH)2 и нанесенного никельсодержащего фотокатализатора в области 430-650 см-1) и Фиг. 2 (ИК-спектр Cu(ОН)2 и нанесенного медьсодержащего фотокатализатора в области 430-650 см-1).
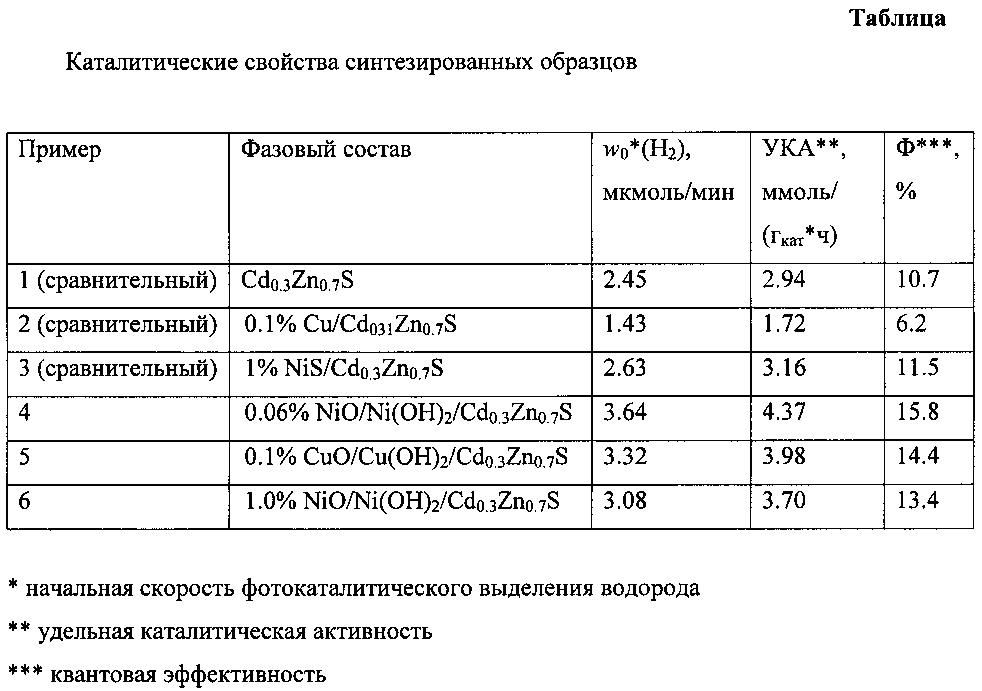
Видно, что нанесение смеси оксидов и гидроксидов никеля повышает активность твердого раствора Cd0.3Zn0.7S в фотокаталитическом выделении водорода, при этом нанесение металла (пример 2) или сульфида металла (пример 3) понижает или не влияет на активность твердого раствора.