Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ МИКРОКАПСУЛИРОВАННОЙ ФОРМЫ ТЕРАПЕВТИЧЕСКОГО ПЕПТИДА ДЛЯ ПЕРОРАЛЬНОГО ПРИМЕНЕНИЯ
Вид РИД
Изобретение
Предложение относится к области высокомолекулярной химии и фармакологии и предназначено для использования в качестве микрокапсулированной формы терапевтического пептида для перорального применения. В качестве целевого пептида используют U2 с ММ 1660 Да и изоточкой pI=9.0.
Препарат U2 - линейный ундекапептид (состоящий из 11 аминокислот) обладает нейропротективным действием, стимулирует когнитивные функции мозга. В настоящее время не известны препараты U2 для перорального применения. Для пероральных лекарственных форм необходимо обеспечить устойчивость в кислой среде желудка и в щелочной среде кишечника. Для пептидных лекарственных форм существенную опасность представляют протеолитические ферменты желудка - пепсин и кишечника - трипсин, химотрипсин, эластаза и др.
Функции пептидов в организме человека достаточно широки - от высокоспецифических антибиотиков или цитотоксичных противоопухолевых лекарств до гормонов, нейропептидов и иммуномодуляторов. Преимущества терапевтических пептидов в их высокой эффективности и минимуме побочных эффектов. Многие пептидные лекарства благодаря успехам биотехнологии производят в промышленных масштабах. До последнего времени инъекционный путь введения терапевтических пептидов оставался единственным вариантом из-за их низкой биодоступности при пероральном приеме. Если учесть, что прием пептидных лекарственных средств показан, в основном, при хронических заболеваниях, то понятно, что пациенты (которые будут избавлены от проблем с обеспечением стерильности и приобретут независимость от медперсонала) могут только приветствовать разработку пероральных вариантов пептидных лекарств. Основными препятствиями на этом пути являются: разрушение пептидов в кислой среде желудка и их энзиматическое разрушение в желудке и кишечнике. Проницаемость сквозь слизистую кишечника пептидных молекул также невысока.
В литературе предложен ряд вариантов повышения биодоступности пептидных лекарств: физико-химическая модификация пептидов, введение ингибторов пептидаз, использование мукоадгезивных полимеров, использование «усилителей адсорбции» и, наконец, использование различных систем доставки.
В качестве одного из вариантов носителей для пероральной доставки пептидов могут служить оболочки спор плауна булавовидного Lycopodium clavatum. Оболочки ликоподия (ОЛ) обладают жесткой регулярной структурой, нетоксичны, недороги, их диаметр равен 25 мкм, внутренний объем 1 г ОЛ составляет 3 см3 [S. Barrier, Physical and chemical properties of sporopollenin exine particles. PHD Thesis, Univer. of Hull, 2008, 348 p., https://hydra.hull.ac.uk/resources/hull:6412].
Известны способы использования ОЛ в качестве носителя в пероральных системах доставки красителей, пептидов и белков [S. Barrier, A. Diego-Taboada, М.J. Thomasson, L. Madden, J.С. Pointon, J.D. Wadhawan, S.T. Beckett, S.L. Atkin and G. Mackenzie. Viability of plant spore exine capsules for microencapsulation, J. Mater. Chem., 21 (2011) 975-981], полиненасыщенных жирных кислот [A. Wakil, G. Mackenzie, A. Diego-Taboada, J.G. Bell, S.L. Atkin. Enhanced bioavailability of eicosapentaenoic acid from fish oil after encapsulation within plant spore exines as microcapsules, Lipids, 45 (2010) 645-649], антител [S.U. Atwe, Y. Ma, H.S. Gill. Pollen grains for oral vaccination Journal of Controlled Release, 194 (2014) 45-52] и других лекарственных и пищевых соединений. Группой ученых из университета Hull (UK) оформлены патенты на композиции, включающие оболочки спор природного происхождения, в которые различными путями (пассивным насыщением, вакуумированием или под давлением) вводят разнообразные активные субстанции (в том числе пептиды и ферменты). Для защиты активных субстанций в процессе совместного инкапсулирования вводят добавки, обеспечивающие физический или химический барьер между активной субстанцией и изменяющимися внешними условиями. Защитные добавки могут быть самой разной структуры, например синтетические полимеры, липиды, материалы с липидными компонентами, желатин, природные полимеры, в том числе полисахариды и целлюлозные материалы. Пути доставки активной субстанции при помощи заявленной композиции предлагаются всевозможные - от перорального до ректального [US 20110002984, 2011-01-06, Formulations comprising exine shells; US 20130309298, 2013-11-21, Formulations comprising exine shells].
Наиболее близким по сущности является способ получения пероральных инкапсулированных пептидных гормонов: энфувритида и гормонов роста человека, заключающийся в насыщении ими при вакуумировании оболочки ликоподия с последующим нанесением на поверхность оболочек ликоподия различных природных соединений: крахмала, гуммиарабика, масла какао, пчелиного воска, шеллака и масла печени трески и др. [L.J. Blackwell, Sporopollenin exines as a novel drug delivery system. PHD Thesis, Univ. of Hull, 2007, 215 p., https://hydra.hull.ac.uk/resources/hull:7162].
Существенным недостатком этого способа получения пероральной микрокапсулированной лекарственной формы является то, что ни одно из использованных покрытий не обеспечивает одновременно защиту инкапсулированного гормона роста в растворе, моделирующем желудочную среду, и постепенное высвобождение его в сыворотку крови. Отметим, что поведение инкапсулированных пептидов вообще не исследовали в растворе, моделирующем кишечную среду.
Технической задачей и положительным результатом заявляемого способа является разработка методики получения микрокапсулированной формы терапевтического пептида U2 (линейного ундекапептида с изоточкой pI=9.0, и ММ=1660 Да, обладающего нейропротективным действием, стимулирующего когнитивные функции мозга) для перорального применения в виде двухуровневой микрокапсулы, обладающей устойчивостью к воздействию кислой среды желудка и с пролонгированным выделением в щелочную среду кишечника, а для защиты пептида U2 от кишечных пептидаз в препарат введен ингибитор пептидаз - овомукоид (ОМ).
Указанная задача и технический результат достигается в способе получения микрокапсулированной пероральной формы терапевтического пептида, включающем формирование двухуровневой микрокапсулы, при этом обеспечивается раздельное введение целевого пептида и ингибитора пептидаз - ОМ. Пептид включают в носители первого уровня - оболочки ликоподия, с последующим включением во вторичную оболочку - альгинатную микрокапсулу (АМК), формируемую методом ионотропной сшивки и содержащую ингибитор пептидаз - ОМ. А именно: используемый в качестве целевого пептида ундекапептид U2 вводят в оболочки ликоподия (ОЛ) методом центрифугирования суспензии ОЛ с концентрацией 2 мг/мл в растворе пептида U2 с концентрацией 0,4 мг/мл при скорости вращения 7000 об/мин в течение 30 мин, осадок отфильтровывают и сушат при комнатной температуре. Для подавления пептидазной активности в кишечной среде при пероральном приеме в систему введен ингибитор пептидаз - овомукоид, который добавляют независимо от ОЛ, содержащих пептид U2, в альгинатные микрокапсулы, служащие наружной оболочкой для ОЛ, которые формируют методом ионотропной сшивки, согласно следующей процедуре: дисперсию ОЛ в 3% растворе альгината натрия, содержащего 10 мг/мл ОМ, не более 20 мг ОЛ в 1 мл раствора, вводят при перемешивании по каплям в осадительную ванну, содержащую 1% раствор CaCl2 в 0.5% растворе хитозана в 1% уксусной кислоте, затем фильтруют на воронке Бюхнера, промывают водой и сушат при комнатной температуре; размеры полученных таким способом альгинатных микрокапсул составляют 800-900 мкм, включение пептида U2 и ОМ в них составляет 20-30 мкг/мг и 10-20 мкг/мг, соответственно.
Незначительный разброс размеров формируемых АМК обусловлен методикой их получения, а именно - многопараметрическим процессом осаждения в ходе ионотропной сшивки. Включение активных соединений в микрокапсулы связаны с незначительными потерями (диффузией инкапсулируемых объектов в окружающий раствор), которые пропорциональны площади поверхности АМК, отсюда следует разброс в значениях включения пептида и ОМ.
Более полно способ инкапсулирования пептида U2 излагается в приводимом ниже примере. Для реализации примера в качестве носителей первого уровня использовали оболочки спор Lycopodium clavatum, которые получали методом освобождения от клеточного содержимого спор ликоподия (Lycopodium clavatum). Использована модифицированная методика из [S. Barrier, A. Diego-Taboada, М.J. Thomasson, L. Madden, J.С. Pointon, J.D. Wadhawan, S.T. Beckett, S.L. Atkinad and G. Mackenzie. Viability of plant spore exine capsules for microencapsulation, J. Mater. Chem., 21 (2011) 975-981], которая заключается в следующем: 250 г ликоподия суспендируют в 750 мл ацетона, перемешивают в течение 4 часов. Отфильтровывают, сушат на воздухе, затем суспендируют в 750 мл 6% раствора КОН и перемешивают в течение 6 часов. После фильтрации операцию повторяют, после этого отфильтровывают, промывают горячей водой (трижды по 300 мл) и горячим этанолом (трижды по 300 мл), сушат на воздухе. Далее суспендируют в 750 мл 85 об. % раствора ортофосфорной кислоты и перемешивают в течение 7 дней. Отфильтровывают, промывают водой (5 раз по 250 мл), ацетоном (250 мл), 2М HCl (250 мл), 2М NaOH (250 мл), водой (5 раз по 250 мл), ацетоном (250 мл), этанолом (250 мл) и высушивают при T=60°C.
В экспериментах использовали следующие реактивы: ликоподий (споры плауна булавовидного Lycopodium clavatum) ГОСТ 22226-76 (Реахим, Россия), пептид U2 (синтезирован в ГосНИИ ОЧБ, Россия), овомукоид (Реахим, Россия), кальций хлористый безводный - puriss р.а, (Sigma-Aldrich), одно- и двузамещенный натрия фосфат - чда (Реахим, Россия), кислоты: уксусная, серная, ортофосфорная, соляная, ацетон, этанол, уксусный ангидрид, гидроокись натрия, гидроокись калия - все чда (Вектон, Россия), вода деионизованная extra pure reagent grade III (Acros Organics), альгинат Na низковязкий медицинский (Архангельский комбинат), хитозан кислоторастворимый ММ=220 кДа (Sigma-Aldrich)
Пример. Двухуровневые АМК, содержащие на первом уровне ОЛ с включенным в них пептидом U2, а на втором - внешнем уровне альгинатной оболочки, содержащие ингибитор пептидазных ферментов, находящихся в кишечнике - трипсина, химотрипсина и эластазы, - ОМ, получают следующим образом. На первом уровне инкапсулирования осуществляют включение пептида U2 в оболочки ликоподия. Навеску ОЛ 20 мг помещают в центрифужную пластиковую пробирку с завинчивающейся пробкой, заливают 10 мл раствора пептида U2 в концентрации 0,4 мг/мл, параллельно ставят холостую пробу: такую же навеску ОЛ заливают 10 мл дистиллированной воды. Центрифугирование обеих суспензий проводят при скорости 7000 об/мин в течение 30 минут. Затем ОЛ фильтруют на фильтрах Шотта (№16) и сушат на воздухе в течение 24 часов. Содержание белковых препаратов в ОЛ рассчитывают по формуле:
[(Cисх-Cост)×V/m]×1000 мкг/мг ОЛ,
где Cисх - исходная концентрация пептида, мг/мл,
Cост - концентрация пептида в супернатанте после центрифугирования, мг/мл,
V - объем центрифугируемого раствора, мл,
m - навеска ОЛ, мг.
Концентрацию белка и пептида в растворах определяют на основании калибровочной концентрационной зависимости спектрофотометрически при λ=280 нм, в качестве раствора сравнения используют супернатант холостой пробы.
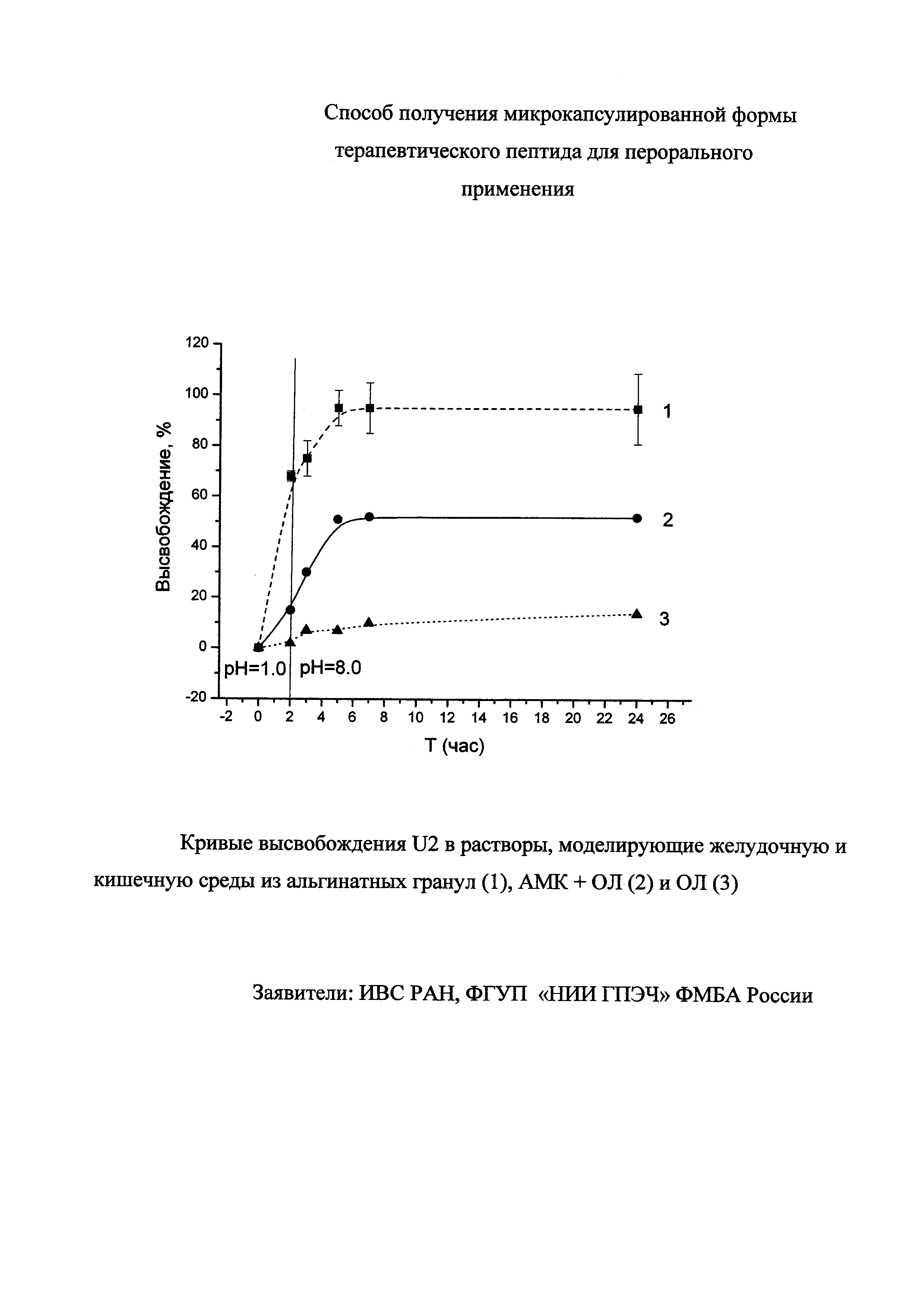
Введение ингибитора пептидаз ОМ на втором уровне инкапсулирования проводят в процессе формирования АМК методом ионотропной сшивки. Дисперсию ОЛ (не более 20 мг на 1 мл раствора) в 3% растворе альгината натрия, содержащего 10 мг/мл ингибитора пептидаз, вводят при перемешивании по каплям в осадительную ванну, содержащую 1% водный раствор CaCl2. Для улучшения качества поверхности АМК вводят добавки хитозана, для этого осадительная ванна CaCl2 содержала 0.5% раствор хитозана в 1% уксусной кислоте. При попадании в ванну альгинат натрия в составе капли пространственно сшивается двухвалентными ионами кальция, образуя прочную эластичную АМК, внутри которой заключены ОЛ с пептидом. Затем АМК фильтруют, промывают водой и сушат при комнатной температуре. Размеры АМК составляют 800-900 мкм. Полученные АМК являются основным компонентом перорального препарата U2 пролонгированного действия. Включение U2 и ОМ в предлагаемые системы составляет 20-30 мкг/мг и 10-20 мкг/мг соответственно. Кривые высвобождения U2 в растворы, моделирующие желудочную и кишечную среды, из двухуровневой системы, а также из ОЛ - системы первого уровня и из альгинатных гранул без ОЛ приведены на чертеже.
Как видно из приведенных данных, высвобождение пептида U2 в раствор, моделирующий желудочную среду - 0.1М HCl pH 1.0 (РМЖ), и в раствор, моделирующий кишечную среду - Na фосфатный буфер, pH 8.0 (РМК), из носителя первого уровня - оболочек ликоподия крайне незначительно в обоих случаях. Вероятное объяснение - взаимодействие положительно заряженного пептида (pI=9.0) с ОЛ.
Из альгинатных гранул без ОЛ пептид высвобождается интенсивнее. За 2 часа в кислую среду РМЖ высвобождается 68% пептида, а за 3 часа в слабощелочную среду РМК - всего 27%. Альгинат Na в кислой среде протонирован, поэтому электростатические взаимодействия между U2 и альгинатом отсутствуют. Структура АМК - пористая, размеры пор, согласно [Gaserod О., Smidsrod О., Skjak-Braek G. Microcapsules of alginate-chitosan. A quantitative study of the interaction between alginate and chitosan, Biomaterials, 19 (1998) 1815-1825] имеют широкий разброс и составляют 10-100 нм. В таких порах не задерживаются маленькие молекулы пептида U2 с ММ=1660 Да.
Профили высвобождения U2 из заявляемой двухуровневой системы свидетельствует о сохранении целевого объекта в РМЖ (высвобождение не более 15%). В РМК U2 высвобождается на 35% за 6 часов, что обеспечивает пролонгированное действие препарата.
Предложен многофункциональный вариант пероральной двухуровневой системы доставки пептидных и белковых препаратов. Изложенная методика позволяет получить препарат, обладающий следующими положительными характеристиками: пероральная форма приема препарата U2 намного удобнее, чем парентеральная, как для пациента, так и для персонала. При производстве пероральных форм требования к стерильности производства менее жесткие, чем при производстве парентеральных форм. PH-зависимая альгинатная оболочка (второй уровень многофункциональной системы доставки) защищает ЦО от воздействия ферментов и кислой среды желудка, постепенно растворяясь в щелочной среде кишечника, что обеспечивает пролонгацию действия ЦО. Пролонгированное действие препарата, позволяет сократить количество приемов лекарственного средства. Добавленный в альгинатную матрицу ингибитор кишечных пептидаз должен защитить ЦО во время его высвобождения из системы доставки в кишечнике. Помимо этого альгинат (в особенности в комплексе с хитозаном) обладает хорошими мукоадгезивными свойствами, удерживая ЦО непосредственно вблизи мукозальной поверхности, увеличивая вероятность его проникновения в кровяное русло. ОЛ - носитель первого уровня фиксирует ЦО, не позволяя ему диффундировать сквозь поры альгинатной матрицы до попадания в щелочную среду кишечника.
Способ получения микрокапсулированной формы терапевтического пептида для перорального применения, включающий формирование двухуровневой микрокапсулы, содержащей внутри целевой пептид, введенный в оболочки спор ликоподия, отличающийся тем, что в качестве целевого пептида используют ундекапептид U2 с ММ 1660 Да и вводят его в оболочки ликоподия (ОЛ) методом центрифугирования суспензии ОЛ с концентрацией 2 мг/мл в растворе пептида U2 с концентрацией 0,4 мг/мл при скорости вращения 7000 об/мин в течение 30 мин, осадок отфильтровывают и сушат при комнатной температуре; для подавления пептидазной активности в кишечной среде при пероральном приеме в систему введен ингибитор пептидаз - овомукоид (ОМ), который добавляют независимо от ОЛ, содержащих пептид U2, в альгинатные микрокапсулы, служащие наружной оболочкой для ОЛ, которые формируют методом ионотропной сшивки, согласно следующей процедуре: дисперсию ОЛ в 3%-ном растворе альгината натрия, содержащего 10 мг/мл ОМ, не более 20 мг ОЛ в 1 мл раствора, вводят при перемешивании по каплям в осадительную ванну, содержащую 1%-ный раствор CaCl в 0.5%-ном растворе хитозана в 1%-ной уксусной кислоте, затем фильтруют на воронке Бюхнера, промывают водой и сушат при комнатной температуре; размеры полученных таким способом альгинатных микрокапсул составляют 800-900 мкм, включение пептида U2 и ОМ в них составляет 20-30 мкг/мг и 10-20 мкг/мг соответственно.