Результат интеллектуальной деятельности: БИС{2-[(2E)-4-ГИДРОКСИ-4-ОКСОБУТ-2-ЕНОИЛОКСИ]-N,N-ДИЭТИЛЭТАНАМИНИЯ} БУТАНДИОАТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ
Вид РИД
Изобретение
Группа изобретений относится к области органической и медицинской химии, а именно: к новому индивидуальному полифункциональному соединению - бис{2-[(2E)-4-гидрокси-4-оксобут-2-еноилокси]-N,N-диэтилэтанаминия} бутандиоату формулы I и способу его получения, которые могут быть использованы в органическом синтезе и в медицине в качестве потенциального нейропротекторного средства.
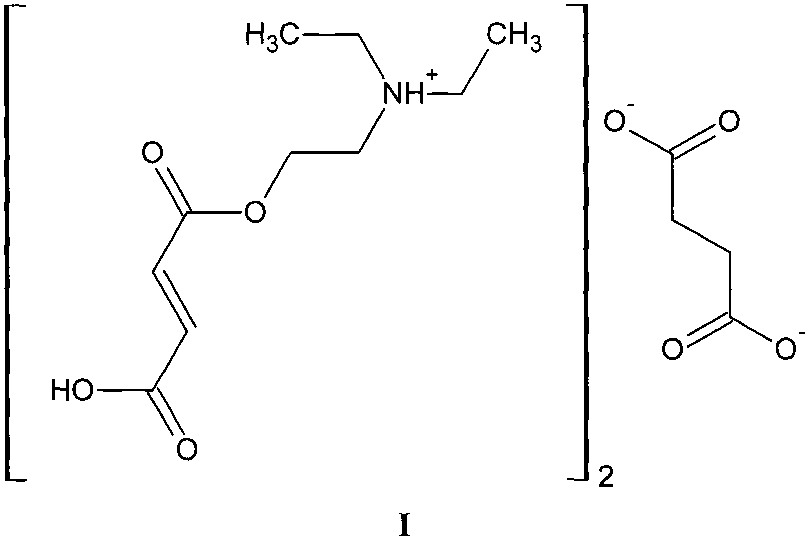
В патентной и научно-технической литературе описаны методы синтеза диэтиламиноэтилового эфира фумаровой кислоты (V), получаемого взаимодействием диэтиламиноэтанола (II) либо с малеиновым ангидридом при кипячении в ксилоле с использованием солей переходных металлов в качестве катализаторов (III) [АС 287925 СССР, МПК C07C. Способ получения аминоалкиловых эфиров фумаровой кислоты], либо с диметилфумаратом (IV) в присутствии о-фенилендиамина и натрия [Пат.2723967 США, C08F 220/44, H01B 3/44. Copolymers of an unsaturated polyester and acrylonitrile]. Недостатком приведенных методов стоит счесть жесткие условия реакции, такие как нагревание до 140-150°C, что может вызывать окисление и полимеризацию продукта реакции. Во избежание этого авторы первого метода прибегают к проведению процесса в инертном газе - азоте, а авторы второго используют ингибитор полимеризации - о-фенилендиамин.
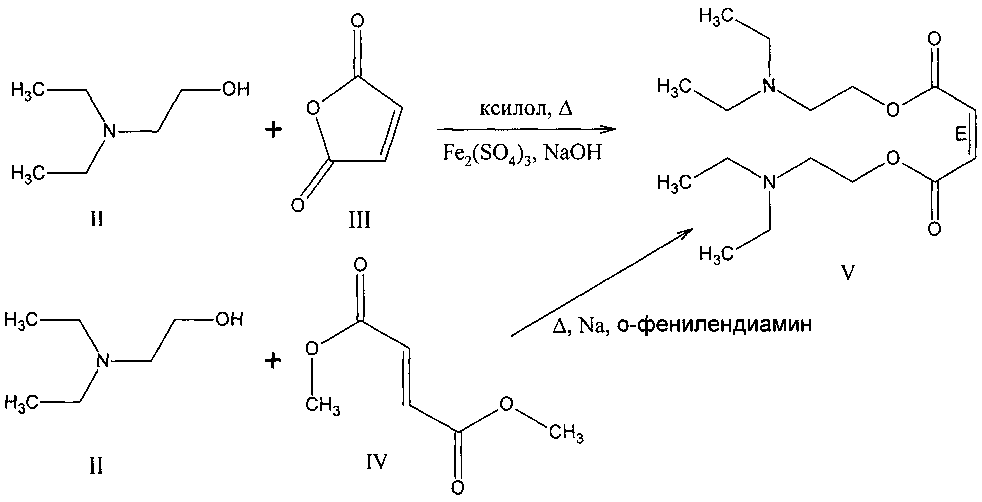
Описан также метод получения аналогичного монодиэтиламиноэтилового эфира, выделяемого в виде гидрохлорида (VII) [Пат. 8669281 США, МПК - 2006.01 A01N 43/36, A61K 31/40, C07D 207/40. Prodrugs of fumarates and their use in treating various diseases]. Метод состоит в ацилировании диэтиламиноэтанола (II) 3-метокси-3-оксоакрилоилхлоридом (VI) в среде метилтретбутилового эфира (МТБЭ).
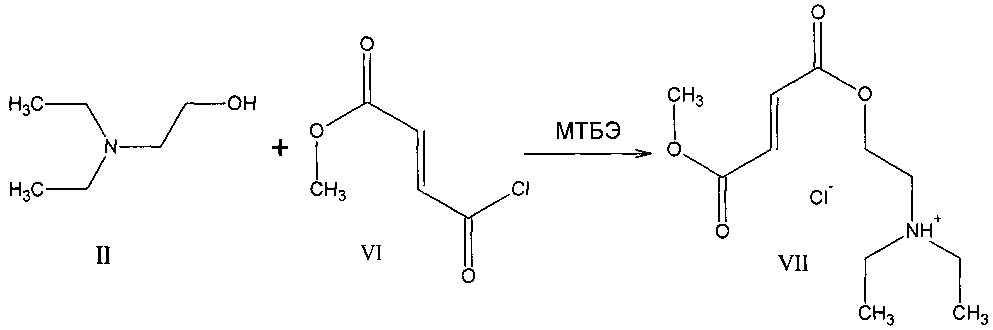
Кроме того, известен сукцинат диметиламиноэтилового эфира янтарной кислоты (X), обладающий адаптогенным и стресс-протективным действием [А.с. 1433957 СССР, МПК4 C07C 69/40, C07C 87/127, A61K 31/22. Сукцинат моно [(2-диметиламино)этилового эфира] янтарной кислоты, обладающий адаптогенным и стресс-протективным действием]. Описанный метод его получения состоит во взаимодействии соответствующего основания (VIII) с янтарной кислотой (IX) в соотношении 2:1 в среде этанола.
Из патентной и научно-технической литературы не выявлены не способ получения нового заявляемого авторами соединения, не сама структура.
Задачей предлагаемой группы изобретений является создание нового неописанного в литературе соединения - бис{2-[(2E)-4-гидрокси-4-оксобут-2-еноилокси]-N,N-диэтилэтанаминия} бутандиоата (I), что позволит расширить ассортимент потенциальных нейропротекторных средств.
Техническими результатами, на решение которых направлена группа изобретений, являются получение нового полифункционального соединения формулы I, которое потенциально может быть использовано в медицине в качестве нейропротекторного средства; разработка простого способа его синтеза.
Поставленная задача осуществляется путем взаимодействия 2-диэтиламиноэтанола (II) с малеиновым ангидридом (III) и янтарной кислотой при соотношении соответственно, моль: 1:1:0,5 в среде безводного апротонного растворителя с последующим получением целевой соли янтарной кислоты по схеме:
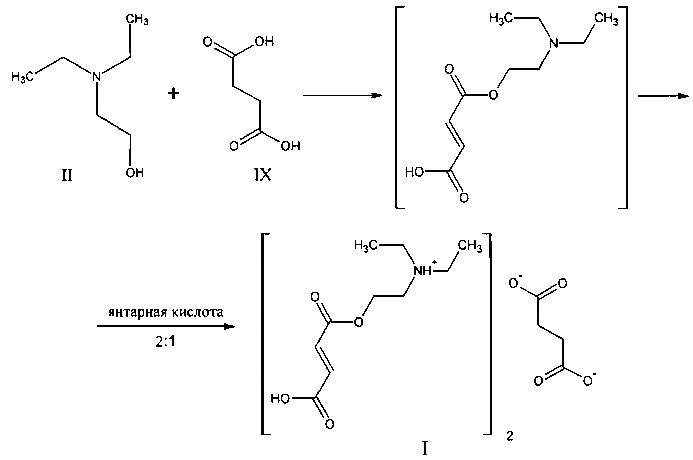 , причем взаимодействие 2-диэтиламиноэтанола и малеинового ангидрида проводят при температуре 50-55°C в течение одного часа, затем прибавляют янтарную кислоту и выдерживают при температуре 50-55°C до полного растворения.
, причем взаимодействие 2-диэтиламиноэтанола и малеинового ангидрида проводят при температуре 50-55°C в течение одного часа, затем прибавляют янтарную кислоту и выдерживают при температуре 50-55°C до полного растворения.
Поставленная задача решается также тем, что выделение целевого продукта осуществляют путем отгонки растворителя под вакуумом.
Способ получения бис{2-[(2E)-4-гидрокси-4-оксобут-2-еноилокси]-N,N-диэтилэтанаминия} бутандиоата изучен и проведен в лабораторных условиях на стандартном товарном сырье. По сравнению с приведенными методами ацилирования 2-диэтиламиноэтанола разработанный метод отличается мягкими условиями реакции и доступными реагентами.
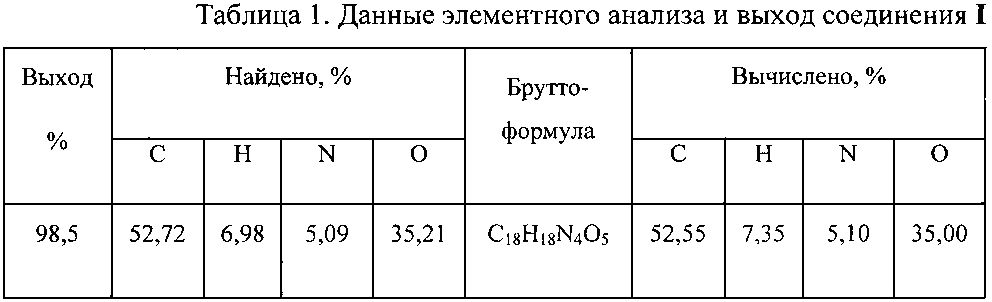
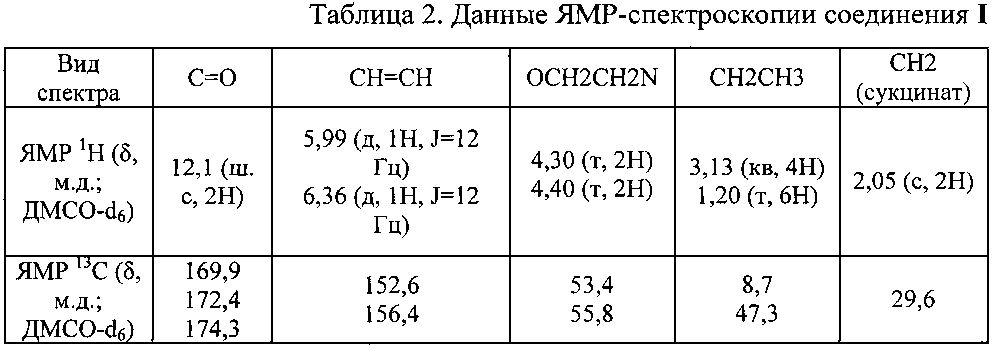
Данные элементного анализа и выход продукта реакции приведены в табл. 1, спектральные характеристики полученного соединения - в табл. 2.
Предлагаемая группа изобретений проиллюстрирована схемой и примерами практического осуществления.
Пример 1
Получение бис{2-[(2E)-4-гидрокси-4-оксобут-2-еноилокси]-N,N-диэтилэтанаминия} бутандиоата (I)
В круглодонную колбу емкостью 500 мл, снабженную обратным холодильником, термометром и механической мешалкой, загружают 100 мл сухого дихлорэтана (х.ч., ТУ 2631-085-44493179-02), в котором растворяют 98 г (1 моль) малеинового ангидрида (ч., ГОСТ 11153-75). Затем при перемешивании прибавляют 117 г (1 моль) осушенного и перегнанного 2-диэтиламиноэтанола (ч., МРТУ 6-09-1311-64). Реакционную массу нагревают до 50-55°C и выдерживают 1 час. Далее прибавляют 59 г (0,5 моль) мелко растертой янтарной кислоты (х.ч., ГОСТ 6341-75) и выдерживают при 50-55°C 1-2 часа до полного растворения. Затем под вакуумом из реакционной смеси отгоняют дихлорэтан. В кубовом остатке находится целевой продукт, представляющий собой бесцветную или желтоватую вязкую некристаллизующуюся жидкость. Выход 270 г (98,5%).
Состав синтезированного соединения подтвержден элементным анализом. Брутто-формула: C18H18N4O5. Найдено, %: C - 52,73, H - 6,98, N - 5,09, O - 35,21. Вычислено %: C - 52,55, H - 7,35, N - 5,11, O - 35,00.
Строение синтезированного вещества было доказано методами 1H- и 13C-ЯМР-спектроскопией.
В спектре ЯМР 1H раствора исследуемого соединения в ДМСО-d6 в слабом поле присутствуют уширенный синглет кислых протонов в области 12,1 м.д. (2H), а также дублеты олефиновых протонов с химическим сдвигом 5,99 (1H) и 6,36 м.д. (1H) и константой спин-спинового взаимодействия 12 Гц, что указывает на транс-конфигурацию двойной связи. В сильном поле спектра находятся сигналы протонов этиленовой (4,30 м.д. (т, 2H) и 4,40 м.д. (т, 2H)) и этильных групп (3,13 м.д. (кв, 4H) и 1,20 м.д. (т, 6H)). Также в сильном поле обнаруживается синглет протонов аниона янтарной кислоты в области 2,05 м.д. с интегральной интенсивностью 2H.
В спектре ЯМР 13С в слабом поле присутствуют сигналы карбоксильных атомов углерода 169,9, 172,4, 174,3 м.д. и олефиновых атомов в области 123,1 и 138,7 м.д. Сигналы с химическими сдвигами 8,7, 47,3, 53,4, 55,8 м.д. принадлежат атомам углерода этильных и этиленовой групп соответственно. Сигналы атомов углерода остатка янтарной кислоты имеют химический сдвиг 29,6 м.д.
Пример 2
Определение острой токсичности
Острую токсичность синтезированного соединения определяли на нелинейных белых мышах-самцах массой тела 18-20 г. Животных распределяли на равные по численности и массе тела группы по 10 животных в каждой. Суспензии соединения в воде, стабилизированные твином-80, вводили однократно внутрибрюшинно в интервале доз 50 мг/кг - 3000 мг/кг. Выживаемость животных определяли, наблюдая через 24 часа и через 48 часов от момента введения исследуемого соединения. Наблюдение за животными осуществляли в течение 72 часов. Регистрировали развитие основных симптомов и время гибели животных.
Соединение отличает высокая безопасность - величину полулетальной дозы (LD50) при пероральном введении мышам обоего пола установить не удалось, она превышает 2000 мг/кг, что позволяет отнести тестируемое соединение к группе мало или умеренно токсичных веществ по различным классификациям.
Пример 3
Определение актопротекторной активности
Для оценки физической работоспособности мелких лабораторных животных (мыши) в работе использовался стандартный для фармакологических исследований метод предельного плавания с нагрузкой. Для его проведения лабораторным животным в области крестца к шкуре прикрепляется груз, составляющий 7,5% от массы тела животного и соответствующий среднему уровню интенсивности аэробно-анаэробной нагрузки.
Для оценки физической работоспособности без учета специфического влияния температурного фактора используется вода термонейтрального диапазона - комнатной температуры (18-22°C). В нашем исследовании использовали именно этот вариант теста - с водой термонейтрального диапазона (18-22°C).
Установлено, что заявляемое средство (доза 75 мг/кг) достоверно (p<0,0001) увеличивало физическую работоспособность мышей на 52% по сравнению с животными контрольной группы и превосходило эффект DMAE + ацетилглутамата (доза 50 мг/кг).
Бис{2-[(2E)-4-гидрокси-4-оксобут-2-еноилокси]-N,N-диэтилэтанаминия} бутандиоат сравним по эффективности с используемыми на практике взятыми отдельно ноотропными, актопротекторными, противогипоксическими препаратами.
![БИС{2-[(2E)-4-ГИДРОКСИ-4-ОКСОБУТ-2-ЕНОИЛОКСИ]-N,N-ДИЭТИЛЭТАНАМИНИЯ} БУТАНДИОАТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ](https://fips.edrid.ru/images/rid/3e/da/4b/6420d2a3d04355dfb70fbdc4bac160de.png)
![БИС{2-[(2E)-4-ГИДРОКСИ-4-ОКСОБУТ-2-ЕНОИЛОКСИ]-N,N-ДИЭТИЛЭТАНАМИНИЯ} БУТАНДИОАТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ](https://fips.edrid.ru/images/rid/3e/da/4b/dce6a6286066d5a40dc85dd97483487d.png)

