Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ ГИДРОКСИДА БЕРИЛЛИЯ ИЗ БЕРИЛЛИЙСОДЕРЖАЩИХ КОНЦЕНТРАТОВ
Вид РИД
Изобретение
Изобретение относится к области получения соединений бериллия, а именно гидроксида бериллия, широко используемого в производстве металлического бериллия, медно-бериллиевой лигатуры, керамики из оксида бериллия и солей бериллия.
Известен ряд методов, описанных в источнике [Блешинский С.В., Абрамова В.Ф., Дружинин И.Г. Химия бериллия. Фрунзе: Академия наук Киргизской ССР, 1955. С. 193]:
- измельченный берилл обрабатывают концентрированным раствором едкого натра, взятым по отношению к бериллу в количестве 1,2-3 весовых частей. При перемешивании массы в течение нескольких часов при температуре 100-400°С берилл разлагается;
- разложение берилла проводят путем обработки раствором едкого натра с концентрацией 50-75% при температуре 175-185°С. Щелок разбавляют водой;
- сплавление измельченной берилловой руды со щелочами с последующим растворением плава в воде.
Известен способ [пат. 2264986 РФ, МПК C01F 3/02] получения гидроксида бериллия из бериллийсодержащих концентратов путем воздействия гидроксида натрия с последующим разделением продуктов реакции. Концентрат или смесь концентратов обрабатывают в автоклаве гидроксидом натрия с концентрацией 400-450 г/дм3 в присутствии оксида кальция при мольном отношении СаО:SiO2=1,1-1,3, температуре 250-260°С и отношении Na2O:ВеО=12-13 в течение 4-5 ч.
Практически эти же параметры вскрытия бертрандит-фенакитового концентрата приведены в отчете [Разработка щелочно-автоклавной очистки бериллиево-флюоритового продукта от фтора и технологии переработки бериллиевого концентрата Ермаковского месторождения с выделением и очисткой гидроксида бериллия: Отчет НИР/ФГУП «ВНИИХТ»; Руководитель М.Л. Коцарь; Инв № ТИ/3506, 2006].
Отчет принят за прототип, поскольку содержит наиболее полные данные, как по технологии щелочного автоклавного вскрытия бериллийсодержащих концентратов, так и дальнейшей переработки растворов бериллата натрия с получением гидроксида бериллия.
Как указано в отчете, оптимальными условиями щелочного автоклавного разложения бертрандит-фенакитового концентрата являются:
- концентрация NaOH - 450 г/дм3;
- каустический модуль Na2O/BeO ~12;
- мольное отношение CaO/SiO2=1,2;
- температура 260°С;
- продолжительность обработки - 4 ч;
- промывка нерастворимого остатка при соотношении Ж:Т=3,5-3,9 при температуре 60°С в течение 0,5 ч.
Технологический раствор после отделения нерастворимого остатка разбавляют конденсатом до остаточной щелочности 170-180 г/дм3 (~ в 2,6 раза), после чего обрабатывают пероксидом водорода для окисления железа и марганца с последующим отделением выделившегося осадка указанных примесей.
Очищенный раствор бериллата натрия разбавляют конденсатом до остаточной концентрации NaOH 29-30 г/дм3 (~ в 5,9 раза), нагревают острым паром до кипения и выдерживают при этой температуре в течение 1 ч. Выделившийся в результате гидролиза гидроксид бериллия отфильтровывают и промывают конденсатом от избытка щелочи. Маточный раствор с концентрацией NaOH ~30 г/дм3 вместе с промывным раствором выпаривают до концентрации NaOH=450 г/дм3 и после отделения содового осадка фильтрованием возвращают на операцию вскрытия концентрата. Извлечение бериллия в гидроксид по данному способу составляет 97-98%.
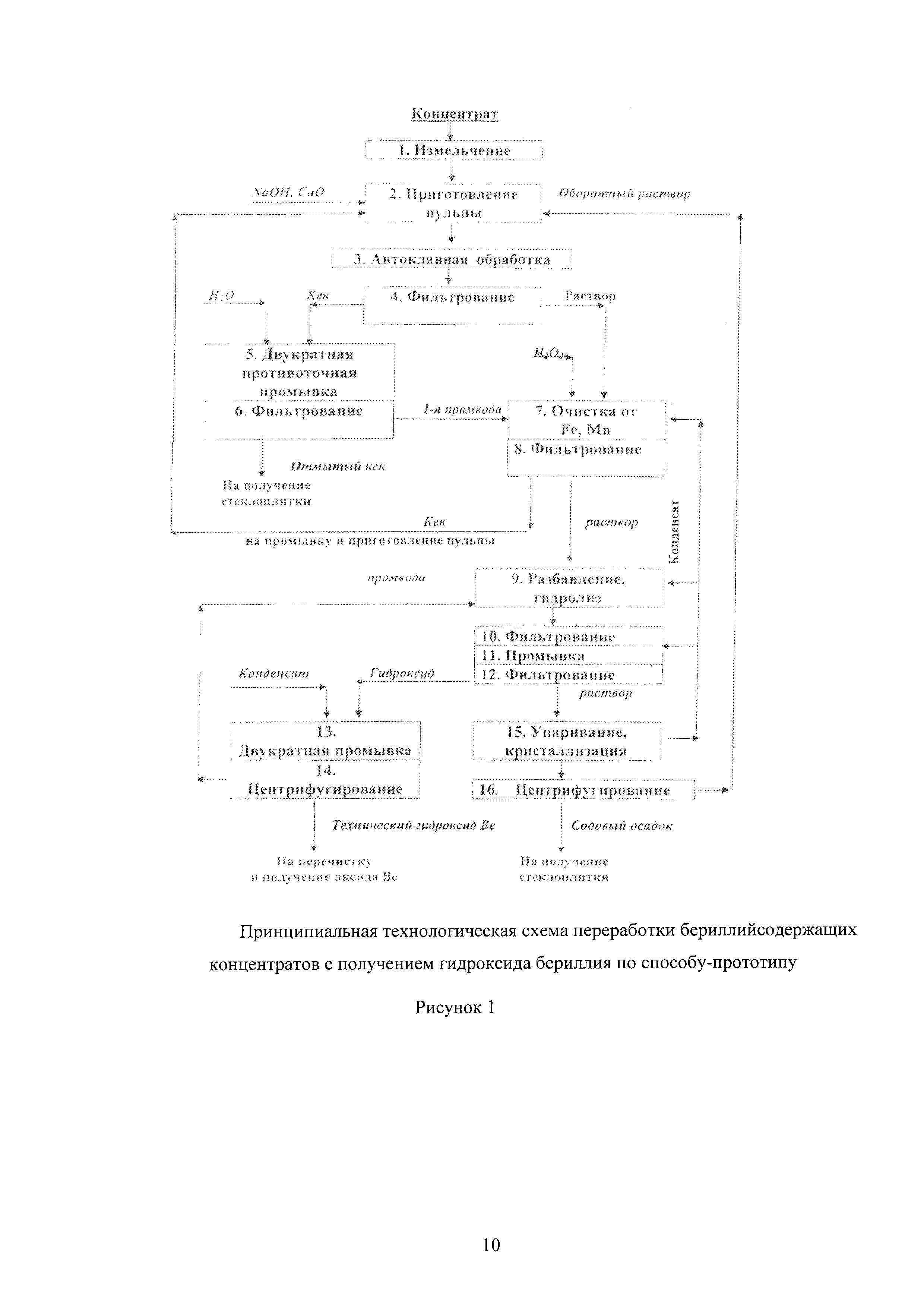
Принципиальная технологическая схема переработки концентратов по способу-прототипу приведена на рисунке 1.
Недостатками указанного способа, принятого за прототип, являются:
- большой расход воды - разбавление в 15 раз основного технологического раствора 450 до 30 г/дм3 NaOH и необходимость ее последующего выпаривания из маточных растворов после выделения гидроксида бериллия с целью концентрирования щелочи с 30 до ~450 г/дм3 NaOH и возврата ее на операцию вскрытия новой порции концентрата. Процесс выпаривания связан со значительными затратами энергии (0,626 кВт·ч/кг воды);
- большое обводнение технологического процесса получения гидроксида бериллия в целом за счет образования в процессе выпарки конденсатов сокового и греющего пара, что предполагает сброс избытка растворов, не замкнутых в технологическом цикле, на хвостохранилище. Это создает дополнительную нагрузку на окружающую среду;
- необходимость применения реагента (пероксида водорода) для очистки технологического раствора от примесей железа и марганца;
- необходимость организации участка фильтрования и промывки от избытка щелочи содового осадка, образующегося в процессе выпаривания щелочного раствора (карбонизация щелочи).
Техническим результатом предлагаемого способа являются снижение энергозатрат, сокращение расхода воды, организация замкнутого водооборота, исключение сброса жидких отходов на хвостохранилище и снижение нагрузки на окружающую среду.
Технический результат данного изобретения достигается за счет того, что в способе получения гидроксида бериллия из бериллийсодержащих концентратов путем воздействия на них концентрированных растворов гидроксида натрия с последующим отделением раствора от кека проводят двухступенчатую электрохимическую нейтрализацию избытка щелочи в анодных камерах электролизеров с выделением нерастворимого осадка гидроксидов железа и марганца между стадиями при концентрации щелочи 170-180 г/дм3, отделяют осадок гидроксида бериллия, образующийся в результате гидролиза бериллата натрия после второй стадии нейтрализации щелочи, а раствор укрепляют до концентрации, требуемой для вскрытия концентрата при прохождении его через катодные камеры электролизеров с компенсацией потерь щелочи добавлением твердого гидроксида натрия.
Расход тока на электрохимическую нейтрализацию щелочи в анодных камерах электролизеров на первой стадии составляет не менее 188 А·ч/дм3, а на 2-й стадии - не менее 93,8 А·ч/дм3. Катодные и анодные камеры электролизеров разделены катионообменными мембранами.
Снижение энергозатрат на получение гидроксида бериллия достигается за счет проведения электрохимической нейтрализации щелочи в анодных камерах электролизеров с параллельной ее регенерацией в катодных камерах и исключения разбавления технологического раствора водой до 30 г/дм3 и последующего выпаривания маточных растворов, образующихся после гидролиза бериллата натрия, до исходной концентрации с целью дальнейшего использования их на операции вскрытия концентрата.
В предлагаемом способе упрощается аппаратурное оформление технологического процесса за счет ликвидации участков выпаривания растворов, фильтрования и промывки соды.
Водород, выделяющийся в катодных камерах электролизеров, может быть аккумулирован геттерами-накопителями водорода на основе интерметаллических соединений (ИМС), например LaNi5, Zr3Al2, ZrNi, или использован для получения пара (при сжигании 1 м3 водорода выделяется 3,55 кВт·ч энергии) с последующим применением его для нагрева технологических растворов и пульп в производстве бериллия.
При проведении электрохимической нейтрализации щелочи в анодной камере электролизера происходит снижение концентрации ионов гидроксила за счет их разряда на положительно заряженном аноде с превращением в воду и образованием кислорода:
4 ОН--4 е-=O2↑+2 H2O.
Снижение содержания ионов ОН- согласно закону Фарадея пропорционально расходу тока. При пропускании 26,8 А·ч содержание NaOH снижается на 1 моль-экв. При этом в раствор не вносится никаких дополнительных реагентов. Более того, отпадает необходимость использования пероксида водорода для очистки технологического раствора от примесей железа и марганца, поскольку их окисление осуществляется кислородом, выделяющимся в анодной камере электролизера.
В катодной камере электролизера протекает обратный процесс образования гидроксильных ионов с одновременным выделением водорода на катоде:
2 H2O+2 е-=Н2↑+2 ОН-.
Таким образом происходит регенерация реагента (щелочи).
Для предотвращения миграции образующихся на катоде гидроксильных ионов к аноду электродные камеры разделены катионообменными мембранами, через которые проходят от анода к катоду ионы натрия.
Проведение электрохимической нейтрализации щелочи в две стадии определяется необходимостью очистки технологического раствора от железа и марганца перед выделением гидроксида бериллия. На 1-й стадии электрохимической нейтрализации в анодной камере содержание щелочи снижают до 170-180 г/дм3, после чего отфильтровывают выделившийся осадок гидроксидов железа и марганца, затем проводят 2-ю стадию электрохимической нейтрализации NaOH до ≈ 30 г/дм3. Данная концентрация щелочи необходима для достижения наиболее полного выделения гидроксида бериллия при гидролизе бериллата натрия, который проводится при температуре кипения раствора в течение 1 ч:
Na2BeO2+2 H2O→Ве(ОН)2↓+2 NaOH.
Предлагаемый способ электрохимической нейтрализации щелочного раствора и регенерации реагента может быть использован при переработке отходов металлического бериллия.
Исходный фенакит-бертрандитовый концентрат после измельчения до крупности 0,05 мм (95%) в количестве 110 г смешивали с оксидом кальция в соотношении СаО:SiO2=1,2 и подвергали обработке растворами щелочи (концентрация NaOH 400-600 г/дм3, объемом 1 дм3) в автоклаве при температуре 250-260°С в течение 4 ч.
После охлаждения полученную пульпу фильтровали: кек подвергали двукратной отмывке от водорастворимого бериллия, а щелочной раствор использовали для получения гидроксида бериллия по прототипу и предлагаемому способу.
Пример 1. Получение гидроксида бериллия по способу-прототипу
Технологический раствор после отделения нерастворимого остатка разбавляли водой в 2,3-3,4 раза (пропорционально исходной концентрации NaOH) до остаточной щелочности 170-180 г/дм3, после чего обрабатывали пероксидом водорода для окисления железа и марганца с последующим отделением выделившегося осадка указанных примесей.
Очищенный раствор бериллата натрия разбавляли дистиллированной водой в 5,8 раза до остаточной концентрации NaOH ~30 г/дм3, нагревали острым паром до кипения и выдерживали при этой температуре в течение 1 ч. Выделившийся в результате гидролиза гидроксид бериллия отфильтровывали и промывали от избытка щелочи. Маточный раствор с концентрацией NaOH ~30 г/дм3 вместе с промывным раствором выпаривали в 15-20 раз до концентрации NaOH=400-600 г/дм3 и фильтровали для отделения содового осадка.
Пример 2. Получение гидроксида бериллия по предлагаемому способу
Технологический раствор, полученный аналогично прототипу, после отделения нерастворимого остатка направляли в анодную камеру электролизера для проведения 1-й стадии электрохимической нейтрализации щелочи. В ходе эксперимента использовали источник постоянного тока (Б5-46). Материал электродов: анод выполнен из никеля, катод - из нержавеющей стали. Анодные и катодные камеры электролизеров разделены катионообменными мембранами МК-40 на основе сорбента КУ-2. При пропускании постоянного тока в количестве 188 А·ч/дм3 в анодной камере содержание NaOH снижали до ~175 г/дм3. При этом за счет выделения кислорода происходило окисление примесей железа и марганца. Полученную суспензию фильтровали: кек отмывали от водорастворимого бериллия, а раствор направляли в анодную камеру электролизера для проведения 2-й стадии электрохимической нейтрализации щелочи до концентрации NaOH ~30 г/дм3 при пропускании тока в количестве 93,8 А·ч/дм3, после чего раствор бериллата натрия подвергали гидролизу при кипячении в течение 1 ч. Суммарный расход тока за 2 стадии нейтрализации составил 281,4 А·ч/дм3.
Выделившийся осадок гидроксида бериллия отделяли фильтрованием и промывали от избытка щелочи. Маточный раствор после гидролиза направляли в катодную камеру электролизера 2-й стадии, где под действием тока происходил обратный процесс образования гидроксильных ионов. При этом содержание щелочи повышалось до 170-180 г/дм3 NaOH. Полученный раствор направляли в катодную камеру электролизера 1-й стадии нейтрализации, где происходила регенерация реагента до требуемой концентрации (400-600 г/дм3 NaOH).
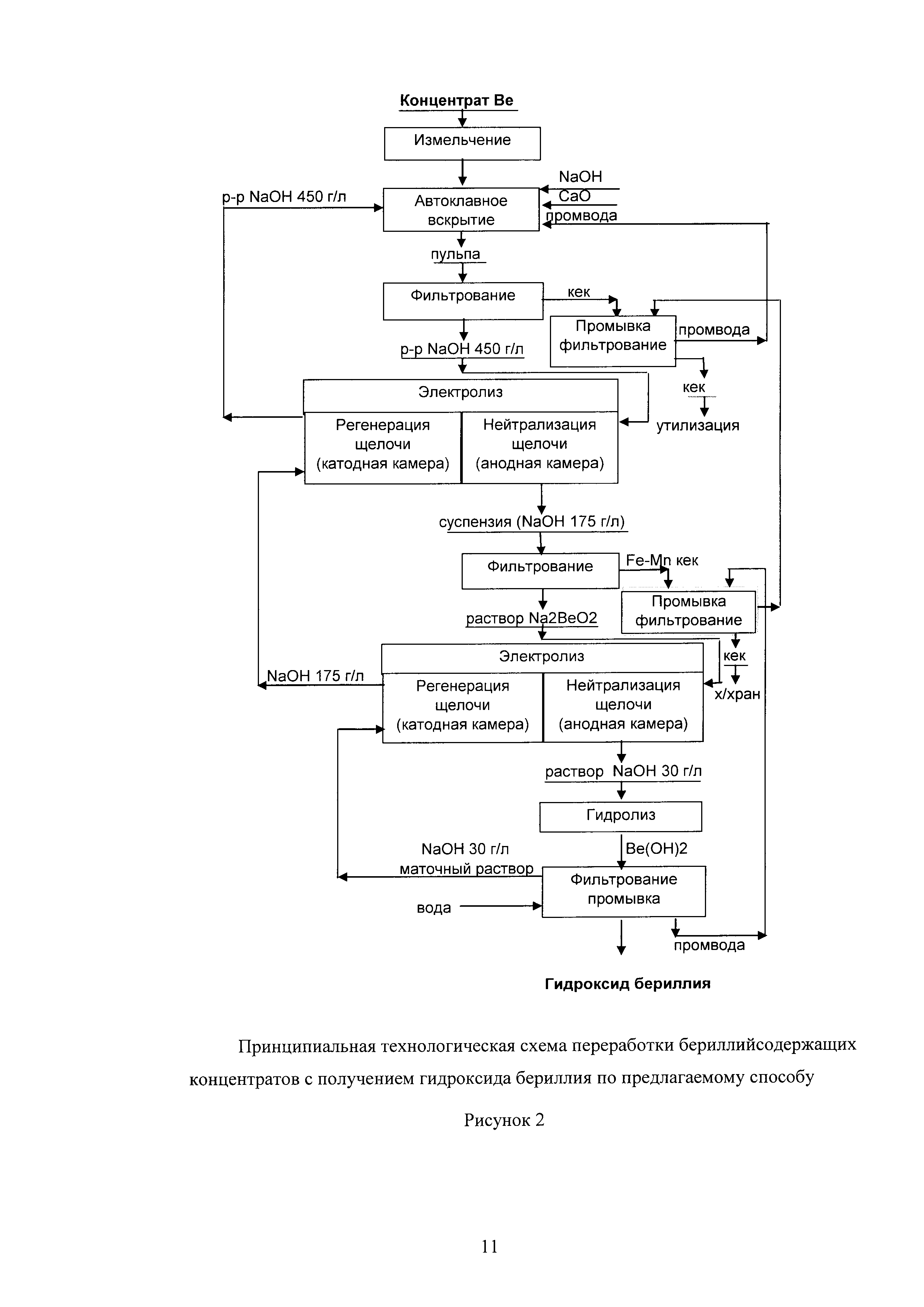
Технологическая схема получения гидроксида бериллия по предлагаемой схеме приведена на рисунке 2.
Сравнительные результаты переработки бериллийсодержащего концентрата (в расчете на 1 кг бериллия в гидроксиде бериллия)


Как видно из таблицы, наибольшее извлечение бериллия в гидроксид достигается при концентрации щелочи, равной 400-600 г/дм3.
Использование щелочных растворов с концентрацией NaOH меньше 400 г/дм3 нецелесообразно из-за недостаточно высокого извлечения бериллия в гидроксид, а использование щелочных растворов с концентрацией NaOH больше 600 г/дм3 не приводит к значительному увеличению извлечения бериллия в гидроксид и сопряжено с получением технологической суспензии с большой вязкостью, что приводит к дополнительным потерям бериллия с кеком вследствие высокой влажности.
Предложенный способ электрохимической нейтрализации щелочи для проведения гидролиза бериллата натрия с последующей ее регенерацией в катодной камере электролизера обеспечивает значительное (в 17 раз) снижение энергозатрат и сокращение водопотребления в среднем на 3,4 м3/кг бериллия в гидроксиде.