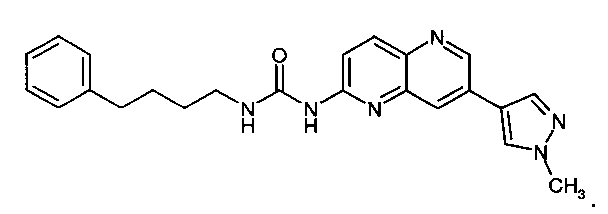
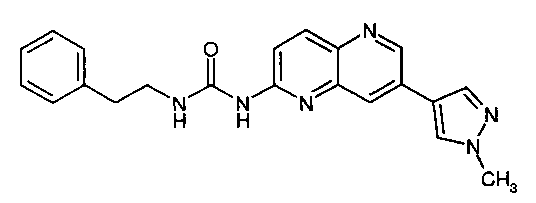
Результат интеллектуальной деятельности: НОВЫЕ ПРОИЗВОДНЫЕ НАФТИРИДИНА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗЫ
Вид РИД
Изобретение
Область техники
Настоящее изобретение относится к модуляторам киназ нафтиридинового типа, а также к получению и применению указанных модуляторов в качестве лекарственных средств для модулирования процессов неверно направленной передачи клеточных сигналов, в частности для влияния на функцию тирозинкиназ и серин/треонинкиназ и для лечения злокачественных или доброкачественных опухолей и других расстройств, основанных на патологической пролиферации клеток, таких как, например, рестеноз, псориаз, артериосклероз и цирроз печени.
Уровень техники
Активация протеинкиназ является ключевым событием в процессах передачи клеточных сигналов. Аберрантная активация киназ наблюдается при различных патологических состояниях. Таким образом, направленное ингибирование киназ является важнейшей терапевтической задачей.
Фосфорилирование белков обычно инициируется внеклеточными сигналами и представляет собой универсальный механизм регулирования различных клеточных событий, таких как, например, метаболические процессы, рост клеток, миграция клеток, дифференцировка клеток, мембранный транспорт и апоптоз. Семейство протеинкиназ отвечает за фосфорилирование белков. Указанные ферменты катализируют перенос фосфата к конкретным белкам-субстратам. На основании специфичности к субстрату указанные киназы делят на два основных класса - тирозинкиназы и серин/треонинкиназы. Как рецепторные тирозинкиназы, так и цитоплазматические тирозинкиназы и серин/треонинкиназы являются белками, играющими важную роль в процессах передачи клеточных сигналов. Избыточная экспрессия или распад данных белков играет важную роль в расстройствах, в основе которых лежит патологическая пролиферация клеток. Указанные расстройства включают, среди прочих, метаболические расстройства, расстройства соединительной ткани и кровеносных сосудов и злокачественные и доброкачественные опухоли. При возникновении и развитии опухоли указанные белки часто выступают в роли онкогенов, т.е. в роли аберрантных, постоянно активных протеинкиназ. Последствиями такой избыточной активации киназ являются, например, неконтролируемый рост клеток и снижение гибели клеток.
Стимуляция факторов роста, индуцированных опухолями, также может быть причиной избыточной стимуляции киназ. Таким образом, разработка модуляторов киназ представляет особенный интерес при всех патологических процессах, на которые оказывают влияние киназы.
Таким образом, настоящее изобретение направлено на создание новых соединений, подходящих в качестве модуляторов рецепторных тирозинкиназ и цитоплазматических тирозин- и серин/треонинкиназ. В связи с тем, что не все киназы, последовательно связанные в каскадах неверно направленной передачи сигналов, - например, как в случае пути Raf/Mek/Erk, - должны проявлять себя как онкогенные киназы или постоянно активные ферменты, в настоящем изобретении неактивные киназы также будут рассматриваться в качестве белков-мишеней для терапевтического воздействия, т.е. новые соединения способны связываться как с активными, так и с неактивными киназами и, следовательно, влиять на передачу сигналов.
Производные нафтиридина находят широкое применение в фармацевтической промышленности в качестве фармакодинамически активных соединений, а также в качестве исходных реагентов для синтеза.
Производные нафтиридина описаны в документе BMCL 2009, 19, 3568 как ингибиторы MCH1R, в патенте WO 2008/153752 как модуляторы гидролазы амидов жирных кислот и в патентах DE 2650826, WO 00/21952, WO 00/43383, WO 01/07432, WO 02/056882, WO 02/08224 и WO 2006/021448 как антибактериальные агенты. В патентах WO 99/58533, US 2007/0160538 и в литературном источнике BMCL 2001, 11, 1907 нафтиридины описаны как антагонисты орексинового рецептора 1. Замещенные нафтиридины описаны в патенте WO2000066583 как ингибиторы тирозинкиназы и в заявке на патент WO2008150827 как ингибиторы Р13-киназы.
Описание изобретения
Настоящее изобретение относится к киназным модуляторам нафтиридинового типа, а также к получению и применению указанных модуляторов в качестве лекарственных средств для модулирования процессов неверно направленной передачи клеточных сигналов, в частности для влияния на функцию тирозинкиназ и серин/треонинкиназ и для лечения злокачественных или доброкачественных опухолей и других расстройств, основанных на патологической пролиферации клеток, таких как, например, рестеноз, псориаз, артериосклероз и цирроз печени.
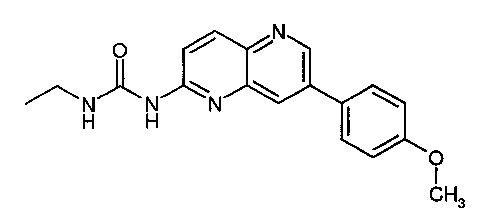
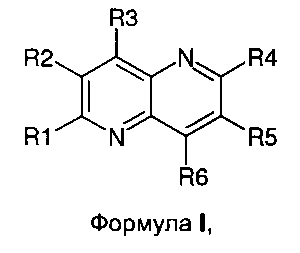
В настоящем изобретении неожиданно было обнаружено, что новые соединения нафтиридинового ряда, замещенные в положениях 2, 3 или 4, например, мочевиной, тиомочевинной, гуанидиновой или амидиновой группами, подходят для получения лекарственных средств для модулирования процессов неверно направленной передачи клеточных сигналов, в частности для влияния на функцию тирозинкиназ и серин/треонинкиназ и для лечения злокачественных или доброкачественных опухолей, таких как, например, опухоли молочных желез, простаты, легких, прямой кишки, кожи и яичников, а также других расстройств, основанных на патологиях пролиферации клеток. Согласно данному аспекту, в настоящей заявке описаны новые соединения нафтиридинового ряда общей Формулы I
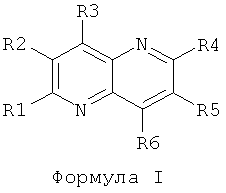
в которой заместители R1-R6 имеют следующее значение:
R1, R2 и R3 могут независимо друг от друга представлять собой
(i) водород,
(ii) незамещенный или замещенный алкил,
(iii) незамещенный или замещенный гетероциклил,
(iv) незамещенный или замещенный арил,
(v) незамещенный или замещенный гетероарил,
(vi) галоген,
(vii) циано,
(viii) гидроксил,
(ix) алкокси,
(x) амино,
(xi) карбоксил, алкоксикарбонил, карбоксиалкил или алкоксикарбонилалкил,
(xii) алкоксикарбониламино, алкоксикарбониламиноалкил и
(xiii) NR7R8,
где по меньшей мере один из заместителей R1-R3 должен представлять собой NR7R8, и где R7 может представлять собой водород, алкил, циклоалкил, гетероциклил, арил, гетероарил, алкилциклоалкил, алкилгетероциклил, алкиларил или алкилгетероарил, и алкильные, циклоалкильные, гетероциклильные, арильные и гетероарильные, алкилциклоалкильные, алкилгетероциклильные, алкиларильные или алкилгетероарильные заместители могут быть, в свою очередь, замещены,
и R8 может представлять собой:
-C(Y)NR9R10, где Y представляет собой О, S, и R9 и R10 могут независимо друг от друга представлять собой
(i) водород,
(ii) незамещенный или замещенный алкил,
(iii) незамещенный или замещенный циклоалкил,
(iv) незамещенный или замещенный гетероциклил,
(v) незамещенный или замещенный арил,
(vi) незамещенный или замещенный гетероарил,
(vii) или R9 и R10 вместе могут представлять собой гетероциклил,
-C(Y)NR11R12, где Y представляет собой NH, и R11 и R12 могут независимо друг от друга представлять собой
(i) водород,
(ii) незамещенный или замещенный алкил,
(iii) незамещенный или замещенный циклоалкил,
(iv) незамещенный или замещенный гетероциклил,
(v) незамещенный или замещенный арил,
(vi) незамещенный или замещенный гетероарил,
(vii) или R11 и R12 вместе могут представлять собой гетероциклил,
-C(NR13)R14, где R13 представляет собой Н, и R14 может представлять собой
(i) незамещенный или замещенный алкил,
(ii) незамещенный или замещенный циклоалкил,
(iii) незамещенный или замещенный гетероциклил,
(iv) незамещенный или замещенный арил,
(v) незамещенный или замещенный гетероарил,
R4, R5 и R6 могут независимо друг от друга представлять собой:
(i) водород,
(ii) незамещенный или замещенный алкил,
(iii) незамещенный или замещенный циклоалкил,
(iv) незамещенный или замещенный гетероциклил,
(v) незамещенный или замещенный арил,
(vi) незамещенный или замещенный гетероарил,
(vii) галоген,
(viii) циано,
(ix) гидроксил,
(x) алкокси,
(xi) NR15R16, где R15 и R16 могут независимо друг от друга представлять собой водород, алкил, циклоалкил, гетероциклил, арил, гетероарил, алкилциклил, алкилгетероциклил, алкиларил или алкилгетероарил, а алкильные, циклоалкильные, гетероциклильные, арильные и гетероарильные, алкилциклоалкильные, алкилгетероциклильные, алкиларильные или алкилгетероарильные заместители могут быть, в свою очередь, замещены,
или R15 и R16 вместе представляют собой гетероциклил, где гетероциклил может быть, в свою очередь, замещен,
(xii) OR17, где R17 может представлять собой алкил, циклоалкил, гетероциклил, арил, гетероарил, алкилциклоалкил, алкилгетероциклил, алкиларил или алкилгетероарил, а алкильные, циклоалкильные, гетероциклильные, арильные, гетероарильные, алкилциклоалкильные, алкилгетероциклильные, алкиларильные или алкилгетероарильные заместители могут быть, в свою очередь, замещены,
(xiii) SR18, где R18 может представлять собой алкил, циклоалкил, гетероциклил, арил, гетероарил, алкилциклоалкил, алкилгетероциклил, алкиларил или алкилгетероарил, а алкильные, циклоалкильные, гетероциклильные, арильные и гетероарильные, алкилциклоалкильные, алкилгетероциклильные, алкиларильные или алкилгетероарильные заместители могут быть, в свою очередь, замещены,
где по меньшей мере один из заместителей R4-R6 должен представлять собой незамещенный или замещенный (гетеро)арил или NR15R16.
Термин «галоген» в контексте настоящего изобретения относится к одному или, где это применимо, к множеству атомов фтора (F, фтор), брома (Вr, бром), хлора (Cl, хлор) или йода (I, йод). Обозначения «дигалоген», «тригалоген» и «пергалоген» относятся соответственно к двум, трем или четырем заместителям, где каждый заместитель может быть независимо выбран из группы, состоящей из фтора, хлора, брома и йода. «Галоген» предпочтительно означает атом фтора, хлора или йода.
Термин «алкил» в контексте настоящего изобретения включает ациклические насыщенные и ненасыщенные углеводородные радикалы, которые могут быть разветвленными или с неразветвленной цепью и незамещенными или моно- и полизамещенными и содержать от 1 до 12 атомов углерода, т.е. С2-12-алканилы, С2-12-алкенилы и С2-12-алкинилы. В этой связи алкенилы содержат по меньшей мере одну двойную углерод-углеродную связь, и алкинилы содержат по меньшей мере одну тройную углерод-углеродную связь. Алкил предпочтительно выбран из группы, включающей метил, этил, н-пропил, 2-пропил, н-бутил, втop-бутил, тpeт-бутил, н-пентил, изопентил, неопентил, н-гексил, 2-гексил, н-октил, н-нонил, н-децил, н-октил, н-ундецил, н-додецил, этиленил (винил), этинил, пропенил (-СН2СН=СН2; -СН=СН-СН3, -С(=СН2)-СН3), пропинил (-СН2-С≡СН, -С≡С-СН3), бутенил, бутинил, пентенил, пентинил, гексенил, гексинил, гептенил, гептинил, октенил и октинил.
Под термином «алкокси» в настоящем описании подразумевается -О(алкил), включая -ОСН3, -ОСН2СН3 и -ОС(СН3)3, где алкил такой, как описано в настоящей заявке.
Термин «циклоалкил» в контексте настоящего изобретения обозначает циклические углеводородные радикалы, содержащие 3-12 атомов углерода, которые могут быть насыщенными или ненасыщенными. Возможно связывание с соединениями общей структуры I посредством любого возможного кольцевого атома циклоалкильного радикала. Циклоалкильный радикал также может являться частью би- или полициклической системы.
Термин «гетероциклил» обозначает 3-, 4-, 5-, 6-, 7- или 8-членный циклический органический радикал, который содержит по меньшей мере один, по возможности 2, 3, 4 или 5 гетероатомов, причем указанные гетероатомы являются одинаковыми или разными, а циклический радикал является насыщенным или ненасыщенным, но не ароматическим. Возможно связывание с соединениями общей структуры I посредством любого возможного кольцевого атома гетероциклильного радикала. Гетероцикл также может быть частью би- или полициклической системы. Предпочтительными гетероатомами являются азот, кислород и сера. Предпочтительно, чтобы гетероциклильный радикал был выбран из группы, включающей тетрагидрофурил, тетрагидропиранил, пирролидинил, пиперидинил, пиперазинил и морфолинил.
Термин «арил» в контексте настоящего изобретения обозначает ароматические углеводороды, содержащие от 6 до 14 атомов углерода, в том числе фенилы, нафтилы и антраценилы. Радикалы также могут быть конденсированы с другими насыщенными, (частично) ненасыщенными или ароматическими системами колец. Возможно связывание с соединениями общей структуры I посредством любого возможного кольцевого атома арильного радикала.
Термин «гетероарил» обозначает 5-, 6- или 7-членный циклический ароматический радикал, который содержит по меньшей мере один, по возможности также 2, 3, 4 или 5 гетероатомов, причем указанные гетероатомы являются одинаковыми или разными. Возможно связывание с соединениями общей структуры I посредством любого возможного кольцевого атома гетероарильного радикала. Гетероцикл также может являться частью би- или полициклической системы. Предпочтительными гетероатомами являются азот, кислород и сера. Предпочтительно, чтобы гетероарильный радикал был выбран из группы, включающей пирролил, фурил, тиенил, тиазолил, оксазолил, оксадиазолил, изоксазолил, пиразолил, имидазолил, пиридинил, пиримидинил, пиридазинил, пиразинил, фталазинил, индонил, индазолил, индолизинил, хинолинил, изохинолинил, хиноксалинил, хиназолинил, карбазолил, феназинил, фенотиазинил, акридинил.
Термины «алкилциклоалкил», «алкилгетероциклил», «алкиларил» или «алкилгетероарил» в контексте настоящего изобретения означают, что алкил и циклоалкил, гетероциклил, арил и гетероарил имеют значения, обозначенные выше, и циклоалкильный, гетероциклильный, арильный или гетероарильный радикал связан с соединениями общей структуры I посредством C1-8-алкильной группы.
Термин «замещенный» в отношении «алкила», «циклоалкила», «гетероциклила», «арила», «гетероарила», «алкилциклоалкила», «алкилгетероциклила», «алкиларила» и «алкилгетероарила» в контексте настоящего изобретения, если это явно не определено выше в описании или в формуле изобретения, означает замещение одного или более водородных радикалов F, Cl, Br, I, CF3, NH2, NH-алкильным, NH-циклоалкильным, NH-гетероциклильным, NH-арильным, NH-гетероарильным, NH-алкилциклоалкильным, NH-алкилгетероциклильным, NH-алкиларильным, NH-алкилгетероарильным, NН-алкил-NН2, NH-алкил-ОН, N(алкил)2, NНС(O)-алкильным, NНС(O)-циклоалкильным, NHC(O)-гетероциклильным, NНС(O)-арильным, NНС(O)-гетероарильным, NHSO2-алкильным, NHSO2-арильным, NНSО2-гетероарильным, NO2, SH, S-алкильным, S-циклоалкильным, S-гетероциклильным, S-арильным, S-гетероарильным, ОН, OCF3, О-алкильным, О-циклоалкильным, О-гетероциклильным, О-арильным, О-гетероарильным, О-алкилциклоалкильным, О-алкилгетероциклильным, О-алкиларильным, О-алкилгетероарильным, О-алкил-ОН, O-(СН2)n-O, ОС(О)-алкильным, ОС(O)-циклоалкильным, ОС(O)-гетероциклильным, ОС(O)-арильным, ОС(O)-гетероарильным, ОSО2-алкильным ОSО2-циклоалкильным, OSO2-арильным, ОSО2-гетероарильным, O-Р(O)(ОН)2, O-Р(O)(O-алкил)2, алкил-Р(O)(ОН)2, алкил-Р(O)(O-алкил)2, С(O)-алкильным, С(O)-арильным, С(О)-гетероарильным, СO2Н, СO2-алкильным, СO2-циклоалкильным, СO2-гетероциклильным, СO2-арильным, СO2-гетероарильным, СO2-алкилциклоалкильным, СO2-алкилгетероциклильным, СO2-алкиларильным, СO2-алкилгетероарильным, C(O)-NH2, С(O)NН-алкильным, С(O)NН-циклоалкильным, С(O)NН-гетероциклильным, С(O)NН-арильным, С(O)NН-гетероарильным, C(O)NH-алкилциклоалкильным, С(O)NН-алкилгетероциклильным, С(O)NН-алкиларильным, С(O)NН-алкилгетероарильным, С(O)N(алкил)2, С(O)N(циклоалкил)2, С(O)N(арил)2, С(O)N(гетероарил)2, SO-алкильным, SO-арильным, SО2-алкильным, SO2-арильным, SO2NH2, SО2NН-алкильным, SО2NН-арильным, SO2NH-гетероарильным, SO3H, SО2О-алкильным, SО2О-арильным, SO2O-гетероарильным, алкильным, циклоалкильным, гетероциклильным, арильным или гетероарильным заместителями, и n может иметь значение 1, 2 или 3, а алкильные, циклоалкильные, гетероциклильные, арильные и гетероарильные заместители в свою очередь также могут быть замещены.
Заместители могут быть одинаковыми или различными, и замещение может иметь место в любом возможном положении алкильного, циклоалкильного, гетероциклильного, арильного и гетероарильного радикала.
Радикалы, имеющие более одного заместителя, означают радикалы, имеющие более одного заместителя, например два или три, у разных или одних и тех же атомов, например три заместителя у одного атома углерода, как в случае CF3, -CH2CF3, или в разных местах, как в случае -CH(OH)-CH=CH-CHCl2. Более чем однократное замещение может осуществляться одинаковыми или различными заместителями.
В случаях, когда соединения общей формулы I согласно настоящему изобретению имеют по меньшей мере один центр асимметрии, они могут существовать в форме соответствующих рацематов, в форме чистых энантиомеров и/или диастереомеров или в форме смесей указанных энантиомеров и/или диастереомеров. Возможно любое соотношение стереоизомеров в смесях. Таким образом, например, соединения согласно настоящему изобретению общей формулы I, имеющие один или более хиральных центров и присутствующие в форме рацематов, могут быть разделены на их оптические изомеры, то есть энантиомеры и диастереоизомеры, известными для этого способами. Разделение может быть проведено при помощи разделительной колонки на хиральных фазах или путем перекристаллизации из оптически активного растворителя, или с использованием оптически активной кислоты или основания, или путем получения производных с оптически активным реагентом, таким как, например, оптически активный спирт, и последующим удалением радикала.
Когда это возможно, соединения согласно настоящему изобретению могут присутствовать в форме таутомеров.
Соединения общей формулы I согласно настоящему изобретению, если они содержат в достаточной мере основную группу, такую как, например, первичная, вторичная или третичная аминогруппа, могут быть переведены в их физиологически приемлемые соли с помощью неорганических или органических кислот. Предпочтительно, фармацевтически приемлемые соли соединений общей структуры I согласно настоящему изобретению образованы с соляной кислотой, бромистоводородной кислотой, серной кислотой, фосфорной кислотой, метансульфоновой кислотой, п-толуолсульфоновой кислотой, угольной кислотой, муравьиной кислотой, уксусной кислотой, трифторуксусной кислотой, сульфоуксусной кислотой, щавелевой кислотой, малоновой кислотой, малеиновой кислотой, янтарной кислотой, винной кислотой, рацемической винной кислотой, яблочной кислотой, памоевой кислотой, миндальной кислотой, фумаровой кислотой, молочной кислотой, лимонной кислотой, глутаминовой кислотой или аспарагиновой кислотой. Образующиеся соли представляют собой, в том числе, гидрохлориды, гидробромиды, сульфаты, бисульфаты, фосфаты, метансульфонаты, тозилаты, карбонаты, бикарбонаты, форматы, ацетаты, трифлаты, сульфоацетаты, оксалаты, малонаты, малеаты, сукцинаты, тартраты, малаты, памоаты, манделаты, фумараты, лактаты, цитраты, глутаматы и аспартаты. Стехиометрическое соотношение солей, образованных соединениями согласно настоящему изобретению, кроме того, может быть целым или нецелым числом, кратным единице.
Соединения общей формулы I согласно настоящему изобретению, если они содержат в достаточной мере кислую группу, такую как, например, карбоксильная группа, могут быть переведены в их физиологически приемлемые соли с неорганическими и органическими основаниями. Примерами приемлемых неорганических оснований являются, например, гидроксид натрия, гидроксид калия, гидроксид кальция, а примерами приемлемых органических оснований являются этаноламин, диэтаноламин, триэтаноламин, циклогексиламин, дибензилэтилендиамин и лизин. Стехиометрическое соотношение солей, образованных соединениями согласно настоящему изобретению, кроме того, может быть целым или нецелым числом, кратным единице.
Предпочтение также отдается сольватам и в особенности гидратам соединений согласно настоящему изобретению, которые могут быть получены, например, путем кристаллизации из растворителя или из водного раствора. В данном случае одна, две, три или любое количество молекул сольвата или воды могут связываться с соединениями согласно настоящему изобретению с образованием сольватов и гидратов.
Известно, что химические вещества образуют твердые формы в различных упорядоченных состояниях, которые называют полиморфными формами или модификациями. Различные модификации полиморфного вещества могут сильно различаться по физическим свойствам. Соединения общей формулы I согласно настоящему изобретению могут существовать в различных полиморфных формах, при этом некоторые модификации могут быть метастабильными.
Наибольшее предпочтение отдается соединениям общей формулы I, выбранным из следующих:
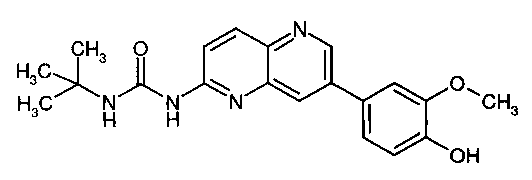
1-Этил-3-[7-(4-метоксифенил)-[1,5]нафтиридин-2-ил]-мочевина (1)
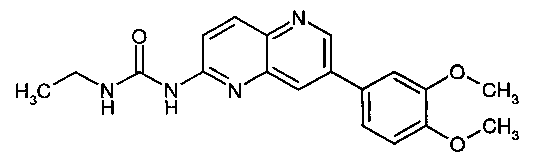
1-[7-(3,4-Диметоксифенил)-[1,5]нафтиридин-2-ил]-3-этилмочевина (2)
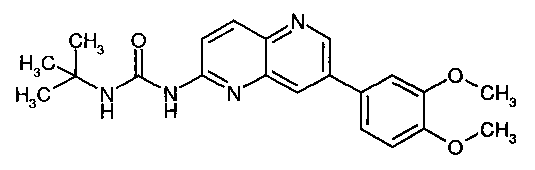
1-трет-Бутил-3-[7-(3,4-диметоксифенил)-[1,5]нафтиридин-2-ил]-мочевина (3)
1-трет-Бутил-3-[7-(4-гидрокси-3-метоксифенил)-[1,5]нафтиридин-2-ил]-мочевина (4)
1-[7-(1-Метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-2-ил]-3-фенэтилмочевина (5)
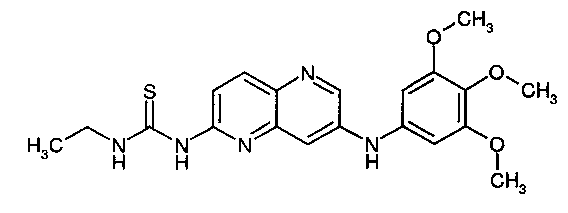
1-Этил-3-[7-(3,4,5-триметоксифениламино)-[1,5]нафтиридин-2-ил]-тиомочевина (6)
1-[7-(3,4-Диметоксифенил)-[1,5]нафтиридин-4-ил]-3-этилмочевина (7)
1-трет-Бутил-3-[7-(3,4-диметоксифенил)-[1,5]нафтиридин-4-ил]-мочевина (8)
1-Этил-3-[7-(4-гидрокси-3-метоксифенил)-[1,5]нафтиридин-4-ил]-мочевина (9)
1-Этил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (10)
1-трет-Бутил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (11)
1-трет-Бутил-3-[7-(4-гидрокси-3-метоксифенил)-[1,5]нафтиридин-4-ил]-мочевина (12)
1-трет-Бутил-3-[7-(3,5-дихлор-4-гидроксифенил)-[1,5]нафтиридин-4-ил]-мочевина (13)
1-Циклопропил-3-[7-(4-гидрокси-3-метоксифенил)-[1,5]нафтиридин-4-ил]-мочевина (14)
1-[7-(3,5-Дихлор-4-гидроксифенил)-[1,5]нафтиридин-4-ил]-3-этилмочевина (15)
1-Этил-3-[7-(4-гидрокси-3,5-диметилфенил)-[1,5]нафтиридин-4-ил]-мочевина (16)
1-Циклобутил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (17)
1-Циклопропил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (18)
1-[7-(1-Метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-3-пропилмочевина (19)
1-[7-(1-Метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-3-(2,2,2-трифторэтил)-мочевина (20)
1-[7-(1-Метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-3-(4-фенилбутил)-мочевина (21)
1-Циклогексил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (22)
1-[7-(1-Метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-3-фенилмочевина (23)
1-(3,3-Дифторциклобутил)-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (24)
1-Гексил-3-[7-(1-метил-1 Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (25)
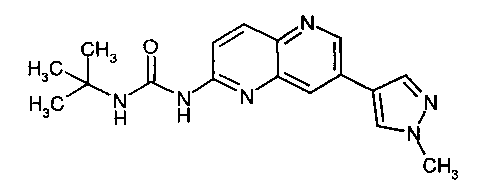
1-трет-Бутил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-2-ил]-мочевина (26)
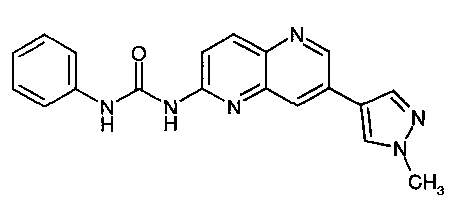
1-[7-(1-Метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-2-ил]-3-фенилмочевина (27)
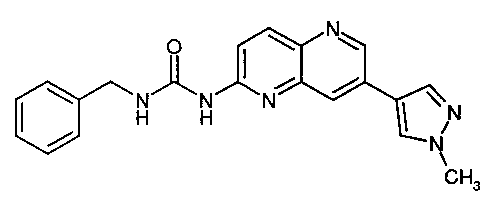
1-Бензил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-2-ил]-мочевина (28)
1-[7-(1-Метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-2-ил]-3-(4-фенилбутил)-мочевина (29)
1-Изопропил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (30)
1-Бензил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (31)
1-Бутил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (32)
1-[7-(1-Метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-3-фенэтилмочевина (33)
1-Циклопентил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (34)
1-Циклопропил-3-[7-(1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (35)
1-Циклопропил-3-(7-тиофен-3-ил-[1,5]нафтиридин-4-ил)-мочевина (36)
1-Циклопропил-3-[7-(2-фторпиридин-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (37)
1-Циклопропил-3-{7-[1-(2-морфолин-4-ил-этил)-1Н-пиразол-4-ил]-[1,5]нафтиридин-4-ил}-мочевина (38)
1-Циклопропил-3-(7-фенил-[1,5]нафтиридин-4-ил)-мочевина (39)
1-Циклопропил-3-[7-(1Н-индол-5-ил)-[1,5]нафтиридин-4-ил]-мочевина (40)
Нафтиридины общей формулы I согласно настоящему изобретению подходят для применения в лекарственных средствах, в частности, в качестве агентов для лечения расстройств, вызванных процессами неверно направленной передачи клеточных сигналов у человека, млекопитающих и домашней птицы. Млекопитающие могут быть одомашненными животными, такими как лошади, крупный рогатый скот, собаки, кошки, зайцы, овцы и т.п.
Согласно еще одному аспекту изобретения предложен способ лечения расстройств, вызванных процессами неверно направленной передачи клеточных сигналов, у человека и других млекопитающих, заключающийся в том, что по меньшей мере один нафтиридин общей формулы I вводят человеку или другому млекопитающему в дозе, эффективной для лечения указанных расстройств. Терапевтически эффективная доза соответствующего нафтиридина согласно настоящему изобретению, которую следует вводить для лечения, зависит в том числе от типа и стадии расстройства, от возраста, веса и пола пациента, от типа введения и от продолжительности лечения. Лекарственные средства согласно настоящему изобретению могут быть введены в жидкой, полутвердой и твердой фармацевтических формах. Введение осуществляется способом, приемлемым для каждого случая, в форме аэрозолей, порошков, присыпок, таблеток, в том числе таблеток, покрытых оболочкой, эмульсий, пен, растворов, суспензий, гелей, мазей, паст, драже, пастилок, капсул или суппозиториев.
Фармацевтические формы, помимо по меньшей мере одного ингредиента согласно настоящему изобретению, содержат, в зависимости от используемой фармацевтической формы, при необходимости, вспомогательные вещества, такие как, среди прочих, растворители, вещества, способствующие растворению, солюбилизаторы, эмульгаторы, смачивающие средства, пеногасители, желатинирующие средства, загустители, пленкообразователи, связующие вещества, буферы, солеобразующие вещества, десиканты, регуляторы текучести, наполнители, консерванты, антиоксиданты, красители, средства, облегчающие выемку из пресс-формы, смазки, разрыхлители и компоненты, маскирующие вкусы и запахи. Выбор вспомогательных веществ и их количества для применения зависит от выбранной фармацевтической формы и основан на прописях, известных специалисту в данной области техники.
Лекарственные средства согласно настоящему изобретению могут быть введены в подходящей лекарственной форме в кожу, накожно в форме раствора, суспензии, эмульсии, пены, мази, пасты или пластыря; через слизистую оболочку рта или языка, буккально, лингвально и сублингвально в форме таблетки, пастилки, таблетки, покрытой оболочкой, микстуры или полоскания; через слизистую оболочку желудка или кишечника, энтерально в форме таблетки, таблетки, покрытой оболочкой, капсулы, раствора, суспензии или эмульсии; через слизистую оболочку прямой кишки, ректально в форме суппозитория, ректальной капсулы или мази; через слизистую оболочку носа, назально в форме капель, мазей или спрея; через бронхиальный и альвеолярный эпителий, пульмонарным путем или путем ингаляции в форме аэрозоля или лекарственной формы для ингаляции; через конъюнктиву, конъюнктивиально в форме глазных капель, глазной мази, глазных таблеток, ламелл или глазного лосьона; через слизистую половых органов, интравагинально в форме вагинальных суппозиториев, мазей и спринцевания, внутриматочным путем в форме маточного пессария; через мочевые пути, внутриуретрально в форме промывания, мази или бужа; в артерию, внутриартериально в форме инъекции; в вену, внутривенно в форме инъекции или инфузии, околовенозно в форме инъекции или инфузии; в кожу, внутрикожно в форме инъекции или имплантата; под кожу, подкожно в форме инъекции или имплантата; в мышцу, внутримышечно в форме инъекции или имплантата; в брюшную полость, внутрибрюшинно в форме инъекции или инфузии.
Лечебный эффект соединений общей структуры I согласно настоящему изобретению может быть продлен применением подходящих мер в свете практических терапевтических требований. Данная цель может быть достигнута химическими и/или фармацевтическими способами. Примерами достижения пролонгации лечебного эффекта являются применение имплантатов, липосом, форм с отсроченным высвобождением, суспензий наночастиц и так называемых пролекарств соединений согласно настоящему изобретению, образование солей и комплексов с низкой растворимостью или применение кристаллических суспензий. Соединения согласно настоящему изобретению могут применяться по отдельности или в комбинации с другими веществами, такими как, например, аспарагиназа, блеомицин, карбоплатин, кармустин, хлорамбуцил, цисплатин, коласпаза, циклофосфамид, цитарабин, дакарбазин, дактиномицин, даунорубицин, доксорубицин (адриамицин), эпирубицин, зтопозид, 5-фторурацил, гексаметилмеламин, гидроксимочевина, ифосфамид, иринотекан, лейковорин, ломустин, мехлорэтамин, 6-меркаптопурин, месна, метотрексат, митомицин С, митоксантрон, преднизолон, преднизон, прокарбазин, ралоксифен, стрептозоцин, тамоксифен, талидомид, тиогуанин, топотекан, винбластин, винкристин, виндезин, аминоглутетимид, L-аспарагиназа, азатиоприн, 5-азацитидин кладрибин, бусульфан, диэтилстилбестрол, 2',2-дифтордеоксицитидин, доцетаксел, эритрогидроксинониладенин, этинилэстрадиол, 5-фтордеоксиуридин, 5-фтордеоксиуридин монофосфат, флударабин фосфат, флуоксиместерон, флутамид, гидроксипрогестерон капроат, идарубицин, интерферон, медроксипрогестерон ацетат, мегестрол ацетат, мелфалан, митотан, паклитаксел, оксалипталин, пентостатин, N-фосфоноацетил-L-аспартат (PALA), пликамицин, семустин, тенипозид, тестостерон пропионат, тиотепа, триметилмеламин, уридин, винорелбин, эпотилон, гемцитабин, таксотер, BCNU, CCNU, DTIC, герцептин, авастин, эрбитукс, сорафениб (нексавар), иматиниб (гливек), гефитиниб (пресса), эрлотиниб (тарцева), рапамицин, актиномицин D, сунитиниб (сутент), дазатиниб (спрайсел), нилотиниб (тасигна), лапатиниб (тайкерб, тайверб), ваталаниб.
Особое предпочтение в настоящем описании отдается лекарственным средствам, включающим по меньшей мере одно соединение из следующей группы нафтиридинов:
1-Этил-3-[7-(4-метоксифенил)-[1,5]нафтиридин-2-ил]-мочевина (1)
1-[7-(3,4-Диметоксифенил)-[1,5]нафтиридин-2-ил]-3-этилмочевина (2)
1-трет-Бутил-3-[7-(3,4-диметоксифенил)-[1,5]нафтиридин-2-ил]-мочевина (3)
1-трет-Бутил-3-[7-(4-гидрокси-3-метоксифенил)-[1,5]нафтиридин-2-ил]-мочевина (4)
1-[7-(1-Метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-2-ил]-3-фенэтилмочевина (5)
1-Этил-3-[7-(3,4,5-триметоксифениламино)-[1,5]нафтиридин-2-ил]-тиомочевина (6)
1-[7-(3,4-Диметоксифенил)-[1,5]нафтиридин-4-ил]-3-этилмочевина (7)
1-трет-Бутил-3-[7-(3,4-диметоксифенил)-[1,5]нафтиридин-4-ил]-мочевина (8)
1-Этил-3-[7-(4-гидрокси-3-метоксифенил)-[1,5]нафтиридин-4-ил]-мочевина (9)
1-Этил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (10)
1-трет-Бутил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (11)
1-трет-Бутил-3-[7-(4-гидрокси-3-метоксифенил)-[1,5]нафтиридин-4-ил]-мочевина (12)
1-трет-Бутил-3-[7-(3,5-дихлор-4-гидроксифенил)-[1,5]нафтиридин-4-ил]-мочевина (13)
1-Циклопропил-3-[7-(4-гидрокси-3-метоксифенил)-[1,5]нафтиридин-4-ил]-мочевина (14)
1-[7-(3,5-Дихлор-4-гидроксифенил)-[1,5]нафтиридин-4-ил]-3-этилмочевина (15)
1-Этил-3-[7-(4-гидрокси-3,5-диметилфенил)-[1,5]нафтиридин-4-ил]-мочевина (16)
1-Циклобутил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (17)
1-Циклопропил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (18)
1-[7-(1-Метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-3-пропилмочевина (19)
1-[7-(1-Метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-3-(2,2,2-трифторэтил)-мочевина (20)
1-[7-(1-Метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-3-(4-фенилбутил)-мочевина (21)
1-Циклогексил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (22)
1-[7-(1-Метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-3-фенилмочевина (23)
1-(3,3-Дифторциклобутил)-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (24)
1-Гексил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (25)
1-трет-Бутил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-2-ил]-мочевина (26)
1-[7-(1-Метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-2-ил]-3-фенилмочевина (27)
1-Бензил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-2-ил]-мочевина (28)
1-[7-(1-Метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-2-ил]-3-(4-фенилбутил)-мочевина (29)
1-Изопропил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (30)
1-Бензил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (31)
1-Бутил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (32)
1-[7-(1-Метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-3-фенэтилмочевина (33)
1-Циклопентил-3-[7-(1-метил-1Н-пиразол-4-илН1,5]нафтиридин-4-ил]-мочевина (34)
1 -Циклопропил-3-[7-(1 Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (35)
1-Циклопропил-3-(7-тиофен-3-ил-[1,5]нафтиридин-4-ил)-мочевина (36)
1-Циклопропил-3-[7-(2-фторпиридин-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (37)
1-Циклопропил-3-{7-[1-(2-морфолин-4-ил-этил)-1Н-пиразол-4-ил]-[1,5]нафтиридин-4-ил}-мочевина (38)
1-Циклопропил-3-(7-фенил-[1,5]нафтиридин-4-ил)-мочевина (39)
1-Циклопропил-3-[7-(1Н-индол-5-ил)-[1,5]нафтиридин-4-ил]-мочевина (40)
Указанные соединения могут присутствовать в форме свободных оснований или в форме солей физиологически приемлемых кислот.
Химический синтез
Соединения общей формулы I могут быть получены согласно Схемам 1-4, приведенным ниже:
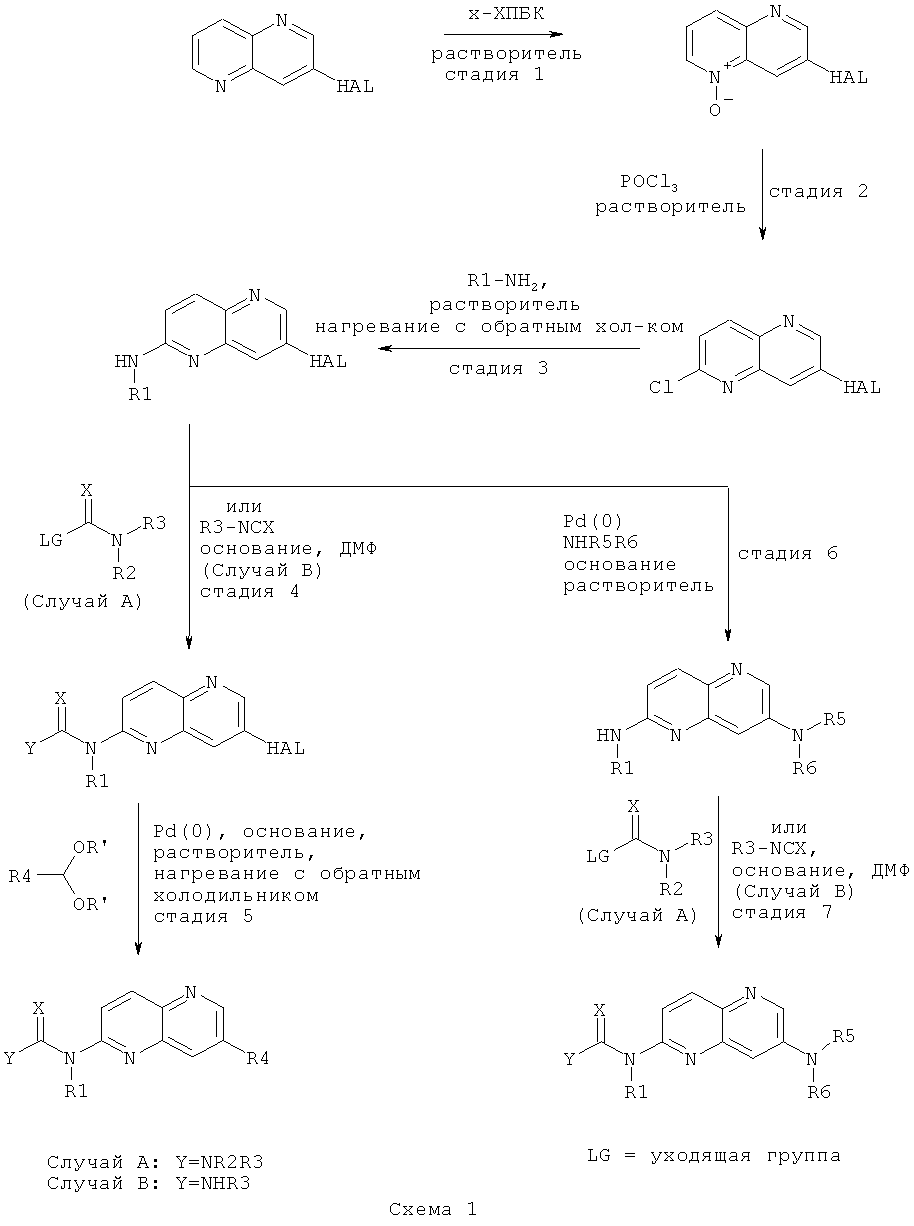
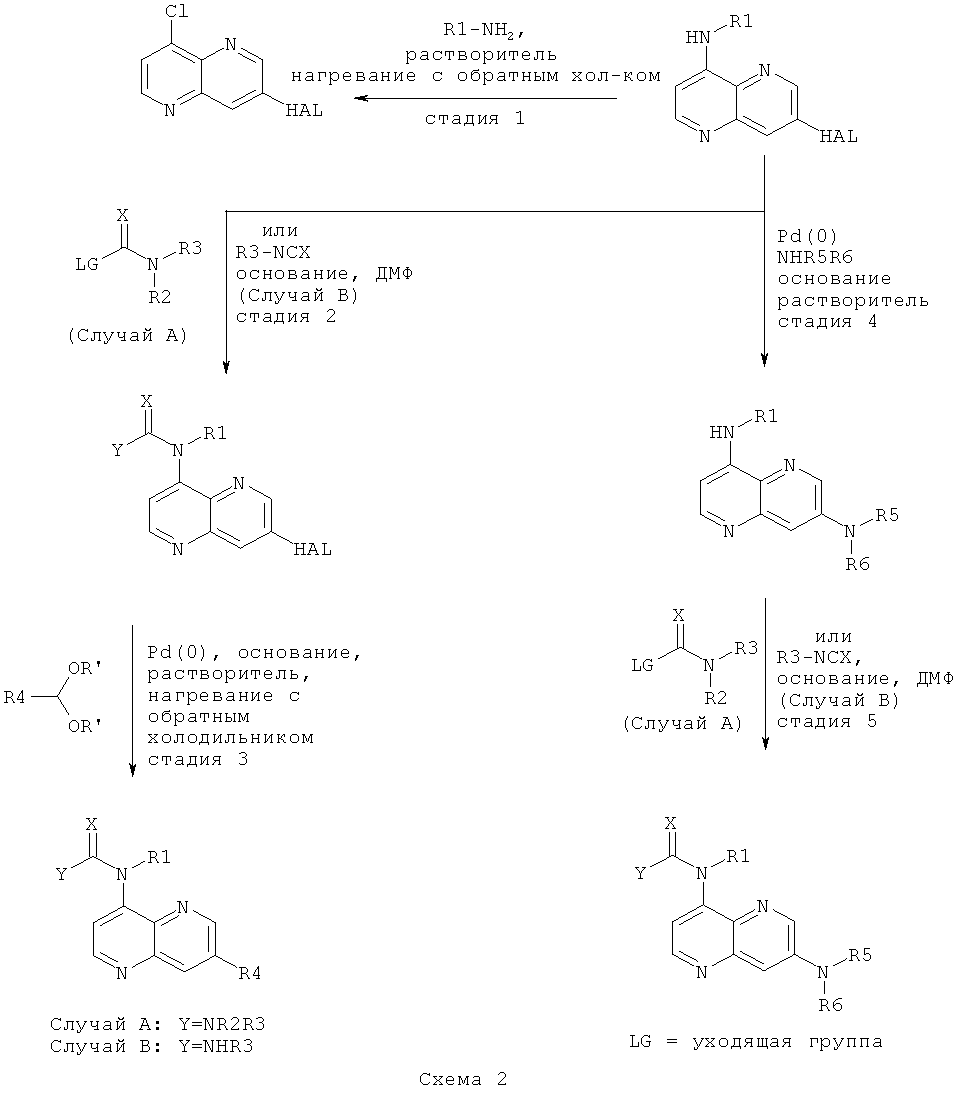
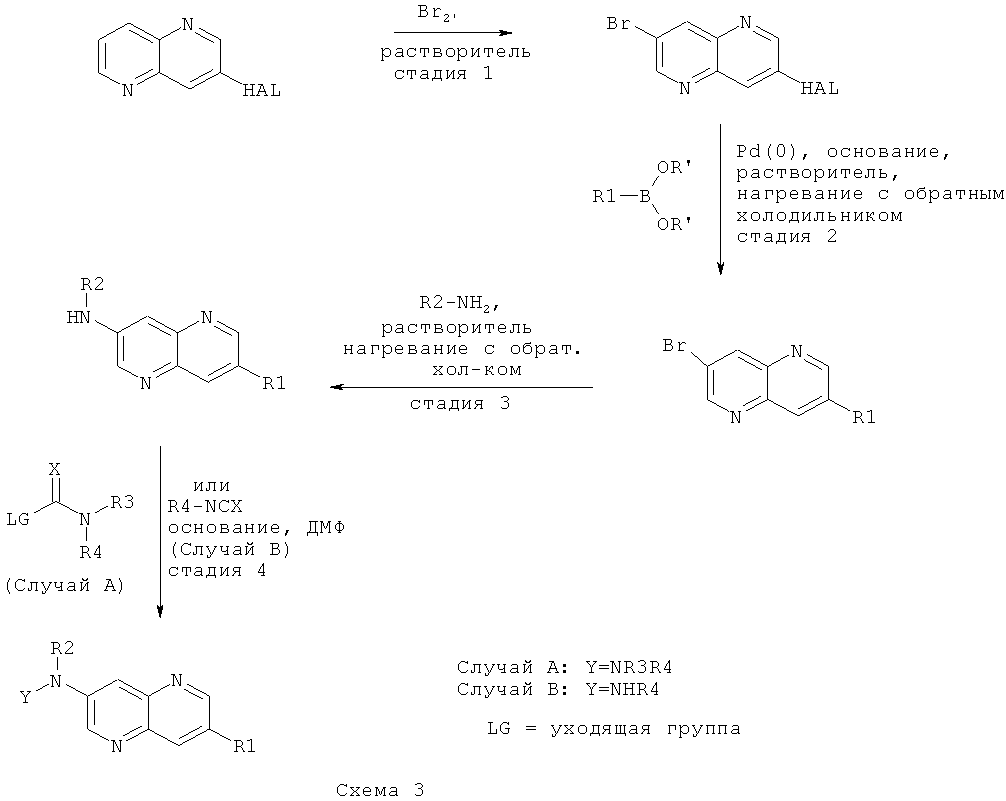
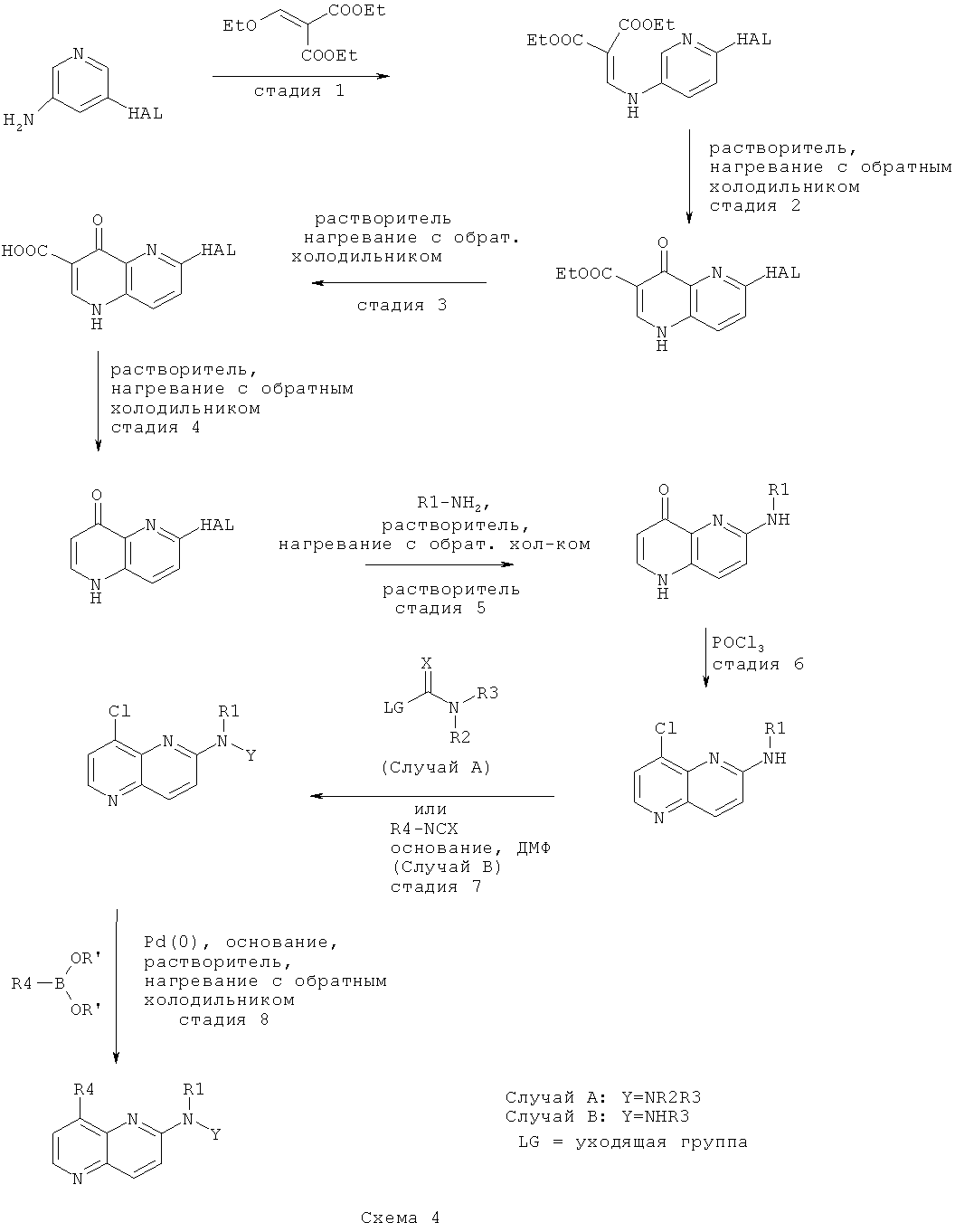
Исходные вещества либо имеются в продаже, либо могут быть получены известными подходящими для этого способами.
Любые растворители или вспомогательные вещества, которые следует использовать, если это необходимо, и параметры реакции, которые следует использовать, такие как температура и продолжительность реакции, известны специалисту в данной области техники в силу его экспертных знаний.
Нижеперечисленные соединения, очевидные из указания соответствующего химического наименования из приведенного ниже обзора, были синтезированы в соответствии со Схемами синтеза 1-4. Аналитическое исследование соединений согласно настоящему изобретению проводилось на основе температуры плавления указанных соединений и/или 1Н-ЯМР спектроскопии при температуре 300 К и/или масс-спектроскопии.
Использованные реагенты и растворители были приобретены у обычных поставщиков (Acros, Avocado, Aldrich, Fluka, Lancaster, Maybridge, Merck, Sigma, TCl и т.д.) или синтезированы.
Примеры
Настоящее изобретение далее описано более подробно посредством следующих примеров, но не ограничивается ими.
Химические названия веществ были получены с использованием программного обеспечения AutoNom 2000 Software (ISIS™/ Draw 2.5 SP2; MDL).
Пример 1 (реакция согласно Схеме 1, стадия 1):
Пример 1.1.1 и Пример 1.1.2: 3-Бром-[1,5]нафтиридин-5-оксид и 3-бром-1,5-нафтиридин-1-оксид
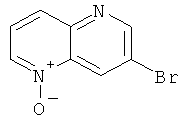
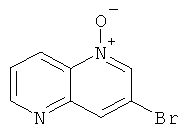
4,43 г (21,2 ммоль, 1 экв.) 3-бром-1,5-нафтиридина (W. Czuba, Recueil des Travaux Chimiques des Pays-Bas 1963, 82, 988-996) вносили в 165 мл метиленхлорида. Затем при 0°С порциями добавляли 5,23 г (21,2 ммоль, 1 экв.) мета-хлорпербензойной кислоты. Смесь перемешивали при комнатной температуре в течение 18 часов. Смесь промывали 1М водным раствором NaOH и водой. Органический слой высушивали над Na2SO4, фильтровали и выпаривали досуха. Осадок очищали с помощью колоночной хроматографии с применением в качестве элюента метиленхлорида и затем метиленхлорида/этанола в соотношении 98/2. Растворитель выпаривали досуха с получением 3,08 г 3-бром-1,5-нафтиридин-5-оксида (бледно-желтый порошок) с выходом 64% и 1,00 г 3-бром-1,5-нафтиридин-1-оксида (желтый порошок) с выходом 21%.
3-Бром-[1,5]нафтиридин-5-оксид
Выход: 3,08 г (64% от теоретического).
Температура плавления: 148-149°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9,21 (d, 1Н); 9,10 (d, 1Н); 8,75 (d, 1Н); 8,06 (d, 1Н); 7,80 (dd, 1Н) ррm.
MS: m/z 226 (M+H+)
3-Бром-[1,5]-нафтиридин-1-оксид
Выход: 1,00 г (21% от теоретического).
Температура плавления: 153-154°С.
1Н-ЯМР (ДMCO-d6, 400 МГц): δ=9,12 (d, 1Н); 9,03 (s, 1Н); 8,86 (d, 1Н); 8,36 (s, 1Н); 7,94 (dd, 1Н) ррm.
MS: m/z 226 (М+Н+).
Пример 2 (реакция согласно Схеме 1, стадия 2):
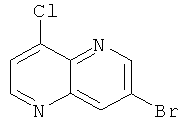
Пример 2.1.1 и Пример 2.1.2: 7-Бром-2-хлор-[1,5]нафтиридин и 7-Бром-4-хлор-[1,5]нафтиридин
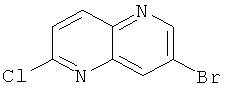
 ,
,
7,97 г (35,4 ммоль, 1 экв.) 3-бром-1,5-нафтиридин-5-оксида и 9,9 мл (106,2 ммоль, 3 экв.) хлорангидрида фосфорной кислоты вносили в 600 мл метиленхлорида. Смесь перемешивали при нагревании с обратным холодильником в течение 18 часов. Метиленхлорид частично выпаривали (3/4). Аккуратно добавляли 1М водный раствор NaOH при 0°С. Водный слой экстрагировали при помощи метиленхлорида. Органические слои высушивали над Na2SO4, фильтровали и выпаривали досуха. Остаток очищали с помощью колоночной хроматографии с применением в качестве элюента метиленхлорида. Растворитель выпаривали досуха с получением 1,97 г 7-бром-2-хлор-1,5-нафтиридина (белый порошок) с выходом 22% и 4,16 г 7-бром-4-хлор-1,5-нафтиридина (белый порошок) с выходом 48%.
7-Бром-2-хлор-[1,5]нафтиридин
Выход: 1,97 г (22% от теоретического).
Температура плавления: 168-169°C.
1Н-ЯМР (ДМСО-d6, 400 МГц): =9,15 (d, 1H); 8,79 (d, 1H); 8,55 (d, 1H); 7,93 (d, 1H) ppm.
MS: m/z 245 (M+H+).
7-Бром-4-хлор-[1,5]нафтиридин
Выход: 4,16 г (48% от теоретического).
Температура плавления: 162-163°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9,22 (d, 1Н); 8,99 (d, 1Н); 8,88 (d, 1Н); 8,11 (d, 1Н) ррm.
MS: m/z 245 (М+Н+).
Пример 3 (реакция согласно Схеме 1, стадия 3):
Пример 3.1: 7-Бром-[1,5]нафтиридин-2-иламин
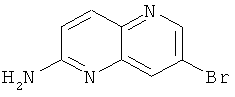
В герметичном реакторе вносили 500 мг (1,23 ммоль, 1 экв.) 7-бром-2-хлор-1,5-нафтиридина и 7 мл (41,6 ммоль, 33 экв.) 20% водного раствора аммиака в 7 мл диоксана. Смесь перемешивали при 160°С в течение 24 часов. Смесь оставляли до достижения ею комнатной температуры, после чего добавляли воду. Водный слой экстрагировали при помощи этилацетата. Органические слои высушивали над Na2SO4, фильтровали и выпаривали досуха. Осадок очищали с помощью колоночной хроматографии с применением в качестве элюента метиленхлорида и затем метиленхлорида/этанола в соотношении 98/2. Растворитель выпаривали досуха с получением 220 мг белого порошка с выходом 80%.
Выход: 220 мг (80% от теоретического).
Температура плавления: 168-169°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=8,57 (d, 1Н); 8,05 (d, 1Н); 7,96 (d, 1Н); 6,04 (d, 1Н); 6,98 (s, 2Н) ppm.
MS: m/z 225 (М+Н+).
Пример 4 (реакция согласно Схеме 1, стадия 4):
Пример 4.1: 1-(7-Бром-[1,5]нафтиридин-2-ил)-3-трет-бутилмочевина
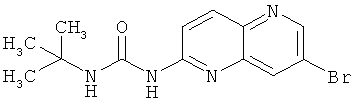
В герметичном реакторе вносили 300 мг (1,34 ммоль, 1 экв.) 7-бром-[1,5]нафтиридин-2-иламина и 305 мкл (2,68 ммоль, 2 экв.) тpeт-бутилизоцианата в 6 мл пиридина. Смесь перемешивали при 140°С в течение 24 часов. Смесь оставляли до достижения ею комнатной температуры, после чего удаляли растворитель под пониженным давлением. Осадок очищали с помощью колоночной хроматографии с применением в качестве элюента метиленхлорида/этанола в соотношении 96/4. Растворитель выпаривали досуха с получением 398 мг белого порошка с выходом 92%. Выход: 398 мг (92% от теоретического).
Температура плавления: >300°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.83 (s, 1Н); 9.07 (s, 1Н); 8.86 (d, 1Н); 8.38 (d, 1Н); 8.29 (d, 1Н); 7.64 (d, 1Н); 1.44 (s, 9Н) ррm. MS: m/z 323 (М+Н+); 325 ((М+2)+Н+).
Промежуточные соединения, описанные ниже, были синтезированы аналогично Примеру 4.1: (1-(7-Бром-[1,5]нафтиридин-2-ил)-3-трет-бутилмочевина).
Пример 4.2: 1-(7-Бром-[1,5]нафтиридин-2-ил)-3-этилмочевина
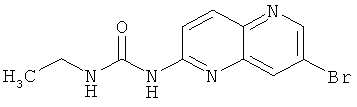
Выход: 102 мг (77 % от теоретического).
Температура плавления: 225-226°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.99 (s, 1Н); 9.12 (sl, 1Н); 8.85 (d, 1Н); 8.67 (d, 1Н); 8.29 (d, 1Н); 7.69 (d, 1Н); 3.37-3.28 (m, 2Н); 1.21 (t, 3Н) ppm.
MS: m/z 295 (M+H+); 297 ((M+2)+H+).
Пример 4.3: 1-(7-Бром-[1,5]нафтиридин-2-ил)-3-циклопропилтиомочевина
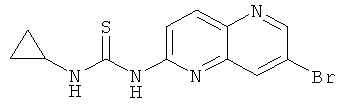
Выход: 109 мг (58% от теоретического).
Температура плавления: 233-234°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=11.90 (d, 1Н); 11.19 (s, 1Н); 8.90 (d, 1Н); 8.70 (d, 1Н); 8.35 (d, 1Н); 7.61 (d, 1Н); 3.30-3.24 (m, 1Н); 0.92-0.88 (m, 4Н) ррm.
MS: m/z 324 (М+Н+).
Пример 4.4: 1-(7-Бром-[1,5]нафтиридин-2-ил)-3-фенилмочевина
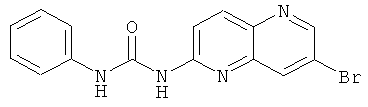
Выход: 130 мг (71% от теоретического).
Температура плавления: 324-325°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=11.45 (s, 1Н); 10.36 (s, 1Н); 8.92 (d, 1Н); 8.82 (d, 1Н); 8.39 (d, 1Н); 7.79-7.72 (m, 3Н); 7.40 (t, 2Н); 7.15-7.11 (m, 1Н) ррm.
MS: m/z 341 (М+Н+); 345 ((М+2)+Н+).
Пример 4.5: 1-(7-Бром-[1,5]нафтиридин-2-ил)-3-бензилмочевина
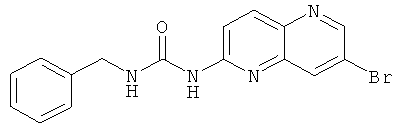
Выход: 144 мг (90% от теоретического).
Температура плавления: 250-252°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=10.13 (s, 1Н); 9.63 (sl, 1Н); 8.86 (d, 1Н); 8.66 (d, 1Н); 8.33 (d, 1Н); 7.63 (d, 1Н); 7.36-7.28 (m, 5Н); 4.54 (d, 2Н).
MS: m/z 357 (М+Н+); 359 ((М+2)+Н+).
Пример 4.6: 1-(7-Бром-[1,5]нафтиридин-2-ил)-3-фенэтилмочевина
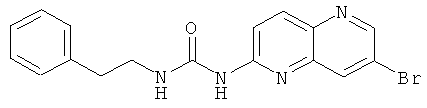
В атмосфере аргона вносили 201 мг (897 мкмоль, 1 экв.) 7-бром-[1,5]нафтиридин-2-иламина и 294 мг (993 мкмоль, 1,1 экв.) трифосгена в 10 мл пиридина при 0°С. Смесь перемешивали при нагревании с обратным холодильником в течение 1 часа. Смесь оставляли до достижения ею комнатной температуры, после чего добавляли 238 мкл (1,89 ммоль, 2,1 экв.) 2-фенэтиламина. Смесь перемешивали при нагревании с обратным холодильником в течение 1 часа, оставляли до достижения ею комнатной температуры и добавляли воду. Водный слой экстрагировали при помощи метиленхлорида. Органические слои высушивали над Na2SO4, фильтровали и выпаривали досуха. Осадок очищали с помощью колоночной хроматографии с применением в качестве элюента метиленхлорида/этанола в соотношении 96/4. Растворитель выпаривали досуха с получением 80 мг желтого порошка с выходом 24%.
Выход: 80 мг (24 % от теоретического).
Температура плавления: 245-246°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=10.03 (s, 1Н); 9.25 (t, 1Н); 8.80 (d, 1Н); 8.23 (d, 1Н); 8.10 (d, 1Н); 7.48 (d, 1Н); 7.36-7.24 (m, 5Н); 3.58 (q, 2Н); 2.88 (t, 2Н) ррm.
MS: m/z 371 (М+Н+); 373 ((М+2)+Н+).
Пример 5 (реакция согласно Схеме 1, стадия 5):
Пример 5.1:1-Этил-3-[7-(4-метоксифенил)-[1,5]нафтиридин-2-ил]-мочевина (1)
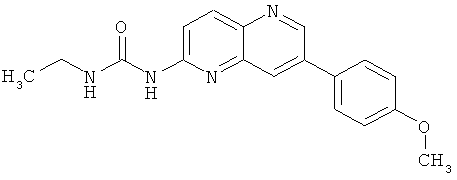
В атмосфере аргона вносили 100 мг (338 мкмоль, 1 экв.) 1-(7-бром-[1,5]нафтиридин-2-ил)-3-этилмочевины, 103 мг (676 мкмоль, 2 экв.) 4-метоксифенилборониевой кислоты, 72 мг (676 мкмоль, 2 экв.) карбоната натрия и 29 мг (25 мкмоль, 0,07 экв.) тетракис(трифенилфосфин)палладия в 10 мл смеси диоксана с водой (8/2). Смесь перемешивали при 90°С в течение 2 часов. Смесь оставляли до достижения ею комнатной температуры, подвергали гидролизу и фильтровали через целитовый фильтр. Фильтрат экстрагировали при помощи метиленхлорида. Органический слой высушивали над Na2SО4, фильтровали и выпаривали досуха. Осадок очищали с помощью колоночной хроматографии с применением в качестве элюента метиленхлорида/этанола в соотношении 99/1 и затем метиленхлорида/этанола в соотношении 97/3. Растворитель выпаривали досуха с получением 56 мг оранжевого порошка с выходом 51%.
Выход: 56 мг (51% от теоретического).
Температура плавления: 264-265°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.89 (s, 1Н); 9.33 (bs, 1Н); 9.12 (d, 1Н); 8.46 (d, 1Н); 8.46 (d, 1Н); 7.92 (d, 2Н); 7.51 (d, 1Н); 7.15 (d, 2Н); 3.87 (s, 1Н); 3.33 (q, 2Н); 1.23 (t, 3Н) ррm.
MS: m/z 323 (M+H+).
Приведенные ниже примеры были получены аналогично Примеру 5.1:1-Этил-3-[7-(4-метоксифенил)-[1,5]нафтиридин-2-ил]-мочевина (1).
Пример 5.2: 1-[7-(3,4-Диметоксифенил)-[1,5]нафтиридин-2-ил]-3-этилмочевина (2)
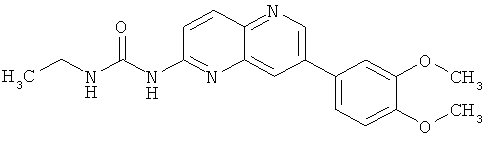
Выход: 58 мг (49% от теоретического).
Температура плавления: 218-219°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.88 (s, 1Н); 9.30 (t, 1Н); 9.16 (d, 1Н); 8.47 (d, 1Н); 8.29 (d, 1Н); 7.57-7.45 (m, 3Н); 7.16 (d, 1Н); 3.94 (s, 3Н); 3.87 (s, 3Н); 3.29-3.16 (m, 2Н); 1.23 (t, 3Н) ррm.
MS: m/z 353 (М+Н+).
Пример 5.3: 1-трет-Бутил-3-[7-(3,4-диметоксифенил)-[1,5]нафтиридин-2-ил]-мочевина (3)
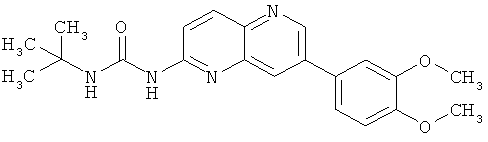
Выход: 42 мг (35 % от теоретического).
Температура плавления: 279-280°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.71 (s, 1Н); 9.33 (s, 1Н); 9.13 (d, 1Н); 8.29 (d, 1Н); 8.19 (d, 1Н); 7.57 (d, 1Н); 7.49-7.44 (m, 2Н); 7.16 (d, 1Н); 3.93 (s, 3Н); 3.87 (s, 3Н); 1.46 (t, 9Н) ppm.
MS: m/z 381 (M+H+).
Пример 5.4: 1-трет-Бутил-3-[7-(4-гидрокси-3-метоксифенил)-[1,5]нафтиридин-2-илмочевина (4)
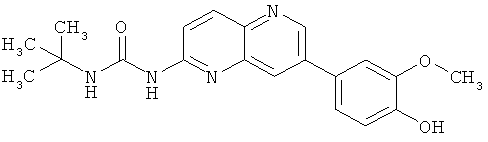
В атмосфере аргона вносили 100 мг (309 мкмоль, 1 экв.) 1-(7-бром-[1,5]нафтиридин-2-ил)-3-трет-бутилмочевины, 230 мг (927 мкмоль, 3 экв.) 2-метокси-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенола, 196 мг (1,854 ммоль, 6 экв.) карбоната натрия и 50 мг (43 мкмоль, 0,14 экв.) тетракис(трифенилфосфин)палладия в 11 мл смеси диметилформамид/вода (10/1). Смесь перемешивали при 80°С в течение 16 часов. Смесь оставляли до достижения ею комнатной температуры и доводили pH до 7 добавлением 1М водного раствора HCl. Фильтрат экстрагировали при помощи метиленхлорида. Органический слой высушивали над Na2SO4, фильтровали и выпаривали досуха. Осадок очищали с помощью колоночной хроматографии с применением в качестве элюента метиленхлорида/этанола в соотношении 98/2. Растворитель выпаривали досуха с получением 62 мг желтого порошка с выходом 53%.
Выход: 62 мг (53% от теоретического).
Температура плавления: 286-287°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.69 (s, 1Н); 9.42 (s, 1Н); 9.33 (s, 1Н); 9.11 (d, 1Н); 8.27 (d, 1Н); 8.15 (d, 1Н); 7.55 (d, 1Н); 7.46 (d, 1Н); 7.34 (dd, 1Н); 6.98 (d, 1Н); 3.94 (s, 3Н); 1.46 (t, 9Н) ррm.
MS: m/z 367 (M+H+).
Приведенные ниже примеры были получены аналогично Примеру 5.4: 1-трет-Бутил-3-[7-(4-гидрокси-3-метоксифенил)-[1,5]нафтиридин-2-ил]-мочевина (4).
Пример 5.5: 1-[7-(1-Метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-2-ил]-3-фенэтилмочевина (5)
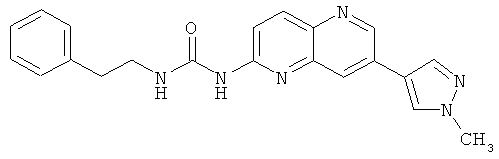
Выход: 50 мг (71% от теоретического).
Температура плавления: 237-238°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.92 (s, 1Н); 9.39 (bs, 1Н); 9.07 (d, 1Н); 8.45 (s, 1Н); 8.22 (d, 1Н); 8.15 (s, 1Н); 8.03 (d, 1Н); 7.44 (d, 1Н); 7.39-7.22 (m, 5Н); 3.98 (s, 3Н); 3.62 (q, 2Н); 2.94 (t, 2Н) ррm.
MS: m/z 373 (М+Н+).
Пример 5.6:1-трет-Бутил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-2-ил]-мочевина (26)
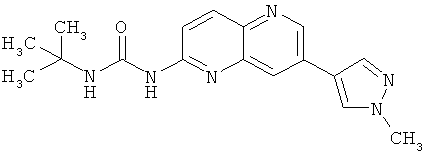
Выход: 40 мг (37% от теоретического).
1Н-ЯМР (ДМСО-d6, 600 МГц): δ=9.62 (s, 1Н); 9.26 (s, 1Н); 9.04 (s, 1Н); 8.46 (s, 1Н); 8.18 (d, 1H); 8.16 (s, 1H); 8.07 (s, 1H); 7.46 (d, 1H); 3.92 (s, 3Н); 1.43 (s, 9H) ppm.
MS: m/z 325 (M+H+).
Пример 5.7: 1-[7-(1-Метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-2-ил]-3-фенилмочевина (27)

Выход: 25 мг (78% от теоретического).
Температура плавления: 270-271°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=11.73 (s, 1Н); 10.23 (s, 1Н); 9.15 (s, 1Н); 8.57 (s, 1Н); 8.45 (s, 1Н); 8.34-8.29 (m, 2Н); 7.78 (d, 2Н); 7.58 (d, 1Н); 7.42 (t, 2Н); 7.14-7.10 (m, 1Н); 3.98 (s, 3Н) ррm.
MS: m/z 345 (М+Н+).
Пример 5.8: 1-Бензил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-2-ил]-мочевина (28)
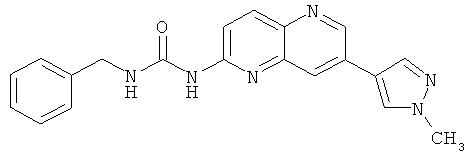
Выход: 40 мг (60% от теоретического).
Температура плавления: 257-258°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=10.00 (s, 1Н); 9.75 (m, 1Н); 9.10 (d, 1Н); 8.46 (s, 1Н); 8.32 (d, 1Н); 8.26 (d, 1Н); 8.15 (s, 1Н); 7,53 (d, 1Н); 7.44-7.28 (m, 5Н); 4.57 (d, 2Н); 3.95 (s, 3Н) ррm.
MS: m/z 359 (М+Н+).
Пример 5.9: 1-[7-(1-Метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-2-ил]-3-(4-фенилбутил)-мочевина (29)
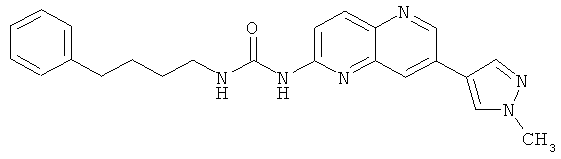
Выход: 32 мг (43% от теоретического).
1Н-ЯМР (ДМСО-d6, 600 МГц): δ=9.80 (s, 1Н); 9.26 (s, 1Н); 9.04 (s, 1Н); 8.40 (s, 1Н); 8.23 (s, 1Н); 8.19 (d, 1Н); 8.10 (s, 1Н); 7,45 (s, 1Н); 7.25-7.19 (m, 4Н); 7.13 (t, 1Н); 3.92 (s, 3Н) 3.33 (t, 2Н); 2.65 (t, 2Н); 1.72-1.56 (dm, 4Н); ррm.
MS: m/z 401 (М+Н+).
Пример 6 (реакция согласно Схеме 1, стадия 6):
Пример 6.1: N*7*-(3,4,5-Триметоксифенил)-[1,5]нафтиридин-2,7-диамин
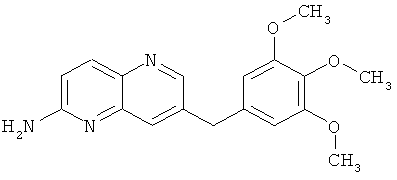
В атмосфере аргона вносили 200 мг (892 мкмоль, 1 экв.) 7-бром-1,5-нафтиридин-2-иламина, 196,3 мг (1,07 ммоль, 1,2 экв.) 3,4,5-триметоксианилина, 2 мг (2,3 мкмоль, 0,0025 экв.) трис(дибензилиденацетон)дипалладия, 4 мг (6,7 мкмоль, 0,0075 экв.) 2,2'-бис(дифенилфосфино)-1,1'-бинафтила и 120 мг (1,24 ммоль, 1,4 экв.) тербутоксида натрия в 6 мл толуола. Смесь перемешивали при 80°С в течение 24 часов. Смесь оставляли до достижения ею комнатной температуры и добавляли воду. Водный слой экстрагировали при помощи метиленхлорида. Органический слой высушивали над Na2SО4, фильтровали и выпаривали досуха. Осадок очищали с помощью колоночной хроматографии с применением в качестве элюента метиленхлорида/этанола в соотношении 96/4. Растворитель выпаривали досуха с получением 50 мг желтого порошка с выходом 17%.
Выход: 50 мг (17% от теоретического).
Температура плавления: 192-194°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=8.58 (s, 1Н); 8.32 (d, 1Н); 7.79 (d, 1Н); 7.33 (d, 1Н); 6.72 (d, 1Н); 6.56 (s, 2Н); 6.52 (s, 2Н); 3.79 (s, 6Н); 3.67 (s, 3Н) ррm.
MS: m/z 327 (М+Н+).
Пример 7 (реакция согласно Схеме 1, стадия 7):
Пример 7.1: 1-Этил-3-[7-(3,4,5-триметоксифениламино)-[1,5]нафтиридин-2-ил]-тиомочевина (6)
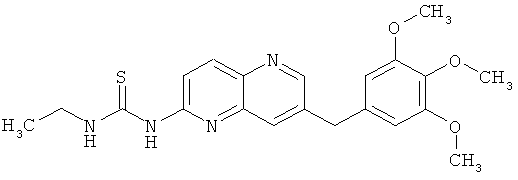
В герметичном реакторе вносили 88 мг (269 мкмоль, 1 экв.) N*7*-(3,4,5-триметоксифенил)-[1,5]нафтиридин-2,7-диамина и 48 мкл (538 мкмоль, 2 экв.) этилизотиоцианата в 3 мл пиридина. Смесь перемешивали при 140°С в течение 24 часов. Смесь оставляли до достижения ею комнатной температуры и растворитель удаляли под пониженным давлением. Водный слой экстрагировали при помощи метиленхлорида. Осадок очищали с помощью колоночной хроматографии с применением в качестве элюента метиленхлорида/этанола в соотношении 96/4. Растворитель выпаривали досуха с получением 56 мг желтого порошка с выходом 51%.
Выход: 56 мг (51% от теоретического).
Температура плавления: 237-238°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=12.21 (t, 1Н); 10.84 (s, 1Н); 8.95 (s, 1Н); 8.59 (d, 1Н); 8.15 (d, 1Н); 7.79 (d, 1Н); 7.27 (d, 1Н); 6.61 (s, 2Н); 3.82 (s, 6Н); 3.72-3.67 (m, 5Н); 1.28 (t, 3Н) ррm.
MS: m/z 414 (M+H+).
Пример 8 (реакция согласно Схеме 2, стадия 1):
Пример 8: 7-Бром-[1,5]нафтиридин-4-иламин
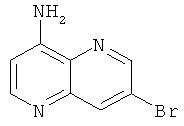
В герметичном реакторе вносили 500 мг (2,04 ммоль, 1 экв.) 7-бром-4-хлор-1,5-нафтиридина (G. В. Barlin et al. Aust. J. Chem. 1985, 38, 459-465) и 12 мл (71,3 ммоль, 35 экв.) 20% водного раствора аммиака в 12 мл диоксана. Смесь перемешивали при 160°С в течение 24 часов. Смесь оставляли до достижения ею комнатной температуры и добавляли воду. Водный слой экстрагировали при помощи этилацетата. Органический слой высушивали над Na2SО4, фильтровали и выпаривали досуха. Осадок очищали с помощью колоночной хроматографии с применением в качестве элюента метиленхлорида и затем метиленхлорида/этанола в соотношении 98/2. Растворитель выпаривали досуха с получением 350 мг белого порошка с выходом 76%.
Выход: 350 мг (76% от теоретического).
Температура плавления: 168-169°C.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=8,82 (d, 1Н); 8,43 (d, 1Н); 8,40 (d, 1Н); 7,08 (s, 2Н); 6,79 (d, 1Н) ppm.
MS: m/z 225 (M+H+).
Пример 9 (реакция согласно Схеме 2, стадия 2):
Пример 9.1: 1-(7-Бром-[1,5]нафтиридин-4-ил)-3-трет-бутилмочевина
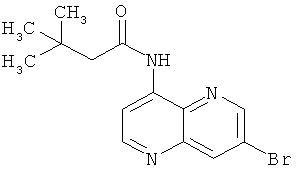
В герметичном реакторе вносили 500 мг (2,23 ммоль, 1 экв.) 7-бром-1,5-нафтиридин-4-иламина и 508 мкл (4,46 ммоль, 2 экв.) трет-бутилизоцианата в 5 мл пиридина. Смесь перемешивали при 140°С в течение 24 часов. Смесь оставляли до достижения ею комнатной температуры и удаляли растворитель под пониженным давлением. Осадок очищали с помощью колоночной хроматографии с применением в качестве элюента метиленхлорида/этанола в соотношении 99/1. Растворитель выпаривали досуха с получением 540 мг белого порошка с выходом 75%.
Выход: 540 мг (75% от теоретического).
Температура плавления: 192-193°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.65 (s, 1Н); 8.98 (d, 1Н); 8.74 (d, 1Н); 8.66 (d, 1Н); 8.42 (d, 1Н); 7.60 (s, 1Н); 1.36 (s, 9Н) ррm.
MS: m/z 323 (М+Н+); 325 ((М+2)+Н+).
Приведенные ниже примеры были получены аналогично Примеру 9.1: 1-(7-Бром-[1,5]нафтиридин-4-ил)-3-трет-бутилмочевина.
Пример 9.2:1-(7-Бром-[1,5]нафтиридин-4-ил)-3-этилмочевина
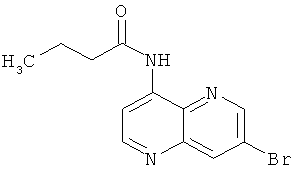
Выход: 95 мг (84% от теоретического).
Температура плавления: 222-223°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.69 (s, 1Н); 9.01 (d, 1Н); 8.77 (d, 1Н); 8.68 (d, 1Н); 8.44 (d, 1Н); 7.67 (t, 1Н); 3.25-3.14 (m, 2Н); 1.13 (t, 3Н) ррm.
MS: m/z 295 (М+Н+); 297 ((М+2)+Н+).
Пример 9.3:1-(7-Бром-[1,5]нафтиридин-4-ил)-3-циклогексилмочевина
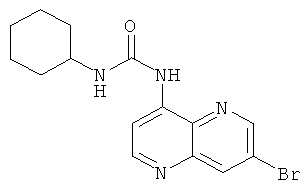
Выход: 129 мг (55% от теоретического).
Температура плавления: 179-180°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.69 (s, 1Н); 9.00 (d, 1Н); 8.77 (d, 1Н); 8.67 (d, 1Н); 8.43 (d, 1Н); 7.68 (d, 1Н); 3.59-3.57 (m, 1Н); 0.92-1.91 (m, 10Н) ррm.
Пример 9.4: 1-(7-Бром-[1,5]нафтиридин-4-ил)-3-фенилмочевина
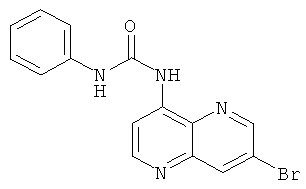
Выход: 202 мг (66% от теоретического).
Температура плавления: 195-196°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=10.08 (s, 1Н); 10.04 (s, 1Н); 9.08 (d, 1Н); 8.86 (d, 1Н); 8.74 (d, 1Н); 8.50 (d, 1Н); 7.57 (d, 2Н); 7.38 (dd, 2Н); 7.08 (t, 1Н) ррm.
MS: m/z 343 (М+Н+); 345 ((М+2)+Н+).
Пример 9.5:1-Аллил-3-(7-бром-[1,5]нафтиридин-4-ил)-мочевина
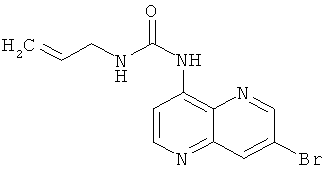
Выход: 140 мг (51% от теоретического).
Температура плавления: 179-180°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.85 (s, 1Н); 9.02 (d, 1Н); 8.78 (d, 1Н); 8.69 (d, 1Н); 8.44 (d, 1Н); 7.80 (t, 1Н); 5.98-5.87 (m, 1Н); 5.26 (dq, 1Н); 5.15 (dq, 1Н); 3.87-3.82 (m, 2Н) ррm.
MS: m/z 307 (М+Н+); 309 ((М+2)+Н+).
Пример 9.6: 1-(7-Бром-[1,5]нафтиридин-4-ил)-3-изопропилмочевина
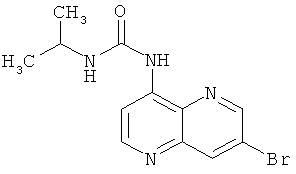
Выход: 150 мг (72% от теоретического).
Температура плавления: 175-177°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.63 (s, 1Н); 9.00 (d, 1Н); 8.77 (d, 1Н); 8.68 (d, 1Н); 8.43 (d, 1Н); 7.64 (d, 1Н); 3.89-3.82 (m, 1Н); 1.17 (d, 6Н).
MS: m/z 309 (М+Н+); 311 ((М+2)+Н+).
Пример 9.7: 1-(7-Бром-[1,5]нафтиридин-4-ил)-3-бензилмочевина
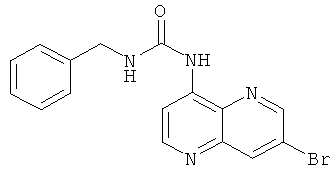
Выход: 232 мг (98 % от теоретического).
Температура плавления: 138-140°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.87 (s, 1Н); 9.01 (d, 1Н); 8.78 (d, 1Н); 8.69 (d, 1Н); 8.46 (d, 1Н); 8.16 (t, 1Н); 7.39-7.27 (m, 5Н); 4.35 (d, 2Н).
MS: m/z 357 (M+H+); 359 ((M+2)+H+).
Пример 9.8: 1-(7-Бром-[1,5]нафтиридин-4-ил)-3-бутилмочевина
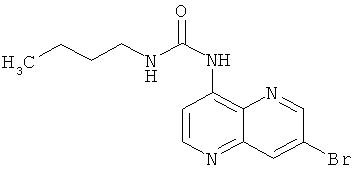
Выход: 50 мг (23% от теоретического).
Температура плавления: 158-160°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.73 (s, 1Н); 9.01 (d, 1Н); 8.77 (d, 1Н); 8.68 (d, 1Н); 8.44 (d, 1Н); 7.67 (t, 1Н); 3.18 (dt, 2Н); 1.51-1.36 (m, 4Н); 0.95 (t, 3Н).
MS: m/z 323 (М+Н+); 325 ((М+2)+Н+).
Пример 9.9: 1-(7-Бром-[1,5]нафтиридин-4-ил)-3-циклопропилмочевина
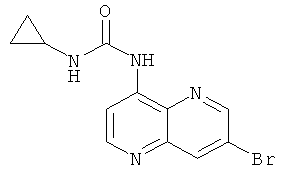
В атмосфере аргона вносили 217 мг (968 мкмоль, 1 экв.) 7-бром-[1,5]нафтиридин-4-иламина, 5 мл (34,9 ммоль, 27 экв.) триэтиламина и 316 мг (1,07 ммоль, 1 экв.) трифосгена в 25 мл дихлометана при 0°С. Смесь перемешивали при нагревании с обратным холодильником в течение 1 часа. Смесь оставляли до достижения ею комнатной температуры и добавляли 148 мкл (2,2 ммоль, 2,1 экв.) циклопропиламина. Затем смесь перемешивали при нагревании с обратным холодильником в течение 1 часа, после чего оставляли до достижения ею комнатной температуры и добавляли воду. Водный слой экстрагировали при помощи метиленхлорида. Органические слои высушивали над Nа2SО4, фильтровали и выпаривали досуха. Осадок очищали с помощью колоночной хроматографии с применением в качестве элюента метиленхлорида/этанола в соотношении 96/4. Растворитель выпаривали досуха с получением 196 мг коричневого порошка с выходом 65%.
Выход: 196 мг (65% от теоретического).
Температура плавления: 205-206°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.62 (s, 1Н); 9.00 (d, 1Н); 8.78 (d, 1Н); 8.68 (d, 1Н); 8.43 (d, 1Н); 7.82 (s, 1Н); 2.69-2.63 (m, 1Н); 0.72 and 0.47 (bs, 4Н) ррm.
MS: m/z 307 (М+Н+); 309 ((М+2)+Н+).
Приведенные ниже примеры были получены аналогично Примеру 9.6: 1-(7-Бром-[1,5]нафтиридин-4-ил)-3-циклопропилмочевина.
Пример 9.10: 1-(7-Бром-[1,5]нафтиридин-4-ил)-3-(4-фенилбутил)-мочевина

Выход: 161 мг (60 % от теоретического).
Температура плавления: 115-116°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.72 (s, 1Н); 9.00 (d, 1Н); 8.76 (d, 1Н); 8.68 (d, 1Н); 8.43 (d, 1Н); 7.67 (t, 1Н); 7.33-7.19 (m, 5Н); 3.21 (q, 2Н); 2.64 (t, 2Н); 1.69-1.61 (m, 2Н); 1.55-1.49 (m, 2Н) ррm.
MS: m/z 399 (М+Н+); 401 ((М+2)+Н+).
Пример 9.11: 1-(7-Бром-[1,5]нафтиридин-4-ил)-3-циклобутилмочевина
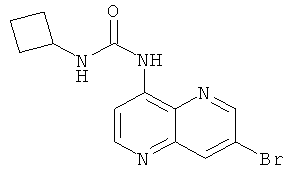
Выход: 202 мг (70% от теоретического).
Температура плавления: 201-202°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.62 (s, 1Н); 9.01 (d, 1Н); 8.77 (d, 1Н); 8.68 (d, 1Н); 8.41 (d, 1Н); 7.98 (d, 1Н); 4.25-4.16 (m, 1Н); 2.32-2.44 and 1.95-1.84 (m, 4Н); 1.75-1.64 (m, 2Н) ррm.
MS: m/z 321 (М+Н+); 323 ((М+2)+Н+).
Пример 9.12: 1-(7-Бром-[1,5]нафтиридин-4-ил)-3-пропилмочевина
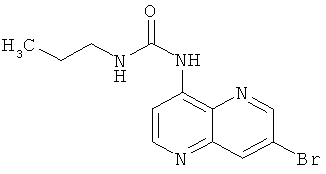
Выход: 151 мг (52% от теоретического).
Температура плавления: 173-174°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.72 (s, 1Н); 8.99 (d, 1Н); 8.76 (d, 1Н); 8.66 (d, 1Н); 8.44 (d, 1Н); 7.68 (t, 1Н); 3.15 (q, 2Н); 1.57-1.47 (m, 2Н); 0.96 (t, 3Н) ррm.
MS: m/z 309 (М+Н+); 311 ((М+2)+Н+).
Пример 9.13: 1-(7-Бром-[1,5]нафтиридин-4-ил)-3-(2,2,2-трифторэтил)-мочевина

Выход: 102 мг (56% от теоретического).
Температура плавления: 181-182°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.99 (s, 1Н); 9.04 (d, 1Н); 8.82 (d, 1Н); 8.71 (d, 1Н); 8.43 (d, 1Н); 8.30 (t, 1Н); 4.13-4.03 (m, 2Н) ррm.
MS: m/z 349 (М+Н+); 351 ((М+2)+Н+).
Пример 9.14: 1-(7-Бром-[1,5]нафтиридин-4-ил)-3-(2-фенилэтил)-мочевина
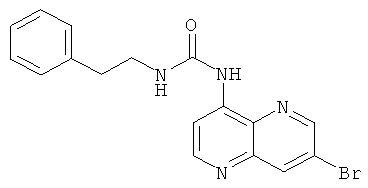
Выход: 119 мг (65% от теоретического).
Температура плавления: 119-121°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.89 (s, 1Н); 9.00 (d, 1Н); 8.75 (d, 1Н); 8.67 (d, 1Н); 8.45 (d, 1Н); 7.85 (t, 1Н); 7.35-7.21 (m, 5Н); 3.45 (dt, 2Н); 2.86 (t, 2Н).
MS: m/z 371 (М+Н+); 373 ((М+2)+Н+).
Пример 9.15: 1-(7-Бром-[1,5]нафтиридин-4-ил)-3-циклопентилмочевина
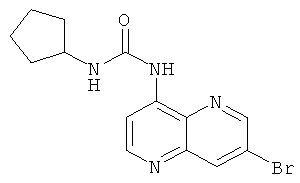
Выход: 55 мг (28% от теоретического).
Температура плавления: 183-185°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.65 (s, 1Н); 9.00 (d, 1Н); 8.75 (d, 1Н); 8.66 (d, 1Н); 8.42 (d, 1Н); 7.82 (d, 1Н); 4.15-4.06 (m, 1Н); 1.95-1.24 (m, 8Н).
MS: m/z 335 (М+Н+); 337 ((М+2)+Н+).
Пример 9.16: 1-(7-Бром-[1,5]нафтиридин-4-ил)-3-(3,3-дифторциклобутил)-мочевина
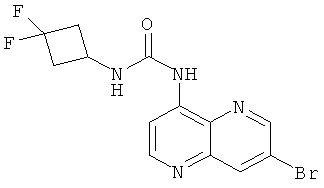
Раствор 424 мг (2,1 ммоль, 1 экв.) 4-нитрофенилового эфира хлормуравьиной кислоты в 5 мл сухого ацетонитрила охлаждали до -5°С при помощи смеси льда и NaCl. К указанному раствору медленно добавляли 300 мг (2,1 ммоль, 1 экв.) гидрохлорида 3,3-дифторциклобутиламина, поддерживая при этом температуру ниже 0°С. После этого добавляли раствор 0,59 мл (4,2 ммоль, 2 экв.) триэтиламина в 5 мл ацетонитрила, поддерживая температуру ниже 0°С. После того как добавление было завершено, реакционную смесь перемешивали при комнатной температуре в течение ночи. Добавляли воду и водный слой экстрагировали с помощью метиленхлорида. Органические слои высушивали над Nа2SО4, фильтровали и выпаривали досуха. Осадок очищали с помощью колоночной хроматографии с применением в качестве элюента метиленхлорида/этанола в соотношении 96/4. Растворитель выпаривали досуха с получением 200 мг белого порошка с выходом 34%.
Смесь 200 мг (734 ммоль, 1 экв.) 4-нитрофенилового эфира N-3,3-дифторциклобутилкарбаминовой кислоты и 82 мг (367 мкмоль, 0,5 экв.) 7-бром-[1,5]нафтиридин-4-иламина, и 10 мкл (7,34 ммоль, 0,1 экв.) триэтиламина в 2 мл сухого ТГФ перемешивали при 60°С в течение 24 часов. Реакционную смесь затем охлаждали до комнатной температуры и выпаривали досуха. Осадок очищали с помощью колоночной хроматографии с применением в качестве элюента метиленхлорида/этанола в соотношении 96/4. Растворитель выпаривали досуха с получением 101 мг белого порошка с выходом 77%.
Выход: 101 мг (77% от теоретического).
Температура плавления: 184-185°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.70 (s, 1Н); 9.03 (d, 1Н); 8.80 (d, 1Н); 8.70 (d, 1Н); 8.41 (d, 1Н); 8.23 (d, 1Н); 4.11 (bs, 1Н); 3.09-2.64 (m, 4Н) ppm. MS: m/z 358 (M+H+).
Приведенные ниже примеры были получены аналогично Примеру 9.11: 1-(7-Бром-[1,5]нафтиридин-4-ил)-3-(3,3-дифторциклобутил)-мочевина.
Пример 9.17: 1-(7-Бром-[1,5]нафтиридин-4-ил)-3-гексилмочевина
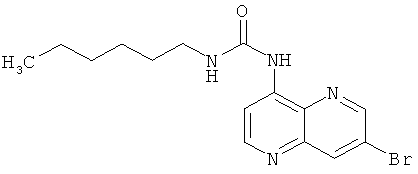
Выход: 157 мг (62% от теоретического).
Температура плавления: 186-187°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.72 (s, 1Н); 9.00 (d, 1Н); 8.76 (d, 1Н); 8.67 (d, 1Н); 8.44 (d, 1Н); 7.66 (t, 1Н); 3.17 (dt, 2Н); 1.51-1.47 (m, 2Н); 1.42-1.34 (m, 6Н); 0.92 (t, 3Н) ррm.
MS: m/z 352 (М+Н+).
Пример 10 (реакция согласно Схеме 2, стадия 3):
Пример 10.1: 1-[7-(3,4-Диметоксифенил)-[1,5]нафтиридин-4-ил]-3-этилмочевина (7)
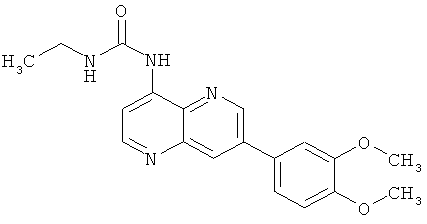
В атмосфере аргона вносили 100 мг (3638 мкмоль, 1 экв.) 1-(7-бром-[1,5]нафтиридин-4-ил)-3-этилмочевины, 122 мг (676 мкмоль, 2 экв.) 3,4-диметоксифенилбороновой кислоты, 108 мг (1,02 ммоль, 3 экв.) карбоната натрия и 39 мг (34 мкмоль, 0,1 экв. тетракис(трифенилфосфин)палладия в 11 мл смеси диметилформамида/воды (10/1). Смесь перемешивали при 80°С в течение 16 часов. Смесь оставляли до достижения ею комнатной температуры и добавляли воду. Водный слой экстрагировали с помощью метиленхлорида. Органические слои высушивали над Na2SO4, фильтровали и выпаривали досуха. Осадок очищали с помощью колоночной хроматографии с применением в качестве элюента метиленхлорида/этанола в соотношении 96/4. Растворитель выпаривали досуха с получением после тритурации с диизопропиловым эфиром 80 мг белого порошка с выходом 67%.
Выход: 80 мг (67% от теоретического).
Температура плавления: 215-216°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.69 (s, 1Н); 9.23 (d, 1Н); 8.77 (d, 1Н); 8.58 (d, 1Н); 8.38 (d, 1Н); 7.71 (t, 1Н); 7.55-7.50 (m, 2Н); 7.17 (d, 1Н); 3.95 (s, 3Н); 3.87 (s, 3Н); 3.29-3.16 (m, 2Н); 1.14 (t, 3Н) ррm.
MS: m/z 353 (М+Н+).
Приведенные ниже примеры были получены аналогично Примеру 10.1: 1-[7-(3,4-Диметоксифенил)-[1,5]нафтиридин-4-ил]-3-этилмочевина (7).
Пример 10.2: 1-трет-Бутил-3-[7-(3,4-диметоксифенил)-[1,5]нафтиридин-4-ил]-мочевина (8)
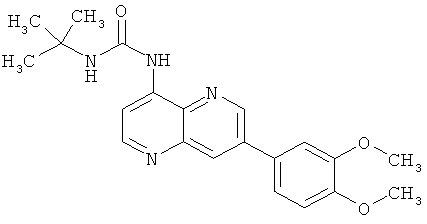
Выход: 61 мг (52% от теоретического).
Температура плавления: 215-216°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.67 (s, 1Н); 9.21 (d, 1Н); 8.72 (d, 1Н); 8.57 (d, 1Н); 8.36 (d, 1Н); 7.63 (s, 1Н); 7.55-7.50 (m, 2Н); 7.17 (d, 1Н); 3.95 (s, 3Н); 3.87 (s, 3Н); 1.14 (s, 9Н) ррm.
MS: m/z 381 (М+Н+).
Пример 10.3: 1-Этил-3-[7-(4-гидрокси-3-метоксифенил)-[1,5]нафтиридин-4-ил]-мочевина (9)
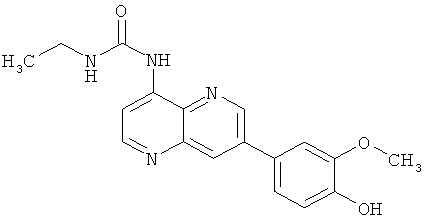
Выход: 54 мг (47% от теоретического).
Температура плавления: 202-203°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.88 (s, 1Н); 9.49 (s, 1Н); 9.26 (d, 1Н); 8.80 (d, 1Н); 8.54 (d, 1Н); 8.43 (d, 1Н); 7.77 (t, 1Н); 7.51 (s, 1Н); 7.42 (d, 1Н); 7.00 (d, 1Н); 3.95 (s, 3Н); 3.28-3.18 (m, 2Н); 1.14 (t, 3Н) ррm.
MS: m/z 339 (М+Н+).
Пример 10.4: 1-Этил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (10)
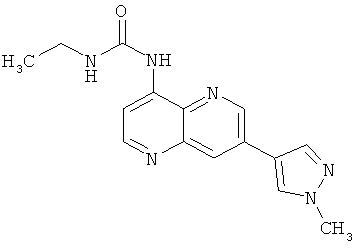
Выход: 51 мг (56% от теоретического).
Температура плавления: 215-216°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.64 (s, 1Н); 9.18 (d, 1Н); 8.71 (d, 1Н); 8.56 (s,1H); 8.49 (d, 1Н); 8.32 (d, 1Н); 8.26 (s, 1Н); 7.68 (t, 1Н); 3.96 (s, 3Н); 3.23-3.19 (m, 2Н); 1.14 (t, 3Н) ррm.
MS: m/z 297 (М+Н+).
Пример 10.5: 1-трет-Бутил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (11)
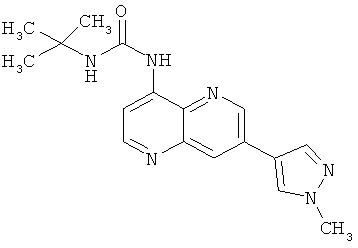
Выход: 52 мг (52 % от теоретического).
Температура плавления: 215-216°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.61 (s, 1Н); 9.16 (d, 1Н); 8.70 (d, 1Н); 8.56 (s,1H); 8.48 (d, 1Н); 8.31 (d, 1Н); 8.25 (s, 1Н); 7.61 (s, 1Н); 3.96 (s, 3Н); 1.37 (s, 9Н) ppm.
MS: m/z 325 (M+H+).
Пример 10.6: 1-трет-Бутил-3-[7-(4-гидрокси-3-метоксифенил)-[1,5]нафтиридин-4-ил]-мочевина (12)
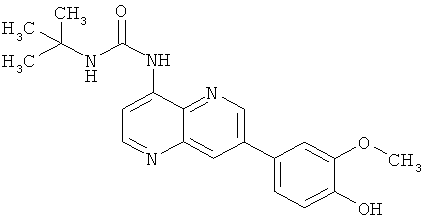
Выход: 100 мг (62% от теоретического).
Температура плавления: 158-159°С.
1Н-ЯМР (ДМСО-d6) 400 МГц): δ=9.66 (s, 1Н); 9.41 (s, 1Н); 9.19 (d, 1Н); 8.73 (d, 1Н); 8.53 (d, 1Н); 8.35 (d, 1Н); 7.62 (s, 1Н); 7.50 (d, 1Н); 7.40 (dd, 1Н); 7.99 (d, 1Н); 3.95 (s, 3Н); 1.14 (s, 9Н) ррm.
MS: m/z 367 (М+Н+).
Пример 10.7: 1-трет-Бутил-3-[7-(3,5-дихлор-4-гидроксифенил)-[1,5]нафтиридин-4-ил]-мочевина (13)
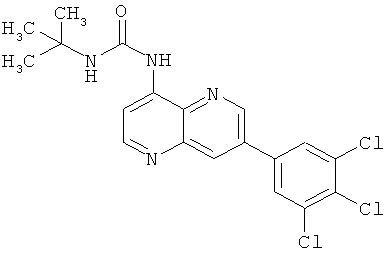
Выход: 52 мг (41% от теоретического).
Температура плавления: >300°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=10.57 (s, 1Н); 9.67 (s, 1Н); 9.21 (d, 1Н); 8.75 (d, 1Н); 8.60 (d, 1Н); 8.38 (d, 1Н); 8.06 (s, 2Н); 7.65 (s, 1Н); 1.38 (t, 9Н) ррm.
MS: m/z 405 (М+Н+); 407 ((М+2)+Н+); 409 ((М+4)+Н+).
Пример 10.8: 1-Циклопропил-3-[7-(4-гидрокси-3-метоксифенил)-[1,5]нафтиридин-4-ил]-мочевина (14)
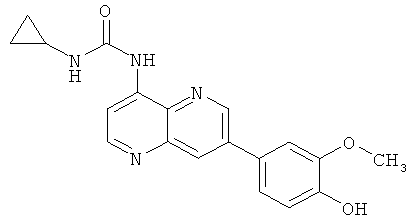
Выход: 20 мг (17% от теоретического).
Температура плавления: 235-236°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.63 (s, 1Н); 9.42 (s, 1Н); 9.21 (s, 1Н); 8.78 (d, 1Н); 8.55 (s, 1Н); 8.34 (d, 1Н); 7.85 (s, 1Н); 7.51 (s, 1Н); 7.41 (d, 1Н); 6.98 (d, 1Н); 3.95 (s, 3Н); 2.72-2.64 (m, 1Н); 0.74 and 0.50 (bs, 4Н) ррm.
MS: m/z 351 (М+Н+).
Пример 10.9: 1-[7-(3,5-Дихлор-4-гидроксифенил)-[1,5]нафтиридин-4-ил]-3-этил-мочевина (15)
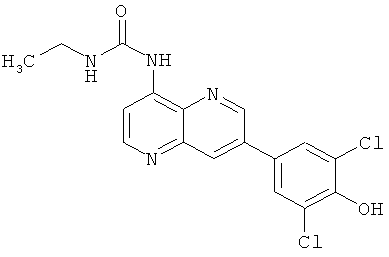
Выход: 23 мг (20% от теоретического).
Температура плавления: >300°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=10.59 (s, 1Н); 9.69 (s, 1Н); 9.23 (d, 1Н); 8.78 (d, 1Н); 8.61 (d, 1Н); 8.40 (d, 1Н); 8.05 (s, 2Н); 7.73 (t, 1Н); 3.25-3.17 (m, 2Н); 1.14 (t, 3Н) ррm.
MS: m/z 377 (М+Н+); 379 ((М+2)+Н+); 381 ((М+4)+Н+).
Пример 10.10: 1-Этил-3-[7-(4-гидрокси-3,5-диметил фенил)-[1,5]нафтиридин-4-ил]-мочевина (16)
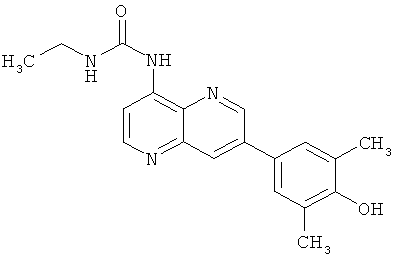
Выход: 60 мг (52% от теоретического).
Температура плавления: 213-214°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.69 (s, 1Н); 9.19 (d, 1Н); 8.75 (d, 1Н); 8.66 (s, 1Н); 8.44 (d, 1Н); 8.36 (d, 1Н); 7.70 (t, 1Н); 7.56 (s, 2Н); 3.23-3.19 (m, 2Н); 2.32 (s, 6Н); 1.14 (t, 3Н) ррm.
MS: m/z 337 (М+Н+).
Пример 10.11: 1-Циклобутил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (17)
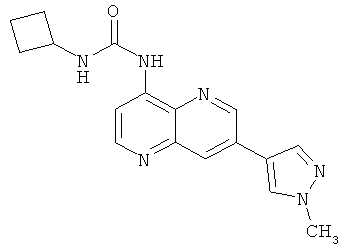
Выход: 53 мг (53% от теоретического).
Температура плавления: 215-216°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.57 (s, 1Н); 9.19 (d, 1Н); 8.71 (d, 1Н); 8.56 (s, 1Н); 8.49 (d, 1Н); 8.30 (d, 1Н); 8.26 (s, 1Н); 8.00 (d, 1Н); 4.26-4.18 (m, 1Н); 3.96 (s, 3Н); 2.33-2.24 and 1.95-1.86 (m, 4Н); 1.75-1.64 (m, 2Н) ррm.
MS: m/z 323 (М+Н+).
Пример 10.12: 1-Циклопропил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (18)
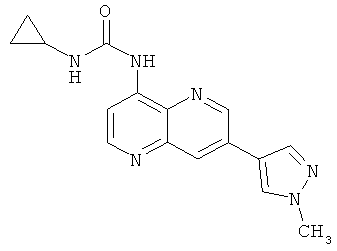
Выход: 53 мг (58% от теоретического).
Температура плавления: 223-224°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.59 (s, 1Н); 9.18 (d, 1Н); 8.74 (d, 1Н); 8.56 (s, 1Н); 8.50 (d, 1Н); 8.32 (d, 1Н); 8.25 (s, 1Н); 7.83 (bs, 1Н); 3.96 (s, 3Н); 2.71-2.64 (m, 1Н); 0.73 and 0.49 (bs, 4Н) ppm.
MS: m/z 309 (M+H+).
Пример 10.13: 1-[7-(1-Метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-3-пропилмочевина (19)
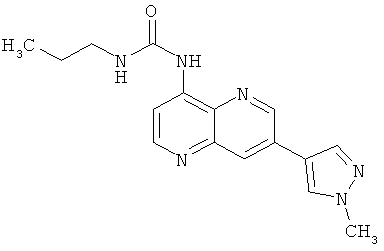
Выход: 72 мг (70% от теоретического).
Температура плавления: 216-217°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.68 (s, 1Н); 9.18 (s, 1Н); 8.72 (d, 1Н); 8.56 (s, 1Н); 8.49 (s, 1Н); 8.33 (d, 1Н); 8.25 (s, 1Н); 7.07 (bs, 1Н); 3.96 (s, 3Н); 3.15 (q, 2Н); 1.56-1.49 (m, 2Н); 0.96 (t, 3Н) ррm.
MS: m/z 311 (М+Н+).
Пример 10.14: 1-[7-(1-Метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-3-(2,2,2-трифторэтил)-мочевина (20)
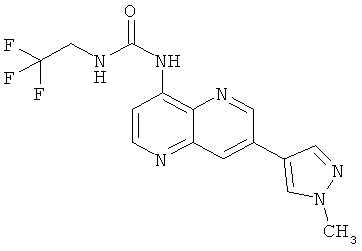
Выход: 71 мг (63% от теоретического).
Температура плавления: >300°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.95 (s, 1Н); 9.22 (d, 1Н); 8.76 (d, 1Н); 8.57 (s, 1Н); 8.52 (d, 1Н); 8.33 (t, 1Н); 8.32 (d, 1Н); 8.27 (s, 1Н); 4.13-4.02 (m, 2Н); 3.96 (s, 3Н) ррm.
MS: m/z 351 (М+Н+).
Пример 10.15: 1-[7-(1-Метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-3-(4-фенилбутил)-мочевина (21)
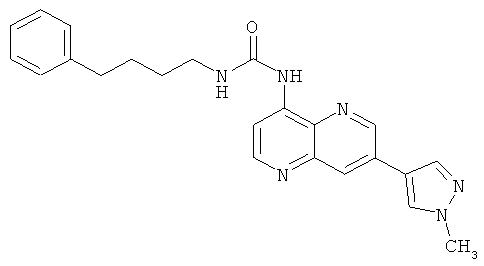
Выход: 70 мг (60 % от теоретического).
Температура плавления: 185-186°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.66 (s, 1Н); 9.18 (d, 1Н); 8.72 (d, 1Н); 8.56 (s, 1Н); 8.49 (d, 1Н); 8.32 (d, 1Н); 8.26 (s, 1Н); 7.69 (t, 1Н); 7.34-7.19 (m, 5Н); 3.96 (s, 3Н); 3.22 (q, 2Н); 2.65 (t, 2Н); 1.72-1.64 (m, 2Н); 1.56-1.49 (m, 2Н) ррm.
MS: m/z 401 (М+Н+).
Пример 10.16: 1-Циклогексил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (22)
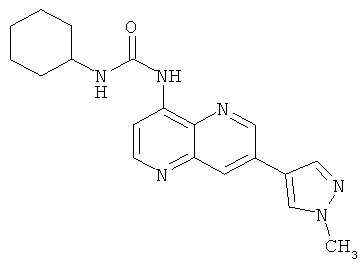
Выход: 30 мг (30% от теоретического).
Температура плавления: 200-201°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.64 (s, 1Н); 9.18 (d, 1Н); 8.71 (d, 1Н); 8.57 (s, 1Н); 8.49 (d, 1Н); 8.32 (d, 1Н); 8.26 (s, 1Н); 7,69 (d, 1Н); 3.60-3.58 (m, 1Н); 1.21-1.94 (m, 10Н); 3.97 (s, 3Н) ррm.
MS: m/z 351 (М+Н+).
Пример 10.17: 1-[7-(1-Метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-3-фенилмочевина (23)
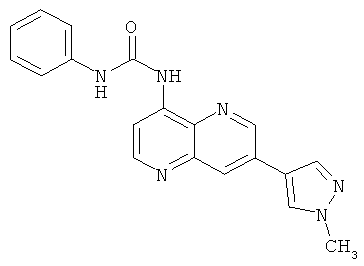
Выход: 33 мг (33% от теоретического).
Температура плавления: 294-295°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=10.10 (s, 1Н); 10.00 (s, 1Н); 9.25 (d, 1Н); 8.80 (d, 1Н); 8.59 (s, 1Н); 8.55 (d, 1Н); 8.39 (d, 1Н); 8.29 (s, 1Н); 7.58 (d, 2Н); 7.38 (dd, 2Н); 7.08 (t, 1Н); 3.99 (s, 3Н) ррm.
MS: m/z 345 (М+Н+).
Пример 10.18: 1-(3,3-Дифторциклобутил)-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (24)
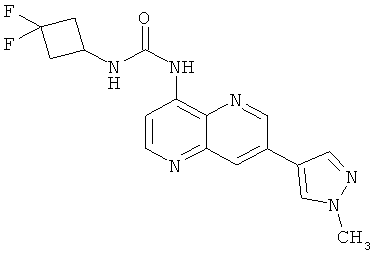
Выход: 14 мг (14 % от теоретического).
Температура плавления: 229-230°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.65 (s, 1Н); 9.20 (d, 1Н); 8.73 (d, 1Н); 8.57 (s, 1Н); 8.50 (d, 1Н); 8.30 (d, 1Н); 8.26 (s, 1Н, Hb); 8.24 (d, 1Н); 4.12 (s, 1Н); 3.96 (s, 3Н); 3.07-2.61 (m, 4Н) ppm.
MS: m/z 359 (M+H+).
Пример 10.19: 1-Гексил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (25)
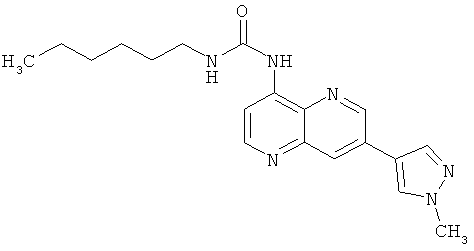
Выход: 50 мг (32% от теоретического).
Температура плавления: 188-189°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.67 (s, 1Н); 9.18 (d, 1Н); 8.71 (d, 1Н); 8.56 (s, 1Н); 8.49 (d, 1Н); 8.32 (d, 1Н); 8.25 (s, 1Н); 7.68 (t, 1Н); 3.96 (s, 3Н); 3.18 (dt, 2Н); 1.53-1.46 (m, 2Н); 1.40-1.32 (m, 6Н); 0.91 (t, 3Н) ррm.
MS: m/z 352 (М+Н+).
Пример 10.20:1-Изопропил-3-[7-(1-метил-1Н-пиразол-4-уl)-[1,5]нафтиридин-4-ил]-мочевина (30)
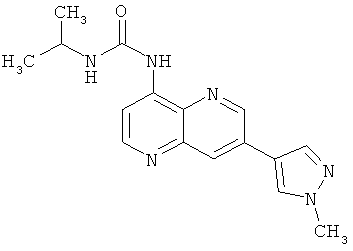
Выход: 25 мг (30% от теоретического).
Температура плавления: 259-230°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.58 (s, 1Н); 9.18 (d, 1Н); 8.71 (d, 1Н); 8.56 (s, 1Н); 8.49 (d, 1Н); 8.32 (d, 1Н); 8.25 (s, 1Н); 7.65 (d, 1Н); 3.96 (s, 3Н); 3.88-3.83 (m, 1Н); 1.71 (d, 6Н) ррm.
MS: m/z 311 (М+Н+).
Пример 10.21: 1-Бензил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (31)
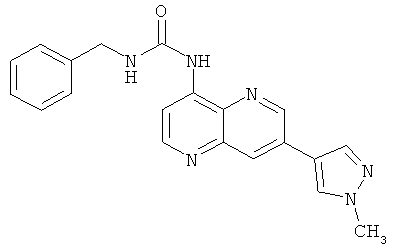
Выход: 50 мг (38% от теоретического).
Температура плавления:237-238°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.81 (s, 1Н); 9.19 (d, 1Н); 8.73 (d, 1Н); 8.56 (s, 1Н); 8.50 (d, 1Н); 8.35 (d, 1Н); 8.26 (s, 1Н); 8.18 (t, 1Н); 7.42-7.29 (m, 5Н); 4.42 (d, 2Н); 3.97 (s, 3Н) ррm.
MS: m/z 359 (М+Н+).
Пример 10.22: 1-Бутил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (32)
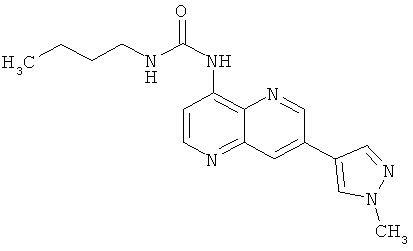
Выход: 14 мг (24% от теоретического).
Температура плавления: 219-220°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=10.12 (s, 1Н); 8.86 (d, 1Н); 8.64 (d, 1Н); 8.48 (s, 1Н); 8.38 (d, 1Н); 7.97 (d, 1Н); 7.87 (s, 1Н); 7.60 (t, 1Н); 3.95 (s, 3Н); 3.42-3.40 (m, 2Н); 1.68-1.65, 1.50-1.47 and 1.00-0.96 (m, 7Н.) ррm.
MS: m/z 325 (М+Н+).
Пример 10.23: 1-[7-(1-Метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-3-фенэтилмочевина (33)
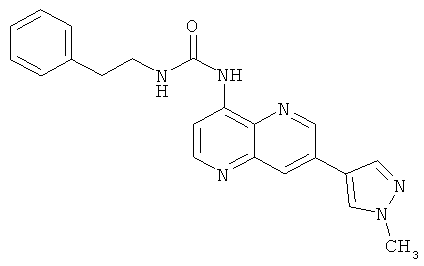
Выход: 50 мг (70% от теоретического).
Температура плавления: 222-223°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.71 (s, 1Н); 9.17 (d, 1Н); 8.72 (d, 1Н); 8.56 (s, 1Н); 8.49 (d, 1Н); 8.34 (d, 1Н); 8.25 (s, 1Н); 7.75 (t, 1Н); 7.38-7.24 (m, 5Н); 3.96 (s, 3Н); 3.48-3.43 (m, 2Н); 2.84 (t, 2Н) ррm.
MS: m/z 373 (М+Н+).
Пример 10.24: 1-Циклопентил-3-[7-(1-метил-1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (34)

Выход: 14 мг (43 % от теоретического).
Температура плавления: 207-208°С.
1Н-ЯМР (ДМСО-d6, 400 МГц): δ=9.60 (s, 1Н); 9.18 (d, 1Н); 8.71 (d, 1Н); 8.56 (s, 1Н); 8.48 (d, 1Н); 8.32 (d, 1Н); 8.26 (s, 1Н); 7,75 (d, 1Н); 4.10-4.02 (m, 1Н); 3.97 (s, 3Н); 1.92-1.26 (m, 8Н) ррm.
MS: m/z 337 (М+Н+).
Пример 10.25: 1-Циклопропил-3-[7-(1Н-пиразол-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (35)
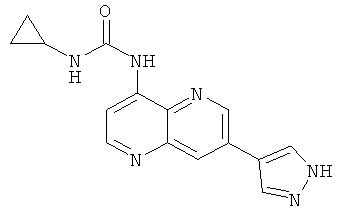
Выход: 30 мг (13% от теоретического).
Температура плавления: 229-231°С.
1Н-ЯМР (ДМСО-d6, 600 МГц): δ=13.13 (s, 1Н); 9.54 (s, 1Н); 9.19 (s, 1Н); 8.69 (d, 1Н); 8.51 (s, 1Н); 8.43 (s, 2Н); 8.28 (d, 1Н); 7.80 (s, 1Н); 2.68-2.62 (m, 1Н); 0.70 (s, 2Н); 0.46 (s, 2H) ррm.
MS: m/z 295 (М+Н+).
Пример 10.26: 1-Циклопропил-3-(7-тиофен-3-ил-[1,5]нафтиридин-4-ил)-мочевина (36)
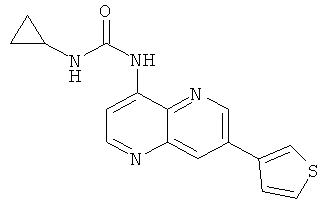
Выход: 159 мг (62% от теоретического).
Температура плавления: 228-229°С.
1Н-ЯМР (ДМСО-d6, 600 МГц): δ=9.58 (s, 1Н); 9.29 (s, 1Н); 8.74 (d, 1Н); 8.62 (s, 1Н); 8.35 (s, 1Н); 8.33 (d, 1Н); 7.88 (d, 1Н); 7.81 (s, 1Н); 7.77 (dd, 1Н); 2.68-2.60 (m, 1Н); 0.70 (s,2H); 0.46 (s,2H)ppm.
MS: m/z 311 (М+Н+).
Пример 10.27: 1-Циклопропил-3-[7-(2-фторпиридин-4-ил)-[1,5]нафтиридин-4-ил]-мочевина (37)

Выход: 68 мг (22% от теоретического).
Температура плавления: 226-229°С.
1Н-ЯМР (ДМСО-d6, 600 МГц): δ=9.65 (s, 1Н); 9.32 (s, 1Н); 8.82 (dd, 2Н); 8.42 (d, 2Н); 8.01 (d, 1Н); 7.89 (s, 1Н); 7.84 (s, 1Н); 2.68-2.62 (m, 1Н); 0.70 (s, 2Н); 0.46 (s, 2Н) ррm.
MS: m/z 324 (M+H+).
Пример 10.28: 1-Циклопропил-3-{7-[1-(2-морфолин-4-илэтил)-1Н-пиразол-4-ил]-[1,5]нафтиридин-4-ил}-мочевина (38)
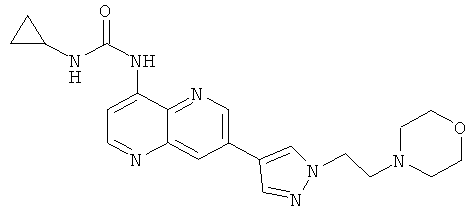
Выход: 280 мг (79% от теоретического).
Температура плавления: 127-129°С.
1Н-ЯМР (ДМСО-d6, 600 МГц): δ=9.54 (s, 1Н); 9.14 (s, 1Н); 8.70 (d, 1Н); 8.56 (s, 1Н); 8.46 (d, 1Н); 8.29 (d, 1Н); 8.22 (s, 1Н); 7.80 (s, 1Н); 4.30 (t, 2Н); 3.60-3.54 (m, 4Н); 2.78 (t, 2Н); 2.67-2.60 (m, 1Н); 2.47-2.41 (m, 4Н); 0.70 (s, 2Н); 0.46 (s, 2Н) ррm.
MS: m/z 408 (М+Н+).
Пример 10.29: 1-Циклопропил-3-(7-фенил-[1,5]нафтиридин-4-ил)-мочевина (39)
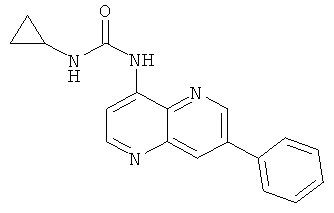
Выход: 80 мг (18% от теоретического).
Температура плавления: 188-190°С.
1Н-ЯМР (ДМСО-d6, 600 МГц): δ=9.63 (s, 1Н); 9.21 (s, 1Н); 8.77 (d, 1Н); 8.56 (s, 1Н); 8.37 (d, 1Н); 7.94 (d, 2Н); 7.81 (s, 1Н); 7.58 (t, 2Н); 7.50 (t, 1Н); 2.68-2.62 (m, 1Н); 0.70 (s, 2Н); 0.46 (s, 2Н); ррm.
MS: m/z 305 (М+Н+).
Пример 10.30: 1-Циклопропил-3-[7-(1Н-индол-5-ил)-[1,5]нафтиридин-4-ил]-мочевина (40)
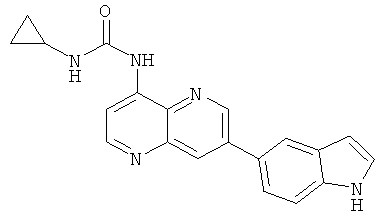
Выход: 100 мг (22% от теоретического).
Температура плавления: 214-215°С.
1Н-ЯМР (ДМСО-d6, 600 МГц): δ=11.27 (s, 1Н); 9.62 (s, 1Н); 9.25 (s, 1Н); 8.74 (d, 1Н); 8.49 (s, 1Н); 8.33 (d, 1Н); 8.12 (s, 1Н); 7.81 (s, 1Н); 7.64 (d, 1Н); 7.57 (d, 1Н); 7.44 (t, 1Н); 6.56 (s, 1Н); 2.68-2.62 (m, 1Н); 0.70 (s, 2Н); 0.46 (s, 2Н) ррm.
MS: m/z 344 (М+Н+).
Биологическое действие соединений согласно настоящему изобретению
Внеклеточные исследования киназы (ALPHA technology)
Ингибирующее действие соединений согласно настоящему изобретению тестировали на различных серин/треонинкиназах и тирозинкиназах человека при помощи ферментных анализов. Применяли рекомбинантные киназы человека, например Aurora-B, cRaf-Mek1-Erk2, Erk2, Pim-1, HIPK1, KDR, TrkA, Yes, с-АbI и другие, в некоторых случаях в виде полноразмерных киназ, в некоторых случаях в виде укороченных фрагментов, но по меньшей мере состоящих из функциональных доменов киназ. Доступные в продаже белки-киназы (Proqinase, Millipore) применяли в качестве рекомбинантных белков с GST-маркером (глутатион-S-трансфераза) или гистидиновым маркером. В зависимости от типа субстрата производили рассчеты различных реакций киназ при помощи подходящих ALPHATM beads (PerkinElmer).
Тесты
Исследование киназы Aurora-B описано детально, и выборочные результаты тестов приведены ниже. Для определения значения показателя IC50 вещества с потенциально ингибирующими свойствами исследовали в 10 полулогарифмически градуированных концентрациях от 3,16 нМ до 100 мкМ. Исследование киназы Aurora-B: Исследуемое соединение, 1,25 нг киназы Aurora-B (#14-835, Upstate/ Millipore), 10 мкМ АТФ и 15 нМ биотинилированного PLK-субстрата (#1300, Cell Signaling) инкубировали на 384-луночном планшете Optiplate (Perkin Elmer) в объеме 15 мкл в течение 1 часа в 25 мМ Tris, 10 мМ MgCl2, 0,1% Твин-20, 100 мкМ NaVO4, 2 мМ ДТТ при значении pH 7,5. Киназную реакцию останавливали путем добавления 10 мл смеси гранул ALPHA (10 мкг/мл, №6760617/ PerkinElmer), предварительно инкубированной с антифосфо-PLK антителом (100 пМ, №5070, Cell Signaling), в 25 мМ Tris, 200 мМ NaCl, 100 мМ ЭДТА и 0,3% БСА, и оставляли стоять на ночь.
На следующее утро при помощи Envision instrument (Perkin Elmer) обнаружили люминесценцию.
Оценка
Расчет % ингибирования на концентрацию соединения производили с применением следующей формулы из исходных данных, определенных при помощи Envision reader:
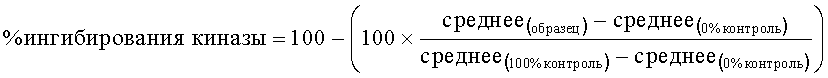
Контроль определяли в 16-кратном размере. 0% контроль не содержал АТФ, в то время как 100% контроль не содержал изучаемого соединения. Значения IC50 определяли с помощью программного обеспечения GraphPadPrism. Соединения согласно настоящему изобретению проявили себя как эффективные ингибиторы Aurora-B и частично Erk2 (см. Таблицу 1).
|
В частности, соединения 10, 17, 18, 19 и 38 характеризуются значениями IC50 менее 100 нМ в отношении Aurora-B и демонстрируют высокую степень селективности в отношении других киназ.
Соединения 1, 2, 3, 4, 5, 26, 27 и 28 демонстрируют двойную активность в отношении Aurora-B и Еrk2 (или каскада cRaf-Mek-Erk, соответственно).