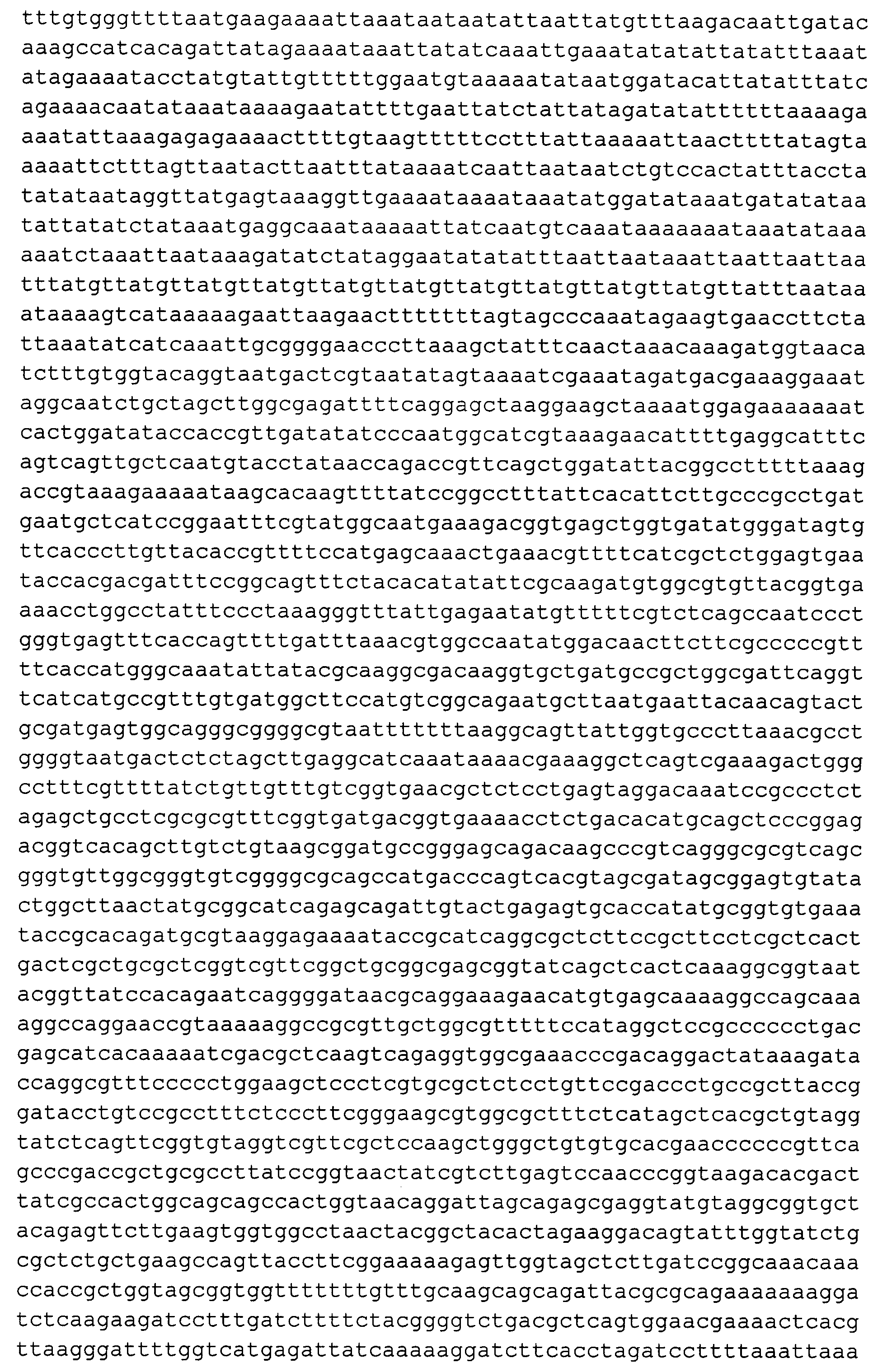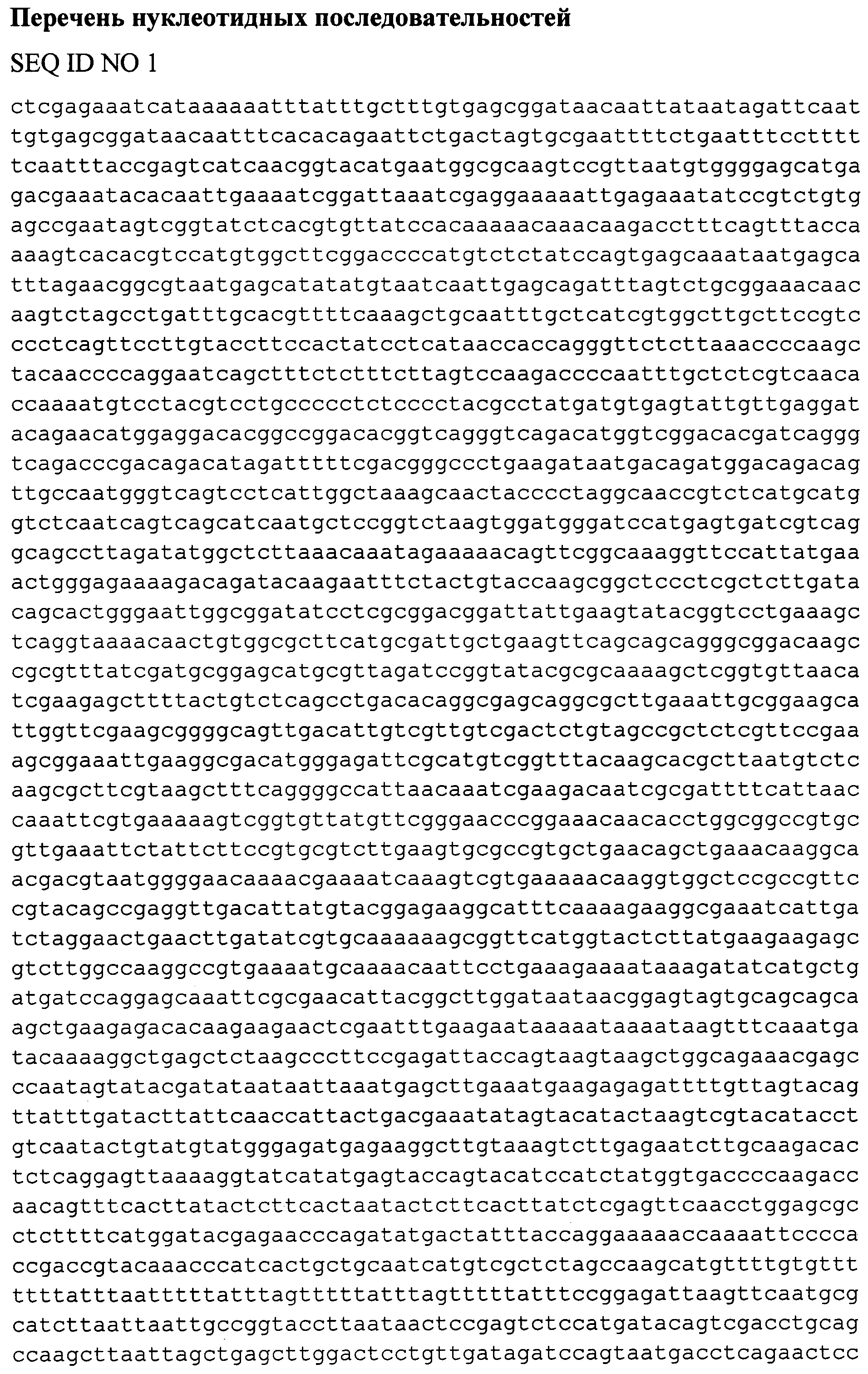Результат интеллектуальной деятельности: ИНТЕГРАТИВНАЯ ГЕНЕТИЧЕСКАЯ КОНСТРУКЦИЯ pQ-SRUS ДЛЯ ПОЛУЧЕНИЯ ШТАММОВ ДРОЖЖЕЙ Yarrowia lipolytica, ОБЛАДАЮЩИХ СПОСОБНОСТЬЮ К ГОМОЛОГИЧНОЙ РЕКОМБИНАЦИИ ГЕНОМА МИТОХОНДРИЙ ЗА СЧЁТ ЭКСПРЕССИИ ГЕНА БЕЛКА RecA БАКТЕРИАЛЬНОГО ПРОИСХОЖДЕНИЯ
Вид РИД
Изобретение
Область техники, к которой относится изобретение:
Изобретение относится к области биоинженерии, в частности к конструированию эукариотических организмов с уникальной способностью осуществлять рекомбинацию ДНК в митохондриях. Предметом изобретения является генетическая конструкция pQ-SRUS с экспрессируемым геном RecA из Bacillus subtilis. При введении конструкции pQ-SRUS в штаммы Yarrowia lipolytica они становятся пригодными для конструирования рекомбинантных продуцентов целевых белков, накапливающих продукт в митохондриях. Это решение может быть особенно эффективным для тех белков, которые из-за неоптимальной структуры N-конца содержат дегроны, запускающие деградацию белка в протеосомах. Кроме того, в перспективе изобретение может быть использовано для получения препаратов интактного митохондриального генома человека путем введения в митохондрии дрожжей и последующей коррекции путем рекомбинации с искусственно вводимыми ДНК.
Уровень техники:
В настоящее время ни для одного известного биологического вида не описан ферментативный механизм рекомбинации митохондриального генома [1, 2]. Имеются опубликованные данные популяционно-генетических исследований по статистическому анализу последовательностей митохондрий, позволяющие предполагать существование в природе явления рекомбинации генома митохондрий [3, 4, 5]. Однако имеющиеся источники не дают точных данных о механизмах и скорости гомологичной рекомбинации в митохондриях [6]. Известны отдельные белки, предположительно участвующие в этом процессе, например, Mgm101 [7]. Однако до настоящего времени не создано ни одной генетической системы, позволяющей направленно изменять митохондриальный геном какого-либо организма, вводя туда необходимые замены или дополнительные фрагменты [8]. Приведенные данные позволяют утверждать, что в митохондриях отсутствует наиболее распространенный фермент, ответственный за гомологичную рекомбинацию, типа RecA, встречающийся у всех известных прокариот и имеющий аналоги у эукариот. Очищенная до гомогенного состояния рекомбиназа RecA способна осуществлять все химические реакции, необходимые для гомологичной рекомбинации ДНК in vitro [9]. Дополнительные белки могут стимулировать ее активность, но не являются абсолютно необходимыми для протекания реакции. Поэтому было выдвинуто предположение, что введение бактериального белка RecA в митохондрии эукариот, например, дрожжей Yarrowia lipolytica, позволит осуществлять гомологичную рекомбинацию с участием эндогенного генома митохондрий. Решение этой задачи позволяет вводить в геном митохондрий дрожжей Y.lipolytica любые желаемые гены с использованием традиционных технологий на основе гомологичных «плеч» - фрагментов ДНК, идентичных участкам эндогенного генома: схемы с участием одного «плеча», находящегося в составе кольцевой ДНК или линейных фрагментов, фланкированных двумя «плечами». Поскольку гены, имеющиеся в митохондриальном геноме Y.lipolytica, входят в состав одного из двух оперонов, транскрибируемых с двух дивергентно расположенных промоторов, введение дополнительных генов в промежутки между эндогенными генами способно обеспечить устойчивую экспрессию трансгенов на уровне, характерном для собственного генома митохондрий, без использования дополнительных промоторов.
В литературе есть примеры генетических конструкций, используемых для введения бактериальных генов RecA и других бактериальных белков, участвующих в гомологичной рекомбинации, в митохондрии эукариот. В статье Paul R. с соавт. [10] описано введение гена белка RecA из Escherichia coli в культивируемые клетки человека. При этом с целью адресации белка RecA в митохондрии на его N-конец был искусственно введен пептид MTS. В работе [11] аналогичный подход был использован для введения в митохондрии Arabidopsis thaliana белка SSB из Е.coli, связывающего однонитевую ДНК и повышающего эффективность работы RecA. При этом на N-конец белка SSB присоединяли митохондриальный адресный пептид A.thaliana длиной 28 а.о., а на С-конец - зеленый флуоресцентный белок GFP. Продукт наблюдали в митохондриях клеток A.thaliana, подвергнутых транзиторному введению ДНК-конструкции с помощью бомбардировки металлическими микрочастицами. В работе [12] описано введение гена RecA из Mycobacterium tuberculosis в клетки пекарских дрожжей Saccharomyces cerevisiae. Для обеспечения транспортировки его продукта в митохондрии использовался адресный пептид MTS от субъединицы цитохром С оксидазы CoxIVp. Скорость транспорта белка RecA в митохондрии исследовалась с помощью «белкового интрона» - последовательности белка интеина, введенного центр последовательности RecA.
Описанные примеры доказывают возможность введения белка RecA в митохондрии эукариот и его стабильность в этой среде. Однако они не позволяют оценивать эффективность рекомбинации митохондриального генома с участием искусственно введенного белка RecA. В опубликованных источниках нет сведений о проведении подобных экспериментов с клетками дрожжей Y.lipolytica, которые являются перспективным объектом биотехнологии: хорошо культивируются в аэробных условиях, имеют разработанную систему для проведения генно-инженерных манипуляций. Кроме того, ни в одной из приведенных работ не упоминается использование альтернативного принципа адресации белка RecA в митохондрии с использованием специфических некодирующих последовательностей мРНК, имеющих сродство к внешней мембране митохондрий и обеспечивающих контрансляционный транспорт продукта внутрь органеллы. Этот принцип описан в работе [13] применительно к адресации белка АТР6 (компонент дыхательного комплекса V) с использованием некодирующих областей 5′-UTR и 3′-UTP гена митохондриальной железомарганцевой супероксиддисмутазы SOD2. Однако работа [13] выполнена с использованием линии клеток человека HeLa, и на клетках дрожжей, в том числе, Y.lipolytica не воспроизводилась.
Характеризуя наиболее близкие аналоги изобретения, касающиеся разработки систем экспрессии генов в Y.lipolytica, целесообразно указать на действующие в РФ патенты Юзбашевой и соавт. №2451749 [14] и Выборной и соавт. №2451075 [15]. В этих патентах описано получение на основе Y.lipolytica продуцентов липазы и генетической конструкции для экспозиции белка на поверхности клеточной стенки дрожжей. В этих заявках не упоминаются ни митохондрии (какие-либо митохондриальные белки), ни способы адресации белков в митохондрии, ни белок RecA. Таким образом, можно утверждать, что изобретение не затрагивает каких-либо принципов, описываемых в цитируемых патентах.
Раскрытие изобретения
В отличие от всех описанных аналогов в рамках изобретения для создания конструкции pQ-SRUS (SEQ ID NO 1, фиг. 1), предназначенной для введения гена, используется последовательность промотора, терминатора транскрипции, 5′-UTR и 3′-UTR гена SOD2 (железно-марганцевая митохондриальная супероксиддисмутаза - NCBI GenBank Locus tag RP1-56L9.2) штамма CLIB122 Y.lipolytica. Целевым геном, вводимым в клетки Y.lipolytica с помощью конструкции pQ-SRUS, является ген рекомбиназы RecA из Bacillus subtilis, штамм 168 (NCBI GenBank Locus tag CP003329.1).
Введение ДНК конструкции pQ-SRUS в клетки Y.lipolytica PO1f проводится методом трансформации с использованием солей Li+ и отбором трансформантов на минимальной синтетической среде, свободной от урацила. Для проведения трансформации ДНК конструкции pQ-SRUS препаративно выделяют из клеток Е.coli TG1 и линеаризуют с помощью рестриктазы BglI. Полученные штаммы-трансформанты тестируют на наличие способности к гомологичной рекомбинации с участием митохондриального генома.
Для проверки функциональности гена RecA, вводимого в клетки Y.lipolytica PO1f с помощью конструкции pQ-SRUS, используется тестерная конструкция pQ-NIHN, содержащая правое и левое плечи для гомологичной рекомбинации с геном ND1 митохондриального генома Y.lipolytica, ген зеленого флуоресцентного белка EYFP с областью инициации трансляции гена митохондриального ND1, ген устойчивости к гигромицину hph с областью инициации трансляции гена митохондриального ND1. Поддержание конструкции pQ-NIHN в Е.coli осуществляется за счет элементов из состава стандартного вектора pQE30 (Qiagen): репликона плазмиды рМС16 и гена β-лактамазы (детерминанта устойчивости к ампициллину) при условии поддержания соответсвующего рекомбинантного штамма Е.coli на среде, содержащей ампициллин в концентрации 100 мкг/мл.
Введение ДНК конструкции pQ-NIHN в клетки Y.lipolytica PO1f, несущие интегрированную конструкцию pQ-SRUS, проводится методом трансформации с использованием солей Li+ и отбором трансформантов на среде, содержащей 200 мкг/мл гигромицина (G458). Для проведения трансформации ДНК конструкции pQ-NIHN препаративно выделяют из клеток Ε.coli TGI и линеаризуют с помощью рестриктазы BglI. Полученные штаммы-трансформанты тестируют на наличие зеленой флуоресценции митохондрий, обусловленной накоплением в них белка EYFP. Выявление зеленой флуоресценции митохондрий проводится в живой культуре с помощью флуоресцентного микроскопа при длине волны возбуждающего света 450 нм. Для достоверности наблюдений с точки зрения интенсивности фоновой флуоресценции необходимо использовать контрольный родительский штамм Y.lipolytica PO1f, несущий интегрированную конструкцию pQ-SRUS, но не подвергавшийся трансформации тестерной конструкцией pQ-NIHN.
Краткое описание графических изображений
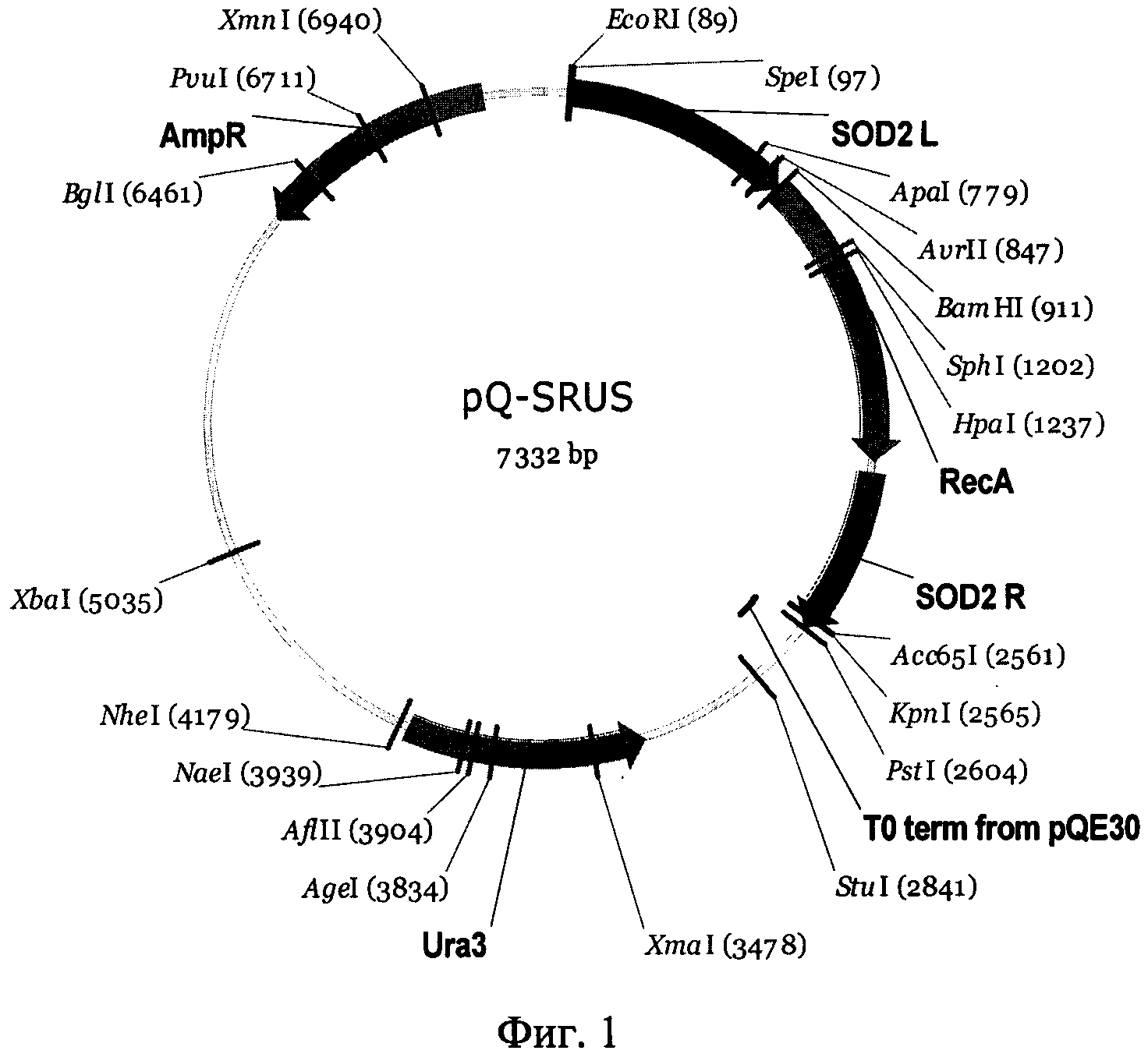
Фиг. 1. Схема функциональных элементов конструкции pQ-SRUS (SEQ ID NO 1), предназначенной для введения в клетки Y.lipolytica белка RecA с последующей адресацией белка в митохондрии за счет последовательностей 5′-UTR и 3′-UTR гена SOD2. Конструкция содержит левое (включая промотор) и правое (включая терминатор) плечи гена SOD2, ген RecA из В.subtilis 168, маркер компенсации ауксотрофности по урацилу URA3. Поддержание конструкции в Е.coli осуществляется за счет элементов из состава стандартного вектора pQE30 (Qiagen): репликона плазмиды рМС16 и гена β-лактамазы (детерминанта устойчивости к ампициллину).
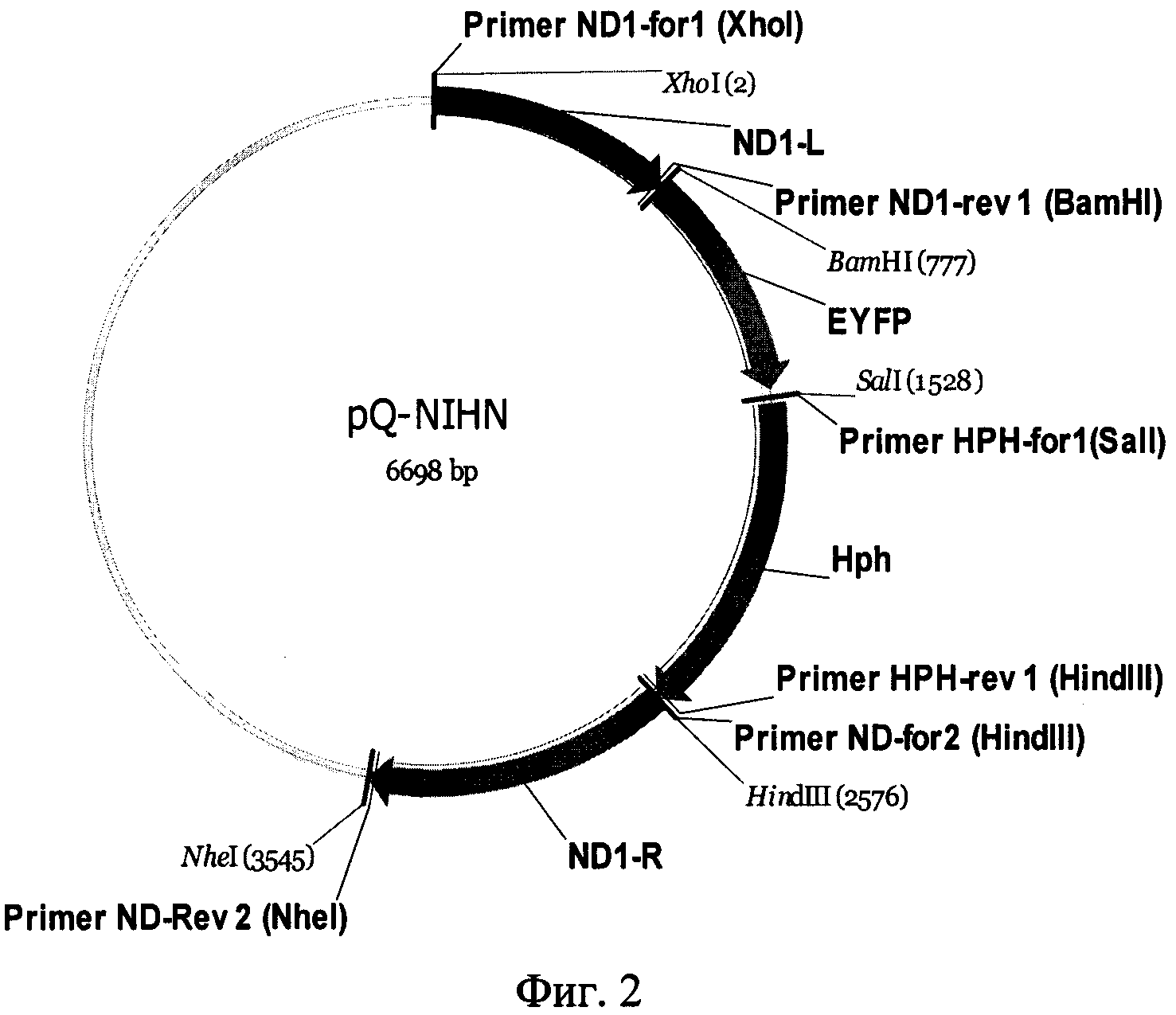
Фиг. 2. Схема функциональных элементов конструкции pQ-NIHN (SEQ ID NO 2), предназначенной для тестирования эффективности работы искусственно введенного в митохондрии Y.lipolytica белка RecA.
Конструкция содержит правое и левое плечи для гомологичной рекомбинации с геном ND1 митохондриального генома, ген зеленого флуоресцентного белка EYFP с областью инициации трансляции гена митохондриального ND1, ген устойчивости к гигромицину hph с областью инициации трансляции гена митохондриального ND1. Поддержание конструкции в Е.coli осуществляется за счет элементов из состава стандартного вектора pQE30 (Qiagen): репликона плазмиды рМС16 и гена β-лактамазы (детерминанта устойчивости к ампициллину).
Осуществление изобретения
1) Фрагмент, кодирующий 5′UTR SOD, амплифицируют с помощью ПЦР на матрице геномной ДНК Y.lipolytica CLIB122 с праймерами SOD2-1 и SOD2-2: размер продукта 840 п.н. Продукт очищают и подвергают рестрикции по сайтам EcoRI и BamHI. Проводят клонирование в вектор pQE-EYFP, линеаризованный по сайтам EcoRI и BamHI. Проводят трансформацию Е.coli TG1, отбирают колонии белого цвета.
2) 3′UTR SOD амплифицируют с помощью ПЦР на матрице геномной ДНК Y.lipolytica CLIB122 с праймерами SOD2-3 и SOD2-4: размер продукта 600 п.н. Продукт очищают и подвергают рестрикции по SacI и SalI. Проводят клонирование в конструкцию, полученную на стадии 1 (pQE-SODL-EYFP), линеаризованную по сайтам SacI и SalI.
3) Маркерный ген URA3 экстрагируют из конструкции pUC18-URA3 по сайтам Ncol и SalI и переносят в конструкцию, полученную на стадии 2 (pQE-SODL-EYFP-SODr), линеаризованную по сайтам Ncol и SalI.
4) Ген RecA амплифицируют с помощью ПЦР на матрице геномной ДНК В.subtilis 168 с праймерами RecA1 и RecA2: размер продукта 1050 п.н. Проводят очистку продукта ПЦР и обработку рестриктазами BamHI nSacI. Проводят лигирование очищенного продукта рестрикции с ДНК конструкции pQE-SODL-EYFP-SODr-URA3, обработанной рестриктазами BamHI nSacI. Проводят трансформацию штамма Е.coli TGI по стандартной методике, высевают транформантов на среду LB с ампициллином в концентрации 100 мкг/мл, культивируют в течение 12-16 ч при 37°С, отбирают колонии, содержащие вставку с целевым фрагментом.
5) При проведении генноинженерного конструирования используют олигонуклеотидные ДНК-праймеры следующей структуры:
Праймер SOD2-1 (EcoRI/SpeI) GGGAAttctgactagtgcgaattttc
Праймер SOD2-2 (BamHI) GG GGA TCc cat cea ctt aga ccg gag ca
Праймер SOD2-3 (SacI) GGGAGCTCtaagcccttccgagattacca
Праймер SOD2-4 (SalI) acggtcgactgtatcatggagactcg
Праймер RecA1 (BamHI) GGGGATCCatgagtgatc gteaggeage
Праймер RecA2 (SacI) GGGAGCTCAGCCTTTTGTATCATTTGAA
Список использованных источников
1. Aanen D.K., Spelbrink J.N., Beekman M. What cost mitochondria? The maintenance of functional mitochondrial DNA within and across generations. Philos Trans R Soc Lond В Biol Sci. - 2014. - V. 369(1646): 20130438.
2. Chattopadhyay K., Aldous C. A brief review on human mtDNA mutations and NRTI-associated mtDNA toxicity and mutations. Mitochondrial DNA.-2014. Sept. 11: 1-3. doi:10.3109/19401736.2014.958728.
3. Zbawicka M., Wenne R., Burzyński A. Mitogenomics of recombinant mitochondrial genomes of Baltic Sea Mytilus mussels. Mol Genet Genomics. - 2014. DOI 10.1007/s00438-014-0888-3.
4. Gerhold J.M., Sedman T., Visacka K., Slezakova J., Tomaska L., Nosek J., Sedman J. Replication intermediates of the linear mitochondrial DNA of Candida parapsilosis suggest a common recombination based mechanism for yeast mitochondria. J Biol Chem. - 2014. - V. 289. №33. - P. 22659-70.
5. Salavirta H., Oksanen I., Kuuskeri J., Mäkelä M., Laine Ρ., Paulin L., Lundell T. Mitochondrial genome of Phlebia radiata is the second largest (156 kbp) among fungi and features signs of genome flexibility and recent recombination events. PLoS One. - 2014. - V. 9. - №5. - e97141.
6. Fritsch E.S., Chabbert C.D., Klaus B., Steinmetz L.M. A Genome-wide map of mitochondrial DNA recombination in yeast. Genetics. - 2014. - V. 198. - №2. - P. 755-71.
7. Wang X., Mbantenkhu M., Wierzbicki S., Chen X.J. Preparation of the Mgm101 recombination protein by MBP-based tagging strategy. J Vis Exp. - 2013. - №76. - e50448.
8. Rai J., Pemmasani J.K., Voronovsky A., Jensen I.S., Manavalan A., Nyengaard J.R., Golas M.M., Sander B. Strep-tag II and twin-Strep based cassettes for protein tagging by homologous recombination and characterization of endogenous macromolecular assemblies in Saccharomyces cerevisiae. Mol Biotechnol. - 2014. - V. 56. - №11. P. 992-1003.
9. Liu J., Sneeden J., Heyer W.D. In vitro assays for DNA pairing and recombination-associated DNA synthesis. Methods Mol Biol. - 2011. V. 745. - P. 363-383.
10. Paul R., Dalibart R., Lemoine S., Lestienne P. Expression of E.coli RecA targeted to mitochondria of human cells. Mutat Res. - 2001. V. 486. - №1. - P. 11-9.
11. Edmondson A.C., Song D., Alvarez L.A., Wall M.K., Almond D., McClellan D.A., Maxwell A., Nielsen B.L. Characterization of a mitochondrially targeted single-stranded DNA-binding protein in Arabidopsis thaliana. Mol Genet Genomics. - 2005. - V. 273. - №2. - P. 115-122.
12. Williams L.R., Ellis S.R., Hopper A.K., Davis E.O., Martin N.C. Splicing before import - an intein in a mitochondrially targeted preprotein folds and is catalytically active in the cytoplasm in vivo. FEBS Lett. - 2000. - V.476. - №3. - P. 301-305.
13. Kaltimbacher V., Bonnet С., Lecoeuvre G., Forster V., Sahel J.A., Corral-Debrinski M. mRNA localization to the mitochondrial surface allows the efficient translocation inside the organelle of a nuclear recoded ATP6 protein. RNA. - 2006. - V. 12. - №7. - P. 1408-17.
14. Юзбашева Ε.Ю., Юзбашев Т.В., Лаптев И.Α., Ларина А.С., Синеокий С.П. Генетическая конструкция для экспозиции белка на поверхности клеточной стенки дрожжей Yarrowia lipolytica. Патент РФ на изобретение №2451749.
15. Выборная Т.В., Юзбашев Т.В., Соболевская Т.И., Лаптев И.Α., Юзбашева Е.Ю., Синеокий С.П. Рекомбинантный штамм дрожжей Yarrowia lipolytica - продуцент липазы. Патент РФ на изобретение №2451075.
Интегративная генетическая конструкция pQ-SRUS, характеризующаяся нуклеотидной последовательностью SEQ ID NO 1, предназначенная для введения в хромосому Yarrowia lipolytica гена RecA из Bacillus subtilis с его последующей транскрипцией под контролем промотора гена SOD2 и адресацией мРНК в митохондрии за счет последовательностей 5′-UTR и 3′-UTR гена SOD2 и обеспечивающая возможность интеграции в митохондриальный геном конструкций по принципу гомологичной рекомбинации.