МЕСТНЫЙ ГЛАЗНОЙ ПЕПТИДНЫЙ СОСТАВ
Вид РИД
Изобретение
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение принадлежит к области медицины и, в частности, относится к фармацевтическому составу в форме местной глазной композиции соматостатина и аналогов соматостатина.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Заболевания сетчатки и стекловидного тела являются основными причинами слепоты, и среди них выделяются диабетическая ретинопатия и возрастная макулярная дегенерация.
Несмотря на наличие ссылок в известном уровне техники на возможное применение соматостатина и аналогов при лечении заболеваний заднего сегмента глаза, основанное на данных о сверхэкспрессии соматостатиновых рецепторов при этих расстройствах, не существует явных примеров терапевтического эффекта.
Недавно описали присутствие эндогенного соматостатина и соматостатиновых рецепторов в разных частях человеческого глаза. Таким образом, например, соматостатиновые рецепторы sstr1, sstr2 и sstr5 обнаружили в слезных железах, конъюнктиве, роговице и носослезных протоках [Minsel et al., Endocrinology, 2009, 150 (5): 2254-2263]. В заднем сегменте глаза описали присутствие генов, соответствующих соматостатиновым рецепторам sstr1, sstr2, sstr3, sstr4 и sstr5 в сетчатке, цилиарном теле и собственно сосудистой оболочке глаза глаз здоровых людей [Klisovic et al., Investigative Ophthalmology & Visual Science, 2001, 42 (10): 2193-2201], присутствие мРНК sstr2 и sstr3 в сетчатке [van Hagen et al., European Journal Endocrinology, 2000, 143: S43-S51; Cervia et al., Molecular and Cellular Endocrinology, 2008, 286: 112-122] и также присутствие эндогенного соматостатина в стекловидном теле и сетчатке [Simo et al., Diabetes Care, 2002, 25 (12): 2282-2286]. В уровне техники также известно, что пониженная экспрессия соматостатина в сетчатке в первой фазе диабетической ретинопатии возможно связана с нейродегенерацией сетчатки [Carrasco et al., Diabetes Care, 2007, 30 (11): 1-7].
Существуют различные пути введения лекарственных средств для лечения заболеваний заднего сегмента глаза, такие как системное, местное, внутриглазное и окологлазное введение.
Документ WO 02/09739 А1 описывает применение соматостатина или его аналога для лечения или предупреждения зрительных расстройств. Среди путей введения, названных в этом документе, предпочтительным путем является системное парентеральное введение, подкожное или внутримышечное, и в указанном документе нет указания на состав в форме глазных капель для введения соматостатина или его аналога. Однако в случае системного введения трудно достигнуть терапевтических концентраций в заднем сегменте глаза из-за гематоретинального барьера, который ограничивает проникновение лекарственного препарата в глаз. Другим основным недостатком системного введения является то, что его эффект не является местным и не направлен исключительно на задний сегмент глаза. Кроме того, в случае соматостатина будут необходимы высокие дозы, вследствие его нестабильности в крови. В случае аналога октреотида различные клинические исследования оценили его эффекты при системном подкожном введении, даже если результаты не показывают явного терапевтического эффекта [Wegewitz et al., Current Pharmaceutical Design, 2005, 11: 2311-2330; Palii et al., Investigative Ophthalmology & Visual Science, 2008, 49 (11): 5094-5102].
Альтернативой низкой доступности системного пути введения в задний сегмент глаза является местное введение в задний сегмент глаза посредством внутриглазных инъекций и периокулярных инъекций, таких как субконъюнктивальная инъекция, субтеноновая и ретробульбарная инъекции или субконъюнктивальные имплантаты в этот сегмент [Geroski et al., Investigative Ophthalmology & Visual Science, 2000, 41 (5): 961-964; Kiagiadaki et al. Investigative Ophthalmology & Visual Science, 2008, 49 (7): 3080-3089]. Однако эти формы введения являются неудобными для пациента и дают вторичные эффекты, чья частота возрастает, если их выполняют многократно. Кроме того, в случае имплантатов они влекут за собой оперативное вмешательство. Хотя эти типы лечения, как было показано в доклинических исследованиях, являются эффективными, они требуют систематического применения инъекций, которые в некоторых случаях обладают вторичными эффектами, такими как отслоение сетчатки, катаракты, покраснение или эндофтальмит [Geroski et al., Investigative Ophthalmology & Visual Science, 2000, 41 (5): 961-964; Herrero-Vanrell et al, Journal of Drug Delivery Science and Technology, 2007, 17 (1): 11-17; Robertson etal., Journal of Ocular Pharmacology and Therapeutics, 1997, 13 (2): 171-177].
Другой альтернативой предыдущим путям введения лекарственных средств в глаз является местное глазное введение. Однако местное введение в глазной канал в качестве пути введения лекарственного препарата, мишень которого находится в заднем сегменте глаза, до сих пор ограничивалось вследствие оценки, что процент активного вещества, способного достигнуть заднего сегмента, является незначительным в большинстве случаев. [Andres-Guerrero et al., Archivos de la Sociedad Espanola de Oftalmologia, 2008, 83: 683-686].
В известном уровне техники были упомянуты некоторые варианты местного глазного введения соматостатина и аналогов. Таким образом, например, документ US 2005/074497 А1 описывает гидрогель, который содержит антиангиогенное лекарственное средство, такое как октреотид, для лечения заболеваний заднего сегмента глаза. Октреотид раскрыт в данной заявке на патент в рамках обширного перечня лекарственных средств. Кроме того, ни один пример октреотида или любого другого лекарственного средства не описан в этом документе. Гидрогель размещают в контакте с глазом с применением контактной линзы или, альтернативно, прикрепляют к глазу с применением клейких веществ или путем оперативного вмешательства. Введение при помощи глазных капель является явно исключенным в этом документе. Однако введение с применением контактной линзы влечет за собой риск инфицирования глаза патогенами и, дополнительно, оно не переносится пациентами с повышенным внутриглазным давлением.
Другой возможностью является местное введение в форме мази или притирания на внутреннюю часть века. Однако мази, как правило, являются неудобными и снижают остроту зрения вследствие их избыточной вязкости и медленной абсорбции.
Документ WO 99/24019 А1 также описывает сухой твердый состав, изготовленный из различных лекарственных средств, в их числе соматостатин, который восстанавливают в жидком растворе и вводят в виде глазных капель. Хотя этот документ не обеспечивает какого-либо примера состава соматостатина или указания одного обозначения, что это или другое лекарственное средство достигает заднего сегмента глаза при применении с помощью глазных капель.
С другой стороны, документ US 5182258 А описывает состав в форме глазных капель, которые через носослезную систему применяют для системного введения, где вводимым активным компонентом, среди многих других, может являться соматостатин. Однако в этом документе ничего не сказано о введении этого или другого активного компонента для лечения заболеваний заднего сегмента глаза. То же самое имеет место для других составов в известном уровне техники, где октреотид вводят местным путем без указания возможного применения для лечения и/или предупреждения заболеваний заднего сегмента глаза [Danesi et al., Clinical Cancer Research, 1997, 3: 265-272; Demiretal. Documenta Ophthalmologica, 2003, 107: 87-92].
Таким образом, в известном уровне техники существует потребность найти форму местного глазного введения соматостатина или его аналога для местного лечения и/или предупреждения заболеваний заднего сегмента глаза, что одновременно решает как проблемы удобства для пациента, так и низкой терапевтической доступности в фармацевтически приемлемом составе.
Целью настоящего изобретения является местная глазная композиция, жидкий фармацевтический состав, который вводят местно в глаз, соматостатина или его аналога, который достигает заднего сегмента глаза, соединяется с присутствующими там соматостатиновыми рецепторами и который применяют для лечения и/или предупреждения заболеваний заднего сегмента глаза, которая оказывает благоприятное действие от связывания соматостатина или его аналогов с соматостатиновыми рецепторами. Настоящее изобретение предоставляет беспрецедентный прорыв в местном глазном введении пептидов и особенно соматостатина или его аналогов.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Неожиданно, настоящее изобретение решает ранее описанные проблемы. В первом аспекте настоящее изобретение относится к местной глазной композиции, которая содержит пептид, отличающаяся тем, что терапевтически эффективное количество данного пептида достигает заднего сегмента глаза. В конкретном варианте осуществления местную глазную композицию выбирают из группы глазных капель, мазей и притираний. В дополнительном аспекте настоящее изобретение относится к глазным каплям, которые содержат пептид, отличающимся тем, что терапевтически эффективное количество данного пептида достигает заднего сегмента глаза.
В контексте настоящего изобретения выражение "глазные капли" относится к фармацевтическому жидкому составу, который вводят в форме капель на наружную поверхность глаза и который обладает местным действием на задний сегмент глаза.
В контексте настоящего изобретения выражение "задний сегмент глаза" включает собственно сосудистую оболочку глаза, пигментный эпителий сетчатки, сетчатку, пятно, ямку, зрительный нерв и стекловидное тело.
В конкретном варианте осуществления пептид выбирают из соматостатина или аналога соматостатина, предпочтительно соматостатин или аналог соматостатина выбирают из группы, образованной соматостатином-28, соматостатином-14, соматостатином-13, просоматостатином, октреотидом, ланреотидом, вапреотидом, пасиреотидом, сеглитидом, кортистатином и их фармацевтически приемлемыми солями.
В другом конкретном варианте осуществления соматостатин или аналог соматостатина является замещенным ацильной группой или полиэтиленгликолевым фрагментом. Предпочтительно, ацильные группы выбирают из групп, состоящих из ацетила, трет-бутаноила, гексаноила, 2-метилгексаноила, циклогексанкарбоксила, октаноила, деканоила, лауроила, миристоила, пальмитоила, стеароила, олеоила и линолеоила. Предпочтительно, полиэтиленгликолевый фрагмент имеет молекулярную массу от 200 до 35000 дальтон.
В другом конкретном варианте осуществления концентрация пептида, предпочтительно соматостатина или аналога соматостатина, составляет от 0,1 мкг/мл до 100 мг/мл, предпочтительно, от 1 мкг/мл до 10 мг/мл, более предпочтительно от 10 мкг/мл до 1 мг/мл.
В другом конкретном варианте осуществления рН глазных капель составляет от 3 до 8, предпочтительно от 4 до 7. Чтобы довести рН глазных капель, будут добавлены кислоты и/или щелочи, известные специалисту в данной области техники, до достижения указанного ранее значения рН.
В другом конкретном варианте осуществления среда для глазных капель по настоящему изобретению представляет собой изотонический водный раствор, такой как изотонический раствор хлорида натрия или борной кислоты, или представляет собой водный раствор поли(винилового спирта), или их смеси.
В другом конкретном варианте осуществления пептид композиции по настоящему изобретению также может быть включен в липосомы, смешанные липосомы, ниосомы, этосомы, наночастицы, твердые липидные наночастицы, наноструктурные липидные носители, мицеллы, смешанные мицеллы поверхностно-активных веществ, смешанные мицеллы поверхностно-активное вещество-фосфолипид, наносферы, липосферы и нанокапсулы.
В другом конкретном варианте осуществления глазные капли по настоящему изобретению могут факультативно содержать консервант. тСпециалист в данной области техники узнает консервирующие средства известного уровня техники, такие как хлорид бензалкония, бензойная кислота, алкилпарабены, алкилбензоаты, хлорбутанол, хлоркрезол, цетиловые спирты, жирные спирты, такие как гексадециловые спирты, металлоорганические соединения ртути, такие как ацетат, нитрат или борат фенилртути, диазолидинилмочевина, диизопропиладипат, диметилполисилоксан, соли EDTA, витамин Е и его смеси.
В другом конкретном варианте осуществления глазные капли по настоящему изобретению могут факультативно содержать средство, которое повышает проникающую способность пептида, предпочтительно пептида соматостатина или аналога соматостатина, в задний сегмент глаза. Предпочтительно средство, которое повышает проникающую способность, выбирают из группы, образованной хлоридом бензалкония, сапонинами, жирными кислотами, эфирами полиоксиэтилена и жирных кислот, алкиловыми сложными эфирами жирных кислот, пирролидонами, поливинилпирролидоном, пировиноградными кислотами, пироглютаминовыми кислотами и их смесями, среди прочих.
Во втором аспекте настоящее изобретение относится к глазным каплям по настоящему изобретению для лечения и/или предупреждения заболеваний заднего сегмента глаза. Предпочтительно, лечение и/или предупреждение заболеваний заднего сегмента глаза оказывает благоприятное воздействие от связывания соматостатина или его аналогов с соматостатиновыми рецепторами. Более предпочтительно, заболевание заднего сегмента глаза выбирают из группы, образованной непролиферативной диабетической ретинопатией, пролиферативной диабетической ретинопатией, возрастной макулярной дегенерацией, заболеванием, связанным с неоваскуляризацией сетчатки, вызванной ишемией ретинопатией, ретинопатией недоношенных, серповидно-клеточной ретинопатией, окклюзией вены сетчатки, пигментным ретинитом, неоваскуляризацией собственно сосудистой оболочки глаза, увеитом, макулярным отеком, цистоидным макулярным отеком. В случае соматостатина его большая стабильность в стекловидном теле заднего сегмента глаза в отношении времени его периода полувыведения из сыворотки благоприятствует его действию на местном уровне для лечения и/или предупреждения ранее упомянутых заболеваний заднего сегмента глаза.
В третьем аспекте настоящее изобретение относится к способу лечения и/или предупреждения заболеваний заднего сегмента глаза, который включает местное введение терапевтически эффективного количества пептида при помощи местной глазной композиции, выбранной из группы, состоящей из глазных капель, мазей и притираний.
В конкретном варианте осуществления пептид выбирают из соматостатина или аналога соматостатина, предпочтительно соматостатин или аналог соматостатина выбирают из группы, образованной соматостатином-28, соматостатином-14, соматостатином-13, просоматостатином, октреотидом, ланреотидом, вапреотидом, пасиреотидом, сеглитидом, кортистатином и их фармацевтически приемлемыми солями.
В другом конкретном варианте осуществления частота введения может в значительной степени варьировать в зависимости от потребностей каждого субъекта и тяжести заболевания, которое нужно лечить или предупредить, с рекомендацией диапазона введения от одного раза в неделю до десяти раз в сутки, предпочтительно от трех раз в неделю до трех раз в сутки, еще более предпочтительно один раз или два раза в сутки.
В другом конкретном варианте осуществления способ лечения и/или предупреждения дополнительно включает введение другого терапевтического средства для лечения и/или предупреждения заболеваний заднего сегмента глаза. Терапевтические средства для лечения и/или предупреждения заболеваний заднего сегмента глаза представляют собой, например, и в неограничивающем смысле, такие средства, выбранные из группы средств, противодействующих фактору роста эндотелия сосудов (VEGF), аналогов простагландина, антагонистов бета-адренергических рецепторов, альфа-2 адренергических агонистов, ингибиторов карбоангидразы, миотических средств, моноклональных антител, кортикостероидов, глюкокортикоидов, ингибиторов киназ, циклоплегиков или антиметаболитов. Введение данных терапевтических средств для лечения и/или предупреждения заболеваний заднего сегмента глаза может осуществляться местно, пероральным или парентеральным путем. В контексте настоящего изобретения выражение "парентеральное" включает интравитреальные, внутриглазные, внутрироговичные, подкожные, внутрикожные, внутрисосудистые инъекции, такие как внутривенные, внутримышечные и любые другие подобные методики инъекции или инфузии.
Следующие конкретные примеры, приведенные в данном документе, служат для иллюстрации основных свойств настоящего изобретения. Эти примеры включены исключительно с иллюстративными целями и не должны интерпретироваться как ограничения настоящего изобретения, заявленного в данном документе.
ОПИСАНИЕ ЧЕРТЕЖЕЙ
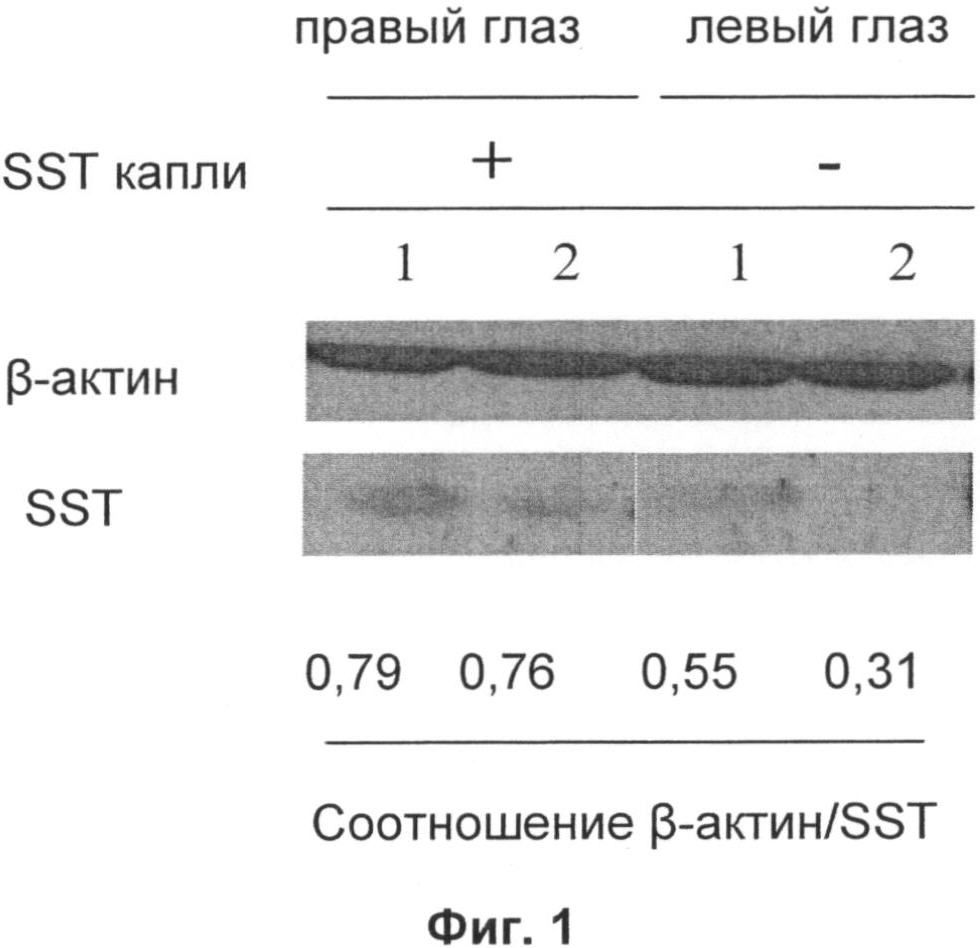
Фигура 1: На Фигуре 1 показаны сетчатки 2 мышей (1 и 2), которые получали соматостатин в правый глаз (+) и плацебо в левый глаз (-).
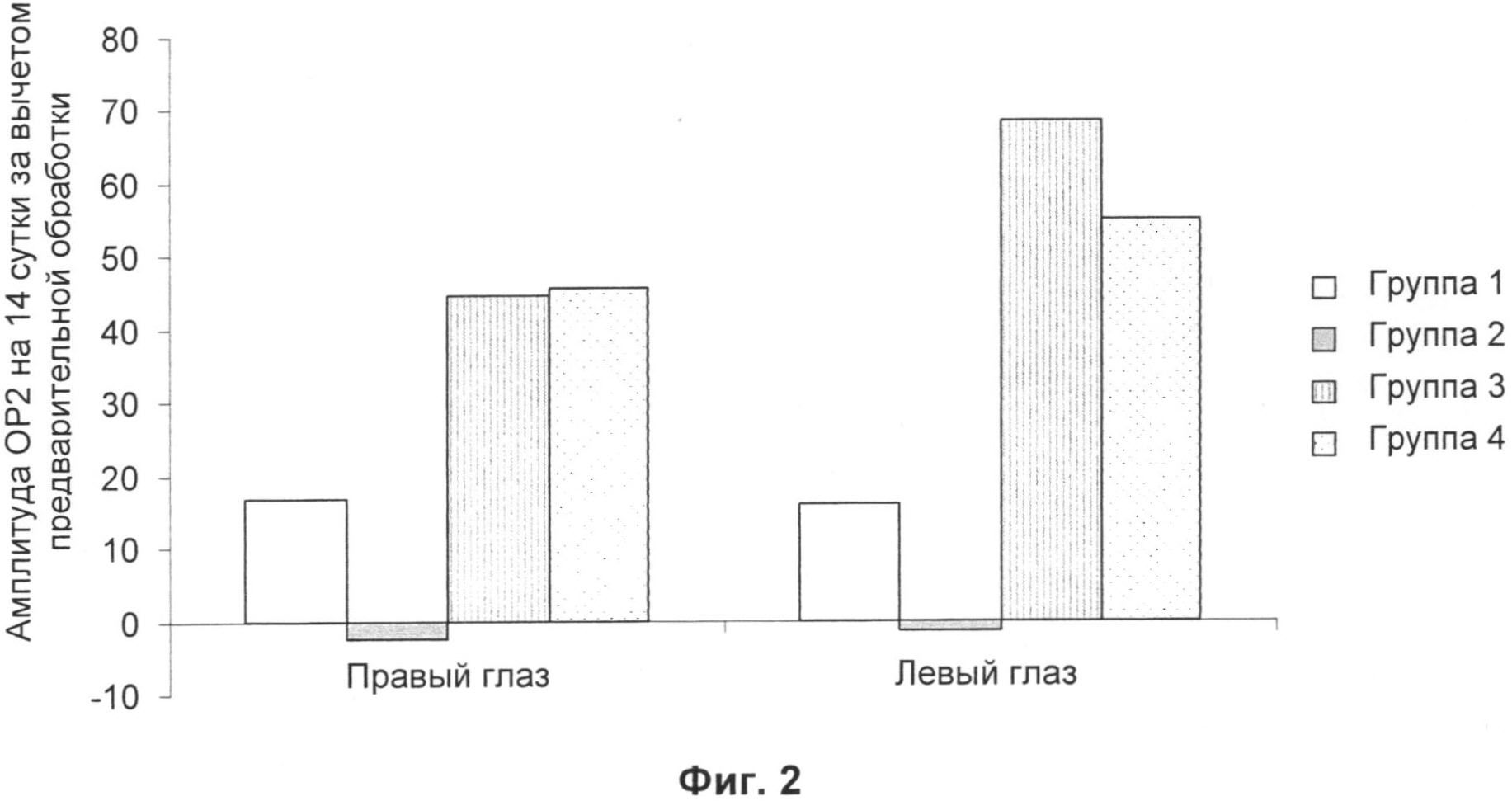
Фигура 2: На Фигуре 2 показано различие между амплитудой второго ОР у крыс контроля (Группа 1); больных диабетом крыс (Группа 2); больных диабетом крыс, подвергнутых обработке соматостатином, (Группа 3) и больных диабетом крыс, подвергнутых обработке октреотидом, (Группа 4).
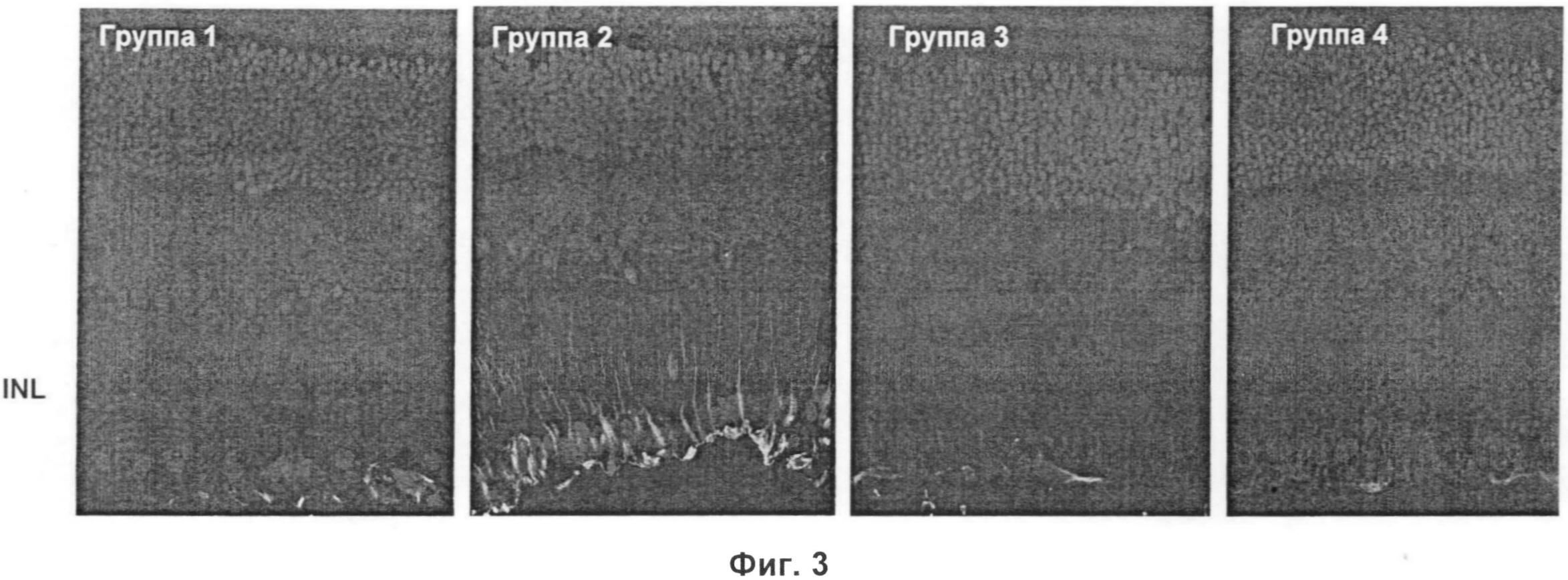
Фигура 3: На Фигуре 3 показаны изображения конфокальной микроскопии. Иммуногистохимическое исследование GFAP при увеличении 40Х на конфокальном микроскопе. Намного более высокую экспрессию GFAP (наиболее яркое мечение) наблюдали в слое ганглиозных клеток крыс с вызванным STZ диабетом, (Группа 2). Обработка соматостатином (Группа 3) или октреотидом (Группа 4) предупреждала активацию глиальных клеток, что коррелировало с уровнем GFAP, подобным таковому контроля (Группа 1).
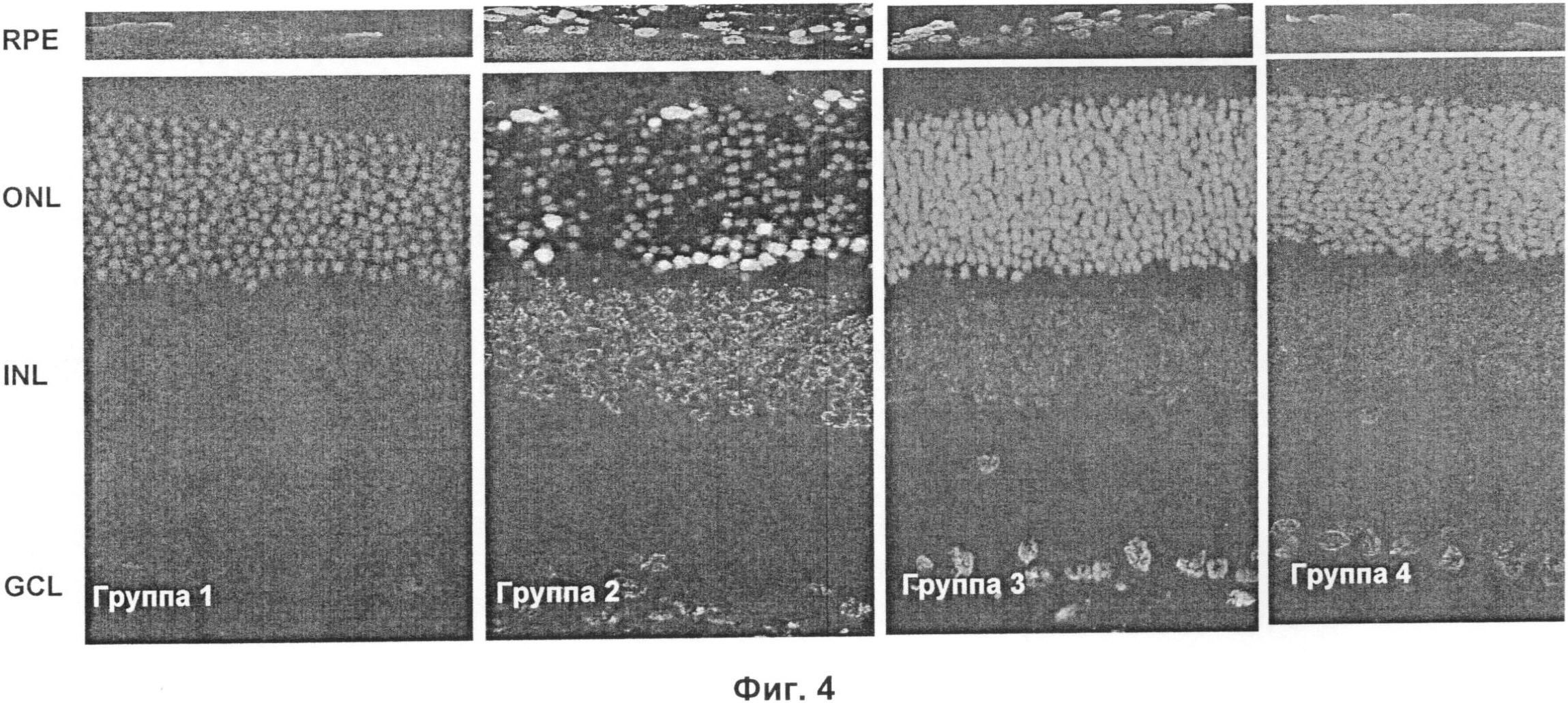
Фигура 4: На Фигуре 4 показаны изображения конфокальной микроскопии. Изображения, полученные в результате применения TUNEL анализа при увеличении 40Х на конфокальном микроскопе. Дегенерацию сетчатки, коррелировавшую с большей численностью апоптических клеток (наиболее яркое мечение означает TUNEL-положительный), особенно в ONL, наблюдали у крыс с вызванным STZ диабетом (Группа 2). Обработка соматостатином (Группа 3) и октреотидом (Группа 4) предупреждала дегенерацию сетчатки и показывала количество клеток, подобное обнаруженному у здоровых крыс контроля (Группа 1).
ПРИМЕРЫ
Пример 1: Глазные капли, которые содержат соматостатин-14.
Фармацевтическую композицию соматостатина приготовили в форме глазных капель путем добавления 125 мкл 0,9% хлорида натрия к 5 мг соматостатина-14.
Пример 2: Оценка концентрации местного глазного соматостатина в сетчатке.
Использовали мышей C57B L/6 восьминедельного возраста. Обращение и уход за животными осуществляли согласно протоколу Institut de Recerca del Hospital Universitari Vail d'Hebron и международным указаниям Европейского Экономического Сообщества и A.R.V.O. (Ассоциация по исследованию зрения и вопросов офтальмологии) (приказ 86/609/СЕЕ). Животных содержали в отдельных клетках в помещениях для животных при контролируемой температуре (20°С) и влажности (60%) при постоянных циклах свет-темнота, которые продолжались 12 часов, и животные имели свободный доступ к корму и воде. Глазные капли соматостатина-14 из примера 1 (1 капля 5 мкл) вводили в правый глаз и плацебо (солевой раствор) - в левый глаз. Вводили две капли в сутки, одну утром и другую вечером, в течение 5 суток. Животных подвергли эвтаназии путем смещения шейных позвонков под воздействием анестезирующего средства через 2 часа после последнего дозирования. Немедленно после этого глазные яблоки извлекли и заморозили при -80°С до обработки. Задний сегмент (сетчатку и стекловидное тело) отделяли от остального глазного яблока рассечением его под увеличительным стеклом. Количество соматостатина-14 в сетчатке определяли вестерн-блоттингом. Белки экстрагировали раствором 50 мМ Трис-HCl, рН 7,9, 300 мМ KCl, 1,5 мМ MgCl2, 0,1% Nonidet Р-40 и 20% глицерина, который содержал коктейль ингибиторов протеаз Complete™, при 4°С в течение 12 часов. В дальнейшем образцы центрифугировали (12000 оборотов в минуту при 4°С) в течение 10 минут. Осуществляли вестерн-блоттинг белков с кроличьими антителами к соматостатину-14 (аb53165, abeam). Для стандартизации концентрации соматостатина-14 полученный β-актин использовали в качестве контроля. Комплексы специфичное антитело-антиген идентифицировали с помощью козьих антител к IgG кролика, меченных HRP, или кроличьих антител к IgG козы вместе с хемилюминесцентными субстратами (Pierce Biotechnology Inc., Рокфорт, Иллинойс, США) путем экспозиции на пленках для авторадиографии. Осуществляли денситометрический анализ (денситометр GS-800. Bio-Rad Laboratories, Геркулес, Калифорния, США), и результаты выражены в относительных единицах. На Фигуре 1 показаны сетчатки 2 мышей (1 и 2), которые получали соматостатин в правый глаз (+) и плацебо в левый глаз (-). Как можно видеть, количество соматостатина было большим в подвергнутом лечению глазе обоих животных. У контрольных мышей, которые получали плацебо в оба глаза, не обнаружили различий в концентрации соматостатина между обоими глазами.
Пример 3: Стабильность соматостатина в стекловидном теле человека и сыворотке человека.
Соматостатин инкубировали с сывороткой человека или стекловидным телом человека при относительной влажности 90% при 37°С. Аликвоты экстрагировали при различном времени инкубации. Ацетонитрил добавляли для осаждения белков сыворотки, ее центрифугировали, и надосадочную жидкость фильтровали и впрыскивали в RP-HPLC (Градиент: 20-80% В за 30 мин, В=0,07% TFA в ацетонитриле). Исчезновение начального продукта анализировали с применением области, соответствующей начальному продукту, и рассчитывали время периода полувыведения. Время периода полувыведения соматостатина составляет 2,7 часов в сыворотке и 64 часа в стекловидном теле.
Пример 4: Глазные капли, которые содержат соматостатин-14.
Фармацевтическую композицию соматостатина приготовили в форме глазных капель путем добавления 1 мл 0,9% водного раствора хлорида натрия к 10 мг соматостатина-14. В конце раствор фильтровали через 0,22 мкм стерилизующий фильтр.
Пример 5: Глазные капли, которые содержат октреотид.
Фармацевтическую композицию октреотида приготовили в форме глазных капель путем добавления 1 мл 0,9% водного раствора хлорида натрия к 10 мг октреотида. В конце раствор фильтровали через 0,22 мкм стерилизующий фильтр.
Пример 6: Глазные капли, которые содержат вапреотид.
Фармацевтическую композицию вапреотида приготовили в форме глазных капель путем добавления 1 мл 0,9% водного раствора хлорида натрия к 10 мг вапреотида. В конце раствор фильтровали через 0,22 мкм стерилизующий фильтр.
Пример 7: Глазные капли, которые содержат кортистатин. Фармацевтическую композицию кортистатина приготовили в форме глазных капель путем добавления 1 мл 0,9% водного раствора хлорида натрия к 10 мг кортистатина. В конце раствор фильтровали через 0,22 мкм стерилизующий фильтр.
Пример 8: Глазные капли, которые содержат соматостатин-14.
Фармацевтическую композицию соматостатина приготовили в форме глазных капель путем добавления 1 мл 0,9% хлорида натрия и 1,4% водного раствора поливинилового спирта) к 0,27 мг соматостатина-14. В конце раствор фильтровали через 0,22 мкм стерилизующий фильтр.
Пример 9: Глазные капли, которые содержат соматостатин-28.
Фармацевтическую композицию соматостатина приготовили в форме глазных капель путем добавления 1 мл 0,9% водного раствора хлорида натрия к 0,05 мг соматостатина-28. В конце раствор фильтровали через 0,22 мкм стерилизующий фильтр.
Пример 10: Глазные капли, которые содержат соматостатин-14, гидроксибензоаты и эфиры полиоксиэтилена и жирных кислот.
Фармацевтическую композицию соматостатина приготовили в форме глазных капель путем добавления 1 мл 0,9% водного раствора хлорида натрия к 50 мкг метил 4-гидроксибензоата, 100 мкг пропил 4-гидроксибензоата, 50 мкг стеарилового эфира полиоксиэтилена-20 (Brij-78) и 1 мг соматостатина-14. В конце раствор фильтровали через 0,22 мкм стерилизующий фильтр.
Пример 11: Глазные капли, которые содержат липосомы соматостатина-14. - Фармацевтическую композицию соматостатина приготовили в 0,9% растворе хлорида натрия, содержащем 20 мг фосфатидилхолина и 2,7 мг соматостатина-14 на мл. Вкратце, фосфатидилхолин медленно добавляли при перемешивании к 0,9% водному раствору хлорида натрия, содержащему соматостатин-14. Композицию дополнительно перемешивали в течение 15 минут до образования суспензии липосом. Затем липосомы поэтапно продавливали через поликарбонатный фильтр с размером пор 400 нм, фильтр с размером пор 200 нм и, в конечном счете, десять раз через фильтр с размером пор 100 нм. В конце раствор липосом фильтровали через 0,22 мкм стерилизующий фильтр.
Пример 12: Глазные капли, которые содержат нанокапсулы соматостатина-14.
Приготовили 10% раствор сополимера молочной и гликолевой кислоты (50:50) молекулярной массой 5000, 1 г, в дихлорметане. Соматостатин-14 (100 мг) растворили в 1 мл воды. Раствор соматостатина добавили к раствору полимера и эмульгировали с применением одного ультразвукового зонда. Затем наноэмульсию фильтровали через 0,22 мкм стерилизующий фильтр. Полученную в результате наноэмульсию затем диспергировали в 1% водном растворе поли(винилового спирта) с применением ультразвукового зонда для уменьшения размера частиц до получения наноэмульсии. Нанокапсулы экстрагировали в 40% водном растворе этанола и их очищали ультрафильтрацией в тангенциальном потоке.
В конце 70 мг нанокапсул, содержащих соматостатин (16 мг), диспергировали в 100 мл 1,4% водного раствора поли)винилового спирта).
Пример 13: Гпазные мази, которые содержат соматостатин-14.
Фармацевтическую композицию соматостатина приготовили в форме глазной мази путем добавления 50 мл белого вазелина по USP (Фармакопея США) к 200 мг соматостатина-14.
Пример 14: Эффект местной глазной обработки соматостатином и октреотидом для предупреждения нейродегенерации сетчатки у больных диабетом крыс.
Стрептозотоцин (STZ), 60 мг/кг, вводили крысам линии Спраг-Доули. Животных разделили на четыре группы, как подробно описано в Таблице 1:
|
Таблица 1: План исследования
Через двое суток после введения STZ животных подвергали обработке ежесуточно одной или двумя каплями среды (Группа 2), глазными каплями из примера 4 (Группа 3) или глазными каплями из примера 5 (Группа 4) в течение дополнительных 14 суток. Здоровых животных контроля подвергали обработке только одной или двумя каплями среды ежесуточно (Группа 1).
Электроретинография представляет собой методику, применяемую клинически для оценки функции сетчатки при диабетической ретинопатии. Несколько параметров могут быть нарушены на ранних стадиях заболевания: латентность, амплитуда и осцилляторные потенциалы [Tzekov et al., Survey of Ophthalmology, 1999, 44 (1): 53-60]. Приращение латентности и уменьшение амплитуды осцилляторных потенциалов (ОР) также наблюдали у крыс с вызванным стрептозотоцином диабетом [Напсок et al., Investigative Ophthalmology & Visual Science, 2004, 45 (3): 1002-1008].
Результаты электроретинографии показывали, что через 14 суток обработки латентность b-волны при 0 дБ значительно возросла по сравнению с предварительной обработкой в группе больных диабетом (Группа 2) (15,5 правый глаз; 15,2 левый глаз) и не претерпела значительного повышения в группе контроля (Группа 1) (-2,3 правый глаз; -7,5 левый глаз) и группах, подвергнутых обработке композицией соматостатина из примера 4 (Группа 3) (9,0 правый глаз; 4,9 левый глаз) или композицией октреотида из примера 5 (Группа 4) (8,8 правый глаз; 1,1 левый глаз).
Что касается амплитуды, соматостатин предупреждал уменьшение амплитуды b-волны при -30 дБ, -10 дБ и 0 дБ по сравнению с группой больных диабетом, и октреотид предупреждал уменьшение амплитуды b-волны при -30 дБ, но был эффективным только при наивысшей дозе при -10 дБ и 0 дБ.
Анализ осцилляторных потенциалов (ОР) b-волны при 0 дБ показывает, что соматостатин и октреотид представляют положительный эффект, предупреждая уменьшение амплитуды второго OP (ОР2). Данный эффект наблюдали уже на 8 сутки, и он сохранялся вплоть до 14 суток. На Фигуре 2 показано различие между амплитудой второго ОР у крыс контроля (Группа 1: 17,0 правый глаз; 15,9 левый глаз); больных диабетом крыс (Группа 2: -2,5 правый глаз; -1,2 левый глаз); больных диабетом крыс, подвергнутых обработке соматостатином, (Группа 3: 44,8 правый глаз; 68,7 левый глаз) и больных диабетом крыс, подвергнутых обработке октреотидом, (Группа 4: 45,5 правый глаз; 55,1 левый глаз).
На 14 сутки животных умерщвляли и глазные ткани заливали парафином. Глиальную активацию и количество апоптических клеток оценивали как маркеры первого этапа при развитии диабетической ретинопатии: нейродегенерации сетчатки [Carrasco etal., Diabetes Care, 2007, 30 (11): 1-7].
Глиальную активацию определяли посредством анализа иммунофлуоресценции глиального фибриллярного белка (GFAP) с помощью конфокальной микроскопии. Глазные срезы толщиной 7 мкм фиксировали на высокоадгезивных покровных стеклах (Visionbiosystems, Ньюкасл-апон-Тайн, Великобритания). Их депарафинировали, регидратировали и отмывали в фосфатно-солевом буфере (PBS). Неспецифические связывания блокировали путем инкубирования образцов в течение 1 часа в PBS с 1% BSA (бычий сывороточный альбумин), 0,5% Triton Х-100. После этого первичные кроличьи антитела к GFAP человека (Sigma, Мадрид, Испания), разведенные в блокирующем буфере (1:100), инкубировали в течение 36 часов при 4°С. После трех отмывок PBS в течение 5 минут срезы инкубировали с вторичными антителами к IgG человека, меченными Alexa Fluor® 488 (Invitrogen, Юджин, Орегон), в течение 1 часа при комнатной температуре. Меченые срезы отмывали и помещали в флуоресцентную среду, содержащую 4,6-диамидин-2-фенилиндол (DAPI) для окрашивания ядер клеток (Vector Laboratories, Берлингейм, Калифорния). GFAP-положительные срезы регистрировали конфокальным микроскопом (FV1000, Olympus, Гамбург, Германия) с получением оптических срезов при помощи 488 нм лазера для Alexa 488 и 405 нм лазера для DAPI. Флуоресценцию GFAP флуоресценцию количественно определяли на каждом изображении при помощи программного обеспечения Fluoview ASW 1.4 (Olympus, Гамбург, Германия). Результаты нормализовали к анализируемой области (21705,33 мкм). На Фигуре 3 показаны изображения конфокальной микроскопии. Более высокую экспрессию GFAP (наиболее яркое мечение) наблюдали в слое ганглиозных клеток крыс с вызванным STZ диабетом (Группа 2). Обработка соматостатином (Группа 3) или октреотидом (Группа 4) предупреждала активацию глиальных клеток, что коррелировало с уровнями GFAP, подобными таковому в контроле (Группа 1).
Эффективность местного глазной обработки соматостатином (Группа 3) и октреотидом (Группа 4) при предупреждении глиальной активации, спровоцированной диабетом, определяли по значениям флуоресценции GFAP, показателю глиальной активации. Значения флуоресценции GFAP составляли 2095±26 для здоровых животных контроля группы 1; 6871±159 для группы 2; 2514±90 для группы 3 и 1696±48 для группы 4.
Определение степени апоптоза сетчатки после 14 суток обработки выполняли с применением методики TUNEL ("ник-концевое мечение dUTP концевой трансферазой"). Использовали набор In Situ Cell Death Detection Kit (Roche Diagnostics, Мангейм, Германия). Глазные срезы депарафинировали, регидратировали и отмывали в PBS. Три конфокальные изображения (40Х), соответствующие поверхности 317,13 мкм X 317,13 мкм, получали для каждого среза. Общее количество ядер и TUNEL-положительных ядер количественно определяли с помощью программного обеспечения Image J (http://rsbweb.nih.gov/ij). Окрашивание пропидиум йодидом (PI) выполняли для изучения морфологии ядра и выбраковки ложноположительных результатов. На Фигуре 4 показаны изображения конфокальной микроскопии. Дегенерацию сетчатки, коррелировавшую с более высоким количеством апоптических клеток (наиболее яркое мечение означает TUNEL-положительный), наблюдали у крыс с вызванным стрептозотоцином диабетом (Группа 2). Обработка соматостатином (Группа 3) и октреотидом (Группа 4) предупреждала дегенерацию сетчатки и показывала количество клеток, подобное обнаруженному у здоровых крыс контроля (Группа 1).
В Таблице 2 показан процент апоптических клеток по отношению к общему количеству клеток в различных слоях сетчатки, таких как пигментный эпителий сетчатки (RPE), наружный ядерный слой (ONL), внутренний ядерный слой (INL) и слой ганглиозных клеток (GCL). Возрастание процента апоптических клеток является значимым у больных диабетом крыс (Группа 2). Местная глазная обработка соматостатином (Группа 3) или октреотидом (Группа 4) снижала количество апоптических клеток до уровня контроля (Группа 1).
|
Таблица 2: Процент апоптических клеток
Нейродегенерация клеток сетчатки является одним из первых этапов в развитии диабетической ретинопатии. Результаты электроретинографии, глиальная активация и апоптоз указывают на то, что местное глазное введение соматостатина или октреотида в течение 14 суток предупреждало дегенерацию сетчатки у крыс с вызванным стрептозотоцином диабетом.