Результат интеллектуальной деятельности: СПОСОБ ПЛАСТИКИ ОБЩЕГО ПЕЧЕНОЧНО-ЖЕЛЧНОГО ПРОТОКА ТОНКОКИШЕЧНЫМ АУТОТРАНСПЛАНТАТОМ ПЕРЕМЕННОГО ДИАМЕТРА
Вид РИД
Изобретение
Изобретение относится к медицине, а именно к хирургии, и может быть использовано для хирургического лечения заболеваний и повреждений внепеченочных желчных путей.
Проблема восстановления желчеоттока из печени в кишечник при доброкачественных и злокачественных поражениях внепеченочных желчных протоков продолжает оставаться актуальной. Несмотря на то что большинство хирургов используют для этого наложение гепатикоеюноанастомоза на отключенной по Ру петле кишки, по мнению многих авторов (Э.И. Гальперин и соавт., 2003, А.А. Шалимов и соавт., 1993, N. Hashimoto et al., 2005, H.P. Heistermann et al., 2006, B. Jablonska, 2012), наиболее физиологичным вмешательством является использование восстановительных и реконструктивных операций с организацией поступления желчи в двенадцатиперстную кишку.
Однако подавляющее большинство предложенных вариантов пластического замещения внепеченочных желчных протоков не отвечают всем требованиям, предъявляемым к трансплантату желчных путей, а именно трансплантат должен иметь полноценную слизистую оболочку, индифферентную к постоянному воздействию желчи; он должен перистальтировать, тем самым направлять ток желчи в ДПК и препятствовать рефлюксу дуоденального содержимого в желчное дерево. И, наконец, по длине и диаметру трансплантат должен быть близким к размерам общего желчного и печеночного протока
Наибольшие сложности для использования пластических операций представляют случаи высоких стриктур, когда анастомоз приходится накладывать глубоко в воротах печени, а часто для анастомоза имеются не один, а два и более долевых печеночных протоков.
Накопленный в нашей клинике опыт по использованию наиболее распространенных в настоящее время желчеотводящих анастомозов, с выключенной по Ру петлей тонкой кишки, не только нефизиологичен, но и не лишен таких недостатков, как несостоятельность соустья, его быстрое рубцевание, если применяются традиционные технологии его формирования, не предусматривающие прецизионную технику шва и использование специального шовного материала. Кроме того, среди недостатков гепатико-энтероанастомоза следует отметить рефлюкс кишечного содержимого в желчные протоки даже при достаточно длинной отключенной по Ру петле кишки и, как результат, высокую частоту развития холангита и постепенное рубцевание анастомоза.
Таким образом, разработка новых способов пластики внепеченочных желчных протоков является актуальной задачей хирургии.
В качестве аналогов взяты следующие способы оперативного лечения:
1. Гепатикоеюностомия по А.А. Шалимову (Шалимов Α.Α., Шалимов С.А., Ничитайло М.Е., Доманский Б.В. "Хирургия печени и желчевыводящих путей", Киев, "Здоровья", 1993, стр. 473-475).
После иссечения рубцовых тканей и освобождения дистального конца общего печеночного протока производят его мобилизацию в проксимальном направлении. Петлю тощей кишки, необходимую для анастомоза, выключают по Ру или Шалимову, подводят к задней поверхности протока так, чтобы последний ложился поперек кишки по длине всей своей свободной части. При малом диаметре протока (5 мм и менее) по задней поверхности его делают продольный разрез длиной 5-8 мм. Непосредственно перед культей протока продольно вскрывают просвет тощей кишки в соответствии с диаметром протока и разрезом его. Отдельными 3-4 швами с интервалом между ними 1,5 мм нитью из нерассасывающейся ткани фиксируют боковые стенки протока к стенке кишки поперек нее. Также отдельными швами нитью из рассасывающегося материала на атравматической игле сшивают края протока и кишки при точном сопоставлении слизистых оболочек. Затем серо-серозными швами анастомоз инвагинируют в складку кишки для уменьшения регургитационного рефлюкса из кишечника.
Недостатком операции является то, что двенадцатиперстную кишку выключают из пассажа желчи, что существенно влияет на качество пищеварения.
2. Способ пластики внепеченочных желчных протоков пупочной аутовеной, предварительно подготовленной в среде 199, предложенный О.М. Горбуновым (Горбунов О.М., Сахно Р.Д. Клиническая оценка способа аутовенозной пластики внепеченочных желчных протоков // Вестник хирургии, 1994. - Т. 152. - №3-4. - С. 55-60).
Под местной анестезией иссекают сегмент большой подкожной вены длиной 6 см, который погружают в стерильную колбу с поддерживающей питательной средой 199, которую помещают в холодильник с температурой +3°C на 7 суток.
По истечении этого срока выполняют лапаротомию, выделяют дистальный и проксимальный концы желчных протоков. Осуществляют пластику дефекта подготовленным аутовенозным сегментом на дренаже-каркасе из полиэтиленовой трубки диаметром 0,6 см. Проксимальный конец ее вводят в один из долевых протоков, дистальный проводят транспапиллярно в двенадцатиперстную кишку. Аутопластику выполняют сшиванием концов консервированной аутовены с концами - проксимальным и дистальным - гепатикохоледоха супрамидной нитью 6/0 на атравматической игле узловыми матрацными швами.
Недостатки:
- необходимо предварительно готовить аутовену для трансплантации в специальной среде;
невозможно добиться полноценной эпителизации венозного трансплантата, таким образом, всегда остается опасность ее рубцевания;
- стенка аутовены, замещаясь рубцом, не способна перистальтировать и, следовательно, активно участвовать в поступательном продвижении желчи в двенадцатиперстную кишку, препятствовать рефлюксу дуоденального содержимого.
В качестве ближайшего аналога взят способ пластики гепатикохоледоха трубчатым тонкокишечным трансплантатом (Патент РФ №2249434. Оноприев В.И., Марков П.В. Способ пластики гепатикохоледоха трубчатым тонкокишечным трансплантатом, заявка №2003125035, заявлено 11.08.2003; опубл. 10.04.05, Бюл. №10).
Выбирают петлю тонкой кишки на расстоянии 40-60 см от связки трейца. Учитывая архитектонику сосудов брыжейки, соответственно предполагаемым границам пересечения кишки рассекают брюшинные листки брыжейки тонкой кишки, перевязывают и пересекают сосуды аркад с сохранением магистрального кровоснабжения. По выбранным границам пересекают кишку так, чтобы получить изолированный участок длиной 8-10 см.
Строго по противобрыжеечному краю выкроенного сегмента тонкой кишки продольно иссекают участок кишечной стенки, оставляя лоскуты шириной 0,5 см от краев брыжейки. При сильном кровотечении из сосудов подслизистого слоя их лигируют. Свободные края кишечной стенки сшивают между собой однорядными серозно-мышечно-подслизистыми узловыми швами монофиламентной нитью. Таким образом формируют тонкую (внешним диаметром до 1 см) трубочку из кишки на участке брыжейки. Сквозь аутотрансплантат проводят тонкую перфорированную на всем протяжении дренажную трубочку такой длины, чтобы она выступала из концов трансплантата на 2-3 см.
В правой части брыжейки поперечно-ободочной кишки в бессосудистой зоне проделывают окно. Через него в подпеченочное пространство перемещают подготовленный трансплантат, который укладывают изоперистальтически по отношению к току желчи от ворот печени вдоль печеночно-двенадцатиперстной связки и далее вдоль нисходящей ветви двенадцатиперстной кишки.
Между концом общего печеночного протока и концом трансплантата накладывают прецизионный однорядный анастомоз узловыми швами рассасывающимся синтетическим шовным материалом 5/0-6/0.
Далее приступают к формированию анастомоза с двенадцатиперстной кишкой. При этом трансплантат располагают вдоль нисходящей ветви двенадцатиперстной кишки. Анастомоз формируют на границе ее средней и нижней трети. Формируют прецизионный однорядный анастомоз узловыми серозно-мышечно-подслизистыми швами рассасывающимся монофиламентным синтетическим шовным материалом 6/0 узлами наружу.
Недостатки:
- способ неприменим при наличии широкого просвета общего печеночного протока для анастомозирования или при наличии двух и более долевых печеночных протоков из-за несовместимости диаметров сшиваемых органов.
Задачи: обеспечить беспрепятственный пассаж желчи в двенадцатиперстную кишку с использованием трубчатого тонкокишечного аутотрансплантата, при этом иметь возможность наложения прецизионного анастомоза высоко в воротах печени между широким просветом общего печеночного протока или отдельными долевыми печеночными протоками и трубчатым тонкокишечным трансплантатом.
Сущность заключается в том, что создают аутотрансплантат переменного диаметра: проксимальная его часть длиной 2-4 см состоит из всей окружности кишки, а далее путем резекции стенки кишки по противобрыжеечному краю на протяжении 1-2 см диаметр постепенно сужается до 1 см и сохраняет цилиндрическую форму на протяжении 6-8 см, причем проксимальный конец трансплантата ушивают наглухо и формируют анастомоз между общим печеночным протоком или долевыми печеночными протоками и трансплантатом типа «конец в бок».
Технический результат.
Использование способа позволяет добиться восстановления желчеоттока по физиологическому пути в двенадцатиперстную кишку, что благотворно сказывается на процессе пищеварения и его регуляции. Наличие у трансплантата проксимального конца во всю ширину тонкой кишки делает возможным применить данный вид пластического замещения внепеченочных желчных протоков при высоких стриктурах во всех случаях, когда возможно сформировать прецизионный анастомоз между кишкой и протоками, но в отличие от традиционной гепатикоеюностомии на петле по Ру - восстановить пассаж желчи непосредственно в двенадцатиперстную кишку. Наличие у трансплантата полноценной стенки со слизистой оболочкой и перистальтирующим мышечным слоем препятствует возникновению сужения создаваемых прецизионных соустий и позволяет добиться поступательного продвижения желчи в кишечник, препятствуя попаданию кишечного содержимого в желчное дерево. Таким образом, применение методики приводит к надежному выздоровлению больных, возвращая их к полноценной жизни и труду.
Способ осуществляют следующим образом.
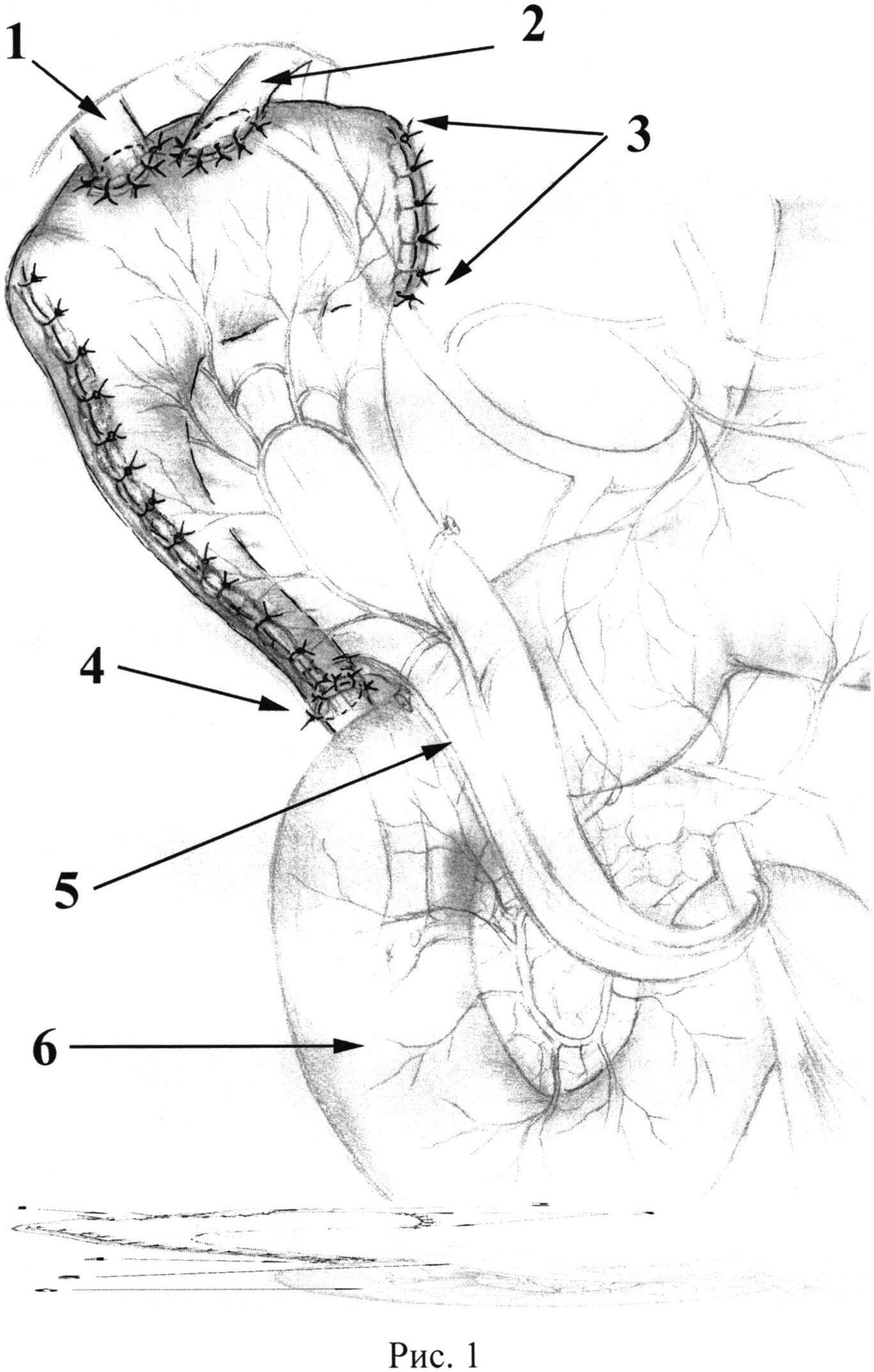
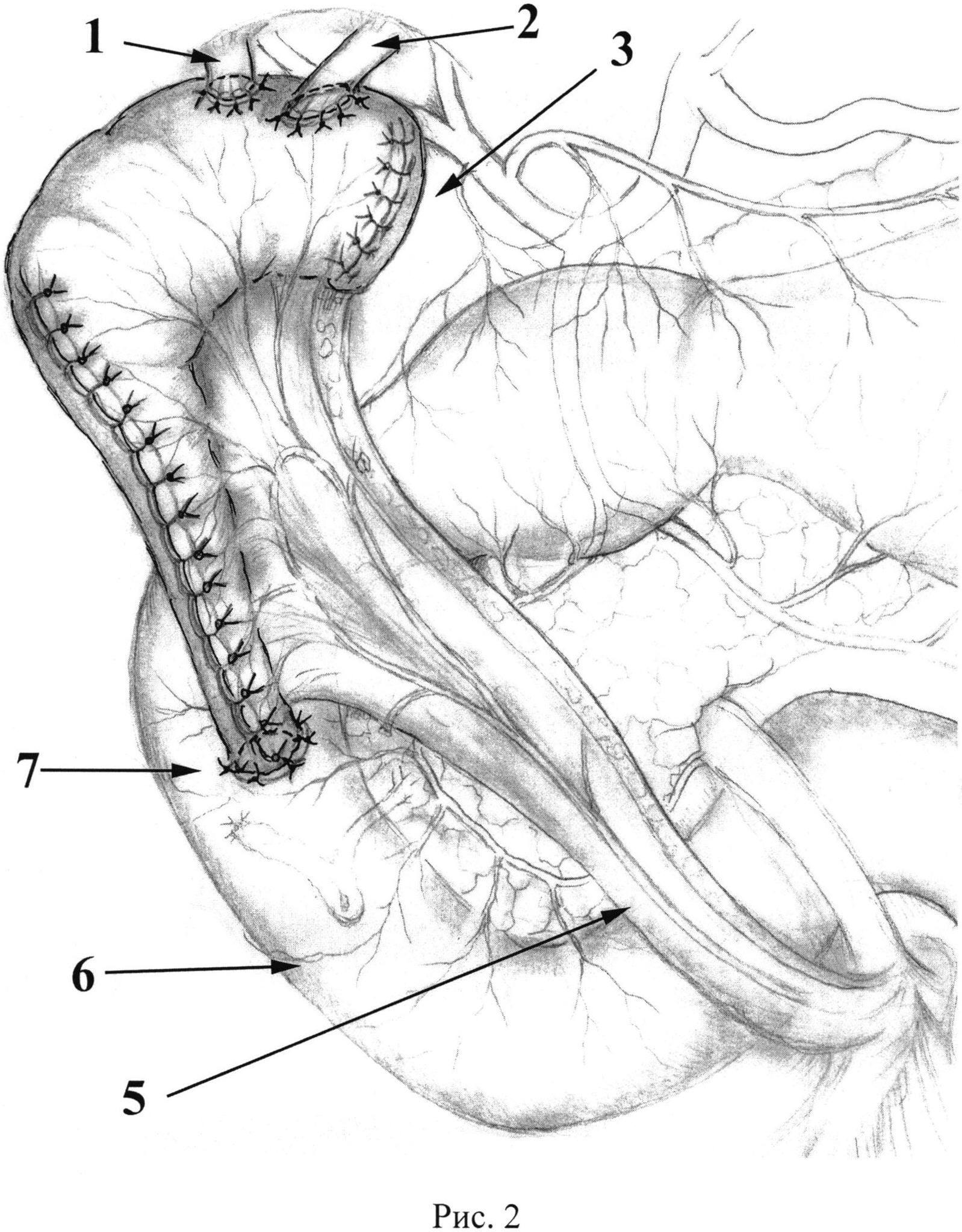
Для наглядности способ иллюстрирован на рисунках 1-2: 1. Вариант пластики внепеченочных желчных протоков тонкокишечным аутотрансплантатом переменного диаметра с включением в пассаж желчи дистальной части холедоха; 2. Вариант пластики внепеченочных желчных протоков тонкокишечным аутотрансплантатом переменного диаметра с дистальным трансплантато-доденоанастомозом, на которых:
1 - правый долевой печеночный проток;
2 - левый долевой печеночный проток;
3 - заглушенный широкий конец тонкокишечного аутотрансплантата;
4 - анастомоз между тонкокишечным аутотрансплантатом и концом общего желчного протока;
5 - брыжейка аутотрансплантата;
6 - вертикальная ветвь двенадцатиперстной кишки;
7 - анастомоз между тонкокишечным аутотрансплантатом и двенадцатиперстной кишкой.
После подготовки конца общего печеночного протока или концов долевых печеночных протоков (1, 2) приступают к формированию трансплантата из тонкой кишки.
Выбирают петлю тонкой кишки на расстоянии 40-60 см от связки трейца. Учитывая архитектонику сосудов брыжейки, соответственно предполагаемым границам пересечения кишки рассекают брюшинные листки брыжейки тонкой кишки, перевязывают и пересекают сосуды аркад с сохранением магистрального кровоснабжения. По выбранным границам пересекают кишку так, чтобы получить изолированный участок на сосудистой ножке (5) длиной 8-10 см. Непрерывность тонкой кишки восстанавливают прецизионным анастомозом «конец в конец» однорядным серозно-мышечно-подслизистым швом мононитью.
Проксимальную часть выкроенного сегмента тонкой кишки длиной 2-4 см оставляют из всей окружности кишки, а далее, путем резекции стенки кишки по противобрыжеечному краю, на протяжении 1-2 см постепенно сужают до внешнего диаметра 1 см и сохраняют цилиндрическую форму на протяжении 6-8 см. При сильном кровотечении из сосудов подслизистого слоя их лигируют. Свободные края кишечной стенки сшивают между собой однорядными серозно-мышечно-подслизистыми узловыми швами либо непрерывным швом монофиламентной нитью. Проксимальный широкий конец аутотрансплантата (3) ушивают наглухо либо узловыми, либо непрерывным прецизионным однорядным серозно-мышечно-подслизистым швом. Таким образом, формируют аутотрансплантат переменного диаметра с проксимальным концом во всю ширину кишки, а далее с внешним диаметром до 1 см.
В правой части брыжейки поперечно-ободочной кишки в бессосудистой зоне проделывают окно. Через него в подпеченочное пространство перемещают подготовленный аутотрансплантат, который укладывают изоперистальтически по отношению к току желчи (широким концом) от ворот печени вдоль печеночно-двенадцатиперстной связки и далее вдоль нисходящей ветви двенадцатиперстной кишки (6).
По противобрыжеечному краю широкой части трансплантата проделывают отверстие, по диаметру соответствующее общему печеночному протоку, либо несколько отверстий соответственно количеству и месту расположения долевых печеночных протоков.
Сквозь аутотрансплантат проводят тонкую перфорированную на всем протяжении дренажную трубочку такой длины, чтобы она выступала из концов трансплантата на 2-3 см. Дренаж необходим в ближайшем послеоперационном периоде для беспрепятственного тока желчи на время стихания воспалительной реакции в зонах анастомозов и в целом в трансплантате.
Накладывают прецизионный анастомоз между общим печеночным протоком или долевыми протоками (1, 2) и аутотрансплантатом однорядными узловыми швами рассасывающимся синтетическим шовным материалом 5/0-6/0, используя при необходимости увеличение. При этом шов на кишке серозно-мышечно-подслизистый, на конце протока - с минимальным захватом слизистой оболочки для полноценного сопоставления подслизистых слоев.
Через анастомоз в правый или левый долевые протоки продвигают конец «скрытого» дренажа.
Далее приступают к формированию анастомоза между концом аутотрансплантата и концом общего желчного протока (4). Используют однорядный узловой прецизионный серозно-мышечно-подслизистый шов монофиламентной синтетической рассасывающейся нитью 5/0-6/0 (Рис. 1). Конец «скрытого» дренажа проводят через анастомоз и далее через большой дуоденальный сосочек в двенадцатиперстную кишку.
При невозможности использовать для анастомоза конец общего желчного протока конец аутотрансплантата соединяют с двенадцатиперстной кишкой. При этом аутотрансплантат располагают вдоль нисходящей ветви двенадцатиперстной кишки. Анастомоз (7) формируют на границе ее средней и нижней трети. Отверстие в стенке двенадцатиперстной кишки проделывают следующим образом: серозную оболочку рассекают на протяжении не более 5 мм, а слизистую вскрывают проколом, т.к. отверстие в стенке кишки легко растяжимо и позволяет сформировать хороший анастомоз, просвет которого будет в последующем легко смыкаться. Формируют прецизионный однорядный анастомоз узловыми серозно-мышечно-подслизистыми швами рассасывающимся монофиламентным синтетическим шовным материалом 5/0-6/0 узлами наружу (Рис. 2). При этом конец «скрытого» дренажа пропускают в просвет двенадцатиперстной кишки.
Дренируют подпеченочное, а при необходимости и поддиафрагмальное пространство двухпросветными дренажами.
Примеры.
Пациент Б., 21 год. Поступил с полной стриктурой в воротах печени и полным наружным желчным свищем, сформировавшимися в результате ятрогенного повреждения протоков во время лапароскопической холецистэктомии и последующего наложения чрескожной чреспеченочной холангиостомы под ультразвуковым контролем.
05.09.2011 г. был оперирован. Под общим обезболиванием с ИВЛ выполнена расширенная верхнесрединная лапаротомия с аппаратной коррекцией доступа ранорасширителем Сигала.
Интраоперационное исследование: в подпеченочном пространстве - умеренный спаечный процесс. Пересечена круглая связка печени, серповидная связка. Разделены сращения в подпеченочном пространстве. Желчный пузырь удален. Из сращений выделена гепатодуоденальная связка и взята на держалку. Имеются эндоклипсы, лежащие на медиальной части ложа желчного пузыря, на пузырной артерии, а также одна из клипс лежит в области ворот печени в верхней трети общего печеночного протока параллельно ему, в этом месте имеется полная стриктура протока. После препарирования элементов гепатодуоденальной связки дистальный отдел холедоха представлен тонким тяжем, дальнейшее его выделение решено не проводить. Удалена клипса со стенки протока, выяснено, что рубцами поражена бифуркация общего печеночного протока. После иссечения всех рубцов имеются отдельно правый печеночный проток (диаметром 8 мм) и левый печеночный проток (диаметр после рассечения вдоль передней стенки 10 мм), площадка между ними 1,5 см. Решено выполнить отдельное анастомозирование каждого протока.
На расстоянии 40 см от трейца изолирован сегмент тонкой кишки длиной 10 см на участке брыжейки. Путем продольной резекции противобрыжеечного края и сшивания свободных краев кишечной стенки непрерывным швом сформирован трубчатый трансплантат переменного диаметра: в проксимальной части - на всю ширину тонкой кишки на протяжении 4 см, а далее на протяжении 1,5 см диаметр аутотрансплантата постепенно сузили до 1 см и создали цилиндрическую трубочку протяженностью 5 см. Аутотрансплантат был проведен в подпеченочное пространство через окно в мезоколон. Проксимальный конец трансплантата заглушен однорядным узловым швом. Сформированы отдельные анастомозы между правым и левым долевыми протоками и боковой стенкой широкой части аутотрансплантата. Транспеченочный дренаж, стоящий через правый долевой проток, заменен на тонкую силиконовую трубочку и проведен через весь аутотрансплантат. Мобилизована вертикальная ветвь ДПК и ее нижний изгиб. Трансплантат уложен вдоль гепатодуоденальной связки и вертиклаьной ветви ДПК. Сформирован прецизионный однорядный трансплантато-дуоденоанастомоз на уровне нижнего изгиба ДПК.
В нижнем этаже брюшной полости непрерывность тонкой кишки восстановлена однорядным непрерывным анастомозом конец в конец. Ушиты окна в брыжейках. Участком большого сальника выполнена оментизация подпеченочного пространства. Установлены двухпросветные дренажи: в правое поддиафрагмальное, подпеченочное пространство и малый таз. Брюшная стенка ушита послойно наглухо.
Послеоперационный период протекал гладко. Желчеистечение по оставленному чреспеченочному дренажу к 10 суткам уменьшилось с 500 до 200 мл в сутки. Дренаж был перекрыт, и пациент выписан. При контрольном обследовании через 1 месяц жалоб не предъявляет. При выполнении контрольной холангиографии контраст заполняет желчное дерево и свободно проходит через трансплантат в ДПК. При этом имеется отчетливая перистальтика аутотрансплантата. Чреспеченочный дренаж удален. При рентгеноскопическом исследовании пассажа контрастного вещества по ДПК и выполнении провоцирующих проб (напряжение брюшной стенки, положение Тренделенбурга) рефлюкса в аутотрансплантат и желчные протоки не выявлено.
При обследовании через год жалоб нет. Биохимические маркеры холестаза в пределах нормы. Клинические и УЗ-признаки холангита и дуодено-билиарного рефлюкса отсутствуют.
Способ пластики внепеченочных желчных путей тонкокишечным аутотрансплантатом переменного диаметра, включающий использование аутотрансплантата переменного диаметра, сформированного из сегмента тонкой кишки на сосудистой ножке, отличающийся тем, что создают аутотрансплантат переменного диаметра: проксимальная его часть длиной 2-4 см состоит из всей окружности кишки, а далее путем резекции стенки кишки по противобрыжеечному краю на протяжении 1-2 см диаметр постепенно сужается до 1 см и сохраняет цилиндрическую форму на протяжении 6-8 см, причем проксимальный конец трансплантата ушивают наглухо и формируют анастомоз между общим печеночным протоком или долевыми печеночными протоками и трансплантатом типа «конец в бок».