Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ ОКИСЛЕННОГО ПРОИЗВОДНОГО ГИАЛУРОНОВОЙ КИСЛОТЫ И СПОСОБ ЕГО МОДИФИКАЦИИ
Вид РИД
Изобретение
Область техники
Данное изобретение относится к новому способу получения производного гиалуроновой кислоты, содержащего альдегидную группу -СН=О вместо первичной гидроксигруппы -СН2-ОН. Окисление может быть выполнено в протонных растворителях с использованием системы 4-замещенный TEMPO (2,2,6,6-тетраметилпиперидинилоксил)/ соокислитель:
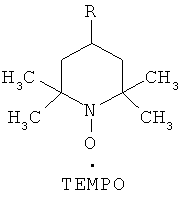
где R - водород или любой заместитель, а в качестве соокислителя используется гипохлорит натрия (NaClO) или трихлоризоциануровая кислота (ТСС).
Уровень техники
Гиалуроновая кислота представляет собой важный полисахарид, состоящий из двух повторяющихся звеньев - β-(1,3)-D-глюкуроновой кислоты и β-(1,4)-N-ацетил-D-глюкозамина. Его молярная масса находится в интервале 5·104-5·106 г-моль-1 в зависимости от исходного материала и от способа выделения продукта. Гиалуроновая кислота или ее натриевая соль - гиалуронан - важный компонент соединительной ткани и синовиальной жидкости суставов; она играет важную роль в таких биологических процессах, как гидратация, организация протеогликанов, а также клеточная дифференциация, пролиферация и ангиогенез. Гиалуроновая кислота - достаточно гидрофильный полисахарид, растворимый в воде в виде солей во всем интервале рН.
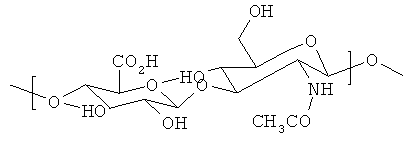
Схема 1. Гиалуроновая кислота
Окисление гиалуроновой кислоты
Окисление полисахаридов - процесс, сопровождающийся изменением степени окисления функциональных групп полисахарида. Как правило, образуются карбоновые кислоты или альдегиды, что может привести к резкому изменению свойств полисахарида. В большинстве случаев в реакции используют реагенты, содержащие атомы в высших степенях окисления.
Окисление проводили согласно способу селективного окисления сахаридов по первичной гидроксильной группе, описанному в работе Angelino, European Journal of Organic Chemistry, 2006, 19, 4323-4326, с помощью системы 2,2,6,6-тетраметил-1-пиперидиноксильного радикала TEMPO и ТСС в ДМФА при температуре 0°С, при этом в качестве основного продукта был получен соответствующий альдегид.
TEMPO - относительно стабильный радикал, который в условиях реакции может существовать в трех окислительно-восстановительных формах. Для окисления спиртов и геминальных диолов эффективна только окисленная форма TEMPO.
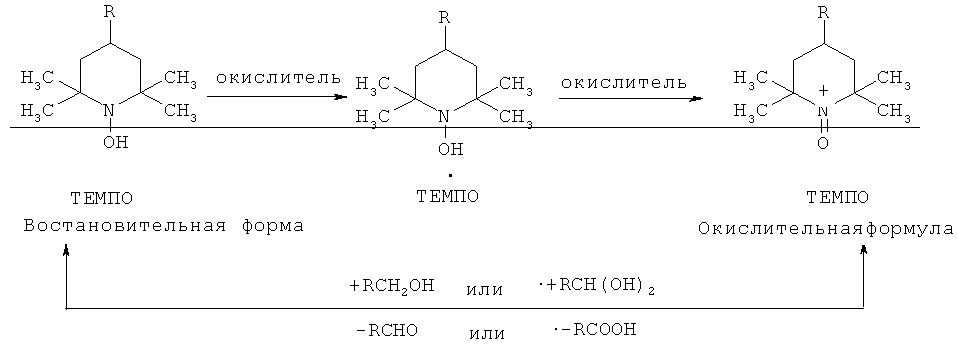 TEMPO вводится в реакционную смесь в каталитических количествах, поэтому необходимо использовать соокислитель, который снова переводит TEMPO в его окисленную форму.
TEMPO вводится в реакционную смесь в каталитических количествах, поэтому необходимо использовать соокислитель, который снова переводит TEMPO в его окисленную форму.
Окисление первичной гидроксигруппы гиалуронана до карбоновой кислоты под воздействием 2,2,6,6-тетраметил-1-пиперидиноксильного радикала (TEMPO) и NaOCl проводили при рН 10,2 и при температуре 0°С (схема 2) (Carbohydr Res 2000, 327 (4), 455-61).
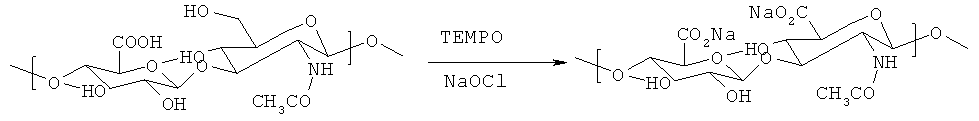
Схема 2. Окисление до карбоновой кислоты
Аналогично другим полисахаридам наблюдались высокая региоселективность и незначительное разложение полимера. При повышении концентрации соли (NaBr, NaCl, Na2SO4) в растворе скорость окисления несколько снижалась.
Окисление гиалуронана под воздействием системы TEMPO/NaClO было описано в патентной заявке WO 02/18448 А2. Авторы также исследовали взаимодействие полностью карбоксилированных полисахаридов при образовании биологических комплексов.
Скорость окисления ГК и других полисахаридов под воздействием периодата натрия исследована в работе Scott et al. (схема 3) (Histochemie 1969, 19 (2), 155-61).
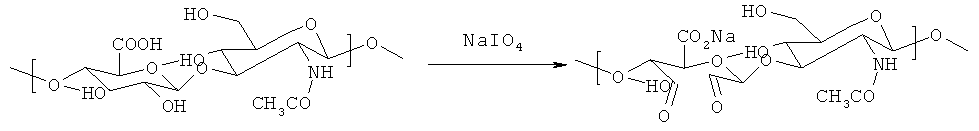
Схема 3. Окисление до диальдегида
Изучалось количественное влияние таких факторов, как длина цепи, природа заместителей, конфигурация полимера и температура. Применение NaIO4 для окисления гиалуронана раскрыто также в патентах № US 6683064 и US 6953784.
Изучены модельные реакции низкомолекулярных аналогов ГК в физиологическом буфере (Carbohydr Res 1999, 321, (3-4), 228-34). Продукты окисления глюкуронового и глюкозаминного фрагментов анализировали методом хромато-масс-спектрометрии. Результаты также позволяют предположить, что окисление идет в основном по глюкуроновому фрагменту, причем в качестве основного продукта образуется мезовинная кислота, которая может служить биомаркером окисления гиалуронана.
Применение окисленной ГК в реакциях сшивки
Применение окисленной ГК для получения сетчатых гидрогелей описано в работе Weng et al. (схема 4), J Biomed Mater Res A 2008, 85 (2), 352-65. В этом случае использовали два прекурсора: частично окисленный гиалуронан и желатин:
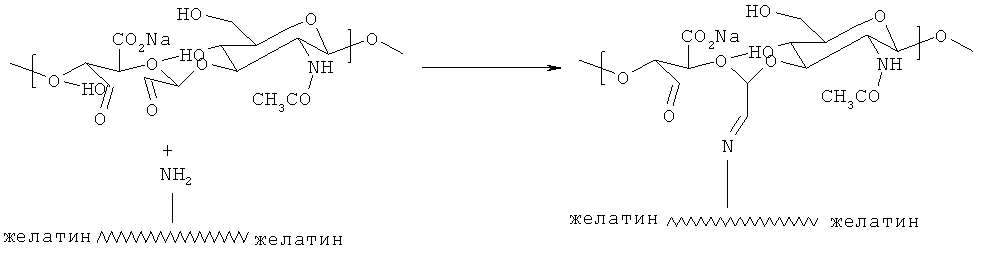
Схема 4. Сшивка окисленного гиалуронана и желатина
Физико-химические свойства полученных гидрогелей исследовали инструментальными методами - Фурье-ИК-спектроскопии, сканирующей электронной микроскопии (СЭМ) и реометрии. При повышении степени замещения в гиалуронане наблюдалось соответствующее увеличение совместимости гидрогелей и снижение водопоглощающей способности. Исследование взаимодействия гидрогеля с клетками проводили с использованием дермальных фибробласт. По данным анализа долгосрочной жизнеспособности клеток, как гидрогели, так и продукты их деградации были биосовместимы. При культивировании с клетками гидрогель разлагался в течение 4 недель с очевидной потерей целостности. Хорошая биосовместимость и биоразлагаемость были далее подтверждены в опытах на мышах при подкожной имплантации. Наконец, депонирование внеклеточного матрикса в гидрогелях in vitro и in vivo было показано методом СЭМ.
Способ получения сшитой ГК из окисленного гиалуронана и желатина методом обратной эмульсии, при котором трехмерный гидрогель получался в отсутствие добавок сшивающего агента, был описан в работе Weng et al., Biomaterials 2008, 29, (31), 4149-56. В указанной публикации методом ВЭЖХ изучали включение модельных лекарственных препаратов в структуру гидрогеля (инкапсулирование) и их высвобождение под воздействием макрофагов.
Получение эластичных гидрогелей сочетанием ГК, окисленной до ГК-альдегида под воздействием периодата натрия, и ГК, модифицированной дигидразидом адипиновой кислоты, было описано в работе Sabiner et al., (схема 5), J. Biomater. Sci. Polym. Ed 2008, 19 (2), 223-43.
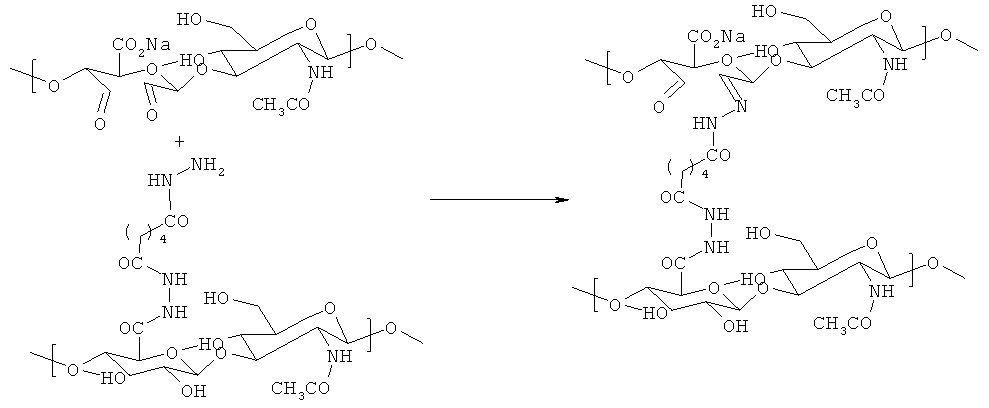
Схема 5. Получение сетчатого гиалуронана
По данным МТТ-теста, полученные производные не оказывали видимого воздействия на пролиферацию культивированных фибробластов.
Раскрытие изобретения
Настоящее изобретение относится к усовершенствованию способа селективного окисления первичной гидроксигруппы гиалуроновой кислоты в положении 6 глюкозаминного фрагмента полисахарида до альдегидной группы. Эта новая реакция проводится с использованием системы 2,2,6,6-тктраметил-1-пиперидинилоксильный радикал TEMPO / соокислитель. В ранее опубликованных методах вводилась либо альдегидная группа в положения 2 и 3 глюкуронового фрагмента гиалуронана с раскрытием сахаридного цикла (схема 6, структура 2), либо карбоксильная группа в положение 6 глюкозаминного фрагмента гиалуронана (схема 6, структура 1).
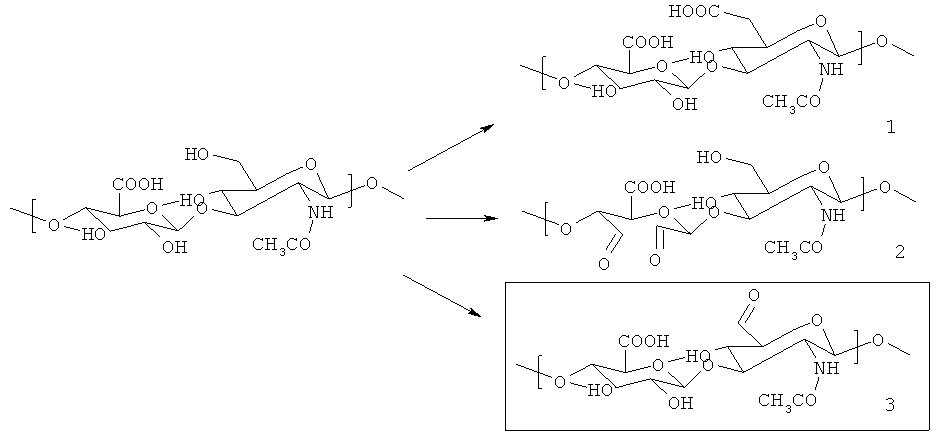
Схема 6. Окисление гиалуронана, продукты реакции
Преимущество способа согласно настоящему изобретению состоит в том, что в соответствующем продукте окисления (структура 3, схема 6) сохраняется строение сопряженных циклов сахаридов. Раскрытие цикла в продукте окисления до диальдегида (структура 2, схема 6) приводит к нарушению линейности цепи и, следовательно, к существенному изменению трехмерной структуры полисахарида по сравнению с немодифицированным гиалуронаном. Несмотря на то, что в продукте окисления до карбоновой кислоты (структура 1, схема 6) разрыва линейности цепи не происходит, карбоксильная группа не обеспечивает столь разнообразных возможностей дальнейшей модификации (связывания), как альдегидная группа. Так как карбоксильная группа уже имеется в составе немодифицированного полисахарида, окисление до структуры 1 (схема 6) приводит только к повышению полярности полисахарида, а не придает ему новое свойство, применимое для связывания новых заместителей.
Известно, что альдегидная группа, связанная с алкильной группой, находится в воде в форме так называемого геминального диола ГК-СН(ОН)2, который взаимодействует с нуклеофилами аналогично альдегидам. По данным ЯМР спектроскопии более 95% гиалуронана, окисленного по положению 6 глюкозаминного фрагмента (продукт 3, схема 6), в водных растворах представляет собой геминальный диол.
Согласно способу настоящего изобретения гиалуроновую кислоту растворяют в воде, затем прибавляют окислитель и перемешивают реакционную смесь при температуре от -10 до 20°С, предпочтительно при 0°С, в течение от 1 до 150 часов, предпочтительно в течение 24 часов.
Полученный окисленный гиалуронан может вступать в реакции связывания с другими веществами, например, содержащими аминогруппу. Связывание может приводить к образованию либо иминной формы, либо - после восстановления - аминной формы (восстановительное аминирование) (схема 7):
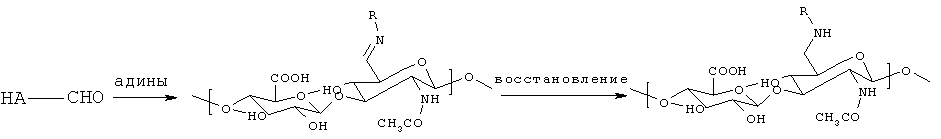
Схема 7. Связывание аминов с окисленным гиалуронаном
Обе части указанной модификации проводят в водном растворе, восстановление идет под воздействием NaBH3CN. Обе реакции, приведенные на схеме 7, можно провести в одну стадию.
Модификация производного гиалуроновой кислоты осуществляется при реакции окисленного производного с амином общей формулы H2N-R либо с гиалуронаном, замещенным группой -R-NH2, в которой R-алкил с линейной или разветвленной цепью С1-С30, не обязательно содержащий ароматические или гетероароматические группы. Данный амин может представлять собой алкиламин, например бутиламин или гександиамин, аминокислоту, пептид или полисахарид, содержащий свободную аминогруппу. В случае применения диамина или соединений, содержащих три или более аминогруппы, возможно получение сетчатых производных гиалуронана. Сетчатые производные образуются также при взаимодействии альдегида с гиалуронаном, замещенным аминоалкильной группой ГК-алкил-NН2.
Подробное описание изобретения
В данном описании DS=степень замещения=100% × число молей введенного заместителя / число молей димеров полисахарида.
Термин «эквивалент (экв.)» в настоящем документе относится к димеру гиалуроновой кислоты, если не указано иное. Процентные доли в настоящем документе соответствуют массовым процентам, если не указано иное.
Молекулярную массу исходного гиалуронана (источник: CPN spol. s r.о., Dolni Dobrouč, CZ) определяли методом SEC-MALLS.
Пример 1. Окисление гиалуроновой кислоты под воздействием системы TEMPO/NaClO
Водный раствор NaClO (0.5 экв.) постепенно добавили к водному раствору гиалуронана (1%) (0.1 г, 20 кДа) (содержащему 10 масс.% NaCl), TEMPO (0.01 экв.) и NаНСО3 (30 экв.). Смесь перемешивали в течение 24 часов при температуре -5°С. Далее раствор разбавляли до концентрации 0.2% дистиллированной водой и диализовали против смеси (0,1% NaCl, 0,1% NaНСО3), 3×5 литров (один раз в сутки), и против дистиллированной воды, 7×5 литров (дважды в сутки). Полученный раствор упаривали и анализировали.
DS 10% (по данным спектроскопии ЯМР).
ЯМР 1Н (D2O) δ 5,26 (с, 1Н, полимер-СH(ОН)2)
HSQC (D2O) кросс-пик 5,26 млн. ед. (1Н) - 90 млн. ед. (13С) полимер-СH(ОН)2)
Фурье-ИК-спектр (КВr) 1740 см-1 -СН=O
Пример 2. Окисление гиалуроновой кислоты под воздействием системы TEMPO/NaClO
Водный раствор NaClO (0.5 экв.) постепенно добавили к водному раствору гиалуронана (0.5%) (0.1 г, 2000 кДа) (содержащему 10 масс.% NaCl), TEMPO (0.01 экв.) и NaHCO3 (30 экв.). Смесь перемешивали в течение 24 часов при температуре -5°С. Далее раствор разбавляли до концентрации 0.2% дистиллированной водой и диализовали против смеси (0,1% NaCl, 0,1% NaНСО3), 3×5 литров (один раз в сутки), и против дистиллированной воды, 7×5 литров (дважды в сутки). Полученный раствор упаривали и анализировали. DS 10% (по данным спектроскопии ЯМР, более подробно см. в Примере 1).
Пример 3. Окисление гиалуроновой кислоты под воздействием системы TEMPO/NaClO
Водный раствор NaClO (0.5 экв.) постепенно добавили к водному раствору гиалуронана (1%) (0.1 г, 20 кДа) (содержащему 10 масс.% NaCl), 4-ацетамидо-ТЕМРО (0.01 экв.) и NaHCO3 (30 экв.). Смесь перемешивали в течение 24 часов при температуре -5°С.Далее раствор разбавляли до концентрации 0.2% дистиллированной водой и диализовали против смеси (0,1% NaCl, 0,1% NaHCO3), 3×5 литров (один раз в сутки), и против дистиллированной воды, 7×5 литров (дважды в сутки). Полученный раствор упаривали и анализировали. DS 10% (по данным спектроскопии ЯМР, более подробно см. в Примере 1).
Пример 4. Окисление гиалуроновой кислоты под воздействием системы TEMPO/NaClO
Водный раствор NaClO (0.5 экв.) постепенно добавили к водному раствору гиалуронана (1%) (0.1 г, 20 кДа) (содержащему 10 масс.% NaCl), 4-ацетамидо-ТЕМРО (0.05 экв.) и NaHCO3 (30 экв.). Смесь перемешивали в течение 10 часов при температуре -10°С. Далее раствор разбавляли до концентрации 0.2% дистиллированной водой и диализовали против смеси (0,1% NaCl, 0,1% NaHCO3), 3×5 литров (один раз в сутки), и против дистиллированной воды, 7×5 литров (дважды в сутки). Полученный раствор упаривали и анализировали.
DS 10% (по данным спектроскопии ЯМР более подробно см. в Примере 1).
Пример 5. Окисление гиалуроновой кислоты под воздействием системы TEMPO/NaClO
Водный раствор NaClO (0.3 экв.) постепенно добавили к водному раствору гиалуронана (1%) (0.1 г, 20 кДа), 4-ацетамидо-ТЕМРО (0.1 экв.) и NaHCO3 (30 экв.). Смесь перемешивали в течение 1 часа при температуре 20°С. Далее раствор разбавляли до концентрации 0.2% дистиллированной водой и диализовали против смеси (0,1% NaCl, 0,1% NaHCO3), 3×5 литров (один раз в сутки), и против дистиллированной воды, 7×5 литров (дважды в сутки). Полученный раствор упаривали и анализировали. DS 5% (по данным спектроскопии ЯМР, более подробно см. в Примере 1).
Пример 6. Окисление гиалуроновой кислоты под воздействием системы ТЕМРО/ТСС
4-Ацетамидо-ТЕМРО (0.01 экв.) и ТСС (0.2 экв.) добавили к раствору гиалуроновой кислоты (1%) (0.1 г, 20 кДа) в смеси N,N-диметилформамид/вода 70/30.
Смесь перемешивали в течение 24 часов при температуре -5°С. Далее раствор разбавляли до концентрации 0,1% и диализовали против смеси (0,1% NaCl, 0,1% NaHCO3), 3×5 литров (один раз в сутки) и против дистиллированной воды 7×5 литров (дважды в сутки). Полученный раствор упаривали и анализировали. DS 5% (по данным спектроскопии ЯМР, более подробно см. в Примере 1).
Пример 7. Окисление гиалуроновой кислоты под воздействием системы ТЕМРО/ТСС
4-Ацетамидо-ТЕМРО (0.01 экв.) и ТСС (0.2 экв.) добавили к раствору гиалуроновой кислоты (1%) (0.1 г, 20 кДа) в смеси N,N-диметилформамид/вода 90/10. Смесь перемешивали в течение 24 часов при температуре 20°С. Затем раствор разбавляли до концентрации 0,1% и диализовали против смеси (0,1% NaCl, 0,1% NaHCO3), 3×5 литров (один раз в сутки) и против дистиллированной воды 7×5 литров (дважды в сутки). Полученный раствор упаривали и анализировали. DS 10% (по данным спектроскопии ЯМР, более подробно см. в Примере 1).
Пример 8. Окисление гиалуроновой кислоты под воздействием системы ТЕМРО/ТСС
4-Ацетамидо-ТЕМРО (0.01 экв.) и ТСС (1 экв.) добавили к раствору гиалуроновой кислоты (1%) (0.1 г, 20 кДа) в смеси N,N-диметилформамид/вода 40/60. Смесь перемешивали в течение 24 часов при температуре -5°С. Затем раствор разбавляли до концентрации 0,1% и диализовали против смеси (0,1% NaCl, 0,1% NaHCO3), 3×5 литров (один раз в сутки) и против дистиллированной воды 7×5 литров (дважды в сутки). Полученный раствор упаривали и анализировали. DS 15% (по данным спектроскопии ЯМР, более подробно см. в Примере 1).
Пример 9. Окисление гиалуроновой кислоты под воздействием системы ТЕМРО/ТСС
4-Ацетамидо-ТЕМРО (0.01 экв.) и ТСС (1 экв.) добавили к раствору гиалуроновой кислоты (0.5%) (0.1 г, 2000 кДа) в смеси N,N-диметилформамид/вода 40/60. Смесь перемешивали в течение 24 часов при температуре -5°С. Далее раствор разбавляли до концентрации 0,1% и диализовали против смеси (0,1% NaCl, 0,1% NaHCO3), 3×5 литров (один раз в сутки) и против дистиллированной воды 7×5 литров (дважды в сутки). Полученный раствор упаривали и анализировали. DS 15% (по данным спектроскопии ЯМР, более подробно см. в Примере 1).
Пример 10. Окисление гиалуроновой кислоты под воздействием системы ТЕМРО/ТСС
TEMPO (0.01 экв.) и ТСС (0.2 экв.) добавили к раствору гиалуроновой кислоты (1%) (0.1 г, 20 кДа) в смеси N,N-диметилформамид/вода 70/30. Смесь перемешивали в течение 1 часа при температуре 20°С. Далее раствор разбавляли до концентрации 0,1% и диализовали против смеси (0,1% NaCl, 0,1% NaHCO3), 3×5 литров (один раз в сутки), и против дистиллированной воды, 7×5 литров (дважды в сутки). Полученный раствор упаривали и анализировали.
DS 5% (по данным спектроскопии ЯМР, более подробно см. в Примере 1).
Пример 11. Окисление гиалуроновой кислоты под воздействием системы ТЕМРО/ТСС
TEMPO (0.01 экв.) и ТСС (0.2 экв.) добавили к раствору гиалуроновой кислоты (1%) (0.1 г, 20 кДа) в смеси ДМФА/вода 70/30. Смесь перемешивали в течение 100 часов при температуре -5°С. Затем раствор разбавляли до концентрации 0,1% и диализовали против смеси (0,1% NaCl, 0,1% NНСО3), 3×5 литров (один раз в сутки) и против дистиллированной воды 7×5 литров (дважды в сутки). Полученный раствор упаривали и анализировали. DS 5% (по данным спектроскопии ЯМР, более подробно см. в Примере 1).
Пример 12. Окисление гиалуроновой кислоты под воздействием системы TEMPO/NaBrO
Водный раствор NaClO (0.5 экв.) постепенно добавили к водному раствору гиалуронана (1%) (0.1 г, 20 кДа) (содержащему 5 масс.% NaBr), 4-ацетамидо-ТЕМРО (0.5 экв.) и NaHCO3 (30 экв.). Смесь перемешивали в течение 24 часов при температуре 0°С. Далее раствор разбавляли до концентрации 0.2% дистиллированной водой и диализовали против смеси (0,1% NaCl, 0,1% NaНСО3), 3×5 литров (один раз в сутки), и против дистиллированной воды, 7×5 литров (дважды в сутки). Полученный раствор упаривали и анализировали. DS 14% (по данным спектроскопии ЯМР, более подробно см. в Примере 1).
Пример 13. Окисление гиалуроновой кислоты под воздействием системы TEMPO/NaClO
Водный раствор NaClO (0.5 экв.) постепенно добавили к водному раствору гиалуронана (1%) (0.1 г, 200 кДа) (содержащему 10 масс.% NaBr), TEMPO (0.5 экв.) и NaHCO3 (5 экв.). Смесь перемешивали в течение 24 часов при температуре 0°С. Далее раствор разбавляли до концентрации 0.2% дистиллированной водой и диализовали против смеси (0,1% NaCl, 0,1% NaHCO3), 3×5 литров (один раз в сутки), и против дистиллированной воды, 7×5 литров (дважды в сутки). Полученный раствор упаривали и анализировали. DS 18% (по данным спектроскопии ЯМР, более подробно см. в Примере 1).
Пример 14. Реакция окисленного гиалуронана с амином
К водному раствору окисленной гиалуроновой кислоты (1%) (0,1 г, степень замещения: DS=18%, Пример 13) добавили бутиламин (0,4 экв.). Смесь перемешивали в течение 24 часов при температуре 20°С. Осаждали двукратным количеством ацетона и 0,1 мл насыщенного водного раствора NaCl, отфильтровывали и сушили в вакууме. Полученное желтое вещество анализировали. ЭСП 328 нм, переход n→π∗-CH=N-
Пример 15. Реакция окисленного гиалуронана с бутиламином и последующее восстановление
К водному раствору окисленной гиалуроновой кислоты (1%) (0,1 г, степень замещения: DS=18%, Пример 13) добавили бутиламин (0,4 экв.). Смесь перемешивали в течение 24 часов при температуре 20°С. Далее раствор смешивали с NaBH3CN (3 экв.) в 0,5 мл воды. Смесь перемешивали в течение 24 часов при температуре 20°С. Затем раствор разбавляли до концентрации 0,1% и диализовали против смеси (0,1% NaCl, 0,1% NaHCO3), 3×5 литров (один раз в сутки) и против дистиллированной воды 7×5 литров (дважды в сутки). Полученный раствор упаривали и анализировали. DS 15% (по данным спектроскопии ЯМР).
|
Пример 16. Реакция окисленного гиалуронана с диамином и последующее восстановление
К водному раствору окисленной гиалуроновой кислоты (1%) (0,1 г, степень замещения: DS=18%, Пример 13) добавили гександиамин (0,4 экв.). Смесь перемешивали в течение 24 часов при температуре 20°С. Далее раствор смешивали с NaBH3CN (3 экв.) в 0,5 мл воды. Смесь перемешивали в течение 24 часов при температуре 20°С. Далее раствор разбавляли до концентрации 0,1% и диализовали против смеси (0,1% NaCl, 0,1% NaHCO3), 3×5 литров (один раз в сутки) и против дистиллированной воды 7×5 литров (дважды в сутки). Полученный раствор упаривали и анализировали.
DS 16% (по данным спектроскопии ЯМР).
|
Пример 17. Реакция окисленного гиалуронана с аминогиалуронаном
Водный раствор окисленной гиалуроновой кислоты (1%) (0,1 g, степень замещения: DS=18%, Пример 13) смешивали с 1%-ным водным раствором производного гиалуронана, замещенного гександиамином (1 экв., DS=16%, Пример 16) при температуре 20°С. Нерастворимый плотный смолистый осадок, образовавшийся через несколько минут, механически измельчали, отделяли фильтрованием и сушили при пониженном давлении.
Фурье-ИК-спектр (КВr) 1700 см-1.
Пример 18 Восстановительное аминирование окисленного гиалуронана под воздействием лизина
К водному раствору окисленной гиалуроновой кислоты (1%) (0,1 г, степень замещения: DS=18%, Пример 13) добавили лизин (0.3 экв.). Смесь перемешивали в течение 24 часов при температуре 20°С. Далее раствор смешивали с NaBH3CN (3 экв.) в 0,5 мл воды. Смесь перемешивали в течение 24 часов при температуре 20°С.Раствор разбавляли до концентрации 0,1% и диализовали против смеси (0,1% NaCl, 0,1% NaHCO3), 3×5 литров (один раз в сутки) и против дистиллированной воды 7×5 литров (дважды в сутки). Полученный раствор упаривали и анализировали. DS 14% (по данным спектроскопии ЯМР).
Спектр 1Н ЯМР (HSQC, DOSY, 2% NaOD/D2O): δ 1,33 (м, 2Н, -СН-СН2-СH2-), 1,48 (м, 2Н, -СН-СН2-СН2-СH2-), 1,55 (м, 1Н, -СН-СHН-), 1,63 (м, 1H, -СН-СНH-), 2,62 (м, 2Н, -СН-СН2-СН2-СН2-СH2-), 2,65 (м, 1Н, полимер-СHН-NH-), 2,99 (м, 1H, полимер-СНH-NH-), 3,16(м, 1H, -СH-СН2).
Пример 19. Восстановительное аминирование окисленного гиалуронана под воздействием лизина
К водному раствору окисленной гиалуроновой кислоты (1%) (0,1 г, степень замещения: DS=18%, Пример 13) добавили лизин (20 экв.). The mixture was stirred for 24 hours at the temperature of 20°C. The solution was then mixed with NaBH3CN (10 eq) in 0.5 ml of water. Смесь перемешивали в течение 24 часов при температуре 20°С.Раствор разбавляли до концентрации 0,1% и диализовали против смеси (0,1% NaCl, 0,1% NaHCO3), 3×5 литров (один раз в сутки) и против дистиллированной воды 7×5 литров (дважды в сутки). Полученный раствор упаривали и анализировали. DS 17% (по данным спектроскопии ЯМР, Пример 10).
Пример 20. Восстановительное аминирование окисленного гиалуронана под воздействием серина
К водному раствору окисленной гиалуроновой кислоты (1%) (0,1 г, степень замещения: DS=18%, Пример 13) добавили серин (0.3 экв.). Смесь перемешивали 1 мин при температуре 20°С. Далее раствор смешивали с NaBH3CN (3 экв.) в 0,5 мл воды. Смесь перемешивали в течение 24 часов при температуре 20°С. Раствор разбавляли до концентрации 0,1% и диализовали против смеси (0,1% NaCl, 0,1% NaHCO3), 3×5 литров (один раз в сутки) и против дистиллированной воды 7×5 литров (дважды в сутки). Полученный раствор упаривали и анализировали.
DS 14% (по данным спектроскопии ЯМР).
1H ЯМР спектр (HSQC, DOSY) (2% NaOD/D2O), 6: 2,74 (м, 1H, полимер-СHН-NH-), 3,08 (м, 1Н, полимер-CHH-NH-), 3,21 (м, 1Н, -СH-СН2-ОН), 3,72 (м, 1H, -СН-СHН-ОН), 3,78 (м, 1Н, -СН-СНH-ОН).
Пример 21. Восстановительное аминирование окисленного гиалуронана под воздействием аргинина
К водному раствору окисленной гиалуроновой кислоты (1%) (0,1 г, степень замещения: DS=18%, Пример 13) добавили аргинин (0.3 экв.). Смесь перемешивали в течение 100 часов при температуре 20°С. Далее раствор смешивали с NaBH3CN (3 экв.) в 0,5 мл воды. Смесь перемешивали в течение 24 часов при температуре 20°С. Раствор разбавляли до концентрации 0,1% и диализовали против смеси (0.1% NaCl, 0,1% NaHCO3), 3×5 литров (один раз в сутки) и против дистиллированной воды 7×5 литров (дважды в сутки). Полученный раствор упаривали и анализировали. DS 11% (по данным спектроскопии ЯМР).
1Н ЯМР спектр (HSQC, DOSY) (2% NaOD/D2O), δ: 1,61 (м, 2Н, -СН-СН2-СH2-), 1,63 (м, 1Н, -СН-СНH-), 1,70 (м, 1Н, -СН-СНH-), 2,65 (м, 1Н, полимер-СHН-NH-), 3,01 (м, 1Н, полимер-СНH-NH-), 3,13 (м, 1H, -СH-СН2-), 3,21 (м, 2Н, -СН-СН2-СН2-СH2-).
Пример 22. Восстановительное аминирование окисленного гиалуронана под воздействием пентапептида PAL-KTTKS (palmytoyl-Lys-Thr-Thr-Lys-Ser)
Раствор окисленной гиалуроновой кислоты (1%) (0,1 г, степень замещения: DS=18%, Пример 13) в смеси вода/изопропиловый спирт 2:1 смешивали с 1%-ным раствором замещенного пентапептида PAL-KTTKS (0,05 экв.) в изопропиловом спирте. Смесь перемешивали в течение 24 часов при температуре 20°С. Далее раствор смешивали с NaBH3CN (3 экв.) в 0,5 мл воды. Смесь перемешивали в течение 24 часов при температуре 20°С. Далее полученный раствор разбавляли до концентрации 0.1% и диализовали против смеси (0.1% NaCl, 0.1% NaHCO3), 3×5 литров (один раз в сутки) и против дистиллированной воды 7×5 литров (дважды в сутки). Полученный раствор упаривали и анализировали.
DS 9% (по данным спектроскопии ЯМР).
1Н ЯМР спектр (HSQC, DOSY) (2% NaOD/D2O), δ: 1,61 (м, 2Н, -СН-СН2-СH2-), 1,63 (м, 1Н, -СН-СНH-), 1,70 (м, 1Н, -СН-СНH-), 2,65 (м, 1Н, полимер-СHН-NH-), 3,01 (м, 1Н, полимер-СНH-NH-), 3,13 (м, 1H, -СH-СН2-), 3,21 (м, 2Н, -СН-СН2-СН2-СH2-).

