Результат интеллектуальной деятельности: N,N'-(СУЛЬФОНИЛДИ-П-ФЕНИЛЕН)БИС-N'',N''-ДИМЕТИЛФОРМАМИДИН, ОБЛАДАЮЩИЙ АКАРИЦИДНЫМ ДЕЙСТВИЕМ
Вид РИД
Изобретение
Область техники, к которой относится изобретение
Изобретение относится к области ветеринарии, медицины и сельского хозяйства, а именно к применению N,N′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидина в качестве вещества, обладающего акарицидным действием.
Уровень техники
Членистоногие подкласса Acarina чрезвычайно широко распространены в природе. Многие из них паразитируют на различных видах животных и растений, а также вызывают различные заболевания у людей. Некоторые виды клещей не только приносят вред здоровью животных и человека вследствие паразитического питания (кровью), но и переносят множество чрезвычайно опасных, часто летальных заболеваний, инфицируя животных и человека при присасывании. В I половине XX века были предложены достаточно активные акарициды - полихлорированные инсектициды, толерантность к которым у членистоногих подкласса Acarina развивалась медленно. Это позволило в значительной степени контролировать численность данных паразитов. Однако в дальнейшем были обнаружены очень опасные экологические последствия применения инсектицидов этого класса - это связанно с очень высокой устойчивостью их в природной среде, в организме животных и накоплением их в пищевых цепочках, что привело к угрозе исчезновения целых видов животных. Кроме этого, производство и применение большинства полихлорированных инсектицидов загрязняет среду полихлордиоксинами, обладающими очень высокой иммунотоксичностью, и к тому же очень устойчивых. В результате применение инсектицидов-акарицидов этой группы к концу XX века повсеместно было запрещено или значительно ограничено. Вместо полихлорированных инсектицидов в практику были введены синтетические аналоги природных инсектицидов - пиретроиды, проявившие значительный акарицидный эффект.Однако скоро обнаружилось, что членистоногие подкласса Acarina очень быстро приобретают толерантность к инсектицидам этого типа, причем практически к любым пиретроидам, и природным, и синтетического происхождения. Хотя к началу XXI века были разработаны весьма эффективные инсектициды новых групп - ингибиторы синтеза хитина, неоникотиноиды, ювенильные гормоны, пиразолоны, авермектины, высокоактивные по отношению к членистоногим класса Insecta, однако по отношению к членистоногим подкласса Acarina они оказались либо не активны, либо у клещей быстро вырабатывалась толерантность и они теряли чувствительность ко всем препаратам группы.
Во II половине XX века была обнаружена высокая акарицидная активность диметилформамидиновых производных ариламинов, из которых в практику были введены форметанат (3-[(EZ)-диметиламинометиленамино]фенилметилкарбамат, cas №22259-30-9) и хлордимеформ (N′-(4-хлор-2-метилфенил)-N,N-диметилформамидин, cas №6164-98-3). Однако форметанат оказался чрезвычайно токсичным для теплокровных, крысы LD50 (орал)=20 мг/кг [World Review of Pest Control. - 1970. - Vol. 9. - P. 119.]. Хлордимеформ, хотя и имеет меньшую токсичность, крысы LD50 (орал) = 160 мг/кг [Химия в сельском хозяйстве. - 1978. - №2. - с. 59.], но не является безопасным, т.к. оказалось, что продукты его разложения нефротоксичны и очень устойчивы, накапливаются в почве и растениях, что экологически неприемлемо [Н.Н. Мельников, А.И. Волков, О.А. Короткова. Пестициды и окружающая среда - М.: Химия, 1977. - 240 с]. Оба продукта практически были выведены из употребления. Наиболее удачным препаратом группы формамидинов оказался N,N-ди(2,4-ксилилиминометил)метиламин (cas №33089-61-1) (далее амитраз), широко применяемый в настоящее время в ветеринарии и сельском хозяйстве. Однако этот препарат имеет также ряд недостатков:
- Довольно высокая токсичность, крысы LD50 (орал) = 400 мг/кг [Merck Index - 11th ed. - 1989. - Vol. 11. - P. 80], что исключает применение в медицине и затрудняет его использование в ветеринарии.
- Низкая химическая стойкость, амитраз легко гидролизуется и окисляется с потерей акарицидной активности, что также затрудняет его применение.
- Амитраз проявляет токсичность вследствие эффектов α2-адренэргического агонизма и ингибирования моноаминооксидазы в ткани головного мозга животных. Это ведет уже в дозах приблизительно 1 мг/кг веса животного к развитию нарушения поведения, а при дозах приблизительно 100 мг/кг интоксикация становится опасной для жизни [Дж. Роудер. Ветеринарная токсикология. - М. Аквариум, 2008. - 416 с].
Раскрытие изобретения
Задачей изобретения был поиск вещества формамидиновой группы, обладающего высокой акарицидной активностью при низкой токсичности для теплокровных и высокой химической стойкостью, в т.ч. в водных средах, но в то же время легко разрушающегося в окружающей среде без образования опасных продуктов. Из исследованных нами формамидинов производных ариламинов наилучшим по всем параметрам (высокая акарицидная активность, низкая токсичность) оказался Ν,Ν′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидин (Methanimidamide, N′,N′′′-(sulfonyldi-4,1-phenylene)bis[N,N-dimethyl-, cas №3217-65-0).
N,N′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидин известен давно [A.W. Hofmann. Annals. - 1858. - Vol. 54. - P. 197]. Он был изучен в качестве антибактериального, противопротозойного, противовирусного и антигельминтного агента Стейгером [US 3073851, опубл.: 15.01.1963] и на иммуномодулирующую и противоопухолевую активность Лином [EP 354303, опубл.: 14.02.1990].
Метилурациловая соль N,N′-(сульфонилди-п-фенилен)бис-N,N-диметилформамидина (далее сульпифон) была предложена в качестве стимулирующей клеточный метаболизм, проявляющей высокую иммунотропную и антимикобактериальную активность [RU 2136668, опубл.: 10.09.19991, однако не получила применения в медицине и ветеринарии.
Предложено также иммуномодулирующее средство, содержащее сульпифон и органическую кислоту (аскорбиновую, янтарную или лимонную) [RU 2292892, опубл.: 10.02.2007], которое также не было принято к использованию в медицине и ветеринарии.
Чрезвычайно высокая акарицидная активность широкого спектра у Ν,Ν′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидина оказалась неожиданной. В доступной литературе указаний на данную активность N,N′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидина нами не обнаружено. Предлагаемое соединение с высокой эффективностью излечивает инвазивные патологии у животных, вызванные чесоточными клещами (псороптоз, саркоптоз, хориоптоз и т.д.), при этом клинический эффект достоверно более выраженный, нежели при использовании амитраза (см. пример 4). С высокой степенью вероятности можно предположить, что будет наблюдаться идентичный эффект при инвазиях у человека (саркоптоз, нотоэдроз). Предлагаемый в качестве акарицида N,N′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидин уничтожает также иксодовых клещей - опасных переносчиков вирусных заболеваний, патогенных риккетсий и простейших (см. пример 3; 5). Соединение обладает низкой токсичностью, крысы LD50 (орал) = 4750 мг/кг (см. пример 1), это делает безопасным его применение в ветеринарии / медицине и делает возможным использование для системного введения (орального, инъекционного, трансдермального). Соединение проявляет также противовоспалительный эффект (см. пример 2), снижая уровень медиаторов воспаления всех групп; это, возможно, также увеличивает клинический эффект, ускоряя заживление поврежденных тканей животного при клещевых инвазиях (см. пример 4).
В сравнении с широко применяемым акарицидом амитразом предлагаемое соединение показало значительно большую активность в отношении чесоточных, иксодовых, фитопатогенных клещей (см. примеры 3; 4; 5; 6).
Кроме того, предлагаемое соединение более устойчиво в водных средах, чем амитраз (см. пример 6). В окружающей среде N,N′-(сульфонилди-п-фенилен)бис-Ν″,Ν″-диметилформамидин распадается до известного 4,4′-диаминодифенилсульфона (дапсона) - малотоксичного соединения, крысы LD50 (орал) = 1000 мг/кг [Logemann W, Miori G.P. Arzneimittelforschung. - 1955. - Vol. 5. - P. 213-221].
Акарициды амидинового ряда в окружающей среде быстро гидролизуются до формамидов соответствующих анилинов и затем относительно медленно до свободного анилина. Последний в зависимости от структуры претерпевает различные превращения. Хлордимиформ образует 2-метил-4-хлоранилин, который устойчив в окружающей среде и способен накапливаться в растениях, при этом обладает подобно всем п-хлоранилинам нефротоксичностью. Амитраз образует 2,4-ксилидин, который сравнительно быстро окисляется по метильной группе в параположении и ассимилируется микроорганизмами почвы как аналог п-аминобензойной кислоты. Вместе с тем 2,4-ксилидин довольно токсичен для теплокровных, крысы LD50 (орал) = 467 мг/кг [National Technical Information Service. PB 214-270].
N,N′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидин медленно ступенчато гидролизуется в итоге до 4,4′-диаминодифенилсульфона (дапсона), который также является структурным аналогом п-аминобензойной кислоты и ассимилируется почвенными микроорганизмами, которые в итоге окисляют структуру до углекислоты и сульфатов аммония. Ввиду быстрой ассимиляции продуктов разложения N,N′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидина микроорганизмами в растениях они не накапливаются и в пищевые цепочки не попадают (в отличие от продуктов разложения хлордимеформа).
Структура ароматического фрагмента молекулы N,N′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидина исключает связывание с α2-адренорецепторами. N,N′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидин не оказывает влияния на активность моноаминооксидаз, т.к. акцепторное влияние арилсульфонильной группы снижает основность формамидиновой структуры до уровня, исключающего связывания с ферментом. При изучении токсичности не обнаружено влияния N,N′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидина на функции ЦНС животных.
Таким образом найдено вещество (N,N′-(сульфонилди-п-фенилен)бис-N,N″-диметилформамидин), обладающее широким спектром акарицидного действия, низкой токсичностью, химически стойкое, в том числе в водных средах, и распадающееся под действием природных факторов без образования опасных продуктов. На основе предлагаемого N,N′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидина могут быть получены общеизвестными для специалистов методами препараты акарицидного действия для использования в медицине, ветеринарии, сельском хозяйстве, средства бытовой химии и т.д.
Краткое описание чертежей
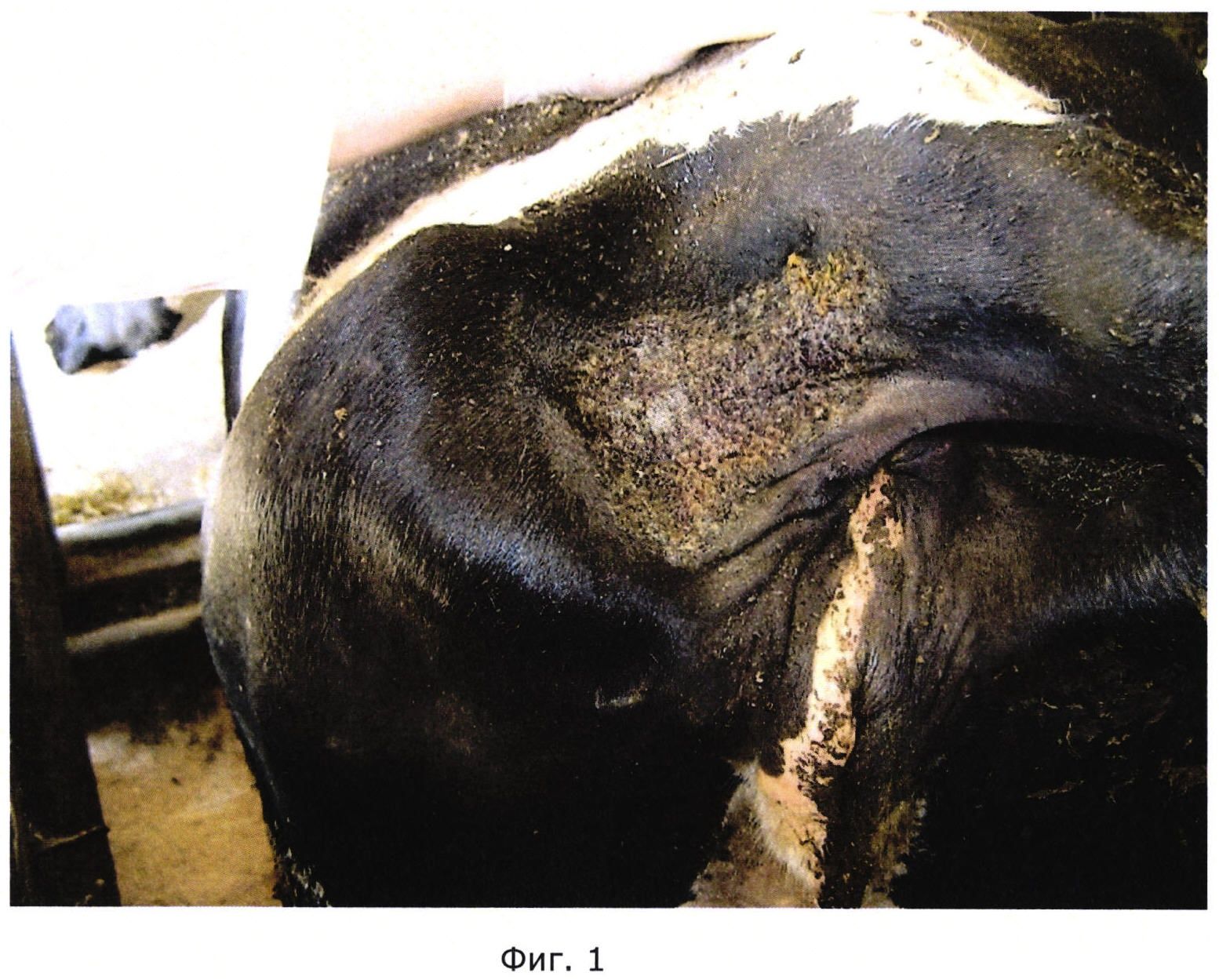
На Фиг. 1 показана хориоптозная колония до обработки гелем на основе Ν,Ν′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидина.
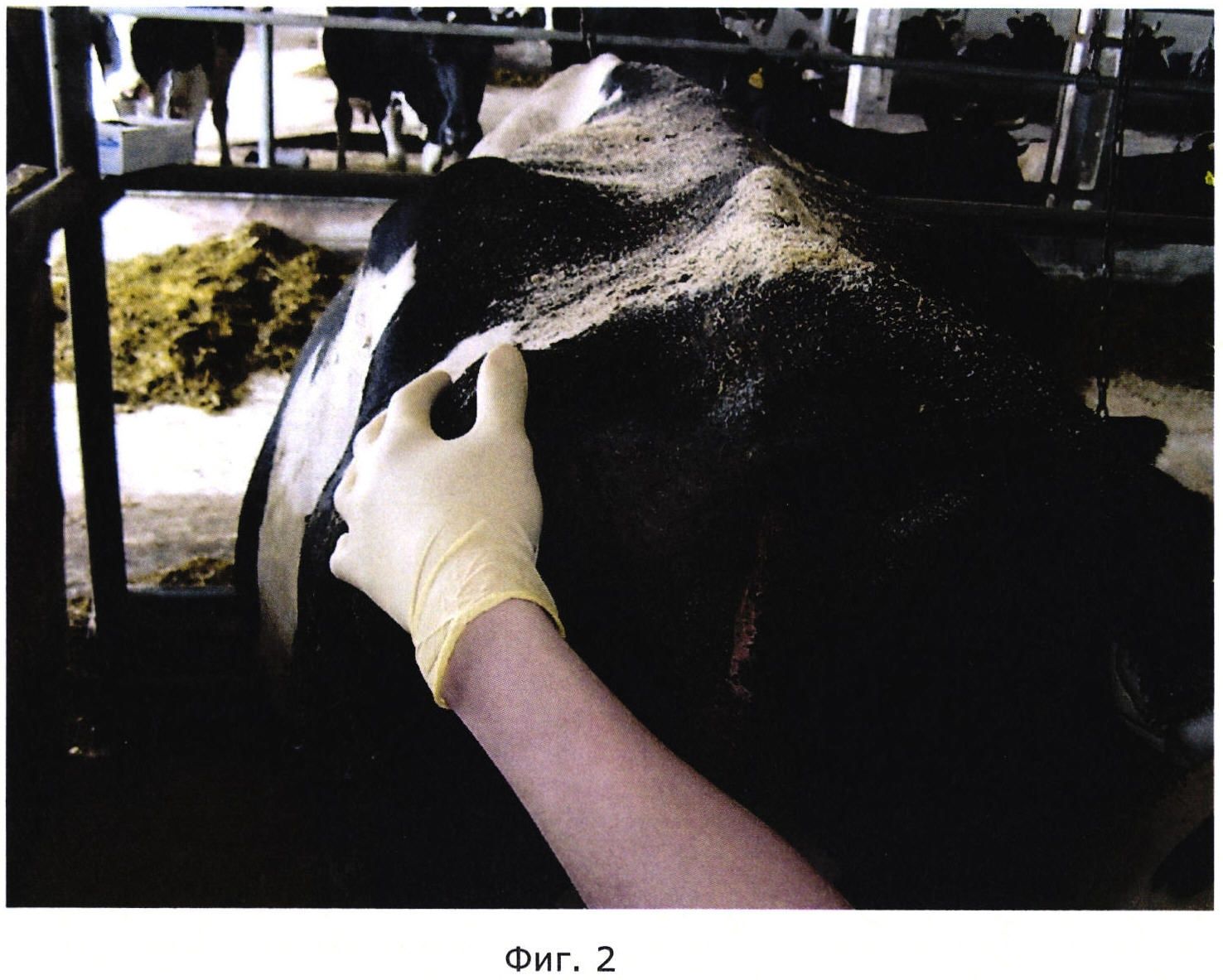
На Фиг. 2 показаны результаты обработки гелем на основе N,N′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидина спустя 7 дней.
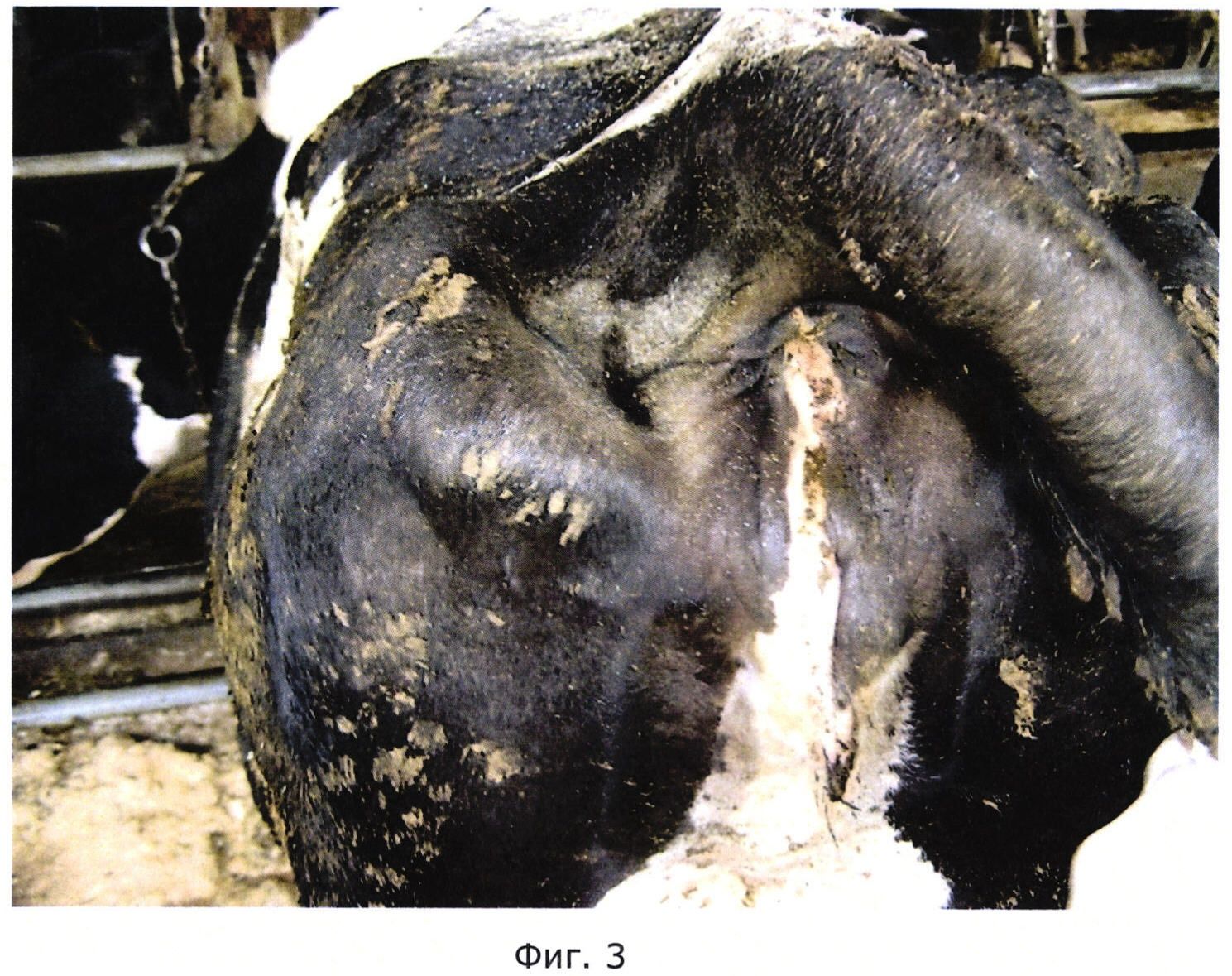
На Фиг. 3 показаны результаты обработки гелем на основе N,N′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидина спустя 14 дней.
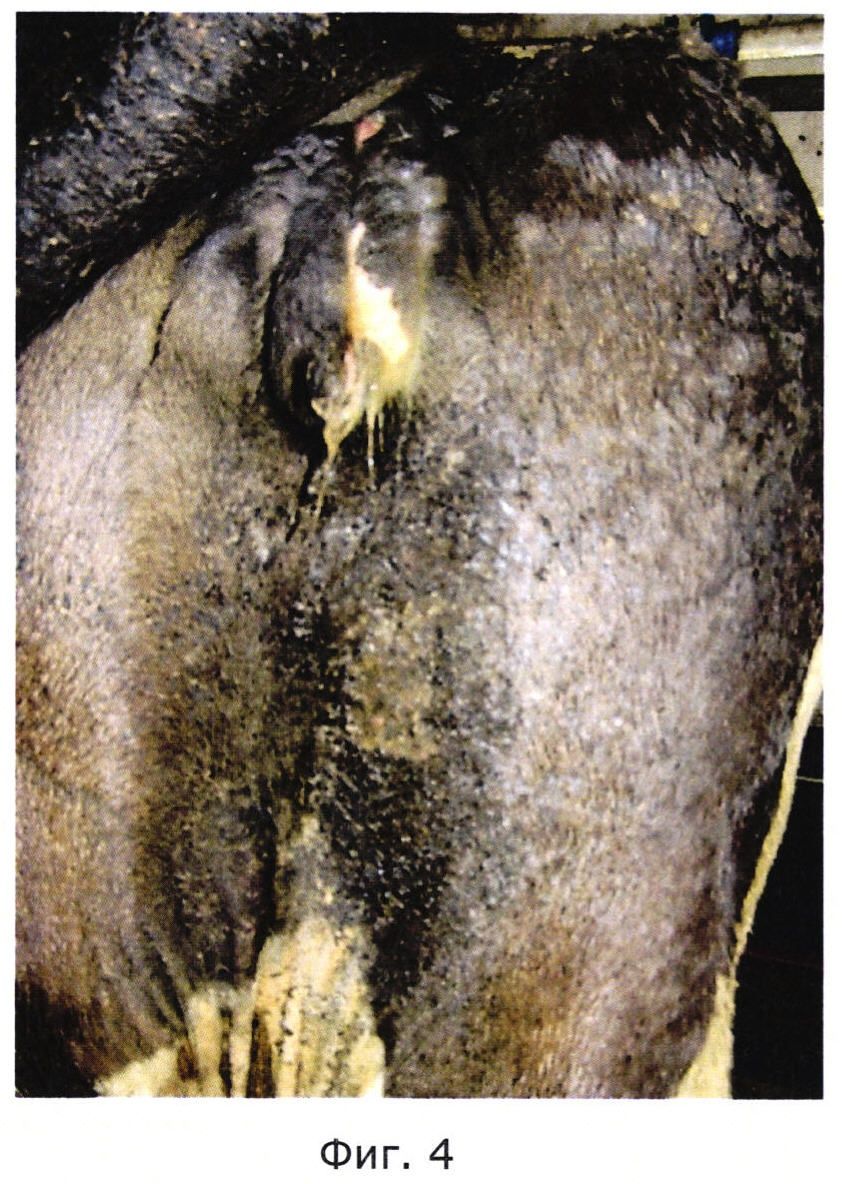
На Фиг. 4 показана хориоптозная колония до обработки гелем на основе амитраза.
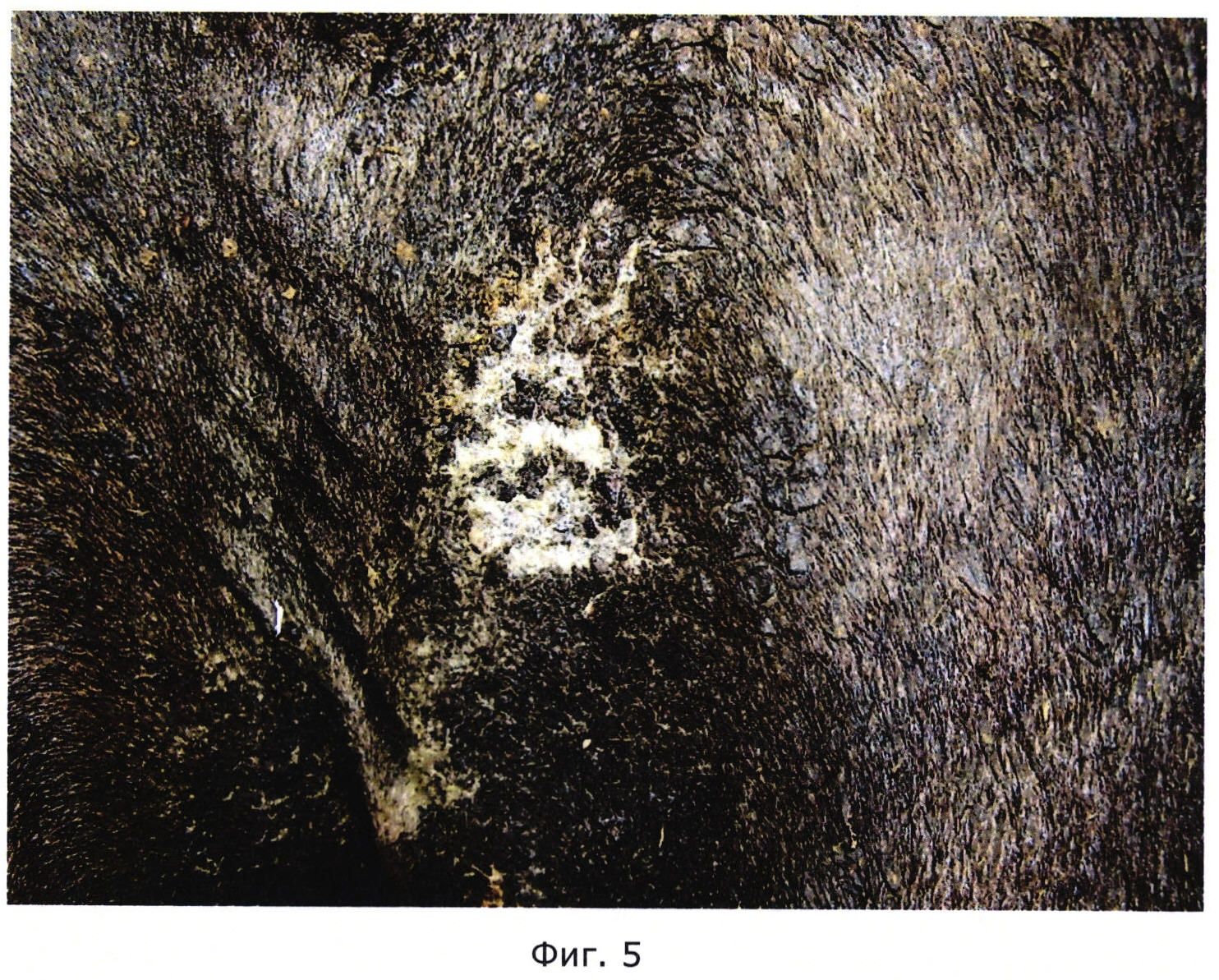
На Фиг. 5 показаны результаты обработки гелем на основе амитраза спустя 7 дней.
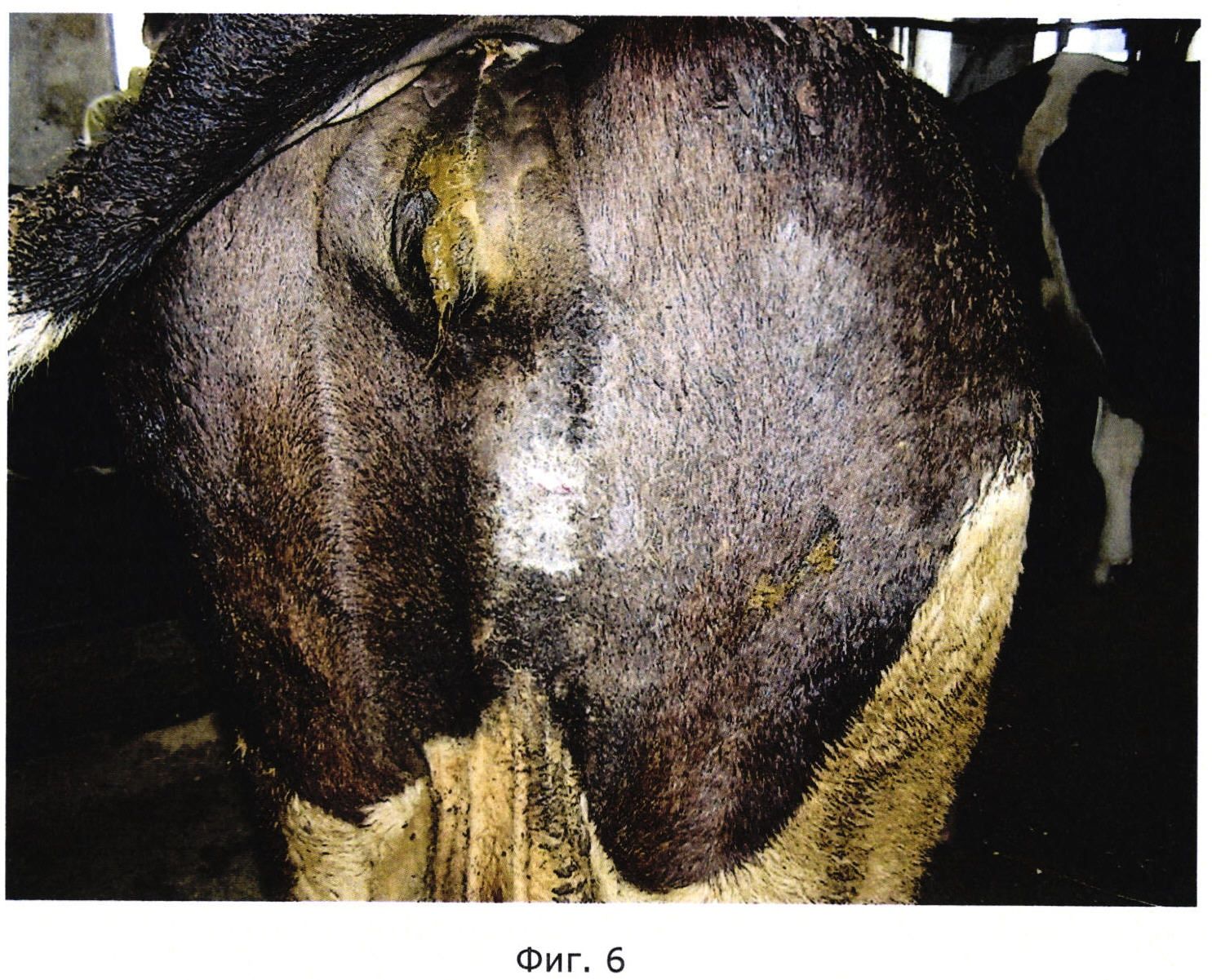
На Фиг. 6 показаны результаты обработки гелем на основе амитраза спустя 14 дней.
Осуществление изобретения
Пример 1. (Острая токсичность N,N′-(сульфонилди-п-фенилен)бис-N″,N′-диметилформамидина)
Материалы и методы
Изучение острой токсичности N,N′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидина проводили на белых крысах массой 200-210 г при внутрижелудочном введении в форме водного раствора препарата в возрастающих дозировках. В опыте использовали клинически здоровых животных, которые предварительно выдерживали на 15-дневном карантине. Статистические группы состояли из 6 животных.
Результаты
Установлено, что LD50 (в/ж) = 4750 мг/кг, что позволяет отнести данный препарат к 3 классу опасности (умеренно опасные вещества) по ГОСТ 12.1.007-76.
Результаты определения параметров острого токсического действия препарата при внутрижелудочном способе введения представлены в Таблице 1.
Клиника острого отравления животных характеризовалась выраженным угнетением, вялостью, снижением подвижности. Смерть наступала в результате остановки дыхания.

Пример 2. (Оценка противовоспалительной и иммуномодулирующей активности N,N′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидина)
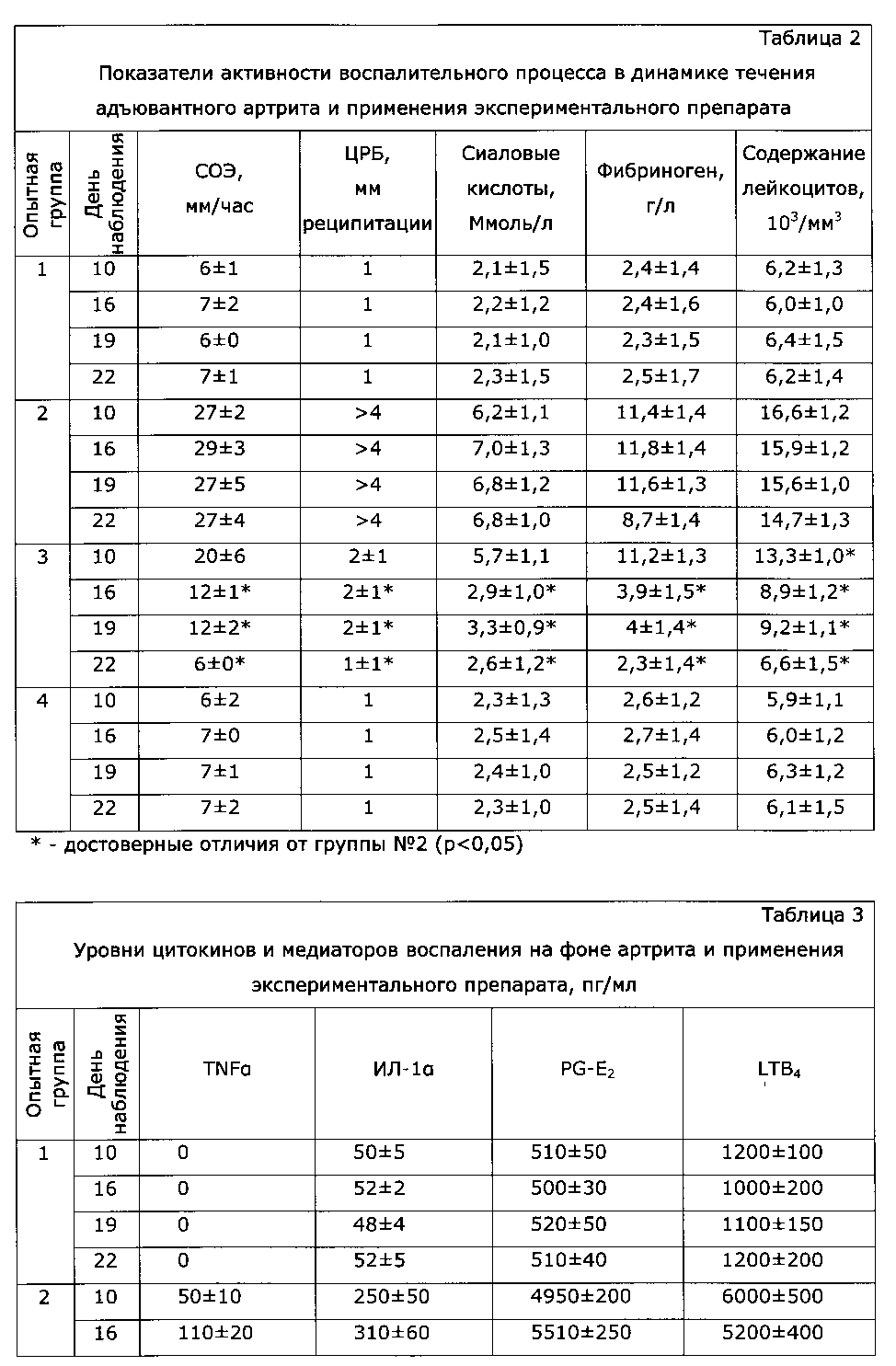
Противовоспалительную и иммуномодулирующую активность препарата оценивали унифицированными биохимическими и гематологическими методами по содержанию СОЭ, ЦРБ, сиаловых кислот, фибриногена, лейкоцитов и «цитокиновому статусу».
Материалы и методы
В опыте использовали крыс-самцов массой 180-200 г. Каждая группа включала по 10 особей. Хроническое иммунное воспаление моделировали субплантарным введением в правую заднюю лапу 0,1 мл адъюванта Фрейнда (взвесь БЦЖ 2,5 мг/мл в вазелиновом масле). Тестируемый препарат начинали вводить внутрижелудочно с 5 дня после введения адъюванта ежедневно на протяжении 12 дней. Всего было исследовано 4 экспериментальные группы:
группа - интактные + крахмальная взвесь;
группа - адъювант + крахмальная взвесь (артрит без лечения);
3 группа - адъювант + N,N′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидин (20 мг/кг в крахмальной взвеси);
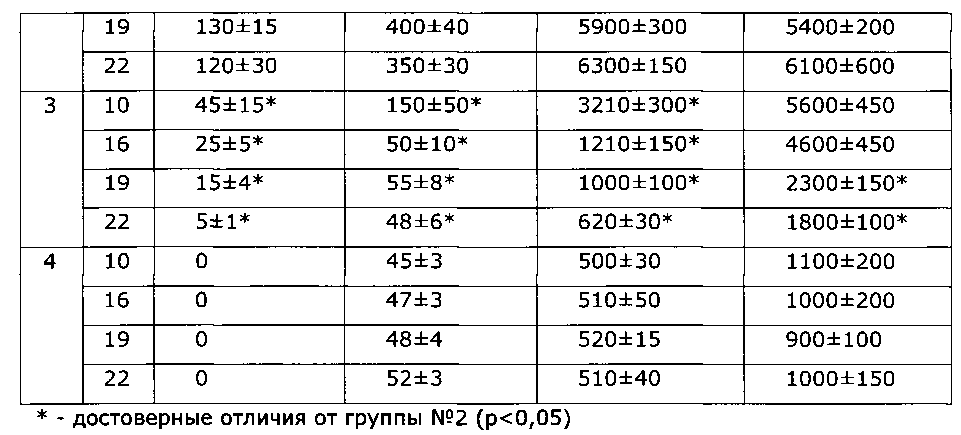
4 группа - N,N′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидин (20 мг/кг в крахмальной взвеси). Оценку осуществляли на 10, 16, 19 и 22 дни после введения адъюванта.
Выводы
Полученные данные свидетельствуют о наличии у тестируемого препарата выраженных противовоспалительных (см. Таблицу 2) и определенных иммуномодулирующих свойств в условиях воспаления (см. Таблицу 3). Введение препарата интактным животным не влияет на их «цитокиновый статус».
Пример 3. (Исследование акарицидной активности N,N′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидина, влияние на иксодовых клещей)
Материалы и методы
Сравнивали два препарата акарицидного действия различного состава.
Состав 1, масс.%:
|
Состав 2, масс.%:
|
Испытания проходили в лаборатории паразитологии ГНУ СНИИЖК. Опыты (in vitro) проводили на изолированных клещах Dermacentor pictus, Dermacentor marginatus, Hyalomma plumbeum.
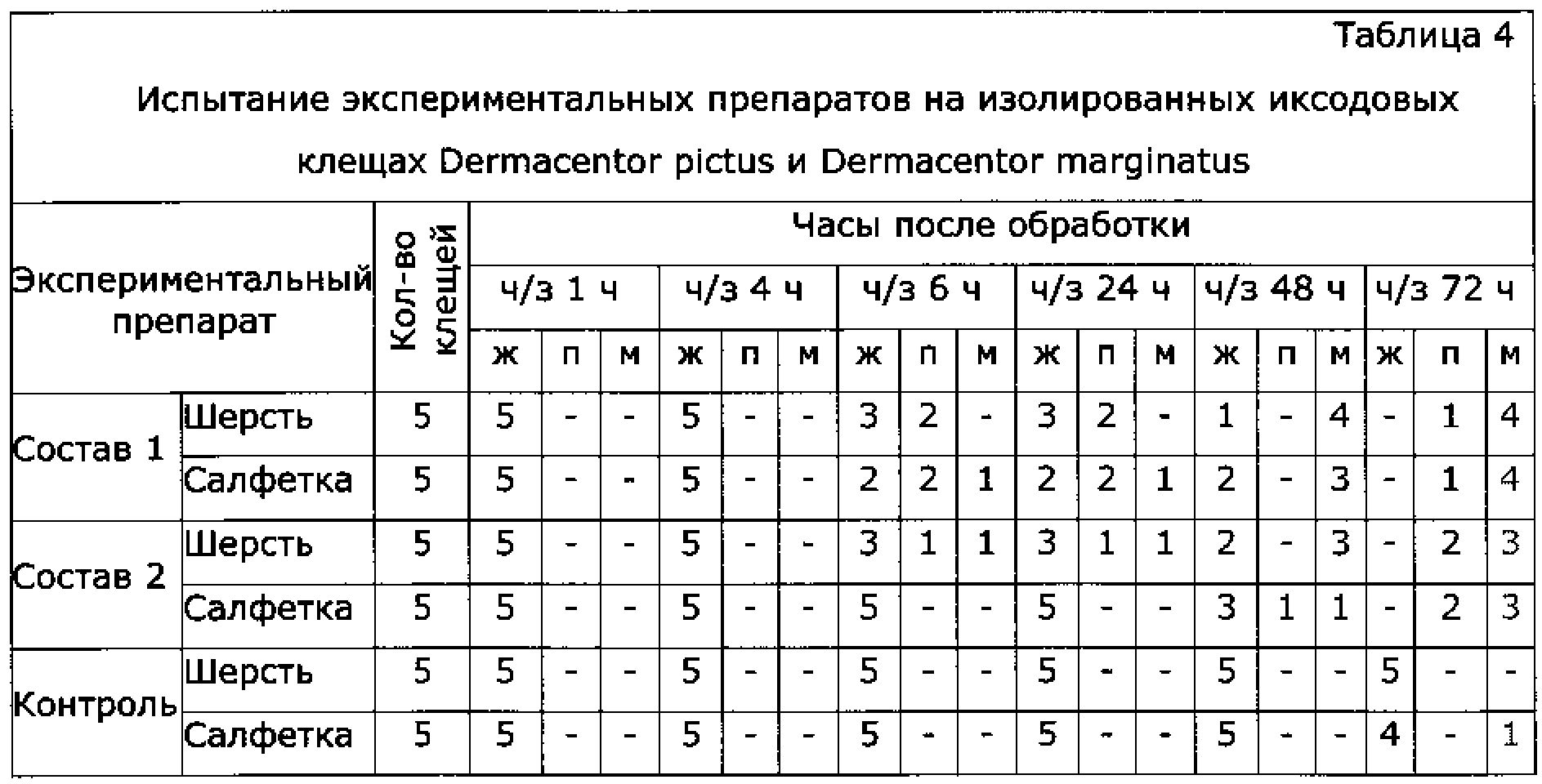
А) Тканевые салфетки размером 12×12 см обрабатывали экспериментальными препаратами путем опрыскивания. Выдерживали 1 час. Обработанные салфетки помещали на дно чашки Петри, куда подсаживали по 5 экземпляров голодных особей (самцов и самок) Dermacentor pictus, Dermacentor marginatus. Аналогично поступали с контролем (n=5), помещая клещей на необработанную салфетку. Те же манипуляции проделывали со стриженой шерстью собаки. Акарицидное действие проверяли методом наблюдения через 1, 4, 6, 24, 48, 72 часа с учетом количества мертвых, парализованных и живых клещей.
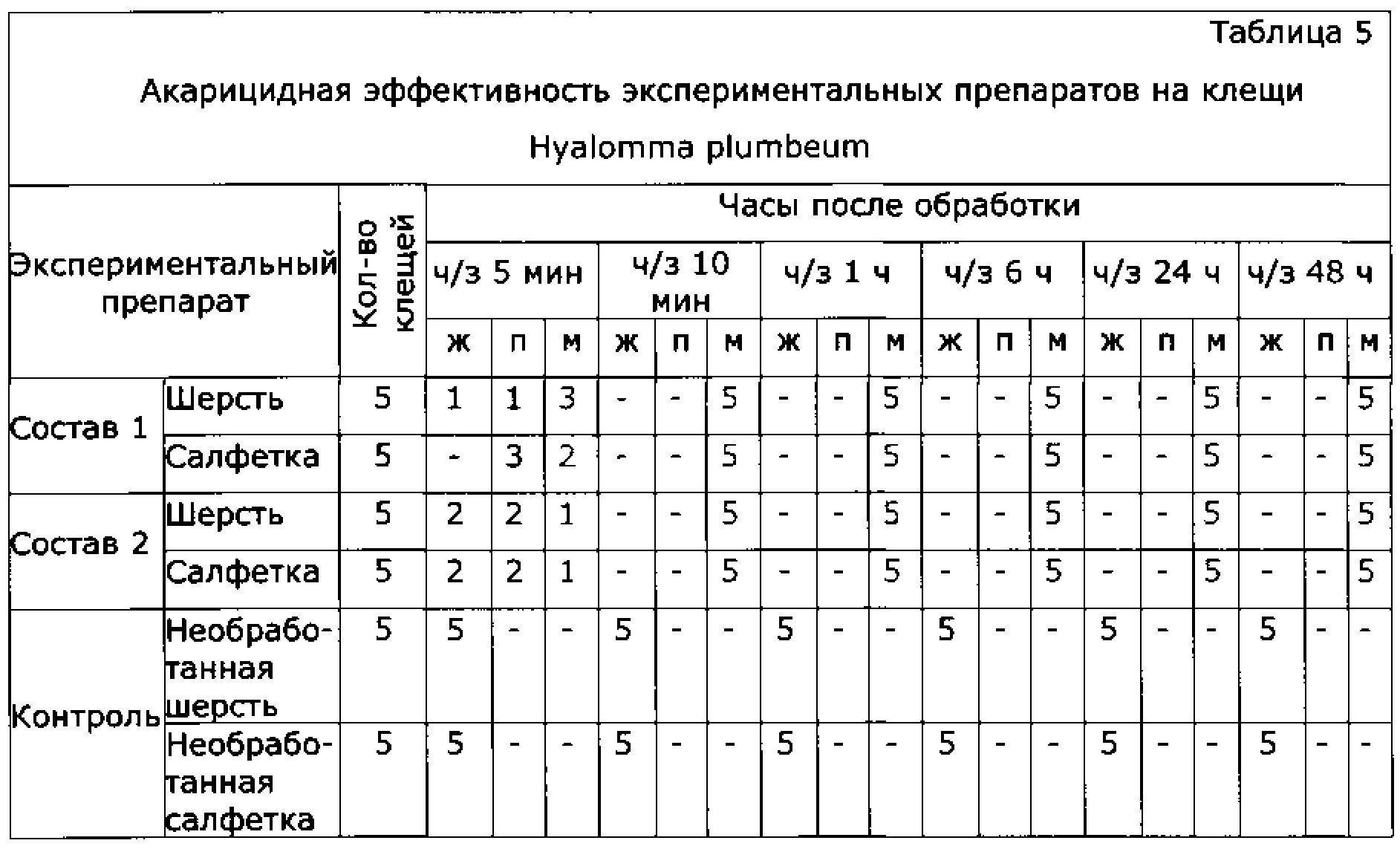
Б) Опыт проводили аналогично опыту А, но салфетки и шерсть не выдерживали в течение 1 часа перед высаживанием клещей. В каждую чашку подсаживали по 5 экземпляров голодных особей (самцов и самок) Hyalomma plumbeum. Аналогично поступали с контролем (n=5), помещая клещей на необработанный материал. Акарицидное действие проверяли методом наблюдения через 5,10 мин, 1, 6, 24, 48 часов с учетом количества мертвых, парализованных и живых клещей.
Выводы
А) N,N′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидин обладает акарицидной активностью. По результатам исследований при обработке составом 1 (N,N′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидин) гибель клещей наступила в 80% случаев, а при обработке составом 2 (амитраз) - в 60% случаев (см. Таблицу 4).
Б) Клещи, помещенные в центры чашек Петри, начинали инстинктивно искать тень в шерсти, которая не отпугивала их, они закапывались и ползали по ней, что говорит о низком репеллентном эффекте исследуемых препаратов. Клещи, помещенные на салфетки, уже в течение первых 2-х минут теряли активность. В обоих случаях гибель всех подопытных наступала через 10-15 минут (см. Таблицу 5).
Пример 4. (Исследование акарицидной активности N,N′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидина, влияние на чесоточных клещей)
Материалы и методы
Опыты проводили на базе СПК «Кобраловский» (Ленинградская область, Гатчинский район). Для проведения опытов были отобраны 14 коров в возрасте от 3-х до 7-и лет с клиническими признаками хориоптоза. Болезнь проявлялась струпом в области корня хвоста и выменного зеркала. Хориоптозные колонии в длину достигали 15 см (см. Фиг. 1; 4). В соскобах, взятых с мест поражения, были обнаружены клещи Chorioptes bovis на всех стадиях развития.
Исследовали 2 вида геля:
Состав 1, масс.%:
|
Состав 2, масс.%:
|
Животных разделили на 2 группы:
группа - обработка гелем Состава 1 (7 животных);
группа - обработка гелем Состава 2 (7 животных).
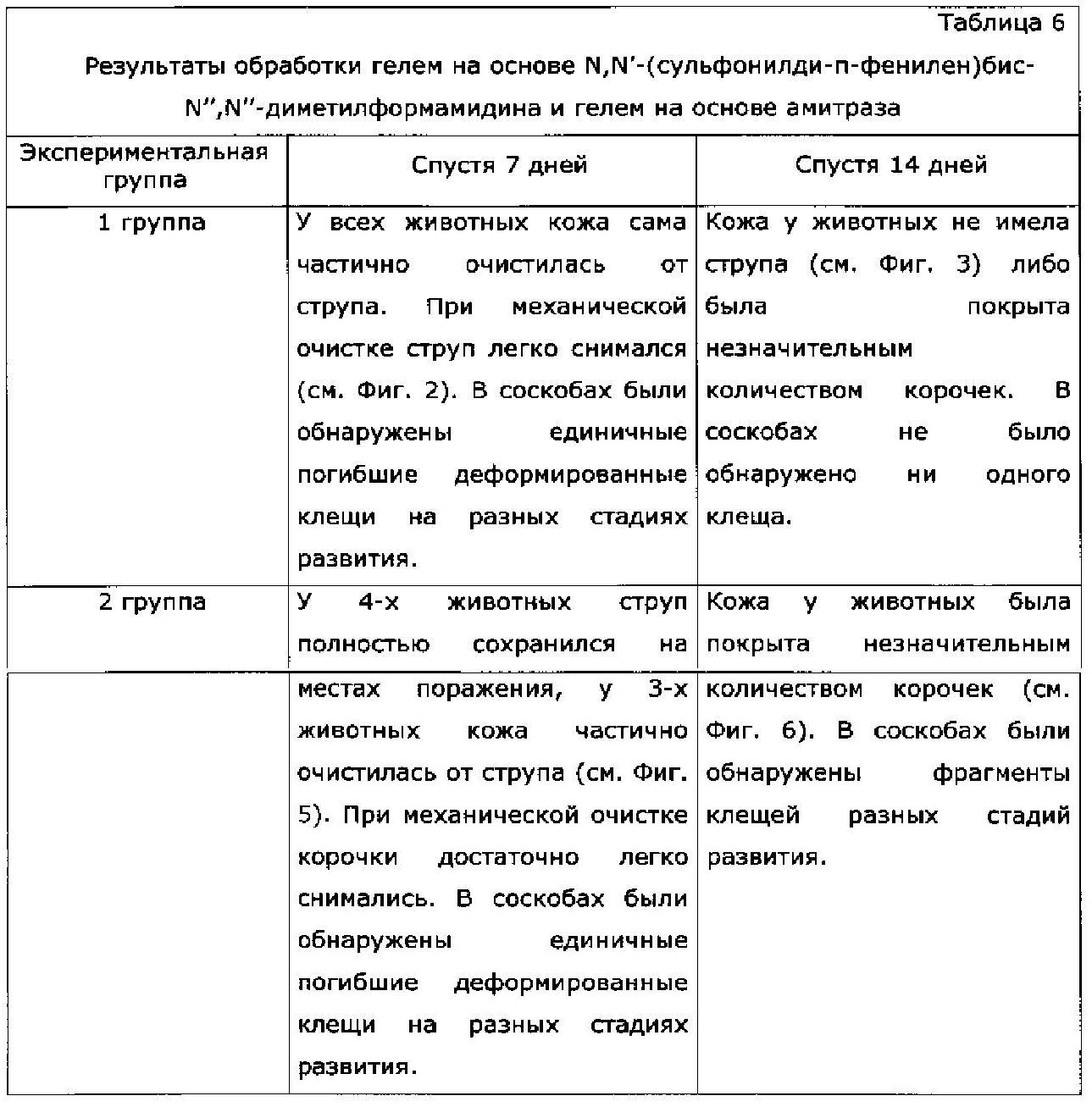
Обработки проводили один раз в неделю в течение двух недель путем втирания гелей на пораженных участках кожи. Результат учитывался спустя 7 и 14 дней после первой обработки визуально и путем взятия соскоба.
Выводы
Установлено, что очищение кожи при обработке гелем на основе N,N′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидина происходит интенсивнее, чем при обработке гелем на основе амитраза (см. Таблицу 6).
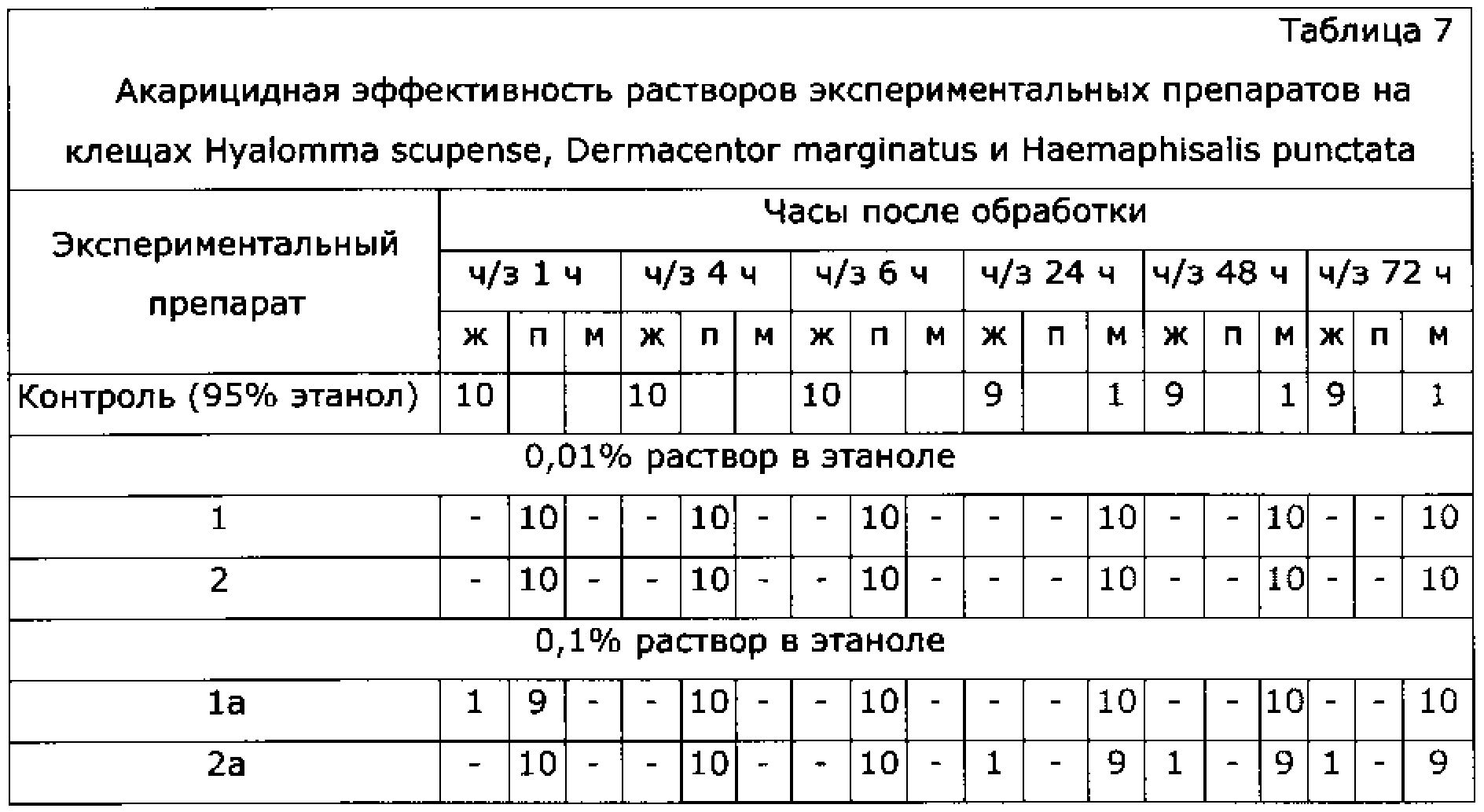
Пример 5. (Исследование акарицидной эффективности этанольного раствора N,N′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидина на иксодовых клещах)
Материалы и методы
Испытуемые растворы
Раствор 1 - 0,01% раствор N,N′-(сульфонилди-п-фенилен)бис-N″,N′-диметилформамидина в 95% этаноле
Раствор 2 - 0,01% раствор амитраза в 95% этаноле
Раствор 1a - 0,1% раствор N,N′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидина в 95% этаноле
Раствор 2a - 0,1% раствор амитраза в 95% этаноле
Опыт (in vitro) проводили на изолированных клещах Dermacentor pictus, Dermacentor marginatus, Hyalomma plumbeum. Для этого 10 экземпляров голодных имаго помещали на тканевые (бязевые или сатиновые) салфетки размером 12×12 см, завязывали ниткой и на 1 мин погружали в испытуемый раствор. Затем помещали в чашки Петри и в термостат при температуре 27-30°C и влажности 95%. Аналогично поступали с контролем, погружая такое же количество клещей в 95%-ный этанол.
Акарицидное действие проверяли методом наблюдения через 1, 4, 6, 24, 48, 72 часа с учетом количества мертвых, парализованных и живых.
Выводы
Все подопытные клещи уже через час утратили способность передвигаться, через сутки погибли, что говорит о высоком акарицидном эффекте исследуемых препаратов. 0,1% раствор N,N′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидина в этаноле обладает большим акарицидным эффектом нежели аналогичный раствор амитраза (при использовании раствора амитраза один из 10 клещей сохранил активную жизнедеятельность) (см. Таблицу 7).
Пример 6. (Исследование действия N,N′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидина на фитопатогенных клещей)
Материалы и методы
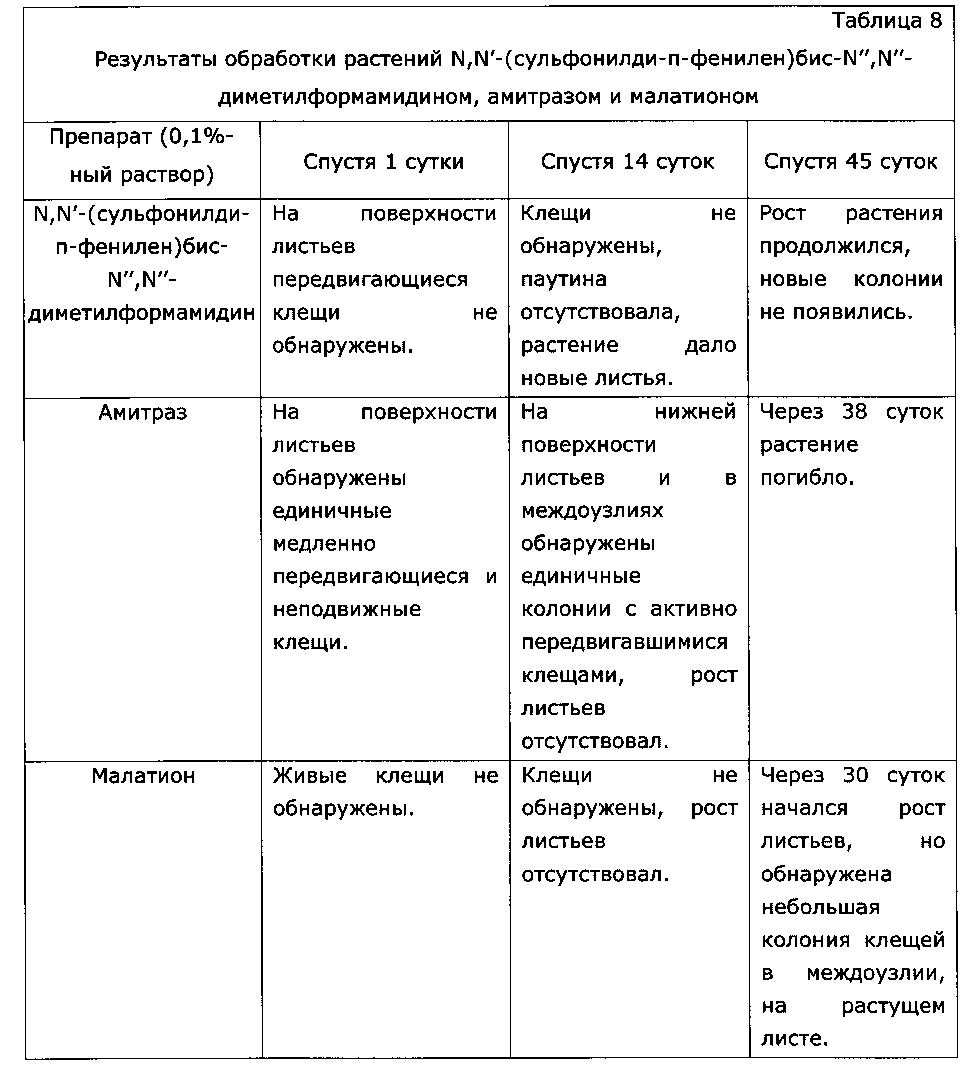
Обрабатывали три растения Fatsia japonica примерно одинаковых размеров, сильно инвазированных клещами Tetranychus cinnabarinus. Листья растений были бледно-желтые с пятнами некроза, с нижней стороны покрытые сплошным слоем паутины, в которой активно передвигались клещи, на 1 см2 находились от 5 до 20 особей. В качестве акарицидов использовали 2%-ные спиртовые растворы N,N′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидина, амитраза и малатиона, которые перед обработкой разбавляли водой до концентрации 0,1%. Каждое растение обрабатывали при помощи аэрозольного распылителя (по 100 мл испытуемого раствора на растение). Состояние растений оценивали через 1 сутки, 14 суток, 45 суток после обработки.
Результаты представлены в Таблице 8.
Выводы
N,N′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидин обеспечил эффективную и длительную защиту растений от фитопатогенных клещей, фитотоксичность его не обнаружена.
Умеренный эффект амитраза, по всей видимости, связан с быстрой дезактивацией во влажной среде, в т.ч. на поверхности листьев. Заявляемое соединение N,N′-(сульфонилди-п-фенилен)бис-N″,N″-диметилформамидин в этих условиях устойчиво и обеспечивает длительный защитный эффект (спустя 45 суток акарицидное действие не прекратилось).