Результат интеллектуальной деятельности: СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ ХЛОРИСТОГО КАЛЬЦИЯ И УГЛЕКИСЛОГО ГАЗА
Вид РИД
Изобретение
Изобретение относится к области производства хлористого кальция и углекислого газа для производства карбоната натрия, которые находят широкое применение в химической, нефтедобывающей и химико-фармацевтической отраслях промышленности, конкретно в производствах хлористого бария, осушки газов, мыла и других моющих средств, при варке целлюлозы, для обработки бокситов в производстве алюминия и в качестве шихты в производстве стекла и т.д.
Известен способ получения хлористого кальция из дистиллерной жидкости содового производства в адиабатических испарителях (SU 842024, опубл. 30.06.1981).
Недостатками известного способа являются большие энергетические затраты, продукт содержит значительное количество хлористого натра, примесей и других металлов.
Известен способ получения хлористого кальция путем взаимодействия соляной кислоты с твердым карбонатом кальция в закрытом футерованном вертикальном цилиндрическом реакторе (FR 2446255, опубл. 08.08.1980).
Недостатками известного способа являются низкое качество готового продукта, отсутствие конкретных параметров процесса.
Наиболее близким по технической сущности к заявляемому способу получения хлористого кальция является способ получения хлористого кальция (RU 2291109, опубл. 10.01.2007), который включает взаимодействие кальцийсодержащего сырья с соляной кислотой при 20-50°С, к кальцийсодержащему сырью дозируют 20-37%-ную соляную кислоту при мольном соотношении СаСО3:HCl=1:2 с последующим пропусканием образовавшегося кислого раствора CaCl2 через СаСО3 и образовавшего кислого углекислого газа через СаСО3 и CaCl2, взятые в мольном соотношении 1-4:1.
Недостатком известного способа является низкая производительность по выработке как хлористого кальция, так и углекислого газа. Другими недостатками известного способа являются захлебывание реактора при подаче соляной кислоты снизу вверх, повышенное пенообразование и задержка выделения СО2.
Задачей настоящего изобретения является разработка способа совместного получения хлористого кальция и углекислого газа для производства карбоната натрия и технологической схемы, увеличение производительности технологического процесса, утилизация всех видов абгазной и технической соляных кислот, возможность использования всех разновидностей природного кальцийсодержащего сырья, кальцийсодержащих отходов и шламов, значительное сокращение выделения вредных веществ в атмосферу и сточные воды.
Вышеуказанный технический результат получения хлористого кальция (далее - CaCl2) и углекислого газа (далее - диоксид углерода, СО2) достигается тем, что кальцийсодержащее сырье (например, природное кальцийсодержащее сырье, выбранное из кальцита, арагонита), включающее карбонат кальция, подвергают взаимодействию с 20-36%-ной соляной кислотой (далее - HCl), подаваемой дозировано, с последующим пропусканием образовавшегося кислого раствора хлористого кальция CaCl2 через карбонат кальция СаСО3 и/или известняковую муку и образовавшегося углекислого газа через СаСО3 или известняковую муку и CaCl2, взятых в мольном соотношении 1:1-3 соответственно, взаимодействие осуществляют в течение 1,5-2,5 ч сначала при температуре 20-40°С с последующим повышением температуры до 55-70°С в двух и более реакторах с обогревом с перемешивающим устройством или без него. Мольное соотношение СаСО3:HCl берут равным 1:1,8-2,2, а взаимодействие возможно осуществляют в присутствии ингибитора кислотной коррозии. Подачу водных растворов соляной кислоты с концентрацией менее 25% или более 32% преимущественно осуществляют в нижнюю часть реакторов, а подачу водных растворов ингибированной соляной кислоты с концентрацией 25-32% - в верхнюю часть реакторов.
В качестве ингибиторов кислотной коррозии используют ингибиторы, полученные на основе полиаминов и хлористого бензила или на основе полиаминов (полипропиленполиаминов), карбоновых кислот и хлористого бензила или имидазолина, полученного реакцией полиаминов с монокарбоновыми кислотами с последующим взаимодействием его с хлористым бензилом в присутствии спирта или амидов кислот, полученных из полиаминов, олеиновой кислоты и хлористого бензила (RU 2350689, опубл. 27.03.2009, RU 2347853, опубл. 27.02.2009, RU 2357006, опубл. 27.05.2009, RU 2347852, опубл. 27.02.2009) в количестве 0,01-0,1% от массы карбоната кальция, содержащегося в кальцийсодержащем сырье.
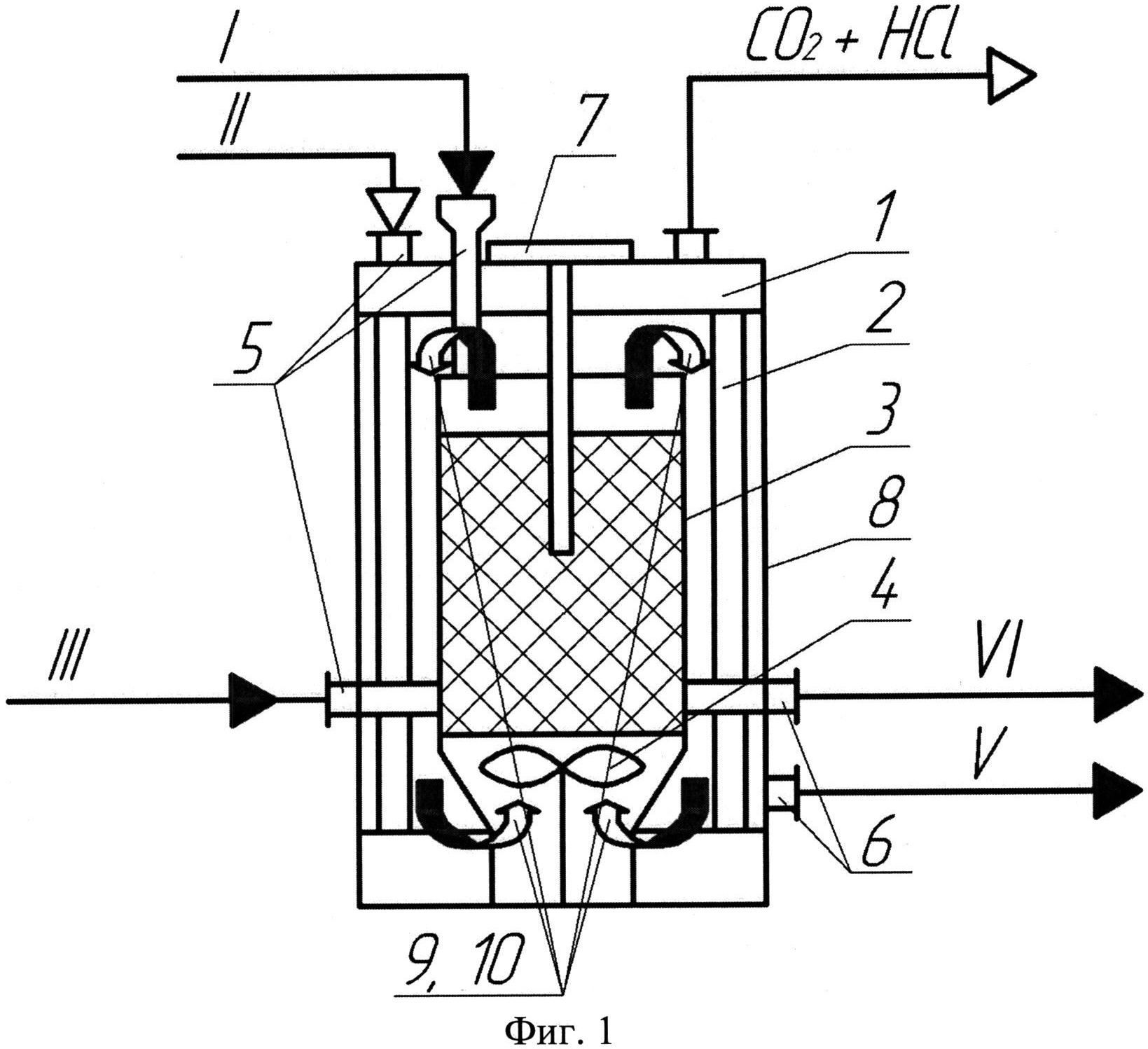
На фиг.1 изображена принципиальная схема реакторов 1 и 2, где:
12 - крышка; 13 - трубки обогрева; 14 - стакан; 15 - мешалка; 16 - штуцеры загрузки сырья; 17 - штуцеры для выгрузки; 18 - термопара; 19 - корпус; 20, 21 - направление потоков.
I - кальцийсодержащее сырье; II - раствор соляной кислоты ингибированной; III - слабоконцентрированная или концентрированная ингибированная соляная кислота; V - нерастворимый осадок; VI - CaCl2+Н2О+HCl.
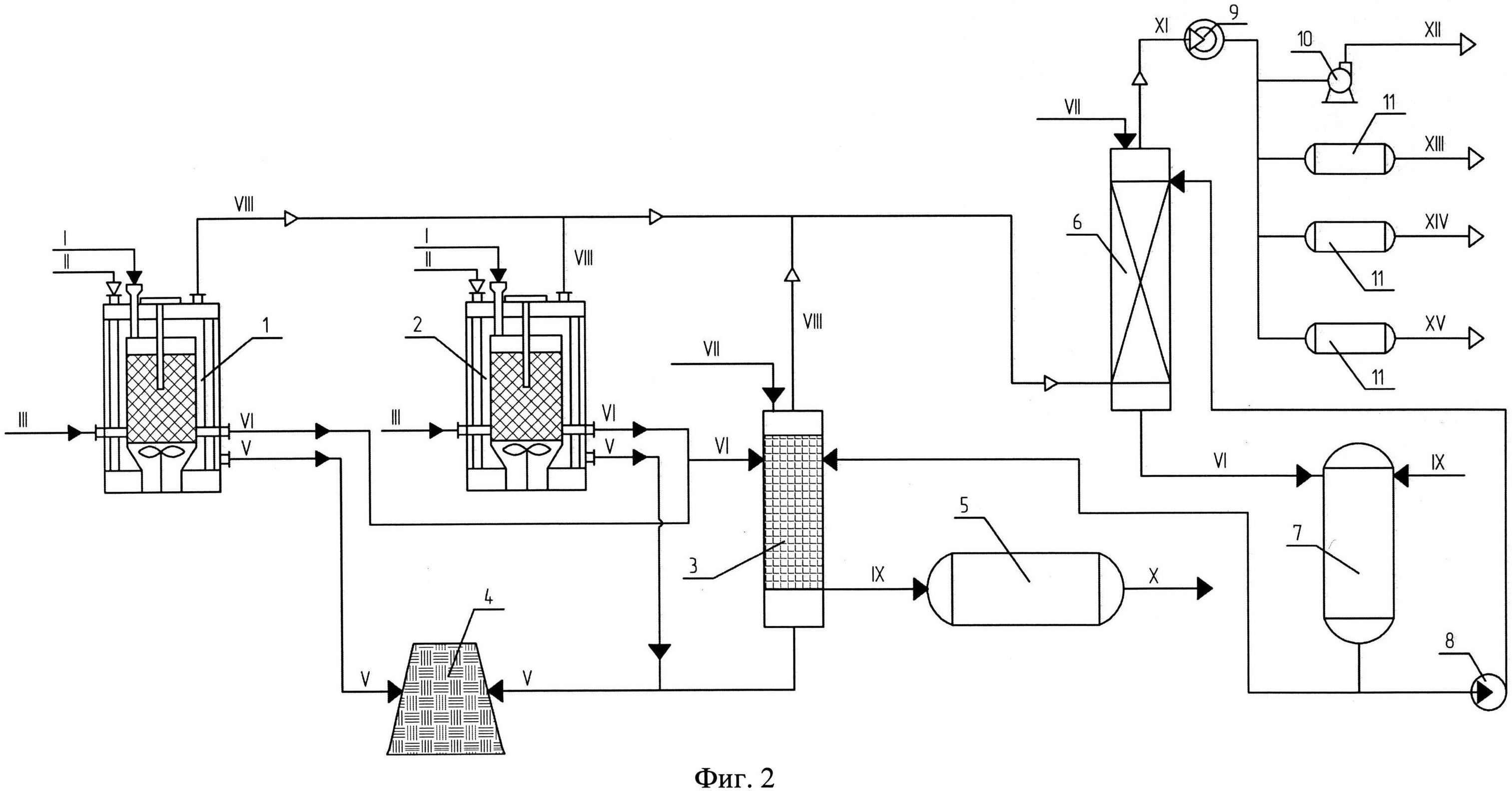
На фиг.2. изображена принципиальная схема получения хлористого кальция и углекислого газа, где:
1-3 - реакторы; 4 - сборник нерастворимого осадка; 5, 7 - емкость для CaCl2; 6 - колонна для очистки CO2; 8 - насос; 9 - каплеуловитель; 10 - вентилятор; 11 - осушитель с плавленым CaCl2 для сушки СО2.
I - природное кальцийсодержащее сырье, вторичное кальцийсодержащее сырье или кальцийсодержащие отходы; II - раствор соляной кислоты ингибированной; III - концентрированная или концентрированная ингибированная соляная кислота; V - нерастворимый осадок; VI - CaCl2+Н2О+HCl; VII - карбонат кальция или известняковая мука; VIII - СО2+HCl; IX - водный раствор CaCl2; Х - CaCl2 на выпарку, сушку или в гранулятор; XI - СО2; XII - СО2 в атмосферу; XIII - СО2 на производство кальцинированной соды; XIV - СО2 для производства карбоната натрия из каустической соды; XV - СО2 для производства мела.
Предложенный способ осуществляют взаимодействием кальцийсодержащего сырья (все разновидности природного известняка: кальцит, арагонит и т.д., известняковая мука, кальцийсодержащие отходы и шламы) с соляной кислотой в реакторах (1-3), внутри реакторов (1,2) вмонтирован стакан 14, в нижний части которого помещена решетка - сито (на чертеже не обозначена), предназначенная для удерживания твердых частиц карбоната кальция. В реактор 1 и 2 загружают сырье, в верхнюю часть реакторов дозируют соляную кислоту. При такой подаче реакция (температура 20-40°С) протекает гладко, и происходит образование хлористого кальция CaCl2 и выделение углекислого газа. По мере протекания реакции образовавшийся раствор CaCl2 постепенно перемещается вниз и сверху легко отводится СО2. Раствор CaCl2 стекает вниз, и при этом включается мешалка 15 (пропеллерная) и осуществляется нагрев до температуры 55-70°С. Образовавшийся водный раствор CaCl2 с небольшим содержанием HCl поступает из реакторов 1 и 2 в реактор колонного типа 3 (объем 5 л), заполненный карбонатом кальция (известняковой мукой), предназначенный для дополнительного получения хлористого кальция и диоксида углерода.
Очистка раствора хлористого кальция от остаточного содержания соляной кислоты в результате вторичной реакции карбоната кальция с соляной кислотой осуществляется в реакторе 3. При этом дополнительно образуются СО2 и хлористый кальций. Поток СО2 и HCl из реактора 3 соединяется с потоком СО2 и HCl из реакторов (1, 2) и поступает в колонну 6, заполненную карбонатом кальция (известняком или известняковой мукой) и раствором хлористого кальция (26-32%-ной концентрации) в соотношении 1:1-3 соответственно. В производстве кальцинированной соды (Na2CO2) диоксид углерода (СО2) получают разложением известняка на оксид кальция (СаО) и диоксид углерода в печах обжига при температуре 900-1200°С.
В природе существует несколько разновидностей известняка: самым распространенными являются арагонит и кальцит (исландский шпат).
Арагонит по своей структуре мягче, и его температура разложения - 900-1200°С, а кальцита температура разложения - 1600°С и более. На Стерлитамакском ОАО «Сода» имеется дробильно-сортировочная фабрика, где происходит дробление и разделение известняка (месторождение Шах-Тау ~ 6 км от Стерлитамакского ОАО «Сода»). Фракцию (50-150 мм) применяют для получения диоксида углерода в печах обжига (45-50% от общего объема известняка). Оставшаяся часть (50-55%) после рассева (кальцит) используется как щебенка при строительстве дорог и как сырье для цементного производства. При обжиге арагонита образуется диоксид углерода всего 37-39%-ной концентрации.
Предложенный метод дает качественный СО2 (концентрация его 95-98%) при 100%-ном использовании сырья.
Для защиты оборудования могут быть использованы ингибиторы кислотной коррозии, которые защищают металл (оборудование, аппаратуру, трубопроводы и т.д.), полученные на основе полиаминов и хлористого бензила (RU 2350689, опубл. 27.03.2009), на основе полиаминов (полипропиленполиаминов), карбоновых кислот и хлористого бензила (RU 2347853, опубл. 27.02.2009), на основе имидазолинов, полученных реакцией полиаминов с монокарбоновыми кислотами с последующим взаимодействием полученного имидазолина с хлористым в присутствии спирта (RU 2357006, опубл. 27.05.2009), на основе амидов кислот, полученных из полиаминов, олеиновой кислоты и хлористого бензила (RU 2347852, опубл. 27.02.2009) с защитным действием 98,5-99,8%.
При концентрации соляной кислоты 20% и ниже предусмотрена подача газообразного хлороводорода совместно с соляной кислотой для подкрепления получаемого слабого раствора хлористого кальция.
Способ поясняется следующими примерами.
Пример 1. В реакторы 1 и 2 (объем каждого реактора по 5 л), в нижней части которых помещены решетка-сито, предназначенная для удержания твердых частиц известняка, загружают через их верхнюю часть расчетное количество известняка, затем дозируют в верхнюю часть реакторов 30%-ный водный раствор HCl. Мольное соотношение СаСО3:HCl=1:2. Дозированная подача соляной кислоты обеспечивает сравнительно спокойное взаимодействие сырья с соляной кислотой. При бурном течении реакции СаСО3 с HCl подача кислоты временно прекращается, а при нормальном течении процесса подача кислоты возобновляется. Реакционную смесь нагревают сначала при температуре 20°С в течение 1 ч, затем при 55°С в течение 1,5 ч.
По окончании реакции СаСО3 с HCl поток жидкости (раствор CaCl2+H2O+HCl) стекает сверху стаканов реакторов 1, 2 вниз, после чего включают в работу мешалку 15 (400 об/мин) и обогрев реакторов до 55°С. При этом происходит усреднение растворов CaCl2 и интенсивное удаление остаточного количества СО2. Реакторы 1, 2 могут работать самостоятельно, разумеется этим обеспечивается не только непрерывный процесс получения CaCl2 и СО2, но при необходимости остановка на ремонт реактора. Каскад реакторов типа 1 и 2 может быть более двух в случае увеличения мощности производства CaCl2 и углекислого газа.
Поток раствора CaCl2 с небольшим содержанием соляной кислоты из реакторов 1 и 2 поступает в реактор 3 колонного типа, заполненный карбонатом кальция или известняковой мукой, где происходит реакция СаСО3 с остаточным количеством HCl, в результате чего дополнительно образуется CaCl2 и СО2 соответственно. В реакторе 3 скорость реакции СаСО3 с HCl ускоряется при применении известняковой муки, т.к. в потоке раствора CaCl2 содержится небольшое количество HCl и при использовании карбоната кальция (известняка) реакция замедляется.
Выделившийся диоксид углерода из реактора 3 соединяется с потоком СО2 из реакторов 1, 2, далее поступает в колонну 6 (санитарная колонна), заполненную карбонатом кальция и 32%-ным водным раствором CaCl2, взятыми в мольном соотношении 1:1 для гарантированной очистки СО2 от HCl.
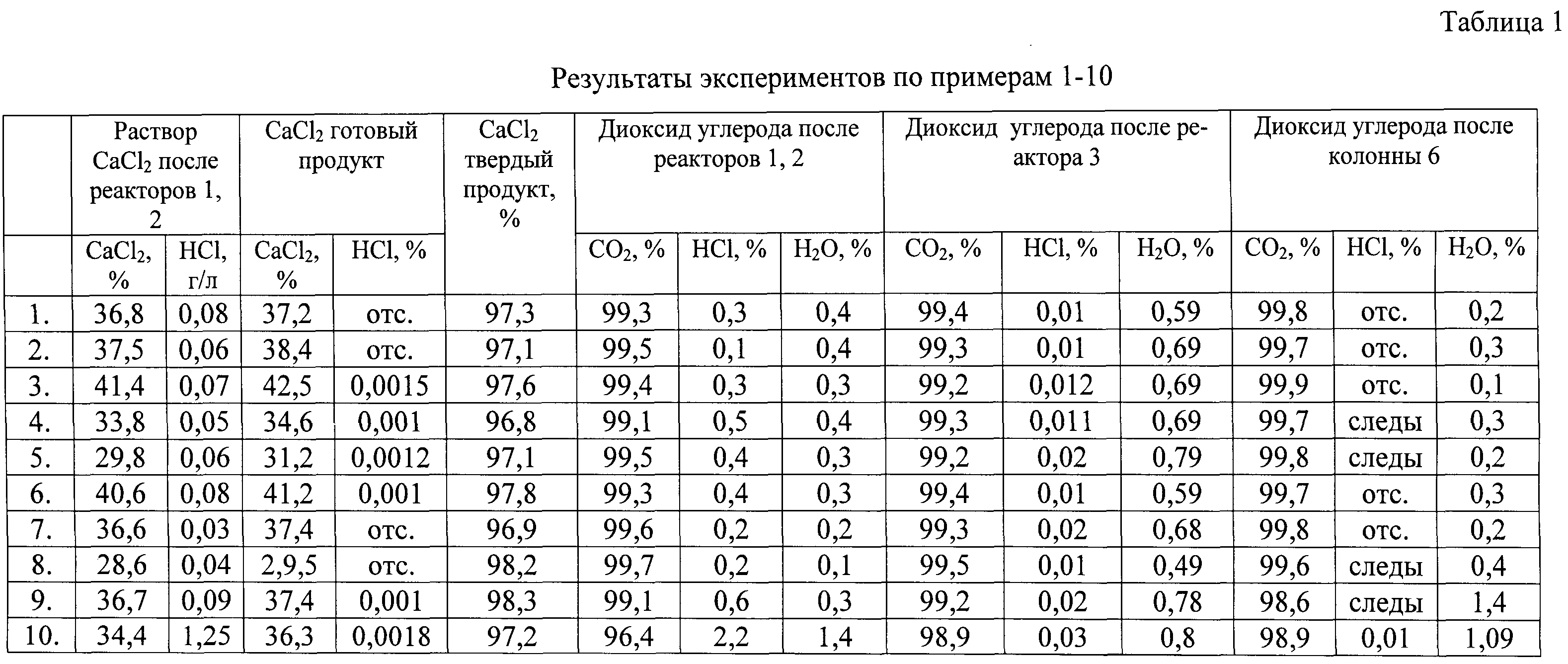
Результаты экспериментов приведены в табл.1.
Пример 2. В условиях примера 1 в реактор 1 и 2 загружают расчетные количества СаСО3, 0,01% от массы СаСО3 ингибитор кислотной коррозии, дозируют 31,5%-ную соляную кислоту в верхнюю часть реакторов 1 и 2 и после перелива раствора CaCl2 из стакана в реактор температуру реакционной смеси поднимают до 65-70°С и включают мешалку 15 (600 об/мин). При том усиливается выделение СО2 и производится отбор раствора CaCl2 из реакторов 1 и 2 в реактор 3. Время прохождения реакционной массы в реакторах 1 и 2 ~ 1,5-2,0 ч. После чего слабокислый раствор CaCl2 проходя через реактор 3, заполненный СаСО3 или известняковой мукой (для быстрого реагирования СаСО3 с HCl).
Для очистки СО2 от HCl в колонне 6 используют смесь СаСО3 и 26%-ный хлористый кальций CaCl2 в колонне в мольном соотношении СаСО3:CaCl2=1:2.
Результаты опытов приведены в табл.1.
Пример 3. В условиях примера 1 в реакторы 1 и 2 загружают сырье и 0,02% от массы СаСО3 ингибитор кислотной коррозии, дозируют 36%-ную соляную кислоту в нижнюю часть реакторов 1 и 2, включают мешалку (800 об/мин) и обогрев до 60-65°С. Время эксперимента 1,5 ч. Раствор CaCl2 из реакторов 1 и 2 поступает в реактор 3, заполненный известняковой мукой. Очистка CO2 происходит в колонне 6, заполненной в мольном соотношении СаСО3:CaCl2=1:3.
Результаты экспериментов приведены в табл.1.
Пример 4. В условиях примера 1 в реакторы 1 и 2 загружают расчетные количества сырья, ингибитор кислотной коррозии (0,015% от массы СаСО3), дозируют 27,5%-ную соляную кислоту. Время прохождения реакционной массы 1,5 ч, затем реакционная масса поступает в реактор 3, заполненный СаСО3, очистка углекислого газа осуществляется в колонне 6 (см. табл.1).
Пример 5. В условиях примера 1 в реакторы 1 и 2 загружают расчетное количество сырья, ингибитор кислотной коррозии (0,02% от массы СаСО3), мольное соотношение СаСО3:HCl=1:1,8, дозируют через верхнюю часть реакторов 25%-ный водный раствор соляной кислоты HCl. Включают обогрев реакторов 1 и 2, мешалку 15 (1000 об/мин) и нагревают реакционную смесь сначала при 40°С в течение 1 ч, затем при 70°С в течение 0,5 ч, при этом происходит обильное выделение СО2 без заметного пенообразования. Время реакции - 1,5 ч. После чего раствор CaCl2 с небольшим количеством HCl поступает в реактор 3, заполненный СаСО3, очистка СО2 осуществляется в колонне 6.
Результаты опытов приведены в табл.1.
Пример 6. В условиях примера 1 в реакторы 1 и 2 загружают известняк (кальцит, непригодный для производства кальцинированной соды), ингибитор кислотной коррозии (0,015% от массы СаСО3, содержащегося в известняке), дозируют 34%-ный водный раствор HCl в нижнюю часть реакторов 1 и 2, мольное соотношение СаСО3:HCl=1:2. При этом происходит небольшое пеновыделение, но дозирование соляной кислоты не прекращается. После включения обогрева реакционную смесь нагревают при 40°С в течение 1 ч, затем при 70°С в течение 1 ч. Время реакции 2 ч. После чего включают мешалку 15 (800 об/мин) и обогрев до 65-70°С. Раствор CaCl2+HCl (слабокислый) поступает в реактор 3, заполненный СаСО3 и известняковой мукой (1:1). Очистка СО2 осуществляется в колонне 6, заполненной СаСО3 и CaCl2 в мольном соотношении СаСО3:CaCl2=1:1,5 (см. табл.1).
Пример 7. В условиях примера 1 в реакторы 1 и 2 загружают расчетное количество сырья, ингибитор кислотной коррозии (0,01% от массы СаСО3 в сырье), дозируют 30%-ную соляную кислоту (мольное соотношение СаСО3:HCl=1:2,2) и по окончании реакции включают мешалку 15 (1000 об/мин) и обогрев до 65°С. Время реакции 1,5 ч. После чего слабокислый раствор CaCl2 поступает в реактор 3, заполненный СаСО3. Очистка СО2 осуществляется в колонне 6 (см. табл.1).
Пример 8. В условиях примера 1 в реакторы 1 и 2 загружают расчетное количество сырья, ингибитор коррозии (0,1% от массы СаСО3), дозируют 27%-ную соляную кислоту в верхнюю часть реакторов 1 и 2 (мольное соотношение СаСО3:HCl=1:2), включают мешалку 15 (1200 об/мин) и обогрев до 65°С. Время реакции 1,5 ч. Затем слабокислый раствор CaCl2 поступает в реактор 3, заполненный СаСО3.
Результаты приведены в табл.1.
Пример 9. В условиях примера 1 в реакторы 1 и 2 загружают расчетное количество кальцийсодержащего вторичного сырья (содержание СаСО3 - 88%), ингибитор кислотной коррозии (0,08% от массы СаСО3), дозируют 12%-ную соляную кислоту, включают мешалку 15 (1000 об/мин). Время реакции 8 ч. После чего слабокислый раствор поступает в реактор 3, заполненный СаСО3. Очистка CO2 осуществляется в колонне 6.
Результаты опытов приведены в табл.1
Пример 10. В условиях примера 1 в реакторы 1 и 2 загружают расчетное количество кальцийсодержащего сырья, ингибитор кислотной коррозии (1,0% от массы СаСО3), 36%-ную HCl без дозированной подачи (наблюдалось захлебывание реактора и после чего дальнейшую подачу соляной кислоты прекратили, затем перешли на дозированную подачу соляной кислоты). После реакционная смесь поступила в реактор 3. Очистка СО2 осуществляется в колонне 6.
Результаты экспериментов приведены в табл.1.
Примеры 1-8 при условии выдерживания параметров процесса дают высокий результат.
Примеры 9, 10 свидетельствуют о том, что отклонение от заявленных параметров процесса приводит к увеличению продолжительности процесса (8 ч) или к захлебыванию реакторов и т.д.
Описание технологической схемы получения хлористого кальция и углекислого газа (фиг.2).
В реакторы 1 и 2 сверху по линии I подают известняк или кальцийсодержащее вторичное сырье (отходы, шламы и т.д.).
В верхнюю часть реакторов 1 и 2 дозируют 25-32%-ные водные растворы HCl II. Для получения более концентрированных растворов CaCl2 или при использовании соляной кислоты менее 25%-ной концентрации предусмотрена подача ее в нижнюю часть реакторов 1 и 2, что имеет место также в случае более концентрированного раствора ингибированной кислоты (>32%-ной концентрации) III. Раствор CaCl2 VI, содержащий небольшое количество HCl и незначительное количество CO2, непрерывно поступает в реактор 3, заполненный СаСО3 и/или известняковой мукой VII. В реакторе 3 происходит нейтрализация остаточного содержания соляной кислоты:
СаСО3+2 HCl=CaCl2+СО2+Н2О.
В результате данной реакции происходит образование дополнительного количества CaCl2 и СО2. Нерастворимый осадок V - соединения кремния и механические примеси, содержащиеся в известняке, и которые могут найти применение в дорожном строительстве, выводятся из нижних частей реакторов 1-3 в сборник 4.
Для получения CaCl2 и СО2 используют соляную кислоту согласно СТП 6-01-08-105-96 «Кислота соляная из абгазов хлорорганических производств» 31,5% (высший сорт), 30,5% (первый сорт), 27,5% (второй сорт), а также концентрированную соляную кислоту с концентрацией 36%, абгазную и техническую соляные кислоты с концентрацией ниже 27,5%.
После ректора 3 раствор CaCl2 IX подают в емкость 5, после него раствор CaCl2 Х подают на выпарку и сушку, затем при необходимости - в гранулятор.
В табл.2 приведена зависимость концентрации хлористого кальция от концентрации исходной соляной кислоты.
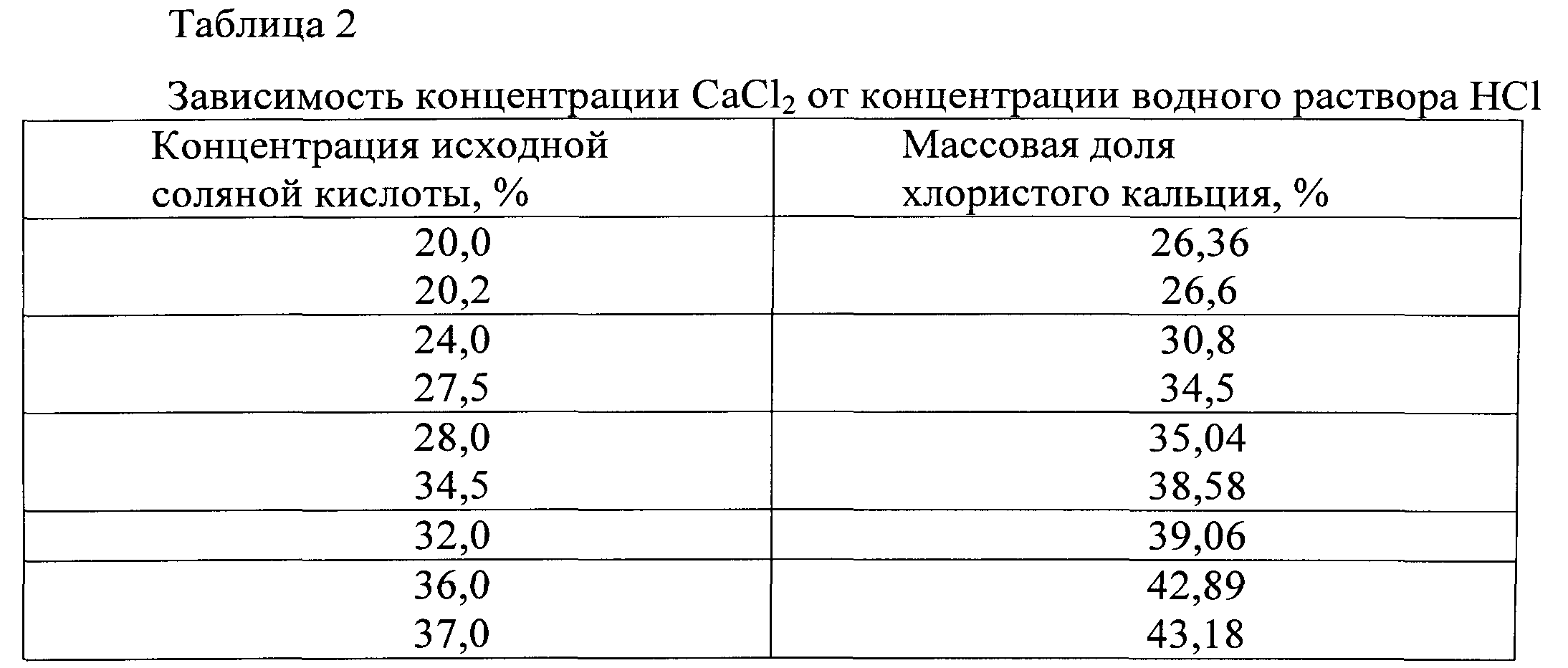
В табл.3 приведены требования СТП 6-01-08-105-96 на абгазную соляную кислоту.

Диоксид углерода VIII из реакторов 1-3 поступает в санитарную колонну 6, заполненную карбонатом кальция (известняком или известняковой мукой) и раствором CaCl2 (26-32%-ной концентрации) VII в мольном соотношении СаСО3:CaCl2=1:1-3 соответственно.
Хлористый кальций со следами HCl и СО2 VI из нижней части колонны 6 поступает в емкость 7 или в реактор 3.
Предусмотрена подпитка емкости 7 раствором CaCl2 IX. Очищенную двуокись углерода пропускают через каплеуловитель 9 и осушитель 11 с плавленым CaCl2.
Диоксид углерода может найти применение в производстве кальцинированной соды XIII по аммиачному методу, карбоната натрия из каустической соды XIV или химосажденного мела XV. В случае необходимости (аварийная остановка, ремонт технологических аппаратов и т.д.) диоксид углерода вентилятором 10 выбрасывается в атмосферу.