Результат интеллектуальной деятельности: (4-БРОМФЕНИЛ)ЭТИЛИДЕНГИДРАЗИД 2-[6-МЕТИЛ-1-(ТИЕТАН-3-ИЛ)УРАЦИЛ-3-ИЛ]УКСУСНОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЙ ГИПОТЕНЗИВНУЮ АКТИВНОСТЬ
Вид РИД
Изобретение
Изобретение относится к органической химии и медицине, а именно к смеси E- и Z-изомеров - (4-бромфенил)этилиденгидразида 2-[6-метил-1-(тиетан-3-ил)урацил-3-ил]уксусной кислоты, обладающей гипотензивной активностью.
Известными гипотензивными препаратами, которые широко применяются для лечения гипертензий, являются небиволол, лизиноприл и амлодипин [Машковский М.Д. Лекарственные средства. // М. ООО «Новая волна», 2004 - т.2, с.423, 416-417].
Небиволол - селективный блокатор β1-адренорецепторов с сосудорасширяющим действием. Противопоказаниями к приему препарата являются: синусовая брадикардия (менее 45-50 уд./мин), артериальная гипотензия, кардиогенный шок, синдром слабости синусного узла; AV блокада II-III степени, резистентная к терапии тяжелая сердечная недостаточность; нарушение периферического кровообращения, синоатриальная блокада, бронхиальная астма, бронхоспазм, нарушения функции печени, беременность, кормление грудью, детский возраст. Препарат имеет ограничение к применению при сахарном диабете (возможна маскировка признаков гипогликемии), гиперфункции щитовидной железы (вероятна тахикардия), склонности к брадикардии, отягощенном аллергологическом анамнезе, пожилом возрасте (старше 75 лет). Терапию небивололом рекомендуется прекращать постепенно (в течение 1-2 нед). Уменьшение дозы препарата необходимо при урежении ЧСС до 55 уд./мин. Препарат может усиливать реакции на пыльцу и другие аллергены. За 24 ч перед оперативным вмешательством с использованием общей анестезии (включая хирургическую стоматологию) небиволол следует отменить или выбрать анестезирующее средство с наименьшим отрицательным инотропным действием. Препарат необходимо применять с осторожностью во время работы водителям транспортных средств и людям, профессия которых связана с повышенной концентрацией внимания. При изучении небиволола в двухгодичном исследовании на мышах в дозе 40 мг/кг в сутки наблюдалось статистически значимое увеличение частоты развития гиперплазии тестикулярной ткани и аденомы яичка. FDA относит небиволол к категории C - изучение репродукции на животных выявило неблагоприятное действие на плод. При введении небиволола крысам на ранних сроках беременности в дозах 20-40 мг/кг в сутки у детенышей наблюдалось снижение массы тела, временная задержка окостенения грудины и ребер, повышение резорбции костей. Ведение небиволола кроликам в период беременности в дозе 20 мг/кг в сутки негативных эффектов на потомство не оказало. Было также показано, что небиволол и его метаболиты способны проникать через гематоплацентарный барьер. При введении небиволола самкам крыс на поздних сроках беременности, во время родов и в период лактации в дозах 1,25 мг/кг и 2,5 мг/кг в сутки отмечалось снижение массы тела у новорожденных детенышей. В дозах 5 мг/кг в сутки и выше небиволол вызывал у крыс случаи переношенной беременности, а также нарушение родовой деятельности и снижение заботы о потомстве, что сопровождалось повышением внутриутробной гибели плодов и мертворождением, рождением детенышей со сниженной массой тела и снижением выживаемости потомства. В связи с недостаточным количеством выживших детенышей оценить репродуктивную способность потомства не удалось. У крыс небиволол и его метаболиты способны экскретироваться с грудным молоком, однако неизвестно, экскретируется ли он с грудным молоком у человека. Тем не менее, учитывая потенциально возможные неблагоприятные эффекты β-блокаторов, которые могут возникнуть у новорожденного, в частности брадикардию, небиволол не рекомендован к применению у кормящих женщин [РЛС 2012].
Лизиноприл - ингибитор АПФ. Лизиноприл обладает рядом побочных действий на сердечно-сосудистую систему: снижение АД, аритмии, боль в груди, редко - ортостатическая гипотензия, тахикардия; нервную систему: головная боль, головокружения, сонливость, повышенная утомляемость, подергивание мышц конечностей и губ, редко - астения, лабильность настроения, спутанность сознания; пищеварительную систему: тошнота, диспепсия, снижение аппетита, изменение вкуса, боль в животе, диарея, сухость во рту; органы кроветворения: лейкопения, тромбоцитопения, нейтропения, агранулоцитоз, анемия (снижение гемоглобина, эритроцитопения). Возможно также возникновение аллергических реакций: ангионевротического отека, кожных высыпаний, зуда. Препарат влияет на лабораторные показатели, вызывая гиперкалиемию, гиперурикемию; редко - повышение активности ″печеночных″ трансаминаз, гипербилирубинемию. При применении лизиноприла также вероятно возникновение “сухого” кашля, снижение потенции; редко - острой почечной недостаточности, артралгии, миалгии, лихорадки, отеков языка, губ или конечностей, нарушение развития почек плода. В связи с побочными эффектами со стороны нервной системы необходимо с осторожностью применять лизиноприл людям, профессия которых связана с повышенной концентрацией внимания.
При применении лизиноприла необходима оценка соотношения риск-польза в случаях: цереброваскулярных заболеваний (в т.ч. недостаточность мозгового кровообращения), ИБС, коронарной недостаточности, при коллагенозах (в т.ч. системной красной волчанке, склеродермии), при угнетении костномозгового кроветворения, артериальной гипотензии, аортальном митральном стенозе или других обструктивных изменениях, затрудняющих отток крови из сердца; при гиперкалиемии или высоком риске ее возникновения (сахарный диабет, выраженная почечная недостаточность, одновременное назначение диуретиков), азотемии, гипонатриемии или ограничение натрия в диете. Осторожность требуется при применении лизиноприла у пациентов, имеющих двусторонний стеноз почечных артерий или стеноз артерии единственной почки, наличие пересаженной почки, первичный альдостеронизм, гиперурикемию, пожилой возраст и беременность [Инструкция по медицинскому применению препарата лизиноприл. Рег. номер: ЛС-000779].
Амлодипин - антагонист кальция II поколения, представляющий собой производное дигидропиридина. Побочные эффекты амлодипина достаточно хорошо известны и изучены в длительных клинических исследованиях (Osterloh, 1989, 1991; Circo и сотр., 1992; Hofling и сотр., 1991; Heynen 1992). Недостатками данного препарата являются отеки голеней и стоп. Вследствие вазодилатации происходит повышение капиллярного гидростатического давления, что способствует фильтрации жидкости в ткани; процессы ауторегуляции капиллярного кровотока и дренажа лимфы являются кальцийзависимыми и поэтому ингибируются антагонистами кальция. Побочные эффекты амлодипина со стороны сердечно-сосудистой системы и крови: гиперемия кожи лица, сердцебиение; редко - нарушения ритма (брадикардия, желудочковая тахикардия, трепетание предсердий), боль в грудной клетке; со стороны органов ЖКТ: запоры, тошнота, боль в животе; со стороны нервной системы и органов чувств: усталость, головная боль, головокружение, сонливость.
Амлодипин ограничивают к применению при сердечной недостаточности, нестабильной стенокардии, выраженном аортальном стенозе, нарушении функции печени и возрасте до 18 лет (не определены безопасность и эффективность применения). Применение препарата при беременности возможно, если ожидаемый эффект терапии превышает потенциальный риск для плода. По данным FDA амлодипин относится к категории C, то есть изучение репродукции на животных выявило неблагоприятное действие на плод, а адекватных и строго контролируемых исследований у беременных женщин не проводилось, однако потенциальная польза для беременной может оправдать его использование [Инструкция по медицинскому применению препарата «Амлодипин», Рег. номер: ЛСР-004932/07 от 17.12.2007 г.].
В патенте SU №1672929, 1991 г. «Способ получения производных гидразина или их фармацевтически совместимых солей» представлены соединения общей формулы:
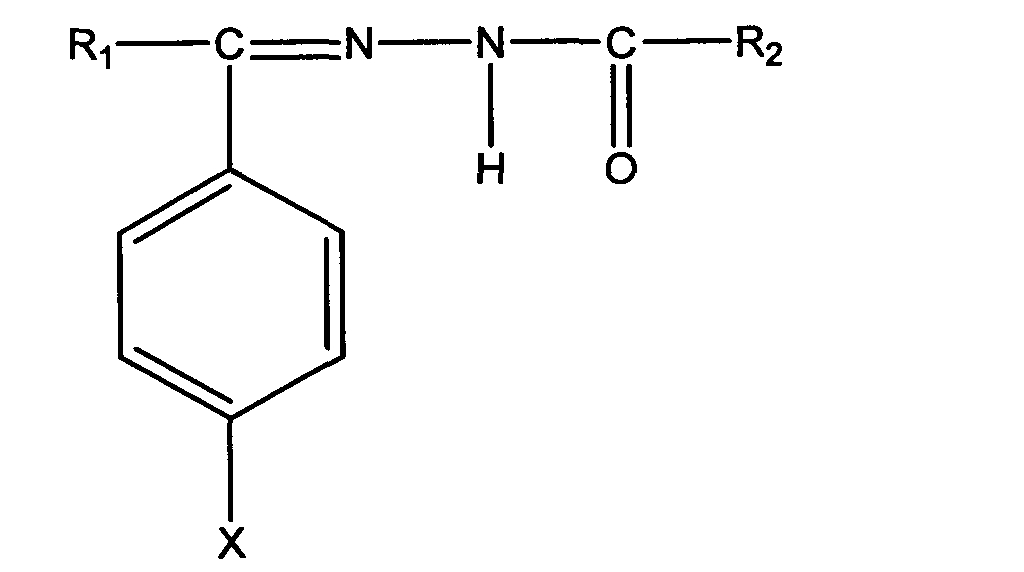
где: X - о-Cl или м-Br,
Из данных соединений 1-(2-оксиизобутироил)-2-(1-о-хлорфенил-1-этилиден)гидразин снижает артериальное давление самопроизвольно гипертонической крысы SHR.
Наиболее близким аналогом изобретения является препарат урапидил-6-[[3-[4-(2-метоксифенил)-1-пиперазинил]пропил]-амино]-1,3-диметил-урацил. Урапидил - антигипертензивный препарат, обладающий центральным и периферическим действием. Блокирует постсинаптические α1-адренорецепторы, благодаря чему снижается общее периферическое сосудистое сопротивление. Регулирует центральный механизм поддержания сосудистого тонуса за счет стимуляции серотониновых 5-HT1A-рецепторов сосудодвигательного центра (предотвращает рефлекторное увеличение тонуса симпатической нервной системы). Обычно указанный препарат применяют для снижения артериального давления при гипертонических кризах [Патент US 4131678 A от 09.02.77].
Задачей изобретения является расширение арсенала биологически активных веществ, в том числе обладающих гипотензивной активностью.
Технический результат - получение биологически активного вещества, проявляющего гипотензивную активность.
Сущность изобретения: смесь E- и Z-изомеров (4-бромфенил)этилиденгидразида 2-[6-метил-1-(тиетан-3-ил)урацил-3-ил]уксусной кислоты в мольном соотношении 3,5:1 общей формулы (I):
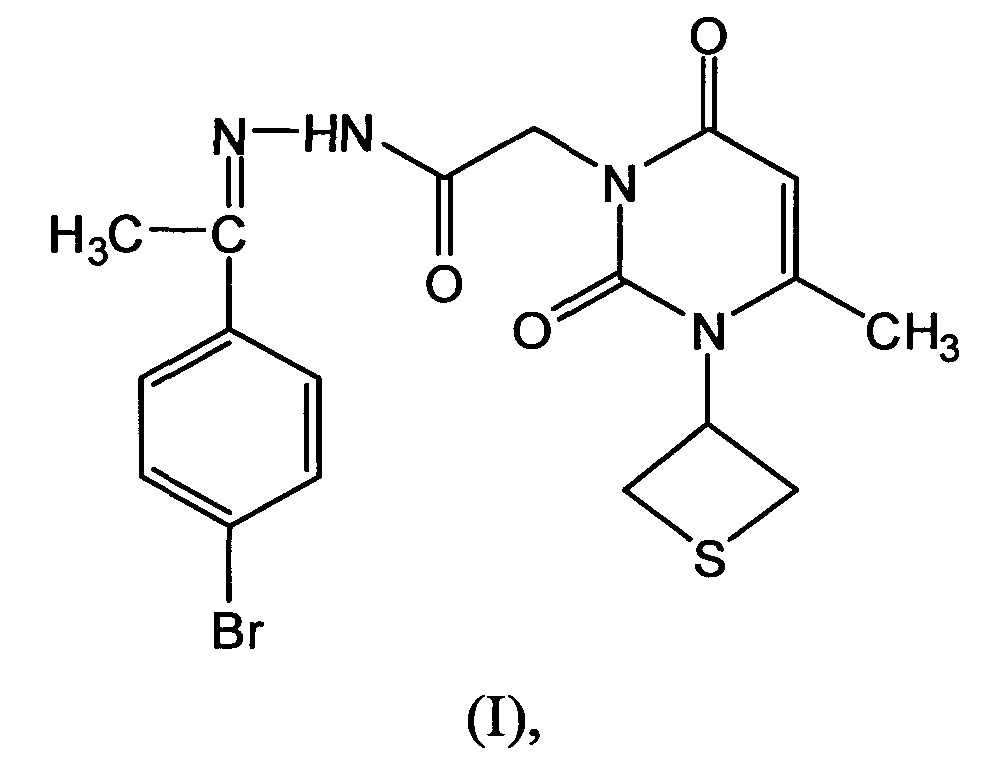
проявляющая гипотензивную активность.
Указанное соединение и его свойства в литературе не описаны.
Заявляемое соединение синтезируют следующим образом.
Взаимодействием 6-метил-1-(тиетан-3-ил)урацила с этиловым эфиром монохлоруксусной кислоты в присутствии карбоната калия получают этиловый эфир 2-[6-метил-1-(тиетан-3-ил)урацил-3-ил]уксусной кислоты, который вступает в реакцию с гидразингидратом, образуя гидразид 2-[6-метил-1-(тиетан-3-ил)урацил-3-ил]уксусной кислоты. Полученный гидразид 2-[6-метил-1-(тиетан-3-ил)урацил-3-ил]уксусной кислоты конденсируется с 4-бромацетофеноном, образуя смесь изомеров (4-бромфенил)этилиденгидразида 2-[6-метил-1-(тиетан-3-ил)урацил-3-ил]уксусной кислоты.
Пример 1. Синтез заявляемого соединения.
6-Метил-1-(тиетан-3-ил)урацил синтезируют по методике, описанной в работах [Катаев В.А., Мещерякова С.А., Лазарев В.В., Кузнецов В.В. // Синтез тиетанилзамещенных пиримидин-2,4(1Н,3Н)-дионов. - Журн. оранич. химии - 2013. - Т.49. Вып.5. - с.760-762; патент RU 2485118 от 20.06.2013 г.]
Суспензию 4,0 г (20 ммоль) 6-метил-1-(тиетан-3-ил)урацила и 4,14 г (30 ммоль) прокаленного измельченного карбоната калия в 125 мл ацетона кипятят на колбонагревателе в течение 30 минут, добавляют 3,68 г (30 ммоль) этилового эфира монохлоруксусной кислоты и продолжают кипячение еще 7 часов. Реакционную массу охлаждают, осадок отфильтровывают, промывают на фильтре ацетоном. Фильтрат упаривают при пониженном давлении досуха. Сухой остаток растворяют в 55 мл этанола, добавляют 4,7 г 85%-ного раствора гидразингидрата и кипятят 3 часа. Охлаждают при 0°C в течение 12 часов, осадок отфильтровывают, промывают водой, сушат. Получают 2,29 г (53%) смеси Z- и E-изомеров гидразида 2-[6-метил-1-(тиетан-3-ил)урацил-3-ил]уксусной кислоты в мольном соотношении 7:1, очищают кристаллизацией из этанола. Тпл. = 199-201°C.
ИК спектр, ν, см-1: 3365-3215 (N-H), 1692, 1654,1631 (C=O, C=C), 1439, 1385 (C-N).
Спектр ЯМР 1H (500 МГц, ДМСО-d6), δ, м.д.:
2,14 (с, 3H, 6-СН3);
3,07-3,11 [м, 2H, S(CH)2]; 4,15-4,19 [м, 2H, S(CH)2];
4,29 (с, 2H, NH2, Z); 4,54 (с, 2H, NH2, E);
4,42 (с, 2H, 3-CH2, Z); 4,79 (с, 2H, 3-CH2, E);
5,66 (с, 1H, 5-H);
6,03-6,07 (м, 1H, NCH);
8,77 (уш.с, 1H, NH, E), 9,36 (уш.с, 1H, NH, Z).
Элементный анализ.
Найдено, %: C 44,44; H 5,19; N 20,74 - C10H14N4O3S.
Вычислено, %: C 44,71; H 5,11; N 20,89.
К раствору 2,16 г (8 ммоль) гидразида 2-[6-метил-1-(тиетан-3-ил)урацил-3-ил]уксусной кислоты в 15 мл этанола прибавляют 1,91 г (9,6 ммоль) 4-бромацетофенона, смесь кипятят 4 часа, охлаждают. Выпавший осадок отфильтровывают, промывают этанолом, сушат. Получают 2,96 г (82%) смеси E- и Z-изомеров (4-бромфенил)этилиденгидразида 2-[6-метил-1-(тиетан-3-ил)урацил-3-ил]уксусной кислоты в мольном соотношении 3,5:1, очищают кристаллизацией из н-бутанола. Тпл. = 251-253°C.
ИК спектр, ν, см-1: 3198 (N-H), 1718, 1661,1626 (C=O, С=N, C=C), 1434, 1399 (C-N).
Спектр ЯМР 1H (500 МГц, ДМСО-d6), δ, м.д.:
2,14 (с, 3Н, 6-СН3);
2,25 (с, 3H, N=C-CH3, E); 2,29 (с, 3H, N=C-CH3, Z);
3,08-3,11 [м, 2H, S(CH)2]; 4,14-4,17 [м, 2H, S(CH)2];
4,69 (с, 2H, 3-CH2, Z); 5,04 (с, 2H, 3-CH2, E);
5,68 (с, 1H, 5-Н);
6,02-6,09 (м, 1H, NCH);
7,61 (д, 2H, Н аром, J 4,3 Гц), 7,77 (д, 2Н, Н аром, J 4,3 Гц)
10,84 (уш.с, 1H, NH, Z), 11,09 (уш.с, 1H, NH, E).
Спектр ЯМР 13C (300 МГц, ДМСО-d6), δ, м.д.: 13,55 (N=C-СН3); 19,15 (6-CH3); 31,47 [S(CH2)2)]; 46,16 (3-CH2); 47,01 (NCH); 100,24 (С5); 122,80 (С4 аром); 128,25 (С2,6 аром); 131,32 (С3,5 аром); 137,06 (С1 аром); 148,02 (N=С-CH3); 151,68 (С6); 153,95 (С2); 161,23 (С4); 169,32 (3-CH2-C=O).
Количественный состав обоих изомеров определен путем сравнения интегральных интенсивностей сигналов соответствующих протонов E-(4-бромфенил)этилиденгидразида 2-[6-метил-1-(тиетан-3-ил)урацил-3-ил]уксусной кислоты и Z-(4-бромфенил)этилиденгидразида 2-[6-метил-1-(тиетан-3-ил)урацил-3-ил]уксусной кислоты, подтверждающих мольное соотношение 3,5:1.
Элементный анализ.
Найдено, %: C 39,91; H 4,21; N 12,42 - C18H19BrN4O3S.
Вычислено, %: C 40,09; H 4,29; N 12,56.
Заявляемое соединение представляет собой светло-желтый кристаллический порошок, нерастворимый в воде, этаноле, эфире, растворимый в диметилформамиде, диметилсульфоксиде.
Пример 2. Изучение гипотензивного действия смеси E- и Z-изомеров - (4-бромфенил)этилиденгидразида 2-[6-метил-1-(тиетан-3-ил)урацил-3-ил]уксусной кислоты в мольном соотношении 3,5:1 при внутривенном введении с использованием методики неинвазивного измерения артериального давления у бодрствующих крыс.
Оценка гипотензивного действия осуществлена по методике, являющейся базисной моделью исследования веществ с гипотензивным действием [Руководство по проведению доклинических исследований лекарственных средств. Часть первая. - М.: Гриф и К, 2012. - 944 с.].
Для изучения влияния заявляемого соединения I на систолическое артериальное давление (САД) и частоту сердечных сокращений (ЧСС) были сформированы 2 группы из крыс-самок массой 280-320 г (по 6 животных в каждой). Исследуемое соединение растворяли в 50% растворе диметилсульфоксида (ДМСО) и вводили в хвостовую вену в дозе 15 мг/кг. Контрольной группе животных вводили 50% раствор ДМСО в эквивалентном объеме. Показатели САД и ЧСС регистрировали через 30, 60 и 90 минут после введения исследуемого соединения с хвоста животного при помощи прибора неинвазивного измерения артериального давления - ПТС 29 (IITC Life Science Inc., США). За исходный уровень принимали значения САД и ЧСС, зафиксированные до введения исследуемых соединений. Для подготовки к неинвазивному измерению АД животных предварительно приучали к нахождению в пластиковых пеналах-держателях, для этого их в течение трех дней помещали в пеналы-держатели на 1 час для ознакомления с окружающей обстановкой. Метод измерения АД заключался в помещении бодрствующего животного в пенал-держатель, на хвост животного надевали манжету с интегрированным фотосенсером, в которую нагнетали воздух (на 10-15 мм рт.ст. выше предполагаемого АД) и затем медленно стравливали, при этом показатели САД и ЧСС автоматически фиксировались прибором.
Установлено, что при внутривенном введении в дозе 15 мг/кг заявляемое соединение I оказывает выраженное гипотензивное действие (таблица 1) и вызывает урежение ЧСС (таблица 2).
Пример 3. Изучение зависимости «доза-гипотензивный эффект» и длительности действия заявляемого соединения I при пероральном введении с помощью методики неинвазивного измерения артериального давления у бодрствующих крыс в сравнении с эталонными препаратами.
Влияние заявляемого соединения I на САД и ЧСС изучали на бодрствующих крысах-самках массой 280-320 г (по 6 животных в каждой группе). Исследуемое соединение суспензировали в 2% крахмальной слизи и вводили перорально внутрижелудочно в дозах: 15 мг/кг, 30 мг/кг и 60 мг/кг. В качестве препаратов сравнения использовали небиволол (небилет, Berlin-Chemie AG, Германия) в дозе 2 мг/кг, лизиноприл (диротон, «Гедеон-Рихтер», Венгрия) в дозе 10 мг/кг и амлодипин (нормодипин, «Гедеон-Рихтер», Венгрия) в дозе 1 мг/кг. Контрольная группа животных получала 2% крахмальную слизь в эквивалентном объеме. Показатели САД и ЧСС регистрировали через час после введения исследуемого соединения с хвоста животного с интервалом в 1 час в течение 8 часов и через 24 часа. За исходный уровень принимали значения САД и ЧСС, зафиксированные до введения исследуемых соединений. Методика измерения артериального давления описана в примере 2.
В результате проведенного исследования установлено, что заявляемое соединение I оказывает наиболее выраженный гипотензивный эффект в дозе 30 мг/кг (таблица 3), схожий с таковыми у препаратов сравнения.
Выполненное исследование свидетельствует о том, что заявляемое соединение I обладает выраженной гипотензивной активностью. В экспериментальных исследованиях на животных эффект препарата наблюдается при его пероральном введении в дозе 30 мг/кг. По гипотензивной активности заявляемое соединение I не уступает препаратам сравнения. Заявляемое соединение I представляет интерес для дальнейшего изучения его гипотензивной активности и разработки на его основе гипотензивного препарата.
Пример 4. Изучение профилактического антигипертензивного действия заявляемого соединения I на модели стрессорной гипертонии при пероральном введении.
Для моделирования гипертонии, вызванной хроническим стрессом, было сформировано 5 групп из крыс-самок массой 280-320 г (по 6 животных в каждой): группа 1 - позитивный контроль, интактные животные, получавшие 2% крахмальную слизь в 0,2 мл на 100 г веса и не подвергавшиеся воздействию стресса; группа 2 - животные, получавшие 2% крахмальную слизь в 0,2 мл на 100 г веса и подвергавшиеся воздействию стресса; группа 3 - опытная, животные, получавшие заявляемое соединение I в дозе 30 мг/кг; группа 4 - диротон в дозе 10 мг/кг; группа 5 - нормодипин в дозе 1 мг/кг. Исследуемое соединение в дозе 30 мг/кг и препараты сравнения - лизиноприл (диротон, «Гедеон-Рихтер», Венгрия) в дозе 10 мг/кг и амлодипин (нормодипин, «Гедеон-Рихтер», Венгрия) в дозе 1 мг/кг суспензировали в 2% крахмальной слизи и вводили перорально внутрижелудочно, ежедневно за 30 минут до стрессирования. Затем животных стрессировали в течение 30 минут в темной камере шириной 28 см, длиной 36 см и высотой 28 см, закрепленной на наклонной плоской металлической платформе с углом наклона 10°, на ее стенках по периметру расположены вентиляционные отверстия, обеспечивающие циркуляцию воздуха. Платформа оборудована электроприводом, совершающим качательные движения с регулируемой частотой от 10 до 40 колебаний в минуту. Камера имеет непрозрачную крышку, которая оснащена источником звукового шума и 3 источниками света, расположенными на высоте 28 см. Источники света снабжены реле-прерывателем со временем срабатывания 2 секунды, что обеспечивает пульсацию света. Камера разделена на 6 изолированных отсеков одинакового объема и рассчитана на одновременное стрессирование от 1 до 6 животных. Крыс помещали в изолированные отсеки и подвергали воздействию стрессоров: пульсирующий свет, громкий звук и вибрация. Установка позволяет комбинировать одновременно несколько стрессорных раздражителей или использовать их в монорежиме. За исходный уровень САД и ЧСС принимали значения, зафиксированные в 1 день эксперимента до стрессирования животных, измерение показателей повторяли на 7 и 14 день эксперимента.
Установлено, что у контрольной группы животных через 7 дней стрессирования САД выросло на 12,6%, а через 14 дней - на 16,7% (таблица 4). Пероральное введение в дозе 30 мг/кг заявляемого соединения I предупредило повышение САД, вызванное комбинированным стрессорным воздействием. Профилактическое антигипертензивное действие заявляемого соединения I сопоставимо с препаратами сравнения.
|
|
|
|
![(4-БРОМФЕНИЛ)ЭТИЛИДЕНГИДРАЗИД 2-[6-МЕТИЛ-1-(ТИЕТАН-3-ИЛ)УРАЦИЛ-3-ИЛ]УКСУСНОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЙ ГИПОТЕНЗИВНУЮ АКТИВНОСТЬ](https://fips.edrid.ru/images/rid/6d/af/f2/f9f604a5ad793ec00512647615fb6513.png)

