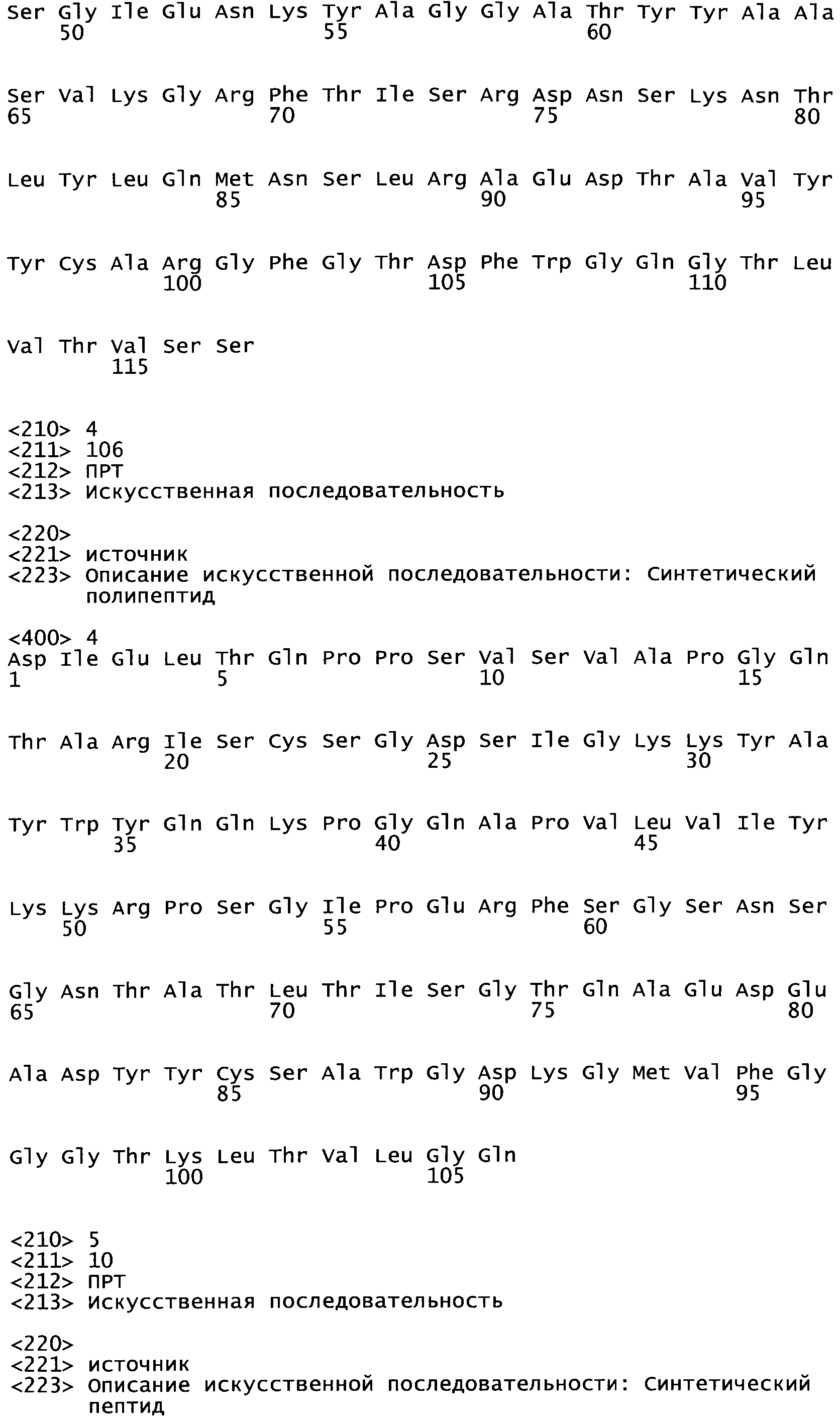Результат интеллектуальной деятельности: ЛЕЧЕНИЕ РАССЕЯННОГО СКЛЕРОЗА
Вид РИД
Изобретение
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННУЮ ЗАЯВКУ
Эта патентная заявка испрашивает приоритет предварительной заявки на патент США с серийным номером 61/175471, поданной 5 мая 2009 года, которая включена сюда посредством ссылки во всей ее полноте.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение, в целом, относится к способу лечения и/или профилактики рассеянного склероза (PC). Согласно настоящему изобретению антагонист GM-CSF (гранулоцитарно-макрофагальный колониестимулирующий фактор) может быть эффективным при лечении рассеянного склероза. Антагонист GM-CSF включает, но не ограничивается, антитело, которое является специфичным в отношении GM-CSF или рецептора GM-CSF.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Рассеянный склероз (PC), также известный как диссеминированный склероз или диссеминированный энцефаломиелит, представляет собой аутоиммунное заболевание, при котором иммунная система атакует центральную нервную систему (ЦНС). По существу PC влияет на способность нервных клеток в головном мозге и спинном мозге к коммуникации друг с другом посредством повреждения миелина. При потере миелина аксоны больше не могут эффективно проводить сигналы.
Были описаны четыре главных подтипа PC (Neurology (1996) 46; 901-911; см. также Фиг.1). Возвратно-ремиттирующий подтип характеризуется непредсказуемыми рецидивами с последующими периодами относительного покоя (ремиссии) без новых признаков активности заболевания, длящимися от нескольких месяцев до нескольких лет. Вторичный прогрессирующий PC характеризует пациентов с исходным возвратно-ремиттирующим PC, у которых затем начинается прогрессирующее неврологическое ухудшение между острыми приступами без каких-либо определенных периодов ремиссии. Первичный прогрессирующий подтип характеризует пациентов, у которых никогда не бывает ремиссии после исходных симптомов PC. Он характеризуется развитием инвалидности с самого начала лишь со временными и небольшими ремиссиями и улучшениями или совсем без них. Наконец, прогрессирующий рецидивирующий PC характеризует тех индивидуумов, которые с самого начала имеют устойчивое неврологическое ухудшение, но также страдают от накладывающихся приступов. Также существуют разные пограничные случаи PC.
Симптомы PC являются сложными и обычно проявляются в эпизодических острых периодах ухудшения (рецидивов), в постепенно прогрессирующем истощении неврологической функции или в комбинации их обоих. Обычными являются сенсорные, зрительные, мозжечковые и моторные симптомы. Пациенты с PC могут страдать практически от любого неврологического симптома или признака, включая изменения в восприятии (гипестезия и парестезия), мышечную слабость, мышечные спазмы, затруднения при движениях; затруднения с координацией и равновесием; проблемы с речью или глотанием; проблемы со зрением; слабость; острую или хроническую боль и затруднения с мочевым пузырем и кишечником. Также обычными являются когнитивное ухудшение разной степени и эмоциональные симптомы депрессии или нестабильного настроения.
PC обычно появляется у тридцатилетних взрослых, но он также может появляться у детей, а первичный прогрессирующих подтип более распространен у пятидесятилетних людей. Как и в случае многих аутоиммунных расстройств, заболевание является более обычным у женщин, и данная тенденция может усиливаться.
При PC иммунная система атакует нервную систему, возможно в результате экспонирования молекулы со структурой, аналогичной структуре одной из ее собственных молекул. Чаще всего поражения при PC охватывают области белого вещества, приближенные к желудочкам мозжечка, стволу мозга, базальным ганглиям, спинному мозгу и зрительному нерву. Функцией клеток белого вещества является проведение сигналов между областями серого вещества, где осуществляется обработка сигналов, и остальными частями организма. PC разрушает олигодендроциты, клетки, ответственные за создание и поддержание жирового слоя, известного как миелиновая оболочка, которая помогает нейронам проводить электрические сигналы. PC приводит к истоньшению или полной потере миелина, и, по мере того как развивается заболевание, - к разрезанию (рассечению) отростков нейронов или аксонов. На ранних фазах заболевания происходит процесс репарации, названный ремиелинизация, но олигодендроциты не могут полностью восстановить миелиновую оболочку клетки. Повторные приступы приводят к последовательно менее эффективным ремиелинизациям, пока вокруг поврежденных аксонов не образуется рубцеподобная бляшка.
Помимо демиелинизации другим патологическим признаком заболевания является воспаление. Т-клетки распознают миелин как чужеродный и атакуют его, как если бы он был инвазивным вирусом. Это запускает воспалительные процессы, стимулируя другие иммунные клетки и растворимые факторы, подобные цитокинам и антителам.
Существует несколько видов терапии рассеянного склероза, но нет известного способа излечения. Различные виды терапии используют для устранения острых приступов, для модификации заболевания и для лечения последствий PC. Традиционной терапией для устранения острых симптоматических приступов является внутривенное или пероральное введение кортикостероидов. Это лечение является эффективным в течение короткого времени для облегчения симптомов, но не имеет значительного влияния на долговременное выздоровления пациента. Применяются многочисленные виды терапии для лечения, модифицирующего заболевание, в зависимости от точной природы и подтипа PC. Способы лечения возвратно-ремиттирующего PC включают интерфероны (интерферон бета-1а и интерферон бета-1b), глатирамера ацетат (копаксон; смесь полипептидов, которые могут защищать миелиновые белки, заменяя их в качестве мишени атаки иммунной системы), митоксантрон (иммунодепрессант, также используемый при химиотерапии рака) и натализумаб (тисабри; гуманизированное моноклональное антитело против молекулы клеточной адгезии α4-интегрина). Способы лечения вторичного прогрессирующего РА и прогрессирующего рецидивирующего PC включают митоксантрон, натализумаб и интерферон-бета-1b (бетаферон). Также применяются другие, главным образом экспериментальные способы лечения. PC ассоциирован со множеством симптомов и функциональных нарушений, которые приводят к ряду прогрессирующих ухудшений и дефектов. Для лечения последствий PC известны и применяются многочисленные виды терапии в зависимости от того, что может требоваться для конкретного случая.
Известно, что в рассеянный склероз вовлечены некоторые цитокины, включая гранулоцитарно-макрофагальный колониестимулирующий фактор (Ponomarev et al.; J Immunol (2007) 178; 39-48; McQualter et al.; J Exp Med., (2001), 194; 873-82). Гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF) представляет собой цитокин, который функционирует в качестве фактора роста лейкоцитов. GM-CSF стимулирует продукцию стволовыми клетками гранулоцитов (нейтрофилы, эозинофилы и базофилы) и моноцитов. Моноциты покидают из кровяного русла и мигрируют в ткань, где они созревают до макрофагов. Таким образом, он является частью природного иммунного/воспалительного каскада, посредством которого активация небольшого числа макрофагов может быстро приводить к увеличению их числа, решающему процессу для борьбы с инфекцией. Активная форма GM-CSF обнаружена экстраклеточно в виде растворимого мономера. В частности, GM-CSF идентифицировали в качестве воспалительного посредника при аутоиммунных расстройствах, таких как ревматоидный артрит (РА), приводящего к повышенной продукции провоспалительных цитокинов, хемокинов и протеаз и, посредством этого, в конечном счете, к разрушению суставов.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
В настоящем изобретении продемонстрировано, что антагонистическое действие в отношении эффектов GM-CSF является действенным подходом для лечения PC. В частности, антитела против GM-CSF или его рецептора являются действенными точками вмешательства при лечении PC. Соответственно, согласно изобретению, например, предложен способ лечения рассеянного склероза у субъекта, включающий стадию введения указанному субъекту эффективного количества антагониста GM-CSF.
В другом аспекте в настоящем изобретении предложен способ профилактики рассеянного склероза у субъекта, включающий стадию введения указанному субъекту эффективного количества антагониста GM-CSF.
В другом аспекте настоящее изобретение относится к композиции, содержащей антагонист GM-CSF, способный оказывать антагонистическое действие в отношении патофизиологической роли GM-CSF при рассеянном склерозе, причем указанная композиция дополнительно содержит один или более чем один фармацевтически приемлемый носитель и/или разбавитель.
В другом аспекте настоящее изобретение относится к композиции, содержащей антагонист GM-CSF, полезный при лечении рассеянного склероза, причем указанная композиция дополнительно содержит один или более чем один фармацевтически приемлемый носитель и/или разбавитель.
В конкретных аспектах настоящего изобретения антагонист GM-CSF представляет собой антитело, специфичное в отношении GM-CSF.
В альтернативных аспектах настоящего изобретения антагонист GM-CSF представляет собой антитело, специфичное в отношении рецептора GM-CSF.
В других аспектах настоящее изобретение относится к применению антагониста GM-CSF в изготовлении лекарственного средства для лечения рассеянного склероза.
В других аспектах согласно настоящему изобретению предложены антагонисты GM-CSF для лечения рассеянного склероза.
Во всем данном описании изобретения будет понятно, что, если контекст не требует иного, слова «содержать», «иметь» и «включать» и их соответствующие вариации, такие как «содержит», «содержащий», «имеет», «имеющий», «включает» и «включающий» подразумевают включение указанного элемента или целого числа или группы элементов или целых чисел, а не исключение любого другого элемента или целого числа или группы элементов или целых чисел.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
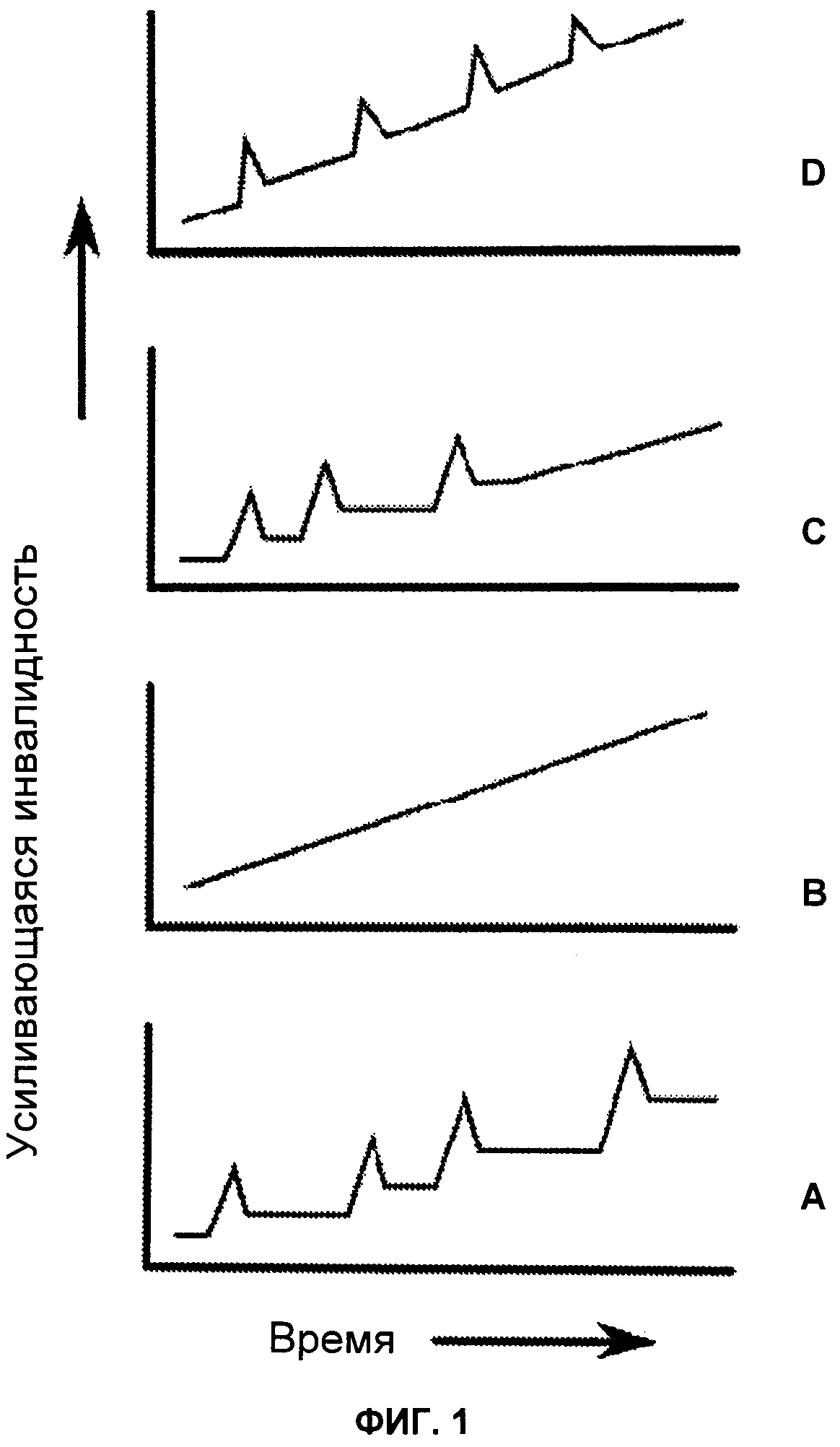
На Фиг.1 описаны типы развития четырех главных подтипов PC.
А - Возвратно-ремиттирующий рассеянный склероз, непредсказуемые приступы, которые могут оставлять или могут не оставлять постоянных нарушений, с последующими периодами ремиссии; В - Первичный прогрессирующий рассеянный склероз, постоянная усиливающаяся инвалидность без приступов; С - Вторичный прогрессирующий рассеянный склероз, исходный возвратно-ремиттирующий рассеянный склероз, при котором внезапно начинается ухудшение без периодов ремиссии; D - Прогрессирующий рецидивирующий рассеянный склероз, постоянное ухудшение с начала с накладывающимися приступами.
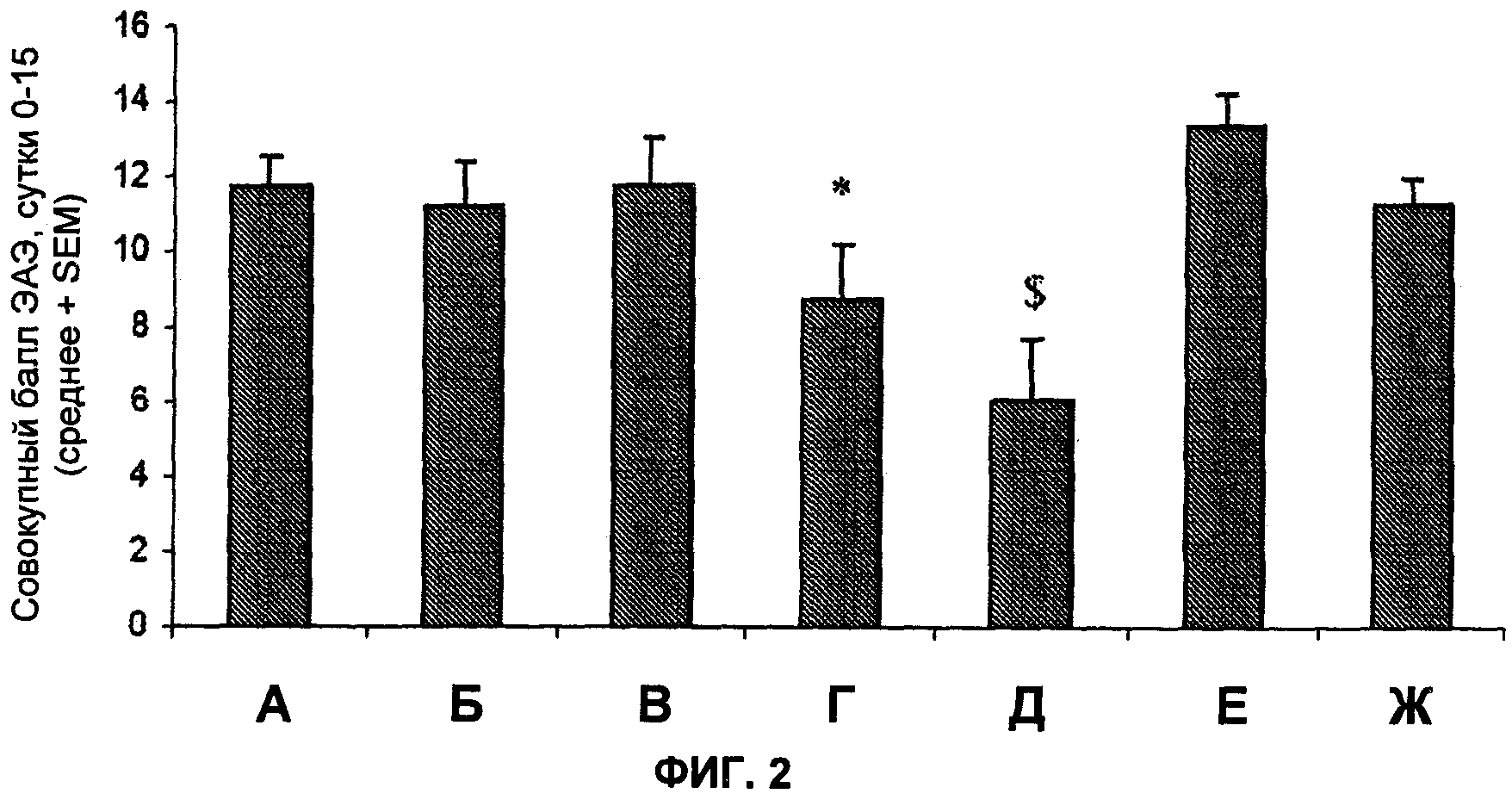
На Фиг.2 показана эффективность антагониста GM-CSF в ЭАЭ (экспериментальный аутоиммунный энцефаломиелит) модели PC, индуцированного MOG (миелин-олигодендроцитарный гликопротеин) (профилактическое лечение). Показаны совокупные балльные показатели ЭАЭ для суток 0-15. А: животные, обработанные носителем (PBS) (фосфатно-солевой буферный раствор); Б: животные, обработанные 10 мг/кг MOR-GM; В: животные, обработанные 20 мг/кг MOR-GM; Г: животные, обработанные 50 мг/кг MOR-GM; Д: животные, обработанные 0,5 мг/кг дексаметазона; Е: животные, обработанные 50 мг/кг MOR-NOGM (изотипическое контрольное антитело); Ж: животные, обработанные 50 мг/кг MOR-GM, с первой обработкой на сутки 14 (терапевтическое лечение). *: P<0,05 по сравнению с изотипическим контрольным антителом. $: P<0,05 по сравнению с обработкой PBS.
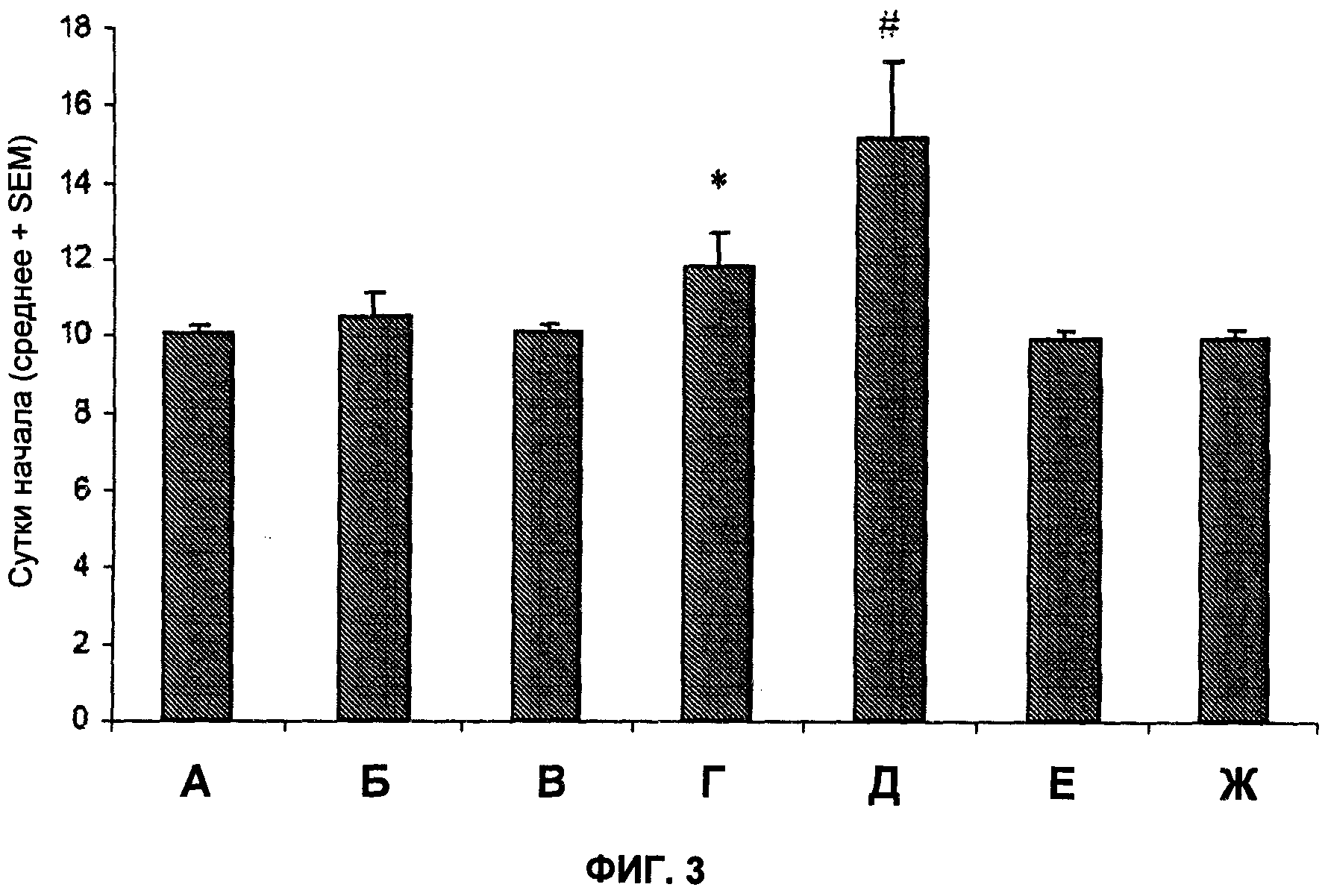
На Фиг.3 показана задержка начала заболевания при обработке MOR-GM. А: животные, обработанные носителем (PBS); Б: животные, обработанные 10 мг/кг MOR-GM; В: животные, обработанные 20 мг/кг MOR-GM; Г: животные, обработанные 50 мг/кг MOR-GM; Д: животные, обработанные 0,5 мг/кг дексаметазона; Е: животные, обработанные 50 мг/кг MOR-NOGM (изотипическое контрольное антитело); Ж: животные, обработанные 50 мг/кг MOR-GM, с первой обработкой на сутки 14 (терапевтическое лечение). *: P<0,05 по сравнению с изотипическим контрольным антителом. $: P<0,10 по сравнению с обработкой PBS.
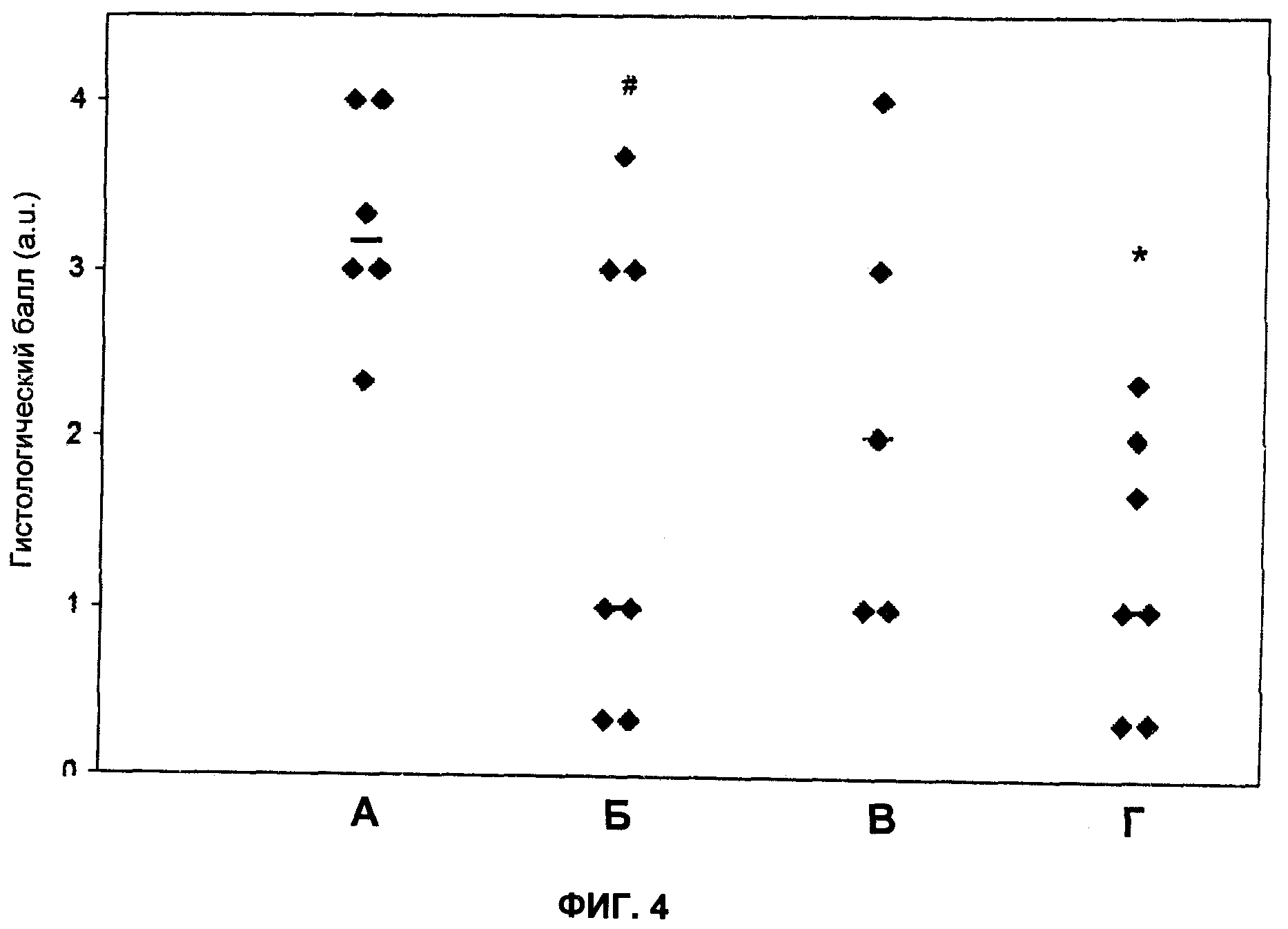
На Фиг.4 показана инфильтрация воспалительных клеток в крестцовый отдел спинного мозга после обработки соединениями по настоящему изобретению. А: животные, обработанные 50 мг/кг MOR-NOGM (изотипическое контрольное антитело; профилактическая обработка); Б: животные, обработанные 50 мг/кг MOR-GM (профилактическая обработка); В: животные, обработанные 50 мг/кг MOR-GM (терапевтическая обработка); Г: животные, обработанные 0,5 мг/кг дексаметазона (профилактическая обработка). Каждая точка данных показывает баллы одного индивидуального животного. #: P<0,10 по сравнению с изотипическим контрольным антителом. *: P<0,05 по сравнению с изотипическим контрольным антителом.
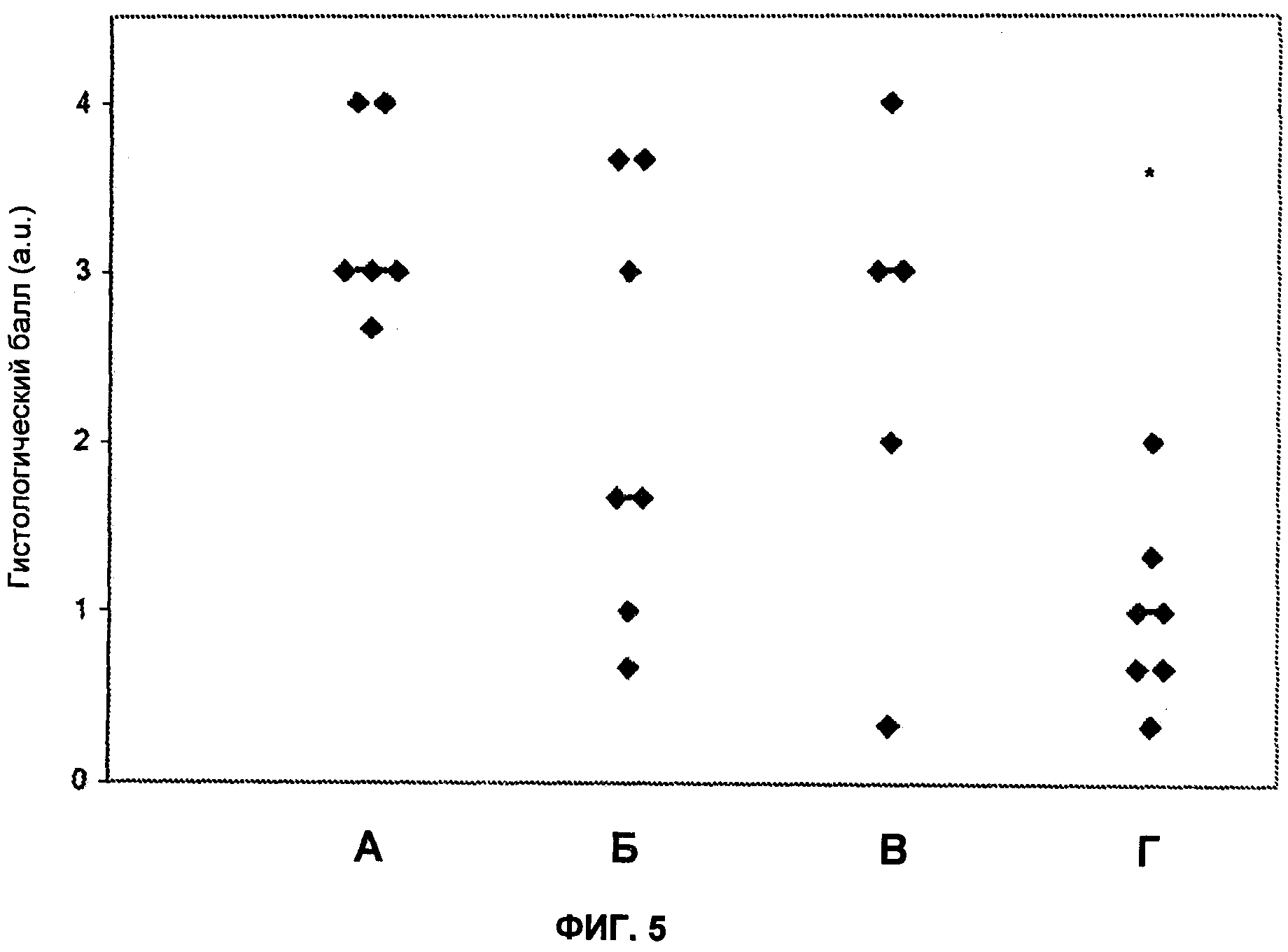
На Фиг.5 показана степень демиелинизации в крестцовом отделе спинного мозга. А: животные, обработанные 50 мг/кг MOR-NOGM (изотипическое контрольное антитело; профилактическая обработка); Б: животные, обработанные 50 мг/кг MOR-GM (профилактическая обработка); В: животные, обработанные 50 мг/кг MOR-GM (терапевтическая обработка); Г: животные, обработанные 0,5 мг/кг дексаметазона (профилактическая обработка). Каждая точка данных показывает баллы одного индивидуального животного. *: P<0,05 по сравнению с изотипическим контрольным антителом.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение демонстрирует, что GM-CSF является действенной мишенью для лечения PC. В этом отношении согласно изобретению в одном аспекте предложены способы применения антагониста GM-CSF для получения профилактической или терапевтической пользы в области PC.
Согласно настоящему изобретению предложены терапевтические способы, включающие введение терапевтически эффективного количества антагониста GM-CSF субъекту, нуждающемуся в таком лечении. Термины «терапевтически эффективное количество» или «эффективное количество» в том виде, как они здесь используются, относятся к количеству антагониста GM-CSF, необходимому для того, чтобы вызвать желательный биологический ответ. Согласно заявленному изобретению, терапевтически эффективное количество представляет собой количество антагониста GM-CSF, необходимое для лечения и/или предупреждения рассеянного склероза.
Термин «антагонисты GM-CSF» в том виде, как он здесь используется, включает антагонисты GM-CSF в их самом широком смысле; включена любая молекула, которая ингибирует активность или функцию GM-CSF или которая любым другим способом оказывает терапевтический эффект на GM-CSF. Термин антагонисты GM-CSF включает, но не ограничивается, антитела, специфично связывающиеся с GM-CSF, ингибиторные нуклеиновые кислоты, специфичные в отношении GM-CSF, и малые органические молекулы, специфичные в отношении GM-CSF. Также в пределах значения термина «антагонист GM-CSF» находятся антитела, специфично связывающиеся с рецептором GM-CSF, ингибиторные нуклеиновые кислоты, специфичные в отношении рецептора GM-CSF, или малые органические молекулы, специфичные в отношении рецептора GM-CSF. Термин «антагонисты GM-CSF» также относится к каркасным молекулам, не являющимся антителами, таким как фибронектиновые каркасы, анкирины, макситела/авимеры, молекулы, происходящие из белка А, антикалины, аффилины, миметики белковых эпитопов (РЕМ) или тому подобное.
Ингибиторные нуклеиновые кислоты включают, но не ограничиваются, антисмысловую ДНК, олигонуклеотиды, образующие триплексы, внешние вспомогательные последовательности, миРНК (малая интерферирующая РНК) и микроРНК. Полезные ингибиторные нуклеиновые кислоты включают нуклеиновые кислоты, которые снижают экспрессию РНК, кодирующей GM-CSF, по меньшей мере на 20, 30, 40, 50, 60, 70, 80, 90 или 95 процентов по сравнению с контролями. Ингибиторные нуклеиновые кислоты и способы их получения хорошо известны в данной области. Доступно программное обеспечение для конструирования миРНК.
Малые органические молекулы (SMOL), специфичные в отношении GM-CSF или рецептора GM-CSF, могут быть идентифицированы через скрининг природных продуктов или скрининг химических библиотек. Типично молекулярная масса SMOL составляет меньше 500 дальтон, более типично от 160 до 480 дальтон. Другими типичными свойствами SMOL являются одно или более чем одно из следующего:
- log Р коэффициента распределения находится в интервале от -0,4 до +5,6,
- молярный показатель преломления составляет от 40 до 130,
- число атомов составляет от 20 до 70.
Для обзоров см. Ghose. et al., (1999), J. Combin. Chem.: 1, 55-68 и Lipinski et al., (1997), Adv. Drug. Del. Rev.: 23, 3-25.
Предпочтительно анатагонист GM-CSF для применения в настоящем изобретении представляет собой антитело, специфичное в отношении GM-CSF или специфичное в отношении рецептора GM-CSF. Такое антитело может быть любого типа, такого как мышиное, крысиное, химерное, гуманизированное или человеческое антитело. «Человеческое» антитело или функциональный фрагмент человеческого антитела определены здесь как антитело или функциональный фрагмент, которые не являются химерными (например, не являются «гуманизированными») и не происходят (либо целиком, либо частично) из видов, не являющихся человеком. Человеческое антитело или функциональный фрагмент антитела могут происходить из человека или могут представлять собой синтетическое человеческое антитело. «Синтетическое человеческое антитело» определено здесь как антитело, имеющее последовательность, полученную, целиком или частично, in silico из синтетических последовательностей, которые основаны на анализе известных последовательностей человеческих антител. Конструирование in silico последовательности человеческого антитела или его фрагмента может достигаться, например, анализом базы данных последовательностей человеческого антитела или фрагментов антитела и конструированием полипептидной последовательности с использованием данных, полученных из нее. Другим примером человеческого антитела или функционального фрагмента антитела являются антитело или функциональный фрагмент антитела, которые кодируются нуклеиновой кислотой, выделенной из библиотеки последовательностей антител человеческого происхождения (т.е. такая библиотека основана на антителах, взятых из природного человеческого источника).
«Гуманизированное антитело» или функциональный фрагмент гуманизированного антитела определены здесь как антитело или функциональный фрагмент антитела, которые (1) происходят из источника, отличного от человеческого (например, трансгенной мыши, которая несет гетерологичную иммунную систему), которые основаны на человеческой последовательности зародышевой линии; или (2) являются химерными, где вариабельный домен имеет происхождение, отличное от человеческого, и константный домен имеет человеческое происхождение, или (3) имеют пересаженные CDR (гипервариабельная область), где CDR вариабельного домена имеют происхождение, отличное от человеческого, тогда как один или более чем один каркас вариабельного домена имеет человеческое происхождение и константный домен (если таковой имеется) имеет человеческое происхождение.
Термин «химерное антитело» или функциональный фрагмент химерного антитела определяется здесь как молекула антитела, которая имеет константные области антитела, происходящие из или соответствующие последовательностям, обнаруженным у одного вида, и вариабельные области антитела, происходящие из другого вида. Предпочтительно константные области антитела происходят из или соответствуют последовательностям, обнаруженным у людей, например в человеческой зародышевой линии или соматических клетках, и вариабельные области антитела (например, области VH, VL, CDR или FR) происходят из последовательностей, обнаруженных у животного, не являющегося человеком, например у мыши, крысы, кролика или хомяка.
При использовании здесь фраза антитело «связывается специфично», «специфично связывается с» означает «специфично к/в отношении» или «специфично распознает» антиген (здесь GM-CSF или, в качестве альтернативы, рецептор GM-CSF), если такое антитело способно различать между таким антигеном и одним или более чем одним контрольным антигеном(ами), поскольку специфичность связывания является не абсолютным, но относительным свойством. Контрольный(е) антиген(ы) может(гут) быть одним или более чем одним близкородственным(и) антигеном(и), который(е) используют в качестве контрольных точек, например IL3 (интерлейкин-3), IL5, IL-4, IL13 или M-CSF (моноцитарный колониестимулирующий фактор). Термин «специфичное связывание» в его самой общей форме (и когда не упоминается определенная ссылка) относится к способности антитела различать между интересующим антигеном и неродственным антигеном, например, при определении согласно одному из следующих способов. Такие способы включают, но не ограничиваются, вестерн-блоттинг, ELISA (твердофазный иммуноферментный анализ), тесты посредством RIA (радиоиммуноанализ), ECL (электрохемилюминисцентный метод), IRMA (иммунорадиометрический анализ) и пептидные сканы. Например, можно проводить стандартный анализ ELISA. Количественную оценку можно проводить по стандартному развитию окрашивания (например, вторичное антитело с пероксидазой хрена и тетраметилбензидином с пероксидом водорода). Реакцию в определенных лунках количественно оценивают по оптической плотности, например, при 450 нм. Типичный фон (=негативная реакция) может быть равен ОП 0,1 (оптическая плотность); типичная позитивная реакция может давать ОП 1. Это означает то, что разница позитивная/негативная реакция может быть более чем 10-кратной. Типично определение специфичности связывания проводят, используя не один контрольный антиген, а набор от примерно трех до пяти неродственных антигенов, таких как сухое молоко, BSA (коровий сывороточный альбумин), трансферрин или тому подобное. Дополнительно термин «специфичное связывание» может относиться к способности антитела различать между разными частями его антигена-мишени, например разными доменами или областями GM-CSF или рецептора GM-CSF, или между одним или более чем одним ключевым аминокислотным остатком или отрезком аминокислотных остатков GM-CSF или рецептора GM-CSF.
Также при использовании здесь термин «иммуноглобулин» (lg) определен как белок, принадлежащий к классу IgG, IgM, IgE, IgA или IgD (или к любому их подклассу) и включает все традиционно известные антитела и их функциональные фрагменты. «Функциональный фрагмент» антитела/иммуноглобулина тем самым определен как фрагмент антитела/иммуноглобулина (например, вариабельная область IgG), который сохраняет антигенсвязывающую область. «Антигенсвязывающая область» антитела типично находится в одной или более чем одной гипервариабельной области(тях) антитела, т.е. в областях CDR-1, -2 и/или -3; однако вариабельные «каркасные» области также могут играть важную роль в связывании антигена, как, например, путем предоставления каркаса для CDR. Предпочтительно «антигенсвязывающая область» содержит по меньшей мере аминокислотные остатки 4-103 вариабельной (области) легкой цепи (VL) и 5-109 вариабельной (области) тяжелой цепи (VH), более предпочтительно аминокислотные остатки 3-107 VL и 4-111 VH и особенно предпочтительно - полные цепи VL и VH (положения аминокислот 1-109 VL и 1-113 VH; нумерация согласно WO 97/08320). Предпочтительным классом иммуноглобулинов для применения в настоящем изобретении является IgG. «Функциональные фрагменты» по изобретению включают домен фрагмента F(ab')2, фрагмент Fab, scFv или конструкции, содержащие одиночные вариабельные домены иммуноглобулинов или полипептиды однодоменного антитела, например одиночные вариабельные домены тяжелой цепи или одиночные вариабельные домены легкой цепи. F(ab')2 или Fab могут быть сконструированы так, чтобы минимизировать или полностью удалить межмолекулярные дисульфидные взаимодействия, которые происходят между доменами СH1 и CL.
Антитело по изобретению может происходить из библиотеки рекомбинантных антител, которая основана на аминокислотных последовательностях, которые были сконструированы in silico и кодируются нуклеиновыми кислотами, которые созданы синтетически. Конструирование последовательности антитела in silico, например, достигается анализом базы данных человеческих последовательностей и разработкой полипептидной последовательности с использованием данных, полученных из нее. Способы конструирования и получения последовательностей, созданных in silico, описаны, например, у Knappik et al., J. Mol. Biol. (2000) 296:57; Krebs et al., J. Immunol. Methods. (2001) 254:67, Rothe et al., J. Mol. Biol. (2008) 376:1182; и патент США №6300064, выданный Knappik et al., которые включены сюда посредством ссылки во всей их полноте.
Любое антитело, специфичное в отношении GM-CSF, можно использовать для целей настоящего изобретения. Типичные антитела включают антитела, содержащие аминокислотную последовательность вариабельной области тяжелой цепи, как описано в SEQ ID NO: 1, или аминокислотную последовательность вариабельной области легкой цепи, как описано в SEQ ID NO: 2. Другие типичные антитела включают антитела, которые происходят из антител, содержащих вариабельную область тяжелой цепи, как описано в SEQ ID NO: 1, или аминокислотную последовательность вариабельной области легкой цепи, как описано в SEQ ID NO: 2. Кроме того, другие типичные антитела включают антитела, которые имеют такую же специфичность и/или связываются с тем же эпитопом, что и антитела, содержащие вариабельную область тяжелой цепи, как описано в SEQ ID NO: 1, или аминокислотную последовательность вариабельной области легкой цепи, как описано в SEQ ID NO: 2. Кроме того, другие типичные антитела включают антитела, которые содержат вариабельную область тяжелой цепи, которая является по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или по меньшей мере на 95% гомологичной последовательности, описанной в SEQ ID NO: 1. Кроме того, другие типичные антитела включают антитела, которые содержат вариабельную область легкой цепи, которая является по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или по меньшей мере на 95% гомологичной последовательности, описанной в SEQ ID NO: 2.
SEQ ID NO: 1:

SEQ ID NO: 2:
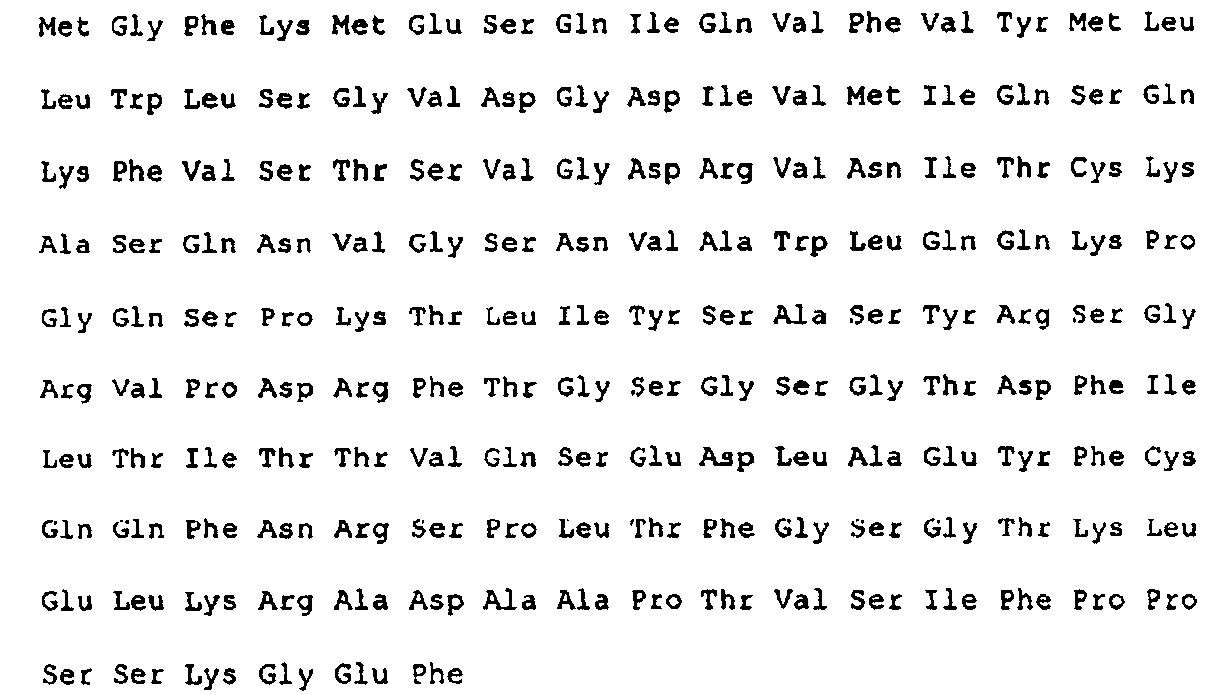
Альтернативные типичные антитела, которые можно использовать в настоящем изобретении, представляют собой антитела, содержащие аминокислотную последовательность вариабельной области тяжелой цепи, как описано в SEQ ID NO: 3, или аминокислотную последовательность вариабельной области легкой цепи, как описано в SEQ ID NO: 4. Другие типичные антитела включают антитела, которые происходят из антител, содержащих вариабельную область тяжелой цепи, как описано в SEQ ID NO: 3, или аминокислотную последовательность вариабельной области легкой цепи, как описано в SEQ ID NO: 4. Кроме того, другие типичные антитела включают антитела, которые имеют такую же специфичность и/или связываются с такимже эпитопом, что и антитела, содержащие вариабельную область тяжелой цепи, как описано в SEQ ID NO: 3, или аминокислотную последовательность вариабельной области легкой цепи, как описано в SEQ ID NO: 4. Кроме того, другие типичные антитела включают антитела, которые содержат вариабельную область тяжелой цепи, которая является по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или по меньшей мере на 95% гомологичной последовательности, описанной в SEQ ID NO: 3. Кроме того, другие типичные антитела включают антитела, которые содержат вариабельную область легкой цепи, которая является по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или по меньшей мере на 95% гомологичной последовательности, описанной в SEQ ID NO: 4.
SEQ ID NO: 3:
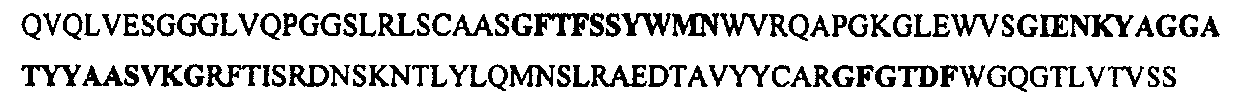
SEQ ID NO: 4
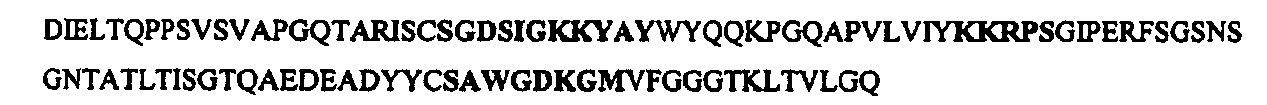
Альтернативные типичные антитела, которые можно использовать в настоящем изобретении, представляют собой антитела, содержащие последовательность H-CDR3, выбранную из:


Предпочтительно антитела, содержащие последовательность H-CDR3, выбраны из любой последовательности из SEQ ID NO: 5-16 (и) дополнительно содержат следующую последовательность H-CDR1:

Альтернативные типичные антитела, которые можно использовать в настоящем изобретении, представляют собой антитела, содержащие следующую последовательность L-CDR1:


Предпочтительно указанное антитело содержит все CDR SEQ ID NO: 21-26.
Рецептор GM-CSF является членом надсемейства гематопоетиновых рецепторов. Он является гетеродимерным, состоящим из альфа и бета субъединиц. Альфа субъединица является высокоспецифичной в отношении GM-CSF, тогда как бета субъединица является общей с другими цитокиновыми рецепторами, включая IL3 и IL5. Это отражено в более широком тканевом распределении бета субъединицы рецептора. Альфа субъединица, GM-CSFR α, главным образом, экспрессируется на миелоидных клетках и негематопоетических клетках, таких как нейтрофилы, макрофаги, эозинофилы, дендритные клетки, эндотелиальные клетки и клетки дыхательного эпителия. Полноразмерный GM-CSFR α представляет собой 400-аминокислотный мембранный гликопротеин типа I, который принадлежит к семейству цитокиновых рецепторов типа I и состоит из 22-аминокислотного сигнального пептида (положения 1-22), 298-аминокислотного внеклеточного домена (положения 23-320), трансмембранного домена в положениях 321-345 и короткого 55-аминокислотного внутриклеточного домена. Сигнальный пептид отщепляется с образованием зрелой формы GM-CSFR α в виде 378-аминокислотного белка. Доступны клоны кДНК человеческого и мышиного GM-CSFR α, и на уровне белка субъединицы рецептора имеют 36% идентичности. GM-CSF способен к связыванию с одной α субъединицей с относительно низкой аффинностью (Kd 1-5 нМ), но совсем не способен к связыванию с одной β субъединицей. Однако присутствие обеих субъединиц α и β приводит к высокоаффинному комплексу лиганд-рецептор (Kd больше 100 пМ). Сигнализация GM-CSF происходит через его исходное связывание с α цепью GM-CSFR и последующее поперечное связывание с большей субъединицей общей β цепи с генерацией высокоаффинного взаимодействия, что фосфорилирует путь JAK-STAT.
При воплощении настоящего изобретения можно использовать любое антитело, специфичное в отношении рецептора GM-CSF. Типичные антитела включают антитела, содержащие аминокислотную последовательность Н-CDR3, описанную в любом из SEQ ID NO: 27-45. Другие типичные антитела включают антитела, которые происходят из антител, содержащих аминокислотную последовательность H-CDR3, описанную в любом из SEQ ID NO: 27-45. Кроме того, другие типичные антитела включают антитела, которые имеют такую же специфичность и/или связываются с таким же эпитопом, что и антитела, содержащие аминокислотную последовательность H-CDR3, описанную в любом из SEQ ID NO: 27-45. Кроме того, другие типичные антитела включают антитела, которые содержат последовательность H-CDR3, которая является по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или по меньшей мере на 95% гомологичной последовательности H-CDR3. описанной в любом из SEQ ID NO: 27-45.


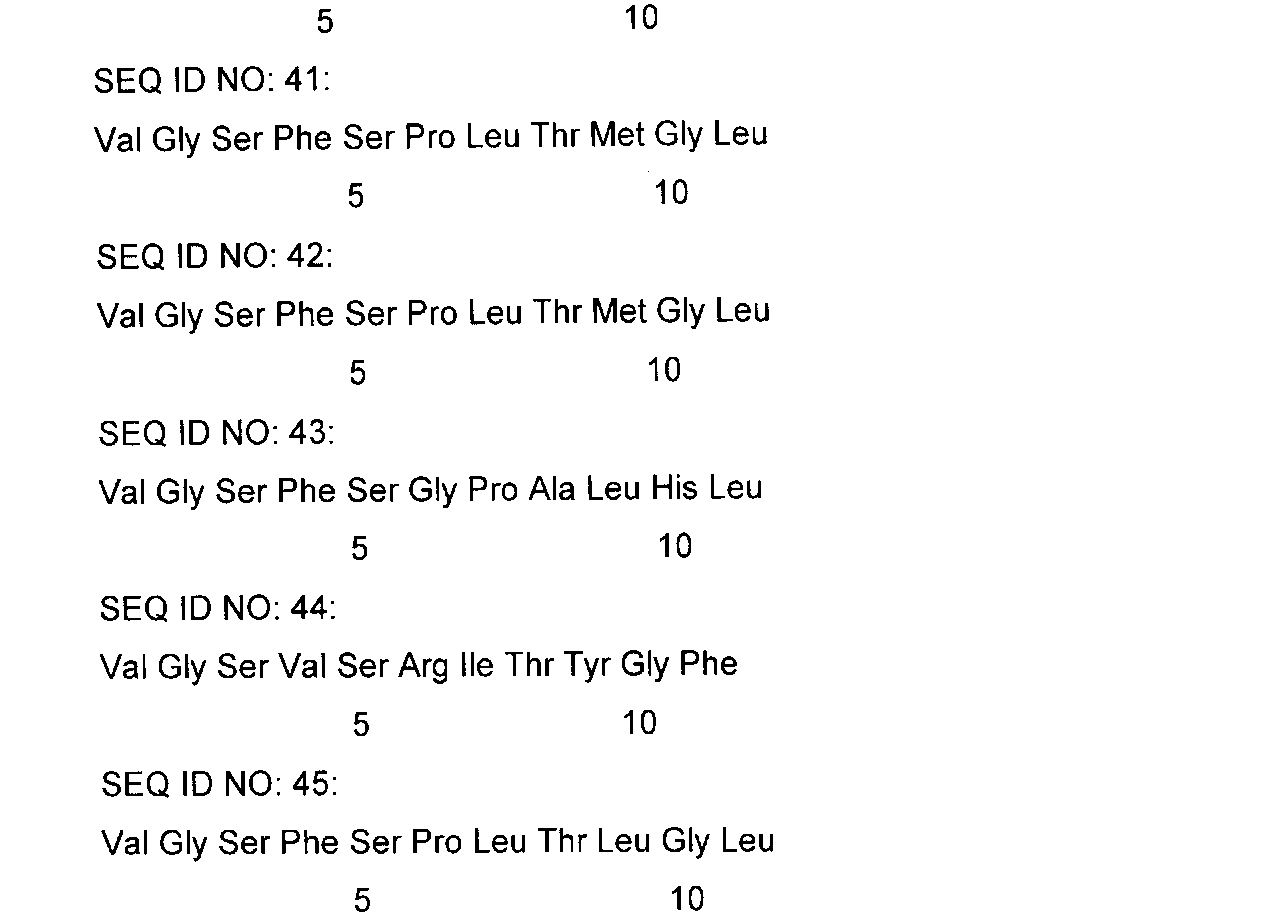
Другие антитела, специфичные в отношении GM-CSF, которые можно использовать при воплощении настоящего изобретения, включают антитела, содержащие аминокислотную последовательность H-CDR3, описанную в любом из SEQ ID NO: 46-56. Другие типичные антитела включают антитела, которые происходят из антител, содержащих аминокислотную последовательность H-CDR3, описанную в любом из SEQ ID NO: 46-56. Кроме того, другие типичные антитела включают антитела, которые имеют такую же специфичность и/или связываются с таким же эпитопом, что и антитела, содержащие аминокислотную последовательность H-CDR3, описанную в любом из SEQ ID NO: 46-56. Кроме того, другие типичные антитела включают антитела, которые содержат последовательность H-CDR3, которая является по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или по меньшей мере на 95% гомологичной последовательности H-CDR3, описанной в любом из SEQ ID NO: 46-56.
SEQ ID NO:46:
EGGYSYGYFDY
SEQ ID NO: 47:
DKWLDGFDY
SEQ ID NO: 48:
DRWLDAFDI
SEQ ID NO: 49
APYDWTFDY:
SEQ ID NO: 50:
DRWLDAFEI
SEQ ID NO: 51:
QRYYYSMDV
SEQ ID NO: 52:
RPWELPFDY
SEQ ID NO: 53:
NGDYVFTYFDY
SEQ ID NO: 54:
FGYFGYYFDY
SEQ ID NO: 55:
DPYTSGFDY
SEQ ID NO: 56:
EDTAMDYFDY.
Композиции по изобретению можно использовать для терапевтических или профилактических применений. Изобретение, следовательно, включает фармацевтическую композицию, содержащую антитело по изобретению (или функциональный фрагмент антитела) и фармацевтически приемлемый носитель или его эксципиент. В связанном с этим аспекте согласно изобретению предложен способ лечения рассеянного склероза. Такой способ включает стадии введения субъекту, нуждающемуся в этом, эффективного количества фармацевтической композиции, которая содержит антитело по изобретению, как здесь описано или рассматривается.
В определенных аспектах согласно настоящему изобретению предложены способы лечения рассеянного склероза у субъекта, включающие стадию введения указанному субъекту антагониста GM-CSF. Термин «субъект» при использовании здесь относится к любому млекопитающему, включая грызунов, таких как мышь или крыса, и приматов, таких как яванский макак (Масаса fascicularis), макак-резус (Масаса mulatta) или человек (Homo sapiens). Предпочтительно субъектом является примат, наиболее предпочтительно человек.
В определенных аспектах согласно настоящему изобретению предложены способы лечения рассеянного склероза, включающие стадию введения субъекту антагониста GM-CSF, который может связываться с GM-CSF с аффинностью меньше чем примерно 100 нМ, более предпочтительно меньше чем примерно 60 нМ и еще более предпочтительно меньше чем примерно 30 нМ. Кроме того, предпочтительными являются антитела, которые связываются с GM-CSF с аффинностью меньше чем примерно 10 нМ, более предпочтительно меньше чем примерно 3 нМ.
В определенных аспектах согласно настоящему изобретению предложены способы лечения рассеянного склероза, включающие стадию введения субъекту антагониста GM-CSF, который конкурирует за связывание с GM-CSF с антителом, где тяжелая цепь указанного антитела содержит аминокислотную последовательность SEQ ID NO: 3. В альтернативных аспектах согласно настоящему изобретению предложены способы лечения рассеянного склероза, включающие стадию введения субъекту антагониста GM-CSF, который конкурирует за связывание с GM-CSF с антителом, где легкая цепь указанного антитела, специфичного в отношении GM-CSF, содержит аминокислотную последовательность SEQ ID NO: 4.
В определенных аспектах согласно настоящему изобретению предложены способы лечения рассеянного склероза, включающие стадию введения субъекту антагониста GM-CSF, представляющего собой антитело, специфичное в отношении GM-CSF и где указанное антитело, специфичное в отношении GM-CSF, перекрестно реагирует с GM-CSF крысы и/или макака-резуса при определении равновесным титрованием раствора (SET) и/или анализом пролиферации TF1.
В определенном аспекте согласно настоящему изобретению предложена композиция, содержащая антагонист GM-CSF, способный оказывать антагонистическое действие в отношении патофизиологической роли GM-CSF при рассеянном склерозе, причем указанная композиция дополнительно содержит один или более чем один фармацевтически приемлемый носитель и/или разбавитель. Антитела против GM-CSF по настоящему изобретению могут оказывать антагонистическое действие в отношении любой из функций GM-CSF при рассеянном склерозе.
В определенных аспектах согласно настоящему изобретению предложена композиция, содержащая антагонист GM-CSF, способный уменьшать демиелинизацию миелинового слоя, причем указанная композиция дополнительно содержит один или более чем один фармацевтически приемлемый носитель и/или разбавитель.
В определенных аспектах согласно настоящему изобретению предложена композиция, содержащая антагонист GM-CSF, способный уменьшать приток воспалительных клеток в спинной мозг, причем указанная композиция дополнительно содержит один или более чем один фармацевтически приемлемый носитель и/или разбавитель.
В определенных аспектах согласно настоящему изобретению предложен способ лечения или профилактики рассеянного склероза у субъекта, включающий стадию введения субъекту эффективного количества антагониста GM-CSF, где указанное введение задерживает начало рассеянного склероза.
В другом аспекте согласно настоящему изобретению предложен способ профилактики рассеянного склероза у субъекта, включающий введение указанному субъекту антагониста GM-CSF. Термин «профилактика» при использовании здесь относится к способам, целью которых является предупреждение начала заболевания или которые задерживают начало заболевания.
В определенных аспектах согласно настоящему изобретению предложен способ лечения или профилактики рассеянного склероза у субъекта, включающий стадию введения субъекту эффективного количества антагониста GM-CSF, где указанное введение снижает пролиферацию Т-клеток.
В определенных аспектах согласно настоящему изобретению предложен способ лечения или профилактики рассеянного склероза у субъекта, включающий стадию введения субъекту эффективного количества антагониста GM-CSF, где указанное введение снижает высвобождение IL 17 Т-клетками.
Анализы для измерения и количественной оценки пролиферации Т-клеток и высвобождения IL 17 известны в данной области.
В определенных аспектах согласно настоящему изобретению предложена композиция, содержащая антагонист GM-CSF, полезный при лечении рассеянного склероза, и дополнительно содержащая один или более чем один фармацевтически приемлемый носитель и/или разбавитель.
В других аспектах согласно настоящему изобретению предложено применение антагониста GM-CSF в изготовлении лекарственного средства для лечения рассеянного склероза.
В других аспектах согласно настоящему изобретению предложены антагонисты GM-CSF для лечения рассеянного склероза.
В конкретных аспектах антагонисты GM-CSF по настоящему изобретению вводят подкожно. В других аспектах антагонисты GM-CSF по настоящему изобретению вводят интраспинально. Антагонисты GM-CSF могут быть особенно эффективными для лечения рассеянного склероза при введении подкожно или интраспинально.
Композиции по настоящему изобретению предпочтительно представляют собой фармацевтические композиции для лечения рассеянного склероза, содержащие антагонист GM-CSF и фармацевтически приемлемый носитель, разбавитель или эксципиент. Такие носители, разбавители и эксципиенты хорошо известны в данной области, и квалифицированный специалист подберет препарат и путь введения, лучше всего подходящий для лечения субъекта антагонистами GM-CSF по настоящему изобретению.
В определенных аспектах согласно настоящему изобретению предложен способ для лечения или профилактики рассеянного склероза у субъекта, включающий стадию введения субъекту эффективного количества антагониста GM-CSF. В определенных аспектах указанный субъект представляет собой человека. В альтернативных аспектах указанный субъект представляет собой грызуна, такого как крыса или мышь.
В определенных аспектах указанный антагонист GM-CSF представляет собой антитело, специфичное в отношении GM-CSF. В конкретных аспектах вариабельная тяжелая цепь указанного антитела, специфичного в отношении GM-CSF, содержит аминокислотную последовательность SEQ ID NO:3. В других конкретных аспектах вариабельная легкая цепь указанного антитела, специфичного в отношении GM-CSF, содержит аминокислотную последовательность SEQ ID NO: 4.
В определенных аспектах указанный антагонист GM-CSF представляет собой антитело, специфичное в отношении рецептора GM-CSF.
В определенных аспектах указанное введение антагониста GM-CSF снижает демиелинизацию миелинового слоя.
В других аспектах указанное введение антагониста GM-CSF снижает приток воспалительных клеток в спинной мозг.
В других аспектах указанное введение антагониста GM-CSF снижает пролиферацию Т-клеток.
В других аспектах указанное введение антагониста GM-CSF снижает высвобождение IL17 Т-клетками.
В других аспектах указанное введение задерживает начало рассеянного склероза.
В определенных аспектах указанный антагонист GM-CSF вводят подкожно или интраспинально.
В определенных аспектах согласно настоящему изобретению предложен антагонист GM-CSF для применения в лечении или профилактике рассеянного склероза. В определенных аспектах указанные лечение или профилактика включают стадию введения субъекту эффективного количества антагониста GM-CSF. В определенных аспектах указанный субъект представляет собой человека. В альтернативных аспектах указанный субъект представляет собой грызуна, такого как крыса или мышь.
В определенных аспектах указанный антагонист GM-CSF представляет собой антитело, специфичное в отношении GM-CSF. В определенных аспектах вариабельная тяжелая цепь указанного антитела, специфичного в отношении GM-CSF, содержит аминокислотную последовательность SEQ ID NO: 3. В определенных аспектах вариабельная легкая цепь указанного антитела, специфичного в отношении GM-CSF, содержит аминокислотную последовательность SEQ ID NO: 4.
В определенных аспектах указанный антагонист GM-CSF представляет собой антитело, специфичное в отношении рецептора GM-CSF.
В определенных аспектах лечение или профилактика указанным антагонистом GM-CSF снижают демиелинизацию миелинового слоя.
В других аспектах лечение или профилактика указанным антагонистом GM-SCF снижают приток воспалительных клеток в спинной мозг.
В других аспектах лечение или профилактика указанным антагонистом GM-SCF снижают пролиферацию Т-клеток.
В других аспектах лечение или профилактика указанным антагонистом GM-SCF снижают высвобождение IL 17 Т-клетками.
В других аспектах лечение или профилактика указанным антагонистом GM-SCF задерживают начало рассеянного склероза.
В определенных аспектах указанный антагонист GM-SCF вводят подкожно или интраспинально.
ПРИМЕРЫ
Пример 1: Типичные антитела и животные, используемые в настоящем изобретении
В качестве типичного антагониста GM-SCF в настоящем изобретении использовали MOR-GM. MOR-GM представляет собой полностью человеческое GM-SCF-специфичное антитело (WO 06/122797). Вариабельная область тяжелой цепи MOR-GM показана в SEQ ID NO: 3, вариабельная область легкой цепи показана в SEQ ID NO: 4.
В других экспериментах использовали антитело 22Е9, антитело против мышиного GM-CSF (AbD Serotec, Martinsried/Германия; Кат. №1023501).
Очевидно, согласно настоящему изобретению можно было использовать любой другой антагонист GM-SCF, например любое антитело, содержащее аминокислотный отрезок, выбранный из SEQ ID NO: 1-45.
7-8-Недельных самцов крыс породы черный агути (DA) (Harlan Laboratories, Inc., Indianapolis/IN) содержали в традиционных чистых условиях при 21±3°C, относительной влажности 40-70% и цикле свет/темнота 12 часов. Крыс содержали парами, и они имели свободный доступ к пищевой диете грызунов (SSNIFF, Bio-Services, Нидерланды). Индивидуальных животных идентифицировали, маркируя хвост. Перед началом эксперимента крыс приручали в течение 4-недельного периода. Крыс распределяли по группам путем рандомизации перед началом эксперимента. В начале экспериментов крысы имели возраст 11-12 недель и массу 200-250 граммов.
Пример 2: терапевтическая эффективность антагонистов GM-CSF в ЕАЕ модели PC, индуцированной MOG.
Для индукции экспериментального аутоиммунного энцефаломиелита (ЭАЭ) самцов крыс DA иммунизировали в двух местах, находящихся по бокам дорсального основания хвоста, внутрикожной инъекцией 15 мкг рекомбинантного миелин-олигодендроцитарного гликопротеина (rMOG), эмульгированного в 200 мкл смеси 1:1 неполного адъюванта Фрейнда (IFA) и 10 мМ NaAc, pH 3,0. Для облегчения иммунизации крыс анестезировали ингаляцией 2-4% изофлурана в смеси кислорода и N2О.
Эффекты внутрибрюшинных введений тестируемого соединения MOR-GM тестировали в сравнении с обработкой носителем (PBS) (фосфатно-солевой буферный раствор) и в сравнении с группой, обработанной неспецифичным/иррелевантным изотипическим контрольным антителом MOR-NOGM (50 мг/кг). Профилактические обработки соединением MOR-GM тестировали в трех дозировках, а именно: 10, 20 и 50 мг/кг. Соединение вводили в сутки 7, 10, 14, 17 и 21. Кроме того, эффективность соединения (50 мг/кг) тестировали по схеме, при которой первую обработку начинали после начала заболевания. В этом случае соединение вводили в сутки 14, 17 и 21. Группы позитивных контролей содержали крыс, обрабатываемых ежесуточно с суток 9 и далее посредством внутрибрюшинного введения дексаметазона (0,5 мг/кг).
Каждая экспериментальная группа содержала 12 животных. Пробы крови отбирали из хвостовых вен в сутки 17 и 21 (до обработки) и в конечный момент времени. Массу тела каждой отдельной крысы измеряли ежесуточно.
ЭАЭ крыс оценивали ежесуточно, используя следующую систему балльной оценки нарушения здоровья:
|
Крысам, которых необходимо было умерщвлять из-за сопутствующей заболеваемости, ассоциированной с ЭАЭ, приписывали значение 3,5 в сутки умерщвления, и балл 4 на все последующие сутки на протяжении всего периода мониторинга.
Фраза «максимальный клинический балл» относится к наивысшему баллу ЭАЭ каждой крысы на протяжении экспериментального периода.
«Совокупный балл» представляет собой сумму всех баллов ЭАЭ для данной крысы на протяжении определенного периода времени (площадь под кривой). Совокупные баллы рассчитывали для полного периода наблюдения, для первой фазы заболевания (сутки 0-15) и для фазы обострения (сутки 16-конец).
Фраза «сутки начала» относится к первым из трех последовательных суток, на которые достигается совокупный балл по меньшей мере 3.
Гистологический анализ: ткани, зафиксированные в формалине, погружали в парафин и 5 мкм срезы тканей окрашивали гематоксилином/эозином для обеспечения полуколичественной градации инфильтрации воспалительных клеток или окрашивали люксолом быстрым синим (Luxol fast blue) согласно KlÜver-Barrera для окрашивания миелина. Степень инфильтрации воспалительными клетками и демиелинизации оценивали полуколичественно на трех непоследовательных (разделенных на 100 мкм) срезах из крестцовой части спинного мозга. Гистологическую градацию осуществляли с использованием систем балльной оценки, как описано в таблицах ниже. Гистологическую градацию проводили слепым способом.
Гистологическая система балльной оценки для полуколичественной градации инфильтрации воспалительных клеток в ткань спинного мозга:
|
Гистологическая система балльной оценки для полуколичественной градации демиелинизации ткани спинного мозга:
|
Все статистические анализы проводили с использованием статистической программы SPSS 14 для Windows (SPSS Inc., Chicago, IL, США). Для множественного группового сравнения в сутки начала (эксперимента) максимальных баллов ЭАЗ, совокупного балла и максимальной потери массы применяли критерий Крускала-Уоллиса с последующим апостериорным U-критерием Манна-Уитни для определения того, какие группы значимо отличались от групп, обработанных носителем. Развитие заболевания тестировали общим линейным способом с последующим дисперсионным анализом и апостериорным критерием LSD для определения того, на какие сутки обработки были значимо отличными. Анализ Каплана-Мейера с использованием критерия Кокса-Мантеля использовали для множественного группового сравнения показателя выживаемости и последующего апостериорного анализа.
Контрольная обработка носителем (PBS: негативный контроль)
Животных обрабатывали в сутки 7, 10, 14, 17 и 21 внутрибрюшинным введением PBS. У всех животных развивался ЭАЭ. Первые признаки заболевания наблюдали на 9 сутки. Средними сутками начала (заболевания) были 10,1±0,7. Первый приступ достигал пика около суток 11-13, второй приступ - около суток 21. Средний максимальный балл ЭАЭ этой группы составлял 3,5±0,6, и средний совокупный балл ЭАЭ в сутки 0-24 составлял 38,7±9,8. Во время первой фазы заболевания (от суток 0 до суток 15) средний совокупный балл составлял 11,7±2,7, во время фазы обострения 26,9±7,6. Все животные демонстрировали потерю массы в связи с признаками паралича. Средний максимальный процент потери массы составлял 21,1±5,7%.
Контрольная обработка изотипическим контрольным антителом (MOR-NOGM: негативный контроль)
Животных обрабатывали в сутки 7, 10, 14, 17 и 21 изотипическим контрольным антителом MOR-NOGM в дозировке 50 мг/кг. У всех животных в этой группе развивался ЭАЭ. Ни один из наблюдавшихся параметров не был статистически значимо отличным от наблюдений в группе, обработанной носителем (PBS). Средними сутками начала заболевания были 9,8±0,8. Средний максимальный балл ЭАЭ составлял 3,4±0,7. Совокупные баллы ЭАЭ были сопоставимыми с баллами групп, обработанных носителем. Совокупный балл ЭАЭ для всего экспериментального периода составлял 36,7±10,9. Совокупный балл для первой фазы заболевания составлял 13,3±3,1 и для фазы обострения 23,5±8,0. Максимальная потеря массы составляла 19,6±5,6%. Животные демонстрировали значительную инфильтрацию крестцовой части спинного мозга воспалительными клетками наряду с обширной демиелинизацией.
Контрольная обработка дексаметазоном (позитивный контроль)
Животных внутрибрюшинно обрабатывали 0,5 мг/кг дексаметазона ежесуточно с суток 9 и далее. Только у 9 из 12 животных развивался ЭАЭ. Обработка не влияла на тяжесть заболевания. Максимальный балл ЭАЭ был значимо снижен до 1,7±1,0 (р=0,001). Средний совокупный балл ЭАЭ снижался до 13,1±13,6 (p<0,005). Совокупный балл во время первой фазы заболевания снижался до 6,0±5,7 (p=0,010) и 7,1±9,3 для фазы обострения (p<0,0005). Несмотря на ингибирование ЭАЭ дексаметазон не влияет на потерю массы тела. Степень инфильтрации воспалительных клеток в крестцовую область спинного мозга была снижена по сравнению с крысами, обработанными изотипическим контрольным антителом MOR-NOGM (p=0,003). Подобным образом уровень демиелинизации был значительно ниже (p=0,002).
Обработка MOR-GM с суток 7 и далее (профилактическое лечение)
Животных внутрибрюшинно обрабатывали в сутки 7, 10, 14, 17 и 21 MOR-GM в дозе 10, 20 или 50 мг/кг. У всех животных действительно развивался ЭАЭ. По сравнению с обработкой изотипическим контрольным антителом (MOR-NOGM) сутки начала заболевания значимо задерживались на 2 суток посредством обработки 50 мг/кг MOR-GM (начало заболевания: 11,8±3,0 суток; р=0,047). Также имеется явная тенденция к снижению совокупного балла ЭАЭ. Совокупный балл ЭАЭ на протяжении суток 0-24 составлял 27,7±12,3 (p=0,094). Совокупный балл ЭАЭ во время исходной фазы заболевания (сутки 0-15) составлял 8,7±4,9. Это существенно ниже по сравнению с контрольной группой, обработанной изотипическим антителом (p=0,040). Обработка не влияла на максимальную потерю массы. Обработка 50 мг/кг MOR-GM снижала ежесуточный средний совокупный балл (p=0,022). При оценке на основе день ко дню, средние совокупные баллы значимо снижались с суток 11 до суток.
Результаты описаны на Фиг.2. Профилактическая обработка MOR-GM (50 мг/кг) показывала сильное и значимое снижение совокупного балла ЭАЭ на сутки 0-15. Результаты были особенно значимыми для первого приступа (сутки 0-15).
Обработка MOR-GM с суток 14 и далее (терапевтическая обработка)
Животные получали первую обработку 50 мг/кг MOR-GM (внутрибрюшинно) в сутки 14, т.е. через четверо суток после начала ЭАЭ. Дополнительную обработку проводили на сутки 17 и 21. Эта схема обработки не имела статистически значимого эффекта на максимальный балл ЭАЭ или на совокупные баллы ЭАЭ. Однако совокупный балл с течением времени показывал менее отчетливое увеличение клинических баллов по сравнению с изотипическим контрольным антителом на старте терапевтической обработки в сутки 14. Отсутствовало влияние на максимальную потерю массы тела.
На Фиг.3 показано, что начало заболевания задерживается при введении MOR-GM в концентрации 50 мг/кг при профилактической обработке (Р<0,10). Гистологические сведения показаны на Фиг.4 (воспаление) и 5 (демиелинизация). Результаты ясно показывают, что антагонисты GM-CSF способны снижать приток воспалительных клеток в нижнюю часть спинного мозга. Антагонисты GM-CSF также способны уменьшать демиелинизацию. Для обоих параметров в контрольной обработке не могли наблюдать гистологические баллы 2 или ниже, что указывает на эффективность лечения MOR-GM.
В целом, эти результаты демонстрируют эффективность антагонистов GM-CSF при лечении рассеянного склероза.
Пример 3: Терапевтическая эффективность антитела, специфичного в отношении GM-CSF, содержащего SEQ ID NO: 3 или 4
Повторяют Пример 2. Как и с антагонистом GM-CSF, используют специфичное антитело в отношении GM-CSF, содержащее аминокислотную последовательность вариабельной области тяжелой цепи, как показано в SEQ ID NO: 1, или содержащее аминокислотную последовательность вариабельной области легкой цепи, как показано в SEQ ID NO: 2. Можно использовать другой вид, отличный от мыши, в частности вид, для которого антитело, используемое в данном эксперименте, имеет перекрестную реактивность. Предпочтительно видом животного, используемого в этом эксперименте, является крыса.
Животные, например крысы, обработанные изотипическим контрольным антителом, показывают значимо возросшие признаки ЭАЭ по сравнению с животными, которые получали антитело, специфичное в отношении GM-CSF, содержащее аминокислотную последовательность вариабельной области тяжелой цепи, как показано в SEQ ID NO: 1, или содержащее аминокислотную последовательность вариабельной области легкой цепи, как показано в SEQ ID NO: 2. Это демонстрирует эффективность антител в лечении ЭАЭ и PC.
Пример 4: терапевтическая эффективность антител, специфичных в отношении GM-CSF, содержащих SEQ ID NO: 5-20
Повторяют Пример 2. Как и с антагонистом GM-CSF, используют антитело, специфичное в отношении GM-CSF, содержащее последовательность H-CDR3, выбранную из любой из SEQ ID NO: 5-16. Предпочтительно указанные антитела дополнительно содержат последовательность H-CDR1 SEQ ID NO: 16 и/или последовательность H-CDR2 SEQ ID NO: 17, и/или последовательность L-CDR1 SEQ ID NO: 18, и/или последовательность L-CDR2 SEQ ID NO: 19, и/или последовательность L-CDR3 SEQ ID NO: 20. Можно использовать другой вид, чем мышь, в частности вид, для которого антитело, используемое в этом эксперименте, имеет перекрестную реактивность. Предпочтительно видом животного, используемым в данном эксперименте, является крыса.
Животные, например крысы, обработанные изотипическим контрольным антителом, показывают значительно усилившиеся признаки ЭАЭ по сравнению с животными, которые получали антитело, специфичное в отношении GM-CSF, согласно настоящему примеру. Это демонстрирует эффективность антител при лечении ЭАЭ и PC.
Пример 5: Терапевтическая эффективность антител, специфичных в отношении GM-CSF, содержащих SEQ ID NO: 21-26
Повторяют Пример 2. Как и с антагонистом GM-CSF, используют антитело, специфичное в отношении GM-CSF, содержащее последовательность L-CDR1 SEQ ID NO: 21 и/или последовательность L-CDR2 SEQ ID NO: 22, и/или последовательность L-CDR3 SEQ ID NO: 23, и/или последовательность H-CDR1 SEQ ID NO: 24, и/или последовательность H-CDR2 SEQ ID NO: 25, и/или последовательность H-CDR3 SEQ ID NO: 26. Предпочтительно указанное антитело содержит все CDR SEQ ID NO: 21-26. Можно использовать другой вид, отличный от мыши, в частности вид, к которому антитело, используемое в данном эксперименте, является перекрестно реактивным. Предпочтительно видом животного, используемого в данном эксперименте, является крыса.
Животные, например крысы, обработанные изотипическим контрольным антителом, показывают значительно усилившиеся признаки ЭАЭ по сравнению с животными, которые получали антитело, специфичное в отношении GM-CSF, согласно настоящему примеру. Это демонстрирует эффективность антител при лечении ЭАЭ и PC.
Пример 6: Терапевтическая эффективность антител, специфичных в отношении GM-CSF, содержащих SEQ ID NO: 46-56
Повторяют Пример 2. Как и с антагонистом GM-CSF, используют антитело, специфичное в отношении GM-CSF, содержащее последовательность H-CDR3, выбранную из любой из SEQ ID NO: 46-56. Можно использовать другой вид, отличный от мыши, в частности вид, к которому антитело, используемое в данном эксперименте, является перекрестно реактивным.
Животные, например макак-резус или яванский макак, обработанные изотипическим контрольным антителом, показывают значительно усилившиеся признаки ЭАЭ по сравнению с животными, которые получали антитело, специфичное в отношении GM-CSF, согласно настоящему примеру. Это демонстрирует эффективность антител при лечении ЭАЭ и PC.
Пример 7: Терапевтическая эффективность антител, специфичных в отношении рецептора GM-CSF
Повторяют Пример 2 с тем отличием, что вместо моноклонального антитела, специфичного в отношении GM-CSF, используют моноклональное антитело, специфичное в отношении рецептора GM-CSF.
В качестве антагониста GM-CSF используют антитело, специфичное в отношении рецептора GM-CSF, содержащее аминокислотную последовательность последовательности H-CDR3, описанной в любом SEQ ID NO:27-45. Можно использовать другой вид, отличный от мыши, в частности вид, для которого антитело, используемое в данном эксперименте, является перекрестно реактивным. Предпочтительно видом животного, используемым в данном эксперименте, является крыса.
Животные, например крысы, обработанные изотипическим контрольным антителом, показывают значительно усилившиеся признаки ЭАЭ по сравнению с животными, которые получали антитело, специфичное в отношении рецептора GM-CSF, согласно настоящему примеру. Это демонстрирует эффективность антител при лечении ЭАЭ и PC.
Пример 8: Клиническое испытание
Эффективность соединений по настоящему изобретению можно тестировать в клиническом испытании для возвратно-ремиттирующего рассеянного склероза. Исследуемая популяция включает пациентов (в возрасте старше 18 и младше 55 лет, как мужчин, так и женщин) с подтвержденным диагнозом возвратно-ремиттирующей формы рассеянного склероза (ВРРС). Соединения вводят внутривенно. Целью является оценка ранней эффективности MOR-GM у пациентов с ВРРС в многоцентровом двойном слепом исследовании по варьированию дозы, контролируемом плацебо.
Пациентов будут объединять в разные группы обработки. Разные группы обработки будут получать либо плацебо, либо 0,75 мг, 1,5 мг или 3,0 мг MOR-GM каждые две недели для первых двух доз и затем MOR-GM один раз в месяц.
Клиническое испытание дополнительно подтверждает эффективность антагонистов GM-CSF по настоящему изобретению. Начало рассеянного склероза после обработки MOR-GM явно задерживается по сравнению с обработкой плацебо.