Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ N', N'-БИС{[АЛКИЛ(ФЕНИЛ)СУЛЬФАНИЛ]МЕТИЛ} АРИЛГИДРАЗИДОВ
Вид РИД
Изобретение
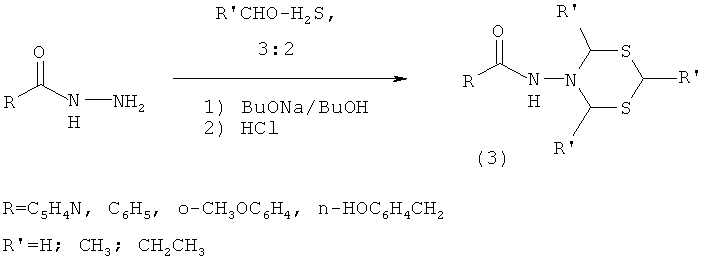
Предлагаемое изобретение относится к области органической химии, конкретно, к способу получения N′,N′-бмс{[алкил(фенил)сульфанилметил]}арилгидразидов общей формулы (1):
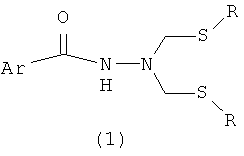
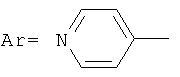 ,
, 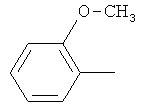 ,
, 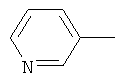
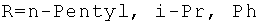
Гетеро(N,O,S)атомные соединения перспективны в качестве новых модифицированных фармакологически активных препаратов [Z.Brzozowski, F.Saczewski and М.Gdaniec. Synthesis, Structural Characterization and In Vitro Antitumor Activity of Novel 6-Chloro-l,l-dioxo-l,4,2-benzodithiaziene Derivatives // Bioorganic & Medicinal Chemistry, 2003, №11, p.3673; Pawar R.В., Mulwad V.V.Synhesis of some biologically active pyrazole, thiazolidinone and azetidinone derivatives // ХГС, 2004, №2, c.257].
Известен способ [Кейко H.А., Степанова Л.Г., Воронков М.Г. и др. Синтез, ДНК-ингибирующая и противоопухолевая активность тиосемикарба-зона 2-формил-2,5-диметокси-2,3-дигидро-4Н-пирана, его этильного аналога и медного комплекса // Хим.-фарм. ж-л. 2002, Т.36, №8, с.11] получения ацилгидразонов (2) конденсацией гидразидов кислот с альдегидами.
Известным способом не могут быть получены N′,N′-бис{[алкил(фенил)сульфанилметил]}арилгидразиды общей формулы (1).
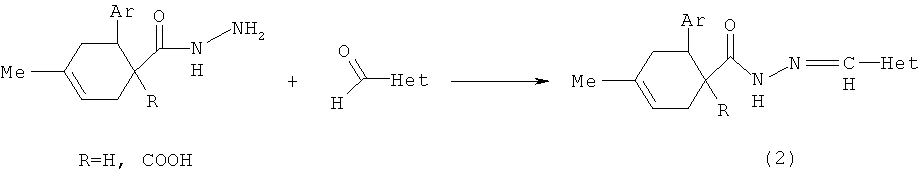
Известен способ [В.Р.Ахметова, P.P.Хайруллина, Т.В.Тюмкина и др. Циклотиометилирование гидразидов карбоновых кислот альдегидами и H2S. Изв. АН. Сер. хим., №2, 2010, с.416] получения N-(1,3,5-дитиазинан-5-ил)амидов (3) реакцией циклотиометилирования гидразидов карбоновых кислот с альдегидами и сероводородом с выходами не более 68% по схеме:
Известным способом не могут быть получены N′,N′-бис{[алкил(фенил)сульфанилметил]}арилгидразиды общей формулы (1).
Таким образом, в литературе отсутствуют сведения о получении N′,N′-бис {[алкил(фенил)сульфанилметил]}арилгидразидов формулы (1).
Предлагается новый способ получения N′,N′-бис{[алкил(фенил)сульфанилметил]}арилгидразидов общей формулы (1).
Сущность способа заключается во взаимодействии арилгидразида общей формулы ArC(O)NHNH2, где Ar=p-C6H4N, м-C6H4N, o-СН3ОС6Н4 (изоникотингидразид, никотингидразид, 2-метоксибензгидразид) с N,N-диметил-N-{[алкил(бензил)сульфанил]метил} амином общей формулы Me2N-CH2-SR, где R=n-Pentyl, i-Pr, Ph, в присутствии катализатора Sm(NO3)3·6H2O, взятыми в мольном соотношении ArC(O)NHNH2:Me2N-CH2-SR: Sm(NO3)3·6H2O=10:20:(0.3-0.7), предпочтительно 10:20:0.5, при температуре 75-85°C (предпочтительно 80°C) и атмосферном давлении в смеси растворителей этиловый спирт - хлороформ (1:1 объемные) в течение 22-26 ч, предпочтительно 24 ч. Выход N′,N′-бис{[алкил(фенил)сульфанилметил]}арилгидразидов (1) составляет 80-98%. Реакция протекает по схеме:
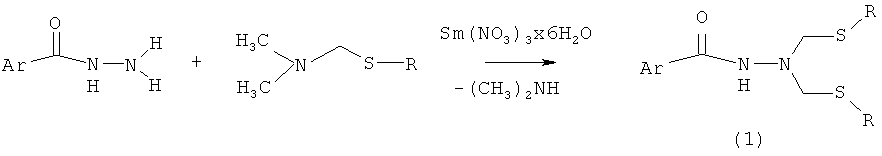
 ,
,  ,
, 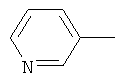 ;
; 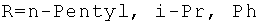
Целевые продукты (1) образуются только лишь с участием арилгидразидов и N,N-диметил-N-{[алкил(бензил)сульфанил]метил} аминов. Исходные реагенты берутся в стехиометрическом соотношении. Изменение соотношения исходных реагентов в сторону увеличения или уменьшения содержания N,N-диметил-N-{[алкил(бензил)сульфанил]метил} аминов по отношению к арилгидразидам приводит к снижению выхода целевых продуктов (1).
Проведение указанной реакции в присутствии катализатора Sm(NO3)3·6H2O больше 0.7 ммолей не приводит к существенному увеличению выхода целевого продукта (1). Использование катализатора Sm(NO3)3·6H2O менее 0.3 ммолей снижает выход (1), что связано, возможно, со снижением каталитически активных центров в реакционной массе. Без катализатора реакция идет с выходом, не превышающим 5%.
Реакции проводили при температуре 80°C. При меньшей температуре (например, 40°C) снижается скорость реакции. В качестве растворителя использовали смесь растворителей этиловый спирт-хлороформ, т.к. в ней хорошо растворимы исходные реагенты и целевые продукты.
Существенные отличия предлагаемого способа:
В известном способе N-(1,3,5-дитиазинан-5-ил)амиды получают взаимодействием гидразидов карбоновых кислот с альдегидами и сероводородом с присутствии эквимольного количества н-BuONa. В предлагаемом способе N′,N′-бис{[алкил(фенил)сульфанилметил]}арилгидразиды (1) получают взаимодействием арилгидразидов с аминосульфидами с участием в качестве катализатора Sm(NO3)3·6H2O.
Предлагаемый способ обладает следующими преимуществами:
Способ позволяет получать с высокой селективностью и выходами N′,N′-бис {[алкил(фенил)сульфанилметил]} арилгидразиды общей формулы (1).
Способ поясняется примерами:
Пример 1. В стеклянный реактор, установленный на магнитной мешалке, помещают 0.24 г (20 ммолей) N,N-диметил-N-[(пентилсульфанил)метил]амина в 2 мл CHCl3, 0.1 г (10 ммолей) изоникотин-гидразида в 2 мл С2Н5ОН, 0.015 г (0.5 ммоль) катализатора кристаллогидрата нитрата самария Sm(NO3)3·6H2O и перемешивают 24 ч при температуре 80°C. Из реакционной массы выделяют N′,N′-бис[(фенилсульфанил)метил]изоникотингидразид (1) с выходом 87%. Другие примеры, подтверждающие способ, приведены в табл.1.
|
Все опыты проводили в смеси растворителей хлороформ-этиловый спирт (1:1, объемные)
Спектральные характеристики N′,N′-бис{[алкил(фенил)сульфанилметил]} арилгидразидов (1).
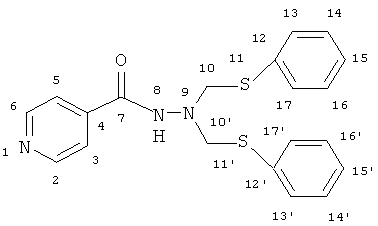
N′,N′-бис[(фенилсульфанил)-метил]изоникотингидразид
ИК-спектр, ν/см-1: 690, 742, 910, 1081, 1267-1306, 1410-1437, 1479, 1551, 1580, 1672, 3054, 3211. Спектр ЯМР 1H δ, м.д.: 4.73 с (4Н, Н10,10'); 7.09-7.65 м (14Н, Ar); 8.59 с (1H, Н8). Спектр ЯМР 13С δ, м.д.: 61.96 с (С10,10'); 120.74 с (С3,5); 127.29 с (С15,15'); 129.40 с (С14,16,14',16'); 130.78 с (С13,17,13',17'); 135.56 с (С12,12'); 139.73 с (С4); 150.32 с (С2,4); 163.07 с (С7). Масс-спектр, m/z (Iотн., %): 420.162 (100) [М+К]+; 404.201 (10) [M+Na]+.
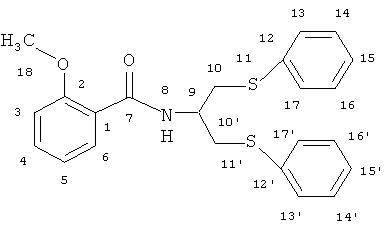
2-Метокси-N′,N′-бис[(фенилсульфанил)метил]бензгидразид
ИК-спектр, ν/см-1: 692, 743, 903, 1023, 1110, 1239-1361, 1481, 1514, 1599, 1666, 1711, 2839, 2942, 3003, 3057, 3303. Спектр ЯМР 1H δ, м.д.: 3.81 с (3H, Н18); 4.76 с (4Н, Н10,10'); 6.90-8.16 м (14Н, Ar); 9.60 с (1H, Н8). Спектр ЯМР 13С δ, м.д.: 55.95 с (С19); 61.97 с (С10,10'); 111.23 с (С3); 114.36 с (С1); 121.19 с (С5); 127.20 с (С15,15'); 127.54 с (С6); 128.91 с (С14,16,14',16'); 130.41 с (С13,17,13',17'); 133.26 с (С4); 135.89 с (С12,12'); 157.44 с (С2); 163.62 с (С7). Масс-спектр, m/z (Iотн., %): 449.145 (100) [М+K]+; 433.186 (30) [M+Na]+.
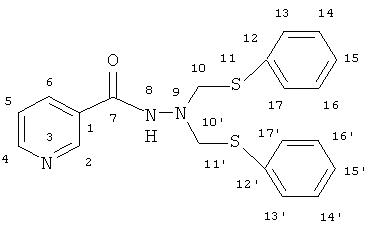
N′,N′-Бис[(фенилсульфанил)-метил] никотингидразид
ИК-спектр, ν/см-1: 691, 738, 906, 1025, 1083, 1196, 1267-1303, 1439, 1479, 1534, 1590, 1667, 2836-2935, 3056. Спектр ЯМР 1H, δ, м.д.: 4.73 с (4Н, Н10,10'); 7.17-7.73 м (13Н, H4,5,6,13-17,13'-17'); 8.45 уш.с (1H, Н2); 8.65 с (1H, Н8). Спектр ЯМР 13С δ, м.д.: 62.01 (С10,10'); 123.31 (С5); 127.23 (С15,15'); 129.07 с (С4); 129.35 (C14,16,14',16'); 130.76 (C13,17,13',17'); 135.09 (С12,12'); 135.59 (С6); 147.75 (С2); 152.43 (С3); 163.70 (С7). Масс-спектр, m/z (Iотн., %): 420.254 (15) [М+K]+; 404.307 (10) [M+Na]+; 382.341 (100) [М+Н]+.
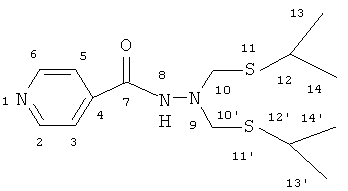
N′,N′-Бис[(изопропилсульфанил)метил]изоникотин-гидразид
ИК-спектр, ν/см-1: 675, 757, 905, 1060, 1242-1303, 1409-1458, 1553, 1601, 1666,2866-2960, 3247. Спектр ЯМР 1H δ, м.д.: 1.30 д (12Н, H13,14,13',14'); 3.13 м (2Н, Н12,12'); 4.27 с (4Н, Н10,10'); 7.61-7.82 м (4Н, Ar); 8.75 с (1Н, Н8). Спектр ЯМР 13С δ, м.д.: 23.22 с (С13,14,13,'14'); 35.46 с (С12,12'); 56.92 с (С10,10'); 120.72 с (С3,5); 140.24 с (С4); 150.38 с (С2,4); 163.36 с (С7). Масс-спектр, m/z (Iотн., %): 314.352 (80) [М+Н]+; 336.313 (50) [M+Na]+; 352.280 (100) [М+К]+.
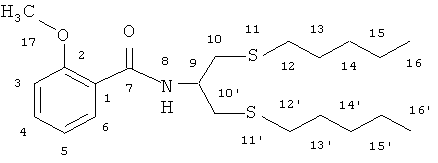
2-Метокси-N′,N′-бис[(пентилсульфанил)метил]бензгидразид
ИК-спектр, ν/см-1: 680, 756, 902, 1022, 1161, 1238-1293, 1481, 1512, 1600, 1668, 2857-2956, 3312, 3403. Спектр ЯМР 1H δ, м.д.: 0.86 т (6Н, Н16,16'); 1.31 м (8Н, Н14,15,14,'15'); 1.62 м (4Н, Н13,13,); 2.68 к (4Н, Н12,12', J 7.2 Гц); 3.99 с (3H, Н17); 4.72 с (4Н, Н10,10'); 6.97 д (1H, Н3, J 8.4 Гц); 7.07 т (1Н, Н4); 7.45 т (1Н, Н5); 8.18 д (1H, Н6, J 8.4 Гц); 9.37 с (1H, Н8). Спектр ЯМР 13С δ, м.д.: 13.90 с (С16,16'); 22.00 с (С15,15'); 29.78 с (С14,14'); 30.40 с (С13,13'); 32.52 с (С12,12'); 55.83 с (С17); 58.44 с (С10,10'); 111.10 с (С3); 120.16 с (С1); 121.11 с (С5); 132.11 с (С6); 132.80 с (С4); 157.06 с (С2); 163.62 с (С7). Масс-спектр, m/z (Iотн., %): 437.279 (100) [М+K]+; 421.321 (10) [M+Na]+.
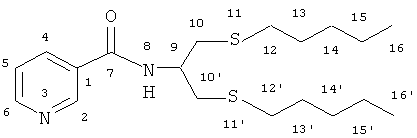
N′,N′-бис[(пентилсульфанил)-метил] никотингидразид
ИК-спектр, ν/см-1: 645, 756, 910, 1042, 1254-1299, 1380-1467, 1535, 1591, 1666, 2780-2956, 3234. Спектр ЯМР 1H δ, м.д.: 0.88 т (6Н, Н16,16'); 1.30 м (8Н, Н14,14',15,15'); 1.61 м (4Н, Н13,13'); 2.69 т (4Н, Н12,12'); 4.27 уш.с (4Н, Н10,10'); 7.41 т (1Н, Н5); 7.73 уш.с (1H, Н2); 8.12 д (1H, Н4, J=7.2 Гц); 8.75 уш.с (1H, Н6); 9.00 уш.с (1Н, Н8). Спектр ЯМР 13С δ, м.д.: 13.95 (С16,16'); 22.25 (С15,15'); 29.68 (С14,14'); 30.94 (С13,13'); 32.79 (С12,12'); 59.01 (С10,10'); 123.60 (С5); 129.20 (С1); 135.28 (С6); 147.98 (С4); 152.66 (С2); 163.83 (С7). Масс-спектр, m/z (Iотн., %): 408.288 (100) [М+K]+; 392.331 (10) [M+Na]+. C18H31N3S2O.
Способ получения N′,N′-бис {[алкил(фенил)сульфанилметил]}арилгидразидов общей формулы (1) , , отличающийся тем, что арилгидразиды общей формулы ArC(O)NHNH[Ar = указанные выше] подвергают взаимодействию с N,N-диметил-N-{[алкил(бензил)сульфанил]метил}аминами общей формулы MeN-CH-SR (R = указанные выше) в присутствии катализатора кристаллогидрата нитрата самария Sm(NO)·6HO, при мольном соотношении ArC(O)NHNH:N,N-диметил-N-{[алкил(бензил)сульфанил]метил}амин : Sm(NO)·6HO = 10:20:(0.3-0.7), при температуре 75-85°C, атмосферном давлении, в смеси растворителей хлороформ-этиловый спирт (1:1 объем.) в течение 22-26 ч.
