Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ 5-МЕТОКСИ-4-АЗАТРИЦИКЛО[4.3.1.1 3,8]УНДЕЦ-4-ЕНА
Вид РИД
Изобретение
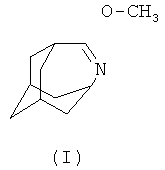
Изобретение относится к способу получения метилового эфира 4-
азатрицикло[4.3.1.13,8]ундекан-5-она (I), который является основным исходным соединением для получения соединений, обладающих высокой фармакологической активностью. В частности, производные 1,2,4-триазола, конденсированные с 4-азатрицикло[4.3.1.13,8]ундеканом, выступают в качестве ингибитора фермента 11-бета-гидроксистероид дегидрогеназы типа I (lip-HSD-1 или HSD-1) [1]. Амидины, полученные конденсацией метилового эфира 4-азатрицикло[4.3.1.13,8]ундекан-5-она (I) с различными моно- и диалкиламинами, обладают высокой активностью против вирусов гриппа типа А Swine, А 2 Japan, В Johannesburg и парагриппозной инфекции Sendai, а так же обладают способностью понижать кровяное давление [2].
Данным изобретением решена задача получения 5-метокси-4-азатрицикло[4.3.1.13,8]ундец-4-ена (I) - ключевого исходного соединения для ряда биологически активных веществ.
Известны методы синтеза 5-метокси-4-азатрицикло[4.3.1.13,8]ундец-4-ена (I) [1, 2] и 5-этокси-4-азатрицикло[4.3.1.13,8]ундец-4-ена (I) [3]. Однако приведенные методы имеют ряд недостатков:
1. Использование дорогостоящих и высокотоксичных реагентов.
2. Длительное время протекания реакции.
3. Применение абсолютных растворителей.
Наиболее близким по технической сущности к заявляемому способу методом является обработка 4-азатрицикло[4.3.1.13,8]ундекан-5-она (II) эквимольным количеством диметилсульфата в абсолютном бензоле [2]. Проведение реакции таким способом требует длительной (22 ч) выдержки реагентов в кипящем бензоле. Существенными недостатками этого метода являются необходимость использовать абсолютный растворитель и длительное время проведения реакции.
Альтернативный подход к получению 5-метокси-4-азатрицикло[4.3.1.13,8]ундец-4-ена (I) предложен авторами [1] и заключается в обработке 4-азатрицикло[4.3.1.13,8]ундекан-5-она (II) метиловым эфиром трифторметансульфокислоты в хлористом метилене. Несмотря на то что реакция протекает в течение 20 мин при температуре кипения хлористого метилена, для достижения удовлетворительного выхода необходимо использование трехкратного избытка дорогостоящего метилового эфира трифторметансульфокислоты, что неоправданно с экономической точки зрения.
Известен способ получения 5-этокси-4-азатрицикло[4.3.1.1']ундец-4-ена, заключающийся во взаимодействии 4-азатрицикло[4.3.1.13,8]ундекан-5-она (II) с эквимольным количеством тетрафторбората триэтилоксония в безводном хлористом метилене в течение 16 ч [3]. Однако ввиду высокой стоимости и токсичности тетрафторбората триэтилоксония использование его представляется нецелесообразным. Длительное время проведения реакции является дополнительным недостатком этого метода.
Полученный нами технический результат - более простой в техническом отношении и экономически эффективный способ получения 5-метокси-4-азатрицикло [4.3.1.13,8] ундец-4-ена (I).
Технический результат достигается тем, что синтез целевого соединения проводили путем метилирования 4-азатрицикло[4.3.1.13,8]ундекан-5-она (II) с диметил сульфатом в мольном соотношении 1:1.0-1,5 без растворителя в течение 3-9 ч при 60-120°С. Разложение реакционной смеси осуществляли с помощью насыщенного раствора гидрокарбоната натрия. Дальнейшей экстракцией из водного раствора хлористым метиленом с последующим упариванием растворителя получали необходимый 5-метокси-4-азатрицикло[4.3.1.1 3,8]ундец-4-ен (I) с выходами, близкими к количественным.
Основные отличительные признаки предлагаемого метода можно сформулировать следующим образом:
1. В предлагаемом методе в качестве алкилирующего агента используется диметилсульфат, являющийся более доступным в сравнении с описанными выше реагентами.
2. Проведение реакции без растворителя полностью соответствует принципам «зеленой химии» и позволяет избежать дополнительных временных затрат на абсолютизацию и регенерацию растворителей.
3. Значительно сокращается время проведения реакции (с 22 ч [2] или 16 ч [1] до 3 ч).
4. Предлагаемый метод не предполагает использование инертной атмосферы, что существенно упрощает схему реактора, и не требует применения сложного и дорогостоящего оборудования.
Получение исходного 4-азатрицикло[4.3.1.13,8]ундекан-5-она (II) проводили по ранее описанному методу [4].
Выполнение метода
Строение синтезированного соединения подтверждено данными ИК и масс-спектров, контроль над ходом реакции и индивидуальность соединения определялись с помощью ТСХ и ГЖХ. ГЖХ анализы проводились на газовом хроматографе «Кристалл 2000М». ИК-спектр записан на спектрометре Shimadzu FTIR-8400S в таблетках бромида калия либо в тонком слое в призмах. Масс-спектр получен на хроматомасс-спектрометре «Finnigan Trace DSQ» при энергии ионизирующих электронов 70 эВ. Элементный анализ выполнен на автоматическом CHNS-анализаторе “Euro Vector ЕА-3000”.
Способ получения 5-метокси-4-азатрицикло[4.3.1.13,8]ундец-4-ена (I)
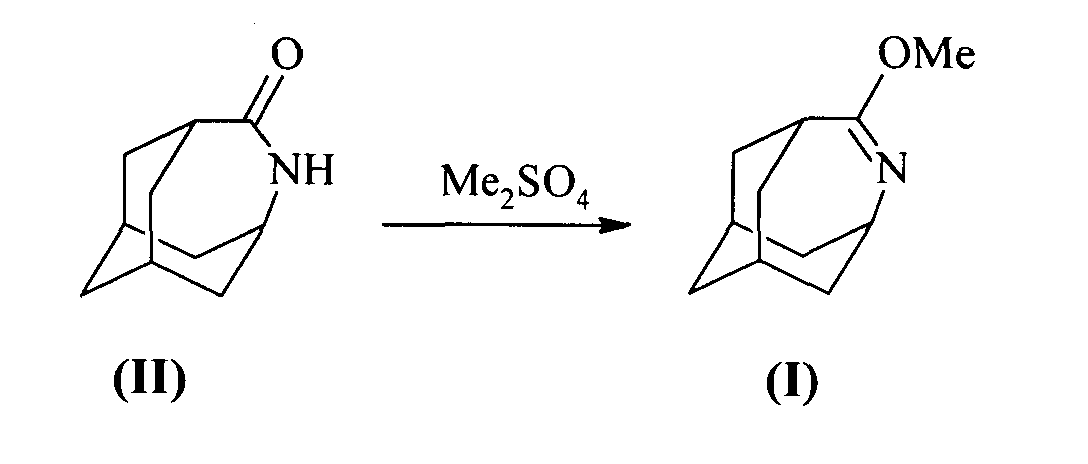
Пример 1. Смесь 16.50 г (0.100 моль) 4-азатрицикло[4.3.1.13,8]ундекан-5-она (II) и 18.90 г (14.18 мл, 0.150 моль) диметилсульфата выдерживали 9 ч при 60°C при перемешивании. После охлаждения смесь нейтрализовали 30 мл насыщенного раствора NaHCO3 до слабощелочной среды, экстрагировали CHCl3, сушили над Na2SO4 и упаривали досуха в вакууме. Выход: 16.47 г (92%). nD 20=1.6383. ИК-спектр, см-1: 2912 (Ad), 1685 (C=N), 1442 (СН3). Масс-спектр, m/z (Iотн, %): 179 (100) [М+]; 164 (53) [М+-СН3]; 148 (24) [М+-ОСН3]; 136 (25) [M+-OCH3-N-CH2]; 122 (23) [М+-57]. Найдено, %: С 73.64; Н 9.60; N 7.82. C11H17NO. Вычислено, %: С 73.70; Н 9.56; N 7.81.
Пример 2. Смесь 16.50 г (0.100 моль) 4-азатрицикло[4.3.1.13,8]ундекан-5-она (II) и 15.75 г (11.82 мл, 0.125 моль) диметилсульфата выдерживали 6 ч при 90°С при перемешивании. После охлаждения смесь нейтрализовали 30 мл насыщенного раствора NaHCO3 до слабощелочной среды, экстрагировали CHCl3, сушили над Na2SO4 и упаривали досуха в вакууме. Выход: 17.18 г (96%).
Пример 3. Смесь 16.50 г (0.100 моль) 4-азатрицикло[4.3.1.13,8]ундекан-5-она (II) и 12.60 г (9.45 мл, 0.100 моль) диметилсульфата выдерживали 3 ч при 120°C при перемешивании. После охлаждения смесь нейтрализовали 30 мл насыщенного раствора NaHCO3 до слабощелочной среды, экстрагировали СНСl3, сушили над Na2SO4 и упаривали досуха в вакууме. Выход: 16.65 г (93%).
Литература
[1] Патент WO 2004/106294 А2. Triazole derivatives as inhibitors of 11-beta hydroxysteroid dehydrogenase-1. / Waddell ST., Santorelli G.M., Maletic M.M., Leeman A.H. -Заявлено 29.05.2003. - Опубликовано 26.05.2004
[2] Keizer V. G., Korsloot J. G., Derivatives of 4-azahomoadamantane. Their synthesis and biological evaluation// J. Med. Chem., vol. 5,1971, p.411-415
[3] Dourin A., Winter D.K., Pichette S., Auber-Nicol S., Lessard J., Spino C. Photochemical Rearrangement of 7V-mesyloxylactams: stereospecific formation of N-heterocycles. // J. Org. Chem., vol. 76,2011,164-169
[4] Korsloot J. G., Keizer V. G., The Beckmann rearrangement of adamantanone oxime// Tetrahedron Lett., 1969, vol.40, p.3517-3520.
Способ получения 5-метокси-4-азатрицикло[4.3.1.1]ундец-4-ена реакцией 4-азатрицикло[4.3.1.1]ундекан-5-она с диметилсульфатом в мольном соотношении 1:1.0-1.5 при температуре 60-120°С в течение 3-9 ч без растворителя.
