Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ [1S-[1α,2α,3β(1S*,2R*),5β]]-3-[7-[2-(3,4-ДИФТОРФЕНИЛ)-ЦИКЛОПРОПИЛАМИНО]-5-(ПРОПИЛТИО)-3H-1,2,3-ТРИАЗОЛО[4,5-d]ПИРИМИДИН-3-ИЛ]-5-(2-ГИДРОКСИЭТОКСИ)-ЦИКЛОПЕНТАН-1,2-ДИОЛА И ЕГО ПРОМЕЖУТОЧНЫХ СОЕДИНЕНИЙ
Вид РИД
Изобретение
Область изобретения
Настоящее изобретение относится к способу получения [1S-[1α,2α,3β(1S*,2R*),5β]]-3-[7-[2-(3,4-дифторфенил)-циклопропиламино]-5-(пропилтио)-3Н-1,2,3-триазоло[4,5-d]пиримидин-3-ил]-5-(2-гидроксиэтокси)-циклопентан-1,2-диола и к промежуточным соединениям, используемым в этом способе.
Предшествующий уровень техники
Было обнаружено, что аденозин-5'-дифосфат (АДФ) действует в качестве ключевого медиатора тромбоза. АДФ-индуцированная агрегация тромбоцитов опосредована рецепторами подтипа P2Y12, локализованными на мембране тромбоцитов. Рецептор P2Y12 (также известный как P2T, P2YADP или P2TAC) представляет собой сопряженный с G-белком рецептор, первично вовлеченный в опосредование активации/агрегации тромбоцитов.
В WO 99/05143 раскрыт в общем ряд соединений триазоло[4,5-d]пиримидина, обладающих активностью в качестве антагонистов P2T (также известного как P2Y12, Р2YADP или Р2ТAC). Недавно был описан новый класс прямых (непролекарственые формы) антагонистов рецептора Р2T, который дает значительные улучшения по сравнению с другими антитромботическими агентами. В публикации международной заявки WO 00/34283 раскрыты новые «прямые» антагонисты рецептора P2T, включая соединение формулы (I). В WO 01/92262 раскрыты кристаллические и аморфные формы соединения формулы (I).
В WO 01/92263 раскрыт способ получения [1S-[1α,2α,3β(1S*,2R*),5β]]-3-[7-[2-(3,4-дифторфенил)-циклопропиламино]-5-(пропилтио)-3H-1,2,3-триазоло[4,5-d]пиримидин-3-ил]-5-(2-гидроксиэтокси)циклопентан-1,2-диола (альтернативно называемого (1S,2S,3R,5S)-3-[7-{[(1R,2S)-2-(3,4-дифторфенил)-циклопропил]амино}-5-(пропилсульфанил)-3H-[1,2,3]триазоло[4,5-d]пиримидин-3-ил]-5-(2-гидроксиэтокси)-1,2-циклопентандиол).
Согласно настоящему изобретению предложен улучшенный способ получения соединения формулы (I). В частности, способ по настоящему изобретению дает более высокий выход соединения формулы (I) по сравнению с предыдущими способами, а также повышенную эффективность способа и более высокую степень чистоты соединения формулы (III). Высокое качество соединения формулы (I) достигается без перекристаллизации.
Краткое описание сущности изобретения
Согласно настоящему изобретению предложен способ получения соединения формулы (I)
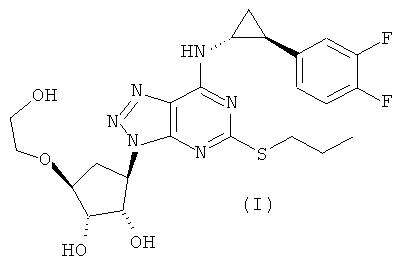
включающий
а) взаимодействие соединения формулы (II)
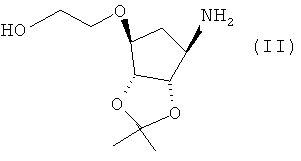
с щавелевой кислотой или дибензоил-L-винной кислотой с образованием соли оксалата или соли дибензоил-L-тартрата соединения формулы (II); и
б) взаимодействие соли соединения формулы (II) с соединением формулы (VI)
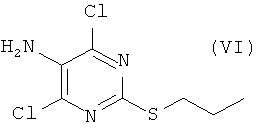
в присутствии третичного амина при температуре от 80° до 115°С при концентрации кислорода менее 2,0% по объему с получением соединения формулы (III)
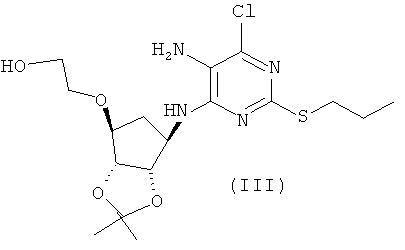
и выделение соединения формулы (III) в кристаллической форме;
в) взаимодействие соединения формулы (III) с уксусной кислотой и нитритом натрия при температуре от 0°С до 40°С с получением соединения формулы (IV)
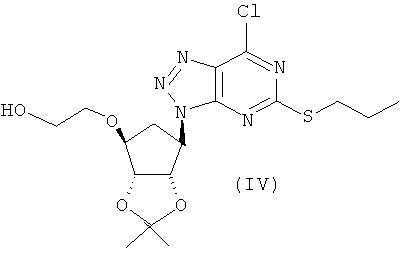
г) взаимодействие соединения формулы (IV) с соединением формулы (VII) при температуре, равной или ниже 40°С,
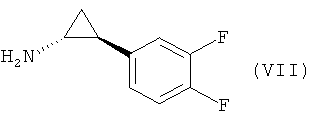
с получением соединения формулы (V)
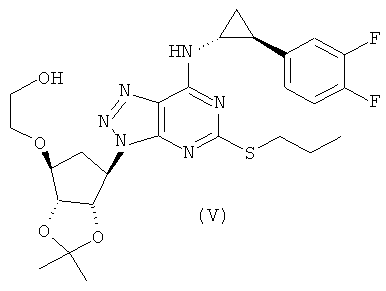
д) снятие защиты с соединения формулы (V) с использованием водного раствора соляной кислоты в метаноле в двухфазной системе с получением соединения формулы (I).
Соединение формулы (II) может быть получено, как описано в WO 01/92263А1.
Соединение формулы (VI) может быть получено, как описано в WO 2005/095358 А2. 4,6-Дихлор-5-нитро-2-(пропилтио)пиримидин также может быть восстановлен до соединения формулы (VI) с использованием методики, описанной в ЕР 0931053, ЕР 0842920 или при применении типов систем реагентов для восстановления ароматических нитрогрупп, отличных от комбинированных катализаторов платина/ванадий, как описано, например, в R. Larock Comprehensive Organic Transformations, ISBN 0-89573-710-8, VCH Publishers Inc., 1989, p.411.
В одном воплощении стадию (а) проводят в этаноле или в смеси воды и этанола. В одном воплощении смесь нагревают до примерно 40-70°С. В одном воплощении щавелевую кислоту добавляют к соединению формулы (II) и смесь нагревают до примерно 60-70°С с последующим добавлением изопропилацетата в течение периода времени 1-3 часа и образованную суспензию охлаждают до примерно 20-30°С в течение примерно 1-3 часов. В одном воплощении осажденное твердое вещество выделяют, перед тем как осуществить дальнейшее взаимодействие.
В одном воплощении стадию (а) проводят в этаноле. В одном воплощении стадию (а) проводят путем добавления дибензоил-L-винной кислоты к соединению формулы (II) при примерно 40-60°С. После перемешивания смеси в течение периода времени от 30 минут до 2 часов эту смесь можно охладить до примерно 5-25°С в течение примерно 1-4 часов. В одном воплощении осажденное твердое вещество выделяют, перед тем как осуществить дальнейшее взаимодействие.
Стадию (б) проводят при температуре 80-115°С. В одном воплощении стадию (б) проводят при температуре 80-100°С. В одном воплощении используемый третичный амин представляет собой триэтиламин. В одном воплощении растворитель, используемый на стадии (б), выбран из этанола, изопропилового спирта, этиленгликоля, триэтиленгликоля, трет-бутилового спирта, изобутилового спирта и диметоксиэтана. В одном воплощении растворитель, используемый на стадии (б), выбран из этанола, изопропилового спирта или этиленгликоля. В одном воплощении стадию (б) проводят в этиленгликоле. В одном воплощении соединение формулы (VI) загружают в избытке. В одном воплощении взаимодействие проводят при атмосферном давлении или при давлении на 0,5-1,5 бар (0,05-0,15 МПа) выше атмосферного давления. В одном воплощении концентрация кислорода составляет менее 1,0% по объему. В одном воплощении концентрация кислорода составляет менее 0,5% по объему.
Стадию (в) проводят при температуре примерно от 0°С до 40°С. В одном воплощении стадию (в) проводят при комнатной температуре, то есть при 20°С-30°С. В одном воплощении взаимодействие проводят в толуоле. В одном воплощении продукт стадии (в) используют на последующей реакционной стадии без выделения. В одном воплощении толуольный раствор соединения формулы (IV) используют непосредственно на следующей стадии без перегонки.
Стадию (г) в одном воплощении проводят при температуре примерно 10-30°С. В одном воплощении соединение формулы (VII) добавляют в реакционную смесь с такой скоростью, чтобы поддерживать температуру реакции при 30°С или ниже. В одном воплощении продукт стадии (в) растворяют в толуоле. В одном воплощении соединение формулы (VII) растворяют в водном растворе карбоната калия и взаимодействие проводят в двухфазной системе. В одном воплощении продукт взаимодействия стадии (г) промывают уксусной кислотой.
Стадию (д) проводят в двухфазной системе. В одном воплощении продукт стадии (г) в толуоле смешивают с метанолом и концентрированным водным раствором соляной кислоты. В одном воплощении NаНСО3 добавляют в реакционную смесь в пределах 5 часов после добавления водного раствора соляной кислоты. В одном воплощении взаимодействие проводят при температуре 10-20°С.
ПРИМЕРЫ
Пример 1. Получение (3аS,4R,6S,6аR)-6-(2-гидроксиэтокси)-2,2-диметилтетрагидро-3аH-циклопента[d][1,3]диоксол-4-аминия оксалата
К этанольному раствору (3аS,4R,6S,6аR)-6-(2-гидроксиэтокси)-2,2-диметилтетрагидро-3аН-циклопента[d][1,3]диоксол-4-амина (приблизительно 100 кг в приблизительно 320 кг этанола, полученный, как описано в WO 01/92263) загружали воду (30 кг). Смесь нагревали до 65°С и добавляли щавелевую кислоту × 2 H2O (57 кг). Добавляли изопропилацетат (665 кг) в течение 2 часов и полученную суспензию охлаждали до 20°С в течение 2 часов. Охлажденную суспензию поддерживали при этой температуре в течение еще 2 часов. Осажденный продукт выделяли, промывали изопропилацетатом (141 кг) и сушили под вакуумом с получением указанного в заголовке соединения в виде белого твердого вещества (116 кг, приблизительно 82%).1H ЯМР (400 МГц, ДМСО-d6) δ 6.51 (кажущийся уширенный s, NH2, СООН и ОН протоны), 4.70 (кажущийся d, J=6 Гц, 1Н), 4.61 (кажущийся d, J=6 Гц, 1Н), 3.91 (кажущийся уширенный s, 1Н), 3.40-3.59 (m, 5Н), 2.12-2.23 (m, 1Н), 1.89-2.01 (m, 1Н), 1,36 (s, 3Н), 1.23 (s, 3H). 13C ЯМР (100 МГц, ДМСО-d6) δ 164.7, 110.8, 82.8, 82.7, 82.1, 70.5, 60.0, 55.1, 32.5, 26.1, 23.9.
Пример 2. Получение бис[(3аS,4R,6S,6аR)-6-(2-гидроксиэтокси)-2,2-диметилтетрагидро-3аН-циклопента[d][1,3]диоксол-4-аминия] 2,3-бис(бензоилокси)сукцината
К этанольному раствору дибензоил-L-винной кислоты (82 кг в 126 кг этанола) добавляли раствор (3а3,4R,6S,6аR)-6-(2-гидроксиэтокси)-2,2-диметилтетрагидро-3аH-циклопента[d][1,3]диоксол-4-амина в этаноле (приблизительно 100 кг в приблизительно 320 кг этанола, полученный, как описано в WO 01/92263) при 50°С. Полученную смесь перемешивали в течение 1 часа при 50°С и затем охлаждали до 10°С в течение 3 часов.
Продукт выделяли, промывали этанолом (150 кг) и сушили под вакуумом с получением указанного в заголовке соединения в виде белого твердого вещества (157 кг, выход приблизительно 86%). 1Н ЯМР (400 МГц, ДМСО-d6) δ 7.96 (кажущийся d, J=8 Гц, 4Н), 7.59-7.66 (m, 2H), 7.50, (кажущийся t, J=8 Гц, 4H), 5.63 (s, 2H), 4.47-4.57 (m, 4Н), 3.73-3.80 (m, 2H), 3.37-3.55 (m, 8H), 3.25-3.34 (m, 2H), 1.93-2.05 (m, 2H), 1.73-1.84 (m, 2H), 1.31 (s, 6H), 1.17 (s, 6H). 13C ЯМР (100 МГц, ДМСО-d6) 5 168.7, 164.9, 133.0, 130.2, 129.1, 128.4, 110.3, 83.6, 83.2, 82.9, 73.3, 70.3, 60.0, 55.5, 33.1, 26.1, 23.9.
Пример 3. Получение 2-[((3аR,4S,6R,6аS)-6-{[5-амино-6-хлор-2-(пропилтио)пиримидин-4-ил]амино}-2,2-диметилтетрагидро-3аH-циклопента[d][1,3]диоксол-4-ил)окси]этанола
4,6-Дихлор-5-нитро-2-(пропилтио)пиримидин (71 кг) и катализатор платина/ванадий (платина и ванадий на угле, 2% Pt и 1% V, 11,15 кг) загружали вместе с метил-трет-бутиловым эфиром (298 кг). Эту смесь охлаждали до приблизительно 5°С и прикладывали давление водорода 8 бар (0,8 МПа) (давление медленно повышали, чтобы контролировать экзотермический эффект). Реакционную смесь перемешивали в течение 9 часов при 30°С и давлении водорода 8 бар (0,8 МПа) и контролировали превращение (>99%). Катализатор отфильтровывали и промывали метил-трет-бутиловым эфиром (117 кг). Гидрирование повторяли со второй порцией 4,6-дихлор-5-нитро-2-(пропилтио)пиримидина (71 кг). Два раствора после гидрирования объединяли. Воду отделяли и органический слой перегоняли при пониженном давлении и при температуре рубашки 30°С. В полученное коричневое масло загружали этиленгликоль (221 кг) и перегонку продолжали до тех пор, пока метил-трет-бутиловый эфир не был полностью отогнан.
К смеси этиленгликоля и 4,6-дихлор-2-(пропилтио)пиримидин-5-амина добавляли (3аS,4R,6S,6аR)-6-(2-гидроксиэтокси)-2,2-диметилтетрагидро-3аH-циклопента[d][1,3]диоксол-4-аминия оксалат (118 кг) и триэтиламин (161 кг). Полученную реакционную смесь делали инертной и нагревали до 100°С в течение 3 часов и выдерживали при этой температуре в течение 9 часов и затем охлаждали до приблизительно 40°С. Добавляли изопропилацетат (740 кг) и воду (644 кг) и эту смесь перемешивали в течение 30 минут при 40°С. Перемешивание прекращали и фазы оставляли для разделения, водный слой отбрасывали. Органический слой промывали водой (644 кг) и фазы снова разделяли. Органический слой концентрировали посредством вакуумной перегонки при температуре рубашки 55°С для удаления воды; добавляли дополнительные порции изопропилацетата (2×130 кг). Когда необходимое содержание воды было достигнуто, концентрацию 2-[((3aR,4S,6R,6aS)-6-{[5-амино-6-хлор-2-(пропилтио)пиримидин-4-ил]амино}-2,2-диметилтетрагидро-3аH-циклопента[d][1,3]диоксол-4-ил)окси]этанола доводили до приблизительно 30% (28%) (в расчете на 2-[((3аR,4S,6R,6аS)-6-{[5-амино-6-хлор-2-(пропилтио)пиримидин-4-ил]амино}-2,2-диметилтетрагидро-3аH-циклопента[d][1,3]диоксол-4-ил)окси]этанол). Этот раствор нагревали до 62°С и добавляли изооктан (1150 кг, предварительно нагретый до 63°С) в течение 30 минут. В эту смесь вводили затравку 2-[((3аR,4S,6R,6аS)-6-{[5-амино-6-хлор-2-(пропилтио)пиримидин-4-ил]амино}-2,2-диметилтетрагидро-3аH-циклопента[d][1,3]диоксол-4-ил)окси]этанола (0,9 кг), перемешивали при 62°С в течение 30 минут и затем охлаждали до 0°С в течение 7 часов. Через 1 час при 0°С осажденный продукт выделяли, промывали предварительно охлажденной (0°С) смесью изопропилацетата (63 кг) и изооктана (182 кг). Наконец, продукт промывали изооктаном (232 кг) и сушили под вакуумом с получением указанного в заголовке соединения в виде твердого вещества от белого до беловатого цвета (143 кг; 88%).
Пример 4. Получение 2-[((3аR,4S,6R,6аS)-6-{[5-амино-6-хлор-2-(пропилтио)пиримидин-4-ил]амино}-2,2-диметилтетрагидро-3аН-циклопента[d][1,3]диоксол-4-ил)окси]этанола
4,6-Дихлор-5-нитро-2-(пропилтио)пиримидин (600 кг; 100%) и катализатор платина/ванадий (платина и ванадий на угле, 2% Pt и 1% V, 46 кг; 100%) загружали вместе с метил-трет-бутиловым эфиром (2492 кг). Прикладывали давление водорода 8 бар (0,8 МПа) в течение некоторого периода при одновременном нагревании до 65°С. Эту реакционную смесь перемешивали в течение 3 часов при 65°С и давлении водорода 8 бар (0,8 МПа) и контролировали превращение (>99%). Катализатор отфильтровывали и промывали метил-трет-бутиловым эфиром (1240 кг). Воду отделяли и органический слой перегоняли при пониженном давлении и при температуре рубашки 30°С. В полученное коричневое масло загружали этиленгликоль (880 кг) и перегонку продолжали до тех пор, пока метил-трет-бутиловый эфир не был полностью отогнан.
К смеси этиленгликоля и 4,6-дихлор-2-(пропилтио)пиримидин-5-амина добавляли (3аS,4R,6S,6аR)-6-(2-гидроксиэтокси)-2,2-диметилтетрагидро-3аH-циклопента[d][1,3]диоксол-4-аминия оксалат (530 кг) и триэтиламин (707 кг). Полученную реакционную смесь делали инертной и нагревали до 100°С и выдерживали при этой температуре в течение 9 часов и затем охлаждали до приблизительно 40°С. Добавляли изопропилацетат (3185 кг) и воду (2773 кг) и смесь перемешивали в течение 30 минут при 40°С. Перемешивание прекращали и фазы оставляли для разделения, водный слой отбрасывали. Органический слой промывали водой (2773 кг) и фазы снова разделяли. Органический слой концентрировали посредством вакуумной перегонки при температуре рубашки 55°С для удаления воды; добавляли дополнительные порции изопропилацетата (1706 кг). Когда необходимое содержание воды было достигнуто, концентрацию 2-[((3аR,4S,6R,6аS)-6-{[5-амино-6-хлор-2-(пропилтио)пиримидин-4-ил]амино}-2,2-диметилтетрагидро-3аН-циклопента[d][1,3]диоксол-4-ил)окси]этанола доводили до приблизительно 27% (в расчете на 2-[((3аR,4S,6R,6аS)-6-{[5-амино-6-хлор-2-(пропилтио)-пиримидин-4-ил]амино}-2,2-диметилтетрагидро-3аH-циклопента[d][1,3]диоксол-4-ил)окси]-этанол). Этот раствор нагревали до 62°С и добавляли изооктан (5051 кг, предварительно нагретый до 63°С) в течение 30 минут. В эту смесь вводили затравку 2-[((3аR,4S,6R,6аS)-6-{[5-амино-6-хлор-2-(пропилтио)пиримидин-4-ил]-амино}-2,2-диметилтетрагидро-3аН-циклопента[d][1,3]диоксол-4-ил)окси]-этанола (0,9 кг) при 62°С и 58°С и затем охлаждали до 0°С в течение 7 часов. Через 1 час при 0°С осажденный продукт выделяли за несколько загрузок центрифуги, промывали предварительно охлажденной (0°С) смесью изопропилацетата и изооктана. Наконец, продукт промывали изооктаном и сушили под вакуумом с получением указанного в заголовке соединения в виде твердого вещества от белого до беловатого цвета (610 кг; 84%).
Пример 5. Получение 2-({(3аR,4S,6R,6аS)-6-[7-хлор-5-(пропилтио)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-3-ил]-2,2-диметилтетрагидро-3аН-циклопента[d][1,3]диоксол-4-ил}окси)этанола
К 2-[((3аR,4S,6R,6аS)-6-{[5-амино-6-хлор-2-(пропилтио)пиримидин-4-ил]-амино}-2,2-диметилтетрагидро-3аН-циклопента[d][1,3]диоксол-4-ил)окси]-этанолу (180 кг) в толуоле (749 кг) и уксусной кислоте (153 кг) добавляли нитрит натрия (33,2 кг) в воде (88 кг), загружаемый с такой скоростью, чтобы поддерживать температуру реакции ≤30°С. После того как был достигнут критерий превращения (>99%), к этому реакционному раствору добавляли карбонат калия (176 кг) в воде (360 кг), после чего водный слой отделяли, а органический слой использовали на следующей стадии.
Пример 6. Получение 2-({(3аR,4S,6R,6аS)-6-[7-хлор-5-(пропилтио)-3Н-[1,2,3]-триазоло[4,5-d]пиримидин-3-ил]-2,2-диметилтетрагидро-3аН-циклопента[d][1,3]диоксол-4-ил}окси)этанола 2-[((3аR,4S,6R,6аS)-6-{[5-Амино-6-хлор-2-(пропилтио)пиримидин-4-ил]-амино}-2,2-диметилтетрагидро-3аН-циклопента[d][1,3]диоксол-4-ил)окси]этанол (320 кг) и нитрит натрия (61 кг) растворяли в смеси воды (224 кг) и толуола (1450 кг) при комнатной температуре. Загружали уксусную кислоту (276 кг) с такой скоростью, чтобы поддерживать температуру реакции:≤30°С. После достижения полного превращения (≥99,9%) к этому реакционному раствору добавляли карбонат калия (317 кг), растворенный в воде (640 кг). После экстракции водный слой отделяли, а органический слой использовали на следующей стадии.
Пример 7. Получение 2-({(3aR,4S,6R,6aS)-6-[7-{[(1R,2S)-2-(3,4-дифторфенил)циклопропил]амино}-5-(пропилтио)-3H-[1,2,3]триазоло[4,5-d]пиримидин-3-ил]-2,2-диметилтетрагидро-3аH-циклопента[d][1,3]диоксол-4-ил}окси)этанола
транс-(1R,2S)-2-(3,4-Дифторфенил)циклопропанаминия (2R)-2-гидрокси-2-фенилэтаноат (146 кг, полученный, как описано в WO 2008/018822, WO 2008/018823, WO 01/92200) и карбонат калия (156 кг) растворяли в воде (576 кг) и загружали в раствор 2-({(3аR,4S,6R,6аS)-6-[7-хлор-5-(пропилтио)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-3-ил]-2,2-диметилтетрагидро-3аH-циклопента[d][1,3]диоксол-4-ил}окси)этанола с такой скоростью, чтобы поддерживать температуру реакции ≤30°С. После того как был достигнут критерий превращения (>99%), водный слой отделяли. Органический слой дважды промывали уксусной кислотой (18 кг) и хлоридом натрия (13 кг) в воде (560 кг) и затем дважды хлоридом натрия (54 кг) в воде (438 кг), после чего этот органический слой использовали на следующей стадии.
Пример 8. Получение 2-({(3aR,4S,6R,6aS)-6-[7-{[(1R,2S)-2-(3,4-дифторфенил)-циклопропил]амино}-5-(пропилтио)-3H-[1,2,3]триазоло[4,5-d]пиримидин-3-ил]-2,2-диметилтетрагидро-3аН-циклопента[d]1,3]диоксол-4-ил}окси)этанола
транс-(1R,2S)-2-(3,4-Дифторфенил)циклопропанаминия (2R)-2-гидрокси-2-фенилэтаноат (258 кг) и карбонат калия (280 кг) растворяли в воде (1024 кг) и загружали в раствор 2-({(3аR,4S,6R,6аS)-6-[7-хлор-5-(пропилтио)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-3-ил]-2,2-диметилтетрагидро-3аH-циклопента[d][1,3]диоксол-4-ил}окси)этанола из вышеприведенного примера 5 с такой скоростью, чтобы поддерживать температуру реакции ≤30°С. После достижения полного превращения (≥99,9%) водный слой отделяли. Органический слой промывали смесью уксусной кислоты (96 кг) и хлорида натрия (96 кг) в воде (768 кг) и затем снова промывали смесью уксусной кислоты (32 кг) и хлорида натрия (22 кг) в воде (952 кг). Третью промывку органического слоя проводили хлоридом натрия (96 кг) в воде (864 кг), после чего этот органический слой использовали на следующей стадии.
Пример 9. Получение [1S-[1α,2α,3β(1S*,2R*),5β]]-3-[7-[2-(3,4-дифторфенил)-циклопропиламино]-5-(пропилтио)-3H-1,2,3-триазоло[4,5-d]пиримидин-3-ил]-5-(2-гидроксиэтокси)циклопентан-1,2-диола
Упомянутый выше раствор 2-({3aR,4S,6R,6aS)-6-[7-{[(1R,2S)-2-(3,4-дифторфенил)циклопропил]амино}-5-(пропилтио)-3H-[1,2,3]триазоло[4,5-d]пиримидин-3-ил]-2,2-диметилтетрагидро-3аH-циклопента[d][1,3]диоксол-4-ил}окси)этанола охлаждали до 15°С, загружали раствор концентрированной водной соляной кислоты (465 кг) в метаноле (623 кг), также охлажденный до 15°С. Эту реакционную смесь перемешивали при 15°С до тех пор, пока не был достигнут критерий превращения (>97%), и фазы оставляли для разделения. Метанольно-водный слой, содержащий продукт, добавляли к бикарбонату натрия (404 кг) в воде (749 кг), поддерживая температуру ниже 22°С. При значении рН ≥6 водный слой экстрагировали этилацетатом (756 кг) и фазы разделяли. Водный слой снова промывали этилацетатом (1080 кг), после чего водный слой отбрасывали. Этилацетатные слои объединяли и промывали один раз водой (490 кг).
Содержание воды в оставшемся этилацетатном растворе снижали до ≤0,8% (мас./мас.) посредством вакуумной перегонки при 50°С с последующей осветляющей фильтрацией и концентрацию доводили до 6,2 л/кг 2-[((3аR,4S,6R,6аS)-6-{[5-амино-6-хлор-2-(пропилтио)пиримидин-4-ил]амино}-2,2-диметилтетрагидро-3аН-циклопента[d][1,3]диоксол-4-ил)окси]этанола. Эту смесь нагревали до 50°С и затем добавляли изооктан (1152 кг) в течение 45 минут. Суспензию охлаждали до 0°С в течение 2,5 часов и затем поддерживали при этой температуре в течение 3,5 часов. Продукт выделяли и промывали холодной (<5°С) смесью этилацетата (722 кг) и изооктана (828 кг). Наконец, выделенный продукт сушили под вакуумом с получением указанного в заголовке соединения в виде белого твердого вещества (203 кг, 90% в расчете на 2-[((3аR,4S,6R,6аS)-6-{[5-амино-6-хлор-2-(пропилтио)пиримидин-4-ил]амино}-2,2-диметилтетрагидро-3аН-циклопента[d][1,3]диоксол-4-ил)окси]этанол).
Пример 10. Получение [1S-[1α,2α,3β(1S*,2R*),5β]]-3-[7-[2-(3,4-дифторсренил)-циклопропиламино]-5-(пропилтио)-3H-1,2,3-триазоло[4,5-d]пиримидин-3-ил]-5-(2-гидроксиэтокси)циклопентан-1,2-диола
Раствор 2-({(3аR,4S,6R,6а3)-6-[7-{[(1R,2φ)-2-(3,4-дифторфенил)-циклопропил]амино}-5-(пропилтио)-3H-[1,2,3]триазоло[4,5-d]пиримидин-3-ил]-2,2-диметилтетрагидро-3аН-циклопента[d][1,3]диоксол-4-ил}окси)этанола (430 кг) в толуоле (1448 кг) охлаждали до 15°С. Загружали раствор концентрированной водной соляной кислоты (831 кг) в метаноле (933 кг), также охлажденный до 15°С, и эту реакционную смесь интенсивно перемешивали при 15°С в течение 2 часов, а затем две фазы оставляли для разделения. Метанольно-водный слой, содержащий продукт, добавляли к суспензии бикарбоната натрия (745 кг) в воде (1024 кг), поддерживая температуру 15-25°С. Значение доведенного рН составило рН 8 после окончания гашения (критерий рН ≥6), и водный слой затем экстрагировали этилацетатом (969 кг). Этилацетатную фазу и некоторое количество водной фазы переносили посредством декантации в другой реактор. Водный слой второй раз промывали этилацетатом (289 кг) и эту вторую этилацетатную фазу и некоторое количество водной фазы переносили посредством декантации в другой реактор. Водный слой третий раз промывали этилацетатом (289 кг) и эту третью этилацетатную фазу и некоторое количество водной фазы переносили посредством декантации в другой реактор. Фазы разделяли и водную фазу отбрасывали. Этилацетатную фазу промывали раствором хлорида натрия (150 кг), растворенного в воде (434 кг). Смесь перемешивали в течение 30 минут при 24°С, после чего перемешивание прекращали и фазы оставляли для разделения. Водную фазу затем отбрасывали и снова загружали этилацетат (1556 кг) в этилацетатную фазу при 24°С. Эту смесь фильтровали через угольные фильтровальные пластины с последующей фильтрацией через фильтр с фильтровальными пластинами из бумаги К200. Фильтры промывали этилацетатом (492 кг) при 24°С и эту промывочную порцию объединяли с отфильтрованным этилацетатным раствором. Содержание воды в этилацетатном растворе снижали далее до 0,4% (мас./мас.) посредством вакуумной перегонки при 50°С и объем доводили до 2200 л (критерий 6,88 л/кг 2-[((3aR,4S,6R,6aS)-6-{[5-aминo-6-xлop-2-(пpoпилтиo)пиpимидин-4-ил]aминo}-2,2-диметилтетрагидро-3аH-циклопента[d][1,3]диоксол-4-ил)окси]этанола). Эту смесь нагревали до 57°С с получением прозрачного раствора и затем его охлаждали до 50°С перед добавлением изооктана (1435 кг) в течение 1,72 часа. Полученную суспензию охлаждали до 0°С в течение 2,35 часа и затем выдерживали при этой температуре в течение 2,33 часа. Продукт выделяли и промывали холодной (примерно 0°С) смесью этилацетата (828 кг) и изооктана (724 кг). Наконец, выделенный продукт сушили под вакуумом при 40°С с получением указанного в заголовке соединения в виде белого твердого вещества (328 кг, 82% в расчете на 2-[((3аR,4S,6R,6аS)-6-{[5-амино-6-хлор-2-(пропилтио)пиримидин-4-ил]амино}-2,2-диметилтетрагидро-3аН-циклопента[d][1,3]диоксол-4-ил)окси]этанол).
Расчет выхода
|
![СПОСОБ ПОЛУЧЕНИЯ [1S-[1α,2α,3β(1S*,2R*),5β]]-3-[7-[2-(3,4-ДИФТОРФЕНИЛ)-ЦИКЛОПРОПИЛАМИНО]-5-(ПРОПИЛТИО)-3H-1,2,3-ТРИАЗОЛО[4,5-d]ПИРИМИДИН-3-ИЛ]-5-(2-ГИДРОКСИЭТОКСИ)-ЦИКЛОПЕНТАН-1,2-ДИОЛА И ЕГО ПРОМЕЖУТОЧНЫХ СОЕДИНЕНИЙ](https://fips.edrid.ru/images/rid/0f/5a/94/1ad151979e25eaaa15d110b76813b908.png)
![СПОСОБ ПОЛУЧЕНИЯ [1S-[1α,2α,3β(1S*,2R*),5β]]-3-[7-[2-(3,4-ДИФТОРФЕНИЛ)-ЦИКЛОПРОПИЛАМИНО]-5-(ПРОПИЛТИО)-3H-1,2,3-ТРИАЗОЛО[4,5-d]ПИРИМИДИН-3-ИЛ]-5-(2-ГИДРОКСИЭТОКСИ)-ЦИКЛОПЕНТАН-1,2-ДИОЛА И ЕГО ПРОМЕЖУТОЧНЫХ СОЕДИНЕНИЙ](https://fips.edrid.ru/images/rid/0f/5a/94/6420d2a3d04355dfb70fbdc4bac160de.png)
![СПОСОБ ПОЛУЧЕНИЯ [1S-[1α,2α,3β(1S*,2R*),5β]]-3-[7-[2-(3,4-ДИФТОРФЕНИЛ)-ЦИКЛОПРОПИЛАМИНО]-5-(ПРОПИЛТИО)-3H-1,2,3-ТРИАЗОЛО[4,5-d]ПИРИМИДИН-3-ИЛ]-5-(2-ГИДРОКСИЭТОКСИ)-ЦИКЛОПЕНТАН-1,2-ДИОЛА И ЕГО ПРОМЕЖУТОЧНЫХ СОЕДИНЕНИЙ](https://fips.edrid.ru/images/rid/0f/5a/94/29af2d006e30932633377425d6929c94.png)
![СПОСОБ ПОЛУЧЕНИЯ [1S-[1α,2α,3β(1S*,2R*),5β]]-3-[7-[2-(3,4-ДИФТОРФЕНИЛ)-ЦИКЛОПРОПИЛАМИНО]-5-(ПРОПИЛТИО)-3H-1,2,3-ТРИАЗОЛО[4,5-d]ПИРИМИДИН-3-ИЛ]-5-(2-ГИДРОКСИЭТОКСИ)-ЦИКЛОПЕНТАН-1,2-ДИОЛА И ЕГО ПРОМЕЖУТОЧНЫХ СОЕДИНЕНИЙ](https://fips.edrid.ru/images/rid/0f/5a/94/dce6a6286066d5a40dc85dd97483487d.png)
![СПОСОБ ПОЛУЧЕНИЯ [1S-[1α,2α,3β(1S*,2R*),5β]]-3-[7-[2-(3,4-ДИФТОРФЕНИЛ)-ЦИКЛОПРОПИЛАМИНО]-5-(ПРОПИЛТИО)-3H-1,2,3-ТРИАЗОЛО[4,5-d]ПИРИМИДИН-3-ИЛ]-5-(2-ГИДРОКСИЭТОКСИ)-ЦИКЛОПЕНТАН-1,2-ДИОЛА И ЕГО ПРОМЕЖУТОЧНЫХ СОЕДИНЕНИЙ](https://fips.edrid.ru/images/rid/0f/5a/94/65ed78f68cc53cd7c87cb4ce56c99573.png)
![СПОСОБ ПОЛУЧЕНИЯ [1S-[1α,2α,3β(1S*,2R*),5β]]-3-[7-[2-(3,4-ДИФТОРФЕНИЛ)-ЦИКЛОПРОПИЛАМИНО]-5-(ПРОПИЛТИО)-3H-1,2,3-ТРИАЗОЛО[4,5-d]ПИРИМИДИН-3-ИЛ]-5-(2-ГИДРОКСИЭТОКСИ)-ЦИКЛОПЕНТАН-1,2-ДИОЛА И ЕГО ПРОМЕЖУТОЧНЫХ СОЕДИНЕНИЙ](https://fips.edrid.ru/images/rid/0f/5a/94/ef03e035fb36a53672bce391182cb091.png)
![СПОСОБ ПОЛУЧЕНИЯ [1S-[1α,2α,3β(1S*,2R*),5β]]-3-[7-[2-(3,4-ДИФТОРФЕНИЛ)-ЦИКЛОПРОПИЛАМИНО]-5-(ПРОПИЛТИО)-3H-1,2,3-ТРИАЗОЛО[4,5-d]ПИРИМИДИН-3-ИЛ]-5-(2-ГИДРОКСИЭТОКСИ)-ЦИКЛОПЕНТАН-1,2-ДИОЛА И ЕГО ПРОМЕЖУТОЧНЫХ СОЕДИНЕНИЙ](https://fips.edrid.ru/images/rid/0f/5a/94/9809deb21420a145f620fafe128967a2.png)
![СПОСОБ ПОЛУЧЕНИЯ [1S-[1α,2α,3β(1S*,2R*),5β]]-3-[7-[2-(3,4-ДИФТОРФЕНИЛ)-ЦИКЛОПРОПИЛАМИНО]-5-(ПРОПИЛТИО)-3H-1,2,3-ТРИАЗОЛО[4,5-d]ПИРИМИДИН-3-ИЛ]-5-(2-ГИДРОКСИЭТОКСИ)-ЦИКЛОПЕНТАН-1,2-ДИОЛА И ЕГО ПРОМЕЖУТОЧНЫХ СОЕДИНЕНИЙ](https://fips.edrid.ru/images/rid/0f/5a/94/d46632054335ee661a3e59520b6c0ba2.png)

