Результат интеллектуальной деятельности: РАСТВОР ДЛЯ ХРАНЕНИЯ РОГОВИЦЫ
Вид РИД
Изобретение
Изобретение относится к области медицины, в частности к офтальмологии, и может быть использовано для длительного сохранения роговичного трансплантата, используемого для послойной и сквозной кератопластик.
Кератопластика широко используется для восстановления зрения при дистрофических, дегенеративных и воспалительных процессах роговицы. Главной проблемой такого метода лечения является отсутствие оптимальных сред для сохранения жизнедеятельности клеточных элементов важной оптической оболочки глаза, какой является роговица.
Среди сред, используемых для консервации, известна среда McCarey-Kaufman, включающая среду 199, буферный раствор HEPES 25 мМоль, декстран 40 кДа, и гентамицин [American journal of ophthalmology, vol.79, N 1, 1975, с.115-120]. Недостатками данной среды являются: отек стромы за счет падения энергетического потенциала эндотелия, определяющего жизнеспособность и трансплантабельность (через 72 ч), достаточно узкий профиль антибиотика, входящего в среду (гентамицин), а также отсутствие противогрибковой защиты.
Известен раствор для консервации роговицы, содержащий HEPES буфер, 1%-ный раствор декстрана, ионы натрия, калия, магния в виде растворимых солей 1%-ного содержания, антибиотики широкого спектра действия в ед. активности, противогрибковые препараты в ед. активности, BSS раствор [заявка RU 2007101966, опубликована 27.07.2008].
Известен раствор для хранения роговицы, содержащий гиалуроновую кислоту с молекулярной массой от 50000 до 15000 Да и ее фармацевтически приемлемую соль в концентрации от 1 до 20 мг/мл, дополнительно может включать антибиотик из группы гентамицина, пенициллина G и стрептомицина, при этом хранение производят при температуре раствора 2-8°C [патент RU 2184448, 2002 г.].
Наиболее близким аналогом изобретения является среда для консервации роговицы глаза, созданная в России на базе МНТК "Микрохирургия глаза", Москва, содержащая базовые среды M199, F12 и DMEM в соотношении 1:1:2, хондроитин-сульфат - 2,7 мас.%, декстран-40-2,0 мас.%, антибиотик гентамицин-сульфат-0,00014 мас.%, антимикотик амфотерицин В - 0,00015 мас.% [патент RU 2069951, 1996 г.]. Максимальный срок хранения донорского материала при использовании данной среды составляет 6 суток. Недостатком данной среды является недостаточная осмолярность применяемого декстрана, обусловливающая развитие отека роговицы, и проявляющего в отношении эндотелиоцитов токсический эффект (Zhao M. et al., 2008).
Задачей данного изобретения является разработка состава консервирующего раствора для продолжительного времени хранения донорских роговиц, предназначенных для сквозной, послойной и эндотелиальной кератопластик, в период между взятием и применением донорского материала.
Технический результат при использовании изобретения - увеличение срока хранения роговицы за счет создания оптимальных для жизнеспособной роговицы условий хранения.
Указанный технический результат достигается тем, что раствор для хранения роговицы, содержащий смесь биологических сред M199 и DMEM (таблица), хондроитина сульфат, L-аланил-L-глутамин, 4-(2-гидроксиэтил)-1-пиперазинэтансульфоновую кислоту (HEPES), пируват натрия, гентамицина сульфат, амфотерицин В, согласно изобретению дополнительно содержит 2,3,5,7,8-пентагидрокси-6-этилнафталиндион-1,4 (эхинохром А) и гидроксиэтилкрахмал при следующем содержании компонентов, мас.%:
|
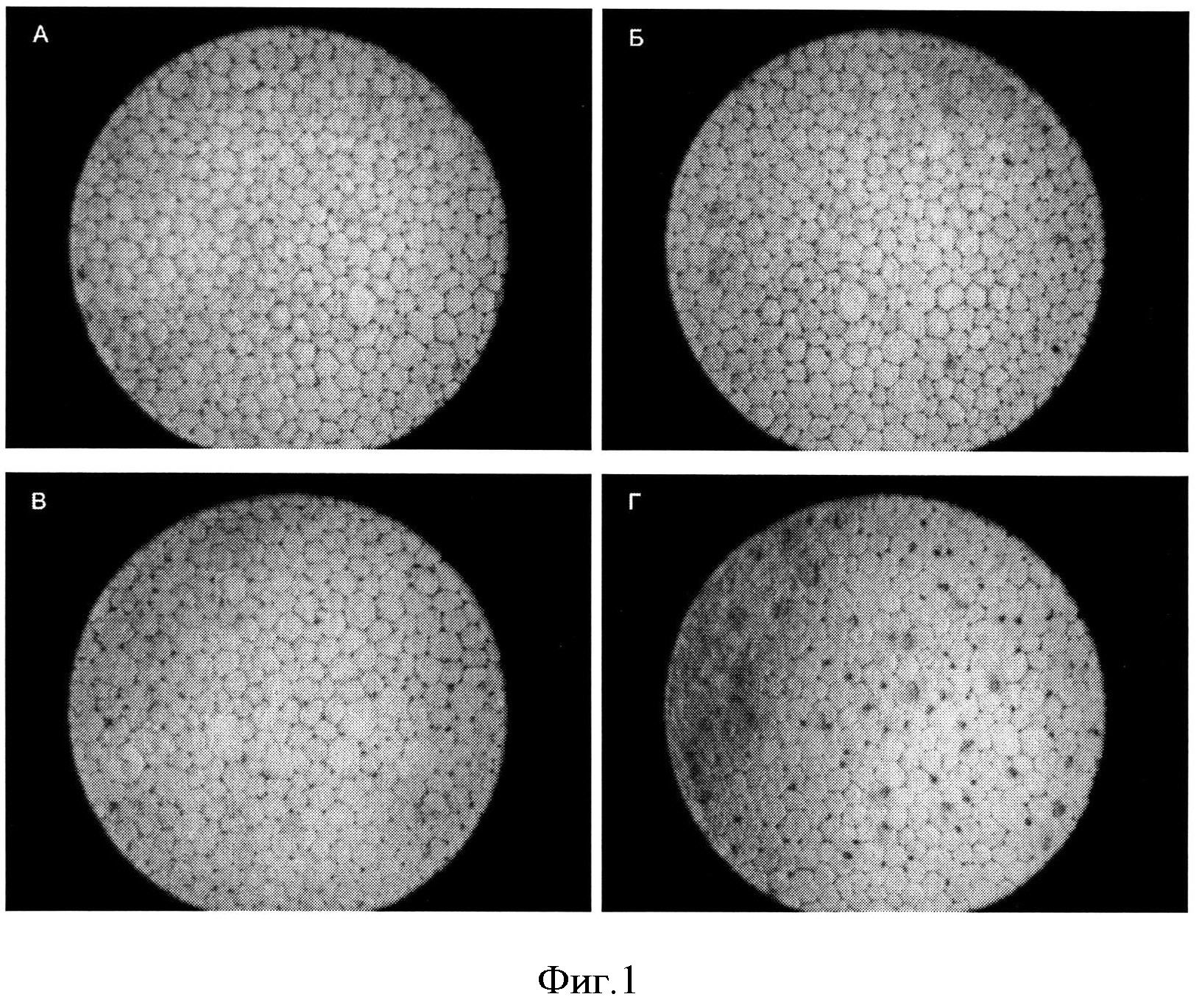
Изобретение иллюстрируется фигурой, на которой представлена морфологическая картина при окраске трипановым синим и ализариновым красным: а) 3 сутки, б) 6 сутки, в) 9 сутки, г) 12 сутки.
Изобретение основано на следующих предположениях:
1) в ходе хранения донорского материала при низкой температуре на фоне пониженной энергетической активности клеточного аппарата происходит апоптоз с образованием свободно-радикальных фрагментов, способствующих гибели близлежащих клеток. В ходе применения антиоксидантов вероятность цитолиза эндотелиоцитов значительно снижается;
2) сбалансированный раствор на базе поликомпонентных сред (таких как M199 и DMEM), дополненный осмолярным соединением, должен быть достаточным для поддержания натуральной формы роговицы. Такая среда является подходящей в отличие от других растворов, в которых содержится декстран.
Увеличение срока хранения роговицы в предлагаемом растворе достигается за счет следующего:
1. С целью снижения риска повреждения клеточных структур радикалами, образующимися в ходе метаболизма, используется эхинохром А в концентрации 0,001-0,01% мас./объем.
2. Для повышения осмотического давления до значений водянистой влаги используется гидроксиэтилкрахмал 200/0,5, с молекулярной массой 200000 Да, в концентрации 5-10% мас./объем.
Выбор компонентов консервирующего раствора основывается на моделировании физиологических условий хранения корнео-склерального лоскута. В результате создана среда, в которой жизнеспособность клеточных элементов роговицы удерживается в течение 10-12 дней хранения при температуре 2-6°C.
Раствор для консервации роговицы производят в стерильных условиях (стерильный бокс и ламинарный поток воздуха на рабочем столе) с использованием стерильной посуды. Для приготовления 100 мл консервационного раствора в колбу с 80 мл дистиллированной воды насыпают сухую среду M199 в количестве 640 мг и DMEM - 447 мг (таблица)), После их полного растворения в раствор добавляют антибиотик гентамицин до конечной концентрации 10 мг и антимикотик амфотерицин В - 25 мкг. Далее в раствор насыпают 54,25 мг L-аланил-L-глутамина; 595,8 мг HEPES; 1-10 мг эхинохрома А; 5,5 мг пирувата натрия; 151 мг β-гидроксибутирата натрия; 220 мг гидрокарбоната натрия. По завершении растворения вышеуказанных соединений раствор разделяют поровну на 2 флакона. В 1-й флакон засыпают 2,5 г хондроитина сульфата, а во второй- 5-10 г гидроксиэтилкрахмала, и оставляют в темноте до их полного набухания и растворения (около 60-80 мин). Затем растворы сливают в стерильную мерную аналитическую колбу, добавляют дистиллированной воды до метки колбы 100 мл и перемешивают. Производят префильтрацию через фильтр "Millipore" с размером пор 0,45 мкм. Затем через фильтр "Millipore" с диаметром пор 0,22 мкм среду разливают во флаконы по 10 мл, укупориваемые стерильными силиконовыми пробками под жесткую обкатку.
В стерильном боксе выкраивают корнеосклеральный лоскут общим диаметром 13,0-13,5 мм и помещают в герметичный флакон с 10 мл консерванта, который хранится в условиях глубокой гипотермии (4-6°C) сроком до 10-12 суток. Роговичные лоскуты в данном поликомпонентном растворе сохраняют жизнеспособность клеток и тканевую структуру на весь срок консервации. Это обеспечивает высокие оптические и трансплантационные свойства донорского материала, как для сквозной, так и для послойной кератопластики.
Использование данной среды позволяет создать региональный банк корнеосклеральных лоскутов на базе ГБУ "Уфимский НИИ глазных болезней АН РБ". Использование материала, консервированного в данной среде, позволяет проводить экстренные и плановые кератопластики после предварительного тестирования донорского материала на HIV, HBV, HCV и Treponema pallidum.
Пример. 1. Донор мужского пола Р., 47 лет, скончался на фоне острого инфаркта миокарда. Через 14 часов после смерти, в морге изъяты глазные яблоки, которые в стерильных условиях при t=6-8°C доставлены в ГБУ "Уф НИИ ГБ АН РБ"; параллельно в лабораторию для исключения инфекционного поражения донорского материала на анализ вышеуказанных инфекций отправлена венозная кровь. Обработку донорского материала проводили в 3 этапа: 1) ополаскивание глазного яблока в 0,5% растворе поливинилпиролидона йодина (PVP-I), растворенного в дистилированной воде с добавлением гидроксида натрия (NaOH) до рН=5,0-6,3; 2) ополаскивание в растворе 1% тиосульфата натрия (0,08-1,2%), растворенного в физиологическом растворе; 3) ополаскивание в физиологическом растворе.
Вырезание корнеосклерального лоскута проводилось в стерильных условиях стерильными инструментами с соблюдением правил асептики. Далее на эндотелиальном микроскопе Konan KeratoAnalyzer ЕКА-10 проводили оценку плотности клеток эндотелиального слоя. Результаты анализа показали, что плотность клеток составляет 3200 кл./мм2.
Для объективной оценки качества хранения проводилось морфологическое исследование эндотелиоцитов в различные сроки хранения. Для этого применен метод M.J. Taylor and C.J. Hunt (1981), основанный на использовании трипанового синего и ализаринового красного (фигура 1).Как видно из фигуры, на третьи сутки морфологическая структура эндотелия полностью сохранена;
на 6 сутки отмечается небольшое расширение границ между несколькими клетками и появление единичных погибших клеток (прокрашены красным в верхнем секторе); на 9 сутки визуализируется укрупнение ряда клеток ввиду их слияния с близлежащими; на 12 сутки отмечается нарушение межклеточного контакта (красные точки на углах клеток), появление как разрушающихся (ядро прокрашено синим), так и погибших клеток.
|