Результат интеллектуальной деятельности: НОВЫЙ СИСТЕМНЫЙ ИНСЕКТИЦИД
Вид РИД
Изобретение
Перекрестная ссылка на родственные заявки
Данная заявка основана и заявляет приоритет, исходя из предшествующей патентной заявки Японии № 329998/2007, поданной 21 декабря 2007 г., полное содержание которой включено в данный документ посредством ссылки.
Предпосылки создания изобретения
Область техники, к которой относится изобретение
Настоящее изобретение относится к композиции для сельского хозяйства или садоводства для применения в качестве нового системного инсектицида и способу борьбы с ее использованием.
Предшествующий уровень техники
Система положительного перечня для остаточных сельскохозяйственных химикатов и т.п. недавно была введена в действие, и значительный интерес был проявлен к мерам для предотвращения проникания сельскохозяйственных химикатов и т.п. В отличие от общепринятой технологии бескорневого нанесения, системные химикаты обычно вносят, например, в почву или ящики для проращивания в целях борьбы с насекомыми-вредителями, и, таким образом, может быть снижено проникание химикатов в окружающую среду. Также, с точки зрения снижения трудозатрат и обеспечения безопасности при сельскохозяйственном химическом нанесении, системные инсектициды превосходят общепринятую технологию бескорневого нанесения. Например, поскольку инсектицидный эффект может быть достигнут только посредством внесения системного инсектицида в ящики для проращивания, объем работ, проводимых при химической обработке, необходимый для работников сельского хозяйства, может быть снижен. Кроме того, системные инсектициды могут быть надлежащим образом нанесены на зерновые и, таким образом могут предотвратить воздействие сельскохозяйственных химикатов на людей, которые их наносят. Соответственно системные инсектициды также являются превосходящими при обеспечении безопасности. Кроме того, также с точки зрения эффективности, композиции, имеющие более длительную остаточную активность, чем композиции для бескорневого нанесения, могут быть предоставлены посредством придания, например, свойств регулируемого высвобождения композициям, содержащим системный инсектицид. На основании пригодности системных инсектицидов разработку системных инсектицидов в качестве технологии для сельского хозяйства или садоводства, отличной от общепринятой технологии бескорневого нанесения или т.п., с недавних пор ожидают на рынках риса-сырца и овощей.
С другой стороны, в WO 2004/060065 и Applied and Environmental Microbiology (1995), 61(12), 4429-35 описывается, что пирипиропен А обладает инсектицидным эффектом против Plutella xylostella, Tenebrio molitor и Helicoverpa armiger.
Кроме того, в WO 2006/129714 описывается, что группа соединений пирипиропена, включая соединения формулы (1), обладает инсектицидной активностью против Myzus persicae Sulzer, Trigonotylus caelestialium, Plutella xylostella и Helicoverpa armigera. Кроме того, в выложенной патентной заявке Японии № 360895/1992, Journal of Antibiotics (1993), 46(7), 1168-69, Journal of Synthetic Organic Chemistry, Japan (1998), vol. 56, No. 6, pp.478-488, WO 94/09147, выложенной патентной заявке Японии № 259569/1996 и выложенной патентной заявке Японии № 269062/1996 описываются пирипиропены, которые являются природными продуктами, или их производные и их ингибиторная активность против АСАТ (ацил КоА: холестеринацилтрансферазы).
Множество литературных источников сообщают об инсектицидной активности соединений, относящихся к пирипиропену. Они, однако, не описывают ни тот факт, что среди соединений, относящихся к пирипиропену, группа конкретных соединений обладает системными свойствами, ни применение группы конкретных соединений в качестве системных инсектицидов.
Вплоть до настоящего времени сообщалось о ряде системных инсектицидов. Для всех них, однако, существуют виды, резистентные к препаратам, и нерегулируемые виды, и разработка новых инсектицидов, обладающих высоким системным эффектом борьбы, еще остается желаемой.
Краткое изложение сущности изобретения
Авторами настоящего изобретения в настоящее время обнаружено, что соединения, представленные формулой (1), или их соли обладают эффектом высокого системного регулирования. Настоящее изобретение было создано на основании этих открытий.
Соответственно цель настоящего изобретения состоит в предоставлении химиката, который может быть эффективно и безопасно использован для применения в области сельского хозяйства или садоводства и обладает высокими системными свойствами, и способа регулирования с использованием данного химиката.
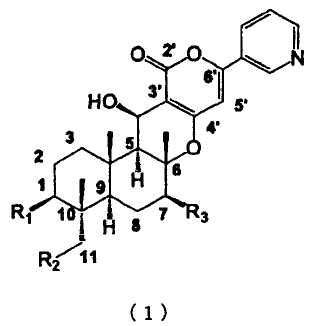
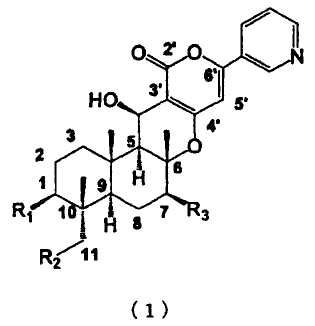
В соответствии с настоящим изобретением системный инсектицид содержит в качестве активных ингредиентов одно или несколько соединений, представленных формулой (1), или их соли:
Химическая формула 1
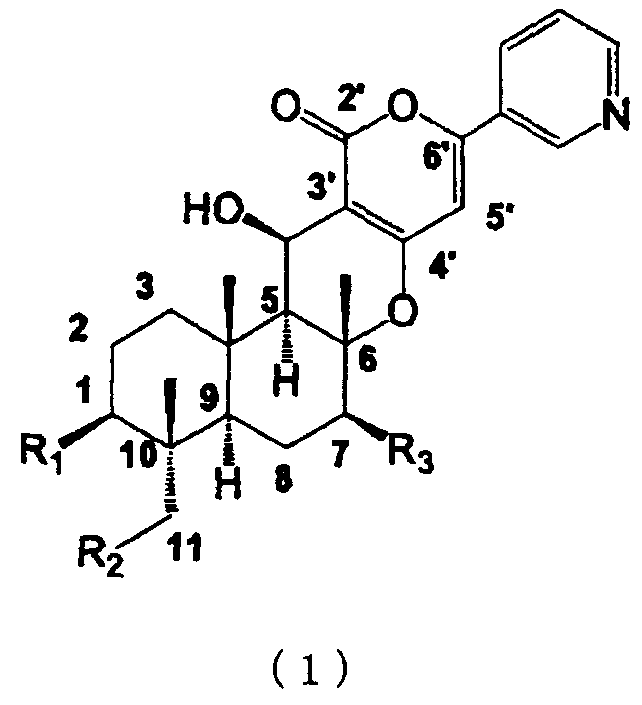
где
R1 представляет собой гидроксил, необязательно замещенный С1-6 алкилкарбонилокси, необязательно замещенный С2-6 алкенилкарбонилокси или необязательно замещенный С2-6 алкинилкарбонилокси;
R2 представляет собой атом водорода, гидроксил, необязательно замещенный С1-6 алкилкарбонилокси, необязательно замещенный С2-6 алкенилкарбонилокси или необязательно замещенный С2-6 алкинилкарбонилокси; и
R3 представляет собой атом водорода, гидроксил, необязательно замещенный метилкарбонилокси или оксо при отсутствии атома водорода в 7-положении.
В соответствии с настоящим изобретением также предоставлен способ борьбы с насекомыми-вредителями сельскохозяйственных или садовых культур, причем данный способ включает:
нанесение эффективного количества одного или нескольких соединений, представленных формулой (1), или их солей на объект, выбранный из группы, состоящей из почвы, питательного раствора в гидропонике, твердой среды в гидропонике и семени, корня, клубня, луковицы и корневища растения; и
системный перенос соединений, представленных формулой (1), на растение.
Подробное описание изобретения
Определение
Агент, обладающий системными свойствами (известный также как “системный инсектицид”), как используется в описании, означает агент, который может быть системно перенесен на растение и может отравить вредителей, которые высасывают или пережевывают растение до его гибели (см. Новое издание “Nouyaku No Kagaku (The Science of Agricultural Chemicals)” (BUNEIDO PUBLISHING CO., LTD, Kyohei Yamashita et al.), p. 14).
Термины “алкил”, “алкенил” и “алкинил”, как используются в описании, в виде группы или части группы, соответственно, означают алкил, алкенил и алкинил, которые составляют группу с прямой цепью, разветвленной цепью или циклического типа, или типа их сочетания, если не обозначено иначе. Кроме того, например, “С1-6” в “С1-6 алкиле” в виде группы или части группы означает, что число атомов углерода в алкильной группе составляет от 1 до 6 и что, в случае циклического алкила, число атомов углерода составляет по меньшей мере три.
Дополнительно, “необязательно замещенный” алкил, как используется в описании, означает, что один или несколько атомов водорода на алкильной группе необязательно замещены одним или несколькими заместителями, которые могут быть одинаковыми или различными. Для рядового специалиста в данной области будет очевидно, что максимальное число заместителей может быть определено в зависимости от числа замещаемых атомов водорода на алкильной группе. Это также относится к алкенилу и алкинилу.
Соединения, представленные формулой (1), или их соли
Системный инсектицид в соответствии с настоящим изобретением содержит в качестве активного ингредиента соединение формулы (1) или его соль. Удивительным фактом является то, что соединения формулы (1) обладают высокой системной инсектицидной активностью.
Предпочтительно в соединении формулы (1) “C1-6 алкилкарбонилокси”, представленный R1 и R2, означает С1-4 алкилкарбонилокси, более предпочтительно ацетилокси, этилкарбонилокси или С3-4 циклический алкилкарбонилокси. Группа С1-6 алкилкарбонилокси является необязательно замещенной, и примеры таких заместителей включают атомы галогена, циано, С3-5 циклоалкил, трифторметилокси или трифторметилтио. Атом галогена или С3-5 циклоалкил являются предпочтительными.
“Метилкарбонилокси”, представленный R3, является необязательно замещенным, и примеры таких заместителей включают атомы галогена, циано, трифторметил или трифторметокси, предпочтительно атом галогена или циано.
Предпочтительно “С2-6 алкенилкарбонилокси”, представленный R1 и R2, означает С2-4 алкенилкарбонилокси. Группа С2-6 алкенилкарбонилокси является необязательно замещенной, и примеры таких заместителей включают атомы галогена, циано, трифторметилокси или трифторметилтио.
Предпочтительно “С2-6 алкинилкарбонилокси”, представленный R1 и R2, означает С2-4 алкинилкарбонилокси. Группа С2-6 алкинилкарбонилокси является необязательно замещенной, и примеры таких заместителей включают атомы галогена, циано, трифторметилокси или трифторметилтио.
В соединениях формулы (1), предпочтительно, R1 представляет собой гидроксил или необязательно замещенный С1-6 алкилкарбонилокси, более предпочтительно гидроксил или необязательно замещенный С3-4 циклический алкилкарбонилокси.
Кроме того, в соединениях формулы (1), предпочтительно, R2 представляет собой необязательно замещенный С1-6 алкилкарбонилокси, более предпочтительно необязательно замещенный С3-4 циклический алкилкарбонилокси.
Более того, в соединениях формулы (1), предпочтительно, R3 представляет собой гидроксил, необязательно замещенный метилкарбонилокси или оксо при отсутствии атома водорода в 7-положении, более предпочтительно гидроксил.
В соответствии с предпочтительным вариантом осуществления настоящего изобретения в соединениях формулы (1) R1 представляет собой гидроксил или необязательно замещенный С1-6 алкилкарбонилокси и R2 представляет собой необязательно замещенный С1-6 алкилкарбонилокси.
В соответствии с другим предпочтительным вариантом осуществления настоящего изобретения в соединениях формулы (1) R1 представляет собой гидроксил или необязательно замещенный С1-6 алкилкарбонилокси и R3 предпочтительно представляет собой гидроксил, необязательно замещенный метилкарбонилокси или оксо при отсутствии атома водорода в 7-положении.
В соответствии с еще одним предпочтительным вариантом осуществления настоящего изобретения в соединениях формулы (1) R2 представляет собой необязательно замещенный С1-6 алкилкарбонилокси и R3 представляет собой гидроксил, необязательно замещенный метилкарбонилокси или оксо при отсутствии атома водорода в 7-положении.
В соответствии с более предпочтительным вариантом осуществления настоящего изобретения в соединениях формулы (1) R1 представляет собой гидроксил или необязательно замещенный С1-6 алкилкарбонилокси, R2 представляет собой необязательно замещенный С1-6 алкилкарбонилокси и R3 представляет собой гидроксил, необязательно замещенный метилкарбонилокси или оксо при отсутствии атома водорода в 7-положении.
В соответствии с другим предпочтительным вариантом осуществления настоящего изобретения в соединениях формулы (1) R1 и R2 представляют собой необязательно замещенный С3-4 циклический алкилкарбонилокси. В соответствии с другим более предпочтительным вариантом осуществления настоящего изобретения в соединениях формулы (1) R3 представляет собой гидроксил. Соединения формулы (1) в вариантах осуществления обладают значительными системными свойствами и могут быть особенно преимущественно использованы для борьбы с насекомыми-вредителями в различных областях применения.
Более конкретно соединения 1-7, показанные в таблице 1, могут быть упомянуты как предпочтительные соединения формулы (1). В таблице 1 заместители R1, R2 и R3 относятся, соответственно, к заместителям R1, R2 и R3 в формуле (1).
|
Дополнительно, в настоящем изобретении также применимыми являются соли соединений формулы (1), и примеры таких солей включают приемлемые в сельском хозяйстве или садоводстве кислотно-аддитивные соли, такие как гидрохлоридные соли, нитратные соли, сульфатные соли, фосфатные соли или ацетатные соли.
Соединения формулы (1), включая соединения, показанные в таблице 1, и соединения, показанные в таблице 6, используемые в сравнительных тестовых примерах, могут быть получены способами, описанными в патенте Японии № 2993767 (выложенная патентная заявка Японии № 360895/1992), выложенной патентной заявке Японии № 259569/1996, WO 2006/129714 и патенте Японии № 4015182, или способами, основанными на этих способах.
Системный инсектицид
Как описано выше, соединения формулы (1) или их соли обладают высокой системной инсектицидной активностью и могут быть преимущественно использованы, например, для борьбы с насекомыми-вредителями, которые высасывают или пережевывают растения. Таким образом, в соответствии с другим аспектом настоящего изобретения предусмотрено применение соединений, представленных формулой (1), или их солей в качестве системного инсектицида.
Насекомые-вредители сельскохозяйственных и садовых культур, против которых системный инсектицид в соответствии с настоящим изобретением дает эффект борьбы, включают лепидоптерановых (чешуекрылых) насекомых-вредителей, например, Noctuidae, таких как Spodoptera litura, Spodoptera exigua, Pseudaletia separata, Mamestra brassicae, Agrotis ipsilon, Trichoplusia spp., Heliothis spp. и Helicoverpa spp., Pyralidae, таких как Chilo suppressalis, Cnaphalocrocis medinalis, Ostrinia nubilalis, Hellula undalis, Parapediasia teterrella, Notarcha derogata и Plodia interpunctella, Pieridae, таких как Pieris rapae, Torticidae, таких как Adoxophyes spp., Grapholita molesta и Cydia pomonella, Carposinidae, таких как Carposina niponensis, Lyonetiidae, таких как Lyonetia spp., Lymantriidae, таких как Lymantria ssp. и Euproctis spp., Yponomeutidae, таких как Plutella xylostella, Gelechiidae, таких как Pectinophora gossypiella, Arctiidae, таких как Hyphantria cunea, и Tineidae, таких как Tinea translucens Meyrick и Tinea bissellinella; гемиптерановых (полужесткокрылых) насекомых-вредителей, например, Aphididae, таких как Myzus persicae Sulzer и Aphis gossypii, Delphacidae, таких как Laodelphax stratella, Nilaparvata lugens Stal и Sogatella furcifera, Cicadellidae, таких как Nephotettix cincticeps и Empoasca onukii, Pentatomidae, таких как Trigonotylus caelestiallium, Plautia crossota stali, Nezara viridula и Riptortus clavatus, Aleyrodidae, таких как Trialeurodes vaporariorum и Bemisia tabaci, Coccoidea, таких как Pseudaulacaspis pentagona, Pseudococcus comstocki Kuwana и Aonidiella aurantii, Tingidae, причем Psyllidae, Aphididae, Coccoidea, Aleyrodidae и Cicadellidae являются предпочтительными; насекомых-вредителей Coleoptera, например, Curculionidae, таких как Sitophilus zeamais, Lissorhoptrus oryzophilus и Callosbruchus chinensis, Tenebrionidae, таких как Tenebrio molitor, Scarabaeidae, таких как Anomala cuprea и Anomala rufocuprea Motschulsky, Chrysomelidae, таких как Phyllotreta striolata, Aulacophora femoralis, Leptinotarsa decemlineata, Diabrotica virgifera virgifera и Diabrotica undecimpunctata howardi, Epilachna, таких как Oulema oryzae Kuwayama, Paederus fuscipes, Bostrychidae, и Epilachna vigintioctopunctata Fabricius и Cerambycidae; Acari, например, Tetranychidae, таких как Tetranychus urticae Koch, Tetranychus kanzawai Kishida, Panonychus citri, Panonychus ulmi и Oligonychus spp., Eriophyidae, таких как Aculops lycopersici, Aculops pelekassi Keifer и Calacarus carinatus, Tarsonemidae, таких как Polyphagotarsonemus latus и Acaridae; гименоптерановых (перепончатокрылых) насекомых-вредителей, например, Tenthredinidae, таких как Athalia rosae ruficornis; насекомых-вредителей Orthopteran, например, Acrididae; насекомых-вредителей Dipteran, например, Agromyzidae, таких как Muscidae, Culex, Anophelinae, Chironomidae, Calliphoridae, Sarcophagidae, Fanniidae, Anthomyiidae, Liriomyza trifolii, Liriomyza sativae и Liriomyza bryoniae, Tephritidae, Phoridae, Drosophilidae, Psychodidae, Sumiliidae, Tabanidae и Stomoxyini; насекомых-вредителей Thysanopteran, например, Thrips palmi Karny, Frankliniella occidentalis Pergande, Thrips tabaci Lindeman, Thrips hawaiiensis, Scirtothrips dorsalis, Frankliniella intonsa и Ponticulothrips diospyrosi; и нематод, паразитирующих на растениях, например, Aphelenchoididae, таких как Meloidogyne hapla, Pratylenchus, Heteroderidae, Aphelenchoides besseyi и Bursaphelenchus xylophilus. Среди них гемиптерановые насекомые-вредители являются предпочтительными в качестве насекомых-вредителей, против которых применяют системный инсектицид в соответствии с настоящим изобретением.
Соединения формулы (1) или их соли, как таковые, могут быть использованы в качестве активного ингредиента системного инсектицида, но обычно их смешивают с подходящими твердыми носителями, жидкими носителями, газообразными носителями, поверхностно-активными веществами, диспергирующими веществами или другими адъювантами (вспомогательными веществами) для композиций и составляют в любые подходящие дозированные формы, например смачиваемые порошки, гранулы, диспергируемые в воде, суспензии, сыпучие вещества, гранулы, микрогранулы, пудры, эмульгируемые концентраты, EW агенты, жидкие композиции, таблетки, масла и аэрозоли для применения в качестве композиций.
Твердые носители включают, например, тальк, бентонит, глину, каолин, диатомовую землю, вермикулит, цеолит, белый уголь, карбонат кальция, кислотную глину, пемзу, аттапульгит и оксид титана.
Жидкие носители включают, например, спирты, такие как метанол, н-гексанол, этиленгликоль и пропиленгликоль; кетоны, такие как ацетон, метилэтилкетон и циклогексанон; алифатические углеводороды, такие как н-гексан, керосин и неочищенный керосин; ароматические углеводороды, такие как толуол, ксилол и метилнафталин; простые эфиры, такие как диэтиловый эфир, диоксан и тетрагидрофуран; сложные эфиры, такие как этилацетат; нитрилы, такие как ацетонитрил и изобутиронитрил; амиды кислот, такие как диметилформамид и диметилацетамид; растительные масла, такие как соевое масло и хлопковое масло; диметилсульфоксид; и воду.
Газообразные носители включают, например, LPG, воздух, азот, диоксид углерода и диметиловый эфир.
Поверхностно-активные вещества или диспергирующие вещества, применимые, например, для эмульгирования, диспергирования или нанесения, включают, например, сложные эфиры алкилсерной кислоты, соли алкил(арил)сульфоновой кислоты, алкил(арил)овые простые эфиры полиоксиалкилена, сложные эфиры многоатомного спирта, сульфосукцинат диоктилнатрия, алкилмалеатный сополимер, алкилнафталинсульфонат натрия, натриевые соли конденсата β-нафталинсульфоната и формальдегида, соли лигнинсульфоновой кислоты, сульфат простого тристирилфенилового эфира полиэксиэтилена или фосфат.
Вспомогательные вещества, применимые для улучшения свойств композиций, включают, например, предварительно желатинизированный крахмал, декстрин, карбоксиметилцеллюлозу, аравийскую камедь, полиэтиленгликоль, стеарат кальция, поливинилпирролидон, альгинат натрия, фенольный антиоксидант, аминный антиоксидант, фосфорный антиоксидант, серный антиоксидант и эпоксидированное растительное масло.
Вышеуказанные носители, поверхностно-активные вещества, диспергирующие вещества и вспомогательные вещества могут быть использованы либо по отдельности, либо в сочетании в соответствии с необходимостью.
Подходящее содержание активного ингредиента в этих композициях обычно составляет от 1 до 75 масс.% для эмульгируемого концентрата, обычно от 0,3 до 25 масс.% для пудры, обычно от 1 до 90 масс.% для увлажняемого порошка и обычно от 0,5 до 10 масс.% для гранул.
Предпочтительно системный инсектицид в соответствии с настоящим изобретением наносят на семена, корни, клубни, луковицы или корневища растений, более предпочтительно на семена растений. Когда растения являются объектом, на который наносят системный инсектицид, соединения формулы (1) могут благоприятным образом поглощаться и проникать в растения для достижения системного инсектицидного эффекта.
Растения
Растения, на которые системно переносили соединение формулы (1), как таковые, обладают инсектицидной активностью, и могут быть преимущественно использованы в борьбе с насекомыми-вредителями, которые высасывают или пережевывают растения. Таким образом, в соответствии с дополнительным аспектом настоящего изобретения представлено растение, обработанное системным инсектицидом в соответствии с настоящим изобретением, где растение выбирают из семян, корней, клубней, луковиц или корневищ. В соответствии с предпочтительным вариантом осуществления обработка включает системный перенос соединения формулы (1) на растение.
Способ борьбы
В соответствии с другим аспектом настоящего изобретения предусмотрен способ, включающий нанесение эффективного количества одного или нескольких соединений формулы (1) или их солей на объект, выбранный из группы, состоящей из почвы, питательного раствора в гидропонике, твердой среды в гидропонике и семени, корня, клубня, луковицы и корневища растений; и системный перенос соединения формулы (1) на растение.
Когда объектом является семя, корень, клубень, луковица или корневище растения, любой способ нанесения, который не ингибирует системный перенос соединения формулы (1), может быть принят без особенного ограничения, и примеры подходящих способов нанесения включают погружение, покрытие опылением, обмазывание, разбрызгивание, гранулирование или покрытие.
В соответствии с предпочтительным вариантом осуществления настоящего изобретения объектом является семя. Когда объектом является семя, способы нанесения, используемые в настоящем изобретении, включают погружение, покрытие опылением, обмазывание, разбрызгивание, гранулирование, покрытие и фумигацию (окуривание). Погружение представляет собой способ, в котором семена погружают в химический раствор. Покрытие опылением классифицируют по двум типам, т.е. сухой способ покрытия опылением, в котором порошкообразный химикат прилипает на сухие семена, и влажный способ покрытия опылением, в котором порошкообразный химикат прилипает на семена, слегка смоченные водой. Обмазывание представляет собой способ, в котором суспендированный химикат наносят на поверхность семян внутри смесителя. Разбрызгивание представляет собой способ, в котором суспендированный химикат разбрызгивают на поверхность семян. Гранулирование представляет собой способ, в котором химикат смешивают с наполнителем, когда семена вместе с наполнителем гранулируют с образованием гранул, имеющих заданные размер и форму. Покрытие представляет собой способ, в котором содержащей химикат пленкой покрывают семена. Фумигация представляет собой способ, в котором семена стерилизуют химикатом, который переводят в газообразное состояние внутри герметически закрытого сосуда.
Соединения формулы (1) или их соли могут быть также нанесены, в дополнение к семенам, на пророщенные растения, которые пересаживают после проращивания или после появления ростков из почвы, и на зародыши растений. Эти растения могут быть защищены путем обработки целого или его части погружением перед пересадкой.
Внесение соединений формулы (1) или их солей в почву, применяемое, например, при насаждении растений, также является предпочтительным. Любой способ внесения в почву, который не ингибирует системный перенос соединений формулы (1), может быть принят без конкретного ограничения. Предпочтительные способы внесения (нанесения) являются следующими.
Примером таких способов является способ, в котором гранулы, содержащие соединение формулы (1) или его соль, вносят в почву или наносят на почву. Предпочтительные способы внесения в почву включают распространение, внесение в полоски, внесение в бороздки и внесение в посадочные лунки. Распространение включает поверхностную обработку по всей площади, подлежащей обработке, и механическое внедрение в почву после поверхностной обработки.
Пропитка почвы раствором, полученным эмульгированием или растворением соединения формулы (1) или его соли в воде, также является преимущественным способом нанесения на почву.
Примеры других предпочтительных способов нанесения включают внесение в питательный раствор в системах культивирования с питательным раствором, таких как водная культура и культура с твердой средой, например, песчаная культура, NFT (технология с пленкой питательных веществ) или культура с каменной ватой, для получения овощей и цветущих растений. Также очевидно, что соединение формулы (1) может быть внесено непосредственно в почву для искусственного культивирования, содержащую вермикулит, и твердую среду, содержащую искусственную подложку для всходов рассады.
На стадии нанесения эффективное количество соединения формулы (1) или его соли предпочтительно равно количеству, достаточно большому, чтобы обеспечить системный перенос соединения формулы (1) на растение на последующей стадии системного переноса.
Эффективное количество может быть надлежащим образом определено с учетом, например, свойств соединений, типа и количества объекта нанесения, продолжительности последующей стадии системного переноса и температуры. Например, в случае семян, соединение формулы (1) или его соль наносят в количестве, составляющем предпочтительно от 1 г до 10 кг, более предпочтительно от 100 г до 1 кг на 100 кг семян. С другой стороны, в случае нанесения на почву, соединение формулы (1) или его соль вносят в количестве, составляющем предпочтительно от 0,1 г до 10 кг, более предпочтительно от 1 г до 1 кг на 10 аров культивируемой земли.
В способе борьбы, в соответствии с настоящим изобретением, соединение формулы (1) или его соль наносят на объект с последующим системным переносом соединения формулы (1) на растение.
Способ системного переноса не является конкретно ограниченным. Его примером является способ, в котором растение, такое как семя, корень, клубень, луковица или корневище, высаживают или погружают в почву или среду, в которые вносят соединение формулы (1) в течение периода времени, достаточно длительного, чтобы обеспечить системный перенос химиката на растение. Когда выбирают количество химиката для нанесения и продолжительность, достаточные для системного переноса, стадия системного переноса также может быть осуществлена путем нанесения соединения формулы (1) непосредственно на растение при обеспечении неподвижности растения. Настоящее изобретение включает этот вариант осуществления.
Время и температура при системном переносе могут быть надлежащим образом определены рядовым специалистом в данной области в зависимости от, например, объекта нанесения и типа и количества химиката. Время системного переноса не является ограниченным конкретно и может составлять, например, 1 час или более. Температура при системном переносе составляет, например, от 5 до 45°C.
Соединения формулы (1) можно использовать в виде смеси с другими химикатами, например фунгицидами, инсектицидами, митицидами, гербицидами, агентами-регуляторами роста растений или удобрениями. Конкретные примеры других добавляемых в смесь химикатов описаны, например, в The Pesticide Manual, the 13th edition, опубликованных The British Crop Protection Council; и SHIBUYA INDEX, the 10th edition, 2005, опубликованных SHIBUYA INDEX RESEARCH GROUP.
Более конкретные примеры других химикатов включают инсектициды, например ацефат, дихлорвос, EPN, фенитотион, фенамифос, протиофос, профенофос, пираклофос, хлорпирифос-метил, хлорфенвинфос, деметон, этион, малатион, кумафос, изоксатион, фентион, диазинон, тиодикарб, алдикарб, оксамил, пропоксур, карбарил, фенобукарб, этиофенкарб, фенотиокарб, пиримикарб, карбофуран, карбосульфан, фуратиокарб, хиквинкарб, аланикарб, бенфуракарб, картап, тиоциклам, бенсультап, дикофол, тетрадифон, циромазин, феноксикарб, дицикланил, бупрофезин, флубендиамид, этипрол, фипронил, имидаклоприд, нитенпирам, клотианидин, ацетамиприд, динотефуран, тиаклоприд, тиаметоксам, пиметрозин, флоникамид, спиносад, авермектин, милбемицин, никотин, эмамектинбензоат, спинеторам, пирифлуквиназон, хлорантранилипрол, спиротетрамат, лепимектин, метафлумизон, пирафлупрол, пирипрол, гидраметилнон и триазамат. Их предпочтительные примеры включают ацефат, этипрол, фипронил, имидаклоприд, клотианидин, тиаметоксам, авермектин и милбемицин. Ацефат и имидаклоприд являются более предпочтительными.
Примеры предпочтительных добавляемых фунгицидов включают соединения стробилурина, такие как азоксистробин, крезоксим-метил, трифлоксистробин, оризастробин, пикоксистробин и фуоксастробин; соединения азола, такие как триадимефон, битертанол, трифлумизол, этаконазол, пропиконазол, пенконазол, флусилазол, миклобутанил, ципроконазол, тебуконазол, гесаконазол, прохлораз и симеконазол; соединения бензимидазола, такие как беномил, тиофанат-метил и карбендазол; соединения фениламида, такие как металаксил, оксадиксил, офурас, беналаксил, фуралаксил и ципрофурам; соединения изоксазола, такие как гидроксиизоксазол; соединения бензанилида, такие как флутоланил и мепронил; соединения морфолина, такие как фенпропиморф и диметоморф; соединения цианопиррола, такие как флудиоксонил и фенпиклонил; и пробеназол, ацибензолар-S-метил, тиадинил, изотианил, карпропамид, диклоцимет, феноксанил, трициклазол, пироквилон, феримзон, флуазинам, цимоксанил, трифорин, пирифенокс, фенаримол, фенпропидин, пенцикурон, циазофамид, цифлуфенамид, боскалид, пентиопирад, проквиназид, хиноксифен, фамоксадон, фенамидон, ипроваликарб, бентиаваликарб-изопропил, флуопиколид, пирибенкарб, касугамицин или валидамицин. Их особенно предпочтительные примеры включают соединения стробилурина, соединения азола и соединения фениламида.
Примеры
Настоящее изобретение далее иллюстрировано следующими примерами, которые не подразумеваются в качестве ограничения изобретения. Соединение 4 в примерах синтезировали способом, описанным в WO 2006/129714.
Примеры синтеза
Пример синтеза 1: Соединение 5
PR-3 (20 мг), синтезированный способом, описанным в выложенной патентной заявке Японии № 259569/1996, и циклопропанкарбоновую кислоту (19 мг) растворяли в безводном N,N-диметилформамиде (1 мл) и к раствору добавляли гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида (84 мг) и 4-(диметиламино)пиридин 5 (мг). Смесь перемешивали при комнатной температуре в течение 6 часов. Реакционный раствор выливали в воду и смесь экстрагировали этилацетатом. Этилацетатный слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния и растворитель удаляли выпариванием при пониженном давлении с получением неочищенного продукта соединения 5. Неочищенный продукт очищали препаративной тонкослойной колоночной хроматографией (силикагель Merck 60F254 (0,5 мм), хлороформ:метанол=10:1) с получением соединения 5 (9,0 мг).
Пример синтеза 2: Соединение 6
Химическая формула 2
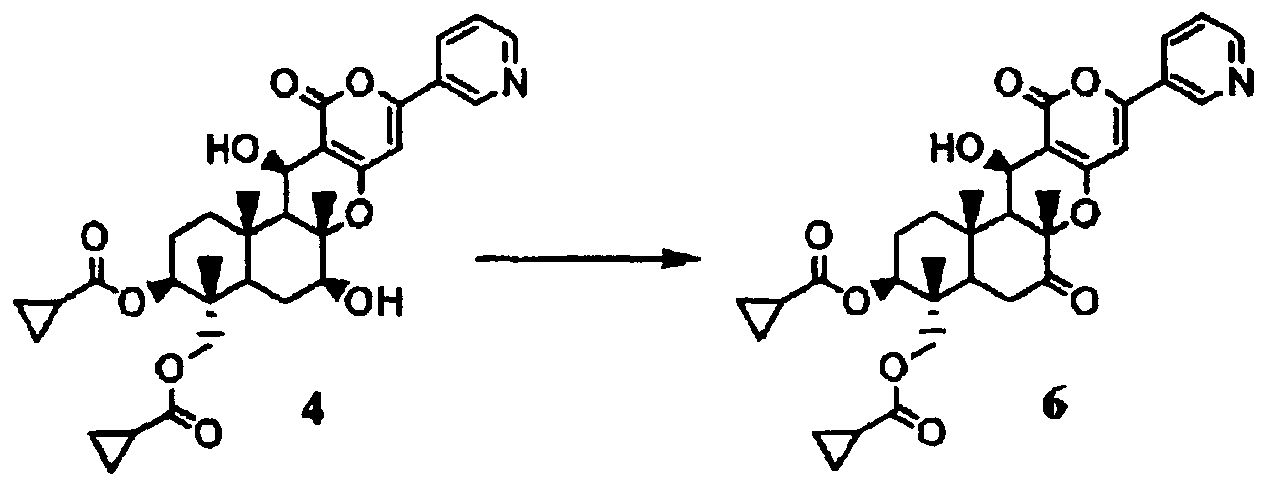
Соединение 4 (20 мг) растворяли в дихлорметане (1 мл). К раствору при 0°C добавляли периодинан Десса-Мартина (21 мг) и в этом состоянии смесь перемешивали в течение 2 часов 40 минут. К реакционному раствору добавляли насыщенный водный раствор тиосульфата натрия и смесь экстрагировали хлороформом. Слой хлороформа промывали насыщенным раствором соли и сушили над безводным сульфатом магния. Растворитель затем удаляли выпариванием при пониженном давлении и полученный таким образом неочищенный продукт очищали препаративной тонкослойной хроматографией (силикагель Merck 60F254 (0,5 мм), ацетон:гексан=1:1) с получением соединения 6 (5,4 мг).
Пример синтеза 3: Соединение 7
Химическая формула 3
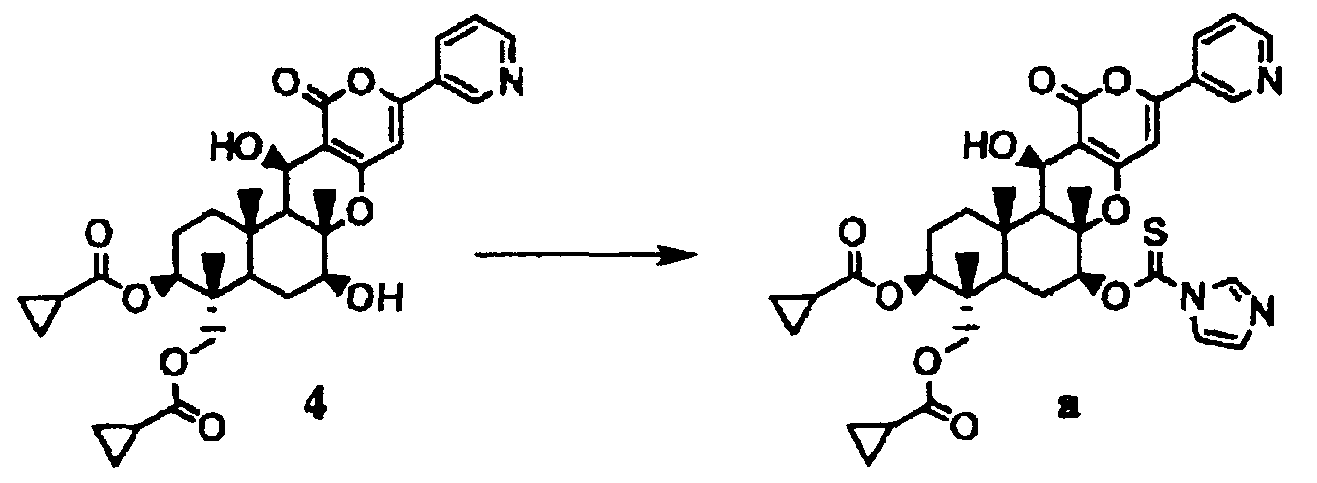
Соединение 4 (50 мг) растворяли в толуоле (3 мл). К раствору при комнатной температуре добавляли 1,1'-тиокарбонилдиимидазол (90 мг) и смесь нагревали при кипении с обратным холодильником в течение 2,5 часов. Реакционный раствор охлаждали до комнатной температуры. К реакционному раствору добавляли воду и смесь экстрагировали этилацетатом. Этилацетатный слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния и растворитель затем удаляли выпариванием при пониженном давлении. Полученный таким образом неочищенный продукт очищали препаративной тонкослойной хроматографией (силикагель Merck 60F254 (0,5 мм), ацетон:гексан=1:1) с получением соединения а (41,1 мг).
Химическая формула 4
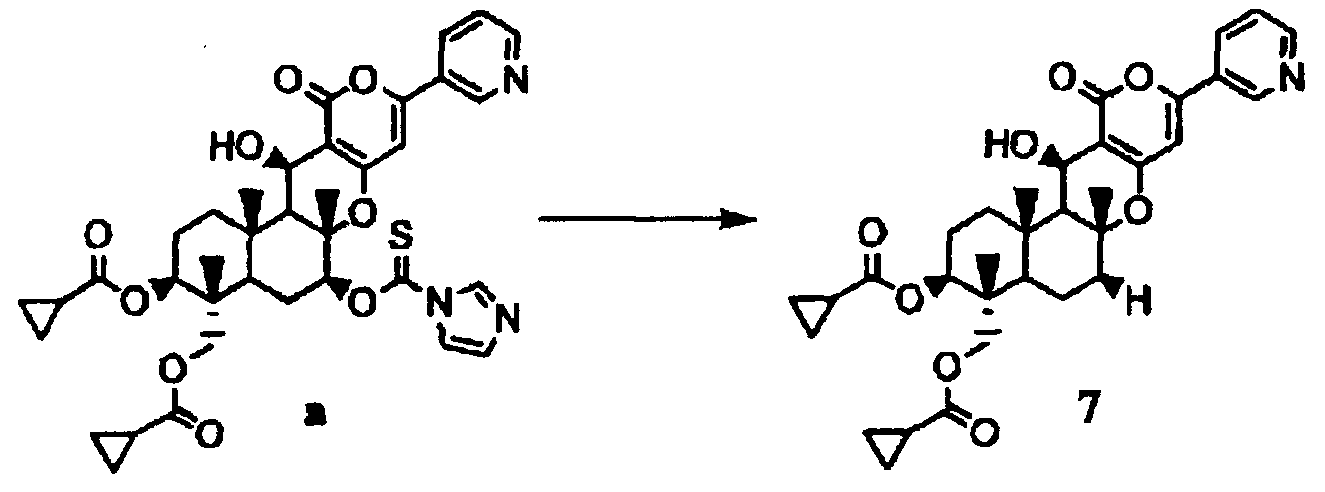
Соединение а (41 мг) растворяли в толуоле (2 мл). К раствору при комнатной температуре добавляли гидрид три-н-бутилолова (20 мг) и смесь нагревали при кипении с обратным холодильником в течение 2,5 часов. Реакционный раствор охлаждали до комнатной температуры. К реакционному раствору добавляли воду и смесь экстрагировали этилацетатом. Этилацетатный слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния и растворитель затем удаляли выпариванием при пониженном давлении. Полученный таким образом неочищенный продукт очищали препаративной тонкослойной хроматографией (силикагель Merck 60F254 (0,5 мм), ацетон:гексан=1:1) с получением соединения 7 (3,5 мг).
Данные 1Н-ЯМР и данные масс-спектрометрии для соединений 5, 6 и 7 соответствовали показанным в таблице 2.
|
Примеры композиций
Пример композиции 1 [гранулы]
|
Ингредиенты гомогенно измельчали и смешивали вместе, к смеси добавляли воду и смесь тщательно размешивали, гранулировали и сушили с получением 0,5% гранул.
Пример композиции 2 [смачивающийся порошок]
|
Ингредиенты гомогенно смешивали вместе и измельчали с получением 5% смачивающегося порошка.
Пример композиции 3 [гранула, диспергируемая в воде]
|
Ингредиенты гомогенно измельчали и смешивали вместе. К смеси добавляли воду с последующим тщательным замешиванием. Затем замешанный продукт гранулировали и сушили с получением 20% гранулы, диспергируемой в воде.
Пример композиции 4 [сыпучие вещества]
|
Все ингредиенты, за исключением 1% водного раствора ксантановой камеди, и подходящее количество воды предварительно смешивали вместе и смесь затем измельчали, используя мельницу с влажным размолом. После этого 1% водный раствор ксантановой камеди и оставшуюся воду добавляли к измельченному продукту с получением 100 масс.% сыпучего вещества.
Пример композиции 5 [эмульгируемый концентрат]
|
Вышеуказанные ингредиенты гомогенно смешивали вместе и растворяли с получением эмульгируемого концентрата.
Тестовые примеры
Тест с обработкой путем орошения почвы
Тестовый пример 1: Инсектицидный эффект против Aphis gossypii
Всходы огурцов обрабатывали путем пропитки почвы разбавленным раствором композиции, доведенной до заранее определенной концентрации с помощью воды. Химикат поглощался через корень в течение шести дней, а затем выпускали пять взрослых Aphis gossypii для каждого из всходов. Далее всходы выдерживали в термостате при 25°C. Количество паразитов на листьях наблюдали через шесть дней после выпуска и показатель плотности рассчитывали по следующему уравнению:
Показатель плотности = (количество паразитов на обработанном участке/количество паразитов на необработанном участке) × 100
Как показано в таблице 3, 5% смачивающийся порошок, 20% гранулы, диспергируемые в воде, и 0,5% гранулы, каждые из которых содержали соединение 4, полученные, как описано соответственно в примере композиции 2, примере композиции 3 и примере композиции 1, обладали системным ингибиторным эффектом высокой плотности против Aphis gossypii.
|
Тестовый пример 2: Инсектицидный эффект против Myzus persicae Sulzer
Всходы баклажана обрабатывали путем пропитки почвы разбавленным раствором композиции, доведенной до заранее определенной концентрации с помощью воды. Химикат поглощался через корень в течение пяти дней, а затем выпускали три взрослых Myzus persicae Sulzer для каждого из всходов. Далее всходы выдерживали в термостате при 25°C. Количество паразитов на листьях наблюдали через пять дней после выпуска и показатель плотности рассчитывали по тому же уравнению, что и в тестовом примере 1. Тест дублировали.
Как показано в таблице 4, смачивающийся порошок, содержащий соединение 4 и полученный, как описано в примере композиции 2, обладал системным ингибиторным эффектом высокой плотности против Myzus persicae Sulzer.
|
Тест с обработкой посредством корневого вымачивания
Тестовый пример 3: Инсектицидный эффект против Rhopalosiphum padi
Корни всходов пшеницы через 48 часов после посева вымачивали в течение 72 часов в тестовом растворе (100 ч./млн), полученном в виде 10% водно-ацетонового раствора. Через 72 часа после обработки 10 личинок Rhopalosiphum padi выпускали на каждый из всходов. Далее всходы выдерживали в термостате при 25°C. Количество паразитов на стеблях и листьях наблюдали через шесть дней после выпуска и показатель плотности рассчитывали по тому же уравнению, что и в тестовом примере 1. Тест дублировали.
В результате, как показано в таблице 5, соединения 1, 2, 3, 4, 5, 6 и 7, описанные в таблице 1, обладали системным ингибиторным эффектом высокой плотности против Rhopalosiphum padi.
|
Сравнительные тесты: Инсектицидный эффект против Rhopalosiphum padi
Для соединений 8 и 9, описанных в таблице 6, инсектицидный эффект против Rhopalosiphum padi оценивали таким же образом, как и в тестовом примере 3. В результате, как показано в таблице 7, соединения 8 и 9 не обладали плотным ингибиторным эффектом.
В таблице 6 заместители R1, R2 и R3 соответствуют заместителям R1, R2 и R3 в формуле (1).
|
|
Ссылочный тест: Инсектицидный эффект против Myzus persicae Sulzer
Диск листа, имеющий диаметр 2,8 см, вырезали из капусты, выращенной в горшке, и помещали в 5,0 см Шале. Четыре взрослых тли Myzus persicae Sulzer выпускали в Шале. Через один день после выпуска взрослых тлей взрослых тлей удаляли. Число личинок первого возраста, родившихся на диске листа, доводили до 10 и 20 ч./млн тестового раствора, который получали в виде 50% водно-ацетонового раствора (0,05% с добавлением Твин 20), разбрызгивали над диском капустного листа. Диск капустного листа затем сушили на воздухе. Затем Шале закрывали крышкой и выдерживали в термостате при 25°C. Через три дня после выпуска личинки наблюдали на предмет выживания или гибели и смертность личинок рассчитывали по следующему уравнению:
Смертность (%) = {число мертвых личинок/(число выживших личинок + число мертвых личинок)} × 100
В результате было обнаружено, что для всех соединений 1, 2, 3, 4, 5, 6, 7, 8 и 9, описанных в таблице 1 или 6, обработка разбрызгиванием показала высокий инсектицидный эффект, равный 100% с точки зрения смертности.
Тест с обработкой семян
Тестовый пример 4: Инсектицидный эффект против Rhopalosiphum padi
Семена пшеницы вымачивали в течение 6 часов в разбавленном растворе композиции, доведенной до заранее определенной концентрации с помощью воды. Семена проращивали в термостате в течение 3 дней и всходы пересаживали в почву. Через два дня после пересадки 10 личинок Rhopalosiphum padi выпускали на каждый из всходов. Далее всходы выдерживали в термостате при 25°C. Количество паразитов на стеблях и листьях наблюдали через шесть дней после выпуска и показатель плотности рассчитывали по тому же уравнению, что и в тестовом примере 1. Тест повторяли трижды.
Как показано в таблице 8, 5% смачивающийся порошок, содержащий соединение 4, обладал ингибиторным эффектом высокой плотности против Rhopalosiphum padi.
|
Тест с обработкой посредством пропитки почвы
Тестовый пример 5: Инсектицидный эффект против Trialeurodes uaporariorum
Взрослых особей Trialeurodes uaporariorum выпускали на всходы огурцов, выращенные в горшке, с целью откладывания яиц на два дня. Через 10 дней после начала откладывания яиц подтверждали, что личинки вылупились из полученных яиц. Почву в горшке для всходов огурцов пропитывали 5 мл тестируемого раствора, доведенного до заранее определенной концентрации с помощью 10% водно-ацетонового раствора. Горшок для огуречной рассады выдерживали в термостате при 25°C (световой период 16 часов - темновой период 8 часов). Через 9 дней после пропитки измеряли число выживших личинок и смертность личинок рассчитывали по следующему уравнению. Тест дублировали:
Смертность (%) = {число личинок перед обработкой - число выживших личинок)/число личинок перед обработкой} × 100
Как показано в таблице 9, соединение 4 обладало высокой системной инсектицидной активностью против Trialeurodes uaporariorum.
Тестовый пример 6: Инсектицидный эффект против Laodelphax stratella
Были предоставлены всходы риса в горшке. Почву в горшке пропитывали тестируемым раствором, доведенным до заранее определенной концентрации с помощью 10% водно-ацетонового раствора. После выдерживания в течение трех дней 10 личинок второго возраста выпускали на рисовые всходы. Затем горшок выдерживали в термостате при 25°C (световой период 16 часов - темновой период 8 часов). Через 3 дня после выпуска измеряли число выживших личинок и смертность личинок рассчитывали по тому же уравнению, что и в ссылочном тесте. Тест дублировали.
Как показано в таблице 9, соединение 4 обладало высокой системной инсектицидной активностью против Laodelphax stratella.
Тестовый пример 7: Инсектицидный эффект против Nephotettix cincticeps
Были предоставлены всходы риса в горшке. Почву в горшке пропитывали тестируемым раствором, доведенным до заранее определенной концентрации с помощью 10% водно-ацетонового раствора. После выдерживания в течение трех дней 10 личинок второго возраста выпускали на рисовые всходы. Затем горшок выдерживали в термостате при 25°C (световой период 16 часов - темновой период 8 часов). Через 3 дня после выпуска измеряли число выживших личинок и смертность личинок рассчитывали по тому же уравнению, что и в ссылочном тесте. Тест дублировали.
Как показано в таблице 9, соединение 4 обладало высокой системной инсектицидной активностью против Nephotettis cincticeps.
|
Количество для обработки выражено в массовых единицах исходного вещества.
Тестовый пример обработки путем пропитки с использованием инсектицидной добавки
Тестовый пример 8: Инсектицидный эффект против Aphis gossypii
Всходы огурцов обрабатывали путем пропитки почвы единственным агентом и добавкой, доведенными до заранее определенной концентрации с помощью воды. Химикат поглощался через корень в течение двух дней, и четыре взрослые особи Aphis gossypii выпускали на каждый из всходов. Затем всходы выдерживали в термостате при 25°C. Через 2 дня после выпуска наблюдали количество паразитов на листьях. Показатель плотности на каждом обработанном участке определяли, предполагая, что плотность на необработанном участке равна 100. Предотвращающее значение рассчитывали по следующему уравнению:
Предотвращающее значение = 100 - показатель плотности
Полученные результаты представлены в таблице 10. Если показатель плотности превышал 100, то предотвращающее значение считали равным 0 (нулю).
Далее теоретические значения, для которых не проявлялся синергический эффект, были рассчитаны по следующей формуле Колби, и результаты представлены в таблице 11.
Формула Колби: Теоретическое значение = А + В - (А × В)/100,
где А - предотвращающее значение, когда обработку осуществляли только соединением 4, и
В - предотвращающее значение, когда обработку осуществляли только каждым из ацефата и имидаклоприда.
Способ определения синергического эффекта
Если численное значение для добавки в таблице 10 превышало теоретическое значение, рассчитанное по формуле Колби и представленное в таблице 11, определяли, что добавка обладала синергическим эффектом.
Все тестированные добавки обладали предотвращающими значениями за пределами теоретических значений, демонстрируя то, что они обладали синергическим эффектом.
|
Количество для обработки выражено в массовых единицах исходного вещества.
|
Количество для обработки выражено в массовых единицах исходного вещества.
Тестовый пример 9: Инсектицидный эффект против Rhopalosiphum padi
Корни всходов пшеницы через 48 часов после посадки вымачивали в течение 72 часов в растворе добавки, доведенном до заранее определенной концентрации с помощью 10% водно-ацетонового раствора. Через 72 часа после обработки 10 личинок Rhopalosiphum padi для каждого из всходов выпускали на всходы. Далее всходы выдерживали в термостате при 25°C. Количество паразитов на стеблях и листьях наблюдали через шесть дней после выпуска. Показатель плотности на каждом обработанном участке определяли, предполагая, что плотность на необработанном участке равна 100, и предотвращающее значение рассчитывали по такому же уравнению, как и в тестовом примере 8.
Результаты представлены в таблице 12. Если показатель плотности превышал 100, то предотвращающее значение считали равным 0 (нулю).
Теоретические значения, для которых не проявлялся синергический эффект, были рассчитаны по следующей формуле Колби, и результаты представлены в таблице 13.
Формула Колби: Теоретическое значение = А + В - (А × В)/100,
где А - предотвращающее значение, когда обработку осуществляли только соединением 4, и
В - предотвращающее значение, когда обработку осуществляли только каждым из ацетамиприда, ацефата и имидаклоприда.
Способ определения синергического эффекта
Когда численное значение против Rhopalosiphum padi для добавки в таблице 12 превышало теоретическое значение, рассчитанное по формуле Колби и представленное в таблице 13, определяли, что добавка обладала синергическим эффектом. Все тестированные добавки обладали предотвращающими значениями за пределами теоретических значений, демонстрируя то, что они обладали синергическим эффектом.

Количество для обработки выражено в массовых единицах исходного вещества.
|
Количество для обработки выражено в массовых единицах исходного вещества.
Тестовый пример 10: Инсектицидный эффект против Laodelphax stratella
Всходы риса, выращенные в горшке, обрабатывали путем пропитки почвы единственным агентом или добавкой, доведенными до заранее определенной концентрации с помощью воды. Всходы выдерживали в течение двух дней. Личинки второго возраста выпускали на рисовые всходы. Затем всходы риса выдерживали в термостате при 25°C (световой период 16 час - темновой период 8 час). Через 4 дня после выпуска наблюдали число выживших личинок и смертность личинок рассчитывали по тому же уравнению, что и в ссылочном тесте. Тест дублировали.
Результаты приведены в таблице 14.
Теоретические значения, для которых не проявлялся синергический эффект, были рассчитаны по следующей формуле Колби и результаты представлены в таблице 15.
Формула Колби: Теоретическое значение (%) = 100 - (А × В)/100,
где А - 100 - (смертность, когда обработку осуществляли только соединением 4), и
В - 100 - (смертность, когда обработку осуществляли только имидаклопридом).
Способ определения синергического эффекта
Когда численное значение для добавки в таблице 14 превышало теоретическое значение, рассчитанное по формуле Колби и представленное в таблице 15, определяли, что добавка обладала синергическим эффектом.
Для тестированной добавки значения смертности находились за пределами теоретических значений, демонстрируя то, что она обладала синергическим эффектом.
|
Количество для обработки выражено в массовых единицах исходного вещества.
|
Количество для обработки выражено в массовых единицах исходного вещества.