Результат интеллектуальной деятельности: ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ОКСИНДОЛА И ИХ ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, ЗАВИСИМЫХ ОТ ВАЗОПРЕССИНА
Вид РИД
Изобретение
Настоящее изобретение относится к новым замещенным производным оксиндола, к содержащим их фармацевтическим средствам и к их применению для лечения заболеваний, зависимых от вазопрессина.
Вазопрессин является эндогенным гормоном, который оказывает самое различное действие на органы и ткани. Считается, что вазопрессиновая система играет роль при разных болезненных состояниях, как, например, сердечная недостаточность и высокое кровяное давление. В настоящее время известны три рецептора (V1a, V1b или V3 и V2), через которые вазопрессин передает свои многочисленные действия. Поэтому исследуются антагонисты этих рецепторов как возможные новые терапевтические разработки для лечения болезней (M. Thibonnier, Exp. Opin. Invest. Drugs 1998, 7(5), 729-740).
Имеются описания новых замещенных оксиндолов, которые в положении 1 имеют фенилсульфонильную группу. 1-фенилсульфонил-1,3-дигидро-2H-индол-2-оны уже описывались как лиганды рецепторов вазопрессина. В документах WO 93/15051, WO 95/18105, WO 98/25901, WO 01/55130, WO 01/55134, WO 01/164668 и WO 01/98295 также описаны производные, которые в положении 1 оксиндольного скелета содержат арилсульфонильные группы. Эти соединения существенно отличаются от соединений по изобретению заместителями в положении 3.
Так, в WO 93/15051 и WO 98/25901 описаны 1-фенилсульфонил-1,3-дигидро-2H-индол-2-оны как лиганды рецепторов вазопрессина, у которых оксиндольный скелет в положении 3 замещен двумя алкильными остатками, которые вместе могут также образовывать циклоалкильный остаток (спиросвязь). Как альтернатива, спироцикл может содержать гетероатомы, такие как кислород и азот (по выбору с заместителями).
Документ WO 95/18105 описывает 1-фенилсульфонил-1,3-дигидро-2H-индол-2-оны как лиганды для рецепторов вазопрессина, которые в положении 3 содержат атом азота. Кроме того, в положении 3 связаны остатки, которые выбраны из алкильного, циклоалкильного, фенильного или бензильного остатков, при необходимости замещенных.
В WO 03/008407 описаны 1-фенилсульфонилоксиндолы, у которых в положении 3 пиридилпиперазин связан с оксиндолом мочевинной, карбаматной или 2-оксоэтильной группой.
Наряду с химическим сродством к рецептору вазопрессина V1b, другие свойства также могут быть преимущественными для лечения и/или профилактики зависимых от вазопрессина заболеваний, таких как, например:
1) селективность к рецептору вазопрессина V1b по сравнению с рецептором вазопрессина V1a, т.е. частное от деления химического сродства к рецептору V1a (Ki(V1a) (определяется в наномолярных единицах (нМ)) и химического сродства к рецептору V1b (Ki(V1b)) (определяется в наномолярных единицах (нМ)). Чем больше частное Ki(V1a)/Ki(V1b), чем больше селективность к V1b;
2) селективность к рецептору V1b вазопрессина по сравнению с рецептором вазопрессина V2, т.е. частное от деления химического сродства к рецептору V2 (Ki(V2) (определяется в наномолярных единицах (нМ)) и химического сродства к рецептору V1b (Ki(V1b)) (определяется в наномолярных единицах (нМ)). Чем больше частное Ki(V2)/Ki(V1b), тем выше селективность к V1b;
3) селективность к рецептору вазопрессина V1b по сравнению с рецептором окситоцина OT, т.е. частное от деления химического сродства к рецептору OT (Ki(OT) (определяется в наномолярных единицах (нМ)) и химического сродства к рецептору V1b (Ki(V1b)) (определяется в наномолярных единицах (нМ)). Чем больше частное Ki(OT)/Ki(V1b), тем выше селективность к V1b;
4) метаболическая стабильность, определяемая, например, посредством устанавливаемого in vitro времени полуразложения в печеночных микросомах различных видов (например, крысы или человека);
5) отсутствие или лишь незначительное ингибирование ферментов цитохрома P450 (CYP): цитохром P450 (CYP) является обозначением суперсемейства гемопротеинов с ферментативной активностью (оксидаза). Они имеют особое значение также для разложения (метаболизма) чужеродных веществ, как лекарственные препараты или ксенобиотики в организмах млекопитающих. Наиболее важными представителями типов и подтипов CYP в человеческом организме являются: CYP 1A2, CYP 2C9, CYP 2D6 и CYP 3A4. При одновременном применении ингибиторов CYP 3A4 (например, грейпфрутовый сок, симетидин, эритромицин) и лекарственных веществ, которые разлагаются этой ферментной системой и тем самым конкурируют за одно и то же место связывания на ферменте, их разложение может замедлиться, и тем самым нежелательно усилятся действия и побочные эффекты принимаемых лекарственных веществ;
6) подходящая растворимость в воде (в мг/мл);
7) подходящая фармакокинетика (временная зависимость концентрации соединения по изобретению в плазме или в тканях, например, головного мозга). Фармакокинетику можно описать следующими параметрами: время полуразложения (в ч), объем распределения (в л/кг), клиренс плазмы (в л/(ч·кг)), AUC ("area under the curve" - площадь под кривой концентрация-время, в нг//(ч·л)), пероральная биодоступность (нормированное на дозу отношение AUC после перорального приема и AUC после внутривенного введения), так называемое отношение мозг-плазма (отношение AUC в ткани мозга к AUC в плазме);
8) отсутствие или незначительная блокада hERG-канала: соединения, которые блокируют hERG-канал, могут вызывать удлинение QT-интервала и тем самым привести к слишком серьезным расстройствам сердечного ритма (например, так называемое "torsade de pointes" - трепетание-мерцание желудочков). С помощью описанного в литературе вытеснительного хроматографического анализа с дофетилидом, меченым радиоактивной меткой (G.J. Diaz et al., Journal of Pharmacological and Toxicological Methods, 50 (2004), 187-199) можно определить потенциал соединений, которые блокируют hERG-канал. Чем меньше IC50 в этом опыте с дофетилидом, тем вероятнее мощная блокада hERG-канала. Кроме того, блокаду hERG-анала можно измерить электрофизиологическими экспериментами на клетках, которые были трансфецированы hERG-каналом, путем так называемого "whole-cell patch clamping" (полноклеточного пэтч-клампа) (G.J. Diaz et al., Journal of Pharmacological and Toxicological Methods, 50 (2004), 187-199).
Задачей настоящего изобретения было предоставить соединения для лечения или профилактики различных заболеваний, зависимых от вазопрессина. Эти соединения должны иметь высокую активность и селективность, прежде всего высокое сродство и селективность в отношении рецептора вазопрессина V1b. Кроме того, вещество согласно изобретению должно обладать одним или несколькими указанными выше преимуществами 1)-8).
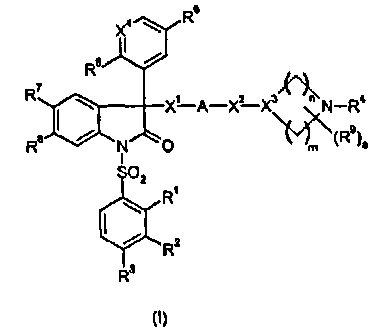
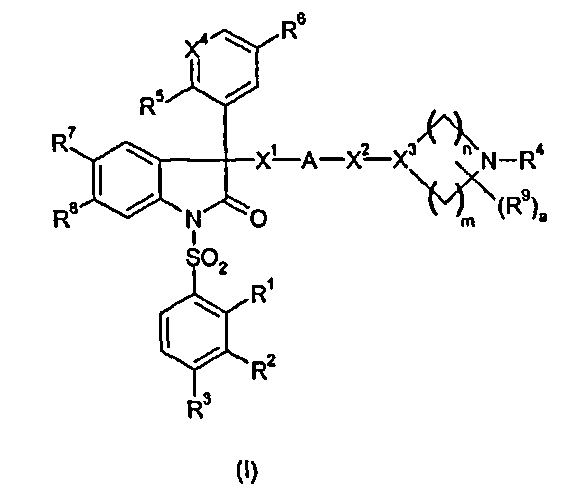
Эта задача решена соединениями формулы 1
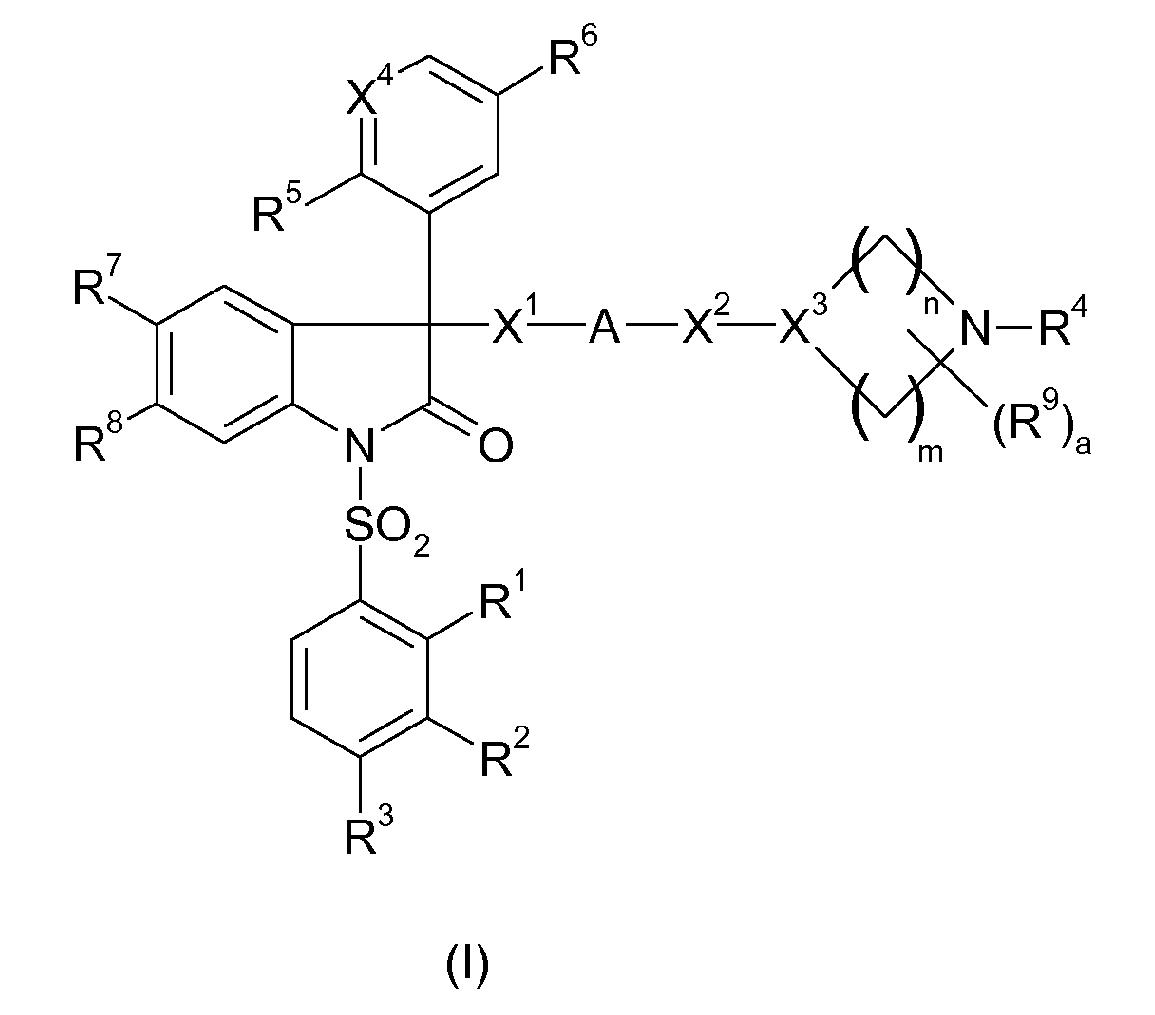
в которой
X1 означает -O-, -O-CH2-, -O-C(=O)-, -NR11-, -NR11-CH2- или -NR11-C(=O)-;
X2 означает простую связь, CO или CH2;
X3 означает N или CH;
X4 означает N или CH;
A означает фенилен или 6-членный гетероарилен с 1 или 2 атомами азота в качестве кольцевых членов, причем фенилен или гетероарилен может быть замещен 1 или 2 остатками R10;
R1 и R3 независимо друг от друга означают водород, C1-C3-алкил, C1-C3-фторалкил, C1-C3-алкокси, C1-C3-фторалкокси, галоген или CN;
R2 означает водород или метокси;
причем по меньшей мере один из остатков R1, R2 и R3 означает водород;
R4 означает водород или C1-C4-алкил;
R5 означает этокси, фторированный этокси, фторметокси, дифторметокси, трифторметокси или изопропокси;
R6 означает водород или метил;
R7 означает водород, I, Br, Cl, F или CN;
R8 означает водород, I, Br, Cl, F или CN;
R9 означает C1-C3-алкил или C1-C3-фторалкил;
R10 означает C1-C3-алкил, C1-C3-фторалкил, C1-C3-алкокси или C1-C3-фторалкокси;
R11 означает водород, C1-C4-алкил, C1-C4-фторалкил, C1-C4-алкокси или C1-C4-фторалкокси;
a означает 0, 1 или 2; и
m и n независимо друг от друга означают 1 или 2;
а также их фармацевтически приемлемыми солями и их пролекарствами.
В соответствии с этим, настоящее изобретение относится к соединениям формулы I (далее также "соединения I"), а также к фармацевтически приемлемым солям соединений I и пролекарствам соединений I.
Фармацевтически приемлемые соли соединений формулы I, которые будут называться также физиологически приемлемыми солями, могут быть получены, как правило, взаимодействием свободных оснований соединений I по изобретению (т.е. соединений I согласно структурной формуле I) с подходящими кислотами. Подходящие кислоты названы, например, в "Fortschritte der Arzneimittelforschung" (Успехи в исследовании лекарственных средств), 1966, Birkhäuser Verlag, Bd.10, S.224-285. Сюда подпадают, например, соляная кислота, лимонная кислота, винная кислота, молочная кислота, фосфорная кислота, метансульфоновая кислота, уксусная кислота, муравьиная кислота, малеиновая кислота и фумаровая кислота.
Под термином "пролекарства" будут пониматься такие соединения, которые метаболизируются in vivo в соединения I согласно изобретению. Типичные примеры пролекарств описаны в G.G. Wermeth (Ed.): The Practice of Medicinal Chemistry (Практика медицинской химии), Academic Press, San Diego, 1996, 671-715. Сюда относятся, например, фосфаты, карбаматы, аминокислоты, сложные эфиры, амиды, пептиды, мочевины и т.п. В настоящем случае подходящими пролекарствами могут быть, например, такие соединения I, в которых внешний атом азота внешнего азотсодержащего кольца образует амидную/пептидную связь, тем, что этот атом азота в положении остатка R4 замещается C1-C4-алкилкарбонильной группой, например, ацетилом, пропионилом, н-пропилкарбонилом, изопропилкарбонилом, н-бутилкарбонилом или трет-бутилкарбонилом (пивалоил), бензоилом, или связанным через CO остатком аминокислоты, например, связанным через CO глицином, аланином, серином, фенилаланином и т.п. Кроме того, в качества пролекарств подходят алкилкарбонилоксиалкилкарбаматы, в которых внешний атом азота внешнего азотсодержащего кольца в положении остатка R4 содержит группу формулы -C(=O)-O-CHRa-O-C(=O)-Rb, в которой Ra и Rb независимо друг от друга означают C1-C4-алкил. Такие карбаматы описаны, например, в J. Alexander, R. Cargill, S.R. Michelson, H. Schwam, J. Medicinal Chem. 1988, 31(2), 318-322. Затем эти группы можно отщепить в метаболических условиях, получая соединения I, в которых R4 означает H.
В рамках настоящего изобретения C1-C3-алкил означает линейный или разветвленный алкильный остаток с 1-3 атомами углерода, такими как метил, этил, н-пропил или изопропил.
В рамках настоящего изобретения C1-C4-алкил означает линейный или разветвленный алкильный остаток с 1-4 атомами углерода, такими как метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изобутил или трет-бутил.
В рамках настоящего изобретения C1-C3-фторалкил означает линейный или разветвленный алкильный остаток с 1-3 атомами углерода, такой как определен выше, в котором по меньшей мере один атом водорода, например, 1, 2, 3, 4 или 5 атомов водорода, замещены атомами фтора. Примерами этого являются фторметил, дифторметил, трифторметил, 1- и 2-фторэтил, 1,1-, 1,2- и 2,2-дифторэтил, 1,1,2-, 1,2,2- и 2,2,2-трифторэтил, 1,1,2,2-тетрафторэтил, 1,2,2,2-тетрафторэтил, пентафторэтил, 1-, 2- и 3-фторпроп-1-ил, 1,1-, 1,2-, 1,3-, 2,2-, 2,3- и 3,3-дифторпроп-1-ил, 1,1,2-, 1,2,2-, 1,1,3-, 2,2,3-, 1,2,3- и 3,3,3-трифторпроп-1-ил, 1- и 2-фторпроп-2-ил, 1,1- и 1,3-дифторпроп-2-ил, 1,1,1-трифторпроп-2-ил и т.п.
В рамках настоящего изобретения C1-C4-фторалкил означает линейный или разветвленный алкильный остаток с 1-4 атомами углерода, такой как определен выше, в котором по меньшей мере один атом водорода, например, 1, 2, 3, 4 или 5 атомов водорода, замещены атомами фтора. Примерами помимо названных выше C1-C3-фторалкильных остатков являются 1-, 2-, 3- и 4-фтор-н-бутил, 1,1-, 2,2-, 3,3- и 4,4-дифтор-н-бутил, 4,4,4-трифтор-н-бутил, 3-фтор-2-(фторметил)-1-пропил, 3,3-дифтор-2-(дифторметил)-1-пропил, 3,3,3-трифтор-2-(трифторметил)-1-пропил и т.п.
C1-C3-алкокси в рамках настоящего изобретения означает связанный через атом кислорода линейный или разветвленный алкильный остаток с 1-3 атомами углерода. Примерами являются метокси, этокси, н-пропокси и изопропокси.
C1-C4-алкокси в рамках настоящего изобретения означает связанный через атом кислорода линейный или разветвленный алкильный остаток с 1-4 атомами углерода. Примерами, помимо остатков, указанных для C1-C3-алкокси, являются н-бутокси, втор-бутокси, изобутокси и трет-бутокси.
C1-C3-фторалкокси в рамках настоящего изобретения означает связанный через атом кислорода линейный или разветвленный алкильный остаток с 1-3 атомами углерода, какой определен выше, в котором по меньшей мере один атом водорода, например, 1, 2, 3, 4 или 5 атомов водорода, замещены атомами фтора. Примерами этого являются фторметокси, дифторметокси, трифторметокси, 1- и 2-фторэтокси,
1,1-, 1,2- и 2,2-дифторэтокси, 1,1,2-, 1,2,2- и 2,2,2-трифторэтокси, 1,1,2,2-тетрафторэтокси, 1,2,2,2-тетрафторэтокси, пентафторэтокси, 1-, 2- и 3-фторпроп-1-окси, 1,1-, 1,2-, 1,3-, 2,2-, 2,3- и 3,3-дифторпроп-1-окси, 1,1,2-, 1,2,2-, 1,1,3-, 2,2,3-, 1,2,3- и 3,3,3-трифторпроп-1-окси, 1- и 2-фторпроп-2-окси, 1,1- и 1,3-дифторпроп-2-окси, 1,1,1-трифторпроп-2-окси и т.п.
В рамках настоящего изобретения C1-C4-фторалкокси означает связанный через атом кислорода линейный или разветвленный алкильный остаток с 1-4 атомами углерода, какой определен выше, в котором по меньшей мере один атом водорода, например, 1, 2, 3, 4 или 5 атомов водорода замещены атомами фтора. Примерами этого, помимо остатков, названных выше для C1-C3-фторалкокси, являются 1-, 2-, 3- и 4-фтор-н-бутокси, 1,1-, 2,2-, 3,3- и 4,4-дифтор-н-бутокси, 4,4,4-трифтор-н-бутокси, 3-фтор-2-(фторметил)-1-пропокси, 3,3-дифтор-2-(дифторметил)-1-пропокси, 3,3,3-трифтор-2-(трифторметил)-1-пропокси и т.п.
Фторированный этокси в рамках настоящего изобретения означает этокси, в котором 1, 2, 3, 4 или 5 атомов водорода замещены атомами фтора. Примерами являются 1-фторэтокси, 2-фторэтокси, 1,1-дифторэтокси, 1,2-дифторэтокси, 2,2-дифторэтокси, 1,1,2-трифторэтокси, 1,2,2-трифторэтокси, 2,2,2-трифторэтокси, 1,1,2,2-тетрафторэтокси и 1,1,2,2,2-пентафторэтокси.
Галоген в рамках настоящего изобретения означает фтор, хлор, бром или йод.
Фенилен означает двухвалентный фенильный остаток, как 1,2-фенилен, 1,3-фенилен и 1,4-фенилен.
6-членный гетероарилен с одним или 2 атомами азота в качестве кольцевых членов означает двухвалентный пиридильный остаток (пиридилен), как 2,3-пиридилен, 2,4-пиридилен, 2,5-пиридилен, 2,6-пиридилен, 3,4-пиридилен, 3,5-пиридилен, 3,6-пиридилен, 4,5-пиридилен, 4,6-пиридилен или 5,6-пиридилен; двухвалентный пиримидильный остаток (пиримидилен), как 2,3-пиримидилен, 2,4-пиримидилен, 4,2-пиримидилен, 4,5-пиримидилен, 4,6-пиримидилен или 5,2-пиримидилен; двухвалентный пиразиновый остаток (пиразинилен), как 2,3-пиразинилен, 2,5-пиразинилен или 2,6-пиразинилен; или двухвалентный пиридазиновый остаток, (пиридазинилен), как 3,4-пиридазинилен, 3,5-пиридазинилен, 3,6-пиридазинилен или 4,5-пиридазинилен.
Соединения формулы I по изобретению, их фармакологически приемлемые соли и их пролекарства могут также присутствовать в виде сольватов или гидратов. Под сольватами в рамках настоящего изобретения понимаются кристаллические формы соединений I или их фармацевтически приемлемых солей или их пролекарств, в кристаллическую решетку которых встроены молекулы растворителя. Предпочтительно, молекулы растворителя вводятся в стехиометрическом соотношении. Особой формой сольватов являются гидраты, в которых растворитель представляет собой воду.
Дающиеся ниже указания на подходящие и предпочтительные признаки изобретения, в частности, указания на переменные R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R11, X1, X2, X3, X4, A, a, m и n в соединении I, на переменные R1, R2, R3, R5, R6, R7, R8, R12, X1, X4 и A в соединении XVIII, а также на отличительные признаки способа по изобретению и на применение согласно изобретению справедливы для взятых как по отдельности, так и, предпочтительно, в любой возможной комбинации друг с другом.
Соединения I предпочтительно готовятся в форме свободных оснований (т.е. согласно структурной формуле I) или в форме их кислотно-аддитивных солей.
В соединениях I по меньшей мере один из остатков R1, R2, R3 означает водород. Предпочтительно, по меньшей мере R2 означает водород. При этом особенно предпочтительно, чтобы R1 или R3, или R1 и R3 отличались от водорода.
В определениях R1 и R3 C1-C3-алкокси предпочтительно означает этокси или метокси, в частности метокси. C1-C3-фторалкокси предпочтительно означает C1-C2-фторалкокси, т.е. фторметокси, дифторметокси, трифторметокси, 1- и 2-фторэтокси, 1,1-, 1,2- и 2,2-дифторэтокси, 1,1,2-, 1,2,2- и 2,2,2-трифторэтокси, 1,1,2,2-тетрафторэтокси, 1,2,2,2-тетрафторэтокси или пентафторэтокси, предпочтительно фторметокси, дифторметокси, трифторметокси, 2,2-дифторэтокси или 2,2,2-трифторэтокси, в частности, трифторметокси, 2,2-дифторэтокси или 2,2,2-трифторэтокси.
В одной предпочтительной форме осуществления R1 и R3 независимо друг от друга означают водород, CN, C1-C3-алкокси или C1-C3-фторалкокси. При этом в определениях остатков R1 и R3 C1-C3-алкокси предпочтительно означает этокси или метокси, в частности, метокси. C1-C3-фторалкокси предпочтительно означает C1-C3-фторалкокси, т.е. фторметокси, дифторметокси, трифторметокси, 1- и 2-фторэтокси, 1,1-, 1,2- и 2,2-дифторэтокси, 1,1,2-, 1,2,2 и 2,2,2-трифторэтокси, 1,1,2,2-тетрафторэтокси, 1,2,2,2-тетрафторэтокси или пентафторэтокси, предпочтительно фторметокси, дифторметокси, трифторметокси, 2,2-дифторэтокси или 2,2,2-трифторэтокси, в частности, трифторметокси, 2,2-дифторэтокси или 2,2,2-трифторэтокси.
В одной особенно предпочтительной форме осуществления R1 означает водород, метокси, этокси, фторметокси, дифторметокси или трифторметокси, более предпочтительно водород, метокси или трифторметокси, в частности, водород или метокси.
В одной особенно предпочтительной форме осуществления R3 означает водород, C1-C3-алкокси или C1-C3-фторалкокси, более предпочтительно водород, метокси, этокси, фторметокси, дифторметокси или трифторметокси, еще более предпочтительно водород, метокси или трифторметокси, в частности, водород или метокси, в частности, метокси.
В одной предпочтительной форме осуществления по меньшей мере один из остатков R1 и R3 означает метокси.
В одной предпочтительной форме осуществления R2 означает водород. Альтернативно, R2 предпочтительно означает метокси, и R1 и R3 одновременно означают водород. Однако особенно предпочтительно R2 означает водород.
В одной особой форме осуществления R1 и R3 означают метокси, а R2 водород; или один из остатков R1 и R3 означает метокси, другой означает водород, и R2 означает водород.
В одной предпочтительной форме осуществления R4 означает водород, метил, этил, н-пропил или изопропил, особенно предпочтительно водород, метил или этил, в частности, водород или метил.
В одной предпочтительной форме осуществления R5 означает этокси или фторированный этокси, особенно предпочтительно этокси, 2,2-дифторэтокси или 2,2,2-трифторэтокси, в частности, этокси.
В одной предпочтительной форме осуществления R6 означает H.
В одной особенно предпочтительной форме осуществления R5 означает этокси, и R6 означает H. При этом X4 означает N или CH, предпочтительно N.
В альтернативной особенно предпочтительной форме осуществления R5 означает этокси, и R6 означает метил. При этом X4 предпочтительно означает N.
В альтернативной особенно предпочтительной форме осуществления R5 означает изопропокси, и R6 означает H. При этом X4 предпочтительно означает N.
В альтернативной особенно предпочтительной форме осуществления R5 означает фторированный этокси, предпочтительно 2,2-дифторэтокси или 2,2,2-трифторэтокси, особенно предпочтительно 2,2-дифторэтокси, и R6 означает H. Одновременно, при этом X4 предпочтительно означает CH.
Особенно предпочтительно X4 означает N.
В частности, R5 означает этокси, и R6 означает H. При этом X4 означает N или CH, предпочтительно N.
В одной предпочтительной форме осуществления R7 и R8 одновременно не являются CN.
В одной предпочтительной форме осуществления R7 и R8 одновременно не являются H.
Предпочтительно, R7 означает F, Cl, I или CN, особенно предпочтительно I, Cl или CN, в частности, CN.
Предпочтительно R8 означает H или F.
В частности, R7 означает CN, и R8 одновременно означает H или F, или R7 означает I, и R8 одновременно означает H или F, в частности, H, или R7 означает Cl, и R8 одновременно означает H или F, в частности, H.
В одной предпочтительной форме осуществления R9 означает метил или этил.
a предпочтительно равно 0 или 1, в частности, 0.
В одной предпочтительной форме осуществления R10 означает метил или метокси.
В одной предпочтительной форме осуществления R11 означает водород, C1-C4-алкил или C1-C4-алкокси, особенно предпочтительно водород, метил или метокси, в частности, водород.
В одной предпочтительной форме осуществления X1 означает -O-CH2-,
-O-C(=O)-, -NR11-, -NR11-CH2- или -NR11-C(=O)-. Особенно предпочтительно, X1 означает -O-C(=O)-, -NR11-, -NR11-CH2- или -NR11-C(=O)-. Более предпочтительно X1 означает -NR11- или -NR11-CH2-, в частности, -NR11-CH2-. При этом в этих предпочтительных значениях X1 R11 предпочтительно имеет одно из вышеуказанных предпочтительных значений, в частности, означает H.
В одной предпочтительной форме осуществления X2 означает простую связь.
В одной предпочтительной форме осуществления X3 означает N. При этом особенно предпочтительно, если m и n оба равны 2. В соответствии с этим кольцо, которое содержит X3 как кольцевой член, особенно предпочтительно означает пиперазин-1-ильное кольцо.
В одной альтернативно предпочтительной форме осуществления X3 означает CH. При этом особенно предпочтительно, если m и n оба равны 2. В соответствии с этим кольцо, которое содержит X3 как кольцевой член, особенно предпочтительно означает пиперидин-4-ильное кольцо.
В одной альтернативно предпочтительной форме осуществления X3 означает CH. При этом особенно предпочтительно, если m и n оба равны 1. В соответствии с этим кольцо, которое содержит X3 как кольцевой член, особенно предпочтительно означает азетидин-3-ильное кольцо.
В одной альтернативно предпочтительной форме осуществления X3 означает CH. При этом особенно предпочтительно, если m означает 1, а n означает 2. В соответствии с этим кольцо, которое содержит X3 как кольцевой член, особенно предпочтительно означает пирролидин-3-ильное кольцо.
Однако особенно предпочтительно X3 означает N, и m и n оба означают 2, или X3 означает CH, и m и n оба означают 1. В частности, X3 означает N, а m и n оба означают 2.
В одной предпочтительной форме осуществления A означает фенилен, например, 1,2-, 1,3- или 1,4-фенилен. При этом особенно предпочтительно A означает 1,3- или 1,4-фенилен, в частности, 1,4-фенилен.
В одной альтернативно предпочтительной форме осуществления A означает пиридилен или пиримидилен, особенно предпочтительно пиридилен. Особенно предпочтительно A в этом случае означает 3,5- или 3,6-пиридилен, в частности, 3,6-пиридилен.
Однако особенно предпочтительно A означает фенилен, например, 1,2-, 1,3- или 1,4-фенилен, более предпочтительно 1,3- или 1,4-фенилен, в частности, 1,4-фенилен.
A предпочтительно не замещено R10.
Предпочтительным объектом изобретения являются соединения формулы I, где
R1 означает H или метокси;
R2 означает H;
R3 означает метокси;
R4 означает H, метил или этил;
R5 означает этокси;
R6 означает H;
R7 означает CN;
R8 означает H или F;
X1 означает -NH- или -NHCH2-;
X2 означает простую связь;
X3 означает N;
X4 означает N;
A означает 1,4-фенилен;
a равно 0; и
m и n означают 2;
а также их фармацевтически приемлемые соли и пролекарства.
Особенно предпочтительным объектом изобретения являются при этом соединения формулы I, в которых:
R1 означает H или метокси;
R2 означает H;
R3 означает метокси;
R4 означает H или метил;
R5 означает этокси;
R6 означает H;
R7 означает CN;
R8 означает H или F;
X1 означает -NHCH2-;
X2 означает простую связь;
X3 означает N;
X4 означает N;
A означает 1,4-фенилен;
a равно 0; и
m и n означают 2;
а также их фармацевтически приемлемые соли и пролекарства.
Предпочтительным объектом изобретения являются соединения формулы I, в которых
R1 означает H или метокси;
R2 означает H;
R3 означает метокси;
R4 означает H, метил или этил;
R5 означает этокси;
R6 означает H;
R7 означает I;
R8 означает H;
X1 означает -NH- или -NHCH2-;
X2 означает простую связь;
X3 означает N;
X4 означает N;
A означает 1,4-фенилен;
a равно 0; и
m и n означают 2;
а также их фармацевтически приемлемые соли и пролекарства.
Особенно предпочтительным объектом изобретения при этом являются соединения формулы I, в которых
R1 означает H или метокси;
R2 означает H;
R3 означает метокси;
R4 означает H или метил;
R5 означает этокси;
R6 означает H;
R7 означает I;
R8 означает H;
X1 означает -NHCH2-;
X2 означает простую связь;
X3 означает N;
X4 означает N;
A означает 1,4-фенилен;
a равно 0; и
m и n означают 2;
а также их фармацевтически приемлемые соли и пролекарства.
Примерами предпочтительных вариантов осуществления настоящего изобретения являются соединения формул I.1-I.56, а также их фармацевтически приемлемые соли и пролекарства, где остатки X1, R1, R2, R3, R4, R7 и R8 имеют указанные выше общие значения или, в частности, предпочтительные значения. Особенно предпочтительно, остатки R1, R2, R3, R4, R7 и R8 имеют значения, приведенные в таблице A.
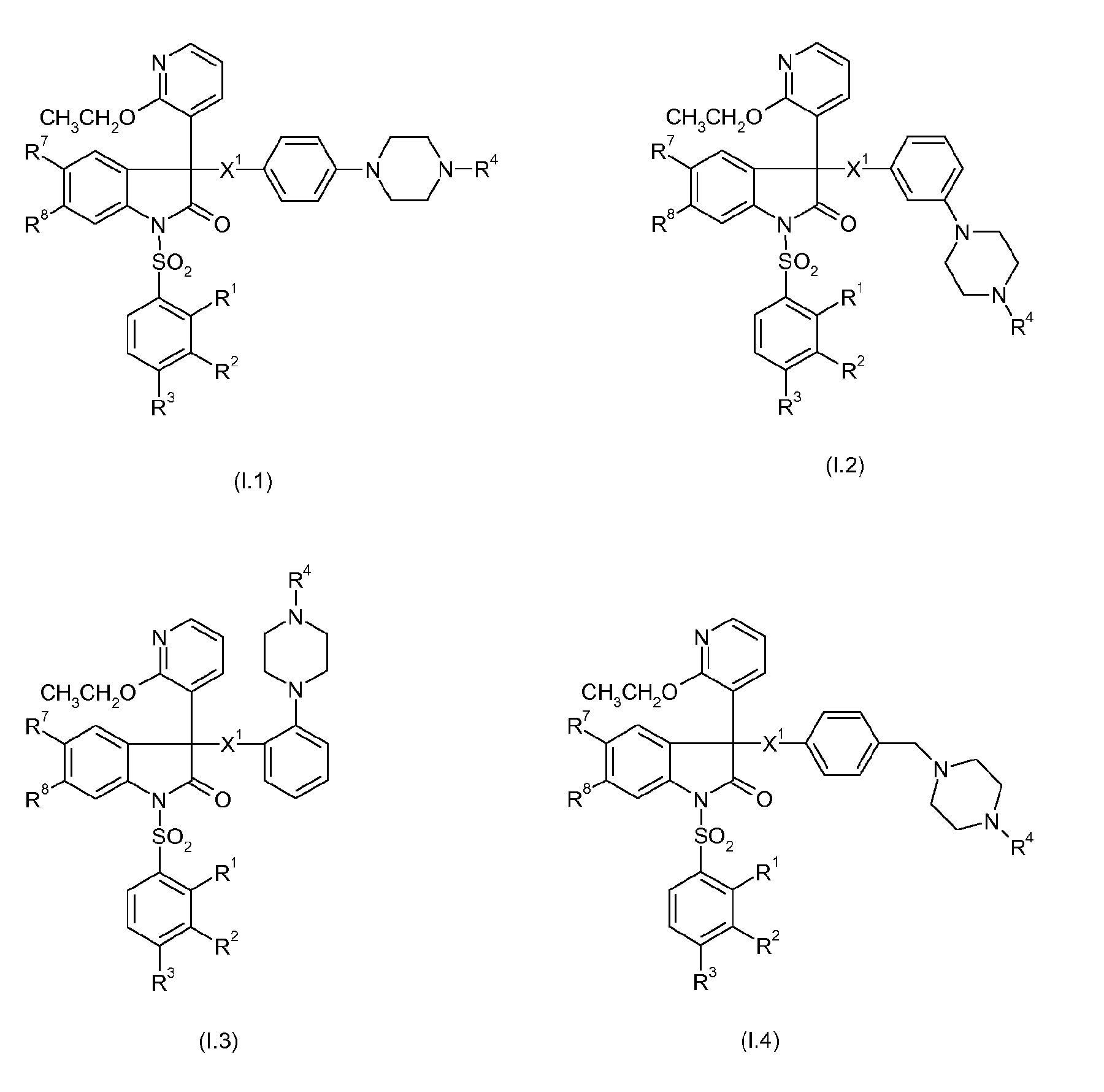
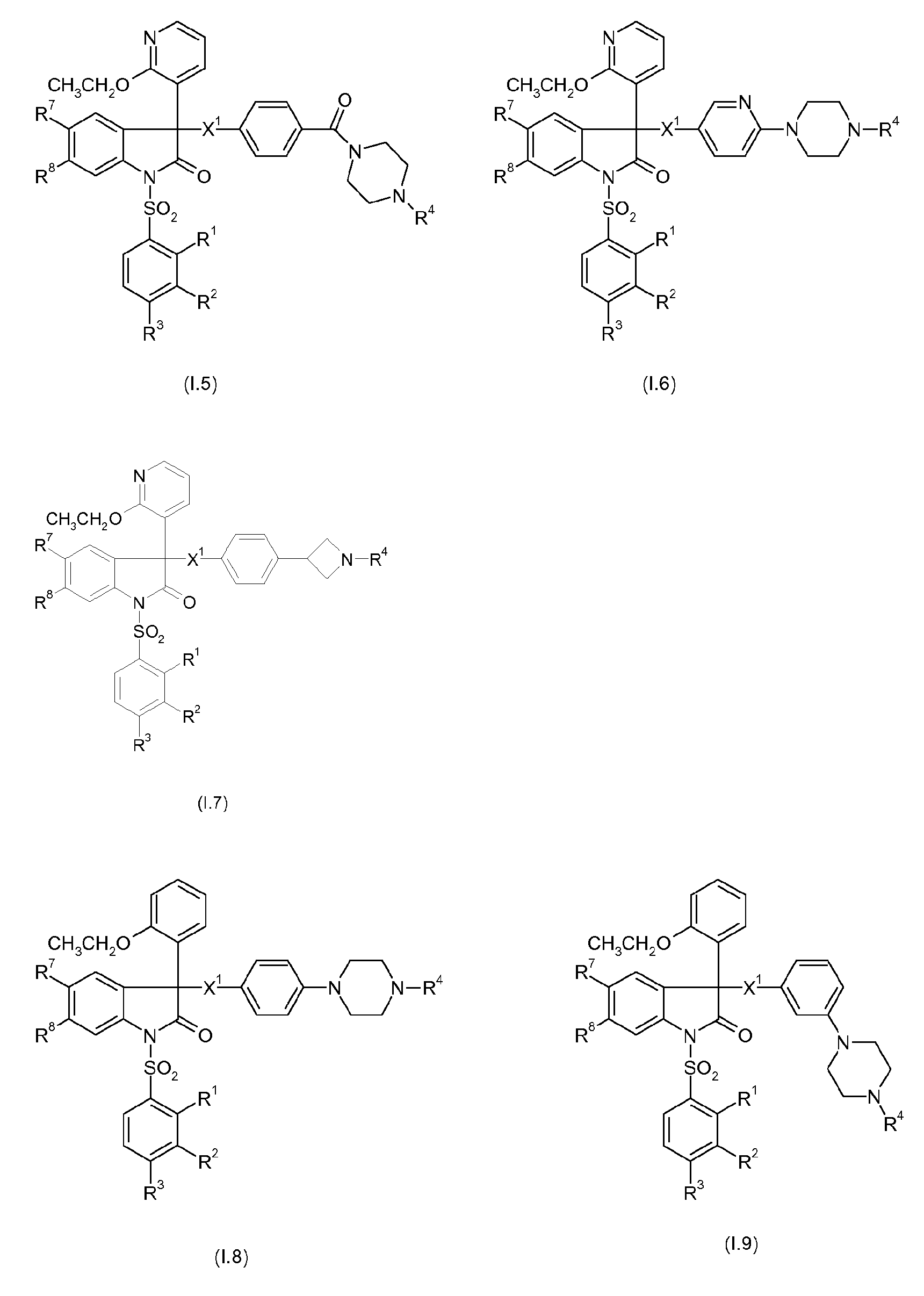
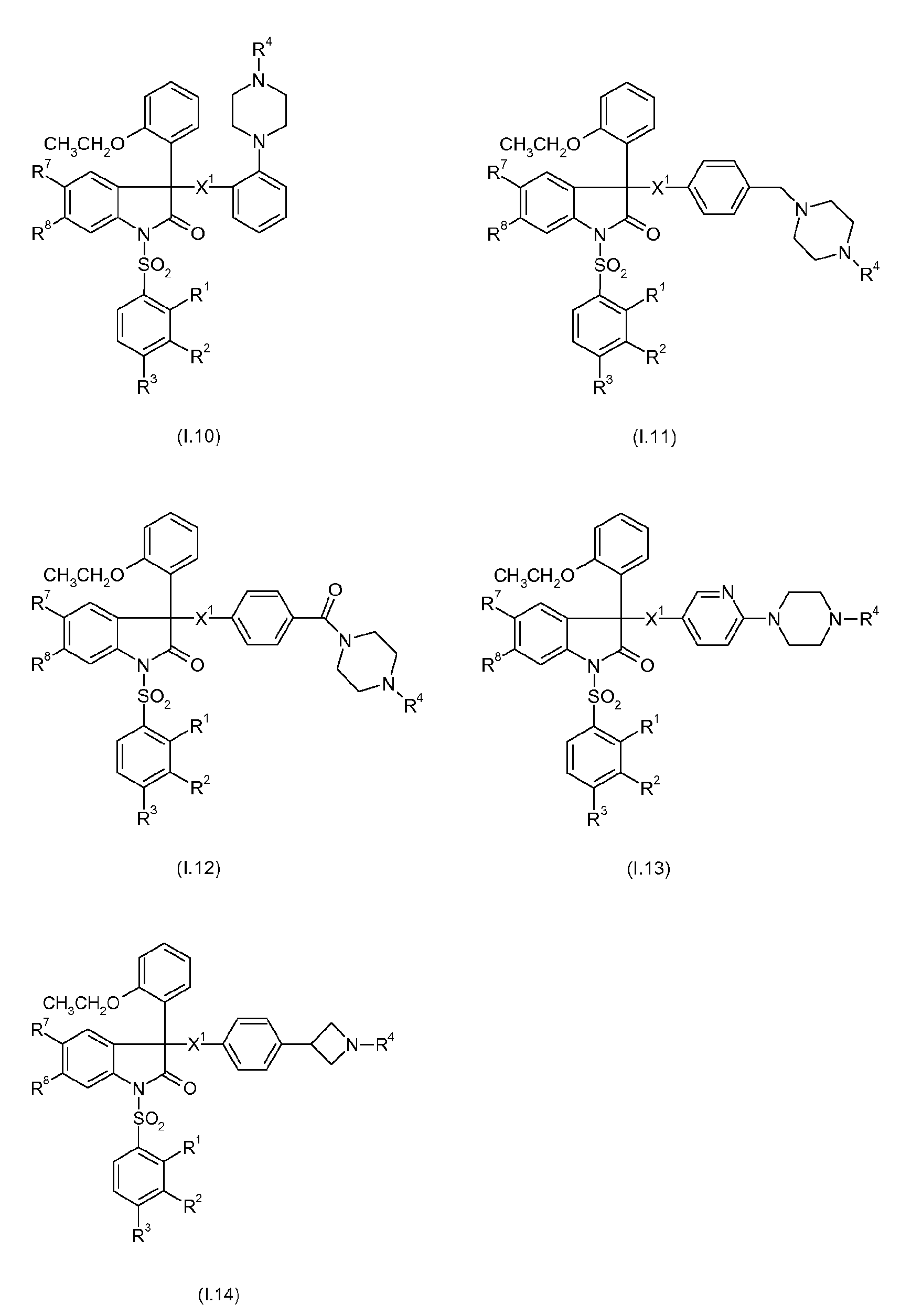
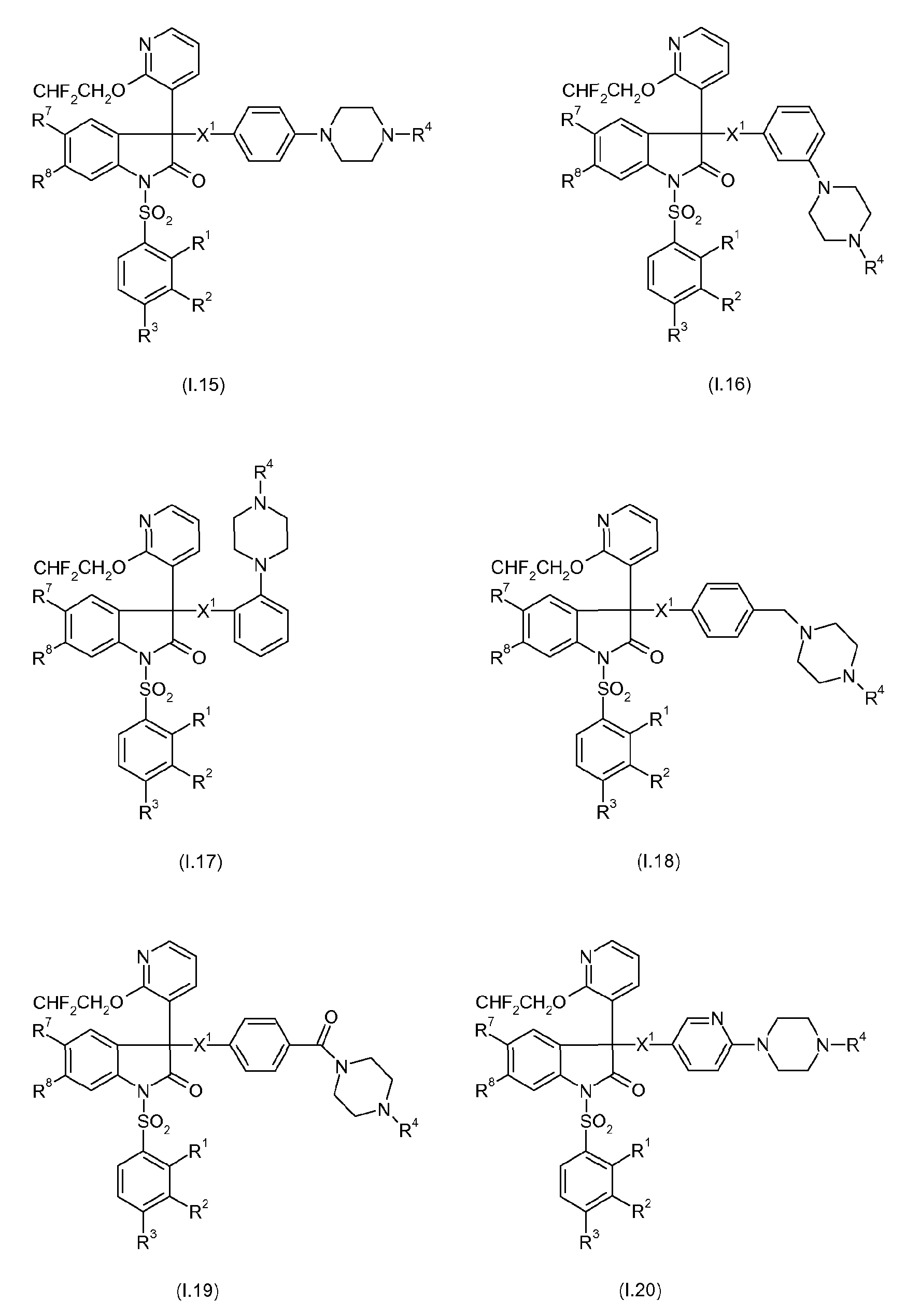
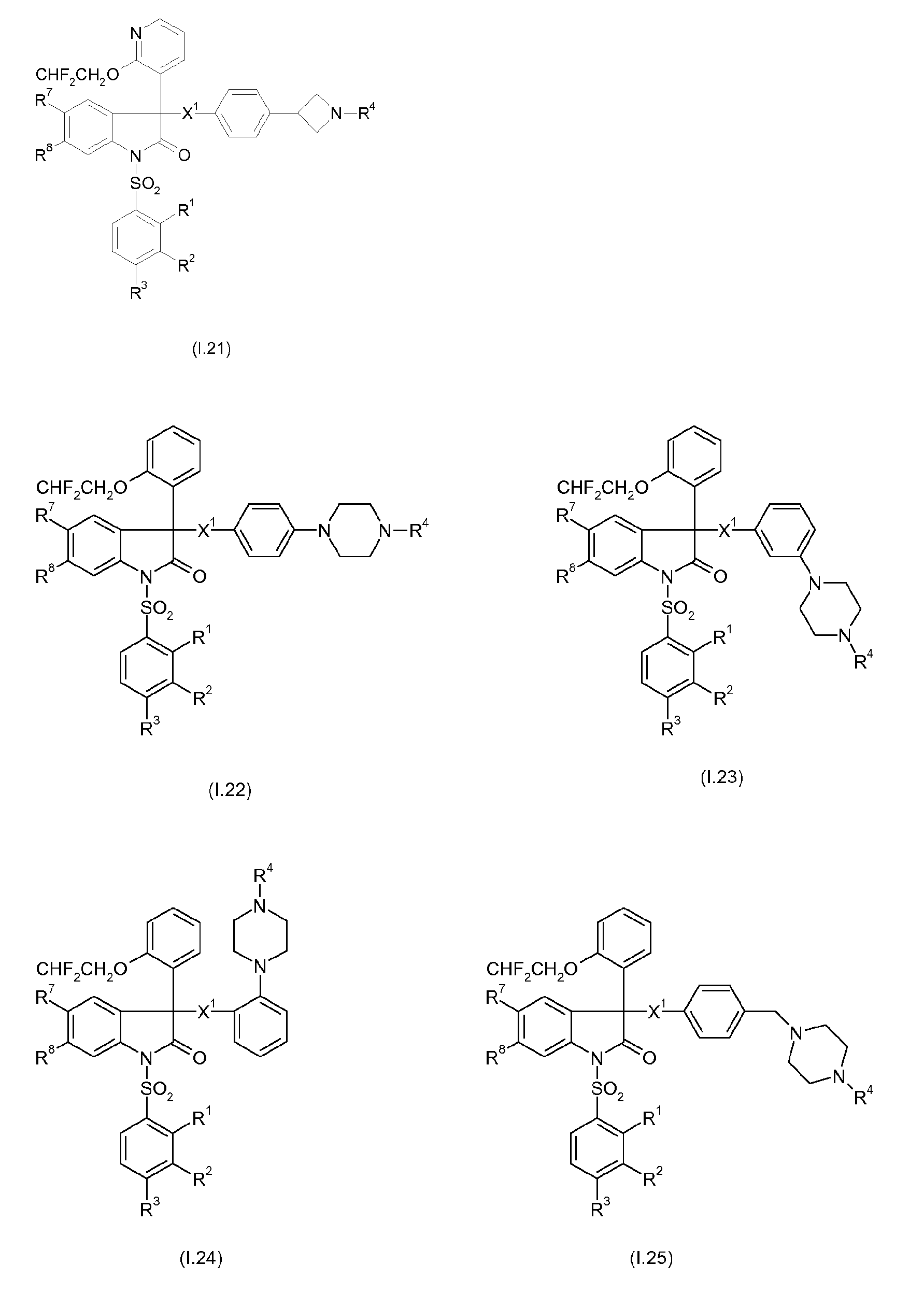
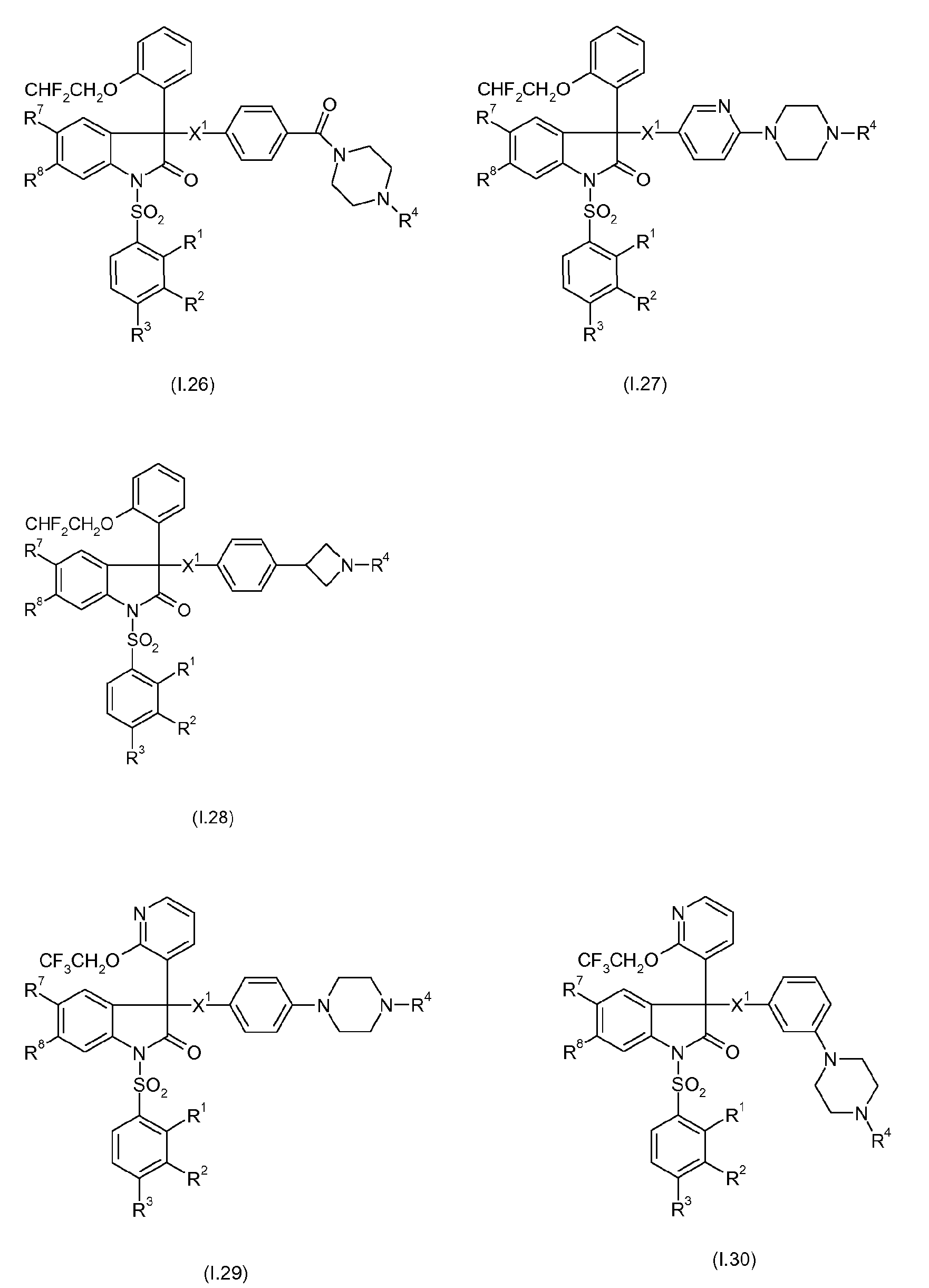
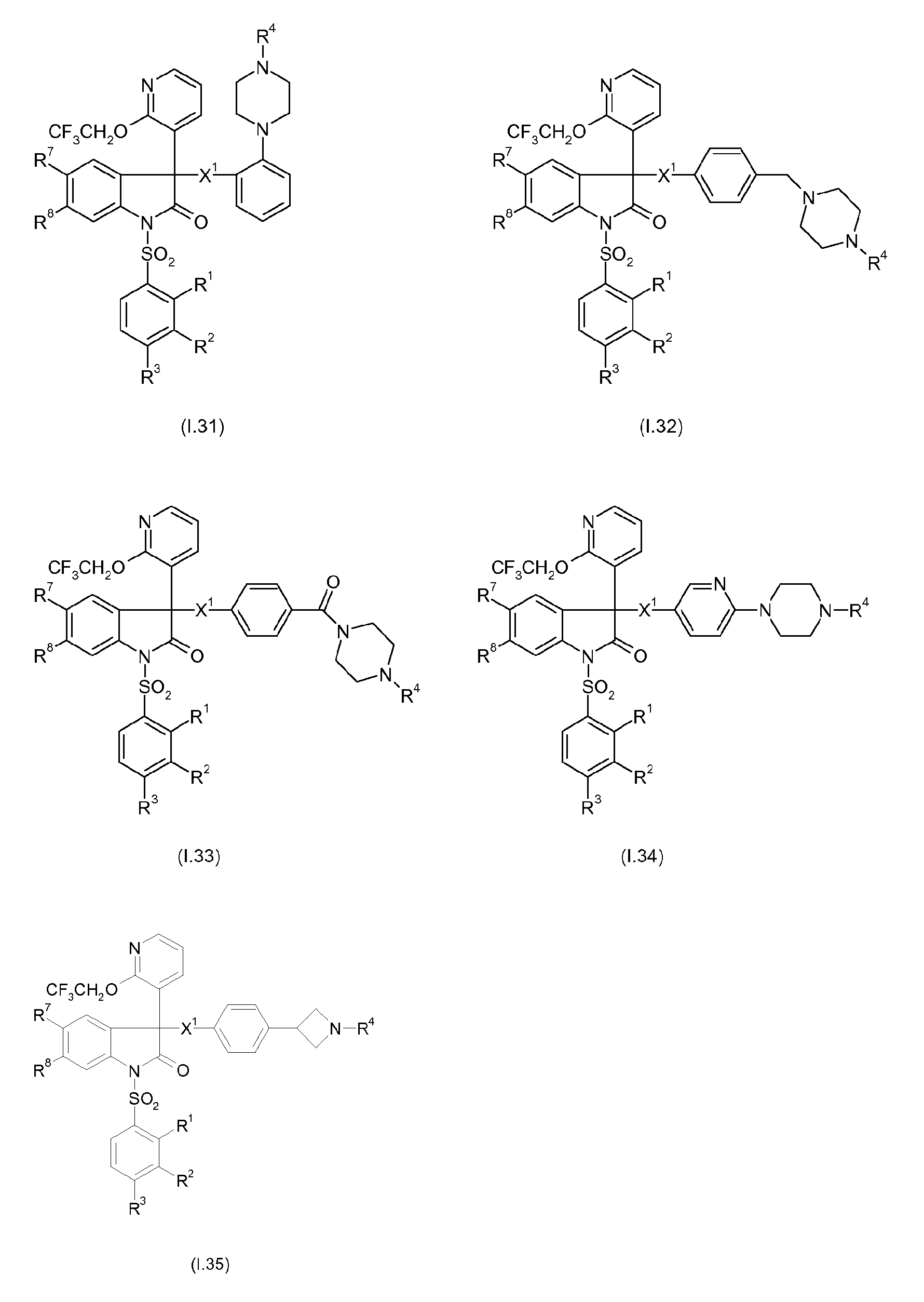
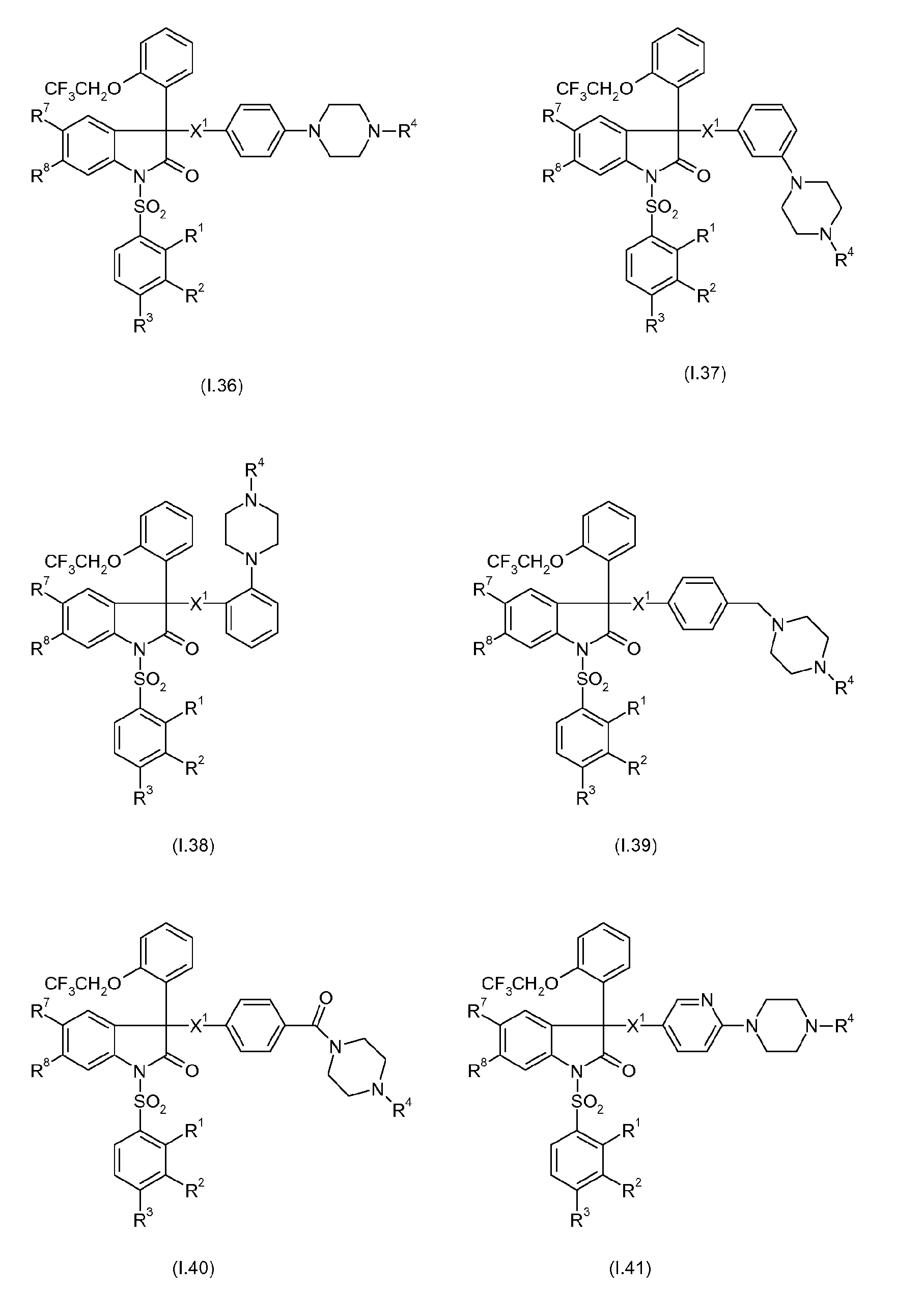
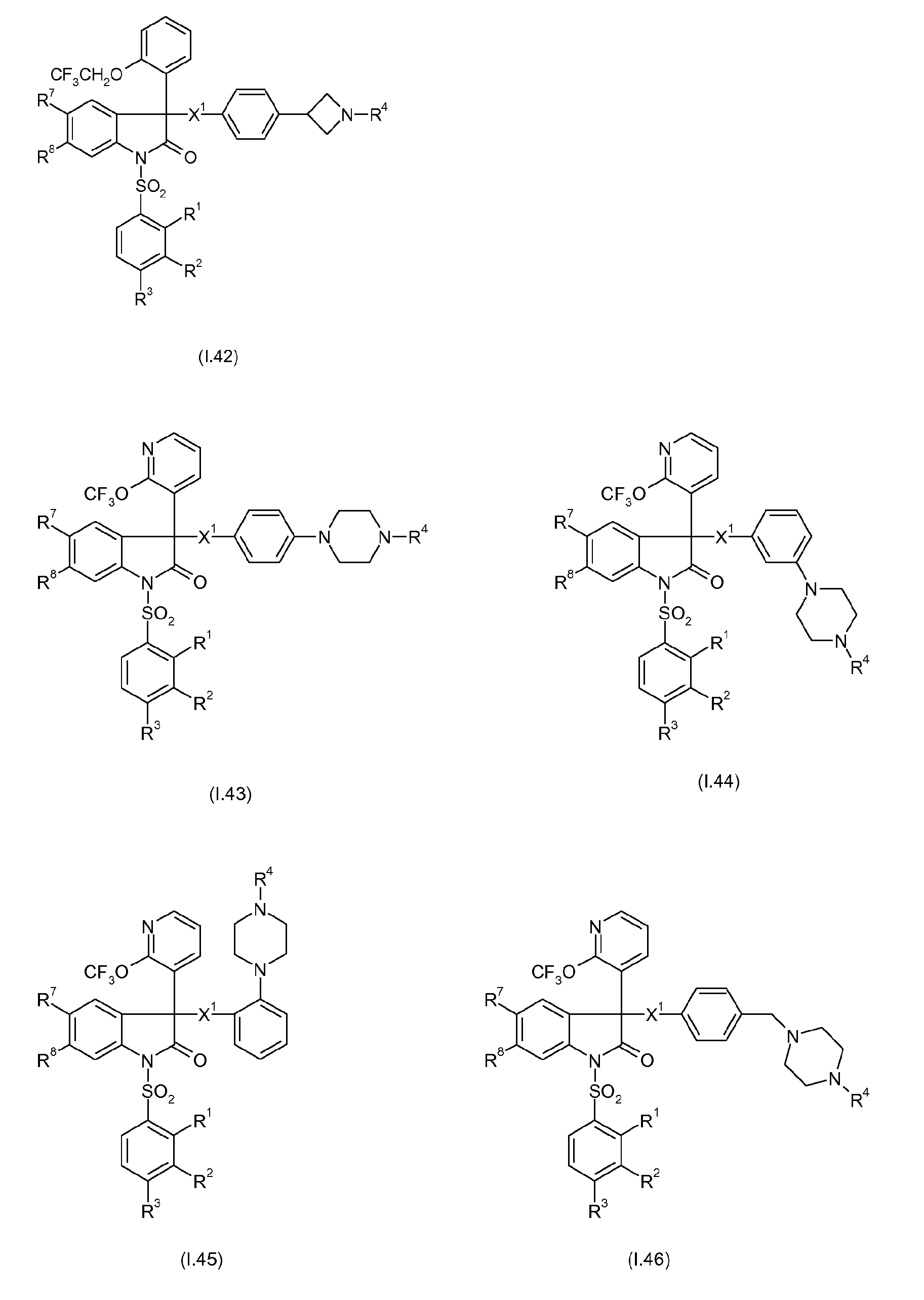
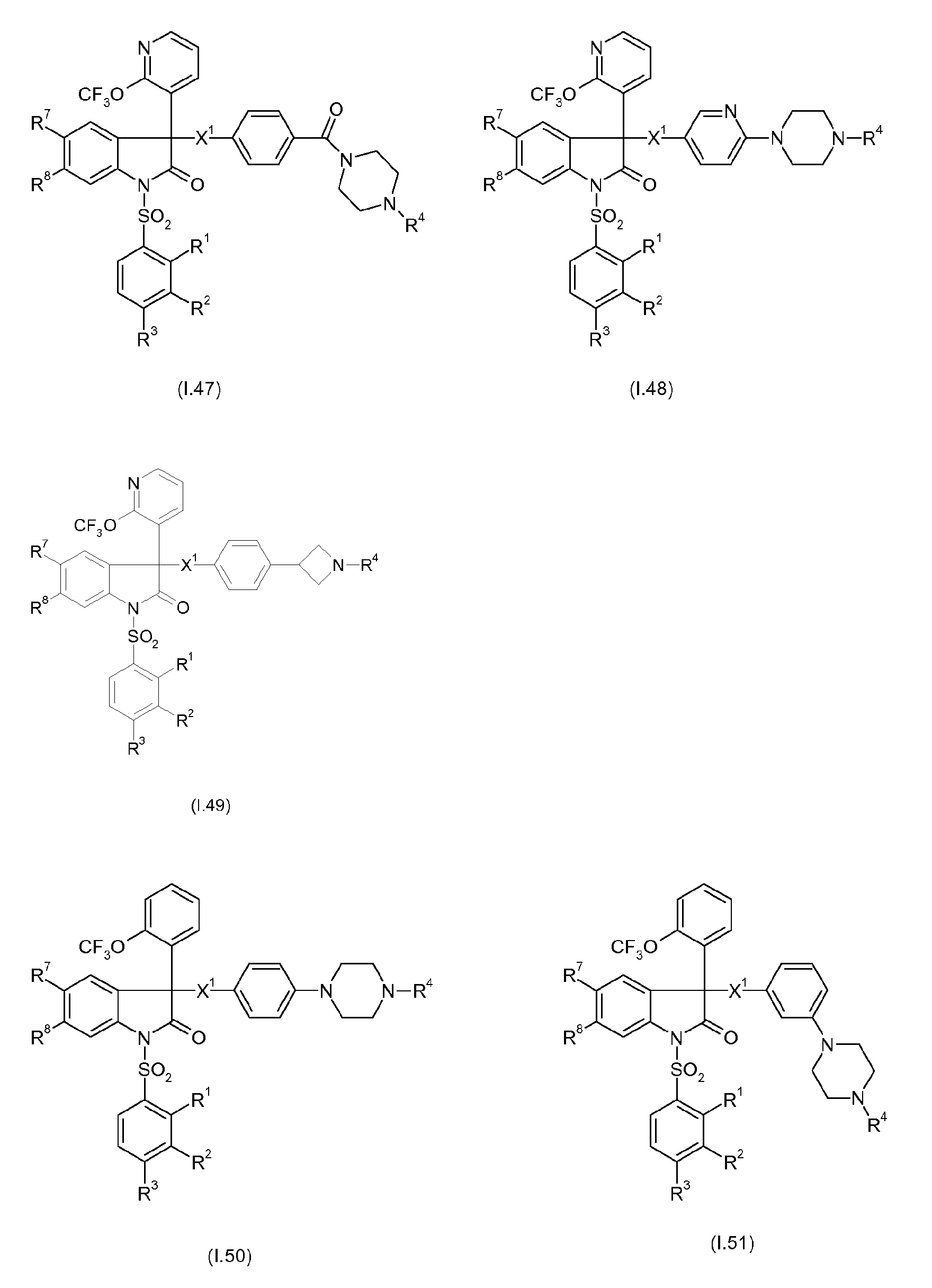
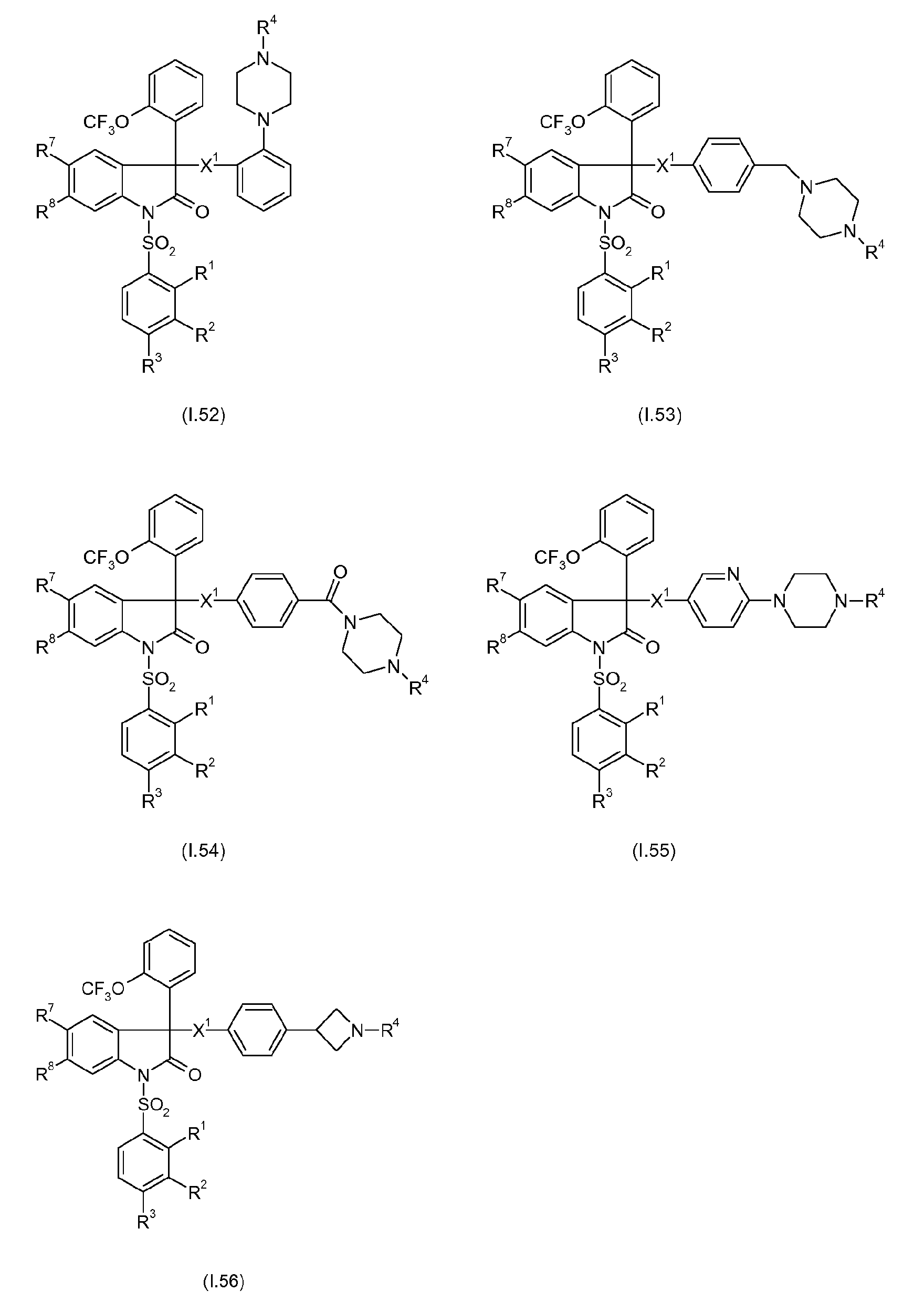
Предпочтительные соединения формул I.1-I.56 указаны в следующих таблицах 1-336.
Таблица 1
Соединения формулы I.1, в которых X1 означает -NH2-CH2-, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблица 2
Соединения формулы I.1, в которых X1 означает -NH-, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблица 3
Соединения формулы I.1, в которых X1 означает -NH-C(=O)-, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблица 4
Соединения формулы I.1, в которых X1 означает -O-CH2-, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблица 5
Соединения формулы I.1, в которых X1 означает -O-, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблица 6
Соединения формулы I.1, в которых X1 означает X1 -O-C(=O)-, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 7-12
Соединения формулы I.2, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 13-18
Соединения формулы I.3, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 19-24
Соединения формулы I.4, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 25-30
Соединения формулы I.5, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 31-36
Соединения формулы I.6, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 37-42
Соединения формулы I.7, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 43-48
Соединения формулы I.8, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 49-54
Соединения формулы I.9, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 55-60
Соединения формулы I.10, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 61-66
Соединения формулы I.11, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 67-72
Соединения формулы I.12, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 73-78
Соединения формулы I.13, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 79-84
Соединения формулы I.14, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 85-90
Соединения формулы I.15, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 91 -96
Соединения формулы I.16, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 97-102
Соединения формулы I.17, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 103-108
Соединения формулы I.18, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 109-114
Соединения формулы I.19, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 115-120
Соединения формулы I.20, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 121-126
Соединения формулы I.21, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 127-132
Соединения формулы I.22, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 133-138
Соединения формулы I.23, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 139-144
Соединения формулы I.24, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 145-150
Соединения формулы I.25, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 151-156
Соединения формулы I.26, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 157-162
Соединения формулы I.27, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 163-168
Соединения формулы I.28, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 169-174
Соединения формулы I.29, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 175-180
Соединения формулы I.30, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 181-186
Соединения формулы I.31, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 187-192
Соединения формулы I.32, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 193-198
Соединения формулы I.33, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 199-204
Соединения формулы I.34, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 205-210
Соединения формулы I.35, причем X1 в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 211-216
Соединения формулы I.36, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 217-222
Соединения формулы I.37, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 223-228
Соединения формулы I.38, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 229-234
Соединения формулы I.39, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 235-240
Соединения формулы I.40, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 241-246
Соединения формулы I.41, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 247-252
Соединения формулы I.42, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 253-258
Соединения формулы I.43, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 259-264
Соединения формулы I.44, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 265-270
Соединения формулы I.45, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 271-276
Соединения формулы I.46, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 277-282
Соединения формулы I.47, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 283-288
Соединения формулы I.48, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 289-294
Соединения формулы I.49, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 295-300
Соединения формулы I.50, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 301-306
Соединения формулы I.51, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 307-312
Соединения формулы I.52, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 313-318
Соединения формулы I.53, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 319-324
Соединения формулы I.54, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 325-330
Соединения формулы I.55, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
Таблицы 331-336
Соединения формулы I.56, в которых X1 имеет соответственно одно из значений, указанных в таблицах 1, 2, 3, 4, 5 или 6, и комбинация R1, R2, R3, R4, R7 и R8 отвечает соответствующей строке в таблице A.
|
Из вышеуказанных соединений I.1-I.56 наиболее предпочтительны соединения формулы I.1.
Соединения I согласно изобретению имеют в положении 3 2-оксиндольного кольца центр хиральности. Поэтому соединения согласно изобретению могут присутствовать как смесь 1:1 энантиомеров (рацематов) или как нерацемическая смесь энантиомеров, которая обогащена одним из двух энантиомеров, либо энантиомером, который вращает плоскость колебаний линейно поляризованного света налево (т.е. левовращающий), далее (-)-энантиомер, либо энантиомером, который вращает плоскость колебаний линейно поляризованного света направо (т.е. правовращающий), далее (+)-энантиомер, или присутствует как по существу энантиомерно-чистые соединения, то есть как по существу энантиомерно-чистый (-)-энантиомер или (+)-энантиомер. Так как у соединений по изобретению в большинстве случаев существует единственный центр асимметрии, и не имеется никакой оси/поверхности хиральности, то нерацемическую смесь в этих случаях можно определить также как смесь энантиомеров, в которой преобладает или R-, или S-энантиомер. В соответствии с этим, по существу энантиомерно-чистые соединения в этих случаях можно определить также как по существу энантиомерно-чистый R-энантиомер или по существу энантиомерно-чистый S-энантиомер.
Под "по существу энантиомерно-чистыми соединениями" в рамках настоящего изобретения понимаются такие соединения, которые имеют избыток энантиомеров (enantiomeric excess, ee; % ee =(R-S)/(R+S)×100 или (S-R)/(S+R)×100) по меньшей мере 80% ee, предпочтительно по меньшей мере 85% ee, более предпочтительно по меньшей мере 90% ee, еще более предпочтительно по меньшей мере 95% ee и, в частности, по меньшей мере 98% ee.
В одном варианте осуществления изобретения соединения согласно изобретению присутствуют как по существу энантиомерно-чистые соединения. Особенно предпочтительны соединения, которые имеют избыток энантиомеров по меньшей мере 85% ee, более предпочтительно по меньшей мере 90% ee, еще более предпочтительно по меньшей мере 95% ee, в частности, по меньшей мере 98% ee.
Таким образом, объектом изобретения являются как чистые энантиомеры, так и их смеси, например, смеси, в которых энантиомер находится в обогащенной форме, но также и рацематы. Объектом изобретения являются также фармацевтически приемлемые соли и пролекарства чистых энантиомеров соединений I, а также энантиомерные смеси в форме фармацевтически приемлемых солей и пролекарств соединений I.
Далее описываются иллюстративные пути синтеза для получения производных оксиндола согласно изобретению.
Получение соединений согласно изобретению можно осуществить с применением инструкций, описанных в WO 2005/030755 и WO 2006/005609 для синтеза аналогичных соединений, и для примера изображено на схемах синтеза 1-5. В этих схемах синтеза переменные имеют те же значения, что и в формуле I.
3-гидрокси-1,3-дигидроиндол-2-оны IV можно получить присоединением металлированных бензолов или гетероциклов III к 3-кето-группе изатина II. Металлированные бензолы или гетероциклы, такие как, например, соответствующее соединение Гриньяра (Mg) или литийорганическое соединение, можно получить обычным путем из галогеновых или углеводородных соединений. Типичные инструкции содержатся в Houben-Weyl, Methoden der Organischen Chemie, Bd. 13, 1-2, Kap. Mg- bzw. Li-Verbindungen (Методы органической химии, т.13, гл.1-2, Соединения Mg или Li). Изатин II можно или купить, или получить по аналогии со способами, описанными в литературе (Advances in Heterocyclic Chemistry, A.R. Katritzky and A.J. Boulton, Academic Press, New York, 1975, 18, 2-58; J. Brazil. Chem. Soc. 12,273-324,2001).
3-гидроксиоксиндолы IV, которые в 6-членных ароматических соединениях, например, в положении 5 и/или 6 в качестве остатка R7 или R8 содержат йод или бром, можно с помощью KCN или Zn(CN)2 в условиях катализа на Pd(0) в растворителях, как диметилформамид или тетрагидрофуран, при необходимости также с добавкой оснований, как K2CO3 или другие карбонаты или амины, при повышенной температуре перевести в аналогичный, содержащий циан, 3-гидроксиоксиндол IV. В качестве солей Pd(0) можно назвать, например, комплексы переходных металлов, которые получают in situ из PdCl2 или Pd(OAc)2 добавлением фосфинов, как трис(орто-толил)фосфин. Можно также использовать покупные комплексы палладия, как, например, катализатор тетракис(трифенилфосфин)-палладий(0) и/или добавки фосфиновых лигандов.
3-гидроксиоксиндолы IV можно перевести в соединения V, которые несут уходящую группу LG' в положении 3, причем уходящая группа LG' является обычной уходящей группой, как, например, хлорид или бромид, а также активированной OH, как тозилат или трифлат. Промежуточный продукт V, например, с LG' = хлор, можно получить обработкой спирта IV тионилхлоридом в присутствии основания, как, например, пиридин, в подходящем растворителе, как, например, дихлорметан.
Затем соединения V можно реакцией замещения с карбоновой кислотой, карбоксамидом, амином или спиртом VIII превратить в амины VI. Позднее соединения VI можно путем обработки сульфохлоридами VII после депротонирования сильным основанием, как, например, трет-бутилат калия или гидрид натрия, в ДМФ, превратить в сульфонилированный продукт I. Используемые сульфохлориды VII можно или купить, или получить известными способами (например, J. Med. Chem. 40, 1149 (1997)) (схема синтеза 1).
Получение соединений I по изобретению с R4=H можно осуществить применением соответствующих защищенных Boc соединений VIII (R4=Boc). Впоследствии защитную группу Boc можно удалить, например, обработкой трифторуксусной кислотой в дихлорметане.
Соединения VIII можно либо купить, либо можно получить обычными реакциями замещения на (гетеро)ароматических соединениях A, при необходимости с применением метода защитных групп.
Схема синтеза 1:
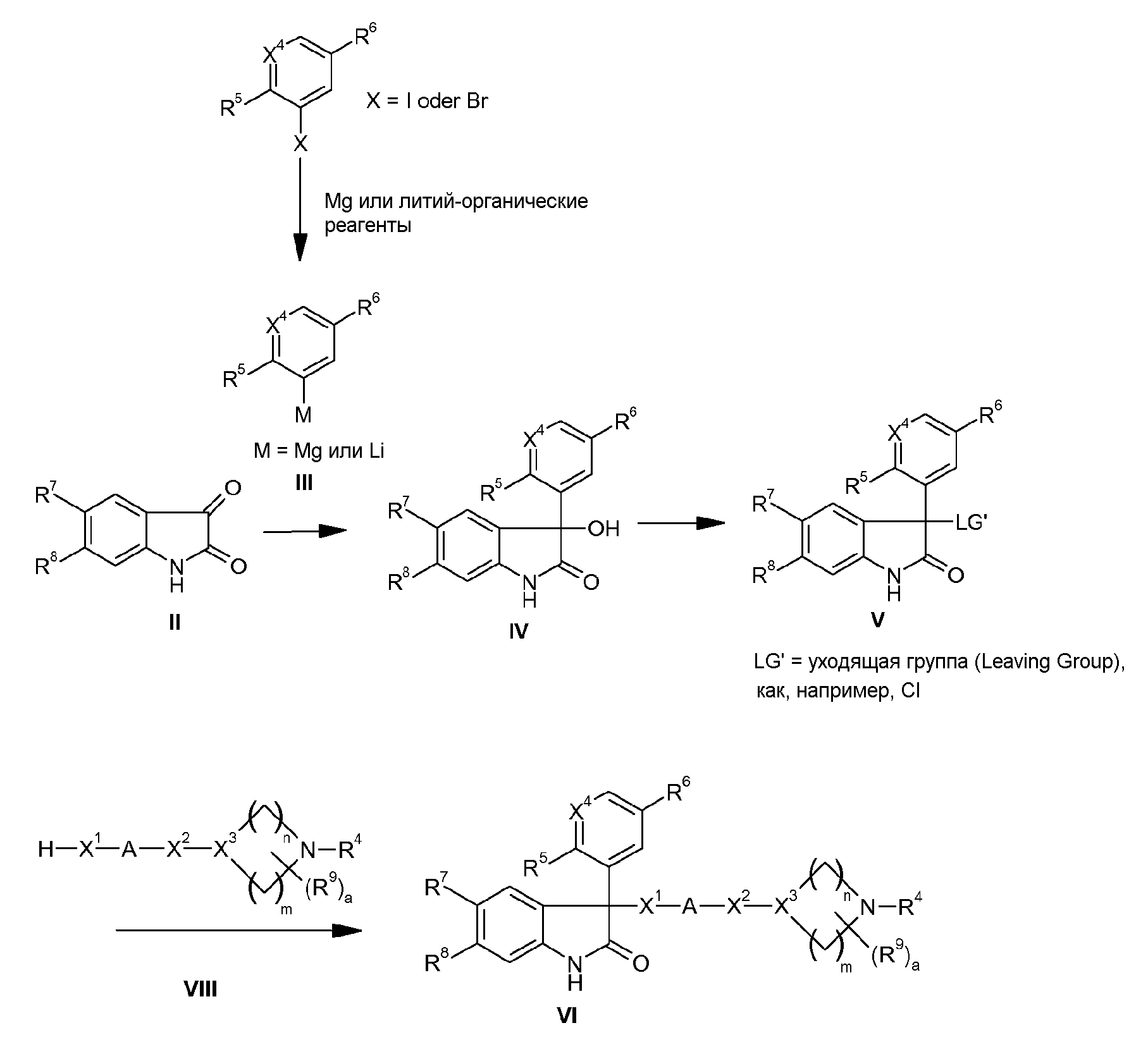
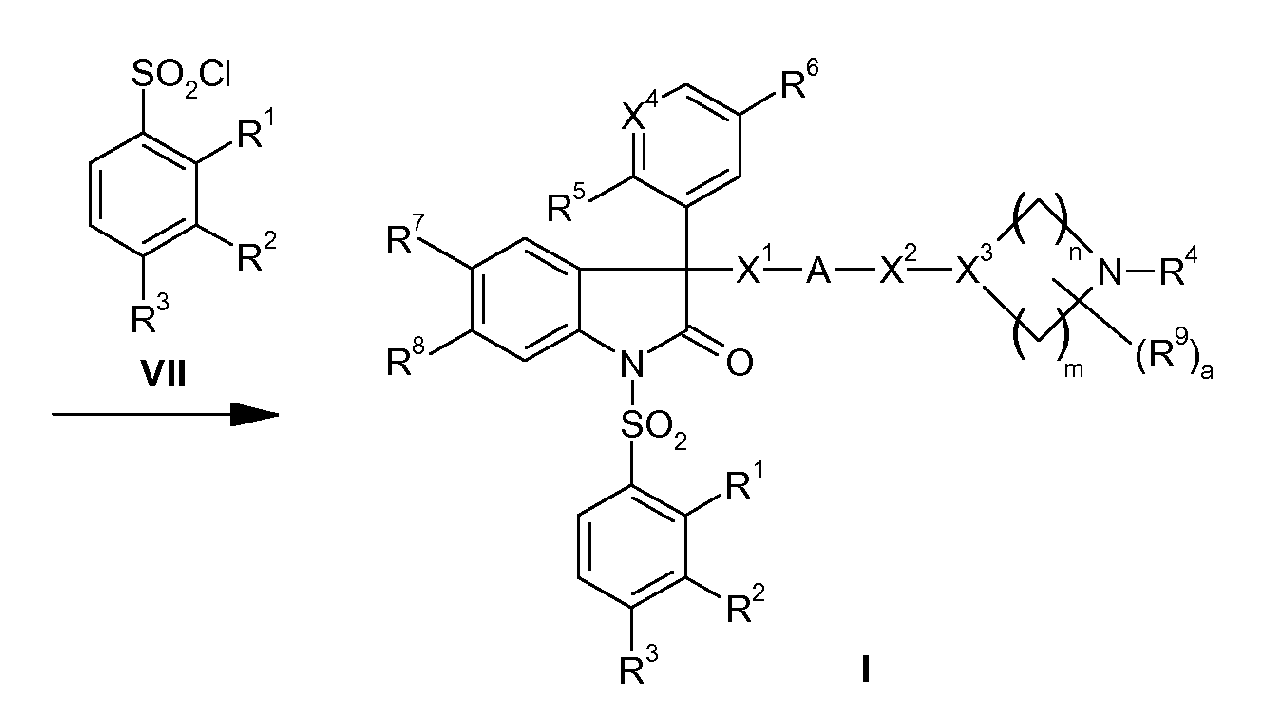
Соединения I, в которых X означает -NR11-CO-, можно альтернативно получить тем, что соединения V реакцией замещения с аминами, такими как, например, аммиак или амин NH2R11, превращают в амин IX.
Наконец, соединения IX обработкой сульфохлоридами VII после депротонирования с сильным основанием, таким как, например, трет-бутилат калия или гидрид натрия в ДМФ, можно перевести в сульфонилированный продукт X. Используемые сульфохлориды VII можно либо купить, либо получить известными способами (например, J. Med. Chem. 40, 1149 (1997)).
Последующая реакция с карбонилхлоридами XI ведет к получению соединений общей формулы (I) согласно изобретению с карбоксамидным мостиком (X1=NR11-CO).
Получение соединений I согласно изобретению с R4=H можно осуществить путем применения соответствующих защищенных Boc соединений XI (R4=Boc). Впоследствии защитную группу Boc можно удалить, например, обработкой трифторуксусной кислотой в дихлорметане.
Соединения XI можно либо купить, либо можно получить обычными реакциями замещения на (гетеро)ароматических соединениях A, при необходимости с применением метода защитных групп.
Схема синтеза 2:
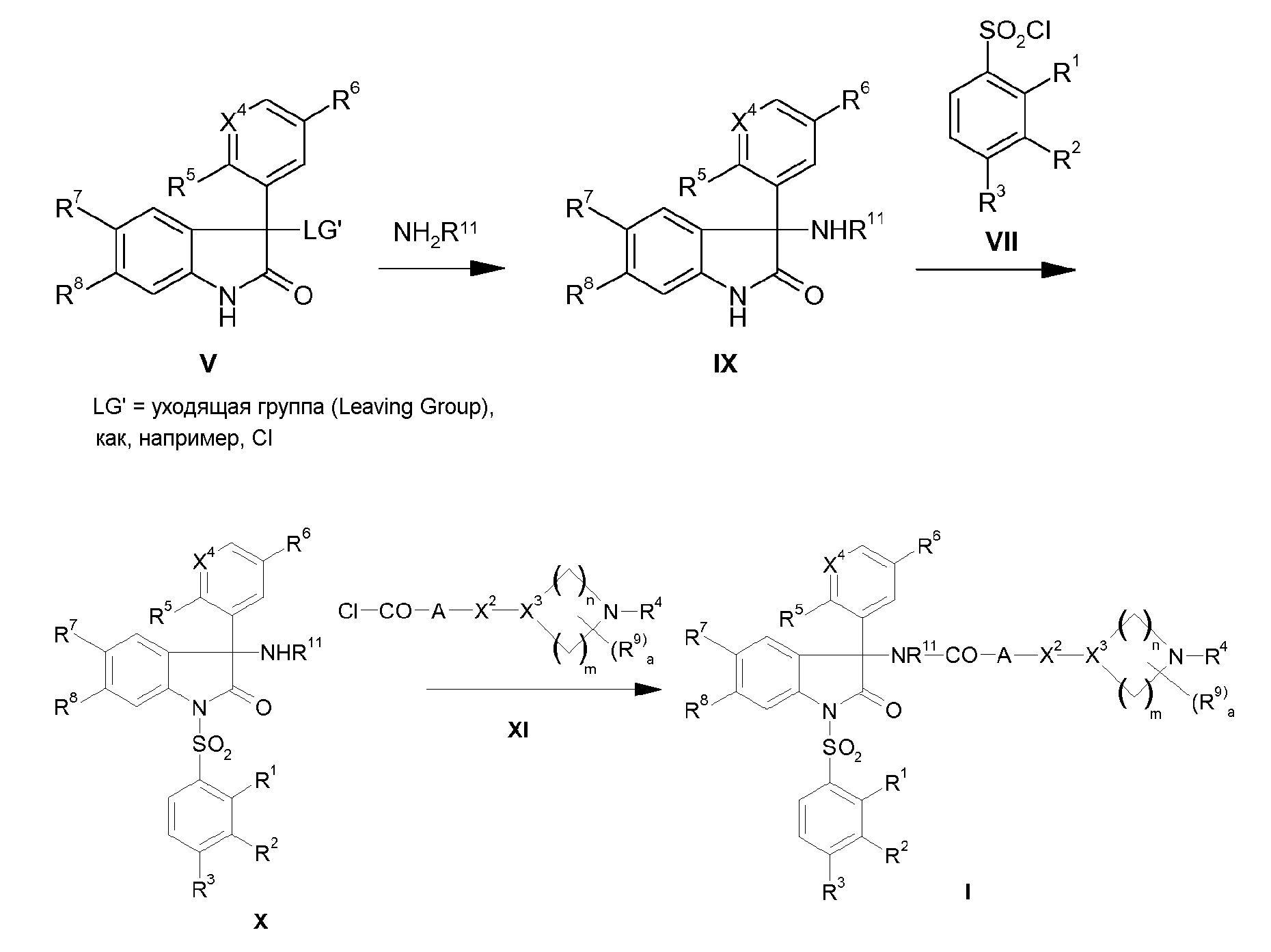
Альтернативно, сульфонилирование в схеме 2 можно также провести только после реакции с соединением XI.
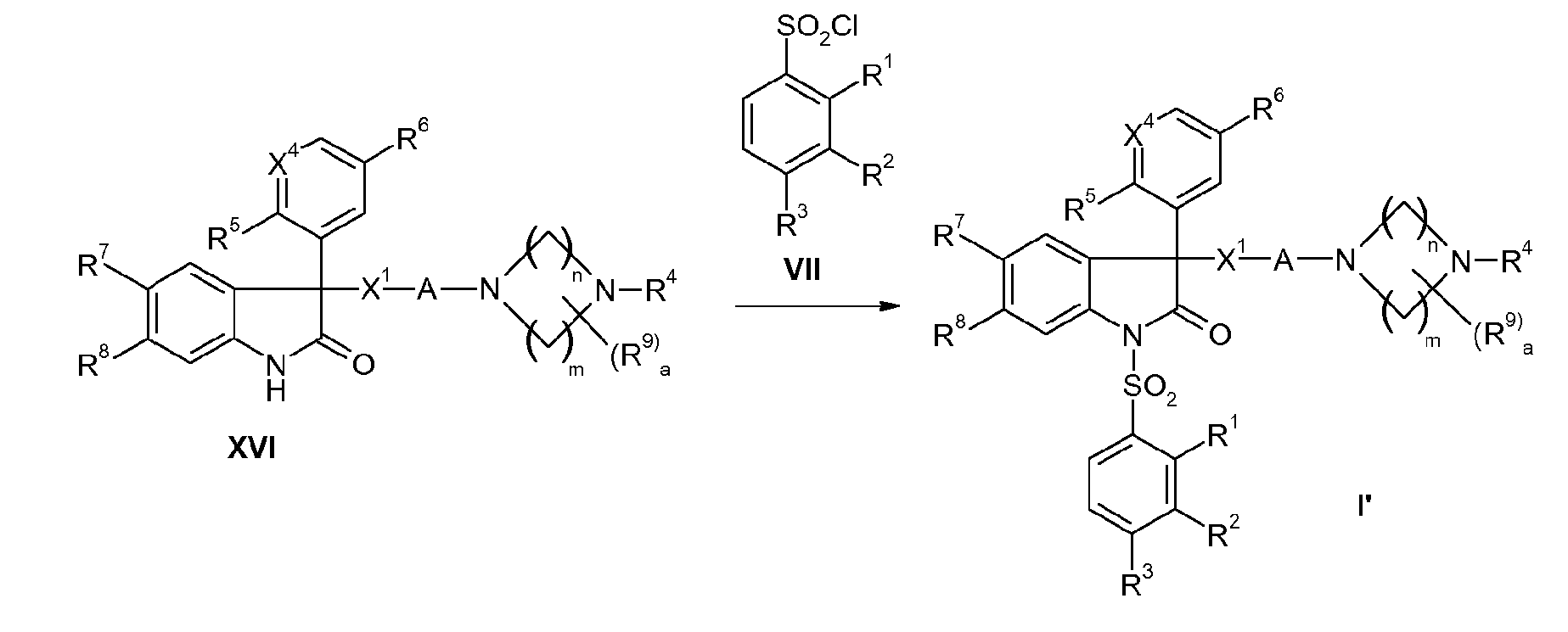
Соединения формулы I, где X2 означает простую связь, и X3 означает N, можно альтернативно получить также тем, что в вышеописанных реакционных схемах 1 и 2 вместо соединения VIII (в схеме 1) или вместо соединения XI (в схеме 2) использовать соединение XII (реакционная схема 3) или соединение XIII (реакционная схема 4), где R12 означает галоген, CN, ORa или NRbRc, причем Ra означает H, C1-C4-алкил, фенил или бензил; и Rb и Rc независимо друг от друга означают H, C1-C4-алкил, C1-C4-алкокси, фенил или бензил, предпочтительно галоген, в частности, Br. Полученное в схеме 3 соединение XIV можно позднее соединить с циклическим амином XV в условиях катализа на палладии, согласно способу, описанному в Tetrahedron Asym. 1999, 10, 1831, с образованием соединения XVI, которое аналогично описанной выше реакции сульфонилирования с сульфонилхлоридом VII можно превратить в соединение I' согласно изобретению, где X2 означает простую связь, и X3 означает N. Соединение XVII, получаемое в схеме 4, можно соединить с циклическим амином XV в условиях катализа на палладии, описанном в Tetrahedron Asym. 1999, 10, 1831, с образованием соединения I'.
Альтернативно, соединение XIV можно также сначала подвергнуть реакции сульфонилирования с получением соединения XVIII, а затем реакцией с амином формулы XV превратить в соединение I (реакционная схема 5).
Описание соединений I согласно изобретению с R4=H можно провести путем применения соответствующих защищенных Boc соединений XV (R4=BOG). Впоследствии защитную группу Boc можно удалить, например, обработкой трифторуксусной кислоты в дихлорметане.
Соединения XII, XIII и XV либо можно купить, либо можно получить обычными реакциями замещения на (гетеро)ароматических соединениях A или N-гетероцикле, при необходимости с применением метода защитных групп.
Реакционная схема 3
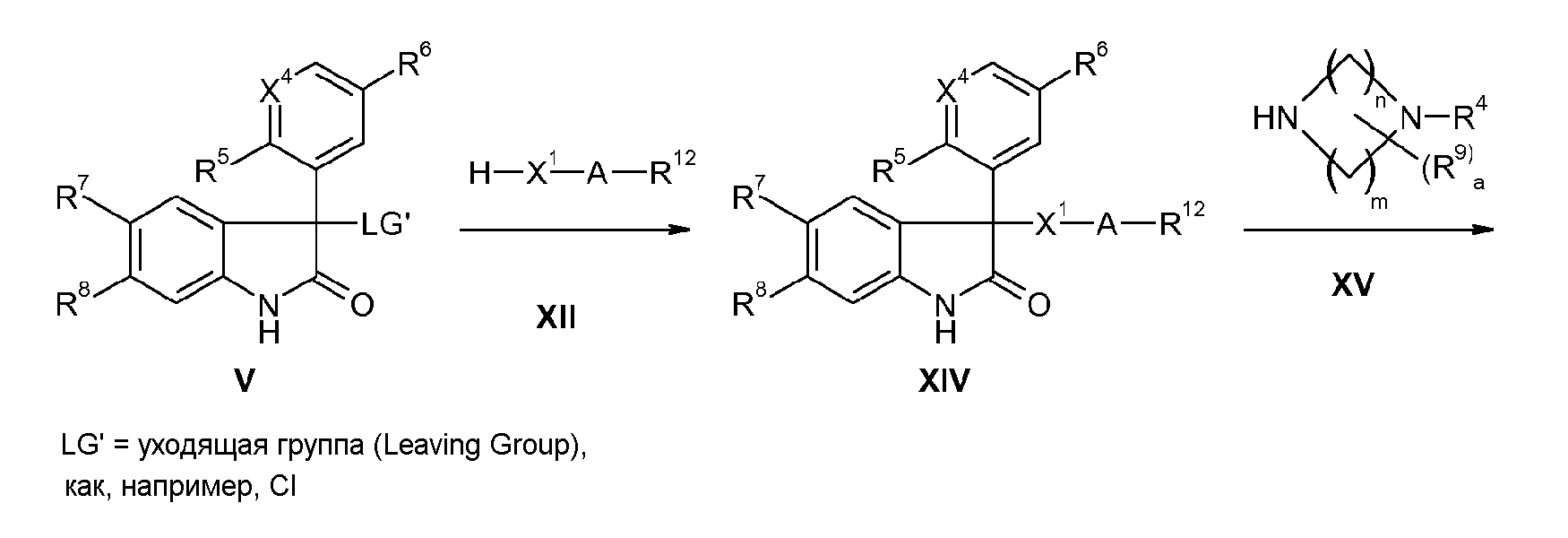
Реакционная схема 4:
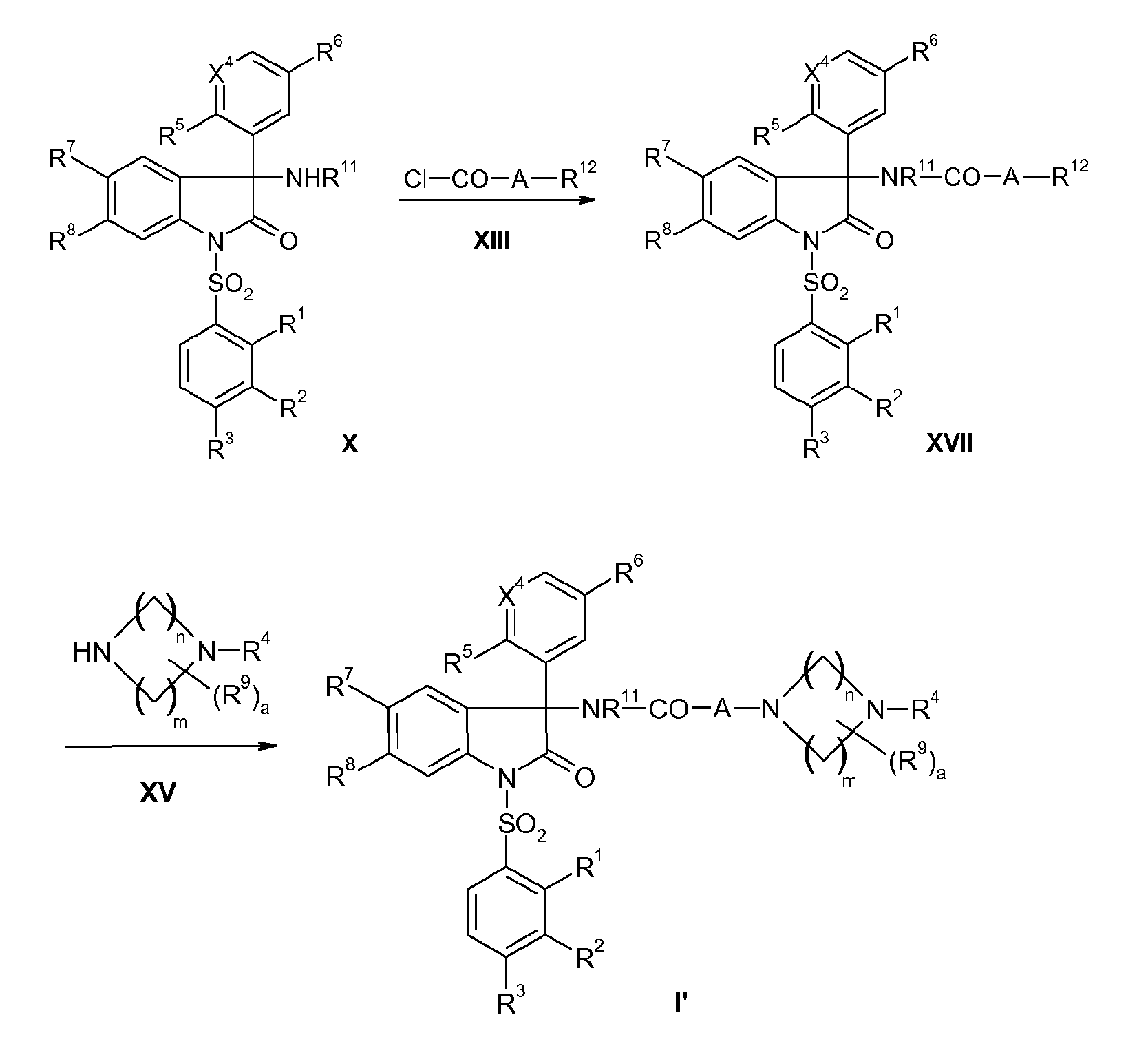

Реакционная схема 5:
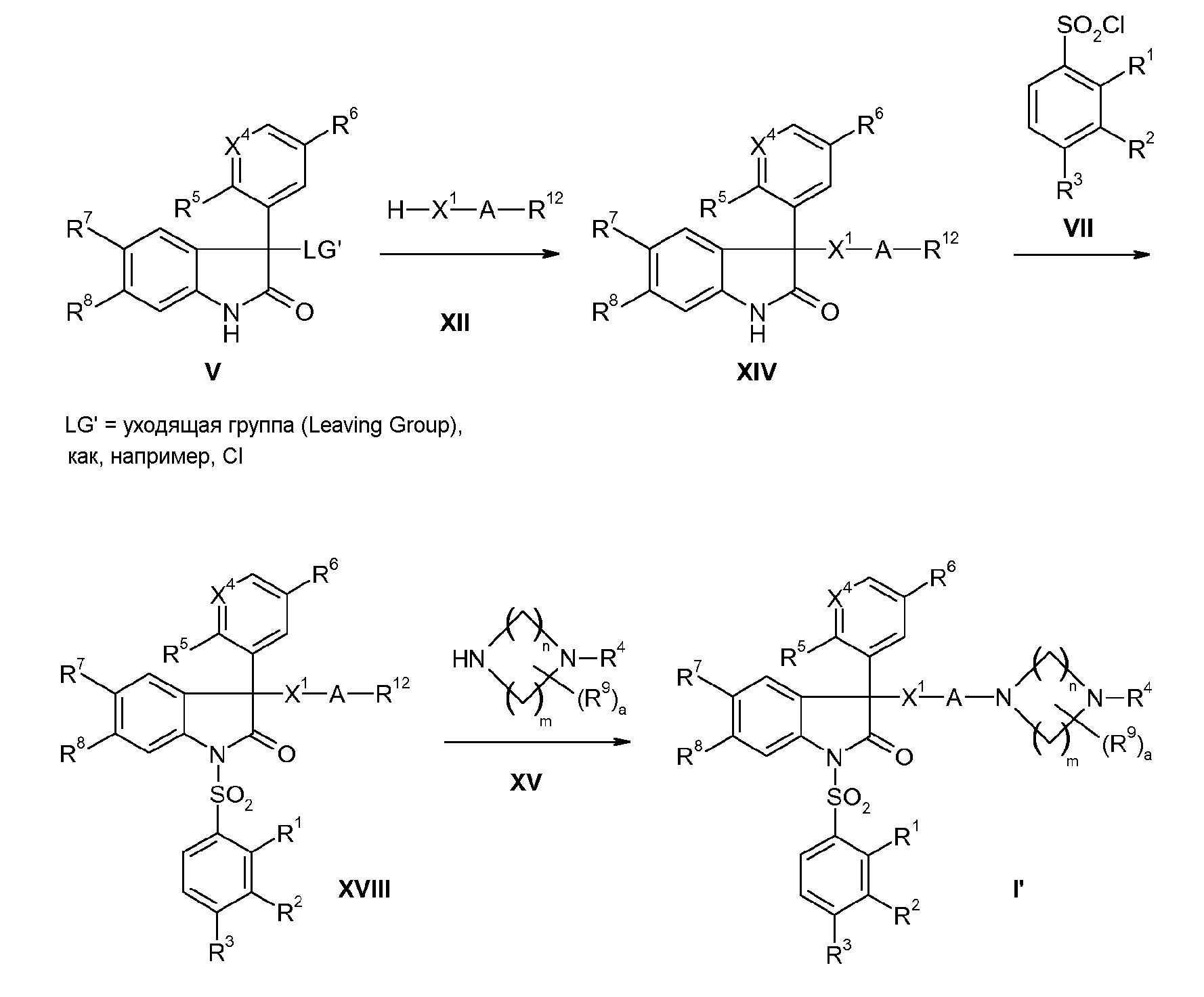
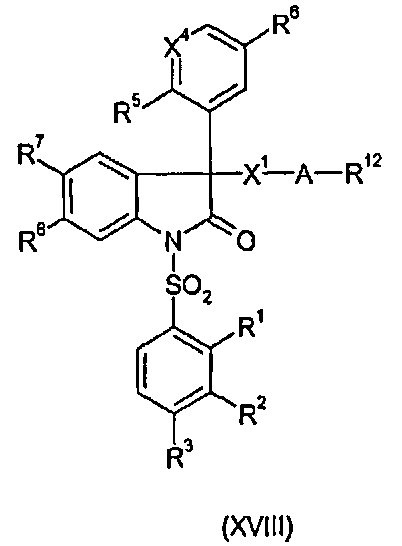
Следующий объект настоящего изобретения относится к соединениям формулы XVIII, которые используются как промежуточный продукт в синтезе соединений I по изобретению:
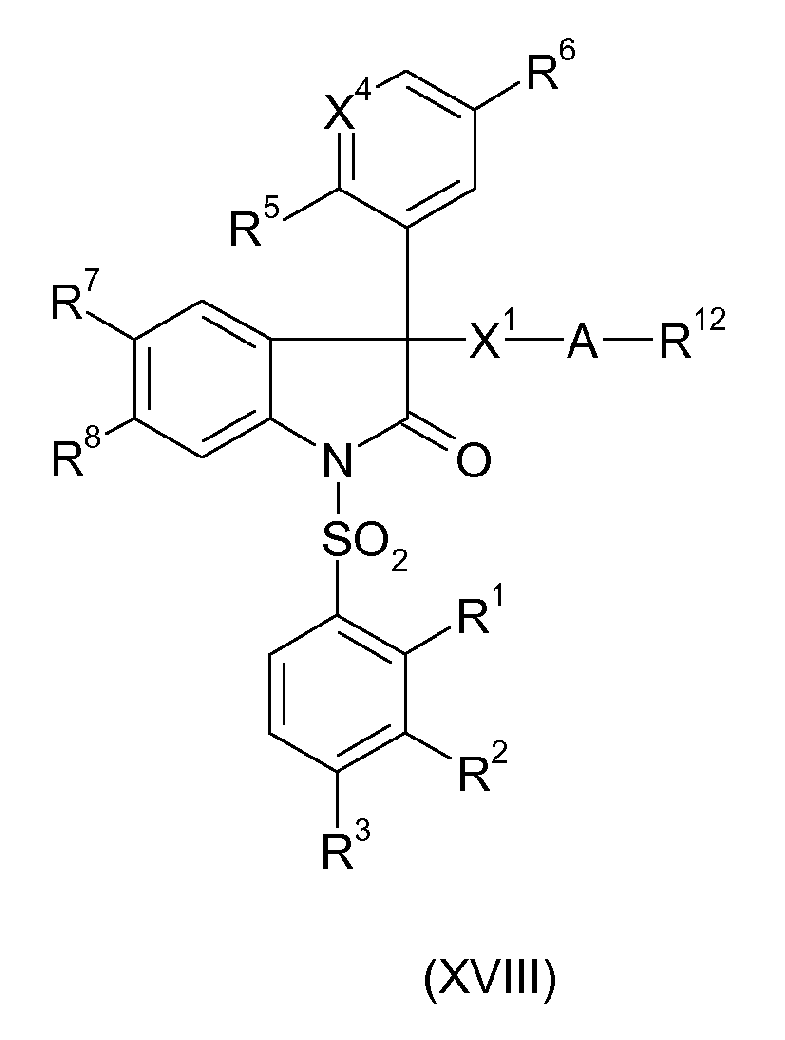
где R1, R2, R3, R5, R6, R7, R8, X1, X4 и A такие, как определено выше для соединения I; и
R12 означает галоген, CN, ORa или NRbRc, где
Ra означает H, C1-C4-алкил, фенил или бензил; и
Rb и Rc независимо друг от друга означают H, C1-C4-алкил, C1-C4-алкокси, фенил или бензил.
Что касается предпочтительных форм осуществления переменных R1, R2, R3, R5, R6, R7, R8, X1, X4 и A, смотри сказанное выше относительно соответствующих переменных в соединениях I.
В определения R12 галоген предпочтительно означает йод, бром или хлор, в частности, бром.
R12 предпочтительно означает галоген или CN, более предпочтительно галоген. Особенно предпочтительно R12 означает йод, бром или хлор, в частности, бром.
Следующий объект настоящего изобретения относится к фармацевтическому средству, содержащему по меньшей мере одно соединение общей формулы I и/или его фармацевтически приемлемую соль или пролекарство, какие описаны выше, и фармацевтически приемлемый носитель. Подходящие носители зависят, кроме прочего, от форм приема средства, и специалисту в принципе известны. Некоторые подходящие носители будут описаны подробнее ниже.
Следующий объект настоящего изобретения относится к применению соединений формулы I и/или их фармацевтически приемлемых солей или пролекарств для получения лекарственного средства для лечения и/или профилактики заболеваний, зависимых от вазопрессина.
Зависимыми от вазопрессина заболеваниями являются такие, при которых протекание болезни по меньшей мере частично зависит от вазопрессина, т.е. заболеваний, которые обнаруживают повышенный уровень вазопрессина, который может вносить свой вклад, непосредственно или косвенно, в картину заболевания. Другими словами, зависимыми от вазопрессина заболеваниями являются такие, на которые можно повлиять модуляцией рецепторов вазопрессина, например, введением лиганда рецептора вазопрессина (агониста, антагониста, частичного антагониста/агониста, обратного агониста и т.д.).
В одной предпочтительной форме осуществления настоящее изобретение относится к применению соединений формулы I согласно изобретению или их фармацевтически приемлемых солей или пролекарств для получения лекарственного средства для лечения и/или профилактики заболеваний, выбранных из диабета, резистентности к инсулину, ночного энуреза, недержания мочи и заболеваний, при которых встречаются нарушения свертываемости крови, и/или для задержания мочеиспускания. Под термином "диабет" следует понимать все формы диабета, прежде всего сахарный диабет (в том числе тип I и особенно тип II), почечный диабет, в частности, несахарный диабет. Предпочтительно под формами диабета имеются в виду сахарный диабет типа II (с резистентностью к инсулину) или несахарный диабет.
В следующей предпочтительной форме осуществления настоящее изобретение относится к применению соединений по изобретению формулы I или их фармацевтически приемлемых солей или пролекарств для получения лекарственного средства для лечения и/или профилактики заболеваний, выбранных из гипертонии, легочной гипертонии, сердечной недостаточности, инфаркта миокарда, коронарных спазмов, нестабильной стенокардии, PTCA (percutaneous transluminal coronary angioplastie - чрескожная транслюминальная коронарная пластика), ишемии сердца, расстройств почечной системы, отеков, почечных вазоспазмов, некроза коркового вещества почки, гипонатринемии, гипокалимии, синдрома Шварца-Бартера, расстройств желудочно-кишечного тракта, желудочных вазоспазмов, цирроза печени, язвы желудка и кишечника, рвоты, рвоты при химиотерапии и укачивания в дороге.
Соединения формулы I согласно изобретению или их фармацевтически приемлемые соли или пролекарства или фармацевтические средства по изобретению могут также применяться для лечения различных расстройств, зависимых от вазопрессина, которые обусловлены центральной нервной системой или изменениями в HPA-системе (hypothalamic pituitary adrenal axis - гипоталамо-гипофизарно-надпочечниковая система), например, при аффективных расстройствах, как депрессивные расстройства и биполярные расстройства. Сюда относятся, например, дистимические расстройства, фобии, посттравматические стрессовые расстройства, генерализованные тревожные расстройства, панические расстройства, сезонные депрессии и нарушения сна.
Равным образом, соединения формулы I согласно изобретению, или их фармацевтически приемлемые соли или пролекарства, или фармацевтические средства согласно изобретению могут применяться для лечения при тревожных расстройствах и обусловленных стрессом тревожных расстройствах, таких как, например, генерализованные тревожные расстройства, фобии, посттравматические тревожные расстройства, панические тревожные расстройства, обцессивно-навязчивые тревожные расстройства, острые тревожные расстройства, обусловленные стрессом, и социофобия.
Кроме того, соединения согласно изобретению могут применяться также для лечения расстройств, препятствующих запоминанию, болезни Альцгеймера, психозов, психотических расстройств, нарушений сна и/или синдрома Кушинга, а также всех обусловленных стрессом заболеваний.
В соответствии с этим, следующий предпочтительный вариант осуществления настоящего изобретения относится к применению соединений формулы I согласно изобретению или их фармацевтически приемлемых солей или пролекарств для получения лекарственного средства для лечения аффективных расстройств.
В следующей предпочтительной форме осуществления настоящее изобретение относится к применению соединений формулы I согласно изобретению или их фармацевтически приемлемых солей или пролекарств для получения лекарственного средства для лечения тревожных расстройств и/или обусловленных стрессом тревожных расстройств.
В следующей предпочтительной форме осуществления настоящее изобретение относится к применению соединений формулы I согласно изобретению или их фармацевтически приемлемых солей или пролекарств для получения лекарственного средства для лечения расстройств, препятствующих запоминанию, и/или болезни Альцгеймера.
В следующей предпочтительной форме осуществления настоящее изобретение относится к применению соединений формулы I согласно изобретению или их фармацевтически приемлемых солей или пролекарств для получения лекарственного средства для лечения психозов и/или психотических расстройств.
В следующей предпочтительной форме осуществления настоящее изобретение относится к применению соединений формулы I согласно изобретению или их фармацевтически приемлемых солей или пролекарств для получения лекарственного средства для лечения синдрома Кушинга или прочих обусловленных стрессом заболеваний.
В следующей предпочтительной форме осуществления настоящее изобретение относится к применению соединений формулы I согласно изобретению или их фармацевтически приемлемых солей или пролекарств для получения лекарственного средства для лечения нарушений сна.
В следующей предпочтительной форме осуществления настоящее изобретение относится к применению соединений формулы I согласно изобретению или их фармацевтически приемлемые солей или пролекарств для получения лекарственного средства для лечения депрессивных заболеваний. Особой формой депрессивных заболеваний являются так называемые "childhood onset mood disorders", т.е. начинающиеся в детстве расстройства настроения.
В следующей предпочтительной форме осуществления настоящее изобретение относится к применению соединений формулы I согласно изобретению или их фармацевтически приемлемых солей или пролекарств для получения лекарственного средства для лечения вазомоторных симптомов и/или сбоя терморегуляции, как, например, симптом "hot flush" (приливы крови).
В следующей предпочтительной форме осуществления настоящее изобретение относится к применению соединений формулы I согласно изобретению или их фармацевтически приемлемых солей или пролекарств для получения лекарственного средства для лечения и/или профилактики зависимостей, вызванных наркотиками, лекарствами и/или прочими факторами, для лечения и/или профилактики стресса, обусловленного лишением одного или нескольких вызывающих зависимость факторов, и/или для лечения и/или профилактики вызванных стрессом рецидивов зависимостей от наркотиков, лекарств и/или иными факторов.
В следующей предпочтительной форме осуществления настоящее изобретение относится к применению соединений формулы I согласно изобретению или их фармацевтически приемлемых солей или пролекарств для получения лекарственного средства для лечения и/или профилактики шизофрении и/или психоза.
Следующий объект изобретения относится к способу лечения и/или профилактики заболеваний, зависимых от вазопрессина, при которых пациенту вводят эффективное количество по меньшей мере одного соединения формулы I согласно изобретению, или по меньшей мере одной его фармацевтически приемлемой соли или пролекарства, или фармацевтического средства согласно изобретению.
Относительно определения заболеваний, зависимых от вазопрессина смотри изложенное выше.
В одной предпочтительной форме осуществления изобретения способ по изобретению служит для лечения и/или профилактики заболеваний, которые выбраны из диабета, резистентности к инсулину, ночного энуреза, недержания мочи и заболеваний, при которых встречаются нарушения свертывания крови, и/или для задержки мочеиспускания. Относительно определений диабета смотри изложенное выше.
В следующей предпочтительной форме осуществления способ согласно изобретению служит для лечения и/или профилактики заболеваний, выбранных из гипертонии, легочной гипертонии, сердечной недостаточности, инфаркта миокарда, коронарных спазмов, нестабильной стенокардии, PTCA (percutaneous transluminal coronary angioplastie - чрескожная транслюминальная коронарная пластика), ишемии сердца, расстройств почечной системы, отеков, почечных вазоспазмов, некроза коркового вещества почки, гипонатринемии, гипокалимии, синдрома Шварца-Бартера, расстройств желудочно-кишечного тракта, желудочных вазоспазмов, цирроза печения, язвы желудка и кишечника, рвоты, рвоты при химиотерапии и укачивания в дороге.
В следующей предпочтительной форме осуществления способ согласно изобретению служит для лечения и/или профилактики аффективных расстройств.
В следующей предпочтительной форме осуществления способ согласно изобретению служит для лечения и/или профилактики тревожных расстройств и/или обусловленных стрессом тревожных расстройств.
В следующей предпочтительной форме осуществления способ согласно изобретению служит для лечения и/или профилактики расстройств, препятствующих запоминанию, и/или болезни Альцгеймера.
В следующей предпочтительной форме осуществления способ согласно изобретению служит для лечения и/или профилактики психозов и/или психотических расстройств.
В следующей предпочтительной форме осуществления способ согласно изобретению служит для лечения и/или профилактики синдрома Кушинга.
В следующей предпочтительной форме осуществления способ согласно изобретению служит для лечения и/или профилактики нарушений сна у пациента.
В следующей предпочтительной форме осуществления способ согласно изобретению служит для лечения и/или профилактики депрессивных заболеваний. Под депрессивными заболеваниями следует особо упомянуть также начинающиеся в детстве расстройства настроения.
В следующей предпочтительной форме осуществления способ согласно изобретению служит для лечения и/или профилактики вазомоторных симптомов и/или сбоев терморегуляции, как, например, симптом "hot flush" (приливы крови).
В следующей предпочтительной форме осуществления способ согласно изобретению служит для лечения и/или профилактики зависимостей, вызванных наркотиками, лекарствами и/или прочими факторами, для лечения и/или профилактики стресса, обусловленного лишением одного или нескольких факторов, вызывающих зависимость, и/или для лечения и/или профилактики вызванных стрессом рецидивов зависимостей, вызванных наркотиками, лекарствами и/или иными факторами.
В следующей предпочтительной форме осуществления способ согласно изобретению служит для лечения и/или профилактики шизофрении и/или психозов.
Под пациентом, получающим профилактическое или терапевтическое лечение способом по изобретению, имеется в виду предпочтительно млекопитающее, например, человек или млекопитающее, отличное от человека, или не являющееся человеком трансгенное млекопитающее. В частности, речь идет о человеке.
Соединения общей формулы I, их фармацевтически приемлемые соли и пролекарства, такие как указаны выше, могут быть получены специалистом, зная технические идеи изобретения, осуществляя известные сами по себе технологические этапы или действуя аналогично этим технологическим этапам.
Соединения I или их пролекарства, и/или их фармацевтически приемлемые соли отличаются тем, что они обладают более высокой селективностью к рецептору вазопрессина подтипа V1b в сравнении с по меньшей мере одним из близкородственных подтипов рецепторов вазопрессина/окситоцина (например, вазопрессина V1a, вазопрессина V2 и/или окситоцина).
Альтернативно или предпочтительно, соединения I, или их пролекарства, и/или их фармацевтически приемлемые соли отличаются, кроме того, тем, что они имеют улучшенную метаболическую стабильность.
Метаболическую стабильность соединения можно измерить, например, тем, что раствор этого соединения инкубируют с печеночными микросомами определенных видов (например, крысы, собаки или человека) и в этих условиях определяют время полуразложения соединения (RS Obach, Curr. Opin. Drug. Discov. Devel. 2001, 4, 36-44). При этом из наблюдаемых более высоких значений времени полуразложения можно сделать вывод об улучшенной метаболической стабильности соединения. Особый интерес представляет стабильность в присутствии человеческих печеночных микросом, так как она позволяет предсказать метаболическое разложение соединения в печени человека. Поэтому вероятно, что соединения с повышенной метаболической стабильностью (измеренной в тесте на печеночных микросомах) будут медленнее разлагаться также и в печени. Более медленное метаболическое разложение в печени может привести к более высоким и/или дольше сохраняющимся концентрациям (уровень действия) соединения в теле, так что время выведения/полуразложения соединений согласно изобретению повышается. Повышенный и/или дольше сохраняющийся уровень активности может привести к улучшенной эффективности соединения при лечении или профилактики различных заболеваний, зависимых от вазопрессина. Кроме того, улучшенная метаболическая стабильность может привести к более высокой биодоступности после перорального приема, так как соединение после последовавшего всасывания в кишечнике подвергается меньшему метаболическому разложению в печени (так называемый "first pass effect - эффект первого попадания"). Повышенная пероральная биодоступность может, вследствие повышенной концентрации (уровень активности) соединения, привести к лучшей эффективности соединения после перорального приема.
Альтернативно или предпочтительно, соединения I или их пролекарства, и/или их фармацевтически приемлемые соли отличаются, кроме того, тем, что они у пациентов или релевантных моделей на животных позволяют сделать прогноз относительно их применимости в лечении, что они по сравнению с известными из уровня техники соединениями оксиндола имеют улучшенную фармакологическую активность.
Соединения по изобретению эффективны при введении различными путями. Введение может проводиться, например, внутривенно, внутримышечно, подкожно, топически, интратрахеально, интраназально, трансдермально, вагинально, ректально, сублингвально, буккально или перорально, и часто осуществляется внутривенно, внутримышечно или, в частности, перорально.
Настоящее изобретение относится также к фармацевтическим композициям, которые содержат эффективную дозу соединения I согласно изобретению, его фармацевтически приемлемой соли или его пролекарства и подходящий фармацевтический носитель (наполнитель для лекарственного средства).
Эти наполнители для лекарственного средства выбираются в соответствии с фармацевтической формой и желаемым типом введения и известны специалистам.
Соединения формулы I согласно изобретению или, в известных случаях, подходящие соли этих соединений могут применяться для получения фармацевтических композиций для орального, сублингвального, буккального, подкожного, внутримышечного, внутривенного, топического, интратрахеального, интраназального, трансдермального, вагинального или ректального введения животному или человеку в единичных формах введения, смешанными с обычными фармацевтическими носителями, для профилактики или лечения вышеописанных расстройств или болезней.
Подходящие формы введения (готовые формы) включают в себя формы для перорального введения, такие как таблетки, желатиновые капсулы, порошки, крупинки и растворы или суспензии для перорального приема, формы для сублингвального, буккального, интратрахеального или интраназального введения, аэрозоли, имплантаты, формы для подкожного, внутримышечного или внутривенного введения и формы для ректального введения.
Для топического введения соединения согласно изобретению могут применяться в кремах, мазях или лосьонах.
Чтобы достичь желаемого профилактического или терапевтического эффекта, доза активного вещества может варьироваться от 0,01 до 50 мг на кг веса тела в сутки.
Каждая разовая доза может содержать от 0,05 до 5000 мг, предпочтительно от 1 до 1000 мг активного вещества в комбинации с фармацевтическим носителем. Эта разовая доза может приниматься 1-5 раз в день, так что вводится суточная доза от 0,5 до 25000 мг, предпочтительно от 1 до 5000 мг.
Если готовится твердая композиция в виде таблеток, то активное вещество смешивают с твердым фармацевтическим носителем, таким как желатин, крахмал, лактоза, стеарат магния, тальк, диоксид кремния или подобное.
Таблетки могут быть покрыты сахарозой, производным целлюлозы или другим подходящим веществом или обработаны по иному, чтобы они имели длительную или замедленную активность и непрерывно высвобождали заданное количество активного вещества.
Препарат в форме желатиновых капсул получают смешением активного вещества с наполнителем и введением полученной смеси в мягкую или жесткую желатиновую капсулу.
Препарат в форме сиропа или эликсира или для приема в виде капель может содержать активные вещества вместе с подсластителем, который предпочтительно не содержит калорий, метилпарабеном или пропилпарабеном в качестве антисептика, ароматизатором и подходящим красителем.
Диспергируемые в воде порошки или крупинки могут содержать активные вещества, смешанные с диспергаторами, смачивателями или суспендирующими агентами, такими как поливинилпирролидон, а также с подсластителями или улучшителями вкуса.
Ректальное или вагинальное введение достигается применением свечей, которые готовятся вместе со связующим, которое плавится при ректальной температуре, например, масло какао или полиэтиленгликоли. Парентеральное введение осуществляется с применением водных суспензий, изотонических солевых растворов или стерильных растворов для инъекций, которые содержат фармакологически приемлемые диспергаторы и/или смачиватели, например, пропиленгликоль или полиэтиленгликоль.
Активное вещество может быть приготовлено также в виде микрокапсул или центросом, если подходит, с одним или несколькими носителями или добавками.
Помимо соединений согласно изобретению, средства по изобретению могут также содержать другие активные вещества, которые могут быть полезны для лечения вышеуказанных расстройств или заболеваний.
Таким образом, настоящее изобретение относится, кроме того, к фармацевтическим средствам, в которых одновременно присутствует несколько активных веществ, причем по меньшей мере одно из них является соединением I по изобретению, его солью или пролекарством.
Далее изобретение подробнее поясняется на примерах, причем примеры не следует понимать как ограничительные.
Получение соединений согласно изобретению можно осуществить различными способами синтеза. В следующих далее примерах синтеза получение указанных соединений проводилось аналогично способам, изображенным на реакционных схемах 1-5. Однако схемы синтеза 1-5 являются всего лишь примерными и не должны пониматься как ограничительные; синтез может осуществляться также и другими путями.
Экспериментальная часть
Используемые сокращения:
DIPEA: диизопропилэтиламин
DMSO: диметилсульфоксид
ТГФ: тетрагидрофуран
TFA: трифторуксусная кислота
p: псевдо (например, pt - псевдо триплет)
b: широкий (например, bs - широкий синглет)
s: синглет
d: дублет
t: триплет
m: мультиплет
dd: двойной дублет
dt: двойной триплет
tt: тройной триплет
I. Получение соединений I
Соединения формулы I синтезированы по аналогии со способами получения, описанными в схемах синтеза 1-5. Соединения можно очистить путем кристаллизации и/или с помощью препаративной ВЭЖХ (время удержания, элюенты ацетонитрил/вода, 0,1% TFA или 0,1% уксусной кислоты). В таком случае соединения I образуются при необходимости в виде соли трифторуксусной кислоты, соли бис(трифторуксусной) кислоты) или соли уксусной кислоты.
I.1 Получение соединений I, где X1 означает -O-C(=O)-
Пример 1:
1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-5-йод-2-оксо-2,3-дигидро-1H-индол-3-иловый сложный эфир 4-(4-метилпиперазин-1-ил)-бензойной кислоты
1.1 3-(2-этоксипиридин-3-ил)-5-йод-2-оксо-2,3-дигидро-1H-индол-3-иловый сложный эфир 4-(4-метилпиперазин-1-ил)-бензойной кислоты
МС-ESI: 599,10 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 10,40 (с, 1H); 8,30 (д, 1H); 8,20 (д, 1H); 7,90 (д, 2H); 7,60 (д, 1H); 7,35 (с, 1H); 7,20 (м, 1H); 7,05 (д, 2H); 6,75 (д, 1H); 4,15 (м, 2H); 3,35 (ушир.с, 4H); 2,45 (ушир.с, 4H); 2,20 (с, 3H); 1,05 (т, 3H).
1.2 1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-5-йод-2-оксо-2,3-дигидро-1H-индол-3-иловый сложный эфир 4-(4-метилпиперазин-1-ил)-бензойной кислоты
МС-ESI: 799,20 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,35 (д, 1H); 8,20 (д, 1H); 7,90 (д, 1H); 7,80 (д, 1H); 7,75 (д, 2H); 7,65 (д, 1H); 7,45 (с, 1H); 7,20 (м, 1H); 7,00 (д, 2H); 6,75 (с, 1H); 6,70 (д, 1H); 4,15 (м, 2H); 3,90 (с, 3H); 3,65 (с, 3H); 3,35 (ушир.с, 4H); 2,45 (ушир.с, 4H); 2,20 (с, 3H); 1,05 (т, 3H).
Пример 2:
5-циано-3-(2-этоксипиридин-3-ил)-1-(4-метоксифенилсульфонил)-2-оксо-2,3-дигидро-1H-индол-3-иловый сложный эфир 4-(4-метилпиперазин-1-ил)-бензойной кислоты
2.1 5-циано-3-(2-этоксипиридин-3-ил)-2-оксо-2,3-дигидро-1H-индол-3-иловый сложный эфир 4-(4-метилпиперазин-1-ил)-бензойной кислоты
МС-ESI: 498,20 [M+H]+
2.2 5-циано-3-(2-этоксипиридин-3-ил)-1-(4-метоксифенил-сульфонил)-2-оксо-2,3-дигидро-1H-индол-3-иловый сложный эфир 4-(4-метилпиперазин-1-ил)-бензойной кислоты
МС-ESI: 668,20 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,45 (д, 1H); 8,20 (м, 1H); 8,05 (м, 3H); 7,95 (д, 1H); 7,75 (м, 1H); 7,70 (д, 2H); 7,25 (м, 3H); 6,95 (д, 2H); 4,10 (м, 1H); 4,00 (м, 1H); 3,90 (с, 3H); 3,35 (ушир.с, 4H); 2,45 (ушир.с, 4H); 2,20 (с, 3H); 0,95 (т, 3H).
Пример 3: 5-циано-1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-2-оксо-2,3-дигидро-1H-индол-3-иловый сложный эфир 4-(4-метилпиперазин-1-ил)-бензойной кислоты
МС-ESI: 698,25 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,40 (д, 1H); 8,20 (м, 1H); 8,00 (д, 1H); 7,95 (д, 1H); 7,85 (д, 1H); 7,70 (м, 3H); 7,20 (м, 1H); 6,95 (д, 2H); 6,75 (д, 1H); 6,65 (дд, 1H); 4,10 (м, 2H); 3,85 (с, 3H); 3,55 (с, 3H); 3,30 (ушир.с, 4H); 2,40 (ушир.с, 4H); 2,15 (с, 3H); 1,00 (т, 3H).
I.2 Получение соединений I, где X1 означает -NH-C(=O)-
Пример 4:
N-[5-циано-3-(2-этоксипиридин-3-ил)-1-(4-метоксифенилсульфонил)-2-оксо-2,3-дигидро-1H-индол-3-ил]-4-(4-метилпиперазин-1-ил)-бензамид
4.1 3-амино-3-(2-этоксипиридин-3-ил)-1-(4-метоксифенилсульфонил)-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 465,10 [M+H]+
4.2 N-[5-циано-3-(2-этоксипиридин-3-ил)-1-(4-метоксифенилсульфонил)-2-оксо-2,3-дигидро-1H-индол-3-ил]-бензамид
МС-ESI: 569,15 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 9,65 (с, 1H); 8,20 (м, 1H); 8,05 (д, 2H); 8,00 (м, 2H); 7,90 (д, 1H); 7,80 (м, 3H); 7,55 (м, 1H); 7,45 (м, 2H); 7,20 (д, 1H); 7,10 (м, 1H); 4,20 (м, 1H); 4,15 (м, 1H); 3,90 (с, 3H); 1,05 (т, 3H).
4.3 4-бром-N-[5-циано-3-(2-этоксипиридин-3-ил)-1-(4-метоксифенилсульфонил)-2-оксо-2,3-дигидро-1H-индол-3-ил]-бензамид
МС-ESI: 647,05/649,05 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 9,75 (с, 1H); 8,20 (м, 1H); 8,05 (д, 2H); 8,00 (м, 2H); 7,85 (д, 1H); 7,75 (с, 1H); 7,70 (м, 4H); 7,20 (д, 1H); 7,10 (м, 1H); 4,20 (м, 1H); 4,15 (м, 1H); 3,90 (с, 3H); 1,05 (т, 3H).
4.4 N-[5-циано-3-(2-этоксипиридин-3-ил)-1-(4-метоксифенилсульфонил)-2-оксо-2,3-дигидро-1H-индол-3-ил]-4-(4-метилпиперазин-1-ил)-бензамид
МС-ESI: 667,25 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 9,30 (с, 1H); 8,20 (м, 1H); 8,05 (м, 2H); 7,95 (м, 2H); 7,85 (д, 1H); 7,75 (с, 1H); 7,65 (д, 1H); 7,20 (д, 2H); 7,10 (м, 1H); 6,95 (д, 2H); 4,15 (м, 1H); 4,10 (м, 1H); 3,90 (с, 3H); 3,25 (м, 4H); 2,45 (м, 4H); 2,25 (с, 3H); 1,05 (т, 3H).
Пример 5:
N-[5-циано-3-(2-этоксипиридин-3-ил)-1-(4-метоксифенилсульфонил)-2-оксо-2,3-дигидро-1H-индол-3-ил]-4-(4-этилпиперазин-1-ил)-бензамид
МС-ESI: 681,30 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 9,30 (с, 1H); 8,20 (м, 1H); 8,05 (д, 2H); 7,95 (м, 2H); 7,85 (д, 1H); 7,75 (с, 1H); 7,65 (д, 1H); 7,20 (д, 2H); 7,10 (м, 1H); 6,95 (д, 2H); 4,15 (м, 1H); 4,10 (м, 1H); 3,90 (с, 3H); 3,30 (ушир.с, 4H); 2,50 (ушир.с, 4H); 2,40 (ушир.с, 2H); 1,05 (м,6H).
Пример 6:
N-[5-циано-1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-2-оксо-2,3-дигидро-1H-индол-3-ил]-4-(4-метилпиперазин-1-ил)-бензамид
6.1 3-амино-1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 495,10 [M+H]+
6.2 N-[5-циано-1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-2-оксо-2,3-дигидро-1H-индол-3-ил]-4-(4-метилпиперазин-1-ил)-бензамид
МС-ESI: 697,30 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 9,35 (с, 1H); 8,25 (м, 1H); 8,05 (м, 2H); 7,95 (д, 1H); 7,90 (с, 1H); 7,75 (м, 3H); 7,15 (м, 1H); 7,00 (д, 2H); 6,80 (м, 2H); 4,35 (м, 2H); 3,95 (с, 3H); 3,60 (с, 3H); 3,35 (м, 4H); 2,50 (ушир.с, 4H); 2,30 (с, 3H); 1,20 (т, 3H).
Пример 7:
N-[5-циано-1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-2-оксо-2,3-дигидро-1H-индол-3-ил]-4-(4-этилпиперазин-1-ил)-бензамид
МС-ESI: 711,25 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 9,30 (с, 1H); 8,20 (м, 1H); 7,95 (м, 2H); 7,85 (д,1H); 7,80 (с, 1H); 7,70 (м, 3H); 7,05 (м, 1H); 6,95 (д, 2H); 6,75 (м, 2H); 4,25 (м, 2H); 3,90 (с, 3H); 3,50 (с, 3H); 3,30 (ушир.с, 4H); 2,50 (ушир.с, 4H); 2,35 (м, 2H); 1,15 (т, 3H); 1,05 (т, 3H).
Пример 8:
N-[1-[4-(2,2-дифторэтокси)-фенилсульфонил]-3-(2-этоксипиридин-3-ил)-5-йод-2-оксо-2,3-дигидро-1H-индол-3-ил]-4-(4-метилпиперазин-1-ил)-бензамид
МС-ESI: 818,20 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 9,25 (с, 1H); 8,20 (м, 1H); 8,05 (д, 2H); 7,75 (д, 1H); 7,70 (м, 2H); 7,65 (д, 2H); 7,60 (д, 1H); 7,30 (д, 2H); 7,05 (м, 1H); 6,95 (д, 2H); 6,45 (т, J=70 Гц, 1H); 4,50 (м, 2H); 4,20 (м, 2H); 3,30 (м, 4H); 2,50 (м, 4H); 2,25 (м, 3H); 1,15 (т, 3H).
I.3 Получение соединений I, где X1 означает -NH-CH2-I.3.1 Соединения I, где X1 означает -NH-CH2-, и A означает 1,4-фенилен
Пример 9:
1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-5-йод-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-1,3-дигидроиндол-2-он
9.1 3-(2-этоксипиридин-3-ил)-5-йод-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-1,3-дигидроиндол-2-он
МС-ESI: 584,10 [M+H]+
9.2 1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-5-йод-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-1,3-дигидроиндол-2-он
МС-ESI: 784,20 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,20 (м, 1H); 8,15 (д, 1H); 8,10 (м, 1H); 7,80 (д, 1H); 7,70 (д, 1H); 7,25 (с, 1H); 6,90 (м, 3H); 6,80 (д, 2H); 6,65 (д, 1H); 6,35 (с, 1H); 4,25 (м, 1H); 4,20 (м, 1H); 3,85 (с, 3H); 3,55 (с, 3H); 3,20 (с, 4H); 3,05 (м, 1H); 2,90 (м, 1H); 2,55 (с, 4H); 2,35 (с, 3H); 2,05 (м, 1H); 1,20 (т, 3H).
Пример 10:
1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-5-йод-3-(4-пиперазин-1-ил-бензиламино)-1,3-дигидроиндол-2-он как соль уксусной кислоты
МС-ESI: 770,15 [M+H]+
Пример 11:
5-хлор-3-(2-этоксипиридин-3-ил)-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-1,3-дигидроиндол-2-он
11,1 5-хлор-3-(2-этоксипиридин-3-ил)-3-[4-(4-метилпиперазин-1 -ил)-бензиламино]-1,3-дигидроиндол-2-он
МС-ESI: 492,25 [M+H]+
11.2 5-хлор-3-(2-этоксипиридин-3-ил)-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-1,3-дигидроиндол-2-он
МС-ESI: 662,25 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,15 (м, 1H); 8,10 (д, 2H); 8,05 (м, 1H); 7,95 (д, 1H); 7,35 (д, 1H); 7,00 (д, 2H); 6,90 (м, 4H); 6,80 (д, 2H); 4,10 (м, 1H); 4,05 (м, 1H); 3,85 (с, 3H); 3,15 (м, 4H); 2,95 (м, 1H); 2,70 (м, 1H); 2,55 (м, 4H); 2,35 (с, 3H); 2,05 (м, 1H); 1,05 (т, 3H).
Пример 12:
5-хлор-3-(2-этоксипиридин-3-ил)-6-фтор-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-1,3-дигидроиндол-2-он
12.1 5-хлор-3-(2-этоксипиридин-3-ил)-6-фтор-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-1,3-дигидроиндол-2-он
МС-ESI: 510,20 [M+H]+
12.2 5-хлор-3-(2-этоксипиридин-3-ил)-6-фтор-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-1,3-дигидроиндол-2-он
МС-ESI: 680,20 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,15 (м, 1H); 8,10 (д, 2H); 8,05 (м, 1H); 7,90 (д, 1H); 7,00 (д, 2H); 6,90 (м, 4H); 6,80 (д, 2H); 4,10 (м, 2H); 3,85 (с, 3H); 3,15 (м, 4H); 2,90 (м, 1H); 2,70 (м, 1H); 2,55 (м, 4H); 2,35 (с, 3H); 2,10 (м, 1H); 1,10 (т, 3H).
Пример 13:
6-хлор-3-(2-этоксипиридин-3-ил)-5-фтор-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-1,3-дигидроиндол-2-он
13.1 6-хлор-3-(2-этоксипиридин-3-ил)-5-фтор-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-1,3-дигидроиндол-2-он
МС-ESI: 510,25 [M+H]+
13.2 6-хлор-3-(2-этоксипиридин-3-ил)-5-фтор-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-1,3-дигидроиндол-2-он
МС-ESI: 680,20 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,20-8,05 (м, 5H); 7,00 (д, 2H); 6,90 (м, 3H); 6,80 (д, 2H); 6,75 (д, 1H); 4,10 (м, 2H); 3,85 (с, 3H); 3,20 (м, 4H); 2,90 (м, 1H); 2,70 (м, 1H); 2,60 (м, 4H); 2,35 (с, 3H); 2,10 (м, 1H); 1,10 (т, 3H).
Пример 14:
5,6-дифтор-3-(2-этоксипиридин-3-ил)-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-1,3-дигидроиндол-2-он
МС-ESI: 664,25 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,15 (д, 1H); 8,10 (д, 2H); 8,05 (м, 1H); 7,95 (м, 1H); 7,00 (д, 2H); 6,90 (м, 3H); 6,80 (м, 3H); 4,15 (м, 1H); 4,10 (м, 1H); 3,85 (с, 3H); 3,15 (м, 4H); 2,90 (м, 1H); 2,70 (м, 1H); 2,60 (м, 4H); 2,35 (с, 3H); 2,10 (м, 1H); 1,10 (т, 3H).
Пример 15:
3-(2-этоксипиридин-3-ил)-5-фтор-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-1,3-дигидроиндол-2-он
МС-ESI: 646,25 [M+H]+
Пример 16:
3-(2-этоксипиридин-3-ил)-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
16.1 3-(2-этоксипиридин-3-ил)-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 483,25 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,25 (д, 1H); 8,10 (м, 1H); 7,65 (д, 1H); 7,15 (м, 3H); 7,10 (м, 1H); 7,05 (д, 1H); 6,90 (д, 2H); 4,05 (м, 3H); 3,50-3,15 (м, 6H); 3,00 (ушир.с, 4H); 2,60 (с, 3); 0,95 (т, 3H).
16.2 3-(2-этоксипиридин-3-ил)-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 653,20 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,30 (д, 1H); 8,20 (м, 3H); 8,15 (д, 1H); 7,95 (д, 1H); 7,40 (с, 1H); 7,30 (д, 2H); 7,20 (м, 1H); 6,95 (д, 2H); 6,85 (д, 2H); 4,05 (м, 1H); 3,90 (м, 4H); 3,80 (м, 1H); 3,15 (м, 4H); 3,00 (м, 1H); 2,95 (м, 1H); 2,50 (м, 4H); 2,30 (с, 3H); 0,90 (т, 3H).
Пример 17:
1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 683,25 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,20 (д, 1H); 8,05 (м, 3H); 7,70 (д, 1H); 7,20 (с, 1H); 6,95 (м, 1H); 6,80 (д, 2H); 6,75 (д, 2H); 6,65 (д, 1H); 6,50 (с, 1H); 4,05 (м, 2H); 3,80 (с, 3H); 3,50 (с, 3H); 3,05 (м, 4H); 2,90 (м, 1H); 2,80 (м, 1H); 2,50 (м, 4H); 2,25 (ушир.с, 3H); 1,05 (т, 3H).
Пример 18:
3-(2-этоксипиридин-3-ил)-1-(4-метокси-2-трифторметоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 737,25 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,35 (д, 1H); 8,15 (м, 2H); 8,10 (м, 1H); 7,70 (д, 1H); 7,25 (м, 1H); 7,00-6,90 (м, 4H); 6,85 (м, 3H); 4,25 (м, 2H); 3,90 (с, 3H); 3,20 (м, 4H); 3,05 (м, 1H); 2,95 (м, 1H); 2,55 (м, 4H); 2,35 (с, 3H); 2,10 (м, 1H); 1,10 (т, 3H).
Пример 19:
3-(2-этоксипиридин-3-ил)-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-1-(4-трифторметоксифенилсульфонил)-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 707,20 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,30 (д, 2H); 8,20 (м, 1H); 8,10 (м, 2H); 7,70 (д, 1H); 7,40 (д, 2H); 7,25 (с, 1H); 6,95 (м, 1H); 6,90 (д, 2H); 6,80 (д, 2H); 4,15 (м, 2H); 4,00 (м, 1H); 3,20 (м, 4H); 2,95 (м, 1H); 2,85 (м, 1H); 2,55 (м, 4H); 2,35 (с, 3H); 2,15 (м, 1H); 0,95 (т, 3H).
Пример 20:
3-(2-этоксипиридин-3-ил)-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-1-[4-(2,2,2-трифторэтокси)-фенилсульфонил]-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 721,20 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,20 (м, 3H); 8,15 (д, 1H); 8,10 (м, 1H); 7,65 (д, 1H); 7,25 (с, 1H); 7,10 (д, 2H); 6,95 (м, 1H); 6,85 (д, 2H); 6,80 (д, 2H); 4,35 (м, 2H); 4,15 (м, 1H); 4,05 (м, 1H); 3,15 (м, 4H); 2,90 (м, 1H); 2,70 (м, 1H); 2,55 (м, 4H); 2,35 (с, 3H); 2,10 (м, 1H); 1,05 (т, 3H).
Пример 21:
1-[4-(2,2-дифторэтокси)-фенилсульфонил]-3-(2-этоксипиридин-3-ил)-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 703,20 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,15 (м, 4H); 8,10 (д, 1H); 7,65 (д, 1H); 7,25 (с, 1H); 7,05 (д, 2H); 6,95 (м, 1H); 6,85 (д, 2H); 6,80 (д, 2H); 6,05 (т, J=70 Гц, 1H); 4,25-4,00 (м, 4H); 3,15 (м, 4H); 2,85 (м, 1H); 2,70 (м, 1H); 2,55 (м, 4H); 2,35 (с, 3H); 2,10 (м, 1H); 1,05 (т, 3H).
Пример 22:
3-(2-этоксипиридин-3-ил)-1-[4-(2-фтор-этокси)-фенилсульфонил]-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 685,20 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,20 (д, 1H); 8,15 (м, 3H); 8,10 (м, 1H); 7,65 (д, 1H); 7,20 (с, 1H); 7,05 (д, 2H); 6,95 (м, 1H); 6,85 (д, 2H); 6,80 (д, 2H); 4,80 (т, 1H); 4,70 (т, 1H); 4,25 (м, 1H); 4,20 (м, 1H); 4,15 (м, 1H); 4,05 (м, 1H); 3,15 (м, 4H); 2,90 (м, 1H); 2,75 (м, 1H); 2,55 (м, 4H); 2,35 (с, 3H); 2,10 (м, 1H); 1,05 (т, 3H).
Пример 23:
1-(4-дифторметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 689,20 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,20 (м, 3H); 8,10 (м, 2H); 7,70 (д, 1H); 7,30 (д, 2H); 7,25 (с, 1H); 6,95 (м, 1H); 6,85 (д, 2H); 6,80 (д, 2H); 6,55 (т, J=70 Гц, 1H); 4,15 (м, 1H); 4,05 (м, 1H); 3,20 (м, 4H); 2,95 (м, 1H); 2,75 (м, 1H); 2,55 (м, 4H); 2,35 (с, 3H); 2,15 (м, 1H); 1,00 (т, 3H).
Пример 24:
3-(2-этоксипиридин-3-ил)-1-(2-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 653,20 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,30 (д, 1H); 8,20 (м, 2H); 8,10 (м, 1H); 7,70 (д, 1H); 7,65 (т, 1H); 7,30 (с, 1H); 7,20 (д, 1H); 6,95 (м, 2H); 6,85 (д, 2H); 6,80 (д, 2H); 4,25 (м, 1H); 4,20 (м, 1H); 3,55 (с, 3H); 3,20 (м, 4H); 3,00 (м, 1H); 2,85 (м, 1H); 2,55 (м, 4H); 2,35 (с, 3H); 2,10 (м, 1H); 1,20 (т, 3H).
Пример 25:
3-(2-этоксипиридин-3-ил)-1-(3-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 653,20 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,20 (м, 1H); 8,15 (д, 1H); 8,10 (м, 1H); 7,75 (м, 2H); 7,65 (м, 1H); 7,45 (т, 1H); 7,20 (м, 2H); 6,95 (м, 1H); 6,90 (д, 2H); 6,80 (д, 2H); 4,15 (м, 1H); 4,05 (м, 1H); 3,85 (с, 3H); 3,20 (м, 4H); 2,90 (м, 1H); 2,85 (м, 1H); 2,55 (м, 4H); 2,35 (с, 3H); 2,15 (м, 1H); 1,05 (т, 3H).
Пример 26:
1-(4-хлорфенилсульфонил)-3-(2-этоксипиридин-3-ил)-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 657,20 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,20 (д, 1H); 8,15 (м, 4H); 7,70 (д, 1H); 7,55 (д, 2H); 7,25 (с, 1H); 6,95 (м, 1H); 6,85 (д, 2H); 6,80 (д, 2H); 4,10 (м, 1H); 4,05 (м, 1H); 3,20 (м, 4H); 2,95 (м, 1H); 2,75 (м, 1H); 2,55 (м, 4H); 2,35 (с, 3H); 2,10 (м, 1H); 1,05 (т, 3H).
Пример 27:
1-фенилсульфонил-3-(2-этоксипиридин-3-ил)-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 623,25 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,20 (м, 3H); 8,15 (д, 1H); 8,10 (м, 1H); 7,70 (м, 2H); 7,60 (м, 2H); 7,20 (с, 1H); 6,85 (д, 2H); 6,80 (д, 2H); 4,10 (м, 1H); 4,00 (м, 1H); 3,20 (м, 4H); 2,90 (м, 1H); 2,75 (м, 1H); 2,55 (м, 4H); 2,35 (с, 3H); 2,15 (м, 1H); 1,00 (т, 3H).
Пример 28:
1-(4-цианофенилсульфонил)-3-(2-этоксипиридин-3-ил)-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 648,25 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,35 (м, 2H); 8,25 (м, 3H); 8,15 (м, 1H); 8,05 (д, 1H); 7,90 (д, 1H); 7,35 (с, 1H); 7,15 (м, 1H); 6,90 (д, 2H); 6,80 (д, 2H); 3,95 (м, 1H); 3,80 (м, 2H); 3,10 (м, 4H); 3,00 (м, 1H); 2,95 (м, 1H); 2,45 (м, 4H); 2,20 (с, 3H); 0,80 (т, 3H).
Пример 29:
1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-2-оксо-3-(4-пиперазин-1-ил-бензиламино)-2,3-дигидро-1H-индол-5-карбонитрил как гидрохлорид
29.1 трет-бутиловый эфир 4-(4-{[5-циано-3-(2-этоксипиридин-3-ил)-2-оксо-2,3-дигидро-1H-индол-3-иламино]-метил}-фенил)-пиперазин-1-карбоновой кислоты
МС-ESI: 569,30 [M+H]+
29.2 трет-бутиловый эфир 4-(4-{[5-циано-1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-2-оксо-2,3-дигидро-1H-индол-3-иламино]-метил}-фенил)-пиперазин-1-карбоновой кислоты
29.3 трет-бутиловый эфир 4-(4-{[5-циано-3-(2-этоксипиридин-3-ил)-1-(4-метоксифенилсульфонил)-2-оксо-2,3-дигидро-1H-индол-3-иламино]-метил}-фенил)-пиперазин-1-карбоновой кислоты
МС-ESI: 639,20 [M-Boc+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,25 (д, 1H); 8,10 (м, 3H); 8,05 (д, 1H); 7,90 (д,1H); 7,30 (с, 1H); 7,25 (д, 2H); 7,10 (м, 1H); 6,90 (д, 2H); 6,80 (д, 2H); 3,95 (м, 1H); 3,85 (с, 3H); 3,80 (м, 1H); 3,75 (м, 1H); 3,45 (м, 4H); 3,05 (м, 4H); 2,95 (м, 1H); 2,90 (м, 1H); 1,40 (с, 9H); 0,80 (т, 3H).
29.4 1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-2-оксо-3-(4-пиперазин-1-илбензиламино)-2,3-дигидро-1H-индол-5-карбонитрил как гидрохлорид
МС-ESI: 669,25 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,25 (д, 1H); 8,10 (м, 1H); 8,05 (д, 2H); 7,95 (д, 1H); 7,45 (с, 1H); 7,10 (м, 1H); 6,95 (д, 2H); 6,85 (д, 2H); 6,80 (д, 1H); 6,75 (с, 1H); 4,05 (м, 2H); 3,85 (с, 3H); 3,65 (м, 1H); 3,55 (с, 3H); 3,20 (ушир.с, 4H); 3,05 (ушир.с, 4H); 2,95 (м, 2H); 0,95 (т, 3H).
Пример 30:
3-(2-этоксипиридин-3-ил)-1-(4-метоксифенилсульфонил)-2-оксо-3-(4-пиперазин-1-ил-бензиламино)-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 639,30 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,25 (д, 1H); 8,10 (м, 3H); 8,05 (д, 1H); 7,90 (д, 1H); 7,35 (с, 1H); 7,25 (д, 2H); 7,10 (м, 1H); 6,90 (д, 2H); 6,80 (д, 1H); 3,95 (м, 1H); 3,85 (с, 3H); 3,80 (м, 1H); 3,75 (м, 1H); 3,05 (ушир.с, 4H); 2,95 (м, 6H); 0,80 (т, 3H).
Пример 31:
3-(2-этоксипиридин-3-ил)-3-[4-(4-этилпиперазин-1-ил)-бензиламино]-1-(4-метоксифенилсульфонил)-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 667,20 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,25 (д, 1H); 8,10 (м, 3H); 8,05 (д, 1H); 7,90 (д, 1H); 7,35 (с, 1H); 7,25 (д, 2H); 7,10 (м, 1H); 6,90 (д, 2H); 6,80 (д, 1H); 3,95 (м, 1H); 3,85 (с, 3H); 3,80 (м, 1H); 3,70 (м, 1H); 3,10 (ушир.с, 4H); 2,95 (м, 1H); 2,85 (м, 1H); 2,50 (ушир.с, 4H); 2,40 (м, 2H); 1,05 (т, 3H); 0,80 (т, 3H).
Пример 32:
1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-3-[4-(4-этилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 697,20 [M+H]+
Пример 33:
3-(2-этоксипиридин-3-ил)-6-фтор-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
33.1 3-хлор-3-(2-этоксипиридин-3-ил)-6-фтор-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 332,00 [M+H]+
33.2 3-(2-этоксипиридин-3-ил)-6-фтор-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 501,25 [M+H]+
33.3 3-(2-этоксипиридин-3-ил)-6-фтор-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 671,25 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,20 (д, 1H); 8,15 (д, 2H); 8,10 (м, 1H); 7,95 (д, 1H); 7,10 (д, 1H); 7,05 (д, 2H); 6,95 (м, 1H); 6,85 (д, 2H); 6,80 (д, 2H); 4,15 (м, 1H); 4,10 (м, 1H); 3,85 (с, 3H); 3,20 (м, 4H); 2,90 (м, 1H); 2,80 (м, 1H); 2,65 (м, 4H); 2,35 (с, 3H); 2,15 (м, 1H); 1,05 (т, 3H).
Пример 34:
3-(2-этоксипиридин-3-ил)-6-фтор-1-(4-метоксифенилсульфонил)-2-оксо-3-(4-пиперазин-1-ил-бензиламино)-2,3-дигидро-1H-индол-5-карбонитрил
34.1 трет-бутиловый эфир 4-(4-{[5-циано-3-(2-этоксипиридин-3-ил)-6-фтор-2-оксо-2,3-дигидро-1H-индол-3-иламино]-метил}-фенил)-пиперазин-1-карбоновой кислоты
МС-ESI: 587,25 [M+H]+
34.2 трет-бутиловый эфир 4-(4-{[5-циано-3-(2-этоксипиридин-3-ил)-6-фтор-1-(4-метоксифенилсульфонил)-2-оксо-2,3-дигидро-1H-индол-3-иламино]-метил}-фенил)-пиперазин-1-карбоновой кислоты
МС-ESI: 757,25 [M+H]+
34.3 3-(2-этоксипиридин-3-ил)-6-фтор-1-(4-метоксифенилсульфонил)-2-оксо-3-(4-пиперазин-1-ил-бензиламино)-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 657,25 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,25 (д, 1H); 8,20 (д, 2H); 8,10 (м, 1H); 7,90 (д, 1H); 7,40 (д, 1H); 7,25 (д, 2H); 7,10 (м, 1H); 6,90 (д, 2H); 6,80 (д, 1H); 3,95 (м, 1H); 3,85 (с, 3H); 3,80 (м, 1H); 3,75 (м, 1H); 3,10 (м, 4H); 2,95 (м, 6H); 0,85 (т, 3H).
Пример 35:
3-(2-этоксипиридин-3-ил)-3-[4-(4-этилпиперазин-1-ил)-бензиламино]-6-фтор-1-(4-метоксифенилсульфонил)-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 685,20 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,25 (д, 1H); 8,20 (д, 2H); 8,15 (м, 1H); 7,40 (д,1H); 7,25 (д, 2H); 7,10 (м, 1H); 6,85 (д, 2H); 6,80 (д, 1H); 3,95 (м, 1H); 3,85 (м, 4H); 3,75 (м, 1H); 3,10 (м, 4H); 3,00 (м, 1H); 2,95 (м, 1H); 2,50 (ушир.с, 4H); 2,40 (м, 2H); 1,05 (т, 3H); 0,80 (т, 3H).
Пример 36:
1-[4-(2,2-дифторэтокси)-фенилсульфонил]-3-(2-этоксипиридин-3-ил)-6-фтор-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 721,25 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,25 (м, 3H); 8,10 (м, 2H); 7,90 (д, 1H); 7,40 (д, 1H); 7,35 (д, 2H); 7,15 (м, 1H); 6,85 (д, 2H); 6,75 (д, 2H); 6,40 (т, J=70 Гц, 1H); 4,45 (м, 2H); 3,95 (м, 1H); 3,85 (м, 1H); 3,80 (м, 1H); 3,05 (м, 4H); 3,00 (м, 1H); 2,95 (м, 1H); 2,45 (м, 4H); 2,25 (м, 3H); 0,85 (т, 3H).
Пример 37:
3-(2-этоксифенил)-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 652,20 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,15 (д, 2H); 8,10 (д, 1H); 8,00 (д, 1H); 7,95 (д, 1H); 7,40 (т, 1H); 7,30 (м, 3H); 7,15 (т, 1H); 6,95 (д, 1H); 6,90 (д, 2H); 6,80 (д, 2H); 4,05 (м, 1H); 3,90 (с, 3H); 3,80 (м, 1H); 3,70 (м, 1H); 3,15 (м, 4H); 2,95 (м, 1H); 2,85 (м, 1H); 2,50 (м, 4H); 2,30 (с, 3H); 0,95 (т, 3H).
I.3.2 Соединения I, где X1 означает -NH-CH2-, а A 1,3-фенилен
Пример 38:
1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-5-йод-3-[3-(4-метилпиперазин-1-ил)-бензиламино]-1,3-дигидроиндол-2-он
38.1 3-(2-этоксипиридин-3-ил)-5-йод-3-[3-(4-метилпиперазин-1-ил)-бензиламино]-1,3-дигидроиндол-2-он
МС-ESI: 584,15 [M+H]+
38.2 1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-5-йод-3-[3-(4-метилпиперазин-1-ил)-бензиламино]-1,3-дигидроиндол-2-он
МС-ESI: 784,15 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,20 (м, 2H); 8,10 (м, 1H); 7,80 (д, 1H); 7,70 (д, 1H); 7,30 (д, 1H); 7,15 (м, 1H); 6,90 (м, 1H); 6,80 (д, 1H); 6,65 (д, 1H); 6,60 (м, 2H); 6,40 (с, 1H); 4,25 (м, 2H); 3,85 (с, 3H); 3,55 (с, 3H); 3,20 (м, 4H); 3,10 (м, 1H); 2,90 (м, 1H); 2,60 (м, 4H); 2,40 (с, 3H); 2,15 (м, 1H); 1,20 (т, 3H).
Пример 39:
3-(2-этоксипиридин-3-ил)-5-йод-1-(4-метокси-2-трифторметоксифенилсульфонил)-3-[3-(4-метилпиперазин-1-ил)-бензиламино]-1,3-дигидроиндол-2-он
МС-ESI: 838,10 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,35 (д, 1H); 8,20 (д, 1H); 8,10 (м, 1H); 7,80 (д, 1H); 7,70 (д, 1H); 7,25 (с, 1H); 7,15 (м, 1H); 6,95 (м, 2H); 6,80 (м, 2H); 6,60 (д, 1H); 6,55 (д, 1H); 4,25 (м, 2H); 3,90 (с, 3H); 3,20 (м, 5H); 3,00 (м, 1H); 2,60 (м, 4H); 2,35 (с, 3H); 2,10 (м, 1H); 1,15 (т, 3H).
Пример 40:
3-(2-этоксипиридин-3-ил)-5-йод-1-(4-метоксифенилсульфонил)-3-[3-(4-метилпиперазин-1-ил)-бензиламино]-1,3-дигидроиндол-2-он
МС-ESI: 754,15 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,20 (д, 1H); 8,15 (м, 3H); 7,80 (д, 1H); 7,70 (д, 1H); 7,20 (с, 1H); 7,15 (м, 1H); 7,00 (д, 2H); 6,95 (м, 1H); 6,60 (д, 1H); 6,55 (м, 2H); 4,10 (м, 2H); 3,85 (с, 3H); 3,20 (м, 4H); 2,95 (м, 1H); 2,75 (м, 1H); 2,60 (м, 4H); 2,35 (с, 3H); 2,15 (м, 1H); 1,10 (т, 3H).
Пример 41:
3-(2-этоксипиридин-3-ил)-5-йод-1-(2-метоксифенилсульфонил)-3-[3-(4-метилпиперазин-1-ил)-бензиламино]-1,3-дигидроиндол-2-он
МС-ESI: 754,15 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,30 (д, 1H); 8,15 (д, 1H); 8,10 (м, 1H); 7,85 (д, 1H); 7,70 (д, 1H); 7,60 (м, 1H); 7,30 (д, 1H); 7,15 (м, 2H); 6,90 (м, 2H); 6,80 (д, 1H); 6,55 (с, 1H); 6,50 (д, 1H); 4,25 (м, 2H); 3,60 (с, 3H); 3,15 (м, 4H); 3,10 (м, 1H); 2,90 (м, 1H); 2,60 (м, 4H); 2,40 (с, 3H); 2,15 (м, 1H); 1,20 (т, 3H).
Пример 42:
1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-3-[3-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
42.1 3-(2-этоксипиридин-3-ил)-3-[3-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 483,20 [M+H]+
42.2 1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-3-[3-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 683,10[M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,35 (д, 1H); 8,20 (м, 1H); 8,10 (м, 2H); 8,00 (д, 1H); 7,50 (с, 1H); 7,15 (м, 2H); 6,90 (д, 1H); 6,85 (м, 2H); 6,65 (м, 2H); 4,15 (м, 2H); 3,95 (с, 3H); 3,80 (м, 1H); 3,65 (с, 3H); 3,15 (ушир.с, 4H); 3,10 (м, 1H); 3,00 (м, 1H); 2,50 (м, 4H); 2,30 (с, 3H); 1,05 (т, 3H).
Пример 43:
3-(2-этоксипиридин-3-ил)-1-(4-метоксифенилсульфонил)-3-[3-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 653,10 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,35 (д, 1H); 8,20 (м, 3H); 8,10 (д, 1H); 7,95 (д, 1H); 7,45 (с, 1H); 7,30 (д, 2H); 7,20 (м, 1H); 7,15 (т, 1H); 6,80 (д, 1H); 6,60 (м, 2H); 4,05 (м, 1H); 3,95 (м, 1H); 3,90 (м, 4H); 3,15 (м, 4H); 3,05 (м, 1H); 2,95 (м, 1H); 2,50 (м, 4H); 2,30 (с, 3H); 0,90 (т, 3H).
Пример 44:
3-(2-этоксипиридин-3-ил)-1-(2-метоксифенилсульфонил)-3-[3-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 653,10 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,35 (д, 1H); 8,20 (м, 2H); 8,10 (д, 1H); 8,00 (д, 1H); 7,85 (м, 1H); 7,55 (с, 1H); 7,35 (д, 1H); 7,30 (м, 1H); 7,15 (м, 2H); 6,80 (д, 1H); 6,65 (с, 1H); 6,60 (д, 1H); 4,15 (м, 2H); 3,85 (м, 1H); 3,70 (с, 3H); 3,15 (ушир.с, 4H); 3,10 (м, 1H); 3,00 (м, 1H); 2,50 (м, 4H); 2,25 (с, 3H); 1,05 (т, 3H).
I.3.3 Соединения I, где X1 означает -NH-CH2-, а A 1,2-фенилен
Пример 45:
1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-3-[2-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
45.1 3-(2-этоксипиридин-3-ил)-3-[2-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 483,20 [M+H]+
45.2 1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-3-[2-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 683,15 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,20 (д, 2H); 8,10 (д, 2H); 7,75 (д, 1H); 7,25 (т, 1H); 7,20 (с, 1H); 7,10 (д, 1H); 7,00 (т, 1H); 6,90 (т, 2H); 6,85 (д, 1H); 6,60 (д, 1H); 6,25 (д, 1H); 4,20 (м, 2H); 3,75 (с, 3H); 3,55 (с, 3H); 3,20 (м, 1H); 3,10 (м, 1H); 3,05 (м, 1H); 2,90 (ушир.с, 2H); 2,75 (м, 2H); 2,35 (м, 4H); 2,30 (с, 3H); 1,15 (т, 3H).
Пример 46:
3-(2-этоксипиридин-3-ил)-1-(4-метоксифенилсульфонил)-3-[2-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 653,10 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,20 (м, 1H); 8,10 (м, 3H); 8,05 (д, 1H); 7,95 (д, 1H); 7,30 (м, 2H); 7,20 (м, 3H); 7,10 (т, 1H); 7,00 (м, 2H); 3,95 (м, 1H); 3,90 (м, 1H); 3,80 (с, 3H); 3,65 (м, 1H); 3,25 (м, 1H); 3,15 (м, 1H); 2,70 (м, 2H); 2,60 (м, 2H); 2,25 (м, 4H); 2,20 (с, 3H); 0,70 (т, 3H).
Пример 47:
3-(2-этоксипиридин-3-ил)-1-(2-метоксифенилсульфонил)-3-[2-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 653,10 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,30 (д, 1H); 8,25 (д, 1H); 8,10 (м, 2H); 7,75 (д, 1H); 7,55 (т, 1H); 7,25 (м, 2H); 7,15 (т, 1H); 7,10 (д, 1H); 7,00 (т, 1H); 6,90 (м, 1H); 6,80 (д, 2H); 4,20 (м, 2H); 3,60 (с, 3H); 3,25 (м, 1H); 3,05 (м, 2H); 2,85 (м, 2H); 2,70 (м, 2H); 2,35 (м, 4H); 2,30 (с, 3H); 1,15 (т, 3H).
I.4 Получение соединений I, где X1 означает -NH-
I.4.1 Соединения I, где X1 означает -NH-, A 1,4-фенилен, X2 простую связь, X3 означает N, n равно 2, и m равно 2
Пример 48:
1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-3-[4-(4-этилпиперазин-1-ил)-фениламино]-5-йод-1,3-дигидроиндол-2-он
48.1 1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-3-гидрокси-5-йод-1,3-дигидроиндол-2-он
Гидрид натрия (145 мг 50%-ной дисперсии в минеральном масле, 3,03 ммол) добавляли в охлажденный льдом раствор 3-(2-этоксипиридин-3-ил)-3-гидрокси-5-йод-1,3-дигидроиндол-2-она (1,0 г, 2,52 ммоль) в ДМФ (20 мл), Реакционную смесь перемешивали 15 минут при 0°C и затем добавляли 2,4-диметоксифенилсульфонилхлорида (99 мг, 0,48 ммоль). Реакционную смесь перемешивали 2 часа при комнатной температуре, соединяли с водой и полученный осадок фильтровали. Осадок, образованный после перемешивания в течение ночи в этиловом эфире (50 мл), отсасывали, с получением 730 мг указанного в заголовке соединения (выход 45%).
МС-ESI: 597,05 [M+H]+
48.2 3-хлор-1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-5-йод-1,3-дигидроиндол-2-он
К охлажденному льдом раствору 1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-3-гидрокси-5-йод-1,3-дигидроиндол-2-она (100 мг, 0,15 ммоль) в дихлорметане (30 мл) добавляли последовательно пиридин (40 мкл, 0,46 ммоль) и тионилхлорид (35 мкл, 0,46 ммоль). Реакционную смесь нагревали до комнатной температуры и перемешивали 3 часа. В реакционную смесь добавляли ледяную воду и водную фазу экстрагировали дихлорметаном. Органическую фазу сушили над сульфатом магния, фильтровали и концентрировали при пониженном давлении. Полученный сырой продукт (110 мг) без дополнительной очистки использовали на следующем этапе.
МС-ESI: 614,90 [M+H]+
48.3 1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-3-[4-(4-этилпиперазин-1-ил)-фениламино]-5-йод-1,3-дигидроиндол-2-он
Добавляли 4-(4-этилпиперазин-1-ил)-фениламин (44 мг, 0,21 ммоль) к раствору 3-хлор-1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-5-йод-1,3-дигидроиндол-2-она (110 мг, 0,18 ммоль) в дихлорметане (15 мл). Реакционную смесь перемешивали в микроволновом реакторе Biotage 4 часа при 120°C. Реакционную смесь концентрировали при пониженном давлении. После хроматографической очистки (силикагель, 0-8% метанол в дихлорметане) получено 16 мг указанного в заголовке соединения (выход 11%).
МС-ESI: 784,20 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,15 (м, 1H); 8,05 (д, 1H); 7,85 (д, 1H); 7,75 (д, 1H); 7,50 (д, 1H); 7,30 (с, 1H), 7,10 (дд, 1H); 6,70 (д, 1H); 6,65 (с, 1H); 6,45 (д, 2H); 6,40 (д, 2H); 4,05 (м, 2H); 3,85 (с, 3H); 3,55 (с, 3H); 2,95 (ушир.с, 4H); 2,45 (ушир.с, 4H); 2,35 (м, 2H); 1,00 (т, 3H); 0,90 (т, 3H).
Пример 49:
1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-5-йод-3-[4-(4-метилпиперазин-1-ил)-фениламино]-1,3-дигидроиндол-2-он
49.1 3-(2-этоксипиридин-3-ил)-5-йод-3-[4-(4-метилпиперазин-1-ил)-фениламино]-1,3-дигидроиндол-2-он
МС-ESI: 570,15 [M+H]+
49.2 1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-5-йод-3-[4-(4-метилпиперазин-1-ил)-фениламино]-1,3-дигидроиндол-2-он
МС-ESI: 770,70 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,25 (д, 1H); 8,15 (м, 1H); 8,05 (д, 1H); 7,60 (м, 2H); 7,45 (с, 1H); 6,95 (м, 1H); 6,55 (д, 1H); 6,35 (м, 4H); 6,25 (м, 1H); 4,25 (м, 2H); 3,90 (с, 3H); 3,35 (с, 3H); 3,05 (м, 4H); 2,55 (м, 4H); 2,35 (с, 3H); 1,20 (т, 3H).
Пример 50:
3-(2-этоксипиридин-3-ил)-5-йод-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-фениламино]-1,3-дигидроиндол-2-он
МС-ESI: 740,15 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,35 (д, 1H); 8,15 (м, 1H); 7,85 (д, 2H); 7,75 (д, 1H); 7,60 (д, 1H); 7,35 (с, 1H); 7,10 (м, 1H); 7,05 (д, 1H); 6,45 (д, 2H); 6,35 (д, 2H); 4,15 (м, 1H); 4,00 (м, 1H); 3,95 (с, 3H); 3,05 (м, 4H); 2,60 (м, 4H); 2,35 (с, 3H); 0,95 (т, 3H).
Пример 51:
5-хлор-3-(2-этоксипиридин-3-ил)-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-фениламино]-1,3-дигидроиндол-2-он
51.1 5-хлор-3-(2-этоксипиридин-3-ил)-3-[4-(4-метилпиперазин-1-ил)-фениламино]-1,3-дигидроиндол-2-он
МС-ESI: 478,20 [M+H]+
51.2 5-хлор-3-(2-этоксипиридин-3-ил)-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-фениламино]-1,3-дигидроиндол-2-он
МС-ESI: 648,15 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,25 (д, 1H); 8,15 (м, 1H); 7,80 (д, 2H); 7,75 (д, 1H); 7,30 (м, 1H); 7,10 (с, 1H); 7,00 (м, 1H); 6,90 (д, 2H); 6,45 (д, 2H); 6,35 (д, 2H); 4,15 (м, 1H); 4,10 (м, 1H); 4,00 (с, 1H); 3,90 (с, 3H); 3,05 (м, 4H); 2,55 (м, 4H); 2,35 (с, 3H); 1,05 (т, 3H).
Пример 52:
5-хлор-3-(2-этоксипиридин-3-ил)-6-фтор-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-фениламино]-1,3-дигидроиндол-2-он
52.1 5-хлор-3-(2-этоксипиридин-3-ил)-6-фтор-3-[4-(4-метилпиперазин-1-ил)-фениламино]-1,3-дигидроиндол-2-он
МС-ESI: 496,20 [M+H]+
52.2 5-хлор-3-(2-этоксипиридин-3-ил)-6-фтор-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-фениламино]-1,3-дигидроиндол-2-он
МС-ESI: 666,20 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,25 (д, 1H); 8,15 (м, 1H); 7,80 (д, 2H); 7,65 (д, 1H); 7,10 (д, 1H); 7,00 (т, 1H); 6,95 (д, 2H); 6,35 (д, 2H); 6,25 (д, 2H); 4,15 (м, 2H); 3,95 (с, 1H); 3,90 (с, 3H); 3,05 (м, 4H); 2,55 (м, 4H); 2,35 (с, 3H); 1,05 (т, 3H).
Пример 53:
6-хлор-3-(2-этоксипиридин-3-ил)-5-фтор-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-фениламино]-1,3-дигидроиндол-2-он
53.1 6-хлор-3-(2-этоксипиридин-3-ил)-5-фтор-3-[4-(4-метилпиперазин-1-ил)-фениламино]-1,3-дигидроиндол-2-он
МС-ESI: 496,20 [M+H]+
53.2 6-хлор-3-(2-этоксипиридин-3-ил)-5-фтор-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-фениламино]-1,3-дигидроиндол-2-он
МС-ESI: 666,20 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,25 (д, 1H); 8,15 (м, 1H); 7,90 (д, 1H); 7,85 (д, 2H); 6,95 (м, 1H); 6,90 (м, 3H); 6,35 (д, 2H); 6,25 (д, 2H); 4,15 (м, 2H); 3,95 (с, 1H); 3,90 (с, 3H); 3,05 (м, 4H); 2,55 (м, 4H); 2,35 (с, 3H); 1,05 (т, 3H).
Пример 54:
3-(2-этоксипиридин-3-ил)-5,6-дифтор-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-фениламино]-1,3-дигидроиндол-2-он
54.1 3-(2-этоксипиридин-3-ил)-5,6-дифтор-3-[4-(4-метилпиперазин-1-ил)-фениламино]-1,3-дигидроиндол-2-он
МС-ESI: 480,20 [M+H]+
54.2 3-(2-этоксипиридин-3-ил)-5,6-дифтор-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-фениламино]-1,3-дигидроиндол-2-он
МС-ESI: 650,25 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,25 (д, 1H); 8,15 (м, 1H); 7,80 (д, 2H); 7,70 (м, 1H); 6,95 (м, 4H); 6,35 (д, 2H); 6,25 (д, 2H); 4,15 (м, 2H); 3,95 (с, 1H); 3,90 (с, 3H); 3,05 (м, 4H); 2,55 (м, 4H); 2,35 (с, 3H); 1,05 (т, 3H).
Пример 55:
1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-3-[4-(4-метилпиперазин-1-ил)-фениламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
55.1 3-(2-этоксипиридин-3-ил)-3-[4-(4-метилпиперазин-1-ил)-фениламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 469,25 [M+H]+
55.2 1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-3-[4-(4-метилпиперазин-1-ил)-фениламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 669,25 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,30 (д, 1H); 8,15 (м, 1H); 8,05 (д, 1H); 7,95 (д, 1H); 7,60 (д, 1H); 7,45 (с, 1H); 7,00 (м, 1H); 6,55 (д, 1H); 6,30 (м, 5H); 4,25 (м, 2H); 3,90 (с, 3H); 3,35 (с, 3H); 3,05 (м, 4H); 2,55 (м, 4H); 2,35 (с, 3H); 1,15 (т, 3H).
Пример 56:
1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-3-[4-(4-этилпиперазин-1-ил)-фениламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
56.1 3-(2-этоксипиридин-3-ил)-3-[4-(4-этилпиперазин-1-ил)-фениламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 483,30 [M+H]+
56.2 1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-3-[4-(4-этилпиперазин-1-ил)-фениламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 683,30 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,30 (д, 1H); 8,15 (м, 1H); 8,05 (д, 1H); 7,95 (д, 1H); 7,60 (д, 1H); 7,45 (с, 1H); 7,00 (м, 1H); 6,60 (д, 1H); 6,30 (м, 5H); 4,25 (м, 2H); 4,00 (м, 1H); 3,90 (с, 3H); 3,30 (с, 3H); 3,10 (м, 4H); 2,65 (м, 4H); 2,55 (м, 2H); 1,15 (м, 6H).
Пример 57:
3-(2-этоксипиридин-3-ил)-3-[4-(4-этилпиперазин-1-ил)-фениламино]-1-(4-метоксифенилсульфонил)-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 653,30 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,30 (д, 1H); 8,15 (м, 1H); 7,95 (д, 1H); 7,90 (м, 2H); 7,60 (д, 1H); 7,40 (с, 1H); 7,00 (т, 1H); 6,95 (д, 2H); 6,35 (д, 2H); 6,25 (д, 2H); 4,15 (м, 1H); 4,05 (м, 1H); 3,90 (с, 3H); 3,80 (м, 1H); 3,30 (с, 3H); 3,10 (м, 4H); 2,65 (м, 4H); 2,55 (м, 2H); 1,15 (т, 3H); 0,95 (т, 3H).
Пример 58:
3-(2-этоксипиридин-3-ил)-3-[4-(4-этилпиперазин-1-ил)-фениламино]-1-(2-метоксифенилсульфонил)-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 653,30 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,30 (д, 1H); 8,15 (м, 1H); 8,10 (д, 1H); 7,95 (д, 1H); 7,65 (д, 1H); 7,55 (т, 1H); 7,45 (с, 1H); 7,10 (т, 2H); 7,00 (м, 1H); 6,85 (д, 1H); 6,30 (м, 4H); 4,25 (м, 2H); 3,95 (с, 1H); 3,80 (м, 1H); 3,35 (с, 3H); 3,15 (ушир.с, 4H); 2,65 (ушир.с, 4H); 2,55 (м, 2H); 1,15 (м, 6H).
Пример 59:
3-(2-этоксипиридин-3-ил)-6-фтор-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-фениламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
59.1 3-(2-этоксипиридин-3-ил)-6-фтор-3-[4-(4-метилпиперазин-1-ил)-фениламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 487,25 [M+H]+
59.2 3-(2-этоксипиридин-3-ил)-6-фтор-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-фениламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 657,25 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,15 (м, 2H); 8,00 (д, 2H); 7,80 (д, 1H); 7,70 (д, 1H); 7,15 (м, 3H); 6,45 (д, 2H); 6,35 (д, 2H); 6,00 (с, 1H); 3,95 (м, 1H); 3,90 (с, 3H); 3,80 (м, 1H); 2,95 (ушир.с, 4H); 2,45 (ушир.с, 4H); 2,25 (с, 3H); 0,75 (м, 6H).
I.4.2 Соединения I, где X1 означает -NH-, A 1,3-фенилен, X2 простую связь, X3 означает N, n равно 2, и m равно 2
Пример 60:
1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-5-йод-3-[3-(4-метилпиперазин-1-ил)-фениламино]-1,3-дигидроиндол-2-он
60.1 3-(2-этоксипиридин-3-ил)-5-йод-3-[3-(4-метилпиперазин-1-ил)-фениламино]-1,3-дигидроиндол-2-он
МС-ESI: 570,15 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,20 (д, 1H); 8,15 (м, 1H); 7,55 (д, 1H); 7,40 (с, 1H); 7,00 (м, 2H); 6,55 (д, 1H); 6,45 (д, 1H); 6,25 (д, 1H); 6,15 (с, 1H); 4,25 (м, 2H); 2,50 (ушир.с, 4H); 2,30 (с, 3H); 2,05 (ушир.с, 3H); 1,15 (т, 3H).
60.2 1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-5-йод-3-[3-(4-метилпиперазин-1-ил)-фениламино]-1,3-дигидроиндол-2-он
МС-ESI: 770,10 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,15 (м, 1H); 7,95 (д, 1H); 7,90 (д, 1H); 7,75 (д, 1H); 7,50 (д, 1H); 7,30 (с, 1H); 7,05 (д, 1H); 6,70 (м, 2H); 6,65 (с, 1H); 6,25 (м, 2H); 6,20 (с, 1H); 6,00 (д, 1H); 4,05 (м, 2H); 3,85 (с, 3H); 3,55 (с, 3H); 2,85 (м, 4H); 2,35 (ушир.с, 4H); 2,20 (ушир.с, 3H); 0,90 (т, 3H).
Пример 61:
3-(2-этоксипиридин-3-ил)-1-(4-метоксифенилсульфонил)-3-[3-(4-метилпиперазин-1-ил)-фениламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
61.1 3-(2-этоксипиридин-3-ил)-3-[3-(4-метилпиперазин-1-ил)-фениламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 469,25 [M+H]+
61.2 3-(2-этоксипиридин-3-ил)-1-(4-метоксифенилсульфонил)-3-[3-(4-метилпиперазин-1-ил)-фениламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 639,25 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,15 (м, 1H); 8,05 (д, 1H); 7,95 (м, 4H); 7,55 (с, 1H); 7,15 (д, 1H); 7,10 (м, 2H); 6,70 (т, 1H); 6,30 (с, 1H); 6,25 (м, 1H); 6,10 (с, 1H); 5,95 (д, 1H); 3,95 (м, 1H); 3,85 (с, 3H); 3,65 (м, 1H); 2,85 (м, 4H); 2,35 (ушир.с, 4H); 2,20 (с, 3H); 0,65 (т, 3H).
Пример 62:
1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-3-[3-(4-метилпиперазин-1-ил)-фениламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 669,25 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,15 (м, 1H); 8,05 (д, 1H); 7,90 (м, 3H); 7,55 (с, 1H); 7,10 (м, 1H); 6,70 (м, 2H); 6,65 (м, 1H); 6,30 (м, 2H); 6,20 (с, 1H); 5,95 (д, 1H); 4,05 (м, 2H); 3,85 (с, 3H); 3,55 (с, 3H); 2,85 (м, 4H); 2,35 (ушир.с, 4H); 2,20 (с, 3H); 0,85 (т, 3H).
I.4.3 Соединения I, где X1 означает -NH-, A означает 1,4-фенилен, X2 означает простую связь, X3 означает CH, n равно 1, и m равно 1
Пример 63:
3-(4-азетидин-3-илфениламино)-1-(2!4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-5-йод-1,3-дигидроиндол-2-он как гидрохлорид
63.1 трет-бутиловый эфир 3-{4-[3-(2-этоксипиридин-3-ил)-5-йод-2-оксо-2,3-дигидро-1H-индол-3-иламино]-фенил}-азетидин-1-карбоновой кислоты
МС-ESI: 626,90 [M+H]+
63.2 трет-бутиловый эфир 3-{4-[1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-5-йод-2-оксо-2,3-дигидро-1H-индол-3-иламино]-фенил]-азетидин-1-карбоновой кислоты
63.3 3-(4-азетидин-3-илфениламино)-1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-5-йод-1,3-дигидроиндол-2-он как гидрохлорид
МС-ESI: 765,00 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 9,75 (ушир.с, 1H); 9,45 (ушир.с, 1H); 8,15 (д, 1H); 8,00 (д,1H); 7,80 (д, 1H); 7,65 (д, 1H); 7,60 (д, 1H), 7,35 (с, 1H); 7,00 (м, 2H); 6,90 (т, 1H); 6,55 (м, 3H); 6,45 (м, 1H); 4,55 (м, 1H); 4,30-4,00 (м, 7H); 3,85 (с, 3H); 3,55 (с, 3H); 1,15 (т, 3H).
Пример 64:
1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-3-[4-(1-этилазетидин-3-ил)-фениламино]-5-йод-1,3-дигидроиндол-2-он как соль трифторуксусной кислоты
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 13,55 (ушир.с, 1H); 8,15 (м, 1H); 8,05 (д, 1H); 7,80 (д, 1H); 7,65 (м, 2H); 7,35 (с, 1H); 6,90 (м, 1H); 6,85 (д, 2H); 6,55 (м, 4H); 6,35 (с, 1H); 4,60 (м, 2H); 4,25 (м, 1H); 4,15 (м, 2H); 3,85 (с, 3H); 3,60 (м, 2H); 3,55 (с, 3H); 3,15 (м, 2H); 1,25 (т, 3H); 1,10 (т, 3H).
Пример 65:
3-(4-азетидин-3-илфениламино)-3-(2-этоксипиридин-3-ил)-5-йод-1-(4-метоксифенилсульфонил)-1,3-дигидроиндол-2-он
65.1 трет-бутиловый эфир 3-{4-[3-(2-этоксипиридин-3-ил)-5-йод-1-(4-метоксифенилсульфонил)-2-оксо-2,3-дигидро-1H-индол-3-иламино]-фенил}-азетидин-1-карбоновой кислоты
МС-ESI: 741,10 [M+Bu+H]+
65.2 3-(4-азетидин-3-илфениламино)-3-(2-этоксипиридин-3-ил)-5-йод-1-(4-метоксифенилсульфонил)-1,3-дигидроиндол-2-он
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 9,80 (ушир.с, 1H); 9,45 (ушир.с, 1H); 8,15 (д, 1H); 7,95 (д, 1H); 7,90 (д, 2H); 7,65 (м, 2H); 7,30 (с, 1H); 7,00-6,80 (м, 5H); 6,45 (м, 2H); 4,30 (ушир.с, 2H); 4,20-3,95 (м, 5H); 3,85 (с, 3H); 0,95 (т, 3H).
Пример 66:
3-(2-этоксипиридин-3-ил)-3-[4-(1-этилазетидин-3-ил)-фениламино]-5-йод-1-(4-метоксифенилсульфонил)-1,3-дигидроиндол-2-он как соль трифторуксусной кислоты
МС-ESI: 725,15 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 13,55 (ушир.с, 1H); 8,15 (м, 1H); 7,95 (м, 3H); 7,70 (д, 1H); 7,65 (д, 1H); 7,30 (с, 1H); 6,95 (м, 1H); 6,90 (д, 2H); 6,80 (д, 2H); 6,45 (д, 2H); 4,60 (м, 2H); 4,10 (м, 2H); 3,95 (м, 1H); 3,90 (с, 3H); 3,65 (м, 2H); 3,15 (м, 2H); 1,25 (т, 3H); 0,90 (т, 3H).
I.4.4 Соединения I, где X1 означает -NH-, A означает пиридилен, X2 означает простую связь, X3 означает N, n равно 2, и m равно 2
Пример 67:
1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-5-йод-3-[6-(4-метилпиперазин-1-ил)-пиридин-3-иламино]-1,3-дигидроиндол-2-он
67.1 3-(2-этоксипиридин-3-ил)-5-йод-3-[6-(4-метилпиперазин-1-ил)-пиридин-3-иламино]-1,3-дигидроиндол-2-он
МС-ESI: 571,20 [M+H]+
67.2 1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-5-йод-3-[6-(4-метилпиперазин-1-ил)-пиридин-3-иламино]-1,3-дигидроиндол-2-он
МС-ESI: 771,15 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,20 (д, 1H); 8,15 (м, 1H); 7,85 (д, 1H); 7,75 (д, 1H); 7,55 (д, 1H); 7,35 (с, 1H); 7,25 (м, 1H); 7,10 (м, 1H); 6,70 (д, 1H); 6,55 (с, 1H); 6,30 (д, 1H); 5,85 (с, 1H); 4,05 (м, 2H); 3,85 (с, 3H); 3,55 (с, 3H); 3,25 (м, 4H); 2,40 (м, 4H); 2,20 (с, 3H); 0,95 (т, 3H).
Пример 68:
3-(2-этоксипиридин-3-ил)-5-йод-1-(4-метоксифенилсульфонил)-3-[6-(4-метилпиперазин-1-ил)-пиридин-3-иламино]-1,3-дигидроиндол-2-он
МС-ESI: 741,10 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,15 (м, 1H); 8,10 (д, 1H); 7,90 (д, 2H); 7,80 (д, 1H); 7,60 (д, 1H); 7,40 (м, 1H); 7,30 (с, 1H); 7,15 (м, 3H); 6,85 (д, 1H); 6,65 (д, 1H); 4,15 (м, 2H); 3,95 (м, 1H); 3,85 (с, 3H); 3,75 (м, 1H); 3,50 (м, 2H); 3,05 (м, 4H); 2,85 (с, 3H); 0,70 (т, 3H).
Пример 69:
1-фенилсульфонил-3-(2-этоксипиридин-3-ил)-5-йод-3-[6-(4-метилпиперазин-1-ил)-пиридин-3-иламино]-1,3-дигидроиндол-2-он
МС-ESI: 711,10 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,15 (м, 2H); 7,95 (д, 2H); 7,80 (м, 2H); 7,65 (м, 3H); 7,40 (м, 1H); 7,35 (с, 1H); 7,15 (м,1H); 6,80 (д, 1H); 6,60 (д, 1H); 4,15 (м, 2H); 3,95 (м, 1H); 3,70 (м, 1H); 3,50 (м, 2H); 3,05 (м, 4H); 2,85 (с, 3H); 0,65 (т, 3H).
1,4,5 Соединения I, где X1 означает -NH-, A означает 1,4-фенилен, X2 означает -C(=O)-, X3 означает N, n равно 2, и m равно 2
Пример 70:
3-(2-этоксипиридин-3-ил)-5-йод-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-карбонил)-фениламино]-1,3-дигидроиндол-2-он
70.1 3-(2-этоксипиридин-3-ил)-5-йод-3-[4-(4-метилпиперазин-1-карбонил)-фениламино]-1,3-дигидроиндол-2-он
МС-ESI: 598,15 [M+H]+
70.2 3-(2-этоксипиридин-3-ил)-5-йод-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-карбонил)-фениламино]-1,3-дигидроиндол-2-он
МС-ESI: 768,10 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,15 (м, 1H); 8,00 (д, 2H); 7,85 (м, 2H); 7,7 (д, 1H); 7,25 (с, 1H), 7,15 (д, 2H); 7,10 (м, 1H); 7,05 (д, 2H); 7,0 (с, 1H); 6,60 (д, 2H); 3,95 (м, 1H); 3,85 (с, 3H); 3,70 (м, 1H); 3,45 (ушир.с, 4H); 2,30 (ушир.с, 4H); 2,20 (с, 3H); 0,65 (т, 3H).
Пример 71:
1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-5-йод-3-[4-(4-метилпиперазин-1-карбонил)-фениламино]-1,3-дигидроиндол-2-он
МС-ESI: 798,10 [M+H]+
Пример 72:
3-(2-этоксипиридин-3-ил)-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-карбонил)-фениламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
72.1 3-(2-этоксипиридин-3-ил)-3-[4-(4-метилпиперазин-1-карбонил)-фениламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 497,20 [M+H]+
72.2 3-(2-этоксипиридин-3-ил)-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-карбонил)-фениламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 667,25 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,10 (м, 1H); 8,00 (м, 3H); 7,95 (д, 1H); 7,85 (д, 1H); 7,5 (м, 1H); 7,15 (д, 2H), 7,05 (м, 3H); 7,0 (с, 1H); 6,55 (д, 2H); 3,85 (м, 1H); 3,80 (с, 3H); 3,60 (м, 1H); 3,50 (ушир.с, 4H); 2,50 (ушир.с, 4H); 2,35 (ушир.с, 3H); 0,55 (т, 3H).
Пример 73:
1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-3-[4-(4-метилпиперазин-1-карбонил)-фениламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 697,25 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,10 (м, 1H); 8,00 (м, 3H); 7,90-7,80 (м, 4H); 7,5 (м, 1H); 7,05 (м, 1H); 7,0 (д, 2H); 6,90 (с, 1H); 6,70 (м, 2H); 6,60 (д, 2H); 4,05-3,95 (м, 2H); 3,80 (с, 3H); 3,60 (с, 3H); 3,40 (ушир.с, 4H); 2,25 (ушир.с, 4H); 2,15 (с, 3H); 0,80 (т, 3H).
1.4.6 Соединения I, где X1 означает -NH-, A означает 1,4-фенилен, X2 означает -CH2, X3 означает N, n равно 2, и m равно 2
Пример 74
1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-3-[4-(4-метилпиперазин-1-илметил)-фениламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
74.1 3-(2-этоксипиридин-3-ил)-3-[4-(4-метилпиперазин-1-илметил)-фениламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
При 0°C добавляли 4-(4-метилпиперазин-1-илметил)-фениламин (425 мг, 2,07 ммоль) к раствору 3-хлор-3-(2-этоксипиридин-3-ил)-2-оксо-2,3-дигидро-1H-индол-5-карбонитрила (500 мг, 1,59 ммоль) в дихлорметане (50 мл) и DIPEA (0,27 мл, 159 ммоль). Реакционную смесь перемешивали 2 ч при комнатной температуре, затем добавляли водный раствор NaHCO3. Водную реакционную смесь экстрагировали дихлорметаном. Объединенные органические фазы сушили над сульфатом магния, фильтровали и концентрировали при пониженном давлении. Хроматографическая очистка (силикагель, 0-20% метанола в дихлорметане) дала 791 мг указанного в заголовке соединения (выход 99%).
МС-ESI: 483,25 [M+H]+
74.2 1-(2,4-диметоксифенилсульфонил)-3-(2-этоксипиридин-3-ил)-3-[4-(4-метилпиперазин-1-илметил)-фениламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 683,25 [M+H]+
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,15 (м, 1H); 7,95 (д, 1H); 7,90 (м, 3H); 7,5 (с, 1H); 7,1 (м, 1H), 6,80 (д, 2H); 6,70 (м, 2H); 6,50 (д, 2H); 6,45 (с, 1H); 4,05 (м, 2H); 3,85 (с, 3H); 3,60 (с, 3H); 3,25 (с, 2H); 2,30 (ушир.с, 8H); 2,15 (с, 3H); 0,85 (т, 3H).
Пример 75
3-(2-этоксипиридин-3-ил)-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-илметил)-фениламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
1H-ЯМР (500 МГц, ДМСО-d6): δ [м.д.] 8,15 (м, 1H); 8,05-7,95 (м, 5H); 7,55 (м, 1H); 7,20 (д, 2H); 7,10 (т, 1H); 6,85 (д, 2H); 6,55 (м, 2H); 3,95 (м, 1H); 3,85 (с, 3H); 3,75 (м, 2H); 3,60 (м, 1H); 3,35 (м, 4H); 2,90 (м, 4H); 2,60 (м, 3H); 0,60 (т, 3H).
Пример 76
3-(2-(2,2-дифторэтокси)-пиридин-3-ил)-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 689,10 [M+H]+
Пример 77
1-(4-метоксифенилсульфонил)-3-(2-(2,2,2-трифторэтокси)-пиридин-3-ил)-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 707,20 [M+H]+
Пример 78
3-(2-(2,2-дифторэтокси)-фенил)-1-(4-метоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-бензиламино]-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 688,20 [M+H]+
Пример 79
3-[4-(4-этилпиперазин-1-ил)-фениламино]-1-(4-метоксифенилсульфонил)-3-(2-(2,2-дифторэтокси)-пиридин-3-ил)-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 689,10 [M+H]+
Пример 80
3-[4-(4-этилпиперазин-1-ил)-фениламино]-1-(4-метоксифенилсульфонил)-3-(2-(2,2,2-трифторэтокси)-пиридин-3-ил)-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 693,20 [M+H]+
Пример 81
3-(2-(2,2-дифторэтокси)-фенил)-3-[4-(4-этилпиперазин-1-ил)-фениламино]-1-(4-метоксифенилсульфонил)-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 674,20 [M+H]+
Пример 82
1-(2,4-диметоксифенилсульфонил)-3-[4-(4-метилпиперазин-1-ил)-фениламино]-3-(2-(трифторметокси)-фенил)-2-оксо-2,3-дигидро-1H-индол-5-карбонитрил
МС-ESI: 736,20 [M+H]+
II. Определение биологической активности
1. Тест на связывание рецептора вазопрессина V1b:
Вещества:
Испытуемые вещества растворяли в DMSO до концентрации 10-2 М и дополнительно разбавляли в DMSO до концентраций от 5×10-4 М до 5×10-9 M. Этот ряд разведений в DMSO разбавляли тестовым буфером 1:10. В начале испытания концентрацию вещества еще раз разбавляли в отношении 1:5 (2% DMSO в исходной смеси).
Приготовление мембраны:
Собирали клетки CHO-K1 со стабильно экспрессированным рецептором человеческого вазопрессина V1b (клон 3H2) и гомогенизировали в 50 мМ Tris-HCl в присутствии ингибиторов протеазы (Roche complete Mini # 1836170) в гомогенизаторе Polytron на среднем положении 2×10 секунд и затем центрифугировали 1 ч при 40000×g. Гранулы мембраны еще раз гомогенизировали и центрифугировали, как описано, и затем вводили в 50 мкМ трис-HCl, pH 7,4, гомогенизировали и аликвотами хранили замороженными в жидком азоте при -190°C.
Испытание на связывание:
Испытание на связывание проводили в соответствии с методом Tahara и др. (Tahara A et al., Brit. J. Pharmacol. 125, 1463-1470 (1998)).
Инкубационный буфер представлял собой 50 мкМ Tris, 10 мкМ MgCl2, 0,1% BSA, pH 7,4.
В исходной смеси для испытания (250 мкл) инкубировали мембраны (50 мкг/мл белка в инкубационном буфере) клеток CHO-K1 со стабильно экспрессированными рецепторами человеческого V1b (клеточная линия hV1b_3H2_CHO) с 1,5 нМ 3H-AVP (8-Arg-вазопрессин, PerkinElmer # 18479) в инкубационном буфере (50 мкМ Tris, 10 мкМ MgCl2, 0,1% BSA, pH 7,4) (полное связывание) или дополнительно с повышающимися концентрациями испытуемого вещества (вытеснительный эксперимент). Неспецифическое связывание проводили с 1 мкМ AVP (Bachern # H1780). Все определения производили трижды. После инкубации (60 минут при комнатной температуре), свободный радиолиганд отфильтровывали с помощью вакуумной фильтрации (сборщик клеток Skatron 7000) через стекловолоконные фильтровальные холсты Wathman GF/B и фильтр переносили в сцинтилляционный реактор. Жидкостное сцинтилляционное измерение проводилось на приборе Tricarb, модель 2000 или 2200CA (Packard). Пересчет измеренных cpm в dpm проводили с помощью стандартного ряда тушения.
Оценка:
Параметры связи рассчитывали нелинейной регрессией в SAS. Алгоритмы программы работают аналогично программе оценки LIGAND (Munson PJ, Rodbard D, Analytical Biochem. 107, 220-239 (1980)). Значение Kd для 3H-AVP относительно рекомбинантных рецепторов hV1b составило 0,4 нМ и использовалось для определения значения Ki.
2. Испытания на связывание рецептора вазопрессина V1a:
Вещества:
Испытуемые вещества растворяли в концентрации 10-2 М в DMSO. Дальнейшее разбавление этих растворов DMSO проводили в инкубационном буфере (50 мкМ Tris, 10 мкМ MgCl2, 0,1% BSA, pH 7,4).
Приготовление мембраны:
Собирали клетки CHO-K1 со стабильно экспрессированным рецептором человеческого вазопрессина V1a (клон 5) и гомогенизировали в 50 мМ Tris-HCl в присутствии ингибиторов протеазы (Roche complete Mini # 1836170) в гомогенизаторе Polytron на среднем положении 2×10 секунд и затем центрифугировали 1 ч при 40000×g. Гранулы мембраны гомогенизировали и центрифугировали еще раз, как описано, затем вводили в 50 мкМ Tris-HCl, pH 7,4, гомогенизировали и аликвотами хранили замороженными в жидком азоте при -190°C.
Тест на связывание:
Испытание на связывание проводили в соответствии с методом Tahara и др. (Tahara A et al., Brit. J. Pharmacol. 125, 1463-1470 (1998)).
Инкубационный буфер представлял собой: 50 мкМ Tris, 10 мкМ MgCl2, 0,1% BSA, pH 7.4.
В исходной смеси для тестирования (250 мкл) инкубировали мембраны (20 мг/мл белка в инкубационном буфере) клеток CHO-K1 со стабильно экспрессированными рецепторами человеческого V1a (клеточная линия hV1a_5_CHO) с 0,04 нМ 125I-AVP (8-Arg-вазопрессин, NEX 128) в инкубационном буфере (50 мкМ Tris, 10 мкМ MgCl2, 0,1% BSA, pH 7,4) (полное связывание) или дополнительно с повышающимися концентрациями испытуемого вещества (вытеснительный эксперимент). Неспецифическое связывании определяли с 1 мкМ AVP (Bachern # H1780). Проводили троекратное измерение.
После инкубации (60 минут при комнатной температуре), свободный радиолиганд отфильтровывали с помощью вакуумной фильтрации (сборщик клеток Skatron 7000) через стекловолоконные фильтровальные холсты Wathman GF/B и фильтр переносили в сцинтилляционный реактор.
Жидкостное сцинтилляционное измерение проводили на приборе Tricarb, модель 2000 или 2200CA (Packard). Пересчет измеренных cpm в dpm проводили с помощью стандартной серии тушения.
Оценка:
Параметры связи рассчитывали нелинейной регрессией в SAS. Алгоритмы программы работают аналогично программе оценки LIGAND (Munson PJ, Rodbard D, Analytical Biochem. 107, 220-239 (1980)). Значение Kd для 125I-AVP относительно рекомбинантных рецепторов hV1a определяли в экспериментах с насыщением. Величина Kd, равная 1,33 нМ, использовалась для определения значения Ki.
3. Тест на связывание рецептора вазопрессина V2:
Вещества:
Испытуемые вещества растворяли в концентрации 10-2 М в DMSO. Дальнейшее разбавление этого раствора DMSO проводили в инкубационном буфере (50 мкМ Tris, 10 мкМ MgCl2, 0,1% BSA, pH 7,4).
Приготовление мембран:
Собирали клетки CHO-K1 со стабильно экспрессированным рецептором человеческого вазопрессина V1b (клон 23) и гомогенизировали в 50 мМ Tris-HCl в присутствии ингибиторов протеазы (Roche complete Mini # 1836170) в гомогенизаторе Polytron на среднем положении 2×10 секунд и затем центрифугировали 1 ч при 40000×g. Гранулы мембраны гомогенизировали и центрифугировали еще раз, как описано, и затем вводили в 50 мкМ Tris-HCl, pH 7,4, гомогенизировали и аликвотами хранили замороженными в жидком азоте при -190°C.
Тест на связывание:
Тест на связывание проводили в соответствии с методом Tahara и др. (Tahara A et al., Brit. J. Pharmacol. 125, 1463-1470 (1998)).
Инкубационный буфер представлял собой 50 мкМ Tris, 10 мкМ MgCl2, 0,1% BSA, pH 7,4.
В исходной смеси для испытаний (250 мкл) инкубировали мембраны (50 мкг/мл белка в инкубационном буфере) клеток CHO-K1 со стабильно экспрессирующими рецепторами человеческого V2 (клеточная линия hV2_23_CHO) с 1-2 нМ 3H-AVP (8-Arg-вазопрессин, PerkinElmer #18479) в инкубационном буфере (50 мкМ Tris, 10 мкМ MgCl2, 0,1% BSA, pH 7,4) (полное связывание) или дополнительно с повышающимися концентрациями испытуемого вещества (вытеснительный эксперимент). Неспецифическое связывании определяли с 1 мкМ AVP (Bachern # H1780). Проводили троекратное измерение.
После инкубации (60 минут при комнатной температуре) свободный радиолиганд отфильтровывали с помощью вакуумной фильтрации (сборщик клеток Skatron 7000) через стекловолоконные фильтровальные холсты Wathman GF/B и фильтр переносили в сцинтилляционный реактор.
Жидкостное сцинтилляционное измерение проводилось на приборе Tricarb, модель 2000 или 2200CA (Packard). Пересчет измеренных cpm в dpm проводили с помощью стандартного ряда тушения.
Оценка:
Параметры связи рассчитывали по нелинейной регрессии в SAS. Алгоритмы программы работают алогично программе оценки LIGAND (Munson PJ, Rodbard D, Analytical Biochem. 107, 220-239 (1980)). Значения Kd для 3H-AVP относительно рекомбинантных рецепторов hV2 составило 2,4 нМ и использовалось для определения значения Ki.
4. Тест на связывание рецептора окситоцина
Вещества
Вещества растворяли в DMSO до концентрации 10-2 М и разбавляли инкубационным буфером (50 мкМ Tris, 10 мкМ MgCl2, 0,1% BSA, pH 7,4).
Приготовление клеток:
Слитые клетки HEK-293 с переходно-экспрессированными рекомбинатными человеческими рецепторами окситоцина центрифугировали при 750×g 5 минут при комнатной температуре. Осадок вводили в охлажденный на льду буфер для лизиса (50 мМ Tris-HCl, 10% глицерин, pH 7,4 и ингибитор протеазы Roche Complete) и подвергали осмотическому удару при 4°C в течение 20 минут. Затем лизированные клетки центрифугировали 20 минут при 750 × g при 4°C, остаток вводили в инкубационный буфер и получали аликвоты по 107 клеток/мл. Эти аликвоты до применения хранили замораженными при -80°C.
Тест на связывание:
В день испытания клетки размораживали, разбавляли инкубационным буфером и гомогенизировали с Multipette Combitip (Eppendorf, Hamburg). Соединяли 0,250 мл реакционной смеси с рекомбинантными клетками в количестве (2-5)×104, 3-4 нМ 3H-окситоцина (PerkinElmer, NET 858) в присутствии испытуемого вещества (кривая ингибирования) или лишь инкубационного буфера (полное связывание). Неспецифическое связывание определяли с 10-6 М окситоцина (Bachern AG, H2510). Определение производили троекратно. Связанный и свободный радиолиганды разделяли фильтрацией в вакууме на стекловолоконном фильтре Whatman GF/B с помощью сборщика клеток Skatron 7000. Связанную радиоактивность определяли измерением по жидкостной сцинтилляции в счетчике Tricarb Beta, модель 2000 или 2200CA (Packard).
Оценка:
Параметры связи рассчитывали с помощью нелинейного регрессионного анализа (SAS), аналогично программе LIGAND, авторы Munson и Rodbard (Analytical Biochem 1980; 107: 220-239). Значение Kd для 3H-окситоцина относительно рекомбинантных рецепторов hOT составляло 7,6 нМ и использовалось для определения значения Ki.
5. Определение времени микросомального полуразложения:
Метаболическую стабильность соединений согласно изобретению определяли в следующем тесте.
Испытуемые вещества в концентрации 0,5 мкМ инкубировали следующим образом: В микротитровальном планшете 0,5 мкМ испытуемого вещества предварительно инкубировали 5 мин вместе с печеночными микросомами разных видов (крысы, человека или других видов) (0,25 мг микросомального белка/мл) в 0,05 М калийфосфатного буфера (pH 7,4) при 37°C. Реакцию начинали добавлением NADPH (1 мг/мл). Через 0, 5, 10, 15, 20 и 30 мин отбирали аликвоту 50 мкл и реакцию сразу же останавливали равными объемами ацетонитрила и охлаждали. Пробы до анализа замораживали. С помощью тандемной масс-спектрометрии определяли остаточную концентрацию неразложившегося испытуемого вещества. Из повышения кривой "сигнал испытуемого вещества в единицу времени" определяли время полуразложения (T1/2), причем время полуразложения испытуемого вещества можно рассчитать, в предположении кинетики первого порядка, из падения концентрации соединения от времени. Микросомальный клиренс (mCI) рассчитывается как mCI= ln2/T1/2/ (содержание микросомального белка в мг/мл)×1000 [мл/мин/мг] (модифицировано относительно литературных источников: Di, The Society for Biomoleculaur Screening, 2003, 453-462; Obach, DMD, 1999 vol 27. N 11, 1350-1359).
6. Способы in vitro определения ингибирования цитохрома P450 (CYP)
Люминесцирующие субстраты для 2C9 и 3A4:
0,4 мг/мл печеночных микросом человека предварительно инкубировали 10 мин с исследуемыми испытуемыми веществами (0-20 мкМ), субстратами, специфичными к CYP, в 0,05 M калийфосфатного буфера (pH 7,4) при 37°C. Cyp-специфичным субстратом для CYP 2C9 является люциферин H, для CYP 3A4 - люциферин BE. Реакцию запускали добавлением NADPH. Через 30 мин инкубации при комнатной температуре добавляли реагент обнаружения люциферина и измеряли образующийся сигнал люминесценции (модифицировано относительно литературного источника: Promega, Technical Bulletin P450-GLO™ Assays).
Зависящее от времени ингибирование мидазолама CYP 3A4
Тест состоит из двух частей. Сначала испытуемое вещество предварительно инкубируют с печеночными микросомами с NADPH (= прединкубирование), затем добавление субстрата, а на втором этапе субстрат и испытуемое вещество добавляют одновременно (= соинкубирование).
Прединкубирование:
0,05 мг/мл микросомального белка (печеночные микросомы человека) предварительно инкубировали 5 минут с 0-10 мкМ (или 50 мкМ) испытуемого вещества в калийфосфатном буфере 50 мМ. Реакцию запускали добавлением NADPH. Через 30 мин добавляли 4 мкМ мидазолама (конечная концентрация) и инкубировали еще 10 мин. Через 10 мин отбирали 75 мкл реакционного раствора и реакцию останавливали 150 мкл раствора ацетонитрила.
Соинкубирование:
0,05 мг/мл микросомального белка (печеночные микросомы человека) предварительно инкубировали 5 мин с 4 мкМ мидазолама (конечная концентрация) и 0-10 мкМ (или 50 мкМ) испытуемого вещества в 50 мМ калийфосфатного буфера. Реакцию запускали добавлением NADPH. Через 10 мин отбирали 75 мкл реакционного раствора и реакцию останавливали 150 мкл раствора ацетонитрила. Пробы для тандемного МС-анализа замораживали (модифицировано относительно литературных источников: Obdach, Journal of Pharmacology & Experimental Therapeutics, Vol 316, 1, 336-348, 2006; Walsky, Drug Metabolism and Disposition Vol 32, 6, 647-660, 2004).
7. Способ определения растворимости в воде (в мг/мл)
Растворимость в воде соединений согласно изобретению можно определить, например, по так называемому методу "shake flask" (встряхиваемой колбы) (согласно международному стандарту ASTM: E 1148-02, Standard test methods for measurement of aqueous solubility (Стандартные методы испытаний растворимости в воде), Book of Standards, Volume 11.05.). При этом добавляют избыток твердого соединения в буферный раствор с определенным значение pH (например, фосфатный буфер с pH 7.4) и образованную смесь встряхивают или перемешивают, пока не установится равновесие (типично 24 или 48 часов, иногда также до 7 дней). Затем нерастворенное твердое вещество удаляют фильтрацией или центрифугированием, и концентрацию растворенного соединения определяют УФ-спектроскопией или жидкостной хроматографией высокого давления (ВЭЖХ) с помощью соответствующей калибровочной кривой.
8. Результаты
Результаты исследований на связывание рецептора выражены как константы связи рецептора [Ki(V1b)] или селективности [Ki(V1a)/ Ki(V1b)]. Результаты исследования метаболической стабильности указаны как микросомальный клиренс (mCI).
В этом тесте соединения согласно изобретению показали очень высокое сродство с рецептором V1b (максимум 100 нМ или максимум 10 нМ, часто <1 нМ). Кроме того, соединения обнаруживают также высокую селективность в отношении рецептора V1a и рецептора окситоцина.
Результаты приведены в таблице 1. Номера соединений относятся к примерам синтеза.
|
Ключ:
|