Результат интеллектуальной деятельности: ЛЕКАРСТВЕННОЕ СРЕДСТВО С АНТИАРИТМИЧЕСКИМ И АНТИФИБРИЛЛЯТОРНЫМ ДЕЙСТВИЕМ
Вид РИД
Изобретение
Изобретение относится к медицине, в частности к фармакологии, и касается применения амида N-сукцинил-L-глутамил-L-лизина (ГК-1), представляющего собой дипептидный антагонист фактора роста нервов (С.Б.Середенин, Т.А.Гудашева. Заявка на выдачу патента на изобретение №2009105176 от 16.02.2009), в качестве средства с антиаритмическим и антифибрилляторным действием, которое может применяться для предупреждения внезапной коронарной смерти.
Предупреждение внезапной коронарной смерти является одной из наиболее актуальных проблем, стоящих перед современной медицинской наукой. Так, например, в США ежегодно регистрируется 300000-500000 случаев коронарной внезапной смерти (Billman G.E. Am. J.Physiol. Heart Circ. Physiol. - 2009. v.297. - P.H1171-H1193.). Несмотря на то, что в клиническую практику внедрено большое количество высокоэффективных лекарственных средств, обладающих выраженной антиаритмической и/или антифибрилляторной активностью, таких как β-блокаторы (атенолол, метопролол, эсмолол и др.), антиаритмики I и III классов по классификации Vaughan Williamse (прокаинамид, лидокаин, амиодарон, соталол), до настоящего времени не удалось создать эффективного препарата для первичной профилактики внезапной коронарной смерти.
Представленные на фармацевтическом рынке препараты не только недостаточно эффективны, но и обладают целым рядом существенных побочных эффектов (бронхоспазм, ортостатическая гипотензия, проатерогенное действие и др.). Не менее важно, что всем им присуще проаритмическое действие (Nishimura H. Nippon Rinsho., 2007, v.65, Suppl.8 - P.430-435; Wolberette D.L. Am. J.CardioL, 2003, v.91, P.39D-44D).
На современном этапе в клинике для профилактики внезапной коронарной смерти у пациентов с острым коронарным синдромом и/или сердечной недостаточностью наиболее часто применяют β-блокаторы, которые препятствуют аритмогенному действию катехоламинов и тем самым повышают электрическую стабильность кардиомиоцитов (Billman G.Е., Am. J.Physiol. Heart Circ. Physiol. - 2009. v.297. - P.H1171-H1193; Zipes D. et al. JACC. - 2006. -v.48, №5. - Р.1064-1108).
Также не решен вопрос и с вторичной фармакопрофилактикой внезапной коронарной смерти. Для этих целей в настоящее время наиболее эффективными считаются имплантируемые кардиовертеры-дефибрилляторы.
Все известные к настоящему времени способы профилактики внезапной коронарной смерти имеют достаточно большие ограничения, связанные как с относительно низкой эффективностью и наличием широкого спектра побочных эффектов (β-блокаторы, антиаритмики), так и высокой стоимостью медицинского пособия (имплантируемые кардиовертеры-дефибрилляторы).
Перспективным подходом к уменьшению избыточного тонического влияния симпатической нервной системы на миокард и, тем самым, повышению его (миокарда) электрической стабильности представляется использование для этих целей антагонистов фактора роста нервов NGF.
Известно, что NGF, помимо центральной нервной системы, синтезируется и экскретируется окончаниями симпатических нервов, локализованными в предсердиях (Glebova N.O., Ginty D.D. J.Neuroscience. - 2004. - v.24, №3. - 743-751; Carmmeliet P., Nat. Rev.: Genetics. - 2003. - v.4. - P.710-720; Pardini B.J. et al., J.Auton. Nerv. Syst. - 1989. - v.28. - P.193-201), т.e. в местах передачи нервного импульса с симпатических нервов на кардиомиоциты. Помимо этого, имеются данные о том, что NGF секретируется и выделяется в межклеточное пространство кардиомиоцитами желудочков (Furukawa Y. et al., J. Biol. Chem. - 1984. - v.259, №2. - P.1259-1264). Также показано, что гиперпродукция NGF сопровождается статистически значимым увеличением содержания норадреналина в миокарде (Hassankhani A. et al., Dev. Biol. - 1995. - v.169, №1. - P.309-321; Kiriazis H. et al.. Am. J.Physiol. Heart Circ. Physiol. - 2005. - v.289. - P.H1359-H1365). Взаимодействуя со специфичными для него Trk-рецепторами, NGF инициирует каскад внутриклеточных биохимических реакций, в результате чего происходит модификация трансмембранных калиевых токов - Ito - транзиторного выходящего калиевого тока, и IKur - сверхбыстрого выходящего калиевого тока задержанного выпрямления (Heath B.M. et al., J.Physiol. - 1998. - v.512, №3. - P.779-791; Ren С.et al., Auton. Neurosci. - 2008. -.144. - №1-2. - P.22-29.), что влечет за собой увеличение продолжительности интервала QT на ЭКГ (Heath B.M. et al., J.Physiol. - 1998. - v.512, №3. - P.779-791). Это хорошо коррелирует с данными о том, что инфузия NGF в левый звездчатый ганглий собак с острым экспериментальным инфарктом миокарда сопровождается удлинением интервала QT и увеличением на 48% случаев внезапной коронарной смерти (Zhou S. et al., J.Cardiovasc. Electrophysiol. - 2001. - v.12, №9. - P.1068-1073; Swissa M. et al., J. Am. Coll. Cardiol. - 2004. - v.43, №5. - P.858-864; Malfatto G. et al., Circ. Res. - 1990. - v.66. - P.427-437; Drapeau J. et al., J. Cell. Physiol. - 2005. - v.204, №1. - P.51-62 и др.).
Кроме того, согласно литературным данным, гиперпродукция NGF влечет за собой увеличение популяции β-адренорецепторов в миокарде (Heath B.M. et al., J.Physiol. - 1998. - v.512, №3. - P.779-791), т.е. на фоне гиперпродукции NGF увеличивается количество мишеней для медиаторов симпатической нервной системы - катехоламинов.
Таким образом, в настоящее время имеется достаточно обширный литературный материал, свидетельствующий о том, что гиперпродукция NGF, особенно в условиях острой ишемии миокарда, понижает электрическую стабильность сердечной мышцы и тем самым повышает риск развития внезапной коронарной смерти.
Антитела к NGF и/или биологически активные вещества, опосредованно подавляющие продукцию NGF, обладают способностью увеличивать электрическую стабильность миокарда (Lee T.-M. et al., Am. J.Physiol. Heart Circ. Physiol. - 2007. - v.294. - P.H1871-H1879; Verbout N.G. et al., Am. J.Physiol. Lung Cell. Mol. Physiol. - 2009. - v.297, №2. - P.L228-L237; Ceausu M. et al., Rom. J.Morphol. Embriol. - 2008. - v.49, №3. - P.315-320; Ieda M. et al., Curr. Med. Chem. - 2008. - v.l5, №17. - P.1731-1736).
При изучении серии дипептидных миметиков фактора роста нервов с агонистической и антагонистической активностью в качестве наиболее активного антагониста проявил себя амид N-сукцинил-L-глутамил-L-лизина (ГК-1), синтез которого осуществляли следующим образом:
Пример 1. Синтез амида N-моносукцинил-глутамил-лизина, НООС-(СН2)2-CO-Glu-Lys-NH2 (ГК-1).
а) Получение амида N-бензилоксикарбонил-γ-трет-бутил-глутамил-Nε-трет-бутилоксикарбонил-лизина, Z-Glu(OBut)-Lys(Boc)-NH2.
Раствор 4.0 г (8.4 ммоль) N-оксисукцинимидного эфира N-бензилоксикарбонил-Nε-трет-бутилоксикарбонил-лизина(Z-Lys(Boc)-OSu) в 20 мл ДМФА обрабатывали 2 мл конц. аммиака, через 5 мин разбавляли водой, выпавший осадок амида N-бензилоксикарбонил-Nε-трет-бутилоксикарбонил-лизина(Z-Lys(Boc)-NH2) отфильтровывали. Затем полученный продукт растворяли в метаноле, добавляли 3.0 г 10% Pd/C и гидрировали при комнатной температуре. Катализатор отфильтровывали, растворитель удаляли в вакууме, остаток растворяли в 20 мл ДМФА. К раствору добавляли 3.9 г (9.0 ммоль) N-оксисукцинимидного эфира N-бензилоксикарбонил-γ-трет-бутил-глутаминовой кислоты(Z-Glu(OBut)-OSu). Реакционную смесь перемешивали 6 ч при комнатной температуре (ТСХ контроль), после чего добавляли 2 мл ДМПДА и выдерживали 30 мин. Реакционную смесь разбавляли 200 мл этилацетата, поочередно промывали 100 мл воды, 100 мл 2% H2SO4 и 100 мл 3% Na2CO3, после чего упаривали. Остаток перекристаллизовывали из 80 мл метанола и 30 мл воды. Далее использовали не высушивая.
б) Получение амида N-моносукцинил-γ-трет-бутил-глутамил-Nε-трет-бутилоксикарбонил-лизина, HOOC(CH2)2CO-Glu(OBut)-Lys(Boc)-NH2.
Весь полученный Z-Glu(OBut)-Lys(Boc)-NH2 гидрировали в метаноле над 10% Pd/C при комнатной температуре. После исчезновения исходного вещества (ТСХ контроль) катализатор отфильтровывали, растворитель удаляли в вакууме. Остаток растворяли в 20 мл ДМФА и добавляли 1.2 г (12.0 ммоль) янтарного ангидрида. Реакционную смесь перемешивали при комнатной температуре до окончания реакции (ТСХ контроль), после чего добавляли 2 мл ДМПДА и выдерживали 30 мин. Реакционную смесь разбавляли 200 мл этилацетата и поочередно промывали 100 мл воды, 100 мл 2% H2SO4 и 100 мл 3% Na2CO3. После упаривания этилацетатного раствора продукт кристаллизовался. Далее использовали не высушивая.
в) Получение амида N-моносукцинил-глутамил-лизина, HOOC(CH2)2CO-Glu-Lys-NH2(ГК-1).
Весь полученный HOOC(CH2)2CO-Glu(OBut)-Lys(Boc)-NH2 обрабатывали 30 мл 4 М HCl в диоксане, при этом соединение растворялось, а затем в ходе реакции выпадал липкий осадок. Через 30 мин растворитель декантировали, остаток промывали диэтиловым эфиром, растворяли в 50 мл воды, добавляли 100 мл уксусной кислоты. Полученную массу, содержащую продукт в виде ацетатной формы, наносили на колонку с ДЭАЭ-сефадексом 5×15 см. Элюировали 0.1 М пиридин-ацетатным буфером. Соответствующие фракции собирали (ТСХ контроль) и упаривали. После сушки в вакууме получили 1.3 г (общий выход 36%) белого кристаллического продукта, Rf 0.50 (A), Rf 0.22 (Б), т.пл. 216°С (с разложением), [α]25 D - 37.0° (с 0.1; вода). C15H26N4O7.
Спектр 1Н-ЯМР (ДМСО-d6-CF3COOO): 1.33 (2 Н, м, СγH2 Lys), 1.54 (2Н, м, СδH2 Lys), 1.50 и 1.72 (2Н, два м, CβH2 Lys), 1.74 и 1.92 (2Н, два м, СβH2 Glu), 2.29 (2Н, т, СγH2 Glu), 2.44 (4Н, м, HOOCCH 2CH 2CO-), 2.78 (2H, м, СεH2 Lys), 4.18 (1Н, м, CαH Lys), 4.23 (1Н, м, СαH Glu), 7.08 и 7.30 (2Н, 2 c, NH2 амид), 7.72 (3Н, м, NH3 + Lys), 7.88 (1Н, д, NH Lys), 8.17 (1Н, д, NH Glu). HOOC(СН2)2CO- и -COOH Glu обмениваются с HDO.
Известно, что заявляемое соединение (ГК-1) обладает способностью антагонизировать такие биологические эффекты фактора роста нервов, как нейропротекторная активность, дифференцирующая активность и способность фосфорилировать тирозинкиназу А (Гудашева Т.А. с соавт. Доклады Академии наук, 2010, в печати).
Поскольку согласно литературным данным NGF реализует свои эффекты на уровне не только нервной, но и сердечно-сосудистой системы (см. выше), была изучена антифибрилляторная активность дипептида ГК-1 и показано ее наличие, а также выявлены возможные механизмы этой активности. Полученные данные позволяют сделать вывод, что на фоне хронического введения антагониста фактора роста нервов ГК-1 происходит изменение чувствительности и/или изменение соотношения пулов β1/β2-адреноструктур в миокарде. Кроме того, хроническое введение дипептида ГК-1 способствует повышению электрической стабильности миокарда, о чем свидетельствует извращенная реакция на агонисты β-адреноструктур. Полученные данные позволяют предложить применение дипептида ГК-1 в качестве антиаритмического (антифибрилляторного) лекарственного средства, которое может быть использовано в клинике для предупреждения внезапной коронарной смерти.
Пример 2. Изучение противофибрилляторной активности ГК-1.
Опыты проводили на анестезированных (уретан, 1300 мг/кг, в/в) беспородных крысах-самцах массой тела 350-400 г. После интубации и перевода животных на искусственное дыхание производили стернэктомию, перикардотомию. В миокард левого желудочка на расстоянии 0,5 см друг от друга имплантировали два позолоченных электрода. Порог электрической фибрилляции сердца определяли повторяющимся сканированием уязвимого периода сердечного цикла серией из 20 прямоугольных импульсов постоянного тока увеличивающейся интенсивности (длительность стимула - 4 мсек, частота - 50 имп/сек). За порог фибрилляции желудочков принимали минимальную силу тока, вызывающую при двухкратном повторении фибрилляцию желудочков. В опыт отбирали только тех животных, у которых фибрилляция желудочков наступала при силе тока не более 6 мА. В работе использовали электростимулятор HSE Stimulator II (Hugo Sach Electronik, Германия). В течение всего эксперимента регистрировали ЭКГ (II стандартное отведение). В качестве регистратора использовали электрокардиограф ЭК 4Т-02 (Россия). Визуальный контроль регистрируемых параметров в течение всего эксперимента производили при помощи 4-канального осциллоскопа фирмы Elema-Siemens (Швеция). Антагонист фактора роста нервов вводили внутривенно в дозе 1 мг/кг с постоянной скоростью и в постоянном объеме (1 мл) 0,9% раствора хлорида натрия. Животным контрольной серии внутривенно вводили 1 мл 0,9% раствора хлорида натрия. Для введения использовали инъектор Syringe pump (Sage Instruments, Италия).
Порог электрической фибрилляции сердца определяли через 5, 10, 20, 30, 40 и 60 минут после окончания в/в введения соединения.
Результаты обрабатывали статистически с использованием непараметрического дисперсионного анализа по Фридману с дальнейшим использованием метода множественных сравнений по Р.Даннету и критерия Манна-Уитни-Вилкоксона.
Показано, что в контрольной серии экспериментов (n=8) порог электрической фибрилляции сердца не изменялся в течение всего периода наблюдения (табл.1), тогда как у всех животных, получавших антагонист фактора роста нервов (n=8), происходило статистически значимое (Р<0,01) увеличение порога электрической фибрилляции сердца (табл.2). Антифибрилляторное действие антагониста фактора роста нервов реализовалось, начиная с 40-60 минуты после окончания его внутривенного введения.
Таким образом, полученные данные свидетельствуют о том, что исследуемое соединение обладает выраженной противофибрилляторной активностью, не уступающей таковой у эталонных антиаритмических лекарственных средств I и III классов по классификации Vaughan Williamse.
|
|
Пример 3. Изучение влияния ГК-1 (хроническое введение) на реактивность β-адренорецепторов миокарда.
Опыты проводили на бодрствующих морских свинках-самцах массой 400-500 г. Перед началом эксперимента животных фиксировали в положении на спине и регистрировали ЭКГ (II стандартное отведение). В качестве регистратора использовали Mingograph-82 (Elema-Siemens, Швеция). Затем оценивали влияние изотонического раствора хлорида натрия (0,5 мл, в/б) и неселективного агониста β-адреноструктур изопротеренола (75 мкг/кг) на хронотропную функцию сердца. Интервал между введением - 1 час. Статистическую обработку проводили с помощью критерия Вилкоксона для попарно связанных вариант.
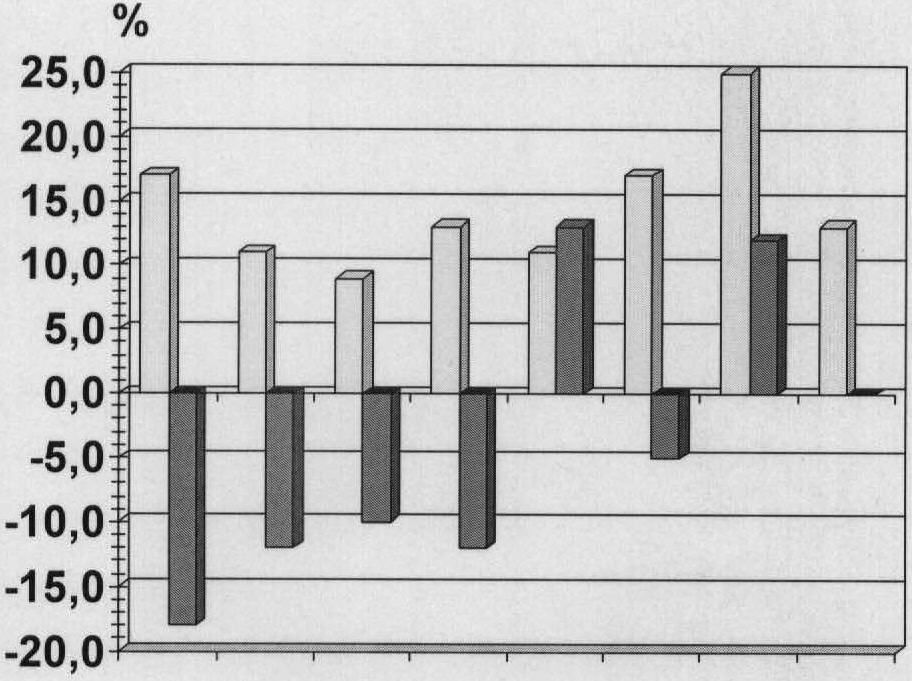
Показано, что физиологический раствор не оказывает влияния на частоту сердечных сокращений, тогда как изопротеренол вызывает статистически значимое (Р<0,05) увеличение частоты сердечных сокращений в среднем на 14,5%. Затем животным ежедневно в течение недели внутрибрюшинно вводили ГК-1 (1,5 мг/кг). Через сутки после последнего внутрибрюшинного введения соединения оценивали хронотропную реакцию сердца в ответ на введение физиологического раствора и изопротеренола. Показано, что на фоне длительного введения ГК-1 физиологический раствор не оказывал какого-либо влияния на частоту сердечных сокращений, тогда как у 5 из 8 животных в ответ на изопротеренол происходило не увеличение, а урежение частоты сердечных сокращений, у одного животного реакция отсутствовала, у одного была на 50% менее выраженной и лишь у одного животного реакция на изопротеренол сохранилась - соответственно, 11 и 13% (рисунок). Выявленные различия статистически достоверны (Р<0,025).
Описание рисунка
На рисунке отображена хронотропная реакция сердца (ЧСС) бодрствующих морских свинок (n=8) на изопротеренол (75 мкг/кг) на фоне хронического введения соединения ГК-1 (1,5 мг/кг, в/б). Обозначения: по оси ординат: % изменения ЧСС в ответ на введение изопротеренола; по оси абсцисс: каждая пара столбиков - реакция на изопротеренол отдельного животного; левый столбик - контроль; правый столбик - реакция на изопротеренол на 10-й день введения соединения ГК-1.
Применение дипептидного антагониста фактора роста нервов - амида N-сукцинил-L-глутамил-L-лизина в качестве антиаритмического и антифибрил-ляторного средства и средства для предотвращения внезапной коронарной смерти.