Результат интеллектуальной деятельности: ПРОМЫШЛЕННЫЙ СПОСОБ ПОЛУЧЕНИЯ И ОЧИСТКИ РЕКОМБИНАНТНОГО ИНТЕРФЕРОНА β-1b ЧЕЛОВЕКА ИЗ ТЕЛЕЦ ВКЛЮЧЕНИЯ
Вид РИД
Изобретение
Изобретение относится к биотехнологии, в частности к промышленному способу получения рекомбинантного человеческого бета-интерферона 1b из телец включения и его очистки.
Интерферон бета человека (INF-β) или фибробластный интерферон секретируется, в основном, фибробластами и является гликопротеином с молекулярной массой около 20 кДа. Его структура обозначается как INF-β-1a. Пептидная часть INF-β-1a представлена 166 аминокислотными остатками. Молекула содержит свободную сульфгидрильную группу цистеина в положении Cys16 и одну внутримолекулярную дисульфидную связь в положении Cys30-Cys140.
Известные лекарственные препараты на основе INF-β-1a получают экспрессией природного гена интерферона (β в клетках млекопитающих. Рекомбинантный INF-β-1a полностью идентичен природному фибробластному интерферону [Mazdeh M., Afzali S., Jaafari MR. The therapeutic effect of Avonex, Rebif and Betaferon on EDSS and relapse in multiple sclerosis: a comparative study. ActaMedIran., 2010, Mar-Apr; V. 48(2), p.83-88].
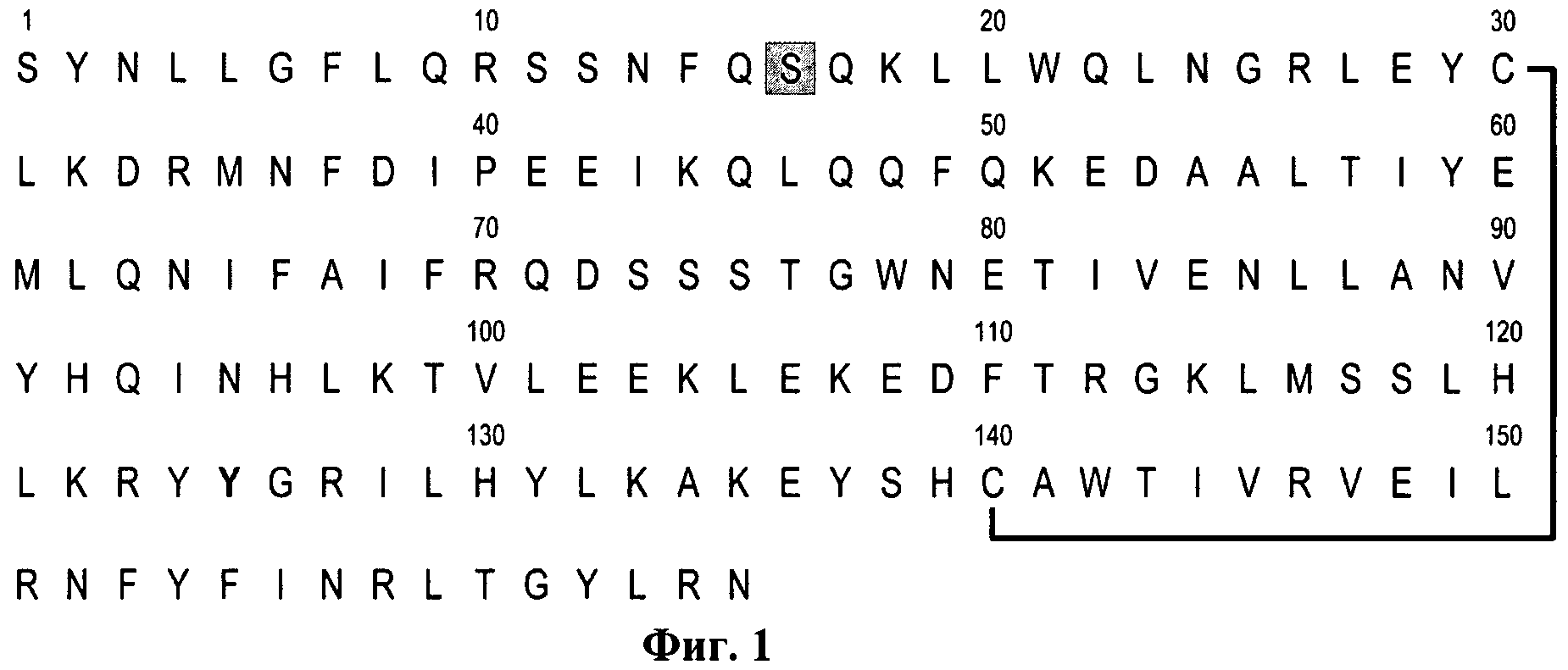
Поскольку гликозилирование белковой молекулы незначительно влияет на биологическую активность белка [Plosker G.L. Interferon-β-1b: a review of its use in multiple sclerosis. CNS Drugs, 2011, Jan 1; V.25(1), p.67-88], то взамен дорогостоящей экспрессии в клетках млекопитающих можно использовать экспрессию в бактериальных клетках, которая является более производительной и менее трудоемкой. Рекомбинантный интерферон бета, получаемый в бактериальной системе, представляет собой негликозилированный белок, имеющий замену цистеина в положении 16 на серин (Фиг.1). Эта замена устраняет проблему образования димеров за счет неправильного замыкания дисульфидных связей [Mark D.F., Lu S.D., Creasey A.A. Yamamoto R., Lin L.S. Site-specific mutagenesis of the human fibroblast interferon gene. Proc. Natl. Acad. Sci USA, 1984, Sep; 81(18):5662-6]. Такая структура фибробластного интерферона носит название INF-β-1b.
Данный белок взаимодействует со специфическими рецепторами, расположенными на поверхности клеток человека [Stark G.R., Kerr I.M., Williams В.R., Silver-man R.H., Schreiber R.D. How cells respond to interferons. Annual. Review of Biochemistry, 1998, V. 67, p.227-264], инактивирует рецепторы, чувствительные к γ-интерфepoну, активирует функцию Т-супрессоров, ослабляет действие антител к основным компонентам миелина, подавляет репликацию вирусов [Fensteri V., Sen G.С. Interferons and viral infections. Biofactors, 2009, Jan-Feb; 35(1):14-20].
Основным терапевтическим эффектом INF-β-1b является противовирусная и иммуномодулирующая активность, снижение частоты обострений рассеянного склероза с ремиттирующим течением на одну треть и уменьшением количеств новых очагов поражения головного мозга. Кроме того, снижается частота обострений при вторично-прогрессирующем течении рассеянного склероза и уменьшается выраженность атрофии головного мозга [Vartanian Т. An examination of the results of the evidence, incoming, and phase III studies of interferon beta products in the treatment of multiple sclerosis. Clin. Ther., 2003, V.25(1), p.105-118].
Создание штамма-продуцента человеческого интерферона бета-1b позволило получать биологически активный белок в количестве, необходимом как для проведения различных структурно-функциональных исследований, так и для использования в медицинской практике. За рубежом созданы лекарственные препараты на основе рекомбинантного интерферона бета-1b (экставиа, бетаферон и др.) для снижения частоты обострений рассеянного склероза, замедления нарастания инвалидизации, уменьшения образования новых очагов поражения головного мозга и его атрофии, а также для лечения иммунных заболеваний.
В связи с этим задача разработки эффективных и экономически выгодных способов получения рекомбинантного интерферона бета-1b является актуальной.
Известны способы получения рекомбинантного интерферона бета-1b, но все они трудоемки, дорогостоящи, описаны для аналитических количеств белка, а их масштабирование неэффективно для производства коммерчески доступных лекарственных средств [патенты США №5066786, №4485017; Lin L.S, Yamamoto R., Drummond RJ. Purification of recombinant human interferon beta expressed in Escherichia coli. Methods Enzymol, 1986, V.119, p.183-92 и др.]. Все эти способы используют стандартные схемы выделения, которые включают в себя солюбилизацию в буферных системах, содержащих хаотропные агенты или ионные детергенты в достаточно высоких концентрациях, которые сильно затрудняют очистку белка на последующих стадиях.
Известен способ очистки интерферона бета (патент США №5814485), включающий многостадийную отмывку телец включения с помощью мочевины и неионных детергентов, а также солюбилизацию в додецилсульфате натрия (ДДСН). Этот способ позволяет получить белок с выходом 0.2 г из 1 г целевого белка, экстрагированного из телец включения. Биологическая активность препарата по ингибированию цитопатического эффекта составляет 32×106 МЕ/мг белка. Недостатками этого способа является использование многостадийной отмывки телец включения, что приводит к значительным потерям белка, а также применение ДДСН, которое нежелательно, т.к. может вызывать денатурацию белка, что усложняет последующую хроматографическую очистку, а также требует дополнительного сложного анализа готового продукта на содержание ДДСН.
Наиболее близким к заявленному способу является способ (патент РФ №2392282), позволяющий получить интактный нативный рекомбинантный интерферон бета-1b, который включает несколько стадий: отмывку телец включения с помощью 2% водного раствора цвиттергента 3-14, солюбилизацию в 7М гуанидин хлориде, проведение рефолдинга с помощью добавления в реакционную смесь окисленного и восстановленного глутатиона, очистку белка на сорбенте HyperD Ceramic S, ионообменном сорбенте Source S30 и последующую хроматографическую очистку с помощью эксклюзивной гель-фильтрации на геле Sephacryl S-200 HR. Данный способ позволяет получить из 37,6 г целевого белка, выделенного из телец включения, 3,76 г рекомбинантного интерферона бета-1b с чистотой по ВЭЖХ 96,5%. Биологическая активность препарата по ингибированию цитопатического эффекта составляет 32×106ME/мг белка.
Недостатком способа-прототипа является то, что использование отмывок телец включения приводит к большим потерям белка - до 40% от начального количества. Еще одним недостатком данного способа является необходимость концентрирования образца с помощью ультрафильтрации перед стадиями хроматографической очистки белка, что при масштабировании процесса приводит также к большим потерям белка.
Техническим результатом заявленного изобретения является упрощение технологии получения и очистки рекомбинантного интерферона бета-1b человека.
Указанный технический результат достигается осуществлением заявленного способа получения и очистки рекомбинантного интерферона бета-1b человека, включающего следующие последовательные стадии.
Тельца включения рекомбинантного интерферона бета-1b человека промывают раствором 0,3% трифторуксусной кислоты (ТФУ). Экстракцию целевого белка проводят раствором 1-пропанол:вода (1:1) с добавлением 0,3% ТФУ.
Хроматографическую очистку экстрагированного белка проводят на обращенно-фазовой колонке, упакованной сорбентом YMC-GEL Butyl C4 (YMC, Japan), представляющим собой силикагель с привитой алкилсилильной группой. Сорбированный белок элюируют в градиенте концентрации от 20 до 50% 1-пропанола. Нагрузка белка на сорбент может достигать 40 мг суммарного белка на 1 мл носителя. Фракции, содержащие целевой белок по результатам анализа на обращенно-фазовой колонке C4, объединяют.
Из фракции, собранной с обращенно-фазовой колонки, высаживают белок добавлением равного объема буферного раствора, содержащего 50 мМ Na2HPO4, и доведением рН полученного раствора до 6,0. Полученный осадок растворяют в 200 мл буферного раствора, содержащего 1% лаурат натрия, 50 мМ Na2HPO4, pH 7.0, добавляют 10 мкМ сульфата меди, предварительно растворенной в аммиаке.
Далее раствор наносят на колонку, упакованную гелем Sephadex G-25 Fine (JE Healthcare, USA). Из фракции, собранной с колонки, высаживают белок внесением дигидрофосфата натрия до суммарной концентрации реактива в растворе 50 мМ и доведением pH раствора до 6,0.
Полученный осадок гомогенизируют в буферном растворе, содержащем 100 мМ NaH2PO4, pH 4,2, прогревают до 65°С, добавляют равный объем предварительно нагретого до 65°С 75% раствора фенола в воде, инкубируют в течение 20 минут в термошейкере при 65°С. Затем реакционную смесь охлаждают до 10°С, добиваясь полного расслоения фаз, и убирают водную фазу.
Полученный раствор белка в феноле разбавляют в 6.5 раз 30% этиловым спиртом, добавляют ТФУ до концентрации 0,1% и наносят на обращенно-фазовую колонку, упакованную сорбентом C18 (YMC, Japan). Сорбированные белки элюируют в градиенте концентрации 1-пропанола (от 20 до 50%). Фракции, содержащие целевой белок по результатам анализа на обращенно-фазовой колонке C18, объединяют.
Раствор целевого белка наносят на колонку, упакованную гелем Sephadex G-25 Fine (JE Healthcare, USA). В полученной фракции белка определяют концентрацию с помощью обращенно-фазовой хроматографии на колонке C18.
В результате получают 0,3 г рекомбинантного интерферона бета-1b с чистотой по ВЭЖХ 96,5% из 1 г целевого белка, полученного из телец включения.
Заявленный способ имеет следующие преимущества.
- Экстракция интерферона бета-1b из телец включения в раствор 50% 1-пропанола с добавлением 0,3% трифторуксусной кислоты исключает стадии отмывок телец включения различными буферными растворами, содержащими детергенты и хаотропные агенты, и длительного центрифугирования. Такой подход помогает значительно сократить потери белка. Данная экстракция позволяет избирательно экстрагировать целевой белок на 75-80%.
- Проведение рефолдинга в буферном растворе фосфата натрия, лаурата натрия и сульфата меди упрощает дальнейшую очистку белка, так как лаурат натрия легко удаляется из раствора с помощью гель-фильтрации на сефадексе G-25 при щелочных значениях рН.
- Применение сульфата меди, растворенного в аммиаке, позволяет провести процесс окисления белка в течение часа.
- Все стадии хроматографической очистки не требуют концентрирования белка.
- Очистка белка от эндотоксинов, ДНК штамма-продуцента и белков штамма продуцента проводится в одну стадию с помощью экстракции белка из водного раствора 75% раствором фенола в воде. Данный вид очистки позволяет полностью удалить бактериальные эндотоксины (до концентрации менее 1ЕЭ/мл), белки штамма продуцента (до концентрации менее 0,03 нг/мкг интерферона-бета 1b) и ДНК штамма-продуцента (до уровня не более 40 пг/мг).
- Применение фенольной экстракции белка из водной фазы с последующей очисткой на обращенно-фазовом сорбенте позволяет полностью избавиться от лаурата натрия.
Высокоочищенный белок INF-β-1b, полученный в результате применения заявленного способа, может быть использован для производства лекарственных препаратов в медицинской промышленности.
Краткое описание фигур
1. На фиг.1 представлено графическое изображение первичной аминокислотной последовательности рекомбинантного человеческого интерферона-бета 1b. Утолщенной сплошной линией показана дисульфидная связь между Cys30 и Cys140. Серым цветом выделено положение замены Cys16 на Ser16.
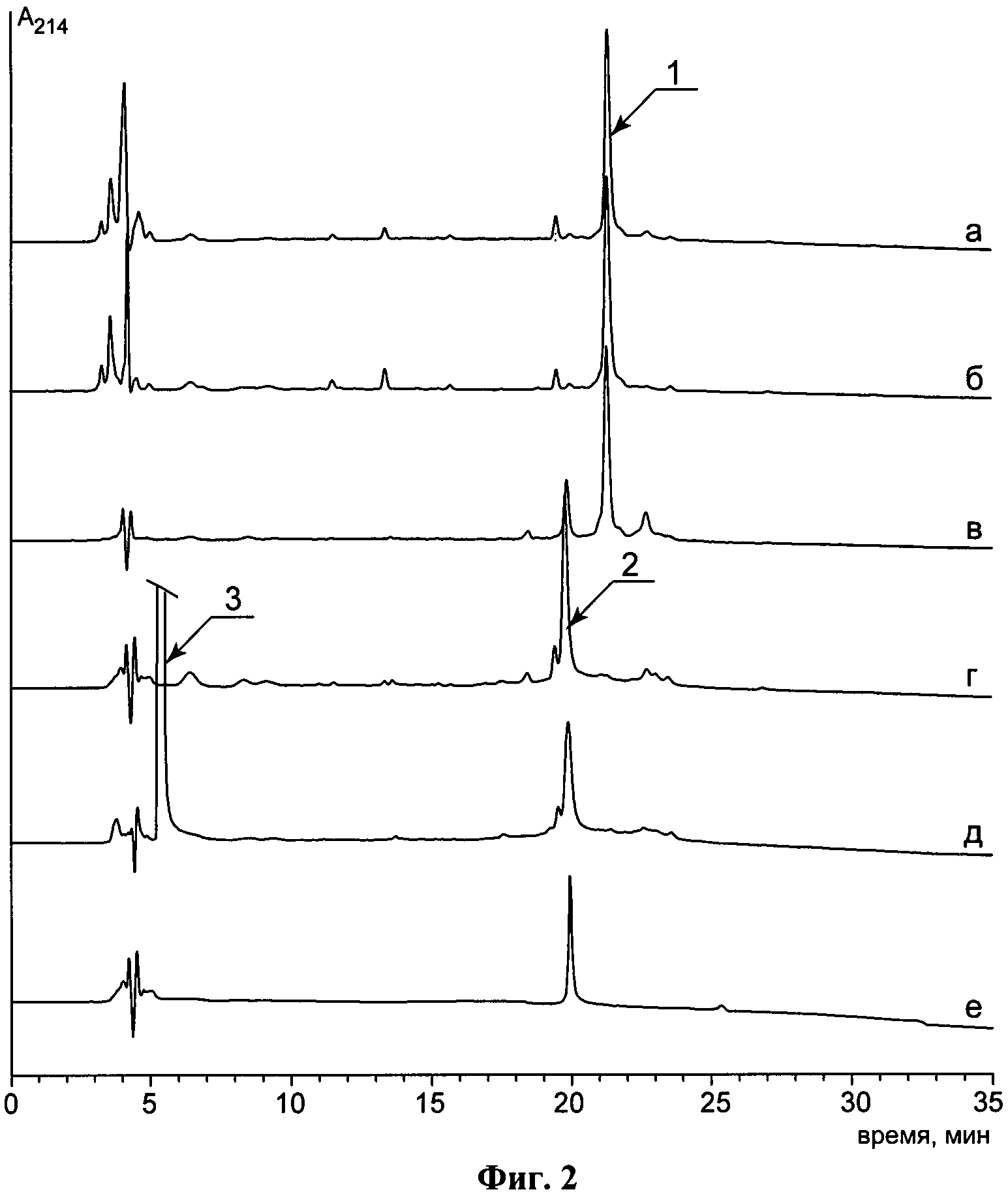
На фиг.2 представлено графическое изображения ОФВЭЖХ анализа основных проб, отобранных на каждой стадии процесса очистки интерферона β-1b из телец включения:
а - 1-стадия: экстракция IFN-β-1b из ТВ 50% 1-пропанолом в 0,3% ТФУ;
б - 2 стадия: хроматографическая очистка IFN-β-1b на ОФ сорбенте C4 300Å;
в - 3 стадия: растворение IFN-β-1b в буферном растворе, содержащем 1% лаурат натрия, 50 мМ Nа2НРO4 при рН 9.0;
г - 4 стадия: ренатурация IFN-β-1b в буферном растворе, содержащем 1% лаурата натрия, 50 мМ Na2HPO4 при рН 9.0, в присутствии 10 мкМ сульфата меди, предварительно растворенной в 30% аммиаке;
д - 5 стадия: очистка IFN-β-1b фенолом;
е - 6 стадия: хроматографическая очистка IFN-β-1b на ОФ сорбенте C18 300Å;
1 - восстановленный IFN-β-1b; 2 - нативный IFN-β-1b; 3 - фенол.
Изобретение иллюстрируется следующими примерами.
Пример 1. Получение высокоочищенного рекомбинантного интерферона бета - 1b человека.
К 150 телец включения рекомбинантного интерферона бета-1b человека приливают 1000 мл раствора, который содержит 0,3% трифторуксусной кислоты (ТФУ). После этого тельца включения гомогенизируют в блендере со скоростью 800 об/мин в течение 1 мин, переносят в стакан с магнитной мешалкой и оставляют перемешиваться в течение 1 ч при температуре 4°С. Далее полученную суспензию центрифугируют при 4°С в течение 40 минут на скорости 10000 об/мин. Полученный осадок переносят в блендер, заливают 1,0 л раствора 1-пропанола:вода (1:1) с добавлением 0,3% ТФУ, гомогенизируют со скоростью 800 об/мин в течение 1 минуты, охлаждают раствор при -20°С в течение 20-30 минут и ставят перемешиваться при 4°С на 1-2 часа.
Полученный экстракт центрифугируют при 4°С в течение 40 минут на скорости 10000 об/мин. Затем полученный супернатант фильтруют через стекловолокно и разбавляют раствором, содержащим 0,3% ТФУ до концентрации 1-пропанола 20%.
На следующем этапе экстракт белка наносят на обращенно-фазовую колонку DAU-100 (размер колонки 10×10 см) (YMC Co., LTD, Japan), упакованную сорбентом GEL-Butyl C4 (YMC Co., LTD, Japan) и уравновешенную раствором, содержащим 0,1% ТФУ и 20% 1-пропанол. Нагрузка на сорбент может достигать 40 мг суммарного белка на 1 мл носителя. После нанесения раствора белка колонку промывают начальным раствором ТФУ и 1-пропанола до показания спектрофотометром значений, равных значениям базовой линии при длине волны 280 нм. Сорбированные белки элюируют в градиенте концентрации 1-пропанола (от 20 до 50%) при длине волны 280 нм. Фракции, содержащие целевой белок по результатам анализа на обращенно-фазовой колонке C4, объединяют. Из объединенной фракции, собранной с обращенно-фазовой колонки, высаживают белок добавлением равного объема буферного раствора, содержащего 50 мМ Nа2НРO4, и доведением рН полученного раствора до 6,0.
Затем суспензию белка центрифугируют с использованием центрифуги при 4°С в течение 30 минут на скорости 14000 об/мин. Полученный осадок размешивают в 400 мл такого же буферного раствора и снова центрифугируют при аналогичных условиях.
Далее осадок растворяют в 200 мл буферного раствора, содержащего 1% лаурат натрия, 50 мМ Na2HPO4, рН 7.0, добавляют 10 мкМ сульфата меди, предварительно растворенной в аммиаке, и оставляют перемешиваться в течение 1 ч.
Затем раствор наносят на колонку BPG 200/500 (размер колонки 20×30 см) (JE Healthcare, USA), упакованную гелем Sephadex G-25 Fine (JE Healthcare, USA) и уравновешенную раствором 10 мМ NaOH. Элюирование ведут в изократическом режиме при длине волны 280 н.м. Из фракции, собранной с колонки, высаживают белок внесением дигидрофосфата натрия до суммарной концентрации реактива в растворе 50 мМ и доведением рН раствора до 6,0 и проводят центрифугирование суспензии белка с использованием центрифуги при 4°С в течение 30 минут при скорости 14000 об/мин.
Полученный осадок гомогенизируют в буферном растворе, содержащем 100 мМ NaH2PO4, pH 4,2 и прогревают до 65°С, добавляют равный объем предварительно нагретого до 65°С 75% раствора фенола в воде. Проводят инкубацию в течение 20 минут в термошейкере при 65°С. Затем реакционную смесь охлаждают до 10°С, добиваясь полного расслоения фаз, и убирают водную фазу с помощью водоструйного насоса.
Полученный раствор белка в феноле разбавляют в 6.5 раз 30% этиловым спиртом, добавляют ТФУ до 0,1% и наносят на обращенно-фазовую колонку DAU-50 (размер колонки 5×20 см) (YMC Co., LTD, Japan), упакованную сорбентом С18 (YMC Co., LTD, Japan) и уравновешенную раствором, содержащим 0,1% ТФУ и 20% 1-пропанол. Нагрузка на сорбент может достигать 40 мг суммарного белка на 1 мл носителя. После нанесения раствора белка колонку промывают начальным раствором ТФУ и 1-пропанола до показания спектрофотометром значений, равных значениям базовой линии при длине волны 280 нм. Сорбированные белки элюируют в градиенте концентрации 1-пропанола (от 20 до 50%) при длине волны 280 нм. Фракции, содержащие целевой белок по результатам анализа на обращенно-фазовой колонке С18, объединяют.
Раствор целевого белка наносят на колонку BPG 200/500 (размер колонки 20×30 см) (JE Healthcare, USA), упакованную гелем Sephadex G-25 Fine (JE Healthcare, USA) и уравновешенную раствором 10 мМ NaOH. Элюирование ведут в изократическом режиме при длине волны 280 нм. В полученной фракции белка определяют концентрацию с помощью обращенно-фазовой хроматографии на колонке C18.
Выход готового продукта с 1 г целевого белка, полученного при экстракции на первом этапе из телец включения, составляет 0,3 г целевого белка. Чистота белка - не менее 98%. Материальный баланс промышленного процесса очистки интерферона-бета 1b представлен в Таблице 1.
|
Пример 2. Анализ рекомбинантного белка интерферона-бета 1b
Анализ полученного интерферона-бета 1b проводят с помощью обращенно-фазовой хроматографии в градиенте концентрации ацетонитрила (от 40 до 70%) в присутствии 0,1% ТФУ на колонке С4, с размером частиц сорбента 5 мкм и размером пор сорбента 300А (YMC Co., LTD, Japan). Продукт элюируется одним пиком, чистота продукта составляет не менее 98% (фиг.2).
Белок дает положительную реакцию с моноклональными антителами к интерферону-бета 1b при проведении иммуноферментного анализа.
Специфическая биологическая активность интерферона-бета 1b определялась стандартным способом по способности подавлять деление клеток линии Дауди (лимфома Беркита человека), определяемой по изменению интенсивности окрашивания содержимого лунок планшета после обработки хромогенным субстратом. Для этого линию клеток Дауди культивируют в суспензии на среде Д, которая содержит 224 мл среды питательной RPMI-1640 (ПанЭко), 25 мл эмбриональной телячьей сыворотки (Highclon, США,), 2,5 мл раствора глутамина (ПанЭко) и 0,25 мл раствора гентамицина, в пластиковых флаконах площадью 25 см2, в инкубаторе, заполненном углекислым газом в объеме 5%, при температуре 37±2°С и относительной влажности ≥90%. Плотность клеточной суспензии должна быть в пределах 0,6-1 миллиона клеток в мл.
Затем в лунки 96-луночного планшета вносят по 100 мкл среды Д, кроме 1-й колонки. Далее в четыре верхние лунки первой колонки (A1 - D1) вносят по 200 мкл стандартного раствора, а в четыре нижние лунки (Е1 - H1) - по 200 мкл испытуемого раствора.
Далее готовят ряд последовательных двукратных разведений стандартного и испытуемого растворов. Для этого из каждой лунки первой колонки переносят по 100 мкл в соответствующие лунки второй колонки (А1→А2, B1→B2, H1→H2), после пипетирования повторяют процедуру вплоть до 11-й колонки, из которой после перемешивания отбирают и удаляют 100 мкл. Последняя 12-я колонка содержит среду без интерферона.
После этого во все лунки планшета приливают по 100 мкл суспензии клеток Дауди (300 тыс.клеток/ мл среды) и выдерживают 72 ч в СО2 - инкубаторе, заполненном углекислым газом в объеме 5%, при температуре 37±2°С и относительной влажности ≥90%. Затем в каждую лунку добавляют по 20 мкл раствора АламарБлю (Biosource, США, кат. № DAL1025 или аналогичного качества) и инкубируют 18 ч при описанных выше условиях. Интерферон подавляет клеточную пролиферацию, соответственно, чем выше его концентрация, тем менее окрашена суспензия клеток Дауди. Изменение окраски оценивают спектрофотометрически при длинах волн 530 и 595 нм.
Полученные данные анализируют методом эквивалентных доз (ГФ XI, вып.1, стр.226). Специфическая биологическая активность интерферона-бета 1b составляла 95-105% по сравнению с международным стандартным образцом интерферона-бета 1b (Interferon Beta Ser 17 Mutein, Human, rDNA derived, NIBC code:00/574), что составляет 32×106ME/мг.
Пример 3. Масштабирование процесса очистки интерферона бета-1b.
|
Данные, приведенные в Таблице 2, были получены на 10 опытно-промышленных сериях препарата.