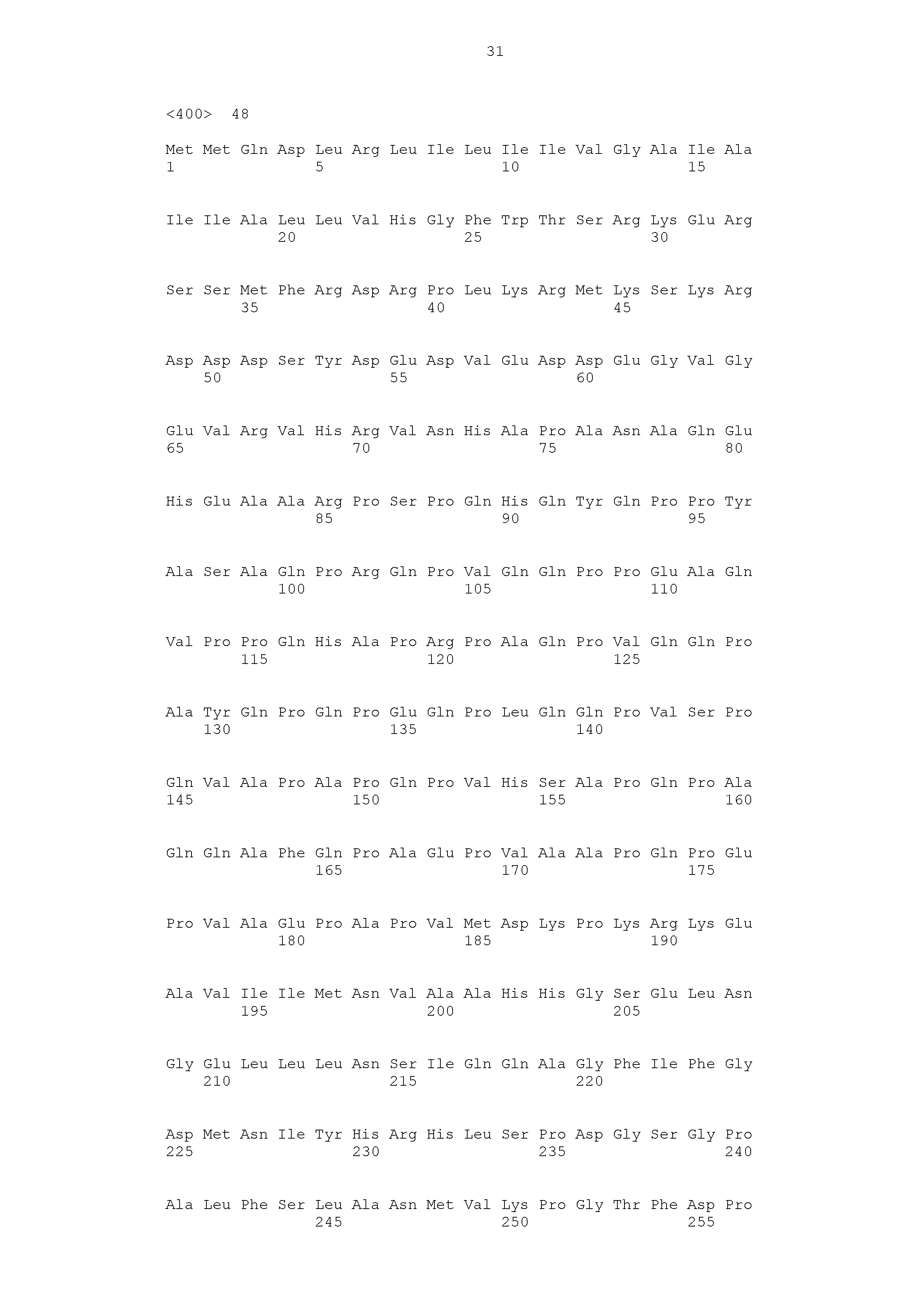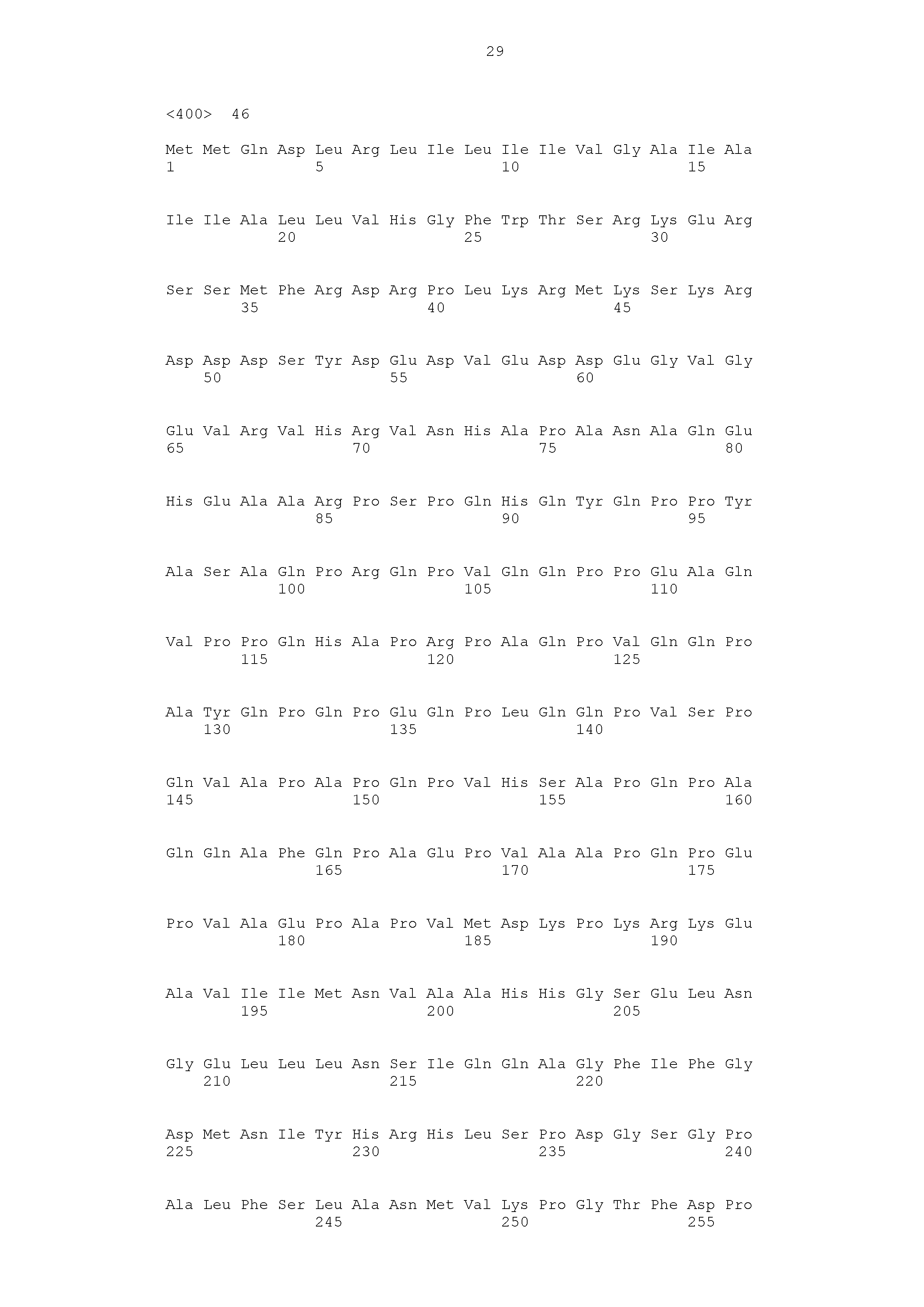Результат интеллектуальной деятельности: РЕКОМБИНАНТНЫЙ МИКРООРГАНИЗМ ДЛЯ УЛУЧШЕННОГО ПОЛУЧЕНИЯ ХИМИЧЕСКИХ ВЕЩЕСТВ ТОНКОГО ОРГАНИЧЕСКОГО СИНТЕЗА
Вид РИД
Изобретение
Согласно настоящей заявке испрашивается приоритет в соответствии с патентными заявками №№61/881968, 61/881969, 61/881975 и 61/881972, все из которых поданы 25 сентября 2013 г. и полностью включены в настоящий документ посредством ссылки.
Область изобретения
Настоящее изобретение относится к рекомбинантной молекуле нуклеиновой кислоты, рекомбинантному микроорганизму, способу получения аланина, пирувата, сукцината, аспартата, малата, лактата, валина и/или лейцина и применению рекомбинантной молекулы нуклеиновой кислоты или рекомбинантного микроорганизма для ферментативного получения аланина, пирувата, сукцината, аспартата, малата, лактата, валина и/или лейцина.
Описание изобретения
Аминокислоты представляют собой органические соединения с карбокси-группой и амино-группой. Наиболее важные аминокислоты представляют собой альфа-аминокислоты, в которых амино-группа расположена рядом с карбокси-группой. Белки состоят из альфа-аминокислот.
Алании вызвал значительный интерес, поскольку использовался в качестве добавки к пище, корму и в фармацевтической промышленности. Более того, аланин представляет собой сырьевой материал для промышленного производства тринатриевой соли N,N-бис(карбоксиметил)-аланина (MGDA, торговое название Trilon M), который представляет собой сильное хелатирующее средство, демонстрирующее превосходное действие при растворении органических и неорганических твердых осадков (международные патентные публикации №№WO 94/29421, WO 2012/150155). Сорта Trilon M легко подвергаются биологическому разложению согласно стандартным тестам OECD (ОЭСР, Организация экономического сотрудничества и развития). Благодаря своему превосходному экологическому и токсикологическому профилю сорта Trilon M являются особенно подходящими для применения в продуктах для конечных потребителей, и потребность в компоненте такого биологически разлагаемого комплекса постоянно растет.
Алании может быть получен путем ферментации с помощью Coryneform bacteria (Hermann, 2003: Industrial production of amino acids by Coryneform bacteria, J. of Biotechnol, 104, 155-172) или с помощью Ε. coli (международные патентные публикации №№WO 2007/120198, WO 2008/119009).
В отношении Е. coli недавно было описано, что избыточная экспрессия гена ygaW улучшает ферментативную производительность аланина микроорганизмом (международная патентная публикация №WO 2012/172822).
Производство аланина в Е. coli является более эффективным и широко используется для промышленного получения аланина в качестве сырьевого материала для химической промышленности. Поскольку в химической промышленности увеличивается потребность в аланине, существует необходимость в улучшении производительности ферментативного получения аланина.
Одной задачей настоящего изобретения является обеспечение микроорганизмов, которые можно использовать в ферментативном получении аланина с высоким выходом и продуктивностью.
Подробное описание изобретения
Вклад в достижение вышеупомянутой цели обеспечивается с помощью рекомбинантного микроорганизма семейства Escherichia coli (Ε. coli), характеризующегося, по сравнению с соответствующим микроорганизмом сравнения, по меньшей мере одним из следующего: i) введенная, увеличенная или усиленная активность и/или экспрессия гена lpd ген, и/или ii) введенная, увеличенная, усиленная или измененная активность и/или экспрессия гена zipA и/или iii) ген ygaW, содержащий мутацию в кодоне в положении 13-15 SEQ ID NO: 1 или в соответствующем кодоне функциональных эквивалентов SEQ ID NO: 1, причем мутация изменяет активность и/или экспрессию транспортера аланина, кодируемого геном ygaW.
Термин "повышенная", "увеличение" или "усиленная", например, в отношении экспрессии и/или активности фермента или выхода или производительности, означает значительно повышенную, увеличенную или усиленную экспрессию и/или активность или выход или производительность.
Термин "сниженная, репрессированная или удаленная экспрессия и/или активность фермента" означает значительно сниженную, репрессированную или удаленную экспрессию и/или активность, а также включает в себя не обнаруживаемую экспрессию и/или активность соответствующих ферментов.
Термин "измененная" экспрессия и/или активность фермента означает экспрессию и/или активность фермента у рекомбинантного микроорганизма, которая значительно отличается от экспрессии и/или активности соответствующего фермента у не рекомбинантного микроорганизма дикого типа.
Неожиданно было обнаружено, что микроорганизм, характеризующийся по меньшей мере одним из следующего i) введенная, увеличенная или усиленная активность и/или экспрессия белка, кодируемого геном lpd и/или ii) введенная, увеличенная, усиленная или измененная активность и/или экспрессия белка, кодируемого геном zipA и или iii) ген ygaW, содержащий мутацию в положении 13-15 SEQ ID NO: 1 или в соответствующем положении его гомолога или функционального эквивалента, характеризуется повышенным выходом и/или производительностью аланина в ферментативном получении по сравнению с таким же микроорганизмом, не характеризующимся введенной, увеличенной или усиленной активностью и/или экспрессией соответствующего гена lpd и/или введенной, увеличенной, усиленной или измененной активностью и/или экспрессией соответствующего гена zipA и/или геном ygaW, не содержащим соответствующую мутацию.
Соответственно, согласно одному варианту осуществления настоящего изобретения предусмотрен рекомбинантный микроорганизм, содержащий по сравнению с соответствующим микроорганизмом сравнения по меньшей мере одно из следующего i) введенная, увеличенная или усиленная активность и/или экспрессия гена lpd, кодирующего белок липоамиддегидрогеназу и/или ii) введенная, увеличенная, усиленная или измененная активность и/или экспрессия гена zipA, кодирующего белок клеточного деления, вовлеченный в сборку Z-кольца и/или iii) ген ygaW, содержащий мутацию в кодоне в положении 13-15 SEQ ID NO: 1 или в соответствующем кодоне функциональных эквивалентов SEQ ID NO: 1, причем мутация изменяет активность и/или экспрессию транспортера аланина, кодируемого геном ygaW, и характеризующийся по сравнению с соответствующим микроорганизмом сравнения повышенным выходом и/или производительностью аланина в ферментативном получении.
Согласно одному варианту осуществления настоящего изобретения рекомбинантный микроорганизм, содержащий по сравнению с соответствующим микроорганизмом сравнения по меньшей мере одно из следующего i) введенная, увеличенная или усиленная активность и/или экспрессия гена lpd, кодирующего белок липоамиддегидрогеназу и/или ii) введенная, увеличенная, усиленная или измененная активность и/или экспрессия гена zipA, кодирующего белок клеточного деления, вовлеченный в сборку Z-кольца и/или iii) ген ygaW, содержащий мутацию в кодоне в положении 13-15 SEQ ID NO: 1 или в соответствующем кодоне функциональных эквивалентов SEQ ID NO: 1, причем мутация изменяет активность и/или экспрессию транспортера аланина, кодируемого геном ygaW, и характеризующийся по сравнению с соответствующим микроорганизмом сравнения повышенным выходом и/или производительностью аланина в ферментативном получении, дополнительно характеризуется удаленными и введенными ферментативными активностями, как описано в международных патентных публикациях №№WO 2007/120198 и WO 2008/119009, которые включены в настоящий документ посредством ссылки.
Используемый в настоящем документе термин "микроорганизм сравнения" означает контрольный микроорганизм, с которым сравнивают рекомбинантный микроорганизм. Указанный микроорганизм сравнения характеризуется по существу таким же генотипом, как и рекомбинантный микроорганизм, за исключением подлежащего анализу различия. Микроорганизм сравнения предпочтительно представляет собой штамм, из которого происходит рекомбинантный микроорганизм. Например, ген был введен в микроорганизм дикого типа, таким образом, создавая рекомбинантный микроорганизм, в этом случае дикий тип будет представлять собой подходящий микроорганизм сравнения для указанного рекомбинантного микроорганизма. Также возможно, чтобы в рекомбинантный микроорганизм А была введена дополнительная мутация, тем самым создавая рекомбинантный микроорганизм В. Рекомбинантный микроорганизм А, таким образом, будет представлять собой подходящий микроорганизм сравнения для рекомбинантного микроорганизма В. В случае, если необходимо сравнить производительность рекомбинантного микроорганизма и соответствующего микроорганизма сравнения, оба микроорганизма выращивают при по существу идентичных условиях.
Специалисту в настоящей области техники очевидно, что микроорганизм, характеризующийся увеличенным выходом и/или производительностью аланина, также можно использовать для получения других метаболитов, которые являются близкородственными аланину, например, метаболиты, которые представляют собой промежуточные вещества в метаболическом пути аланина, которые характеризуются общими промежуточными веществами с метаболическим путем аланина или которые представляют собой метаболиты, которые используют аланин в качестве промежуточного вещества в своих метаболических путях. Микроорганизмы согласно настоящему изобретению также можно легко приспособить для увеличенного выхода и/или производительности таких родственных метаболитов путем увеличения или введения определенных ферментативных активностей или путем нокаута или уменьшения определенных ферментативных активностей.
Такие метаболиты, например, представляют собой пируват, сукцинат, аспартат, малат, лактат, валин и лейцин.
Например, для использования рекомбинантного микроорганизма согласно настоящему изобретению для получения сукцината, гены ldh, pfl, pta и adhE должны быть подвергнуты нокауту, и ген РЕР-карбоксилазы и/или ген пируваткарбоксилазы должны быть введены в геном микроорганизма согласно настоящему изобретению. Соответствующий путь и необходимые мутации описаны, например, в Zhang et al. (2009), PNAS (106) pp 20180-20185.
Соответственно, согласно другому варианту осуществления настоящего изобретения предусмотрен рекомбинантный микроорганизм, содержащий по сравнению с соответствующим микроорганизмом сравнения по меньшей мере одно из следующего i) введенная, увеличенная или усиленная активность и/или экспрессия гена lpd, кодирующего белок липоамиддегидрогеназу, и/или ii) введенная, увеличенная, усиленная или измененная активность и/или экспрессия гена zipA, кодирующего белок клеточного деления, вовлеченный в сборку Z-кольца и/или iii) ген ygaW, содержащий мутацию в кодоне в положении 13-15 SEQ ID NO: 1 или в соответствующем кодоне функциональных эквивалентов SEQ ID NO: 1, причем мутация изменяет активность и/или экспрессию транспортера аланина, кодируемого геном ygaW, и характеризующийся по сравнению с соответствующим микроорганизмом сравнения повышенным выходом и/или производительностью пирувата, сукцината, аспартата, малата, лактата, валина и/или лейцина в ферментативном получении.
Согласно некоторым вариантам осуществления микроорганизм представляет собой прокариотическую клетку. Подходящие прокариотические клетки включают в себя грамположительные, грамотрицательные и грамвариабельные бактериальные клетки, предпочтительно грамотрицательные.
Таким образом, микроорганизмы, которые можно использовать в настоящем изобретении, включают в себя без ограничения Gluconobacter oxydans, Gluconobacter asaii, Achromobacter delmarvae, Achromobacter viscosus, Achromobacter lacticum, Agrobacterium tumefaciens, Agrobacterium radiobacter, Alcaligenes faecalis, Arthrobacter citreus, Arthrobacter tumescens, Arthrobacter paraffineus, Arthrobacter hydrocarboglutamicus, Arthrobacter oxydans, Aureobacterium saperdae, Azotobacter indicus, Brevibacterium ammoniagenes, Brevibacterium divaricatum, Brevibacterium lactofermentum, Brevibacterium flavum, Brevibacterium globosum, Brevibacterium fuscum, Brevibacterium ketoglutamicum, Brevibacterium helcolum, Brevibacterium pusillum, Brevibacterium testaceum, Brevibacterium roseum, Brevibacterium immariophilium, Brevibacterium linens, Brevibacterium protopharmiae, Corynebacterium acetophilum, Corynebacterium glutamicum, Corynebacterium callunae, Corynebacterium acetoacidophilum, Corynebacterium acetoglutamicum, Enterobacter aerogenes, Erwinia amylovora, Erwinia carotovora, Erwinia herbicola, Erwinia chrysanthemi, Flavobacterium peregrinum, Flavobacterium fucatum, Flavobacterium aurantinum, Flavobacterium rhenanum, Flavobacterium sewanense, Flavobacterium breve, Flavobacterium meningosepticum, Micrococcus sp. CCM825, Morganella morganii, Nocardia opaca, Nocardia rugosa, Planococcus eucinatus, Proteus rettgeri, Propionibacterium shermanii, Pseudomonas synxantha, Pseudomonas azotoformans, Pseudomonas jluorescens, Pseudomonas ovalis, Pseudomonas stutzeri, Pseudomonas acidovolans, Pseudomonas mucidolens, Pseudomonas testosteroni, Pseudomonas aeruginosa, Rhodococcus erythropolis, Rhodococcus rhodochrous, Rhodococcus sp. ATCC 15592, Rhodococcus sp. ATCC 19070, Sporosarcina ureae, Staphylococcus aureus, Vibrio metschnikovii, Vibrio tyrogenes, Actinomadura madurae, Actinomyces violaceochromogenes, Kitasatosporia parulosa, Streptomyces avermitilis, Streptomyces coelicolor, Streptomyces flavelus, Streptomyces griseolus, Streptomyces lividans, Streptomyces olivaceus, Streptomyces tanashiensis, Streptomyces virginiae, Streptomyces antibioticus, Streptomyces cacaoi, Streptomyces lavendulae, Streptomyces viridochromogenes, Aeromonas salmonicida, Bacillus pumilus, Bacillus circulans, Bacillus thifminolyticus, Escherichia freundii, Microbacterium ammoniaphilum, Serratia marcescens, Salmonella typhimurium, Salmonella schottmulleri, Xanthomonas citri, Synechocystis sp., Synechococcus elongatus, Thermosynechococcus elongatus, Microcystis aeruginosa, Nostoc sp., N. commune, N. sphaericum, Nostoc punctiforme, Spirulina platensis, Lyngbya majuscula, L. lagerheimii, Phormidium tenue, Anabaena sp., Leptolyngbya sp и тому подобное.
Согласно некоторым вариантам осуществления микроорганизм представляет собой эукариотическую клетку. Подходящие эукариотические клетки включают в себя дрожжи клетки, как, например, виды Saccharomyces, такие как Saccharomyces cerevisiae, виды Hansenula, такие как Hansenula polymorpha, виды Schizosaccharomyces, такие как Schizosaccharomyces pombe, виды Kluyveromyces, такие как Kluyveromyces lactis и Kluyveromyces marxianus, виды Yarrowia, такие как Yarrowia lipolytica, виды Pichia, такие как Pichia methanolica, Pichia stipites и Pichia pastoris, виды Zygosaccharomyces, такие как Zygosaccharomyces rouxii и Zygosaccharomyces bailii, виды Candida, такие как Candida boidinii, Candida utilis, Candida freyschussii, Candida glabrata и Candida sonorensis, виды Schwanniomyces, такие как Schwanniomyces occidentalis, виды Arxula, такие как Arxula adeninivorans, виды Ogataea, такие как Ogataea minuta, виды Klebsiella, такие как Klebsiella pneumonia.
Различные бактериальные промышленные штаммы являются особенно подходящими для применения в способах, раскрытых в настоящем документе. Согласно некоторым вариантам осуществления микроорганизм представляет собой вид рода Corynebacterium, например, С. acetophilum, С. glutamicum, С. callunae, С. acetoacidophilum, С. acetoglutamicum. Согласно некоторым вариантам осуществления микроорганизм представляет собой вид рода Bacillus, например, В. thuringiensis, В. anthracis, В. megaterium, В. subtilis, В. lentils, В. circulans, В. pumilus, В. lautus, B. coagulans, В. brevis, В. firmus, В. alkaophius, В. licheniformis, В. clausii, В. stearothermophilus, В. halodurans, В. subtilis, В. pumilus, и В. amyloliquefaciens. Согласно некоторым вариантам осуществления микроорганизм представляет собой вид рода Erwinia, например, Е. uredovora, Ε. carotovora, Ε. ananas, Ε. herbicola, Ε. punctata и Ε. terreus. Согласно некоторым вариантам осуществления микроорганизм представляет собой вид рода Escherichia, например, Е. coli. Согласно другим вариантам осуществления микроорганизм представляет собой вид рода Pantoea, например, P. citrea или P. agglomerans. Согласно другим вариантам осуществления микроорганизм представляет собой вид рода Streptomyces, например, S. ambofaciens, S. achromogenes, S. avermitilis, S. coelicolor, S. aureofaciens, S. aureus, S. fungicidicus, S. griseus или S. lividans. Согласно дополнительным вариантам осуществления микроорганизм представляет собой вид рода Zymomonas, например, Z. mobilis или Z. lipolytica. Согласно дополнительным вариантам осуществления микроорганизм представляет собой вид рода Rhodococcus, например, R opacus.
Микроорганизм предпочтительно выбран из семейства Enterobacteriaceae, предпочтительно из рода Escherichia, например, Escherichia coli (Ε. coli), предпочтительно штамма Ε. coli W, который соответствует DSMZ 1116, который соответствует АТСС9637.
В дополнение к введенной, увеличенной или усиленной активности и/или экспрессии гена Lpd, кодирующего белок липоамиддегидрогеназу и/или введенной, увеличенной, усиленной или измененной активности и/или экспрессии гена zipA, кодирующего белок клеточного деления, вовлеченный в сборку Z-кольца и/или гену ygaW, содержащему мутацию в кодоне в положении 13-15 SEQ ID NO: 1 или в соответствующем кодоне функциональных эквивалентов SEQ ID NO: 1, причем мутация изменяет активность и/или экспрессию транспортера аланина, кодируемого геном ygaW, рекомбинантный микроорганизм согласно настоящему изобретению может дополнительно характеризоваться (а) сниженной, репрессированной или удаленной активностью и/или экспрессией гена pflB, кодирующего пируватформиатлиазу I, причем снижение, репрессию или удаление активности и/или экспрессии гена pflB определяют по сравнению с соответствующим микроорганизмом сравнения.
В дополнение к введенной, увеличенной или усиленной активности и/или экспрессии гена lpd, кодирующего белок липоамиддегидрогеназу, и/или введенной, увеличенной, усиленной или измененной активности и/или экспрессии гена zipA, кодирующего белок клеточного деления, вовлеченный в сборку Z-кольца, и/или гену ygaW, содержащему мутацию в кодоне в положении 13-15 SEQ ID NO: 1 или в соответствующем кодоне функциональных эквивалентов SEQ ID NO: 1, причем мутация изменяет активность и/или экспрессию транспортера аланина, кодируемого геном ygaW, рекомбинантный микроорганизм согласно настоящему изобретению может дополнительно характеризоваться (b) сниженной, репрессированной или удаленной активностью и/или экспрессией гена adhE, кодирующего бифункциональную ацетальдегид-СоА-дегидрогеназу/железозависимую алкогольдегидрогеназу/деактивазу пируватформиатлиазы, причем снижение, репрессию или удаление активности и/или экспрессии гена adhE определяют по сравнению с соответствующим микроорганизмом сравнения.
В дополнение к введенной, увеличенной или усиленной активности и/или экспрессии гена lpd, кодирующего белок липоамиддегидрогеназу, и/или введенной, увеличенной, усиленной или измененной активности и/или экспрессии гена zipA, кодирующего белок клеточного деления, вовлеченный в сборку Z-кольца, и/или гену ygaW, содержащему мутацию в кодоне в положении 13-15 SEQ ID NO: 1 или в соответствующем кодоне функциональных эквивалентов SEQ ID NO: 1, причем мутация изменяет активность и/или экспрессию транспортера аланина, кодируемого геном ygaW, рекомбинантный микроорганизм согласно настоящему изобретению может дополнительно характеризоваться (с) сниженной, репрессированной или удаленной активностью и/или экспрессией гена ldhA, кодирующего NAD-зависимую ферментативную D-лактатдегидрогеназу, причем снижение, репрессию или удаление активности и/или экспрессии гена ldhA определяют по сравнению с соответствующим микроорганизмом сравнения.
В дополнение к введенной, увеличенной или усиленной активности и/или экспрессии гена lpd, кодирующего белок липоамиддегидрогеназу, и/или введенной, увеличенной, усиленной или измененной активности и/или экспрессии гена zipA, кодирующего белок клеточного деления, вовлеченный в сборку Z-кольца, и/или гену ygaW, содержащему мутацию в кодоне в положении 13-15 SEQ ID NO: 1 или в соответствующем кодоне функциональных эквивалентов SEQ ID NO: 1, причем мутация изменяет активность и/или экспрессию транспортера аланина, кодируемого геном ygaW, рекомбинантный микроорганизм согласно настоящему изобретению может дополнительно характеризоваться (d) сниженной, репрессированной или удаленной активностью и/или экспрессией гена pta, кодирующего фосфатацетилтрансферазу, причем снижение, репрессию или удаление активности и/или экспрессии гена pta определяют по сравнению с соответствующим микроорганизмом сравнения.
В дополнение к введенной, увеличенной или усиленной активности и/или экспрессии гена lpd, кодирующего белок липоамиддегидрогеназу, и/или введенной, увеличенной, усиленной или измененной активности и/или экспрессии гена zipA, кодирующего белок клеточного деления, вовлеченный в сборку Z-кольца, и/или гену ygaW, содержащему мутацию в кодоне в положении 13-15 SEQ ID NO: 1 или в соответствующем кодоне функциональных эквивалентов SEQ ID NO: 1, причем мутация изменяет активность и/или экспрессию транспортера аланина, кодируемого геном ygaW, рекомбинантный микроорганизм согласно настоящему изобретению может дополнительно характеризоваться (е) сниженной, репрессированной или удаленной активностью и/или экспрессией гена frdA, кодирующего фумаратредуктазу, причем снижение, репрессию или удаление активности и/или экспрессии гена frdA определяют по сравнению с соответствующим микроорганизмом сравнения.
В дополнение к введенной, увеличенной или усиленной активности и/или экспрессии гена lpd, кодирующего белок липоамиддегидрогеназу, и/или введенной, увеличенной, усиленной или измененной активности и/или экспрессии гена zipA, кодирующего белок клеточного деления, вовлеченный в сборку Z-кольца, и/или гену ygaW, содержащему мутацию в кодоне в положении 13-15 SEQ ID NO: 1 или в соответствующем кодоне функциональных эквивалентов SEQ ID NO: 1, причем мутация изменяет активность и/или экспрессию транспортера аланина, кодируемого геном ygaW, рекомбинантный микроорганизм согласно настоящему изобретению может дополнительно характеризоваться (f) введенной, увеличенной или усиленной активностью и/или экспрессией гена alaD, кодирующего аланиндегидрогеназу, причем увеличение или усиление активности и/или экспрессии гена alaD определяют по сравнению с соответствующим микроорганизмом сравнения.
Рекомбинантный микроорганизм согласно настоящему изобретению, содержащий введенную, увеличенную или усиленную активность и/или экспрессию гена lpd, кодирующего белок липоамиддегидрогеназу, и/или введенную, увеличенную, усиленную или измененную активность и/или экспрессию гена zipA, кодирующего белок клеточного деления, вовлеченный в сборку Z-кольца, и/или ген ygaW, содержащий мутацию в кодоне в положении 13-15 SEQ ID NO: 1 или в соответствующем кодоне функциональных эквивалентов SEQ ID NO: 1, причем мутация изменяет активность и/или экспрессию транспортера аланина, кодируемого геном ygaW, предпочтительно дополнительно характеризуется по меньшей мере двумя, более предпочтительно по меньшей мере тремя, даже более предпочтительно по меньшей мере четырьмя, даже более предпочтительно по меньшей мере пятью, наиболее предпочтительно всеми из признаков, выбранных из следующей группы:
(а) сниженная, репрессированная или удаленная активность и/или экспрессия гена pflB, кодирующего пируватформиатлиазу I и
(b) сниженная, репрессированная или удаленная активность и/или экспрессия гена adhE, кодирующего бифункциональную ацетальдегид-СоА дегидрогеназу/железозависимую алкогольдегидрогеназу/деактивазу пируватформиатлиазы и
(c) сниженная, репрессированная или удаленная активность и/или экспрессия гена ldhA, кодирующего NAD-зависимую ферментативную D-лактатдегидрогеназу и
(d) сниженная, репрессированная или удаленная активность и/или экспрессия гена pta, кодирующего фосфатацетилтрансферазу и
(e) сниженная, репрессированная или удаленная активность и/или экспрессия гена frdA, кодирующего фумаратредуктазу и
(f) введенная, увеличенная или усиленная активность и/или экспрессия гена alaD, кодирующего аланиндегидрогеназу,
причем снижение, репрессию, удаление, увеличение или усиление активности и/или экспрессии гена определяют по сравнению с соответствующим микроорганизмом сравнения.
Ген alaD может быть получен из любого организма или может представлять собой синтетический ген, разработанный человеком, например, характеризующийся оптимизированной частотой использования кодона для экспрессии в рекомбинантном микроорганизме согласно настоящему изобретению или оптимизированный в отношении ферментативной активности, например, характеризующийся улучшенными показателями Vmax или Km. Ген alaD предпочтительно получен из микроорганизма одного из родов Bacillus, Geobacillus, Paenibacillus, Halobacillus, Brevibacillus. Согласно более предпочтительному варианту осуществления ген alaD получен из микроорганизма рода Geobacillus. Согласно наиболее предпочтительному варианту осуществления ген alaD получен из Geobacillus stearothermophilus.
Согласно предпочтительному варианту осуществления ген alaD был подвергнут оптимизации кодона для экспрессии в рекомбинантном микроорганизме согласно настоящему изобретению.
Микроорганизм согласно настоящему изобретению может содержать дополнительные генетические модификации, такие как мутации, нокауты или усиленные или введенные ферментативные активности, которые дополнительно улучшают выход и/или производительность аланина, пирувата, сукцината, аспартата, малата, лактата, валина и/или лейцина, предпочтительно сукцината или аланина, более предпочтительно аланина.
Согласно дополнительному варианту осуществления ген lpd, кодирующий белок липоамиддегидрогеназу с введенной, увеличенной или усиленной активностью и/или экспрессией в рекомбинантном микроорганизме согласно настоящему изобретению, выбран из следующей группы:
(i) молекула нуклеиновой кислоты, содержащая последовательность SEQ ID NO: 49, или
(ii) молекула нуклеиновой кислоты, характеризующаяся по меньшей мере 80%, предпочтительно по меньшей мере 85%, например, по меньшей мере 90%, более предпочтительно по меньшей мере 95%, например, по меньшей мере 96%, даже более предпочтительно по меньшей мере 97%, например, по меньшей мере 98%, наиболее предпочтительно по меньшей мере 99% идентичностью относительно молекулы нуклеиновой кислоты согласно SEQ ID NO: 49, или
(iii) молекула нуклеиновой кислоты, гибридизующаяся с молекулой нуклеиновой кислоты, характеризующейся SEQ ID NO: 49, при условиях средней жесткости, более предпочтительно при условиях высокой жесткости, наиболее предпочтительно при условиях очень высокой жесткости, или
(iv) молекула нуклеиновой кислоты, кодирующая полипептид согласно SEQ ID NO: 50, или
(v) молекула нуклеиновой кислоты, кодирующая полипептид, характеризующийся по меньшей мере 60%, предпочтительно по меньшей мере 70%, например, по меньшей мере 75%, более предпочтительно по меньшей мере 80%, например, по меньшей мере 85%, даже более предпочтительно по меньшей мере 90%, например, по меньшей мере 95%, наиболее предпочтительно по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% гомологией относительно полипептида согласно SEQ ID NO: 50,
причем полипептид, кодируемый (ii), (iii) или (v), характеризуется по меньшей мере 10%, 20%, предпочтительно по меньшей мере 30% или 50%, более предпочтительно по меньшей мере 60% или 70%, даже более предпочтительно по меньшей мере 75%, 80%, 85% или 90%, наиболее предпочтительный по меньшей мере 95% активности относительно полипептида, характеризующегося SEQ ID NO: 50.
Согласно одному примеру ген lpd, кодирующий белок липоамиддегидрогеназу с введенной, увеличенной или усиленной активностью и/или экспрессией в рекомбинантном микроорганизме согласно настоящему изобретению, характеризуется последовательностью согласно SEQ ID NO: 51, кодирующей белок, характеризующийся SEQ ID NO: 52.
Согласно дополнительному варианту осуществления ген zipA, кодирующий белок клеточного деления, вовлеченный в сборку Z-кольца, с введенной, увеличенной, усиленной или измененной активностью и/или экспрессией в рекомбинантном микроорганизме согласно настоящему изобретению, выбран из следующей группы:
(i) молекула нуклеиновой кислоты, содержащая последовательность SEQ ID NO: 45, или
(ii) молекула нуклеиновой кислоты, характеризующаяся по меньшей мере 80%, предпочтительно по меньшей мере 85%, например, по меньшей мере 90%, более предпочтительно по меньшей мере 95%, например, по меньшей мере 96%, даже более предпочтительно по меньшей мере 97%, например, по меньшей мере 98%, наиболее предпочтительно по меньшей мере 99% идентичностью относительно молекулы нуклеиновой кислоты согласно SEQ ID NO: 45, или
(iii) молекула нуклеиновой кислоты, гибридизующаяся с молекулой нуклеиновой кислоты, характеризующейся SEQ ID NO: 45, при условиях средней жесткости, более предпочтительно при условиях высокой жесткости, наиболее предпочтительно при условиях очень высокой жесткости, или
(iv) молекула нуклеиновой кислоты, кодирующая полипептид согласно SEQ ID NO: 46, или
(v) молекула нуклеиновой кислоты, кодирующая полипептид, характеризующийся по меньшей мере 60%, предпочтительно по меньшей мере 70%, например, по меньшей мере 75%, более предпочтительно по меньшей мере 80%, например, по меньшей мере 85%, даже более предпочтительно по меньшей мере 90%, например, по меньшей мере 95%, наиболее предпочтительно по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% гомологией относительно полипептида согласно SEQ ID NO: 46,
причем полипептид, кодируемый (ii), (iii) или (v), характеризуется по меньшей мере 10%, 20%, предпочтительно по меньшей мере 30% или 50%, более предпочтительно по меньшей мере 60% или 70%, даже более предпочтительно по меньшей мере 75%, 80%, 85% или 90%, наиболее предпочтительный по меньшей мере 95% активности относительно полипептида, характеризующегося SEQ ID NO: 46.
Согласно одному примеру ген zipA, кодирующий белок клеточного деления, вовлеченный в сборку Z-кольца, с введенной, увеличенной, усиленной или измененной активностью и/или экспрессией в рекомбинантном микроорганизме согласно настоящему изобретению, характеризуется последовательностью согласно SEQ ID NO: 47, кодирующей белок, характеризующийся SEQ ID NO: 48.
Согласно дополнительному варианту осуществления ген ygaW, кодирующий транспортер аланина с измененной активностью и/или экспрессией в рекомбинантном микроорганизме согласно настоящему изобретению, выбран из следующей группы:
(i) молекула нуклеиновой кислоты, содержащая последовательность SEQ ID NO: 1, или
(ii) молекула нуклеиновой кислоты, характеризующаяся по меньшей мере 80%, предпочтительно по меньшей мере 85%, например, по меньшей мере 90%, более предпочтительно по меньшей мере 95%, например, по меньшей мере 96%, даже более предпочтительно по меньшей мере 97%, например, по меньшей мере 98%, наиболее предпочтительно по меньшей мере 99% идентичностью относительно молекулы нуклеиновой кислоты согласно SEQ ID NO: 1, или
(iii) молекула нуклеиновой кислоты, гибридизующаяся с молекулой нуклеиновой кислоты, характеризующейся SEQ ID NO: 1, при условиях средней жесткости, более предпочтительно при условиях высокой жесткости, наиболее предпочтительно при условиях очень высокой жесткости, или
(iv) молекула нуклеиновой кислоты, кодирующая полипептид согласно SEQ ID NO: 2, или
(v) молекула нуклеиновой кислоты, кодирующая полипептид, характеризующийся по меньшей мере 60%, предпочтительно по меньшей мере 70%, например, по меньшей мере 75%, более предпочтительно по меньшей мере 80%, например, по меньшей мере 85%, даже более предпочтительно по меньшей мере 90%, например, по меньшей мере 95%, наиболее предпочтительно по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% гомологией относительно полипептида согласно SEQ ID NO: 2, и
причем кодон генов согласно (i)-(v), соответствующий положению 13-15 SEQ ID NO: 1, не кодирует аминокислоту глутамин и не представляет собой стоп-кодон, или аминокислота белков, кодируемых генами согласно (i)-(v), соответствующая положению 5 в SEQ ID NO: 2, не представляет собой глутамин, и
причем белок, кодируемый геном согласно приведенному выше определению в (1)-(5) характеризуется измененной активностью и/или экспрессией по сравнению с белком, характеризующимся SEQ ID NO: 2, и
причем микроорганизм, содержащий мутированный ген и/или белок согласно приведенному выше определению, характеризуется улучшенным выходом аланина в ферментации.
Согласно одному примеру ген ygaW, кодирующий транспортер аланина с измененной активностью и/или экспрессией в рекомбинантном микроорганизме согласно настоящему изобретению, характеризуется последовательностью согласно SEQ ID NO: 3, 56, 58 или 60, кодирующей белок, характеризующийся SEQ ID NO: 4, 57, 59 или 61.
Рекомбинантный микроорганизм согласно настоящему изобретению, характеризующийся введенной, увеличенной или усиленной экспрессией и/или активностью гена lpd, кодирующего белок липоамиддегидрогеназу, и/или введенной, увеличенной, усиленной или измененной активностью и/или экспрессией гена zipA, и/или геном ygaW, содержащим мутацию в кодоне в положении 13-15 SEQ ID NO: 1 или в соответствующем кодоне функциональных эквивалентов SEQ ID NO: 1, причем мутация изменяет активность и/или экспрессию транспортера аланина, кодируемого геном ygaW, может дополнительно характеризоваться любым одним, двумя, тремя, четырьмя, пятью или всеми из признаков согласно приведенному выше определению в (а)-(f),
причем ген pflB выбран из группы, состоящей из следующего:
(A) молекула нуклеиновой кислоты, содержащая последовательность SEQ ID NO: 5, или
(B) молекула нуклеиновой кислоты, характеризующаяся по меньшей мере 80%, предпочтительно по меньшей мере 85%, например, по меньшей мере 90%, более предпочтительно по меньшей мере 95%, например, по меньшей мере 96%, даже более предпочтительно по меньшей мере 97%, например, по меньшей мере 98%, наиболее предпочтительно по меньшей мере 99% идентичностью относительно молекулы нуклеиновой кислоты согласно SEQ ID NO: 5, или
(C) молекула нуклеиновой кислоты, гибридизующаяся с молекулой нуклеиновой кислоты, характеризующейся SEQ ID NO: 5, при условиях средней жесткости, более предпочтительно при условиях высокой жесткости, наиболее предпочтительно при условиях очень высокой жесткости, или
(D) молекула нуклеиновой кислоты, кодирующая полипептид согласно SEQ ID NO: 6, или
(Ε) молекула нуклеиновой кислоты, кодирующая полипептид, характеризующийся по меньшей мере 60%, предпочтительно по меньшей мере 70%, например, по меньшей мере 75%, более предпочтительно по меньшей мере 80%, например, по меньшей мере 85%, даже более предпочтительно по меньшей мере 90%, например, по меньшей мере 95%, наиболее предпочтительно по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% гомологией относительно полипептида согласно SEQ ID NO: 6,
причем полипептид, кодируемый (В), (С) или (Е), характеризуется по меньшей мере 10%, 20%, предпочтительно по меньшей мере 30% или 50%, более предпочтительно по меньшей мере 60% или 70%, даже более предпочтительно по меньшей мере 75%, 80%, 85% или 90%, наиболее предпочтительный по меньшей мере 95% активности относительно полипептида, характеризующегося SEQ ID NO: 6 и
причем ген adhE выбран из группы, состоящей из следующего:
(F) молекула нуклеиновой кислоты, содержащая последовательность SEQ ID NO: 7, или
(G) молекула нуклеиновой кислоты, характеризующаяся по меньшей мере 80%, предпочтительно по меньшей мере 85%, например, по меньшей мере 90%, более предпочтительно по меньшей мере 95%, например, по меньшей мере 96%, даже более предпочтительно по меньшей мере 97%, например, по меньшей мере 98%, наиболее предпочтительно по меньшей мере 99% идентичностью относительно молекулы нуклеиновой кислоты согласно SEQ ID NO: 7, или
(H) молекула нуклеиновой кислоты, гибридизующаяся с молекулой нуклеиновой кислоты, характеризующейся SEQ ID NO: 7, при условиях средней жесткости, более предпочтительно при условиях высокой жесткости, наиболее предпочтительно при условиях очень высокой жесткости, или
(I) молекула нуклеиновой кислоты, кодирующая полипептид согласно SEQ ID NO: 8, или
(J) молекула нуклеиновой кислоты, кодирующая полипептид, характеризующийся по меньшей мере 60%, предпочтительно по меньшей мере 70%, например, по меньшей мере 75%, более предпочтительно по меньшей мере 80%, например, по меньшей мере 85%, даже более предпочтительно по меньшей мере 90%, например, по меньшей мере 95%, наиболее предпочтительно по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% гомологией относительно полипептида согласно SEQ ID NO: 8,
причем полипептид, кодируемый (G), (Н) или (J), характеризуется по меньшей мере 10%, 20%, предпочтительно по меньшей мере 30% или 50%, более предпочтительно по меньшей мере 60% или 70%, даже более предпочтительно по меньшей мере 75%, 80%, 85% или 90%, наиболее предпочтительный по меньшей мере 95% активности относительно полипептида, характеризующегося SEQ ID NO: 8 и
причем ген ldhA выбран из группы, состоящей из следующего:
(K) молекула нуклеиновой кислоты, содержащая последовательность SEQ ID NO: 9, или
(L) молекула нуклеиновой кислоты, характеризующаяся по меньшей мере 80%, предпочтительно по меньшей мере 85%, например, по меньшей мере 90%, более предпочтительно по меньшей мере 95%, например, по меньшей мере 96%, даже более предпочтительно по меньшей мере 97%, например, по меньшей мере 98%, наиболее предпочтительно по меньшей мере 99% идентичностью относительно молекулы нуклеиновой кислоты согласно SEQ ID NO: 9, или
(M) молекула нуклеиновой кислоты, гибридизующаяся с молекулой нуклеиновой кислоты, характеризующейся SEQ ID NO: 9, при условиях средней жесткости, более предпочтительно при условиях высокой жесткости, наиболее предпочтительно при условиях очень высокой жесткости, или
(N) молекула нуклеиновой кислоты, кодирующая полипептид согласно SEQ ID NO: 10, или
(О) молекула нуклеиновой кислоты, кодирующая полипептид, характеризующийся по меньшей мере 60%, предпочтительно по меньшей мере 70%, например, по меньшей мере 75%, более предпочтительно по меньшей мере 80%, например, по меньшей мере 85%, даже более предпочтительно по меньшей мере 90%, например, по меньшей мере 95%, наиболее предпочтительно по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% гомологией относительно полипептида согласно SEQ ID NO: 10,
причем полипептид, кодируемый (L), (М) или (О), характеризуется по меньшей мере 10%, 20%, предпочтительно по меньшей мере 30% или 50%, более предпочтительно по меньшей мере 60% или 70%, даже более предпочтительно по меньшей мере 75%, 80%, 85% или 90%, наиболее предпочтительный по меньшей мере 95% активности относительно полипептида, характеризующегося SEQ ID NO: 10 и
причем ген pta выбран из группы, состоящей из следующего:
(Р) молекула нуклеиновой кислоты, содержащая последовательность SEQ ID NO: 11, или
(Q) молекула нуклеиновой кислоты, характеризующаяся по меньшей мере 80%, предпочтительно по меньшей мере 85%, например, по меньшей мере 90%, более предпочтительно по меньшей мере 95%, например, по меньшей мере 96%, даже более предпочтительно по меньшей мере 97%, например, по меньшей мере 98%, наиболее предпочтительно по меньшей мере 99% идентичностью относительно молекулы нуклеиновой кислоты согласно SEQ ID NO: 11, или
(R) молекула нуклеиновой кислоты, гибридизующаяся с молекулой нуклеиновой кислоты, характеризующейся SEQ ID NO: 11, при условиях средней жесткости, более предпочтительно при условиях высокой жесткости, наиболее предпочтительно при условиях очень высокой жесткости, или
(S) молекула нуклеиновой кислоты, кодирующая полипептид согласно SEQ ID NO: 12, или
(Τ) молекула нуклеиновой кислоты, кодирующая полипептид, характеризующийся по меньшей мере 60%, предпочтительно по меньшей мере 70%, например, по меньшей мере 75%, более предпочтительно по меньшей мере 80%, например, по меньшей мере 85%, даже более предпочтительно по меньшей мере 90%, например, по меньшей мере 95%, наиболее предпочтительно по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% гомологией относительно полипептида согласно SEQ ID NO: 12,
причем полипептид, кодируемый (Q), (R) или (Т), характеризуется по меньшей мере 10%, 20%, предпочтительно по меньшей мере 30% или 50%, более предпочтительно по меньшей мере 60% или 70%, даже более предпочтительно по меньшей мере 75%, 80%, 85% или 90%, наиболее предпочтительный по меньшей мере 95% активности относительно полипептида, характеризующегося SEQ ID NO: 12 и
причем ген frdA выбран из группы, состоящей из следующего:
(U) молекула нуклеиновой кислоты, содержащая последовательность SEQ ID NO: 13, или
(V) молекула нуклеиновой кислоты, характеризующаяся по меньшей мере 80%, предпочтительно по меньшей мере 85%, например, по меньшей мере 90%, более предпочтительно по меньшей мере 95%, например, по меньшей мере 96%, даже более предпочтительно по меньшей мере 97%, например, по меньшей мере 98%, наиболее предпочтительно по меньшей мере 99% идентичностью относительно молекулы нуклеиновой кислоты согласно SEQ ID NO: 13, или
(W) молекула нуклеиновой кислоты, гибридизующаяся с молекулой нуклеиновой кислоты, характеризующейся SEQ ID NO: 13, при условиях средней жесткости, более предпочтительно при условиях высокой жесткости, наиболее предпочтительно при условиях очень высокой жесткости, или
(X) молекула нуклеиновой кислоты, кодирующая полипептид согласно SEQ ID NO: 14, или
(Y) молекула нуклеиновой кислоты, кодирующая полипептид, характеризующийся по меньшей мере 60%, предпочтительно по меньшей мере 70%, например, по меньшей мере 75%, более предпочтительно по меньшей мере 80%, например, по меньшей мере 85%, даже более предпочтительно по меньшей мере 90%, например, по меньшей мере 95%, наиболее предпочтительно по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% гомологией относительно полипептида согласно SEQ ID NO: 14,
причем полипептид, кодируемый by (V), (W) или (Y) характеризуется по меньшей мере 10%, 20%, предпочтительно по меньшей мере 30% или 50%, более предпочтительно по меньшей мере 60% или 70%, даже более предпочтительно по меньшей мере 75%, 80%, 85% или 90%, наиболее предпочтительный по меньшей мере 95% активности относительно полипептида, характеризующегося SEQ ID NO: 14 и
причем ген alaD выбран из группы, состоящей из следующего:
(Z) молекула нуклеиновой кислоты, содержащая последовательность SEQ ID NO: 15, или
(АА) молекула нуклеиновой кислоты, характеризующаяся по меньшей мере 80%, предпочтительно по меньшей мере 85%, например, по меньшей мере 90%, более предпочтительно по меньшей мере 95%, например, по меньшей мере 96%, даже более предпочтительно по меньшей мере 97%, например, по меньшей мере 98%, наиболее предпочтительно по меньшей мере 99% идентичностью относительно молекулы нуклеиновой кислоты согласно SEQ ID NO: 15, или
(ВВ) молекула нуклеиновой кислоты, гибридизующаяся с молекулой нуклеиновой кислоты, характеризующейся SEQ ID NO: 15, при условиях средней жесткости, более предпочтительно при условиях высокой жесткости, наиболее предпочтительно при условиях очень высокой жесткости, или
(СС) молекула нуклеиновой кислоты, кодирующая полипептид согласно SEQ ID NO: 16, или
(DD) молекула нуклеиновой кислоты, кодирующая полипептид, характеризующийся по меньшей мере 60%, предпочтительно по меньшей мере 70%, например, по меньшей мере 75%, более предпочтительно по меньшей мере 80%, например, по меньшей мере 85%, даже более предпочтительно по меньшей мере 90%, например, по меньшей мере 95%, наиболее предпочтительно по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% гомологией относительно полипептида согласно SEQ ID NO: 16,
причем полипептид, кодируемый (АА), (ВВ) или (DD), характеризуется по меньшей мере 10%, 20%, предпочтительно по меньшей мере 30% или 50%, более предпочтительно по меньшей мере 60% или 70%, даже более предпочтительно по меньшей мере 75%, 80%, 85% или 90%, наиболее предпочтительный по меньшей мере 95% активности относительно полипептида, характеризующегося SEQ ID NO: 16.
Молекула нуклеиновой кислоты согласно определению в (Z)-(DD) предпочтительно находится под контролем последовательности, функционирующей в качестве промотора в микроорганизме, характеризующейся следующей последовательностью:
(1) молекула нуклеиновой кислоты, содержащая последовательность SEQ ID NO: 54 или 55, или
(2) молекула нуклеиновой кислоты, характеризующаяся по меньшей мере 80%, предпочтительно по меньшей мере 85%, например, по меньшей мере 90%, более предпочтительно по меньшей мере 95%, например, по меньшей мере 96%, даже более предпочтительно по меньшей мере 97%, например, по меньшей мере 98%, наиболее предпочтительно по меньшей мере 99% идентичностью относительно молекулы нуклеиновой кислоты согласно SEQ ID NO: 54 или 55, или
(3) молекула нуклеиновой кислоты, гибридизующаяся с молекулой нуклеиновой кислоты, характеризующейся SEQ ID NO: 54 или 55, при условиях средней жесткости, более предпочтительно при условиях высокой жесткости, наиболее предпочтительно при условиях очень высокой жесткости или
(4) фрагмент, составляющий по меньшей мере 10 нуклеотидов, предпочтительно по меньшей мере 20 нуклеотидов, по меньшей мере 30 нуклеотидов или по меньшей мере 40 нуклеотидов, более предпочтительно фрагмент, составляющий по меньшей мере 50 нуклеотидов, по меньшей мере 75 нуклеотидов или по меньшей мере 100 нуклеотидов, даже более предпочтительно по меньшей мере 150 или по меньшей мере 200 нуклеотидов молекулы нуклеиновой кислоты, характеризующейся SEQ ID NO: 54 или 55. Фрагмент SEQ ID NO: 54 или 55 предпочтительно представляет собой фрагмент, содержащий 3' область SEQ ID NO: 54 или 55, следовательно, фрагмент содержит делецию на 5' конце SEQ ID NO: 54 или 55.
Согласно дополнительному варианту осуществления настоящего изобретения предусмотрена композиция, содержащая один или более рекомбинантных микроорганизмов согласно настоящему изобретению согласно приведенному выше определению. Композиция может дополнительно содержать среду, которая обеспечивает возможность роста рекомбинантного микроорганизма согласно настоящему изобретению. Среда может дополнительно содержать такой источник углерода, как гексозы, пентозы или многоатомные спирты, например, сахарозу, глюкозу, фруктозу, галактозу, маннозу, раффинозу, ксилозу, арабинозу, ксилулозу, глицерин, маннит, арабит, ксилит, крахмал, целлюлозу, лигноцеллюлозу или их комбинации. Источник углерода предпочтительно представляет собой глюкозу или сахарозу, более предпочтительно источник углерода представляет собой глюкозу.
Согласно предпочтительному варианту осуществления композиция содержит микроорганизм согласно настоящему изобретению и среду NBS, среду AM1 или среду РРМ01. Более предпочтительно композиция дополнительно содержит источник углерода, предпочтительно сахар. Ингредиенты указанных сред известны специалисту в настоящей области техники.
Среда NBS предпочтительно содержит из расчета на литр
1-5 г, предпочтительно 3,5 г KH2PO4 и
1-10 г, предпочтительно 5,0 г K2HPO4 и
1-5 г, предпочтительно 3,5 г (NH4)2HPO4 и
0,1-1 г, предпочтительно 0,25 г MgSO4 - 7 H2O и
5-25 мг, предпочтительно 15 мг CaCL2 - 2 Н2О и
0,1-1 мг, предпочтительно 0,5 мг тиамина и
0,1-5 мл, предпочтительно 1 мл маточного раствора микроэлементов,
причем маточный раствор микроэлементов содержит 0,5-5 г, предпочтительно 1,6 г FeCL3 - 6 Н2О; 0,05-0,5 г, предпочтительно 0,2 г CoCl2 - 6 H2O; 0,01-0,5 г, предпочтительно 0,1 г CuCl2 - 2 H2O; 0,1-0,5 г, предпочтительно 0,2 г ZnCl2; 0,05-0,5 г, предпочтительно 0,2 г NaMoO4 - 2 Н2О; 0,001-0,1 г, предпочтительно 0,05 г Н3ВО3 на литр 0,01-1 М, предпочтительно 0,1 M HCL.
Предпочтительный источник углерода в среде NBS представляет собой глюкозу или сахарозу, предпочтительно 2%-18% глюкозу или 2%-16% сахарозу.
Среда AM 1 предпочтительно содержит из расчета на литр 0,1-10 мМ, предпочтительно 1 мМ раствора бетаина
1-10 г, предпочтительно 2,6 г (NΗ4)2ΗΡO4 и
0,1-5 г, предпочтительно 0,87 г NH4H2PO4 и
0,05-2,5 г, предпочтительно 0,15 г KCl и
0,05-5 г, предпочтительно 0,37 г MgSO4-7H2O и
0,1-5 мл, предпочтительно 1 мл маточного раствора микроэлементов,
причем маточный раствор микроэлементов содержит на литр 0,01-1 М, предпочтительно 0,12 M HCL, 1-5 г, предпочтительно 2,4 г FeCL3-6Н2О; 0,1-1 г, предпочтительно 0,3 г CoCl2-6H2O; 0,1-1 г, предпочтительно 0,21 г CuCl2 - 2 Н2О; 0,1-1 г, предпочтительно 0,3 г ZnCl2; 0,1-1 г, предпочтительно 0,27 г NaMoO4 - 2 Н2О; 0,01-0,5 г, предпочтительно 0,068 г Н3ВО3 и 0,1-1 г, предпочтительно 0,5 г MnCl2 - 4 Н2О,
и необязательно 1-30 г, предпочтительно 15 г (NH4)2SO4.
Предпочтительный источник углерода в среде NBS представляет собой глюкозу или сахарозу, предпочтительно 2%-18% глюкозу или 2%-16% сахарозу.
Среда РРМ01 предпочтительно содержит из расчета на литр
0,05-5 г, предпочтительно 0,37 г MgSO4 - 7 Н2О и
0,1-10 г, предпочтительно 1 г (NH4)2SO4 и
0,05-5 г, предпочтительно 0,46 г бетаина и
0,001-0,5 г, предпочтительно 0,05 г цианокобаламина (В12) и
1-10 г, предпочтительно 3,74 г KH2PO4 и
0,1-5 мл, предпочтительно 1 мл маточного раствора микроэлементов,
причем маточный раствор микроэлементов содержит на литр 10-100 мМ, предпочтительно 60 мМ серной кислоты, 1-10 г, предпочтительно 3,48 г (NH4)2Fe(II)(SO4)2 - 7 H2O; 0,1-1 г, предпочтительно 0,35 г CoSO4 - 7 H2O; 0,1-1 г, предпочтительно 0,31 г CuSO4 - 5 H2O; 0,1-5 г, предпочтительно 0,63 г ZnSO4 - 7 H2O; 0,1-1 г, предпочтительно 0,27 г MnSO4 - H2O; 0,01-1 г, предпочтительно 0,07 г NaMoO4 - 2 H2O и 0,1-5 г, предпочтительно 0,43 г Н3ВО3.
Предпочтительный источник углерода в среде РРМ01 представляет собой моногидрат глюкозы, предпочтительно 10-500 г, более предпочтительно 140 г моногидрата глюкозы на литр среды.
Согласно дополнительному варианту осуществления настоящего изобретения предусмотрен способ получения рекомбинантного микроорганизма с усиленным выходом или производительностью аланина, пирувата, сукцината, аспартата, малата, лактата, валина и/или лейцина, предпочтительно сукцината или аланина, более предпочтительно аланина, который предусматривает следующие стадии:
(I) введение, увеличение или усиление по меньшей мере одного из следующего: i) одна или более активность и/или экспрессия гена lpd, и/или ii) введение, увеличение, усиление или изменение одной или более активности и/или экспрессии гена zipA, и/или iii) введение гена ygaW, содержащего мутацию в кодоне в положении 13-15 SEQ ID NO: 1 или в соответствующем кодоне функциональных эквивалентов SEQ ID NO: 1, причем мутация изменяет активность и/или экспрессию транспортера аланина, кодируемого геном ygaW, и необязательно дополнительное введение одной или более из модификаций согласно приведенному выше определению в (а)-(е) в микроорганизм; и
(II) создание, идентификация и выделение рекомбинантного микроорганизма с усиленным выходом или производительностью аланина, пирувата, сукцината, аспартата, малата, лактата, валина и/или лейцина, предпочтительно сукцината или аланина, более предпочтительно аланина по сравнению с соответствующим микроорганизмом без модификации согласно приведенному выше определению в (I).
Согласно предпочтительному варианту осуществления ген lpd с введенной, увеличенной или усиленной активностью и/или экспрессией характеризуется последовательностью согласно SEQ ID NO: 51 и/или кодирует полипептид согласно SEQ ID NO: 52.
Согласно предпочтительному варианту осуществления ген zipA с введенной, увеличенной, усиленной или измененной активностью и/или экспрессией характеризуется последовательностью согласно SEQ ID NO: 47 и/или кодирует полипептид согласно SEQ ID NO: 48.
Согласно предпочтительному варианту осуществления ген ygaW с измененной активностью и/или экспрессией характеризуется последовательностью согласно SEQ ID NO: 3, 56, 58 или 60 и/или кодирует полипептид согласно SEQ ID NO: 4, 57, 59 или 61.
Согласно предпочтительному варианту осуществления способа получения рекомбинантного микроорганизма согласно настоящему изобретению способ дополнительно предусматривает стадию снижения, репрессии или удаления активности и/или экспрессии по меньшей мере одного, по меньшей мере двух, по меньшей мере трех, по меньшей мере четырех или всех из гена pflB, гена adhE, гена ldhA, гена pta или гена frdA, например, согласно приведенному выше определению в (А)-(Y) и/или стадию введения, увеличения или усиления активности и/или экспрессии гена alaD, например, согласно приведенному выше определению в (Z)-(DD).
Согласно дополнительному предпочтительному варианту осуществления способа получения рекомбинантного микроорганизма согласно настоящему изобретению молекула нуклеиновой кислоты согласно определению в (Z)-(DD) находится под контролем последовательности, функционирующей в качестве промотора в микроорганизме, характеризующейся следующей последовательностью:
(1) молекула нуклеиновой кислоты, содержащая последовательность SEQ ID NO: 54 или 55, или
(2) молекула нуклеиновой кислоты, характеризующаяся по меньшей мере 80%, предпочтительно по меньшей мере 85%, например, по меньшей мере 90%, более предпочтительно по меньшей мере 95%, например, по меньшей мере 96%, даже более предпочтительно по меньшей мере 97%, например, по меньшей мере 98%, наиболее предпочтительно по меньшей мере 99% идентичностью относительно молекулы нуклеиновой кислоты согласно SEQ ID NO: 54 или 55, или
(3) молекула нуклеиновой кислоты, гибридизующаяся с молекулой нуклеиновой кислоты, характеризующейся SEQ ID NO: 54 или 55, при условиях средней жесткости, более предпочтительно при условиях высокой жесткости, наиболее предпочтительно при условиях очень высокой жесткости, или
(4) фрагмент, составляющий по меньшей мере 10 нуклеотидов, предпочтительно по меньшей мере 20 нуклеотидов, по меньшей мере 30 нуклеотидов или по меньшей мере 40 нуклеотидов, более предпочтительно фрагмент, составляющий по меньшей мере 50 нуклеотидов, по меньшей мере 75 нуклеотидов или по меньшей мере 100 нуклеотидов, даже более предпочтительно по меньшей мере 150 или по меньшей мере 200 нуклеотидов молекулы нуклеиновой кислоты, характеризующейся SEQ ID NO: 54 или 55. Фрагмент SEQ ID NO: 54 или 55 предпочтительно представляет собой фрагмент, содержащий 3' область SEQ ID NO: 54 или 55, следовательно, фрагмент содержит делецию на 5' конце SEQ ID NO: 54 или 55.
Наиболее предпочтительный способ получения рекомбинантного микроорганизма согласно настоящему изобретению предусматривает стадию i) снижения, репрессии или удаления активности и/или экспрессии всех из гена pflB, гена adhE, гена ldhA, гена pta и гена frdA и ii) стадию введения, увеличения или усиления активности и/или экспрессии гена alaD предпочтительно под контролем промотора, содержащего последовательность SEQ ID NO: 54 или 55, и iii) введения, увеличения или усиления активности и/или экспрессии гена lpd, предпочтительно характеризующегося последовательностью согласно SEQ ID NO: 51 и/или кодирующего полипептид согласно SEQ ID NO: 52, и iv) введения или изменения активности и/или экспрессии гена zipA, предпочтительно характеризующегося последовательностью согласно SEQ ID NO: 47 и/или кодирующего полипептид согласно SEQ ID NO: 48, и v) введения гена ygaW с измененной активностью и/или экспрессией или введения мутации в эндогенный ген ygaW, который характеризуется последовательностью согласно SEQ ID NO: 3, 56, 58 или 60 и/или кодирует полипептид согласно SEQ ID NO: 4, 57, 59 или 61.
Согласно одному варианту осуществления способа получения рекомбинантного микроорганизма согласно настоящему изобретению микроорганизм выбран из группы, состоящей из вида рода Corynebacterium, например, С. acetophilum, С. glutamicum, С. callunae, С. acetoacidophilum, С. acetoglutamicum, вида рода Bacillus, например, В. thuringiensis, В. anthracis, В. megaterium, В. subtilis, В. lentils, В. circulans, В. pumilus, В. lautus, B. coagulans, В. brevis, В. fírmus, В. alkaophius, В. licheniformis, В. clausii, В. stearothermophilus, В. halodurans, В. subtilis, В. pumilus, и В. amyloliquefaciens, вида рода Erwinia, например, Е. uredovora, Ε. carotovora, Ε. ananas, Ε. herbicola, Ε. punctate, Ε. terreus, вида рода Escherichia, например, Ε. coli, вида рода Pantoea, например, P. citrea, P. agglomerans, вида рода Streptomyces, например, S. ambofaciens, S. achromogenes, S. avermitilis, S. coelicolor, S. aureofaciens, S. aureus, S. fungicidicus, S. griseus, S. lividans, вида рода Zymomonas, например, Ζ. mobilis или Ζ. Lipolytica, и вида рода Rhodococcus, например, R. opacus.
Микроорганизм предпочтительно выбран из семейства Enterobacteriaceae, предпочтительно рода Escherichia, например, Escherichia coli (Ε. coli), предпочтительно штамма Ε. coli W, который соответствует DSMZ 1116, который соответствует АТСС9637.
Согласно дополнительному варианту осуществления настоящего изобретения предусмотрен способ получения аланина, пирувата, сукцината, аспартата, малата, лактата, валина и/или лейцина, предпочтительно сукцината или аланина, более предпочтительно аланина, наиболее предпочтительно L-аланина, предусматривающий культивирование одного или более рекомбинантных микроорганизмов согласно приведенному выше определению при условиях, которые обеспечивают возможность производства аланина, пирувата, сукцината, аспартата, малата, лактата, валина и/или лейцина, предпочтительно сукцината или аланина, более предпочтительно аланина, наиболее предпочтительно L-аланина.
Согласно некоторым вариантам осуществления рекомбинантные микроорганизмы, предусмотренные настоящим изобретением, выращивают при условиях периодической или непрерывной ферментации. Классическая периодическая ферментация представляет собой закрытую систему, в которой составы среды устанавливают в начале ферментации и не подвергают искусственны изменениям во время. Вариант периодической системы представляет собой периодическая ферментация с добавлением субстрата. В этом варианте субстрат добавляют с поэтапным наращиванием с течением ферментации. Системы периодической ферментации с добавлением субстрата применимы, когда репрессия катаболита, вероятно, ингибирует метаболизм клеток и когда необходимо иметь ограниченные количества субстрата в среде. Периодическая ферментация и периодическая ферментация с добавлением субстрата являются широко используемыми и хорошо известными в настоящей области техники. Непрерывная ферментация, которая также находит применение в настоящем изобретении, представляет собой систему, в которой определенную среду для ферментации добавляют непрерывно в биореактор и равное количество кондиционированной среды (например, содержащей требуемые конечные продукты) удаляют одновременно для обработки. При непрерывной ферментации, как правило, культура поддерживается при постоянной высокой плотности, при которой клетки преимущественно находятся в фазе роста, в которой производство конечных продуктов усилено. Системы непрерывной ферментации стараются поддерживать условия стационарного роста. Способы модулирования питательных веществ и факторов роста для способов непрерывной ферментации, а также техники для максимального увеличения скорости образования продуктов хорошо известны в области промышленной микробиологии.
Согласно некоторым вариантам осуществления ферментации проводят при температуре в пределах диапазона, составляющего от приблизительно 10°С до приблизительно 60°С, от приблизительно 15°С до приблизительно 50°С, от приблизительно 20°С до приблизительно 45°С, от приблизительно 25°С до приблизительно 45°С, от приблизительно 30°С до приблизительно 45°С и от приблизительно 25°С до приблизительно 40°С. Согласно предпочтительному варианту осуществления температура составляет приблизительно 34°С, 35°С или 36°С. Согласно наиболее предпочтительному варианту осуществления температура составляет приблизительно 37°С или 38°С.
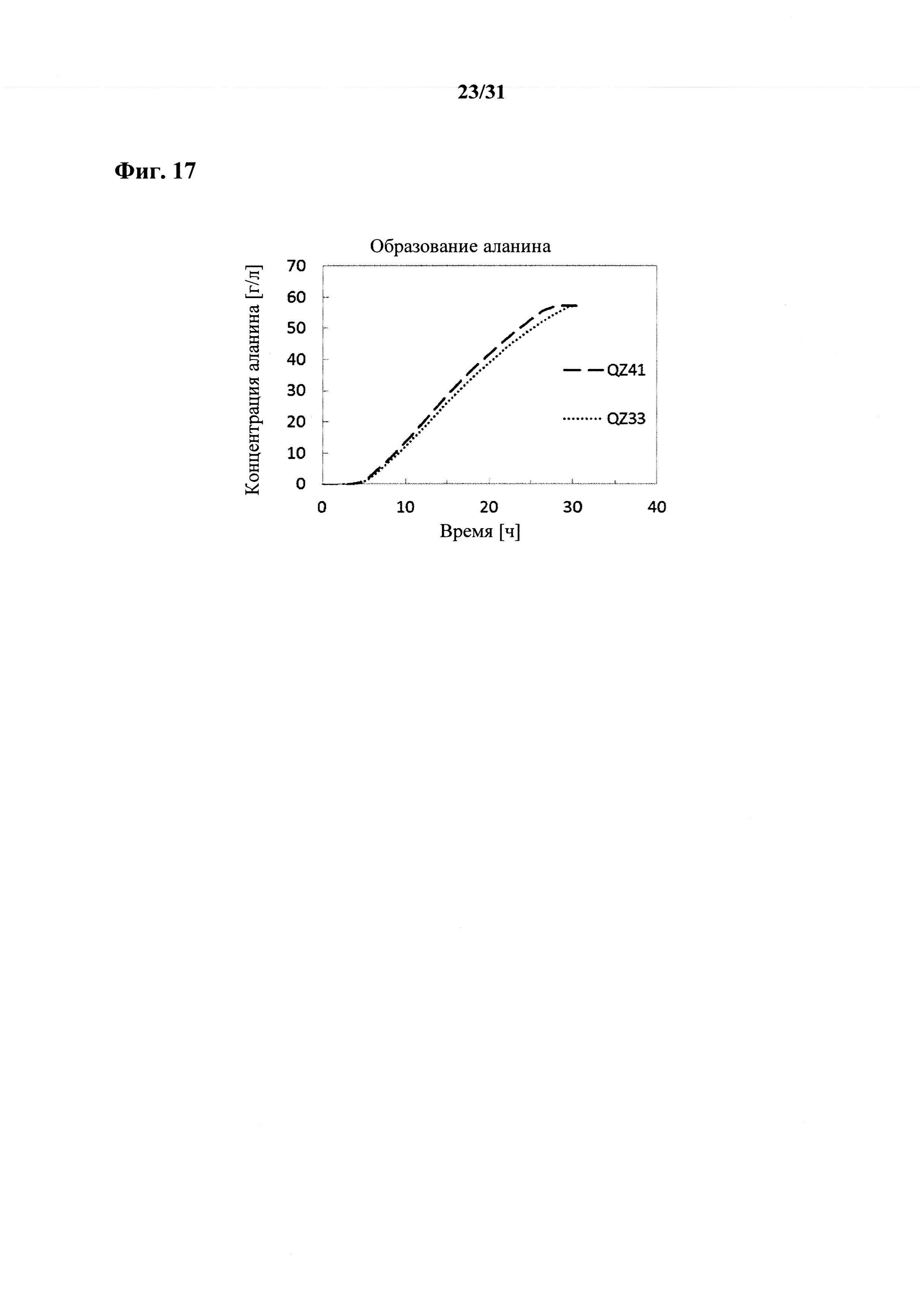
Согласно другим вариантам осуществления ферментацию проводят в течение периода времени в пределах диапазона, составляющего от приблизительно 8 часов до 240 часов, от приблизительно 8 часов до приблизительно 168 часов, от приблизительно 10 часов до приблизительно 144 часов, от приблизительно 15 часов до приблизительно 120 часов, или от приблизительно 20 часов до приблизительно 72 часов. Ферментацию предпочтительно проводят от приблизительно 20 часов до приблизительно 40 часов.
Согласно другим вариантам осуществления ферментацию проводят при рН в диапазоне, составляющем от приблизительно 4 до приблизительно 9, в диапазоне от приблизительно 4,5 до приблизительно 8,5, в диапазоне от приблизительно 5 до приблизительно 8 или в диапазоне от приблизительно 5,5 до приблизительно 7,5. Ферментацию предпочтительно будут проводить при рН, составляющем 7.
Согласно одному варианту осуществления способа получения аланина, пирувата, сукцината, аспартата, малата, лактата, валина и/или лейцина, предпочтительно сукцината или аланина, более предпочтительно аланина, микроорганизм культивируют в среде, содержащей от 1% до 30% (масс/объем) сахара, от 5% до 25% (масс/объем) сахара, от 10% до 20% (масс/объем) сахара, от 14% до 18% (масс/объем) сахара. Микроорганизм предпочтительно культивируют в среде, содержащей от 15% до 17% (масс/объем) сахара.
Согласно другому варианту осуществления способа получения аланина, пирувата, сукцината, аспартата, малата, лактата, валина и/или лейцина, предпочтительно сукцината или аланина, более предпочтительно аланина выход аланина, пирувата, сукцината, аспартата, малата, лактата, валина и/или лейцина составляет по меньшей мере 80%, например, по меньшей мере 81%, по меньшей мере 82%, по меньшей мере 83%, по меньшей мере 84% или по меньшей мере 85%. Выход предпочтительно составляет по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89% или по меньшей мере 90%. Более предпочтительно выход составляет по меньшей мере 90,5%, по меньшей мере 91%, по меньшей мере 91,5%, по меньшей мере 92%, по меньшей мере 92,5%, по меньшей мере 93%, по меньшей мере 93,5%, по меньшей мере 94% или по меньшей мере 94,5%. Согласно даже более предпочтительному варианту осуществления выход составляет по меньшей мере 95% или по меньшей мере 95,5%. Согласно наиболее предпочтительному варианту осуществления выход составляет по меньшей мере 96%. Выход в процентах рассчитывают как продукт в граммах, произведенный из глюкозы в граммах в среде. Следовательно, если среда содержала 100 г глюкозы и ферментация дала в результате 98 г аланина, то выход составит 98%.
Согласно другому варианту осуществления способа получения аланина получают предпочтительно L-аланин, причем хиральная чистота L-аланина составляет по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93% или по меньшей мере 94%. Согласно предпочтительному варианту осуществления хиральная чистота L-аланина составляет по меньшей мере 95% или по меньшей мере 95,5%. Согласно более предпочтительному варианту осуществления хиральная чистота L-аланина составляет по меньшей мере 96%, или по меньшей мере 96,5%, или по меньшей мере 97%. Согласно даже более предпочтительному варианту осуществления хиральная чистота L-аланина составляет по меньшей мере 97,5%, по меньшей мере 98% или по меньшей мере 98,5%, например, по меньшей мере 99%. Даже более предпочтительно хиральная чистота L-аланина составляет по меньшей мере 99,5% или по меньшей мере 99,6%, например, по меньшей мере 99,7%, по меньшей мере 99,8% или по меньшей мере 99,9%. Согласно наиболее предпочтительному варианту осуществления получают хирально чистый L-аланин.
Согласно другому варианту осуществления настоящего изобретения предусмотрен способ культивирования или выращивания любого из генетически модифицированных микроорганизмов согласно приведенному выше определению, причем способ предусматривает инокуляцию среды для культивирования с одним или более генетически модифицированными микроорганизмами и культивирование или выращивание указанного генетически модифицированного микроорганизма в среде для культивирования при условиях согласно приведенному выше определению.
Применение рекомбинантного микроорганизма согласно приведенному выше определению или композиции согласно приведенному выше определению для ферментативного получения аланина, пирувата, сукцината, аспартата, малата, лактата, валина и/или лейцина, предпочтительно сукцината или аланина, более предпочтительно аланина, наиболее предпочтительно L-аланина представляет собой дополнительный вариант осуществления настоящего изобретения.
Рекомбинантный микроорганизм согласно настоящему изобретению характеризуется тем, что по сравнению с соответствующим микроорганизмом сравнения, например, дикого типа, экспрессия и/или активность фермента, кодируемого геном lpd, является увеличенной, и/или экспрессия и/или активность фермента, кодируемого геном zipA, является увеличенной или измененной, и/или активность и/или экспрессия гена ygaW изменена путем введения мутации в ко дон в положении 13-15 SEQ ID NO: 1 или в соответствующем кодоне функциональных эквивалентов SEQ ID NO: 1.
Согласно одному варианту осуществления уменьшение экспрессии и/или активности гена достигается путем деактивации, мутации или нокаута гена. Это можно осуществить путем делеции части или всей кодирующей области и/или промотора гена, путем мутации гена, такой как вставка или делеция ряда нуклеотидов, например, одного или двух нуклеотидов, приводящая к сдвигу рамки считывания в кодирующей области гена, путем введения стоп-кодонов в кодирующую область, инактивации промотора гена, например, путем делеции или мутации промоторных боксов, таких как сайта связывания рибосомы, ТАТА-бокс и подобное. Уменьшение также может быть достигнуто путем разрушения транскрипта гена, например, посредством введения рибозимов, дцРНК, антисмысловой РНК или антисмысловых олигонуклеотидов. Уменьшение активности гена может быть достигнуто путем экспрессии антител или аптамеров в клетке, специфически связывающихся с целевым ферментом. Другие способы уменьшения экспрессии и/или активности гена известны специалисту в настоящей области техники.
Согласно одному варианту осуществления настоящего изобретения увеличение экспрессии и/или активности гена lpd достигается путем введения мутации в ген, предпочтительно точечной мутации, которая приводит к замене аминокислоты в положении 70 белка согласно SEQ ID 50 с аланина на пролин.
Увеличение экспрессии и/или активности гена lpd предпочтительно достигается путем введения мутации в ген lpd, причем мутированный ген lpd характеризуется последовательностью согласно SEQ ID NO: 51, кодирующей белок согласно SEQ ID NO: 52.
Согласно одному варианту осуществления настоящего изобретения увеличение экспрессии и/или активности гена zipA достигается путем введения мутации в ген, предпочтительно точечной мутации. Более предпочтительно точечная мутация введена в кодон 913-915 гена zipA, кодируемого SEQ ID NO: 45, или его функционального гомолога, что приводит к замене в положении 305 соответствующего белка аминокислоты аргинин на глицин или другую алифатическую аминокислоту или аминокислоту, родственную глицину, как показано в таблице 2.
Увеличение экспрессии и/или активности гена zipA предпочтительно достигается путем введения мутации в zipA ген, причем мутированный ген zipA характеризуется последовательностью согласно SEQ ID NO: 47, кодирующей белок согласно SEQ ID NO: 48.
Сниженная экспрессия и/или активность ферментов, раскрытых в настоящем документе, в частности сниженная экспрессия и/или сниженная активность фермента, кодируемого геном лактатдегидрогеназы (ldhA), пируватформиатлиазы I (pflB), бифункциональной ацетальдегид-СоА дегидрогеназы/железозависимой алкогольдегидрогеназы/деактивазы пируватформиатлиазы (adhE), фосфатацетилтрансферазы (pta) и/или фумаратредуктазы (frdA), может представлять собой снижение экспрессии и/или ферментативной активности по меньшей мере на 50% по сравнению с экспрессией и/или активностью указанного фермента в соответствующем микроорганизме сравнения, например, диком типе микроорганизма, или снижение экспрессии и/или ферментативной активности по меньшей мере на 90%, или более предпочтительно снижение экспрессии и/или ферментативной активности по меньшей мере на 95%, или более предпочтительно снижение экспрессии и/или ферментативной активности по меньшей мере на 98%, или даже более предпочтительно снижение экспрессии и/или ферментативной активности по меньшей мере на 99%, или даже более предпочтительно снижение экспрессии и/или ферментативной активности по меньшей мере на 99,9%. Согласно наиболее предпочтительному варианту осуществления экспрессия и/или активность ферментов является не обнаруживаемой в микроорганизме согласно настоящему изобретению.
Усиленная или увеличенная экспрессия и/или активность ферментов, раскрытых в настоящем документе, в частности усиленная или увеличенная экспрессия и/или активность фермента, кодируемого геном lpd и/или геном zipA и/или геном ygaW, может представлять собой увеличение экспрессии и/или ферментативной активности по меньшей мере на 25% по сравнению с экспрессией и/или активностью указанного фермента в соответствующем микроорганизме сравнения, например, диком типе микроорганизма, или увеличение экспрессии и/или ферментативной активности по меньшей мере на 50%, или более предпочтительно увеличение экспрессии и/или ферментативной активности по меньшей мере на 100%, или более предпочтительно увеличение экспрессии и/или ферментативной активности по меньшей мере в 3 раза, например, по меньшей мере в 5 раз, или даже более предпочтительно увеличение экспрессии и/или ферментативной активности по меньшей мере в 10 раз, или даже более предпочтительно увеличение экспрессии и/или ферментативной активности по меньшей мере в 20 раз.
Увеличение экспрессии и/или активности гена lpd и/или гена zipA и/или гена ygaW приводит к улучшенному выходу и/или производительности аланина, пирувата, сукцината, аспартата, малата, лактата, валина и/или лейцина, предпочтительно сукцината или аланина, более предпочтительно аланина в рекомбинантном микроорганизме согласно настоящему изобретению по сравнению с соответствующим микроорганизмом сравнения. Следовательно увеличение экспрессии и/или активности гена lpd и/или гена zipA и/или гена ygaW можно определить путем измерения выхода или производительности аланина, пирувата, сукцината, аспартата, малата, лактата, валина и/или лейцина, предпочтительно сукцината или аланина, более предпочтительно аланина в отношении рекомбинантного микроорганизма согласно настоящему изобретению по сравнению с соответствующим микроорганизмом сравнения. Способы ферментативного получения метаболитов, например, аланина, известны специалисту в настоящей области техники, а также описаны в настоящем документе. Улучшенный выход, например, аланина при ферментации микроорганизмом согласно настоящему изобретению по сравнению с выходом аланина при ферментации соответствующим микроорганизмом сравнения представляет собой величину увеличения экспрессии и или активности гена lpd и/или гена zipA и/или гена ygaW.
Способы определения экспрессии или активности лактатдегидрогеназы (ldhA), например, раскрыты Bunch с соавт. в "The ldhA gene encoding the fermentative lactate de hydrogenase of Escherichia Coli", Microbiology (1997), Vol. 143, pages 187-155; или Bergmeyer, H.U., Bergmeyer J. и Grassl, M. (1983-1986) в "Methods of Enzymatic Analysis", 3rd Edition, Volume III, pages 126-133, Verlag Chemie, Weinheim; или Enzymes in Industry: Production and Applications, Second Edition (2004), Wolfgang Aehle, page 23. Предпочтительным является последний способ.
Способы определения экспрессии или активности пируватформиатлиазы I (pflB), например, раскрыты в Knappe J, Blaschkowski HP, Grobner Ρ, Schmitt Τ (1974). "Pyruvate formate-lyase of Escherichia coli: the acetyl-enzyme intermediate." Eur J Biochem 974; 50(1); 253-63. PMID: 4615902; в KNAPPE, Joachim, et al. "Pyruvate Formate-Lyase of Escherichia coli: the Acetyl-Enzyme Intermediate." European Journal of Biochemistry 50.1 (1974): 253-263; в Wong, Kenny K., et al. "Molecular properties of pyruvate formate-lyase activating enzyme." Biochemistry 32.51 (1993): 14102-14110 и в Nnyepi, Mbako R., Yi Peng, and Joan B. Broderick. "Inactivation of E. coli pyruvate formate-lyase: Role of AdhE and small molecules." Archives of biochemistry and biophysics 459.1 (2007): 1-9.
Способы определения экспрессии или активности бифункциональной ацетальдегид-СоА-дегидрогеназы/железозависимой алкогольдегидрогеназы/деактивазы пируватформиатлиазы (adhE), например, раскрыты в  Jorge, et al. "Evolution of the adhE Gene Product of Escherichia coli from a Functional Reductase to a Dehydrogenase GENETIC AND BIOCHEMICAL STUDIES OF THE MUTANT PROTEINS." Journal of Biological Chemistry 275.43 (2000): 33869-33875 и в Mbako R. Nnyepi, Yi Peng, Joan B. Broderick, Inactivation of E. coli pyruvate formate-lyase: Role of AdhE and small molecules, Archives of Biochemistry and Biophysics, Volume 459, Issue 1, 1 March 2007, Pages 1-9.
Jorge, et al. "Evolution of the adhE Gene Product of Escherichia coli from a Functional Reductase to a Dehydrogenase GENETIC AND BIOCHEMICAL STUDIES OF THE MUTANT PROTEINS." Journal of Biological Chemistry 275.43 (2000): 33869-33875 и в Mbako R. Nnyepi, Yi Peng, Joan B. Broderick, Inactivation of E. coli pyruvate formate-lyase: Role of AdhE and small molecules, Archives of Biochemistry and Biophysics, Volume 459, Issue 1, 1 March 2007, Pages 1-9.
Способы определения экспрессии или активности фосфатацетилтрансферазы (pta), например, раскрыты в Dittrich, Cheryl R., George N. Bennett, and Ka-Yiu San. "Characterization of the Acetate-Producing Pathways in Escherichia coli." Biotechnology progress 21.4 (2005): 1062-1067 и в Brown, T.D.Κ., M.С. Jones-Mortimer, and H.L. Kornberg. "The enzymic interconversion of acetate and acetyl-coenzyme A in Escherichia coli." Journal of general microbiology 102.2 (1977): 327-336.
Способы определения экспрессии или активности фумаратредуктазы (frdA), например, раскрыты в Dickie, Peter, and Joel H. Weiner. "Purification and characterization of membrane-bound fumarate reductase from anaerobically grown Escherichia coli." Canadian journal of biochemistry 57.6 (1979): 813-821; в Cecchini, Gary, et al. "Reconstitution of quinone reduction and characterization of Escherichia coli fumarate reductase activity." Journal of Biological Chemistry 261.4 (1986): 1808-1814 и в Schroder, I., et al. "Identification of active site residues of Escherichia coli fumarate reductase by site-directed mutagenesis." Journal of Biological Chemistry 266.21 (1991): 13572-13579.
Способы определения экспрессии или активности аланиндегидрогеназы (alaD) раскрыты, например, в Sakamoto, Y., Nagata, S., Esaki, V., Tanaka, Η., Soda, Κ. "Gene cloning, purification and characterization of thermostable alanine dehydrogenase of Bacillus stearothermophilus" J Fermen. Bioeng. 69 (1990): 154-158.
Термин "сниженная экспрессия фермента" включает в себя, например, экспрессию фермента указанным подвергнутым генетическому воздействию (например, генетически сконструированным) микроорганизмом на более низком уровне, чем он экспрессируется соответствующим микроорганизмом сравнения, например, диким типом указанного микроорганизма. Генетические манипуляции для снижения экспрессии фермента могут включать в себя без ограничения делецию гена или его части, кодирующей фермент, изменение или модификацию регуляторных последовательностей или сайтов, связанных с экспрессией гена, кодирующего фермент (например, путем удаления сильных промоторов или репрессируемых промоторов), модификацию белков (например, регуляторных белков, супрессоров, энхансеров, активаторов транскрипции и подобного), вовлеченных в транскрипцию гена, кодирующего фермент, и/или в трансляцию генного продукта, или любые общепринятые способы снижения экспрессии конкретного гена, рутинные в настоящей области техники (включая в себя без ограничения применение антисмысловых молекул нуклеиновых кислот или других способов для осуществления нокаута или блокирования экспрессии целевого белка). Далее в иРНК могут быть введены дестабилизирующие элементы или генетические модификации, приводящие к повреждению рибосомальных сайтов связывания (RBS) РНК. Также возможно изменить частоту использования кодона гена таким образом, чтобы уменьшалась эффективность и скорость трансляции.
Сниженная активность фермента также может быть получена путем введения одной или более вредных генных мутаций, которые приводят к сниженной активности фермента. Более того, снижение активности фермента также может включать в себя инактивацию (или сниженную экспрессию) активирующих ферментов, которые необходимы для активации фермента, активность которого подлежит снижению. В соответствии с последним подходом фермент, активность которого подлежит снижению, предпочтительно поддерживается в инактивированном состоянии.
Вредная мутация может представлять собой любую мутацию в пределах гена, содержащего промотор и кодирующую область, которая приводит к сниженной или удаленной активности белка, кодируемого кодирующей областью гена. Такие вредные мутации предусматривают, например, сдвиги рамки считывания, введение стоп-кодонов в кодирующую область, мутацию промоторных элементов, таких как ТАТА-бокс, которая препятствует транскрипции, и подобное.
Микроорганизмы, характеризующиеся увеличенной или усиленной экспрессией и/или активностью фермента, кодируемого геном Lpd и/или геном zipA и/или геном ygaW, могут возникать в природе, а именно вследствие спонтанных мутаций. Микроорганизм может быть модифицирован так, чтобы он характеризовался значительно увеличенной активностью фермента, кодируемого одним или более из указанных генов, с помощью различных техник, таких как химическая обработка или облучение. С этой целью микроорганизмы будут обработаны, например, вызывающим мутагенез химическим средством, рентгеновскими лучами или ультрафиолетовым облучением. На последующей стадии будут отобраны те микроорганизмы, которые характеризуются увеличенной экспрессией и/или активностью фермента, кодируемого одним или более из указанных генов. Рекомбинантные микроорганизмы также могут быть получены с помощью техник гомологичной рекомбинации, которые содействуют замещению одного или более указанных генов соответствующим геном, который кодирует фермент, который по сравнению с ферментом, кодируемым геном дикого типа, характеризуется увеличенной экспрессией и/или активностью.
Согласно одному варианту осуществления рекомбинантного микроорганизма согласно настоящему изобретению увеличение экспрессии и/или активности фермента, кодируемого геном lpd и/или геном zipA и/или геном ygaW, можно достичь путем модификации гена lpd и/или гена zipA и/или гена ygaW, причем эта/эти генная(ые) модификация(и) предпочтительно реализуются путем увеличения числа копий гена lpd и/или гена zipA и/или гена ygaW в геноме микроорганизма, путем введения гена на самореплицирующемся экспрессионном векторе в микроорганизм, путем обмена промотора гена lpd и/или гена zipA и/или гена ygaW на более сильный промотор или путем превращения эндогенного промотора гена в более сильный промотор, например, путем введения точечных мутаций в промоторную последовательность.
Дополнительно активность гена lpd и/или гена zipA и/или гена ygaW может быть усилена путем мутирования гена для достижения замен аминокислот в белке, которые улучшают активность гена. Такие способы известны специалисту в настоящей области техники.
Мутация в описанный выше ген может быть введена, например, путем сайт-направленного или случайного мутагенеза с последующим введением модифицированного гена в геном микроорганизма путем рекомбинации. Варианты генов могут быть сконструированы путем мутирования генных последовательностей посредством ПЦР. Набор "Quickchange Site-directed Mutagenesis Kit" (Stratagene) можно использовать для проведения направленного мутагенеза. Случайный мутагенез в пределах полной кодирующей последовательности, или же только ее части, можно провести при помощи набора "GeneMorph II Random Mutagenesis Kit" (Stratagene). Частоту мутагенеза устанавливают до требуемого количества мутаций посредством используемого количества матричной ДНК. Множественные мутации создаются путем направленной комбинации отдельных мутаций или путем последовательного проведения нескольких циклов мутагенеза.
Ниже описана подходящая техника рекомбинации, в частности, для введения мутации или для делеции последовательностей.
Указанная техника также иногда в настоящем документе называется "рекомбинация Campbell" (Leenhouts et al., Appl Env Microbiol. (1989), Vol. 55, pages 394-400). Используемый в настоящем документе термин "Campbell in" относится к трансформанту исходной клетки - хозяина, у которого целая кольцевая двухцепочечная молекула ДНК (например, плазмида) интегрирована в хромосому с помощью одного события гомологичной рекомбинации (событие введения), и которое эффективно дает в результате вставку линеаризированной версии указанной кольцевой молекулы ДНК в первую последовательность ДНК хромосомы, которая является гомологичной первой последовательности ДНК указанной кольцевой молекулы ДНК. Термин "подвергнутый процедуре Campbell in" относится к линеаризированной последовательности ДНК, которая была интегрирована в хромосому трансформанта "Campbell in". "Campbell in" содержит дупликацию первой последовательности гомологичной ДНК, каждая копия которой включает в себя и окружает копию кроссоверного сайта гомологичной рекомбинации.
Используемый в настоящем документе термин "Campbell out" относится к клетке, происходящей от трансформанта "Campbell in", в которой второе событие гомологичной рекомбинации (событие удаления) произошло между второй последовательностью ДНК, которая содержится на линеаризированной вставленной ДНК, подвергнутой процедуре "Campbell in" ДНК, и второй последовательностью ДНК хромосомного происхождения, которая является гомологичной второй последовательности ДНК указанной линеаризированной вставки, причем второе событие рекомбинации приводит к делеции (удалению) части интегрированной последовательности ДНК, но, что важно, также приводит к тому, что часть (она может составлять не больше одного основания) интегрированной подвергнутой процедуре "Campbell in" ДНК остается в хромосоме так, что по сравнению с исходной клеткой хозяином, клетка "Campbell out" содержит одно или более преднамеренных изменений в хромосоме (например, замена одного основания, множественные замены оснований, вставка гетерологичного гена или последовательности ДНК, вставка дополнительной копии или копий гомологичного гена или модифицированного гомологичного гена или вставка последовательности ДНК, содержащей более одного из вышеперечисленных примеров, представленных выше). Клетку "Campbell out" предпочтительно получают с помощью противоселекции против гена, который содержится в части (части, которая, желательно, должна быть удалена) последовательности ДНК, подвергнутой процедуре "Campbell in", например, ген sacB Bacillus subtilis, который является летальным, если экспрессируется в клетке, которую выращивают в присутствии приблизительно 5%-10% сахарозы. Либо с помощью противоселекции, либо без нее, требуемая клетка "Campbell out" может быть получена или идентифицирована путем скрининга в отношении требуемой клетки с использованием любого подлежащего скринингу фенотипа, такого как без ограничения морфология колоний, цвет колоний, присутствие или отсутствие устойчивости к антибиотикам, присутствие или отсутствие данной последовательности ДНК, определяемое с помощью полимеразной цепной реакции, присутствие или отсутствие ауксотрофии, присутствие или отсутствие фермента, гибридизация нуклеиновых кислот колонии, скрининг антител и т.д. Термин "Campbell in" и "Campbell out" также можно использовать как глаголы в различных временах для обозначения способа или процесса, описанного выше.
Следует понимать, что события гомологичной рекомбинации, которые приводят к "Campbell in" или "Campbell out", могут происходить в диапазоне оснований ДНК в пределах гомологичной последовательности ДНК, и поскольку гомологичные последовательности будут идентичны друг другу по меньшей мере в части этого диапазона, не всегда можно точно установить, где произошло событие кроссовера. Другими словами, невозможно с точностью установить, какая последовательность изначально происходила из вставленной ДНК, а какая исходно была из хромосомной ДНК. Более того, первую последовательность гомологичной ДНК и вторую последовательность гомологичной ДНК, как правило, разделяют посредством области частичного отсутствия гомологии, и это представляет собой ту область отсутствия гомологии, которая сохраняется в хромосоме клетки "Campbell out".
Первая и вторая гомологичная последовательность ДНК по меньшей мере предпочтительно составляют приблизительно 200 пар нуклеотидов в длину, и могут составлять до нескольких тысяч пар нуклеотидов в длину. Тем не менее, можно произвести определенную процедуру для работы с более короткими или более длинными последовательностями. Например, длина первой и второй гомологичных последовательностей может находиться в диапазоне от приблизительно 500 до 2000 нуклеотидов, и получение "Campbell out" из "Campbell in" облегчается путем компоновки первой и второй гомологичных последовательностей так, чтобы они были приблизительно одинаковой длины, предпочтительно с различием меньше чем в 200 парах нуклеотидов и наиболее предпочтительно, чтобы более короткая из двух составляла по меньшей мере 70% длины более длинной в парах нуклеотидов.
Согласно одному варианту осуществления индукция экспрессии и/или активности lpd достигается путем активации гена lpd, который кодирует липоамиддегидрогеназу.
Согласно одному варианту осуществления индукция экспрессии и/или активности zipA достигается путем активации гена zipA, который кодирует белок клеточного деления, вовлеченный в сборку Z-кольца.
Используемые в контексте настоящего изобретения термины "аланин, пируват, сукцинат, аспартат, малат, лактат, валин и/или лейцин следует понимать в их самом широком смысле, а также они охватывают их соли, как, например, соли щелочных металлов, такие как соли Na+ и K+, или соли щелочно-земельных металлов, такие как соли Mg2+ и Са2+, или соли аммония или ангидриды аланина, пирувата, сукцината, аспартата, малата, лактата, валина и/или лейцина.
Предпочтительно аланин, пируват, сукцинат, аспартат, малат, лактат, валин и/или лейцин, предпочтительно сукцинат или аланин, более предпочтительно аланин получают при микроаэробных условиях. Также можно использовать аэробные или анаэробные условия.
Микроаэробный означает, что концентрация кислорода меньше, чем таковая в воздухе. Согласно одному варианту осуществления микроаэробный означает давление кислорода, составляющее от 5 до 27 мм рт.ст., предпочтительно 10-20 мм рт.ст. (Megan Falsetta et al. (2011), The composition and metabolic phenotype of Neisseria gonorrhoeae biofilms, Frontiers in Microbiology, Vol 2, page 1-11). Микроаэробные условия предпочтительно устанавливают при потоке воздуха, составляющем 0,1-1 объем/объем/мин.
Анаэробные условия можно установить посредством общепринятых техник, как, например, путем дегазации компонентов реакционной среды и поддержания анаэробных условий путем введения диоксида углерода или азота или их смесей и необязательно водорода при объемной скорости потока, составляющей, например, 0,1-1 или 0,2-0,5 объем/объем/мин. Аэробные условия можно установить посредством общепринятых техник, как, например, путем введения воздуха или кислорода при объемной скорости потока, составляющей, например, 0,1-1 или 0,2-0,5 объем/объем/мин. При необходимости к процессу можно приложить небольшое избыточное давление, составляющее 0,1-1,5 бар.
Согласно одному варианту осуществления способа согласно настоящему изобретению ассимилируемый источник углерода может представлять собой глюкозу, глицерин, глюкозу, мальтозу, мальтодекстрин, фруктозу, галактозу, маннозу, ксилозу, сахарозу, арабинозу, лактозу, раффинозу и их комбинации.
Согласно предпочтительному варианту осуществления ассимилируемый источник углерода представляет собой глюкозу, сахарозу, ксилозу, арабинозу, глицерин или их комбинации. Предпочтительные источники углерода представляют собой глюкозу, сахарозу, глюкозу и сахарозу, глюкозу и ксилозу и/или глюкозу, арабинозу и ксилозу. Согласно одному варианту осуществления способа согласно настоящему изобретению ассимилируемый источник углерода может представлять собой сахарозу, глицерин и/или глюкозу.
Начальную концентрацию ассимилируемого источника углерода, предпочтительно начальную концентрацию предпочтительно доводят до значения в диапазоне, составляющем 5-250 г/л, предпочтительно 50-200 г/л и более предпочтительно 125-150 г/л и ее могут поддерживать в указанном диапазоне в течение культивирования. рН реакционной смеси можно контролировать путем добавления подходящих оснований, например, газообразного аммиака, NH4OH NH4HCO3, (NH4)2CO3, NaOH, Na2CO3, NaHCO3, KOH, K2CO3, KHCO3, Mg(OH)2, MgCO3, Mg(HCO3)2, Ca(OH)2, СаСО3, Ca(HCO3)2, CaO, CH6N2O2, C2H7N и/или их смесей.
Согласно другому варианту осуществления настоящего изобретения предусмотрен способ ферментативного получения аланина, пирувата, сукцината, аспартата, малата, лактата, валина и/или лейцина, предпочтительно сукцината или аланина, более предпочтительно аланина, наиболее предпочтительно L-аланина, предусматривающий следующие стадии
I) выращивание микроорганизма согласно настоящему изобретению согласно приведенному выше определению в ферментере и
II) извлечение аланина, пирувата, сукцината, аспартата, малата, лактата, валина и/или лейцина, предпочтительно сукцината или аланина, более предпочтительно аланина, наиболее предпочтительно L-аланина из ферментативного бульона, полученного в I).
Стадию ферментации I) согласно настоящему изобретению, например, можно проводить в ферментерах с мешалкой, барботажных колонках и петлевых реакторах. Исчерпывающий обзор возможных типов способа, включая в себя типы с мешалкой и геометрические решения, можно найти в Chmiel: "Bioprozesstechnik:  in die Bioverfahrenstechnik", Volume 1. В способе согласно настоящему изобретению типичные доступные варианты представляют собой следующие варианты, известные специалистам в настоящей области техники или объясняемые, например, в Chmiel, Hammes and Bailey: "Biochemical Engineering", такие как периодическая ферментация, периодическая ферментация с добавлением субстрата, многократная периодическая ферментация с добавлением субстрата или другая непрерывная ферментация с рециркуляцией биомассы или без нее. В зависимости от штамма, участвующего в производстве, барботирование воздухом, кислородом, диоксидом углерода, водородом, азотом или соответствующими газовыми смесями может быть эффективным для достижения высокого выхода (YP/S (выход продукта/субстрат)).
in die Bioverfahrenstechnik", Volume 1. В способе согласно настоящему изобретению типичные доступные варианты представляют собой следующие варианты, известные специалистам в настоящей области техники или объясняемые, например, в Chmiel, Hammes and Bailey: "Biochemical Engineering", такие как периодическая ферментация, периодическая ферментация с добавлением субстрата, многократная периодическая ферментация с добавлением субстрата или другая непрерывная ферментация с рециркуляцией биомассы или без нее. В зависимости от штамма, участвующего в производстве, барботирование воздухом, кислородом, диоксидом углерода, водородом, азотом или соответствующими газовыми смесями может быть эффективным для достижения высокого выхода (YP/S (выход продукта/субстрат)).
Особенно предпочтительные условия для получения аланина, пирувата, сукцината, аспартата, малата, лактата, валина и/или лейцина, предпочтительно сукцината или аланина, более предпочтительно аланина, наиболее предпочтительно L-аланина на стадии способа I) представляют собой следующие:
Ассимилируемый источник углерода: глюкоза
Температура: 30-45°С
рН: 6,0-7,0
Микроаэробные условия
На стадии способа II) аланин извлекают из ферментативного бульона, полученного на стадии способа I).
Как правило, способ извлечения предусматривает стадию отделения рекомбинантных микроорганизмов от ферментативного бульона в виде так называемой "биомассы". Способы удаления биомассы известны специалистам в настоящей области техники и предусматривают фильтрацию, седиментацию, флотацию или их комбинацию. Впоследствии биомассу можно удалить, например, с помощью центрифуг, сепараторов, декантаторов, фильтров или во флотационном приборе. Для максимального извлечения представляющего ценность продукта зачастую предусмотрено промывание биомассы, например, в форме диафильтрации. Выбор способа зависит от содержания биомассы в ферментативном бульоне и свойств биомассы, а также взаимодействия биомассы с органическим соединением (т.е. представляющим ценность продуктом). Согласно одному варианту осуществления ферментативный бульон можно стерилизовать или пастеризовать. Согласно дополнительному варианту осуществления ферментативный бульон концентрируют. В зависимости от требования указанное концентрирование можно выполнить по партиям или непрерывно. Диапазон давлений и температуры необходимо выбирать так, чтобы, во-первых, не происходило повреждение продукта, и, во-вторых, требовалась минимальная эксплуатация устройства и потребление энергии. Квалифицированный выбор уровней давления и температуры для многостадийного выпаривания, в частности, обеспечивает экономию энергии.
Способ извлечения может дополнительно предусматривать дополнительные стадии очистки, на которых продукт ферментации дополнительно очищают. Тем не менее, если продукт ферментации превращается во вторичный органический продукт в результате химической реакции, как описано ниже, дополнительная очистка продукта ферментации, в зависимости от типа реакции и условий реакции, не является необходимой. Для очистки продукта ферментации, полученного на стадии способа II), можно использовать способы, известные специалисту в настоящей области техники, например, кристаллизацию, фильтрацию, электродиализ и хроматографию. Полученный раствор можно дополнительно очистить посредством ионообменной хроматографии для удаления нежелательных остаточных ионов.
Согласно одному варианту осуществления усиленная или увеличенная экспрессия и/или активность гена Lpd достигается путем введения мутации в ген дикого типа. Предпочтительно это достигается путем введения специфической мутации в кодон в положении 208-210 гена дикого типа, характеризующегося SEQ ID NO: 1, или ее функциональный вариант.
Следовательно, согласно дополнительному варианту осуществления настоящего изобретения предусмотрена рекомбинантная молекула нуклеиновой кислоты, характеризующаяся последовательностью, выбранной из следующей группы:
(1) молекула нуклеиновой кислоты, содержащая последовательность SEQ ID NO: 49, или
(2) молекула нуклеиновой кислоты, характеризующаяся по меньшей мере 80%, предпочтительно по меньшей мере 85%, например, по меньшей мере 90%, более предпочтительно по меньшей мере 95%, например, по меньшей мере 96%, даже более предпочтительно по меньшей мере 97%, например, по меньшей мере 98%, наиболее предпочтительно по меньшей мере 99% идентичностью относительно молекулы нуклеиновой кислоты согласно SEQ ID NO: 49, или
(3) молекула нуклеиновой кислоты, гибридизующаяся с молекулой нуклеиновой кислоты, характеризующейся SEQ ID NO: 49, при условиях средней жесткости, более предпочтительно при условиях высокой жесткости, наиболее предпочтительно при условиях очень высокой жесткости, или
(4) молекула нуклеиновой кислоты, кодирующая полипептид согласно SEQ ID NO: 50, или
(5) молекула нуклеиновой кислоты, кодирующая полипептид, характеризующийся по меньшей мере 60%, предпочтительно по меньшей мере 70%, например, по меньшей мере 75%, более предпочтительно по меньшей мере 80%, например, по меньшей мере 85%, даже более предпочтительно по меньшей мере 90%, например, по меньшей мере 95%, наиболее предпочтительно по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% гомологией относительно полипептида согласно SEQ ID NO: 50, и
причем кодон генов согласно (1)-(5), соответствующий положения 208-210 в SEQ ID NO: 49, не кодирует аминокислоту аланин и не представляет собой стоп-кодон, или аминокислота белков, кодируемых генами согласно (1)-(5), соответствующая положению 70 в SEQ ID NO: 50, не представляет собой аланин, и
причем белок, кодируемый геном согласно приведенному выше определению в (1)-(5), характеризуется усиленной или увеличенной активностью по сравнению с белком, характеризующимся SEQ ID NO: 50, и
причем микроорганизм, содержащий мутированный ген и/или белок согласно приведенному выше определению, характеризуется улучшенным выходом аланина в ферментации.
Рекомбинантная молекула нуклеиновой кислоты предпочтительно характеризуется последовательностью, выбранной из следующей группы:
(6) молекула нуклеиновой кислоты, содержащая последовательность SEQ ID NO: 51, или
(7) молекула нуклеиновой кислоты, характеризующаяся по меньшей мере 80%, предпочтительно по меньшей мере 85%, например, по меньшей мере 90%, более предпочтительно по меньшей мере 95%, например, по меньшей мере 96%, даже более предпочтительно по меньшей мере 97%, например, по меньшей мере 98%, наиболее предпочтительно по меньшей мере 99% идентичностью относительно молекулы нуклеиновой кислоты согласно SEQ ID NO: 51, или
(8) молекула нуклеиновой кислоты, гибридизующаяся с молекулой нуклеиновой кислоты, характеризующейся SEQ ID NO: 51, при условиях средней жесткости, более предпочтительно при условиях высокой жесткости, наиболее предпочтительно при условиях очень высокой жесткости, или
(9) молекула нуклеиновой кислоты, кодирующая полипептид согласно SEQ ID NO: 52, или
(10) молекула нуклеиновой кислоты, кодирующая полипептид, характеризующийся по меньшей мере 60%, предпочтительно по меньшей мере 70%, например, по меньшей мере 75%, более предпочтительно по меньшей мере 80%, например, по меньшей мере 85%, даже более предпочтительно по меньшей мере 90%, например, по меньшей мере 95%, наиболее предпочтительно по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% гомологией относительно полипептида согласно SEQ ID NO: 52,
причем кодон генов согласно (7)-(10), соответствующий положению 208-210 в SEQ ID NO: 51, кодирует аминокислоту пролин, или аминокислота белков, кодируемых генами согласно (7)-(10), соответствующая положению 70 в SEQ ID NO: 52, представляет собой пролин, и
причем белок, кодируемый геном согласно приведенному выше определению в (7)-(10), характеризуется усиленной или увеличенной активностью по сравнению с белком, характеризующимся SEQ ID NO: 52, и
причем микроорганизм, содержащий мутированный ген и/или белок согласно приведенному выше определению, характеризуется улучшенным выходом аланина в ферментации.
Согласно другому варианту осуществления усиленная, увеличенная или измененная экспрессия и/или активность гена zipA достигается путем введения мутации в ген дикого типа. Предпочтительно это достигается путем введения специфической мутации в кодон в положении 913-915 гена дикого типа, характеризующегося SEQ ID NO: 45, или ее функциональный вариант.
Следовательно, согласно дополнительному варианту осуществления настоящего изобретения предусмотрена рекомбинантная молекула нуклеиновой кислоты, характеризующаяся последовательностью, выбранной из следующей группы:
(1) молекула нуклеиновой кислоты, содержащая последовательность SEQ ID NO: 45, или
(2) молекула нуклеиновой кислоты, характеризующаяся по меньшей мере 80%, предпочтительно по меньшей мере 85%, например, по меньшей мере 90%, более предпочтительно по меньшей мере 95%, например, по меньшей мере 96%, даже более предпочтительно по меньшей мере 97%, например, по меньшей мере 98%, наиболее предпочтительно по меньшей мере 99% идентичностью относительно молекулы нуклеиновой кислоты согласно SEQ ID NO: 45, или
(3) молекула нуклеиновой кислоты, гибридизующаяся с молекулой нуклеиновой кислоты, характеризующейся SEQ ID NO: 45, при условиях средней жесткости, более предпочтительно при условиях высокой жесткости, наиболее предпочтительно при условиях очень высокой жесткости, или
(4) молекула нуклеиновой кислоты, кодирующая полипептид согласно SEQ ID NO: 46, или
(5) молекула нуклеиновой кислоты, кодирующая полипептид, характеризующийся по меньшей мере 60%, предпочтительно по меньшей мере 70%, например, по меньшей мере 75%, более предпочтительно по меньшей мере 80%, например, по меньшей мере 85%, даже более предпочтительно по меньшей мере 90%, например, по меньшей мере 95%, наиболее предпочтительно по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% гомологией относительно полипептида согласно SEQ ID NO: 46, и
причем кодон генов согласно (1)-(5), соответствующий положению 913-915 в SEQ ID NO: 45, не кодирует аминокислоту аргинин и не представляет собой стоп-кодон, или аминокислота белков, кодируемых генами согласно (1)-(5), соответствующая положению 305 в SEQ ID NO: 46, не представляет собой аргинин, и
причем белок, кодируемый геном согласно приведенному выше определению в (1)-(5), характеризуется усиленной или увеличенной или измененной активностью по сравнению с белком, характеризующимся SEQ ID NO: 46, и
причем микроорганизм, содержащий мутированный ген и/или белок согласно приведенному выше определению, характеризуется улучшенным выходом аланина в ферментации.
Рекомбинантная молекула нуклеиновой кислоты предпочтительно характеризуется последовательностью, выбранной из следующей группы:
(6) молекула нуклеиновой кислоты, содержащая последовательность SEQ ID NO: 47, или
(7) молекула нуклеиновой кислоты, характеризующаяся по меньшей мере 80%, предпочтительно по меньшей мере 85%, например, по меньшей мере 90%, более предпочтительно по меньшей мере 95%, например, по меньшей мере 96%, даже более предпочтительно по меньшей мере 97%, например, по меньшей мере 98%, наиболее предпочтительно по меньшей мере 99% идентичностью относительно молекулы нуклеиновой кислоты согласно SEQ ID NO: 47, или
(8) молекула нуклеиновой кислоты, гибридизующаяся с молекулой нуклеиновой кислоты, характеризующейся SEQ ID NO: 47, при условиях средней жесткости, более предпочтительно при условиях высокой жесткости, наиболее предпочтительно при условиях очень высокой жесткости, или
(9) молекула нуклеиновой кислоты, кодирующая полипептид согласно SEQ ID NO: 48, или
(10) молекула нуклеиновой кислоты, кодирующая полипептид, характеризующийся по меньшей мере 60%, предпочтительно по меньшей мере 70%, например, по меньшей мере 75%, более предпочтительно по меньшей мере 80%, например, по меньшей мере 85%, даже более предпочтительно по меньшей мере 90%, например, по меньшей мере 95%, наиболее предпочтительно по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% гомологией относительно полипептида согласно SEQ ID NO: 48,
причем ко дон генов согласно (7)-(10), соответствующий положению 913-915 в SEQ ID NO: 47, кодирует аминокислоту глицин или родственную аминокислоту или другую алифатическую аминокислоту, или аминокислота белков, кодируемых генами согласно (7)-(10), соответствующая положению 305 в SEQ ID NO: 48, представляет собой глицин или родственную аминокислоту или другую алифатическую аминокислоту, и
причем белок, кодируемый геном согласно приведенному выше определению в (7)-(10), характеризуется усиленной, увеличенной или измененной активностью по сравнению с белком, характеризующимся SEQ ID NO: 48, и
причем микроорганизм, содержащий мутированный ген и/или белок согласно приведенному выше определению, характеризуется улучшенным выходом аланина в ферментации.
Согласно одному варианту осуществления усиленный или увеличенный выход и/или производительность аланина или родственных соединений достигается путем введения мутации в ген ygaW дикого типа.
Следовательно, согласно одному варианту осуществления настоящего изобретения предусмотрена рекомбинантная молекула нуклеиновой кислоты, характеризующаяся последовательностью, выбранной из следующей группы:
(1) молекула нуклеиновой кислоты, содержащая последовательность SEQ ID NO: 1, или
(2) молекула нуклеиновой кислоты, характеризующаяся по меньшей мере 80%, предпочтительно по меньшей мере 85%, например, по меньшей мере 90%, более предпочтительно по меньшей мере 95%, например, по меньшей мере 96%, даже более предпочтительно по меньшей мере 97%, например, по меньшей мере 98%, наиболее предпочтительно по меньшей мере 99% идентичностью относительно молекулы нуклеиновой кислоты согласно SEQ ID NO: 1, или
(3) молекула нуклеиновой кислоты, гибридизующаяся с молекулой нуклеиновой кислоты, характеризующейся SEQ ID NO: 1, при условиях средней жесткости, более предпочтительно при условиях высокой жесткости, наиболее предпочтительно при условиях очень высокой жесткости, или
(4) молекула нуклеиновой кислоты, кодирующая полипептид согласно SEQ ID NO: 2, или
(5) молекула нуклеиновой кислоты, кодирующая полипептид, характеризующийся по меньшей мере 60%, предпочтительно по меньшей мере 70%, например, по меньшей мере 75%, более предпочтительно по меньшей мере 80%, например, по меньшей мере 85%, даже более предпочтительно по меньшей мере 90%, например, по меньшей мере 95%, наиболее предпочтительно по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% гомологией относительно полипептида согласно SEQ ID NO: 2, и
причем кодон генов согласно (1)-(5), соответствующий положению 13-15 в SEQ ID NO: 1, не кодирует аминокислоту глутамин и не представляет собой стоп-кодон, или аминокислота белков, кодируемых генами согласно (1)-(5), соответствующая положению 5 в SEQ ID NO: 2, не представляет собой глутамин, и
причем белок, кодируемый геном согласно приведенному выше определению в (1)-(5), характеризуется измененной активностью и/или экспрессией по сравнению с белком, характеризующимся SEQ ID NO: 2, и
причем микроорганизм, содержащий мутированный ген и/или белок согласно приведенному выше определению, характеризуется улучшенным выходом аланина в ферментации.
Рекомбинантная молекула нуклеиновой кислоты предпочтительно характеризуется последовательностью, выбранной из следующей группы:
(6) молекула нуклеиновой кислоты, содержащая последовательность SEQ ID NO: 3, 56, 58 или 60, или
(7) молекула нуклеиновой кислоты, характеризующаяся по меньшей мере 80%, предпочтительно по меньшей мере 85%, например, по меньшей мере 90%, более предпочтительно по меньшей мере 95%, например, по меньшей мере 96%, даже более предпочтительно по меньшей мере 97%, например, по меньшей мере 98%, наиболее предпочтительно по меньшей мере 99% идентичностью относительно молекулы нуклеиновой кислоты согласно SEQ ID NO: 3, 56, 58 или 60, или
(8) молекула нуклеиновой кислоты, гибридизующаяся с молекулой нуклеиновой кислоты, характеризующейся SEQ ID NO: 3, 56, 58 или 60, при условиях средней жесткости, более предпочтительно при условиях высокой жесткости, наиболее предпочтительно при условиях очень высокой жесткости, или
(9) молекула нуклеиновой кислоты, кодирующая полипептид согласно SEQ ID NO: 4, 57, 59 или 60, или
(10) молекула нуклеиновой кислоты, кодирующая полипептид, характеризующийся по меньшей мере 60%, предпочтительно по меньшей мере 70%, например, по меньшей мере 75%, более предпочтительно по меньшей мере 80%, например, по меньшей мере 85%, даже более предпочтительно по меньшей мере 90%, например, по меньшей мере 95%, наиболее предпочтительно по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% гомологией относительно полипептида согласно SEQ ID NO: 4, 57, 59 или 60,
причем кодон генов согласно (7)-(10), соответствующий положению 13-15 в SEQ ID NO: 3, кодирует аминокислоту гистидин или родственную аминокислоту или другую основную аминокислоту или кодирует аминокислоту аспарагин или родственную аминокислоту или другую алифатическую аминокислоту или кодирует аминокислоту аргинин или родственную аминокислоту или другую алифатическую аминокислоту или кодирует аминокислоту тирозин или родственную аминокислоту или другую ароматическую аминокислоту, или аминокислота белков, кодируемых генами согласно (7)-(10), соответствующая положению 5 в SEQ ID NO: 2, представляет собой гистидин или родственную аминокислоту или другую основную аминокислоту, или представляет собой аспарагин или родственную аминокислоту или другую алифатическую аминокислоту, или представляет собой аргинин или родственную аминокислоту или другую алифатическую аминокислоту, или представляет собой тирозин или родственную аминокислоту или другую ароматическую аминокислоту, и
причем белок, кодируемый геном согласно приведенному выше определению в (7)-(10), характеризуется измененной активностью и/или экспрессией по сравнению с белком, характеризующимся SEQ ID NO: 2, и
причем микроорганизм, содержащий мутированный ген и/или белок согласно приведенному выше определению, характеризуется улучшенным выходом аланина в ферментации.
Термин "родственная аминокислота" или "консервативная аминокислотная замена" означает, что аминокислота заменена аминокислотой, характеризующейся сходной боковой цепью. Перечень родственных аминокислот представлен в таблице 2 ниже. Таблицы консервативных замен хорошо известны в настоящей области техники (см., например, Creighton (1984) Proteins. W.H. Freeman and Company (Eds) и таблицу 2 ниже).
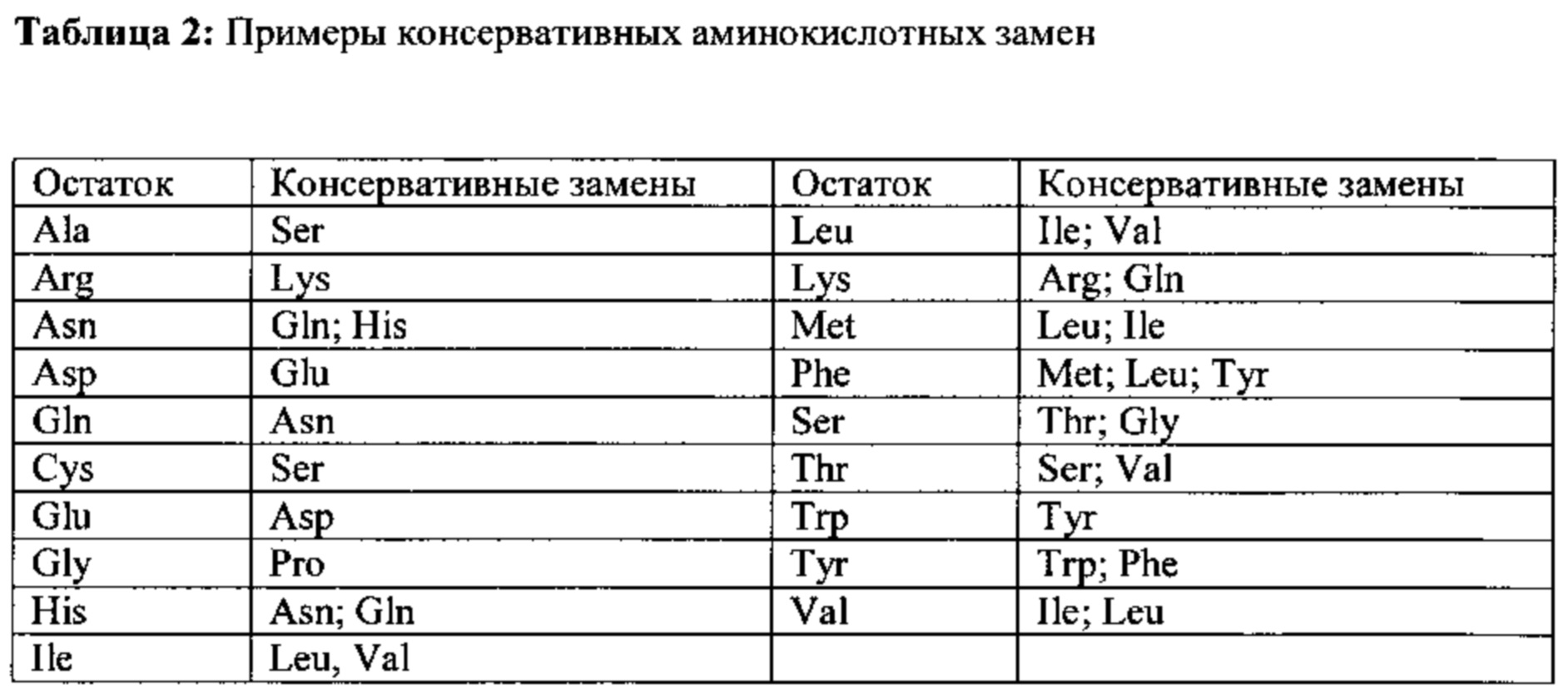
Согласно предпочтительному варианту осуществления рекомбинантная молекула нуклеиновой кислоты характеризуется SEQ ID NO: 3, 56, 58, 60, 47 или 51 и кодирует белок, характеризующийся SEQ ID NO: 4, 57, 59, 61, 48 или 52.
Согласно дополнительному варианту осуществления настоящего изобретения предусмотрена рекомбинантная молекула аминокислоты, характеризующаяся последовательностью, выбранной из следующей группы:
(11) молекула аминокислоты, содержащая последовательность согласно SEQ ID NO: 52, или
(12) молекула аминокислоты, характеризующаяся 60%, предпочтительно по меньшей мере 70%, например, по меньшей мере 75%, более предпочтительно по меньшей мере 80%, например, по меньшей мере 85%, даже более предпочтительно по меньшей мере 90%, например, по меньшей мере 95%, наиболее предпочтительно по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% гомологией относительно полипептида согласно SEQ ID NO: 52,
причем аминокислота белка согласно (12), соответствующая положению 70 в SEQ ID NO: 52, представляет собой пролин, и
причем белок согласно приведенному выше определению в (12) характеризуется усиленной или увеличенной активностью по сравнению с белком, характеризующимся SEQ ID NO: 50, и
причем микроорганизм, содержащий мутированный ген и/или белок согласно приведенному выше определению, характеризуется улучшенным выходом аланина в ферментации.
Рекомбинантная молекула аминокислоты согласно настоящему изобретению предпочтительно характеризуется SEQ ID NO: 52.
Согласно дополнительному варианту осуществления настоящего изобретения предусмотрена рекомбинантная молекула аминокислоты, характеризующаяся последовательностью, выбранной из следующей группы:
(11) молекула аминокислоты, содержащая последовательность согласно SEQ ID NO: 48, или
(12) молекула аминокислоты, характеризующаяся 60%, предпочтительно по меньшей мере 70%, например, по меньшей мере 75%, более предпочтительно по меньшей мере 80%, например, по меньшей мере 85%, даже более предпочтительно по меньшей мере 90%, например, по меньшей мере 95%, наиболее предпочтительно по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% гомологией относительно полипептида согласно SEQ ID NO: 48,
причем аминокислота белка согласно (12), соответствующая положению 305 в SEQ ID NO: 48, представляет собой глицин или родственную аминокислоту или другую алифатическую аминокислоту, и
причем белок согласно приведенному выше определению в (12) характеризуется усиленной, увеличенной или измененной активностью по сравнению с белком, характеризующимся SEQ ID NO: 46, и
причем микроорганизм, содержащий мутированный ген и/или белок согласно приведенному выше определению, характеризуется улучшенным выходом аланина в ферментации.
Рекомбинантная молекула аминокислоты согласно настоящему изобретению предпочтительно характеризуется SEQ ID NO: 48.
Согласно дополнительному варианту осуществления настоящего изобретения предусмотрена рекомбинантная молекула аминокислоты, характеризующаяся последовательностью, выбранной из следующей группы:
(11) молекула аминокислоты, содержащая последовательность согласно SEQ ID NO: 4, 57, 59 или 61, или
(12) молекула аминокислоты, характеризующаяся 60%, предпочтительно по меньшей мере 70%, например, по меньшей мере 75%, более предпочтительно по меньшей мере 80%, например, по меньшей мере 85%, даже более предпочтительно по меньшей мере 90%, например, по меньшей мере 95%, наиболее предпочтительно по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% гомологией относительно полипептида согласно SEQ ID NO: 4, 57, 59 или 61
причем аминокислота белка согласно (12), соответствующая положению 5 в SEQ ID NO: 4, представляет собой гистидин или родственную аминокислоту или другую основную аминокислоту, и
причем аминокислота белка согласно (12), соответствующая положению 5 в SEQ ID NO: 57, представляет собой аспарагин или родственную аминокислоту или другую алифатическую аминокислоту, и
причем аминокислота белка согласно (12), соответствующая положению 5 в SEQ ID NO: 59, представляет собой аргинин или родственную аминокислоту или другую алифатическую аминокислоту и
причем аминокислота белка согласно (12), соответствующая положению 5 в SEQ ID NO: 61, представляет собой тирозин или родственную аминокислоту или другую ароматическую аминокислоту, и
причем белок согласно приведенному выше определению в (12) характеризуется измененной активностью и/или экспрессией по сравнению с белком, характеризующимся SEQ ID NO: 2, и
причем микроорганизм, содержащий мутированный ген и/или белок согласно приведенному выше определению, характеризуется улучшенным выходом аланина в ферментации.
Рекомбинантная молекула аминокислоты согласно настоящему изобретению предпочтительно характеризуется SEQ ID NO: 4, 57, 59 или 61.
Согласно дополнительному варианту осуществления настоящего изобретения обеспечивается рекомбинантная экспрессионная конструкция, содержащая промотор, являющийся функциональным в микроорганизме, функционально связанный с нуклеиновой кислотой согласно приведенному выше определению в (1)-(5).
Согласно дополнительному варианту осуществления настоящего изобретения предусмотрен рекомбинантный вектор, содержащий молекулу нуклеиновой кислоты согласно приведенному выше определению в (1)-(5) или рекомбинантную экспрессионную конструкцию согласно приведенному выше определению.
Согласно дополнительному варианту осуществления настоящего изобретения предусмотрен промотор, являющийся функциональным в микроорганизме, например, Е. Coli, характеризующийся последовательностью, выбранной из следующей группы:
(I) молекула нуклеиновой кислоты, содержащая последовательность SEQ ID NO: 54 или 55, или
(II) молекула нуклеиновой кислоты, характеризующаяся по меньшей мере 80%, предпочтительно по меньшей мере 85%, например, по меньшей мере 90%, более предпочтительно по меньшей мере 95%, например, по меньшей мере 96%, даже более предпочтительно по меньшей мере 97%, например, по меньшей мере 98%, наиболее предпочтительно по меньшей мере 99% идентичностью относительно молекулы нуклеиновой кислоты согласно SEQ ID NO: 54 или 55, или
(III) молекула нуклеиновой кислоты, гибридизующаяся с молекулой нуклеиновой кислоты, характеризующейся SEQ ID NO: 54 или 55, при условиях средней жесткости, более предпочтительно при условиях высокой жесткости, наиболее предпочтительно при условиях очень высокой жесткости, или
(IV) фрагмент, составляющий по меньшей мере 10 нуклеотидов, предпочтительно по меньшей мере 20 нуклеотидов, по меньшей мере 30 нуклеотидов или по меньшей мере 40 нуклеотидов, более предпочтительно фрагмент, составляющий по меньшей мере 50 нуклеотидов, по меньшей мере 75 нуклеотидов или по меньшей мере 100 нуклеотидов, даже более предпочтительно по меньшей мере 150 или по меньшей мере 200 нуклеотидов молекулы нуклеиновой кислоты, характеризующейся SEQ ID NO: 54 или 55. Фрагмент SEQ ID NO: 54 или 55 предпочтительно представляет собой фрагмент, содержащий 3' область SEQ ID NO: 54 или 55, следовательно, фрагмент содержит делецию на 5' конце SEQ ID NO: 54 или 55.
Молекулы нуклеиновой кислоты согласно определению в (II)-(IV) предпочтительно характеризуются промоторной активностью в микроорганизмах согласно определению в настоящем документе.
Согласно дополнительному варианту осуществления настоящего изобретения предусмотрена рекомбинантная экспрессионная конструкция, содержащая промотор согласно приведенному выше определению в (I)-(IV), являющийся функциональным в микроорганизме, функционально связанный с нуклеиновой кислотой, подлежащей экспрессии, которая является гетерологичной по отношению к промотору согласно определению в (I)-(IV).
Согласно дополнительному варианту осуществления настоящего изобретения предусмотрен рекомбинантный вектор, содержащий молекулу нуклеиновой кислоты согласно приведенному выше определению в (I)-(IV) или рекомбинантную экспрессионную конструкцию согласно приведенному выше определению.
Согласно дополнительному варианту осуществления настоящего изобретения предусмотрен рекомбинантный микроорганизм, содержащий рекомбинантную экспрессионную конструкцию согласно приведенному выше определению или вектор согласно приведенному выше определению. Микроорганизм предпочтительно выбран из группы микроорганизмов, перечисленных в настоящем документе.
Согласно дополнительному варианту осуществления настоящего изобретения предусмотрен способ экспрессии молекулы нуклеиновой кислоты в микроорганизме, предусматривающий стадии функционального связывания промотора согласно приведенному выше определению с гетерологичной молекулой нуклеиновой кислоты, подлежащей экспрессии, тем самым создавая рекомбинантную экспрессионную конструкцию, и введения указанной экспрессионной конструкции в микроорганизм. Промотор согласно настоящему изобретению может быть функционально связан с подлежащей экспрессии молекулой нуклеиновой кислоты посредством технологии рекомбинантной ДНК за пределами микроорганизма и впоследствии может быть введен в микроорганизм или он может быть функционально связан путем введения нуклеиновой кислоты, подлежащей экспрессии, в геном микроорганизма вблизи от промотора согласно настоящему изобретению, присутствующего в микроорганизме, тем самым связывая подлежащую экспрессии нуклеиновую кислоту с промотором согласно настоящему изобретению.
Согласно дополнительному варианту осуществления настоящего изобретения предусмотрено применение промотора согласно приведенному выше определению, рекомбинантной экспрессионной конструкции согласно приведенному выше определению или вектора согласно приведенному выше определению для экспрессии молекулы нуклеиновой кислоты в микроорганизме.
Определения
Следует понимать, что настоящее изобретение не ограничено конкретной методологией или протоколами. Также следует понимать, что используемая в настоящем документе терминология предусмотрена исключительно с целью описания конкретных вариантов осуществления и не предусмотрено, что она ограничивает объем настоящего изобретения, который будет определяться только приложенной формулой изобретения. Необходимо отметить, что используемые в настоящем документе и в приложенной формуле изобретения формы единственного числа включают в себя ссылку на формы множественно числа, если только контекст явно не диктует иное. Таким образом, например, ссылка на "вектор" представляет собой ссылку на один или более векторов и включает в себя его эквиваленты, известные специалистам в настоящей области техники, и тому подобное. Используемый в настоящем документе термин "приблизительно" означает примерно, приближенно, около или порядка. Если термин "приблизительно" используется в отношении числового диапазона, он модифицирует указанный диапазон путем расширения его границ выше и ниже перечисленных числовых значений. Как правило, термин "приблизительно" используется в настоящем документе для модификации числовой величины выше и ниже указанной величины с отклонением на 20%, предпочтительно на 10% вверх или вниз (выше или ниже). Используемое в настоящем документе слово "или" означает любого одного представителя конкретного перечня, а также включает в себя любую комбинацию представителей перечня. Слова "содержат", "содержащий", "включают в себя", "включая в себя" и "включает в себя", используемые в настоящем описании и в последующей формуле изобретения, предусмотрены, чтобы установить присутствие одного или более заявленных признаков, целых, компонентов или стадий, но они не исключают присутствия или добавления одного или более других признаков, целых, компонентов, стадий или их групп. Для ясности определенные термины, используемые в настоящем описании, определены и используются следующим образом:
Кодирующая область: Используемый в настоящем документе термин "кодирующая область" при использовании со ссылкой на структурный ген относится к нуклеотидным последовательностям, которые кодируют аминокислоты, встречающиеся в образующемся полипептиде, в результате трансляции молекулы иРНК. Кодирующая область ограничена у эукариот на 5'-конце нуклеотидным триплетом "ATG", который кодирует инициатор метионин, прокариоты также используют триплеты "GTG" и "TTG" в качестве старт-кодона. На 3'-конце он ограничен одним из трех триплетов, которые обозначают стоп-кодоны (т.е. ТАА, TAG, TGA). Кроме того, ген может включать в себя последовательности, расположенные как на 5'-, так и на 3'-конце последовательностей, которые присутствуют на транскрипте РНК. Указанные последовательности носят название "фланкирующие" последовательности или области (указанные фланкирующие последовательности расположены 5' или 3' относительно нетранслируемых последовательностей, присутствующих на транскрипте иРНК). 5'-фланкирующая область может содержать регуляторные последовательности, такие как промоторы и энхансеры, которые контролируют или оказывают влияние на транскрипцию гена. 3'-фланкирующая область может содержать последовательности, которые управляют терминацией транскрипции, посттранскрипционным отщеплением и полиаденилированием.
Комплементарный: "Комплементарный" или "комплементарность" относится к двум нуклеотидным последовательностям, которые содержат антипараллельные нуклеотидные последовательности, способные образовывать пару друг с другом (по правилам спаривания оснований) при образовании водородных связей между остатками комплементарных оснований в антипараллельных нуклеотидных последовательностях. Например, последовательность 5'-AGT-3' комплементарна последовательности 5'-АСТ-3'. Комплементарность может быть "частичной" или "полной." "Частичная" комплементарность имеет место в случае, когда одно или более оснований нуклеиновых кислот не совпадают согласно правилам спаривания оснований. "Абсолютная" или "полная" комплементарность между молекулами нуклеиновых кислот имеет место, когда любое и каждое основание нуклеиновых кислот совпадает с другим основанием согласно правилам спаривания оснований. Степень комплементарности между цепями молекулы нуклеиновой кислоты оказывает существенное влияние на эффективность и силу гибридизации между цепями молекулы нуклеиновой кислоты. Используемый в настоящем документе термин "комплементарная" последовательности нуклеиновой кислоты относится к нуклеотидной последовательности, чьи молекулы нуклеиновой кислоты демонстрируют полную комплементарность молекулам нуклеиновой кислоты последовательности нуклеиновой кислоты.
Эндогенный: "Эндогенная" нуклеотидная последовательность относится к нуклеотидной последовательности, которая присутствует в геноме микроорганизма дикого типа.
Усиленная экспрессия: "усиление" или "увеличение" экспрессии молекулы нуклеиновой кислоты в микроорганизме в настоящем документе используются эквивалентно и означают, что уровень экспрессии молекулы нуклеиновой кислоты в микроорганизме является выше по сравнению с микроорганизмом сравнения, например, микроорганизмом дикого типа. Используемые в настоящем документе термины "усиленная" или "увеличенная" означают в настоящем документе повышенную, предпочтительно значительно повышенную экспрессию молекулы нуклеиновой кислоты, подлежащей экспрессии. Используемые в настоящем документе термины "усиление" или "увеличение" содержания такого средства, как белок, иРНК или РНК, означает, что содержание увеличивается по отношению к по существу идентичному микроорганизму, выращенному при по существу идентичных условиях. Используемые в настоящем документе термины "усиление" или "увеличение" содержания такого средства, как, например, преРНК, иРНК, рРНК, тРНК, экспрессируемого целевым геном и/или белкового продукта, кодируемого им, означает, что содержание увеличено на 50% или более, например, на 100% или более, предпочтительно на 200% или более, более предпочтительно в 5 раз или более, даже более предпочтительно в 10 раз или более, наиболее предпочтительно в 20 раз или более, например, в 50 раз относительно подходящего микроорганизма сравнения. Усиление или увеличение можно определить с помощью способов, с которыми хорошо знаком специалист в настоящей области техники. Таким образом, усиление или увеличение количества нуклеиновой кислоты или белка можно определить, например, путем иммунологического обнаружения белка. Более того, такие техники, как белковый анализ, флуоресценция, нозерн-гибридизация, анализ на основании защиты от нуклеаз, обратная транскрипция (количественная ОТ-ПЦР, или qRT-PCR), ELISA (фермент-связанный иммуносорбентный анализ), вестерн-блоттинг, радиоиммуноанализ (RIA) или другие иммуноанализы и клеточный анализ с активированной флуоресценцией (FACS) можно использовать для измерения конкретного белка или РНК в микроорганизме. В зависимости от типа индуцированного белкового продукта также можно определить его активность или действие на фенотип микроорганизма. Способы определения количества белка известны специалисту в настоящей области техники. Примеры, которые можно упомянуть, представляют собой следующие: микробиуретовый способ (Goa J (1953) Scand J Clin Lab Invest 5:218-222), способ Фолина-Чокальтеу (Lowry ОН et al. (1951) J Biol Chem 193: 265-275) или измерение абсорбции CBB G-250 (Bradford MM (1976) Analyt Biochem 72: 248-254.
Экспрессия: "Экспрессия" относится к биосинтезу генного продукта, предпочтительно к транскрипции и/или трансляции нуклеотидной последовательности, например, эндогенного гена или гетерологичного гена, в клетке. Например, в случае структурного гена экспрессия предусматривает транскрипцию структурного гена в иРНК и - необязательно - последующую трансляцию иРНК в один или более полипептидов. В других случаях экспрессия может относиться только к транскрипции ДНК, содержащей молекулу РНК.
Чужеродный: Термин "чужеродный" относится к любой молекуле нуклеиновой кислоты (например, генной последовательности), которая введена в клетку с помощью экспериментальных манипуляций и может включать в себя последовательности, встречающиеся в такой клетке, при условии, что введенная последовательность содержит некоторую модификацию (например, точечную мутацию, присутствие селектируемого маркерного гена и т.д.) и, следовательно, отличается от встречающейся в природе последовательности.
Функциональная связь: Термин "функциональная связь" или "функционально связанный" следует понимать как обозначение, например, последовательного расположения регуляторного элемента (например, промотора) с последовательностью нуклеиновой кислоты, подлежащей экспрессии и, в соответствующем случае, дополнительными регуляторными элементами (такими как, например, терминатор) таким образом, что каждый из регуляторных элементов может выполнять свою предусмотренную функцию, чтобы обеспечить возможность, модифицировать, облегчить или иным образом повлиять на экспрессию указанной последовательности нуклеиновой кислоты. Экспрессия может давать в результате зависимости от расположения последовательностей нуклеиновых кислот смысловую или антисмысловую РНК. С этой целью прямая связь в химическом смысле не является обязательно необходимой. Осуществляющие генетический контроль последовательности, такие как, например, энхансерные последовательности, также могут проявлять свою функцию на целевую последовательность из положений, которые дополнительно удалены, или фактически происходят из других молекул ДНК. Предпочтительные расположения представляют собой те, в которых последовательность нуклеиновой кислоты, подлежащая экспрессии, рекомбинантно расположена вслед за последовательностью, действующей в качестве промотора, так что две последовательности ковалентно соединены друг с другом. Согласно предпочтительному варианту осуществления последовательность нуклеиновой кислоты, подлежащей транскрипции, расположена после промотора таким образом, что начало транскрипции является идентичным требуемому началу химерной РНК согласно настоящему изобретению. Функциональная связь и экспрессионная конструкция могут быть сконструированы посредством общепринятых техник рекомбинации и клонирования, как описано, например, в Maniatis Τ, Fritsch EF and Sambrook J (1989) Molecular Cloning: A Laboratory Manual, 2nd Ed., Cold Spring Harbor Laboratory, Cold Spring Harbor (NY); Silhavy et al. (1984) Experiments with Gene Fusions, Cold Spring Harbor Laboratory, Cold Spring Harbor (NY); Ausubel et al. (1987) Current Protocols in Molecular Biology, Greene Publishing Assoc. and Wiley Interscience; Gelvin et al. (Eds) (1990) Plant Molecular Biology Manual; Kluwer Academic Publisher, Dordrecht, The Netherlands). Тем не менее, дополнительные последовательности, которые, например, действуют в качестве линкера со специфическими сайтами расщепления для рестрикционных ферментов или в качестве сигнального пептида, также могут быть расположены между двумя последовательностями. Вставка последовательностей также может приводить к экспрессии белков слияния. Экспрессионная конструкция, состоящая из соединения регуляторной области, например, промотора и подлежащей экспрессии последовательности нуклеиновой кислоты, предпочтительно может существовать в интергрированной в вектор форме или может быть вставлена в геном, например, путем трансформации.
Ген: Термин "ген" относится к области, функционально связанный с соответствующими регуляторными последовательностями, способными к регуляции экспрессии генного продукта (например, полипептида или функциональной РНК) некоторым образом. Ген включает в себя нетранслируемые регуляторные области ДНК (например, промоторы, энхансеры, репрессоры и т.д.), предшествующие (расположенные против хода транскрипции) и следующие (расположенные по ходу транскрипции) за кодирующей областью (открытой рамкой считывания, ORF). Предусмотрено, что используемый в настоящем документе термин "структурный ген" означает последовательность ДНК, которая транскрибируется в иРНК, которая затем транслируется в последовательность аминокислот, характерных для конкретного полипептида.
Геном и геномная ДНК: Термины "геном" или "геномная ДНК" относятся к наследуемой генетической информации организма - хозяина. Указанная геномная ДНК содержит ДНК нуклеоида, а также ДНК самореплицирующейся плазмиды.
Гетерологичный: Термин "гетерологичный" в отношении молекулы нуклеиновой кислоты или ДНК относится к молекуле нуклеиновой кислоты, которая функционально связана или подвергнута воздействию, чтобы стать функционально связанной со второй молекулой нуклеиновой кислоты, с которой она не связана функционально в природе, или с которой она функционально связана в природе в другом положении. Гетерологичная экспрессионная конструкция, содержащая молекулу нуклеиновой кислоты и одну или более регуляторную молекулу нуклеиновой кислоты (такую как промотор или сигнал терминации транскрипции), соединенную с ней, например, представляет собой конструкции, полученные путем экспериментальных манипуляций, в которых или а) указанная молекула нуклеиновой кислоты, или b) указанная регуляторная молекула нуклеиновой кислоты или с) обе (т.е. (а) и (b)) не расположены в своем природном (нативном) генетическом окружении или были модифицированы путем экспериментальных манипуляций, причем пример модификации представляет собой замену, добавление, делецию, инверсию или вставку одного или более нуклеотидных остатков. Природное генетическое окружение относится к природному геномному локусу в организме происхождения или к присутствию в геномной библиотеке. В случае геномной библиотеке природное генетическое окружение последовательности молекулы нуклеиновой кислоты предпочтительно сохраняется, по меньшей мере частично. Окружение отграничивает последовательность нуклеиновой кислоты по меньшей мере с одной стороны и характеризуется последовательностью, составляющей по меньшей мере 50 п.н., предпочтительно по меньшей мере 500 п.н., особенно предпочтительно по меньшей мере 1000 п.н., особенно предпочтительно по меньшей мере 5000 п.н. в длину. Встречающаяся в природе экспрессионная конструкция, например, встречающаяся в природе комбинация промотора с соответствующим геном, становится трансгенной экспрессионнй конструкцией, когда она модифицирована с помощью не встречающихся в природе, синтетических "искусственных" способов, таких как, например, индукция мутаций. Такие способы были описаны (патент США №US 5565350; международная патентная публикация №WO 00/15815). Например, кодирующая белок молекула нуклеиновой кислоты, функционально связанная с промотором, который не представляет собой нативный промотор этой молекулы, считается гетерологичной в отношении промотора. Гетерологичная ДНК предпочтительно не является эндогенной или не является природно ассоциированной с клеткой, в которую она введена, но она была получена из другой клетки или была синтезирована. Гетерологичная ДНК также включает в себя эндогенную последовательность ДНК, которая содержит некоторую модификацию, не встречающуюся в природе, множественные копии эндогенной последовательности ДНК или последовательность ДНК, которая не является природно ассоциированной с другой последовательностью ДНК, физически связанной с ней. Как правило, хотя и не обязательно, гетерологичная ДНК кодирует РНК или белки, которые в норме не производятся клеткой, в которой она экспрессирована.
Гибридизация: Используемый в настоящем документе термин "гибридизация" включает в себя "любой процесс, с помощью которого цепь молекулы нуклеиновой кислоты соединяется с комплементарной цепью посредством спаривания оснований." (J. Coombs (1994) Dictionary of Biotechnology, Stockton Press, New York). Гибридизация и сила гибридизации (т.е. сила ассоциации между молекулами нуклеиновой кислоты) подвержена воздействию таких факторов, как степень комплементарности между молекулами нуклеиновой кислоты, жесткость применяемых условий, Tm образованного гибрида и отношение G:C в пределах молекул нуклеиновой кислоты. Используемый в настоящем документе термин "Tm" используется в отношении "температуры плавления". Температура плавления представляет собой температуру, при которой популяция двухцепочечных молекул нуклеиновой кислоты становится наполовину диссоциированной на отдельные цепи. Уравнение для расчета Tm молекул нуклеиновой кислоты хорошо известно в настоящей области техники. Как указано в стандартных ссылках, простая оценка значения Tm может быть рассчитана с помощью следующего уравнения: Tm=81,5+0,41(% G+C), если молекула нуклеиновой кислоты находится в водном растворе с 1 M NaCl [см., например, Anderson and Young, Quantitative Filter Hybridization, in Nucleic Acid Hybridization (1985)]. Другие ссылки включают в себя более сложные вычисления, которые для расчета Tm принимают во внимание структурные характеристики, а также характеристики последовательностей. Жесткие условия известны специалистам в настоящей области техники и их можно найти в Current Protocols in Molecular Biology, John Wiley & Sons, N.Y. (1989), 6.3.1-6.3.6.
Подходящие условия гибридизация, представляют собой, например, гибридизацию при условиях, эквивалентных гибридизации в 7% додецилсульфата натрия (SDS), 0,5 M NaPO4, 1 мМ EDTA при 50°С с отмывкой в 2 X SSC, 0,1% SDS при 50°С (условие низкой жесткости) с молекулой нуклеиновой кислоты, содержащей по меньшей мере 50, предпочтительно по меньшей мере 100, более предпочтительно по меньшей мере 150, даже более предпочтительно по меньшей мере 200, наиболее предпочтительно по меньшей мере 250 последовательных нуклеотидов последовательности, комплементарной указанной последовательности. Другие подходящие условия гибридизации представляют собой гибридизацию в 7% додецилсульфата натрия (SDS), 0,5 M NaPO4, 1 мМ EDTA при 50°С с отмывкой в 1 X SSC, 0,1% SDS при 50°С (условия средней жесткости) или 65°С (условия высокой жесткости) с молекулой нуклеиновой кислоты, содержащей по меньшей мере 50, предпочтительно по меньшей мере 100, более предпочтительно по меньшей мере 150, даже более предпочтительно по меньшей мере 200, наиболее предпочтительно по меньшей мере 250 последовательных нуклеотидов последовательности, комплементарной указанной последовательности. Другие подходящие условия гибридизации представляют собой гибридизацию в 7% додецилсульфата натрия (SDS), 0,5 M NaPO4, 1 мМ EDTA при 50°С с отмывкой в 0,1 X SSC, 0,1% SDS при 65°С (условия очень высокой жесткости) с молекулой нуклеиновой кислоты, содержащей по меньшей мере 50, предпочтительно по меньшей мере 100, более предпочтительно по меньшей мере 150, даже более предпочтительно по меньшей мере 200, наиболее предпочтительно по меньшей мере 250 последовательных нуклеотидов последовательности, комплементарной указанной последовательности.
"Идентичность": "Идентичность" при использовании в отношении сравнения двух или более молекул нуклеиновых кислот или аминокислот означает, что последовательности указанных молекул характеризуются определенной степенью сходства последовательностей, причем последовательности являются частично идентичными.
Для определения идентичности в процентах (гомология в настоящем документе используется взаимозаменяемо относительно последовательностей нуклеиновых кислот) двух аминокислотных последовательностей или двух молекул нуклеиновой кислоты, последовательности выписываются одна под другой для оптимального сравнения (например, пропуски могут быть введены в последовательность белка или нуклеиновой кислоты для получения оптимального выравнивания с другим белком или другой нуклеиновой кислотой).
Аминокислотные остатки или молекулы нуклеиновой кислоты в соответствующих аминокислотных положениях или нуклеотидных положениях затем сравнивают. Если положение в одной последовательности занято таким же аминокислотным остатком или такой же молекулой нуклеиновой кислоты, как и соответствующее положение в другой последовательности, молекулы являются идентичными в указанном положении. Идентичность в процентах между двумя последовательностями представляет собой функцию от числа идентичных положений, общих для последовательностей (т.е. % идентичности = число идентичных положений/общее число положений × 100). Термины "гомология" и "идентичность", таким образом, считаются синонимами, если относятся к последовательностям нуклеиновых кислот. При ссылке на аминокислотные последовательности термин "идентичность" относится к идентичным аминокислотам в конкретном положении в последовательности, термин гомология относится к гомологичным аминокислотам в конкретном положении в последовательности. Гомологичные аминокислоты представляют собой аминокислоты, характеризующиеся сходной боковой цепью. Семейства аминокислотных остатков, характеризующихся сходными боковыми цепями, были установлены в настоящей области техники.
Молекула нуклеиновой кислоты, кодирующая белок, гомологичный белок согласно настоящему изобретению, может быть создана путем введения одной или более нуклеотидных замен, добавлений или делеций в нуклеотидную последовательность так, чтобы одна или более аминокислотных замен, добавлений или делеций были введены в кодируемый белок. Мутации могут быть введены в одну из последовательностей согласно настоящему изобретению с помощью стандартных техник, таких как сайт-направленный мутагенез и опосредованный ПЦР мутагенез., Консервативные аминокислотные замены предпочтительно осуществляют на одном или более спрогнозированном остатке заменимой аминокислоты. "Консервативная аминокислота замена" представляет собой аминокислотную замену, при которой аминокислотный остаток замещен аминокислотным остатком, характеризующимся сходной боковой цепью. Семейства аминокислотных остатков, характеризующихся сходными боковыми цепями, были определены в настоящей области техники. Эти семейства включают в себя аминокислоты с основными боковыми цепями (например, ллизин, аргинин, гистидин), кислыми боковыми цепями (например, аспарагиновая кислота, глутаминовая кислота), незаряженными полярными боковыми цепями (например, глицин, аспарагин, глутамин, серии, треонин, тирозин, цистеин), неполярными боковыми цепями (например, аланин, валин, лейцин, изолейцин, пролин, фенилаланин, метионин, триптофан), бета-разветвленными боковыми цепями (например, треонин, валин, изолейцин) и ароматическими боковыми цепями (например, тирозин, фенилаланин, триптофан, гистидин). Таким образом, спрогнозированный остаток заменимой аминокислоты в белке согласно настоящему изобретению предпочтительно замещен другим аминокислотным остатком из того же семейства боковых цепей.
Альтернативно, согласно другому варианту осуществления мутации могут быть введены случайным образом по всей кодирующей последовательности или ее части, например, с помощью насыщающего мутагенеза, и полученные мутанты могут быть подвергнуты скринингу в отношении соответствующей активности, описанной в настоящем документе, для идентификации мутантов, которые сохраняют свою активность. После мутагенеза одной из последовательностей согласно настоящему изобретению кодируемый белок может быть экспрессирован рекомбинантно и активность белка может быть определена с использованием, например, описанных в настоящем документе анализов.
Для определения процентной идентичности двух или более аминокислот или двух или более нуклеотидных последовательностей были разработаны некоторые компьютерные программы. Идентичность двух или более последовательностей можно рассчитать с помощью, например, программного обеспечения fasta, которое в настоящее время используется в версии fasta 3 (W.R. Pearson and D.J. Lipman, PNAS 85, 2444(1988); W.R. Pearson, Methods in Enzymology 183, 63 (1990); W.R. Pearson and D.J. Lipman, PNAS 85, 2444 (1988); W.R. Pearson, Enzymology 183, 63 (1990)). Другая применимая программа для расчета идентичностей различных последовательностей представляет собой стандартную программу blast, которая включена в программное обеспечение Biomax pedant (Biomax, Мюнхен, ФРГ). К сожалению, иногда она дает субоптимальные результаты, поскольку blast не всегда включает в себя полные последовательности субъекта и поискового запроса. Тем не менее, поскольку эта программа является очень эффективной, ее можно использовать для сравнения огромного количества последовательностей. Следующие установочные параметры, как правило, используются для таких сравнений последовательностей:
-р Название программы [Строка]; -d База данных [Строка]; по умолчанию = nr; -i Файл поискового запроса [Файл ввода]; по умолчанию = stdin; -е Ожидаемое значение (Е) [Действительное]; по умолчанию = 10,0; -m опции просмотра выравнивания: 0 = попарное; 1 = привязанные к поисковому запросу, показывающие идентичности; 2 = привязанные к поисковому запросу без идентичностей; 3 = одноуровневые привязанные к поисковому запросу, показывают идентичности; 4 = одноуровневые привязанные к поисковому запросу, нет идентичностей; 5 = привязанные к поисковому запросу, нет идентичностей и тупые концы; 6 = одноуровневые привязанные к поисковому запросу, нет идентичностей и тупые концы; 7 = вывод XML Blast; 8 = табличный; 9 табличный со строками комментариев [Целое]; по умолчанию = 0; -о Файл вывода отчета BLAST [Файл вывода], необязательно; по умолчанию = стандартный выход; -F Фильтр искомая последовательность (DUST с blastn, SEG с другими) [Строка]; по умолчанию = Т; -G Штраф на введение пробела (0 ссылается на поведение по умолчанию) [Целое]; по умолчанию = 0; -Е Штраф на удлинение пробела (0 ссылается на поведение по умолчанию) [Целое]; по умолчанию = 0; -X кратность уменьшения величины для выравнивания с пробелами (в битах) (0 ссылается на поведение по умолчанию); blastn 30, megablast 20, tblastx 0, все другие 15 [Целое]; по умолчанию = 0; -I Показать GI в строках описания [T/F]; по умолчанию = F; -q Штраф на несовпадение нуклеотидов (только blastn) [Целое]; по умолчанию = -3; -r Вознаграждение за совпадение нуклеотидов (только blastn) [Целое]; по умолчанию = 1; -v Число последовательностей в базе данных, чтобы показать однострочные описания для (V) [Целое]; по умолчанию = 500; -b Число последовательностей в базе данных, чтобы показать выравнивания для (В) [Целое]; по умолчанию = 250; -f Порог для увеличения совпадений, по умолчанию, если ноль; blastp 11, blastn 0, blastx 12, tblastn 13; tblastx 13, megablast 0 [Целое]; по умолчанию = 0; -g Провести выравнивание с пробелами (не доступно с tblastx) [T/F]; по умолчанию = Т; -Q Искомый генетические код для использования [Целое]; по умолчанию = 1; -D DB Генетический код (только для tblast[nx]) [Целое]; по умолчанию = 1; -а Число процессоров для использования [Целое]; по умолчанию = 1; -О Файл SeqAlign [Файл вывода], необязательно; -J Предположить искомую строку описания [T/F]; по умолчанию = F; -М Матрица [Строка]; по умолчанию = BLOSUM62; -W Длина сегмента, по умолчанию, если ноль (blastn 11, megablast 28, all others 3) [Целое]; по умолчанию = 0; -z Эффективная длина базы данных (применять ноль для действительного размера) [Действительное]; по умолчанию = 0; -K Число лучших совпадений из исследуемой области (не предусмотрено по умолчанию, если используемое значение 100 является рекомендуемым) [Целое]; по умолчанию = 0; -Р 0 для множественного совпадения, 1 для одного совпадения [Целое]; по умолчанию = 0; -Υ Эффективная длина поискового пространства (использовать ноль для действительного размера) [Действительное]; по умолчанию = 0; -S Искомые цепи для поиска по базе данных (для blast[nx] и tblastx); 3 - это обе, 1 - это верх, 2 - это низ [Целое]; по умолчанию = 3; -Т Производят вывод HTML [T/F]; по умолчанию = F; -1 Ограничить поиск по базе данных до перечня GI [Строка], необязательно; -U Применить фильтрование по нижнему регистру последовательности FASTA [T/F], необязательно; по умолчанию = F; -у Кратность падения величины для удлинений без пробелов в битах (0,0 ссылается на поведение по умолчанию); blastn 20, megablast 10, все другие 7 [Действительное]; по умолчанию = 0,0; -Z Кратность падения величины для конечного выравнивания с пробелами в битах (0,0 ссылается на поведение по умолчанию); blastn/megablast 50, tblastx 0, все другие 25 [Целое]; по умолчанию = 0; -R файл контрольной точки PSI-TBLASTN [файл ввода], необязательный; -n поиск MegaBlast [T/F]; по умолчанию = F; -L Расположение на искомой последовательности [Строка], необязательно; -А Размер окна множественных совпадений, по умолчанию, если ноль (blastn/megablast 0, все другие 40 [Целое]; по умолчанию = 0; -w Штраф на сдвиг рамки считывания (алгоритм OOF для blastx) [Целое]; по умолчанию = 0; -t Длина наибольшего интрона, разрешенного в tblastn для связывания HSP (0 делает связывание невозможным) [Целое]; по умолчанию = 0.
Результаты высокого качества считываются с использованием алгоритма согласно Needleman и Wunsch или Smith и Waterman. Следовательно, программы, основанные на указанных алгоритмах, являются предпочтительными. Преимущественно сравнения последовательностей можно осуществить с помощью программы PileUp (J. Mol. Evolution., 25, 351 (1987), Higgins et al., CABIOS 5, 151 (1989)) или предпочтительно с помощью программ "Gap" и "Needle", причем обе основаны на алгоритмах Needleman и Wunsch (J. Mol. Biol. 48; 443 (1970)), и "BestFit", которая основана на алгоритме Smith и Waterman (Adv. Appl. Math. 2; 482 (1981)). "Gap" и "BestFit" являются частью пакета программного обеспечения GCG (Genetics Computer Group, 575 Science Drive, Madison, Wisconsin, USA 53711 (1991); Altschul et al., (Nucleic Acids Res. 25, 3389 (1997)), "Needle" является частью программного обеспечения The European Molecular Biology Open Software Suite (EMBOSS) (Trends in Genetics 16 (6), 276 (2000)). Следовательно, предпочтительно расчеты для определения процентных отношений идентичности последовательностей выполняют с помощью программ "Gap" или "Needle" по всему диапазону последовательностей. Следующие стандартные настройки для сравнения последовательностей нуклеиновых кислот использовали для "Needle": матрица: EDNAFULL, штраф на введение делеции: 10,0, штраф на удлинение делеции: 0,5. Следующие стандартные настройки для сравнения последовательностей нуклеиновых кислот использовали для "Gap": штраф на введение делеции: 50, штраф на удлинение делеции: 3, среднее совпадение: 10,000, среднее несовпадение: 0,000.
Например, последовательность, которая, как указано, характеризуется 80% идентичностью относительно последовательности SEQ ID NO: 1 на уровне нуклеиновых кислот, следует понимать как определение последовательности, которая при сравнении с последовательностью, представленной в SEQ ID NO: 1, с помощью описанной выше программы "Needle" с описанными выше установочными параметрами, характеризуется 80% идентичностью. Идентичность предпочтительно рассчитывают по всей длине искомой последовательности, например, SEQ ID NO: 1.
Выделенный: Используемый в настоящем документе термин "выделенный" означает, что материал был удален человеком и существует отдельно от своего источника, нативного окружения и, следовательно, не является продуктом природы. Выделенный материал или молекула (такая как молекула ДНК или фермент) может существовать в очищенной форме или может существовать в ненативном окружении, таком как, например, в трансгенной клетке - хозяине. Например, встречающаяся в природе молекула нуклеиновой кислоты или полипептид, присутствующий в живой клетке, не является выделенным, но эта же молекула нуклеиновой кислоты или полипептид, отделенные от некоторых или всех сосуществующих материалов в природной системе, является выделенным. Такие молекулы нуклеиновой кислоты могут быть частью вектора и/или такие молекулы нуклеиновой кислоты или полипептиды могут быть частью композиции, и будут выделены так, чтобы вектор или композиция не представляла собой часть их исходного окружения. Термин "выделенный" при использовании в отношении молекулы нуклеиновой кислоты, как в "выделенная последовательность нуклеиновой кислоты" предпочтительно относится к последовательности нуклеиновой кислоты, которая идентифицирована и отделена по меньшей мере от одной посторонней молекулы нуклеиновой кислоты, с которой она, как правило, ассоциирована в своем природном источнике. Выделенная молекула нуклеиновой кислоты представляет собой молекулу нуклеиновой кислоты, присутствующую в форме или окружении, которое отличается от того, в котором она встречается в природе. Напротив, не выделенные молекулы нуклеиновой кислоты представляют собой молекулы нуклеиновой кислоты, такие как ДНК и РНК, которые встречаются в состоянии, в котором они существуют в природе. Например, данная последовательность ДНК (например, ген) встречается на хромосоме клетки-хозяина в непосредственной близости от прилегающих генов; последовательности РНК, такие как конкретная последовательность иРНК, кодирующая конкретный белок, встречаются в клетке в виде смеси с различными другими иРНК, которые кодируют множество белков. Тем не менее, выделенная последовательность нуклеиновой кислоты, содержащая, например, SEQ ID NO: 1, включает в себя, в качестве примера, такие последовательности нуклеиновой кислоты в клетках, которые, как правило, содержат SEQ ID NO: 1, где последовательность нуклеиновой кислоты находится в положении в геноме или плазмиде, отличающемся от такового в природных клетках, или иным образом ограничена последовательностью нуклеиновой кислоты, отличной от той, которая встречается в природе. Выделенная последовательность нуклеиновой кислоты может присутствовать в одноцепочечной или двухцепочечной форме. Если выделенная последовательность нуклеиновой кислоты подлежит применению для экспрессии белка, последовательность нуклеиновой кислоты будет содержать, как минимум, по меньшей мере часть смысловой или кодирующей цепи (т.е. последовательность нуклеиновой кислоты может быть одноцепочечной). Альтернативно, она может содержать как смысловые, так и антисмысловые цепи (т.е. последовательность нуклеиновой кислоты может быть двухцепочечной).
Некодирующая: Термин "некодирующая" относится к последовательностям молекул нуклеиновой кислоты, которые не кодируют часть или весь экспрессируемый белок. Некодирующие последовательности включают в себя без ограничения энхансеры, промоторные области, 3' нетранслируемые области и 5' нетранслируемые области.
Нуклеиновые кислоты и нуклеотиды: Термины "нуклеиновые кислоты" и "нуклеотиды" относятся к встречающейся в природе или синтетической или искусственной нуклеиновой кислоте или нуклеотидам. Термины "нуклеиновые кислоты" и "нуклеотиды" предусматривают дезоксирибонуклеотиды или рибоуклеотиды или любой нуклеотидный аналог и их полимеры или гибриды либо в одноцепочечной, либо двухцепочечной, смысловой или антисмысловой формах. Если не указано иное, конкретная последовательность нуклеиновой кислоты также потенциально включает в себя ее консервативно модифицированные варианты (например, замены вырожденного кодона) и комплементарные последовательности, а также конкретно указанную последовательность. Термин "нуклеиновая кислота" в настоящем документе используется взаимозаменяемо с термином "ген", "кДНК", "иРНК", "олигонуклеотид" и "молекула нуклеиновой кислоты". Нуклеотидные аналоги включают в себя нуклеотиды, характеризующиеся модификациями в химической структуре основания, сахара и/или фосфата, включая в себя без ограничения модификации в 5 положении пиримидина, модификации в 8 положении пурина, модификации на экзоциклических аминах цитозина, замену 5-бром-урацила и подобное; и модификации в 2' положении сахара, включая в себя без ограничения рибонуклеотиды с модифицированным сахаром, в которых 2'-ОН замещен группой, выбранной из Н, или, R, гало, SH, SR, NH2, NHR, NR2 или CN. Короткие шпилечные РНК (кшРНК) также могут содержать неприродные элементы, такие как неприродные основания, например, ионозин и ксантин, неприродные сахара, например, 2'-метоксирибоза, или неприродные фосфодиэфирные связи, например, метилфосфонаты, фосфоротиоаты и пептиды.
Последовательность нуклеиновой кислоты: Фраза "последовательность нуклеиновой кислоты" относится к одноцепочечному или двухцепочечному полимеру дезоксирибонуклеотидных или рибонуклеотидных оснований, читаемому с 5'- к 3'-концу. Он включает в себя хромосомную ДНК, самореплицирующиеся плазмиды, инфекционные полимеры ДНК или РНК и ДНК или РНК, которая выполняет, главным образом, структурную роль. "Последовательность нуклеиновой кислоты" также относится к непрерывному перечню сокращений, букв, символов или слов, которые представляют нуклеотиды. Согласно одному варианту осуществления нуклеиновая кислота может представлять собой "зонд", который представляет собой относительно короткую нуклеиновую кислоту, как правило, меньше чем 100 нуклеотидов в длину. Зачастую нуклеиновокислотный зонд составляет от приблизительно 50 нуклеотидов в длину до приблизительно 10 нуклеотидов в длину. "Целевая область" нуклеиновой кислоты представляет собой часть нуклеиновой кислоты, которая идентифицирована как представляющая интерес."Кодирующая область" нуклеиновой кислоты представляет собой часть нуклеиновой кислоты, которая транскрибируется и транслируется специфическим для последовательности способом для того, чтобы стать конкретным полипептидом или белком, будучи помещенной под контроль соответствующих регуляторных последовательностей. Кодирующая область, как указано, кодирует такой полипептид или белок.
Олигонуклеотид: Термин "олигонуклеотид" относится к олигомеру или полимеру рибонуклеиновой кислоты (РНК) или дезоксирибонуклеиновой кислоты (ДНК) или его миметикам, а также к олигонуклеотидам, характеризующимся не встречающимися в природе частями, которые функционируют аналогичным образом. Такие модифицированные или замещенные олигонуклеотиды зачастую являются предпочтительнее нативных форм благодаря требуемым свойствам, таким как, например, усиленное клеточное поглощение, усиленная аффинность в отношении целевой нуклеиновой кислоты и увеличенная стабильность в присутствии нуклеаз. Олигонуклеотид предпочтительно включает в себя два или более нуклеомономера, ковалентно связанных друг с другом с помощью связей (например, фосфодиэфиров) или связей заместителей.
Липкий конец: "Липкий конец" представляет собой относительно короткую одноцепочечную нуклеотидную последовательность на 5'- или 3'-гидроксильном конце двухцепочечной олигонуклеотидной молекулы (также называемый "выступающий участок", "выступающий конец").
Полипептид: Термины "полипептид", "пептид", "олигопептид", "полипептид", "генный продукт", "продукт экспрессии" и "белок" используются взаимозаменяемо в настоящем документе для обозначения полимера или олигомера следующих друг за другом аминокислотных остатков.
Промотор: Термины "промотор", или "промоторная последовательность" являются эквивалентами и используются в настоящем документе для обозначения последовательности ДНК, которая, будучи функционально связанной с представляющей интерес нуклеотидной последовательностью, способна контролировать транскрипцию представляющую интерес нуклеотидную последовательность в РНК. Промотор расположен 5' (т.е. против хода транскрипции), рядом с сайтом начала транскрипции представляющей интерес нуклеотидной последовательности, чью транскрипция в иРНК он контролирует, и обеспечивает сайт для специфического связывания РНК-полимеразой и другими факторами транскрипции для инициации транскрипции. Промотор не содержит кодирующие области или 5' нетранслируемые области. Промотор, например, может являться гетерологичным или гомологичным по отношению к соответствующей клетке. Последовательность молекулы нуклеиновой кислоты является "гетерологичной" организму или второй последовательности молекулы нуклеиновой кислоты, если она происходит из чужеродного вида или, если происходит из того же вида, модифицирована относительно ее исходной формы. Например, промотор, функционально связанный с гетерологичной кодирующей последовательностью, относится к кодирующей последовательности из вида, отличающегося от того, из которого был получен промотор, или, если она происходит из того же вида, то кодирующая последовательность не является естественным образом ассоциированной промотором (например, генетически сконструированная кодирующая последовательность или аллель из другого экотипа или вариетета). Подходящие промоторы можно получить из генов клеток-хозяев, в которых должна происходить экспрессия, или из патогенов для этого хозяина.
Очищенный: Используемый в настоящем документе термин "очищенный" относится к молекулам, либо нуклеиновым, либо аминокислотным последовательностям, которые удалены из своего природного окружения, выделены или отделены. "По существу очищенные" молекулы не содержат по меньшей мере на 60%, предпочтительно по меньшей мере на 75% и более предпочтительно по меньшей мере на 90% другие компоненты, с которыми они ассоциированы в природе. Очищенная последовательность нуклеиновой кислоты может представлять собой выделенную последовательность нуклеиновой кислоты.
Рекомбинантный: Термин "рекомбинантный" в отношении молекул нуклеиновой кислоты относится к молекулам нуклеиновой кислоты, полученным с помощью техник рекомбинантной ДНК. Термин также содержит молекулы нуклеиновой кислоты, которые сами по себе не существуют в природе, но являются модифицированными, измененными, мутированными или подвергнутыми человеком иным манипуляциям. "Рекомбинантная молекула нуклеиновой кислоты" предпочтительно представляет собой не встречающуюся в природе молекулу нуклеиновой кислоты, которая отличается в отношении последовательности от встречающейся в природе молекулы нуклеиновой кислоты по меньшей мере на одну нуклеиновую кислоту. "Рекомбинантная молекула нуклеиновой кислоты" также может содержать "рекомбинантную конструкцию", которая содержит, предпочтительно функционально связанную, последовательность молекул нуклеиновой кислоты, не встречающихся в природе в таком порядке. Предпочтительные способы получения указанной рекомбинантной молекулы нуклеиновой кислоты могут предусматривать техники клонирования, направленный или ненаправленный мутагенез, техники синтеза или рекомбинации.
Значительное увеличение: Увеличение, например, ферментативной активности, генной экспрессии, производительности или выхода определенного продукта, которое превышает предел погрешности, присущий технике измерения, предпочтительно увеличение приблизительно на 10% или 25%, предпочтительно на 50% или 75%, более предпочтительно в 2 раза или в 5 раз или больше относительно активности, экспрессии, производительности или выхода контрольного фермент или экспрессии в контрольной клетке, производительности или выхода контрольной клетки, даже более предпочтительно увеличение приблизительно в 10 раз или больше.
Значительное уменьшение: Уменьшение, например, ферментативной активности, генной экспрессии, производительности или выхода определенного продукта, которое превышает предел погрешности, присущий технике измерения, предпочтительно уменьшение по меньшей мере приблизительно на 5% или 10%, предпочтительно по меньшей мере приблизительно на 20% или 25%, более предпочтительно по меньшей мере приблизительно на 50% или 75%, даже более предпочтительно по меньшей мере приблизительно на 80% или 85%, наиболее предпочтительно по меньшей мере приблизительно на 90%, 95%, 97%, 98% или 99%.
По существу комплементарный: В своем самом широком смысле термин "по существу комплементарный" при использовании в настоящем документе в отношении нуклеотидной последовательности по отношению к эталонной или целевой нуклеотидной последовательности означает нуклеотидную последовательность, характеризующуюся процентным значением идентичности между по существу комплементарной нуклеотидной последовательностью и точно комплементарной последовательностью указанной эталонной или целевой нуклеотидной последовательности по меньшей мере на 60%, более желательно по меньшей мере на 70%, более желательно по меньшей мере на 80% или 85%, предпочтительно по меньшей мере на 90%, более предпочтительно по меньшей мере на 93%, еще более предпочтительно по меньшей мере на 95% или 96%, еще более предпочтительно по меньшей мере на 97% или 98%, еще более предпочтительно по меньшей мере на 99% или наиболее предпочтительно на 100% (последнее является эквивалентом термину "идентичный" в настоящем контексте). Идентичность предпочтительно оценивают по длине, составляющей по меньшей мере 19 нуклеотидов, предпочтительно по меньшей мере 50 нуклеотидов, более предпочтительно по всей длине последовательности нуклеиновой кислоты относительно указанной эталонной последовательности (если не установлено иное). Сравнения последовательностей проводят с использованием анализа GAP с настройками по умолчанию с приложением SEQWEB к GAP согласно University of Wisconsin GCG, основанному на алгоритме Needleman и Wunsch (Needleman and Wunsch (1970) J Mol. Biol. 48: 443-453; согласно приведенному выше определению). Нуклеотидная последовательность, "по существу комплементарная" эталонной нуклеотидной последовательности, гибридизуется с эталонной нуклеотидной последовательностью при условиях низкой жесткости, предпочтительно при условиях умеренной жесткости, наиболее предпочтительно при условиях высокой жесткости (согласно приведенному выше определению).
Трансген: Используемый в настоящем документе термин "трансген" относится к любой последовательности нуклеиновой кислоты, которая введена в геном клетки с помощью экспериментальных манипуляций. Трансген может представлять собой "эндогенную последовательность ДНК" или "гетерологичную последовательность ДНК" (т.е. "чужеродную ДНК"). Термин "эндогенная последовательность ДНК" относится к нуклеотидной последовательности, которая встречается в природе в клетке, в которую она введена при условии, что она не содержит некоторой модификации (например, точечной мутации, присутствия селектируемого маркерного гена и т.д.) относительно встречающейся в природе последовательности.
Трансгенный: Термин трансгенный при обозначении организма означает трансформированный, предпочтительно стабильно трансформированный рекомбинантной молекулой ДНК, которая предпочтительно содержит подходящий промотор, функционально связанный с представляющей интерес последовательностью ДНК.
Вектор: Используемый в настоящем документе термин "вектор" относится к молекуле нуклеиновой кислоты, способной переносить другую молекулу нуклеиновой кислоты, с которой он был связан. Один тип вектора представляет собой интегрированный в геном вектор, или "интегрированный вектор", который может стать интегрированным в геномную ДНК клетки-хозяина. Другой тип вектора представляет собой эписомный вектор, т.е. плазмиду или молекулу нуклеиновой кислоты, способную к экстрахромосомной репликации. Векторы, способные направлять экспрессию генов, с которыми они функционально связаны, в настоящем документе называются "экспрессионные векторы". В настоящем описании "плазмида" и "вектор" используются взаимозаменяемо, если из контекста ясно не следует иное.
Дикий тип: Термин "дикий тип", "природный" или "природное происхождение" в отношении организма означает, что указанный организм не изменен, не мутирован или не подвергся иным манипуляциям со стороны человека. В отношении полипептида или последовательности нуклеиновой кислоты, этот полипептид или последовательность нуклеиновой кислоты встречается в природе или доступна по меньшей мере в одном встречающемся в природе организме, который не изменен, не мутирован или не подвергнут иным манипуляциям со стороны человека.
Дикий тип микроорганизма относится к микроорганизму, чей геном присутствует в таком состоянии, как до введения генетической модификации определенного гена. Генетическая модификация может представлять собой, например, делецию гена или его части или точечную мутацию или введение гена.
Термины "производство" или "производительность" являются общепринятыми в настоящей области техники и включают в себя концентрацию продукта ферментации (например, аланина), образованного в пределах данного периода времени и в данном объеме ферментации (например, кг продукта в час на литр). Термин "эффективность производства" включает в себя время, требуемое для достижения конкретного уровня производства (например, сколько потребуется времени, чтобы клетка достигла конкретной нормы выработки химического вещества тонкого органического синтеза).
Термин "выход" или "отношение выхода продукта к углероду" является общепринятым в настоящей области техники и включает в себя эффективность превращения источника углерода в продукт (т.е. химическое вещество тонкого органического синтеза). Как правило, он записывается в виде, например, кг продукта на кг источника углерода. Путем увеличения выхода или производства соединения увеличивается количество извлеченных молекул или применимых извлеченных молекул этого соединения в данном количестве культуры за данный период времени.
Термин "рекомбинантный микроорганизм" включает в себя микроорганизмы, которые были генетически модифицированы так, что они проявляют измененный или отличающийся генотип и/или фенотип (например, когда генетическая модификация воздействует на кодирующие последовательности нуклеиновой кислоты микроорганизма) по сравнению с микроорганизмом дикого типа, из которого он происходит. Рекомбинантный микроорганизм содержит по меньшей мере одну рекомбинантную молекулу ДНК.
Термин "рекомбинантный" в отношении ДНК относится к молекулам ДНК, полученным человеком с использованием техник рекомбинантной ДНК. Термин предусматривает молекулы ДНК, которые сами по себе не существуют в природе или не существуют в организме, из которого получена ДНК, но которые являются модифицированными, измененными, мутированными или подвергнутыми иным манипуляциям со стороны человека другие. "Рекомбинантная молекула ДНК" предпочтительно представляет собой не встречающуюся в природе молекулу нуклеиновой кислоты, которая отличается в отношении последовательности от встречающейся в природе молекула нуклеиновой кислоты по меньшей мере на одну нуклеиновую кислоту. "Рекомбинантная молекула ДНК" также может содержать "рекомбинантная конструкция", которая содержит, предпочтительно функционально связанную, последовательность молекулы нуклеиновой кислоты, не встречающуюся в природе в таком порядке. Предпочтительные способы получения указанной рекомбинантной молекула ДНК могут предусматривать техники клонирования, направленный или ненаправленный мутагенез, генный синтез или техники рекомбинации.
Термин "направленная эволюция" в настоящем документе используется в качестве синонима термина "метаболическая эволюция" и предусматривает приложение селекционного давления, которое поддерживает рост мутантов с представляющими интерес признаками. Селекционное давление может быть основано на различных условиях культивирования, сопряженной с действием АТФ (аденозинтрифосфат) и ростом селекции и связанной с окислительно-восстановительными реакциями селекции. Селекционное давление можно осуществить с периодической ферментацией с помощью серийного переноса инокуляции или в непрерывной культуре с тем же давлением.
Пример такой рекомбинантной ДНК представляет собой плазмиду, в которую была введена гетерологичная последовательность ДНК, или ген или промотор, который был мутирован по сравнению с геном или промотором, из которого происходит рекомбинантная ДНК. Мутация может быть введена посредством технологий направленного мутагенеза, известных в настоящей области техники, или с помощью технологий случайного мутагенеза, таких как мутагенез под действием химического средства, ультрафиолетового или рентгеновского облучения, или технологий направленной эволюции.
Термин "экспрессия" или "генная экспрессия" означает транскрипцию конкретного(ых) гена(ов) или конкретной конструкции генетического вектора. Термин "экспрессия" или "генная экспрессия", в частности, означает транскрипцию гена(ов) или конструкции генетического вектора в иРНК. Процесс включает в себя транскрипцию ДНК и может включать в себя процессинг полученного продукта РНК. Термин "экспрессия" или "генная экспрессия" также может включать в себя трансляцию иРНК и синтез с ее помощью кодируемого белка, т.е. экспрессию белка.
Краткое описание графических материалов
Фигура 1
Валидация клона после инактивации генов ackA-pta.
А: Ампликон ПЦР, полученный из геномной ДНК Е. coli, W ΔackA-pta::FRT с праймерами P395-ackA-pta-check2 и P395-ackA-pta-check5 (338 п.н.). М: Маркер размера ДНК. В: Секвенирование ампликона ПЦР с P395-ackA-pta-check2 и Р395-аскА-pta-check5 подтвердило точную в отношении пар нуклеотидов модификацию локуса ackA-pta. Нуклеотиды, которые подтверждали с помощью секвенирования, показаны курсивом. Оставшийся сайт FRT показан зеленым, фланкирующие сайты связывания с праймером показаны красным. Прописные буквы: кодирующая последовательность. Строчные буквы: межгенные области.
Валидация клона после инактивации гена adhE.
А: Ампликон ПЦР, полученный из геномной ДНК Е. coli W, ΔackA-pta::FRT ΔadhE::FRT с праймерами Р395-adhE-check2 и P395-adhE-check5 (569 п.н.). M: Маркер размера ДНК. В: Секвенирование ампликона ПЦР с P395-adhE-check2 и Р395-adhE-check5 подтвердило точную в отношении пар нуклеотидов модификацию локуса adhE. Нуклеотиды, которые подтверждали с помощью секвенирования, показаны курсивом. Оставшийся сайт FRT показан зеленым, фланкирующие сайты связывания с праймером показаны красным. Прописные буквы: кодирующая последовательность. Строчные буквы: межгенные области.
Фигура 3
Валидация клона после инактивации генов frdABCD.
А: Ампликон ПЦР, полученный из геномной ДНК Е. coli W, ΔackA-pta::FRT ΔadhE::FRT ΔfrdABCD::FRT с праймерами P395-frd-check1 и P395-frd-check4 (797 п.н.). M: Маркер размера ДНК. В: Секвенирование ампликона ПЦР с P395-frd-check1 и Р395-frd-check4 подтвердило точную в отношении пар нуклеотидов модификацию локуса frd. Нуклеотиды, которые подтверждали с помощью секвенирования, показаны курсивом. Оставшийся сайт FRT показан зеленым, фланкирующие сайты связывания с праймером показаны красным. Прописные буквы: кодирующая последовательность. Строчные буквы: межгенные области.
Фигура 4
Валидация клона после инактивации гена pflB.
А: Ампликон ПЦР, полученный из геномной ДНК Е. coli W, ΔackA-pta::FRT ΔadhE::FRT ΔfrdABCD::FRT ΔpflB::FRT с праймерами P395-pflB-check1 и P395-pflB-check3 (511 п.н.). M: Маркер размера ДНК. В: Секвенирование ампликона ПНР с Р395-pflB-check1 и P395-pflB-check3 подтвердило точную в отношении пар нуклеотидов модификацию локуса pflB. Нуклеотиды, которые подтверждали с помощью секвенирования, показаны курсивом. Оставшийся сайт FRT показан зеленым, фланкирующие сайты связывания с праймером показаны красным. Прописные буквы: кодирующая последовательность. Строчные буквы: межгенные области.
Фигура 5
Валидация клона после интеграции гена alaD-gstear.
А: Ампликон ПЦР, полученный из геномной ДНК Е. coli W, ΔackA-pta::FRT ΔadhE::FRT ΔfrdABCD::FRT ΔpflB::FRT ΔldhA::alaD-gstear с праймерами P395-ldhA-check1 и P395-ldhA-check2 (1833 п.н.). M: Маркер размера ДНК. В: Секвенирование ампликона ПЦР с P395-ldhA-check1 и P395-ldhA-check2 подтвердило точную в отношении пар нуклеотидов модификацию локуса ldhA и интеграцию alaD-gstear. Нуклеотиды, которые подтверждали с помощью секвенирования, показаны курсивом. ORF (открытая рамка считывания) alaD-gstear показана синим, Оставшийся сайт FRT показан зеленым, фланкирующие сайты связывания с праймером показаны красным. Прописные буквы: кодирующая последовательность. Строчные буквы: межгенные области.
Фигура 6
Путь биосинтеза аланина в штамме Ex1 Е. coli (взаимозаменяемо называемый QZ16), который содержит все мутации, описанные в примере 1.
Фигура 7
Геномная организация нового локуса на сайте вставки гена alaD в штамме Ev3 (взаимозаменяемо называемом QZ20), содержащем частичную делецию кодирующей области ydbH и делецию промотора ldhA (который управлял экспрессией гена alaD в штамме QZ16).
Фигура 8
Анализ SDS-PAGE (электрофорез в полиакрилмидном геле с додецилсульфатом натрия) растворимых белковым фракций E. coli W, E. coli QZ16, E. coli QZ20 и E. coli QZ32, выращенных в течение ночи в среде LB при 37 С. Полоса 39,37 кДа аланиндегидрогеназы (AlaD) обведена белой рамкой. Культуры E. coli нормировали к OD600 (оптическая плотность при 600 нм) перед тем, как клетки лизировали. М: Маркер
Фигура 9
Волюметрическую активность аланиндегидрогненазы (alaD) подвергали мониторингу в анализе in vitro с сырыми клеточными лизатами E. coli. Превращение L-аланина в пируват подвергали мониторингу спектрофотометрически по образованию NADH при 340 нм.
Фигура 10
Анализ относительной генной экспрессии alaD в E. coli QZ16 и QZ20 через 8 ч, 11 ч и 28 ч во время периодической ферментации по отношению к E. coli QZ16 через 8 ч. Все полученные от количественной ПЦР данные нормировали к гену rrsA в качестве эталона.
Фигура 11
Периодическая ферментация E. coli QZ16, E. coli QZ32 и E. coli QZ63 в 500 мл среды NBS с 80 г/л глюкозы. Ферментацию контролировали при 37°С, 400 об/мин, при рН 6,8 с 5 н. NH4OH без аэрации. На графике показано образование аланина в корреляции от концентраций аланина в образцах и скорости потребления NH4OH.
Волюметрическая производительность аланина (выход продукта за один проход в единицу времени), определенная как количество образованного продукта, деленное на объем реактора и на время, Е. coli QZ16 (через 50 ч) и QZ32 (ΔydbH-lpdA) и QZ63 (ΔlpdA) до достижения полного потребления глюкозы во время периодической ферментации в 500 мл среды NBS с 80 г/л глюкозы в качестве источника углерода.
Фигура 13
Периодическая ферментация Е. coli QZ33 (ΔydbH-lpdA, Q5H ygaW) и Ε. coli QZ32 (ΔydbH-lpdA) в 500 мл среды NBS с 80 г/л глюкозы. Ферментацию контролировали при 37°С, 400 об/мин, при рН 6,8 с 5 н. NH4OH без аэрации. На графике показано образование аланина в корреляции от концентраций аланина в образцах и скорости потребления NH4OH.
Фигура 14
Волюметрическая производительность аланина (выход продукта за один проход в единицу времени), определенная как количество образованного продукта, деленное на объем реактора и на время, Е. coli QZ32 (ΔydbH-ldhA), QZ60 (ΔydbH-ldhA, ygaW Q5N), QZ61 (ΔydbH-ldhA, ygaW Q5R), QZ62 (ΔydbH-ldhA, ygaW Q5Y) и QZ33 (ΔydbH-ldhA, Q5H ygaW) до достижения полного потребления глюкозы во время периодической ферментации в 500 мл среды NBS с 80 г/л глюкозы в качестве источника углерода.
Фигура 15
Периодическая ферментация Е. coli QZ60 (ΔydbH-lpdA, ygaW Q5N), Ε.coli QZ61 (ΔydbH-lpdA, ygaW Q5R) и Ε. coli QZ62 (ΔydbH-lpdA, ygaW Q5Y) по сравнению с Ε. coli QZ32 (ΔydbH-lpdA) и E. coli QZ33 (ΔydbH-lpdA, Q5H ygaW) в 500 мл среды NBS с 80 г/л глюкозы. Ферментацию контролировали при 37°С, 400 об/мин, при рН 6,8 с 5 н. NH4OH без аэрации. На (А) показано образование биомассы в ходе ферментации. На (В) показано образование аланина в корреляции от концентраций аланина в образцах и скорости потребления NH4OH.
Фигура 16
Анализ относительной генной экспрессии ygaW in Ε. coli QZ16 и QZ20 через 8 ч, 11 ч и 28 ч в периодической ферментации по отношению к Е. coli QZ16 через 8 ч, что определяли с помощью ОТ-кПЦР (количественная полимеразная цепная реакция с обратной транскриптазой). Все полученные от кПЦР данные нормировали к гену rrsA в качестве эталона.
Фигура 17
Периодическая ферментация Е. coli QZ41 (ΔydbH-ldhA, Q5H ygaW, SNP (однонуклеотидный полиморфизм) zipA) и Ε. coli QZ33 (ΔydbH-ldhA, Q5H ygaW) в 500 мл среды NBS с 80 г/л глюкозы. Ферментацию контролировали при 37 С, 400 об/мин, при рН 6,8 с 5 н. NH4OH без аэрации. На графике показано образование аланина в корреляции от концентраций аланина в образцах и скорости потребления NH4OH.
Фигура 18
Волюметрическая производительность аланина (выход продукта за один проход в единицу времени), определенная как количество образованного продукта, деленное на объем реактора и на время, Е. coli QZ33 (ΔydbH-ldhA, Q5H ygaW) и QZ 41 (ΔydbH-ldhA, Q5H ygaW, SNP zipA) до достижения полного потребления глюкозы во время периодической ферментации в 500 мл среды NBS с 80 г/л глюкозы в качестве источника углерода.
Фигура 19
Периодическая ферментация Е. coli QZ52 (ΔydbH-ldhA, Q5H ygaW, SNP lpd) и Ε. coli QZ33 (ΔydbH-ldhA, Q5H ygaW) в 500 мл среды NBS с 100 г/л глюкозы. Ферментацию контролировали при 37°С, 400 об/мин, при рН 6,8 с 5 н. NH4OH без аэрации. На (А) показано образование биомассы обоих штаммов в ходе ферментации. На (В) показано образование аланина в корреляции от концентраций аланина в образцах и скорости потребления NH4OH.
Фигура 20
Волюметрическая производительность аланина (выход продукта за один проход в единицу времени), определенная как количество образованного продукта, деленное на объем реактора и на время, E. coli QZ33 (ΔydbH-ldhA, Q5H ygaW) и QZ52 (ΔydbH-ldhA, Q5H ygaW, SNP lpd) через 41 ч периодической ферментации в 500 мл среды NBS с 100 г/л глюкозы в качестве источника углерода. В то время как QZ53 полностью потребил всю глюкозу через 41 ч, QZ33 не был способен полностью потребить глюкозу при исследуемых условиях вплоть до 53 ч.
Фигура 21
Волюметрическая производительность аланина (выход продукта за один проход в единицу времени), определенная как количество образованного продукта, деленное на объем реактора и на время, E. coli QZ32 (ΔydbH-ldhA), QZ33 (ΔydbH-ldhA, Q5H ygaW), QZ41 (ΔydbH-ldhA, Q5H ygaW, SNP zipA) и QZ53 (ΔydbH-ldhA, Q5H ygaW, SNP zipA, SNP lpd) до достижения полного потребления глюкозы во время периодической ферментации в 500 мл среды NBS с 80 г/л глюкозы в качестве источника углерода.
Фигура 22
Периодическая ферментация E. coli QZ53 (ΔydbH-ldhA, Q5H ygaW, SNP zipA, SNP lpd) и Ε.coli QZ41 (ΔydbH-ldhA, Q5H ygaW, SNP zipA) в 500 мл среды NBS с 100 г/л глюкозы. Ферментацию контролировали при 37°С, 400 об/мин, при рН 6,8 с 5 н. NH4OH без аэрации. На графике показано образование титра аланина в корреляции от концентраций аланина в образцах и скорости потребления NH4OH.
Фигура 23
Волюметрическая производительность аланина (выход продукта за один проход в единицу времени), определенная как количество образованного продукта, деленное на объем реактора и на время, Е. coli QZ53 (ΔydbH-ldhA, Q5H ygaW, SNP zipA, SNP lpd) и QZ41 (ΔydbH-ldhA, Q5H ygaW, SNP zipA) до достижения полного потребления глюкозы во время периодической ферментации в 500 мл среды NBS с 80 г/л глюкозы в качестве источника углерода.
Фигура 24
Периодическая ферментация Е. coli QZ33 (ΔydbH-ldhA, Q5H ygaW) с контрольной плазмидой pACYC184 и Е. coli QZ33 с плазмидой pACYC184-lpd с дополнительной копией ORF lpd в 500 мл среды NBS с 80 г/л глюкозы. Ферментацию контролировали при 37°С, 400 об/мин, при рН 6,8 с 5 н. NH4OH без аэрации. На графике показано образование титра аланина в корреляции от концентраций аланина в образцах и скорости потребления NH4OH.
Фигура 25
Волюметрическая производительность аланина (выход продукта за один проход в единицу времени), определенная как количество образованного продукта, деленное на объем реактора и на время, Е. coli QZ33 (ΔydbH-ldhA, Q5H ygaW) с контрольной плазмидой pACYC184 и Е. coli QZ33 с плазмидой pACYC184-lpd с дополнительной копией ORF lpd до достижения полного потребления глюкозы во время периодической ферментации в 500 мл среды NBS с 80 г/л глюкозы в качестве источника углерода.
Примеры
Химические соединения и общие способы
Если не указано иное, процедуры клонирования, проведенные для целей согласно настоящему изобретению, включая в себя обработку рестрикционными ферментами, электрофорез в агарозном геле, очистка нуклеиновых кислот, лигирование нуклеиновых кислот, трансформацию, селекцию и культивирование бактериальных клеток, проводили, как описано (Sambrook et al., 1989). Анализы последовательностей рекомбинантной ДНК проводили с помощью лазерного флуоресцентно секвенатора ДНК (Applied Biosystems, Фостер-Сити, Калифорния, США) с использованием технологии Sanger (Sanger et al., 1977). Если не описано иное, химические соединения и реагенты получали от Sigma Aldrich (Sigma Aldrich, Сент-Луис, США), от Promega (Мэдисон, Висконсин, США), Duchefa (Харлем, Нидерланды) или Invitrogen (Карлсбад, Калифорния, США). Рестрикционные энонуклеазы получали от New England Biolabs (Ипсвич, Массачусетс, США) или Roche Diagnostics GmbH (Пензберг, Германия). Олигонуклеотиды синтезировали Eurofíns MWG Operon (Эберсберг, Германия).
Пример 1:
Е. coli W (LU17032) конструировали для получения L-аланина путем инактивации ORF ackA-pta, adhE, frdABCD и pflB и замещения ORF ldhA кодон-оптимизированным вариантом гена alaD (alaD-gstear).
ORF ackA-pta, adhE, frdABCD и pflB инактивировали путем вставки фланкированной FRT кассеты устойчивости к канамицину с последующим удалением кассеты устойчивости к антибиотику с помощью рекомбинации FLP.
Ген ldhA замещали на alaD-gstear и расположенную ниже по ходу транскрипции фланкированную FRT кассету устойчивости к зеоцину, которую в конце удаляли с помощью рекомбинации FLP.
Материалы и способы
Бактериальная культура
Е. coli W (LU17032) культивировали в жидкой среде Лурия-Бертани (LB) или на твердой среде Лурия-Бертани. По мере необходимости клоны пересевали на М9 минимальный агар, содержащий 10 мМ сахарозы для подтверждаения идентичности штамма W. Антибиотики добавляли к жидкой и твердой средам при необходимости до конечных концентраций, составляющих 15 мкг/мл (канамицин, хлорамфеникол), 25 мкг/мл (зеоцин) или 3 мкг/мл (тетрациклин).
Рекомбинация Red/ET
Рекомбинацию Red/ET проводили с использованием стандартных протоколов Gene Bridges GmbH (wvvw.genebridges.com). Кратко, Red/ET-компетентную Ε. coli W аэробно выращивали при 30°С до OD600 нм, составляющей ~0,3. Экспрессию генов red индуцировали путем добавления 50 мкл 10% (масс/объем) L-арабинозы с последующим увеличением температуры до 37°С. От действия арабинозы исключали неиндуцированные контрольные культуры. Через 35 мин инкубации при 37°С клетки отмывали дважды ледяным 10% (объем/объем) глицерином и подвергали электропорации с помощью 500 нг продукта ПЦР при 1,35 кВ, 10 мкФ, 600 Ом. Затем клетки ресуспендировали в 1 мл ледяной среды LB и аэробно выращивали при 37°С в течение приблизительно 1,5 ч. Культуры затем помещали на LB агар, содержащий 15 мкг/мл канамицина (нокауты) или 25 мкг/мл зеоцина (нокин).
Рекомбинация FLP
Фланкирующие сайты FRT обеспечивали возможность удаления маркеров устойчивости к антибиотикам с помощью рекомбинации FLP после модификации хромосомы Е. coli. Рекомбинация FLP оставляет один сайт FRT (34 п.н.), а также короткие фланкирующие последовательности (приблизительно 20 п.н. каждая), которые используют в качестве сайтов связывания с праймером в амплификации кассет.
Для проведения рекомбинации FLP плазмиду 708-FLPe (таблица 1), кодирующую рекомбиназу FLP, вводили в Red/ET рекомбинанты путем электропорации. Трансформанты KanR CmR или ZeoR CmR использовали для инокуляции 0,2 мл культур LB, которые инкубировали при 30°С в течение 3 ч. Затем индуцировали активность FLP путем сдвига температуры до 37°С с последующей трехчасовой инкубацией при 37°С. Отдельные колонии, полученные из этих культур, впоследствии подвергали скринингу в отношении фенотипа CmS и KanS или ZeoS.
Получение и анализ ДНК
Геномную ДНК (гДНК) Е. coli выделяли из ночных культур с помощью набора Gentra Puregene Yeast/Bact. Kit В (Qiagen, Хильден, Германия). Продукты ПЦР, содержащие кассеты нокаута или нокина, амплифицировали из матричных плазмид с высокоточной ДНК-полимеразой PRECISOR (BioCat, Гейдельберг) и реакции аналитической ПЦР проводили с помощью системы ПЦР PCR Extender System (5PRIME GmbH, Гамбург, Германия) согласно рекомендациям производителя. Ампликоны ПЦР очищали с использованием набора для очистки GeneJET PCR Purification Kit или набора для гель-экстракции GeneJET Gel Extraction Kit (Fermentas, Санкт-Леон-Рот, Германия) и секвенирование проводили с помощью GATC Bio Tech (Констанц, Германия) или BioSpring (Франкфурт-на-Майне, Германия).




1.1. Локус ackA-pta - Нацеленное воздействие на ackA-pta
Около 500 нг конструкции ПЦР ΔackA-pta (1737 п.н.) подвергали электропорации в Red/ET-компетентные клетки Е. coli W, содержащие модификацию. 8 трансформантов KanR анализировали в отношении правильной интеграции маркерной кассеты устойчивости с помощью ПЦР со специфическими для генома праймерами. Три клона подвергали рекомбинации FLP, которую проводили, как описано в разделе Материалы и способы (данные не показаны).
Валидация клона. Инактивацию локуса ackA-pta локус и удаление кассеты устойчивости к канамицину подтверждали с помощью ПЦР по оставшемуся отпечатку FRT. Один клон, который давал на выходе правильный сигнал ПЦР, также подтверждали с помощью секвенирования (фиг. 1).
1.2 Локус adhE - Нацеленное воздействие на adhE
Около 500 нг конструкции ПЦР ΔadhE (1093 п.н.) подвергали электропорации в Red/ET-компетентные клетки Е. coli W, содержащие модификацию ΔackA-pta::FRT. 8 трансформантов KanR анализировали в отношении правильной интеграции маркерной кассеты устойчивости с помощью ПЦР со специфическими для генома праймерами. Два клона подвергали рекомбинации FLP, которую проводили, как описано в разделе Материалы и способы (данные не показаны).
Валидация клона. Инактивацию локуса adhE и удаление кассеты устойчивости к канамицину подтверждали с помощью ПЦР по оставшемуся отпечатку FRT. Один клон, который давал на выходе правильный сигнал ПЦР, также подтверждали с помощью секвенирования (фиг. 2).
1.3 Локус frd - Нацеленное воздействие на frdABCD
Около 500 нг конструкции ПЦР ΔfrdABCD (1093 п.н.) подвергали электропорации в Red/ET-компетентные клетки Е. coli W, содержащие модификации ΔackA-pta::FRT и ΔadhE::FRT. 8 трансформантов KanR анализировали в отношении правильной интеграции маркерной кассеты устойчивости с помощью ПЦР со специфическими для генома праймерами. Один клон подвергали рекомбинации FLP, которую проводили, как описано в разделе Материалы и способы (данные не показаны).
Валидация клона. Инактивацию локуса frd и удаление кассеты устойчивости к канамицину подтверждали с помощью ПЦР по оставшемуся отпечатку FRT. Один клон, который давал на выходе правильный сигнал ПЦР, также подтверждали с помощью секвенирования (фиг. 3).
1.4 Локус pflB - Нацеленное воздействие на pflB
Около 500 нг конструкции ПЦР ΔpflB (1093 п.н.) подвергали электропорации в Red/ET-компетентные клетки Е. coli W, содержащие модификации ΔackA-pta::FRT, ΔadhE::FRT и ΔfrdABCD::FRT. 8 трансформантов KanR анализировали в отношении правильной интеграция маркерной кассеты устойчивости с помощью ПЦР со специфическими для генома праймерами. Четыре клона подвергали рекомбинации FLP, которую проводили, как описано в разделе Материалы и способы (данные не показаны).
Валидация клона. Инактивацию локуса pflB и удаление кассеты устойчивости к канамицину подтверждали с помощью ПЦР по оставшемуся отпечатку FRT. Один клон, который давал на выходе правильный сигнал ПЦР, также подтверждали с помощью секвенирования (фиг. 4).
1.5 Локус ldhA - Нокин alaD-gstear
Около 500 нг конструкции ПЦР ΔldhA::alaD-gstear (1783 п.н.) подвергали электропорации в Red/ET-компетентные клетки Е. coli W, содержащие модификации ΔackA-pta::FRT, ΔadhE::FRT, ΔfrdABCD::FRT и ΔpflB::FRT. 4 трансформанта ZeoR анализировали в отношении правильной интеграция маркерной кассеты устойчивости с помощью ПЦР со специфическими для генома праймерами. Один клон подвергали рекомбинации FLP, которую проводили, как описано в разделе Материалы и способы (данные не показаны).
Валидация клона. Интеграцию alaD-gstear и удаление кассеты устойчивости к зеоцину подтверждали с помощью ПЦР по оставшемуся отпечатку FRT. Один клон, который давал на выходе правильный сигнал ПЦР, также подтверждали с помощью секвенирования (фиг. 5).
Пример 2 Обнаружение и количественная оценка аланина с помощью HPLC (высокоэффективной жидкостной хроматографии)
Использовали следующий способ HPLC для обнаружения аланина в культуре для культивирования клеток:
Колонка: колонка Aminex НРХ-87С (Bio-Rad), 300×7,8 мм, внутренний диаметр частиц 9 м км
Подвижная фаза: Са(NO3)2 при 0,1 моль/л 90%, ацетонитрил 10%
Объемная скорость потока: 0,6 мл/мин
Температура колонки: 60°С
Обнаружение: рефрактометрический детектор
При описанном выше способе основные оцениваемые компоненты в матриксе образца клеточной культуры могут быть хорошо отделены от аланина, не оказывая воздействия на количественное определение аланина.
Количество аланина в образце определяли с помощью способа калибровки внешнего стандарта. Стандартные образцы, содержащие аланин от 0,5 до 10,0 г/л, вводили в хроматограф и площади пиков использовали для калибровки. Коэффициент линейной регрессии калибровочной кривой составлял 0,9995.
Образцы вводили в хроматограф один раз в объеме, составляющем 20 мкл. Площади пиков использовали для расчета количества, присутствующего в образце с помощью программного обеспечения Waters LC Millenium.
Пример 3 Обнаружение и количественное определение с помощью HPLC глюкозы, сукцината, лактата, формиата, ацетата и этанола
Используемый способ HPLC
Колонка: колонка Aminex НРХ-87Н (Bio-Rad), 300×7,8 мм, внутренний диаметр частиц 9 мкм
Подвижная фаза: H2SO4 4 мМ
Объемная скорость потока: 0,4 мл/мин
Температура колонки: 45°С
Обнаружение: рефрактометрический детектор
Количество аналитов определяли с помощью способа калибровки внешнего стандарта. Стандартные образцы, содержащие глюкозу в концентрации, составляющей 0,1-38,0 г/л, сукцинат, лактат, формиат, ацетат и этанол в концентрации, составляющей 0,05-10,0 г/л, вводили в хроматограф и площади пиков использовали для калибровки. Коэффициенты линейной регрессии для всех шести калибровочных кривых были лучше, чем 0,999.
Образцы вводили в хроматограф один раз в объеме, составляющем 20 мкл. Площади пиков использовали для расчета количества, присутствующего в образце с помощью программного обеспечения Waters LC Millenium.
Пример 4 Метаболическая эволюция штамма E. coli W, полученного из примера 1, для улучшенного выхода аланина
Штамм Е. Coli, содержащий все мутации, описанные в примере 1, имеющий название Е. coli Ex1 или QZ16, использовали для процедуры метаболической эволюции для улучшения выхода аланина для штамма Е. coli Ex1.
Метаболическую эволюцию проводили следующим образом: В первом и втором цикле эволючии проводили непрерывную эволюцию в течение 500 часов и 750 часов, соответственно, в среде NBS с содержанием 5% глюкозы.
Среда NBS:
3,5 г KH2PO4
5,0 г K2HPO4
3,5 г (NH4)2HPO4
0,25 г MgSO4-7H2O
15 мг CaCL2-2H2O
0,5 мг тиамина
1 мл маточного раствора микроэлементов
Маточный раствор микроэлементов готовили в 0,1 M HCL, 1,6 г FeCL3-6H2O; 0,2 г CoCl2-6H2O; 0,1 г CuCl2-2H2O; 0,2 г ZnCl2; 0,2 г NaMoO4-2H2O; 0,05 г H3BO3.
Клетки сеяли штрихом на планшеты с LB и исследовали с отношении выхода аланина. Лучший штамм Е. coli (Ε. coli Evl или QZ17) давал в результате при ферментации со средой NBS, содержащей 5% глюкозы, в течение 24 и 48 ч при 37°С выход аланина, составляющий 84%-86% по сравнению с выходом аланина исходного штамма Е. coli Ex1, дающем в результате 80%-83%.
Е. coli Evl использовали для дополнительных стадий эволюции, которые проводили как периодическую эволюцию в течение 20 дней. 5% клеток повторно инокулировали в свежую среду каждые 24 ч, 48 ч, 72 ч и так далее в среде AM1, содержащей 14% глюкозы, при 37°С.
Среда AM1:
|
15 г/л сульфата аммония добавляли на первой стадии
1 мм бетаина
1 мл маточного раствора микроэлементов
Для получения 1 л маточного раствора микроэлементов:
Маточный раствор микроэлементов получали в 0,12 M HCL, 2,4 г FeCL3-6H2O; 0,3 г CoCl2-6H2O; 0,21 г CuCl2-2H2O; 0,3 г ZnCl2; 0,27 г NaMoO4-2H2O; 0,068 г H3BO3; 0,5 г MnCl2-4H2O
Из этой эволюция выделяли штамм Е. coli Ev2, который также называется QZ18. Указанный штамм исследовали в ферментации, которую проводили в ферментере со средой AM1 с 14% глюкозы. Штамм Е. coli Ev2 характеризовался выходом аланина, составляющим 92%-94%, по сравнению с выходом аланина для Е. coli Ev1, составляющим 91%-92% при таких же условиях.
После таких дополнительных стадий периодической эволюции в течение 300 ч в среде AM1, содержащей 12% глюкозы, и последующих 10 стадий периодической эволюции в среде AM1, содержащей 12% глюкозы, выделяли штамм Е. coli Ev3, который также называется QZ20.
Исследование в отношении выхода аланина выявило, что штамм Е. coli Ev3 характеризовался выходом аланина, составляющим 94%-96% в среде AM1, содержащей 12% глюкозы, по сравнению с выходом аланина, характерным для Е. coli Ev2, составляющим 92% - 93% при таких же условиях.
Пример 5 Определение мутаций в штамме Б. coli Ev3 по сравнению с Е. coli Ex1
Геномы штаммов Е. Coli, Ε. coli Ex1 и Ε. coli Εv3, секвенировали и результаты сравнивали для определения мутаций, которые приводят к увеличенному выходу аланина, характерному для штамма Е. coli Ev3.
Идентифицировали мутацию в гене lpd, которая изменяла последовательность гена lpd с SEQ ID NO 49, кодирующей белок, характеризующийся SEQ ID NO 50 в штамме Е. coli Ex1, на SEQ ID NO 51, кодирующую белок, характеризующийся SEQ ID NO 52 в штамме Ε. coli Ev3.
Дополнительно идентифицировали мутацию в гене zipA, которая изменяла последовательность гена zipA с SEQ ID NO 45, кодирующей белок, характеризующийся SEQ ID NO 46 в штамме Е. coli Ex1, на SEQ ID NO 47, кодирующую белок, характеризующийся SEQ ID NO 48 в штамме Ε. coli Ev3.
Также идентифицировали мутацию в гене ygaW, которая изменяла последовательность гена ygaW с SEQ ID NO 1, кодирующей белок, характеризующийся SEQ ID NO 2 в штамме Е. coli Ex1, на SEQ ID NO 3, кодирующую белок, характеризующийся SEQ ID NO 4 в штамме Ε. coli Ev3.
Более того, идентифицировали частичную делецию кодирующей области ydbH и делецию промотора ldhA, управляющего экспрессией гена alaD, и частичную делецию 5' кодирующей области гена ydbH перед геном alaD, которые приводят ген alaD под контроль промотора, характеризующегося SEQ ID NO: 55. В отношении деталей геномной организации нового локуса смотрите фигуре 7.
Пример 6 Подтверждение эффекта мутированного промотора гена alaD на выход аланина
Для подтверждения эффекта делеции, расположенной против хода транскрипции гена alaD, которая была обнаружена в Е. coli Ev3/QZ20, на выход и производительность аланина, делецию вводили в геном Е. coli Ex1 (QZ16) для создания Е. coli QZ32.
Конструирование штамма Е. coli QZ32
Кассета ydbH-ldhA-cat-sacB (3091 п.н.) с селектируемым маркером устойчивости к хлорамфениколу и маркером контрселекции sacB (подтверждает чувствительность к сахарозе) амплифицировали из матричного вектора pQZ11 Genescript) с праймерами Rec1_1_F и Rec 1_1_R с помощью высокоточной ДНК-полимеразы Phusion Hot Start High-Fidelity DNA Polymerase (Thermo). Продукт ПЦР обрабатывали DpnI (NEB) при 37C в течение 1 ч для снижения фона плазмиды - матрицы и подвергали гель-экстракции из 1% агарозного геля с помощью набора QIAquick Gel Extraction Kit (Qiagen). Кассету делеции ydbH-ldhA (116 п.н.) амплифицировали из набора способных к самоотжигу праймеров Rec1_2_F и Rec 1_2_R с помощью высокоточной ДНК-полимеразы Phusion Hot Start High-Fidelity ДНК Polymerase (Thermo) и очищали с помощью набора QIAquick PCR Purification Kit (Qiagen).
Для рекомбинация Red/ET использовали набор Genebridges Red/ET Recombination Kit согласно протоколу производителя. Приблизительно 200 нг продукта ПЦР ydbH-ldhA-cat-sacB подвергали электропорации в Red/ET-компетентные клетки Е. coli Ex1. Культуры помещали на планшеты, содержащие агар LB с 10 мкг/мл хлорамфеникола для селекции положительных трансформантов после электропорации. Несколько колоний подвергали скринингу в отношении интеграции маркерной кассеты с помощью ПЦР с геном-специфическими праймерами Rec1_seq_F и Rec1_seq_R. Подтвержденный с помощью ПЦР клон использовали для второй рекомбинации Red/ET с кассетой делеции ydbH-ldhA для замещения маркерной кассеты cat-sacB. Культуры помещали на планшеты с агаром и LB с 6% сахарозы без NaCl для селекции положительных трансформантов после электропорации. Несколько колоний исследовали с помощью геном-специфических праймеров Rec1_seq_F и Rec1_seq_R в отношении потери маркерной кассеты cat-sacB. По меньшей мере один клон, который давал на выходе продукт ПЦР правильного размера, также подтверждали с помощью секвенирования (Genewiz). Термочувствительную, полученную с помощью рекомбинационной инженерии плазмиду pRedET (amp) извлекали из штаммов при 42°С в течение ночи на планшетах с LB перед тем, как штаммы исследовали в биореакторе. Делецию ydbH-ldhA вводили в штамм Ε coli Ex1 (QZ16). Полученный штамм QZ16 с делецией промотора ydbH-ldhA обозначали как QZ32.
Определение ролей делеции ydbH и нового промотора alaD
Для того чтобы дополнительно охарактеризовать механизм, с помощью которого достигается избыточная экспрессия alaD вследствие делеции промотора 529 п.н. ydbH-ldhA и для определения того, играет ли в этом роль делеция частичного гена ydbH, конструировали два штамма на основе Е. coli QZ16. В Е. coli QZ63 удаляли только 50 пн. промоторную последовательность ldhA и вместо нее добавляли дополнительные пары оснований TATTG, которые, как предполагают, являются комплементарными новой промоторной последовательности alaD, с образованием нового промотора (SEQ ID NO: 55). В Ε. coli QZ64 весь ген ydbH удаляли, тогда как исходный промотор ldhA оставляли неизменным.
Конструирование штамма Е. coli QZ63 и Е. coli QZ64
Конструирование штамма для Е. coli QZ63 и Е. coli QZ64 проводили, как описано ранее. Кассету ΔPldhA-cat-sacB (3091 п.н.) амплифицировали с праймерами Rec1B_1_F и Rec1B_1_R и кассету ΔydbH-cat-sacB (3091 п.н.) с праймерами Rec1C_1_F и Rec1C_1_R. Полученные ампликоны ПЦР использовали в качестве субстратов для рекомбинации Red/ET в Е. coli QZ16. Кассету делеции PldhA (125 п.н.) и кассету делеции ydbH- (108 п.н.) амплифицировали со способными к самоотжигу праймерами Rec1B_2_F и Rec1B_2_R и Rec1C_2_F и Rec1C_2_R, соответственно. Ампликоны ПЦР использовали для замещения маркерных кассет cat-sacB и для создания требуемых генотипов Е. coli QZ63 и Е. coli QZ64. Колонии Е. coli QZ63 исследовали посредством ПЦР с геном-специфическими праймерами Rec1B_seq_F и Rec1B_seq_R и по меньшей мере один положительный клон подтверждали путем секвенирования. Колонии Е. coli QZ64 исследовали с помощью ПЦР с геном-специфическими праймерами Rec1C_seq_F и Rec1C_seq_R и по меньшей мере один положительный клон подтверждали путем секвенирования.
Анализ SDS-PAGE
Для исследования эффекта делеции промотора ydbH-ldhA на уровень экспрессии alaD, анализ SDS-PAGE созданного Е. coli QZ32 проводили в сравнении с Е. coli W, Ε. coli QZ16 и Ε. coli QZ20. Клетки из ночной культуры в среде LB при 37 С, 200 об/мин, нормировали к OD600, собирали и лизировали. Растворимые белковые фракции загружали на SDS-PAGE для сравнения.
Количество экспрессированного alaD (39,37 кДа) в штамме с 529 п.н. делецией промотора ydbH-ldhA (QZ32), обнаруженная в Е. coli QZ20, было значительно выше, чем в QZ16 и сравнимо с уровнями экспрессии AlaD в QZ20 (фигура 8). Этот результат показывает, что 529 п.н. делеция, обнаруженная в Е. coli QZ20, расположенная против хода транскрипции alaD, вызывает значительную избыточную экспрессию гена alaD.
Ферментативный анализ AlaD in vitro
Е. coli QZ32 исследовали в отношении активности AlaD в сырых клеточных лизатах in vitro в сравнении с клеточными лизатами Е. coli W, Е. coli QZ16 и Е. coli QZ20.
Сырые лизаты получали из ночных культур, выращенных при 37С в среде LB. Клетки осаждали путем центрифугирования и лизировали с использованием детергента BugBuster (Novagen) согласно рекомендуемому производителем протоколу. Концентрации общего белка сырых лизатов определяли с использованием анализа Брэдфорда Brad&od Assay (Amresco) и стандартной кривой бычьего сывороточного альбумина (BSA). Реакция, катализируемая alaD (L-аланин + Н2О + NAD +  пируват + NH3 + NADH + Н+) является обратимой и обратное превращение L-аланина в пируват подвергали мониторингу опосредованно через образование NADH с помощью спектрофотометра при λ=340 нм.
пируват + NH3 + NADH + Н+) является обратимой и обратное превращение L-аланина в пируват подвергали мониторингу опосредованно через образование NADH с помощью спектрофотометра при λ=340 нм.
Реакция анализа in vitro содержала 125 мМ глицин/KOH (рН 10,2), 100 мМ L-аланин в 125 мМ глицине/KOH (рН 10,2), 1,25 мМ NAD+ в 10 мМ трис-HCl (рН 7,0) и 10 мкл сырого клеточного лизата, нормированного к OD600 в смеси глицин/KOH (общий анализируемый объем составил 300 мкл). Компоненты для анализа объединяли на льду и реакцию начинали путем добавления NAD. Регистрацию кинетических параметров (λ=340 нм) проводили при 37°С × 15 мин (каждые 30 с).
Сырой лизат Е. coli W, который не содержит ген alaD, производил результаты, сходные с отрицательным контролем без сырого клеточного лизата (фигура 9). Как предполагали из анализа SDS-PAGE (фигура 8), Е. coli QZ16, в котором ген ldhA замещали геном alaD, показал только небольшую ферментативную активность alaD по сравнению с Е. coli W. QZ20 с делецией промотора ydbH-alaD, который продемонстрировал значительно повышенную волюметрическую ферментативную активность alaD по сравнению с Е. coli QZ16, что предполагали на основании наблюдаемого увеличения экспрессии AlaD. Волюметрическая ферментативная активность alaD у Е. coli QZ32 была близка к ферментативной активности у Е. coli QZ20.
Анализ ОТ-кПЦР уровня транскрипции гена alaD
Наряду с проведением анализа SDS-PAGE для мониторинга экспрессии белка alaD уровни транскрипции alaD определяли с помощью количественной ПЦР с обратной транскрипцией (ОТ-кПЦР). Набор iTaq Universal One-Step Kit от Biorad использовали для одностадийных реакций с обратной транскрипцией (ОТ)-кПЦР на основе SYBR Green. Из параллельной периодической ферментации Е. coli QZ16 и Е. coli QZ20, которую проводили, как описано выше, образцы культуры забирали через 8, 11, 22, 28 и 48 ч. Образцы немедленно обрабатывали реагентом RNAprotect Bacteria Reagent (Qiagen) для стабилизации РНК. РНК экстрагировали из образцов с помощью набора AurumTotal RNA Mini Kit (Biorad) согласно руководству производителя. Выделенную РНК дополнительно обрабатывали с помощью набора DNA-free DNA Removal Kit (lifetechnologies) для удаления геномной ДНК - примеси и снижения фона во время кПЦР. РНК количественно определяли спектрофотометрически при λ=260 нм.
7-стадийную серию 10-кратного разведения 100 нг РНК Е. coli QZ16 исследовали с помощью праймеров ОТ-кПЦР (таблица 1)) alaD_RT_F и alaD_RT_R, специфических в отношении гена alaD, и rrsA_RT_F и rrsA_RT_R, специфических в отношении гена rrsA, кодирующего рибосомную 16S РНК, который служил в качестве эталонного гена во время испытаний кПЦР. Подходящий линейным динамический диапазон разведений РНК, который приводил к эффективностям сигнала амплификации 90%<Ε<110% и фактор линейной регрессии R2>0,985 определяли для каждого набора праймеров ОТ-кПЦР. rrsA исследовали в отношении его применимости в качестве внутреннего эталонного гена для нормализации и обнаружили, что он стабильно экспрессировался во всех исследуемых образцах (данные не показаны). Реакции ОТ-кПЦР проводили с помощью системы CFX96 Touch Real-Time PCR Detection System (Biorad) согласно протоколу производителя. Относительное количественное определение генной экспрессии рассчитывали с помощью РНК Е. coli QZ16 через 8 ч в качестве внутреннего калибровочного стандарта согласно способу ΔΔCt.
alaD демонстрирует увеличенную в 11 раз экспрессию в Е. coli QZ20 по сравнению с Е. coli QZ16 (фигура 10) через 8 ч. Это является еще одним подтверждением влияния делеции промотора ydbH-ldhA на экспрессию гена alaD.
Испытание ферментации Е. coli QZ32 по сравнению с Е. coli QZ16
Штамм Е. coli QZ32 исследовали в отношении его производительности во время ферментации биореакторе лабораторного масштаба. Образование аланина подвергали мониторингу по сравнению со штаммами Е. сой QZ16 и QZ20.
Прекультуры выращивали во встряхиваемых колбах со средой LB, с 20% объемом наполнения при 37С и 200 об/мин в течение ночи. Ферментацию проводили в системе 1,5 л параллельных биореакторов DASGIP (Eppendorf) в 500 мл среды NBS (3,50 г/л KH2PO4, 5,00 г/л K2HPO4, 0,25 г/л MgSO4⋅7 H2O, 3,50 г/л (NΗ4)2ΗΡΟ4 0,5 мг/л тиамина, 15,00 мг/л CaCl2⋅2 H2O, 15,00 г/л (NH4)2SO4 153,61 мг/л бетаина, 1 мл/л маточного раствора микроэлементов). Маточный раствор микроэлементов содержал 1,6 г/л FeCL3⋅6 H2O; 0,2 г/л CoCl2⋅6 H2O; 0,1 г/л CuCl2⋅2 H2O; 0,2 г/л ZnCl2; 0,2 г/л NaMoO4⋅2 H2O; 0,05 г/л Н3ВО3, 0,1 M HCL. 80 г/л глюкозы использовали в качестве источника углерода в среде ферментации.
Клетки Е. coli, эквивалент 7 мл при OD600, собирали посредством центрифугирования и ресуспендировали в 5 мл среды NBS. # OD600⋅мл=(OD600 неразведенной культуры) × (объем культуры в мл). 5 мл ресуспендированных клеток использовали для инокуляции 500 мл среды ферментации в 1,5 л биореакторе DASGIP. Каждый штамм исследовали в двух параллелях при 37°С и скорости мешалки, составляющей 400 об/мин. 5 н. NH4OH использовали для контроля рН до 6,8 и обеспечения культуры аммонием в качестве предшественника аланина в ходе ферментации. Во время ферментации не распыляли воздух и сосуд не находился под давлением, так что после начального потребления растворенного кислорода в среде клетками ферментация проходила при микроаэробных условиях. Образцы забирали в ходе ферментации и анализировали с помощью HPLC в отношении концентраций аланина и глюкозы.
Было очевидно, что делеция промотора ydbH-ldhA и полученный повышенный уровень экспрессии ключевого фермента alaD в QZ32 оказали сильное влияние на образование аланина (фигура 11). Значительно повышенная максимальная волюметрическая скорость образования аланина, составляющая 2,00±0,07 г/(л ч) достигалась с Е. coli QZ32 по сравнению с Е. coli QZ16, который проявлял максимальную волюметрическую скорость образования аланина. составляющую приблизительно 0,74±0,02 г/(л ч). Е. coli QZ16 не был способен полностью потребить 80 г/л глюкозы в среде ферментации даже через длительный период времени ферментации, составляющий >50 ч. Волюметрическая производительность аланина (выход продукта за один проход в единицу времени), определенная как количество образованного продукта, деленное на объем реактора и на время, в отношении QZ16 через 50 ч составляла 0,58±0,04 г/(л ч). Е. coli QZ32 показал общую волюметрическую производительность аланина, составляющую 1,47±0,04 г/(л ч) при истощении глюкозы (фигура 12).
Испытание ферментации Е. coli QZ63 и Е. coli QZ64
Ферментацию проводили, как описано ранее. Е. coli QZ63, Ε. coli QZ64, Ε. coli QZ16 и Ε. coli QZ32 исследовали в двух параллелях.
Делеция гена ydbH в QZ64 не приводила к увеличению производительности аланина по сравнению с QZ16 (данные не показаны). Тем не менее, замещение 50 п.н. в промоторе ldhA дикого типа нуклеотидами TATTG, которые, как предполагали, комплементарны новому промотору alaD, привело к значительному увеличению образования аланина QZ63 по сравнению с QZ16 (фигура 11). Образование аланина QZ63 было сопоставимо с QZ32, который содержит делецию увеличенного промотора ydbH-ldhA длиной 529 п.н. QZ63 также продемонстрировал волюметрическую производительность аланина, составляющую 1,36±0,08 г/(л ч), сходную с QZ32, у которого данный показатель составлял 1,47±0,05 г/(л ч) (фигура 12).
Указанные данные показали, что только новый промотор, расположенной против хода транскрипции alaD, отвечает за увеличенную экспрессию alaD и, таким образом, лучшую производительность аланина.
Пример 7 Подтверждение эффекта SNP в гене ygaW на выход аланина
В геномной последовательности Е. coli QZ20 идентифицировали G15T в гене ygaW, который приводит к аминокислотной замене Q5H. Ранее определили, что ygaW, который также называется alaE, представляет собой экспортер аланина. Было показано, что избыточная экспрессия ygaW из плазмиды приводила к экскреции аланина (международная патентная публикация WO 2012/172822). Для исследования влияния SNP в гене ygaW на выход аланина вводили соответствующую мутацию в генетический фон Е. coli QZ32 ch усиленной экспрессией alaD по сравнению с QZ16. Дополнительные мутации вводили в тот же кодон для исследования того, характеризуются ли другие аминокислотные замены благоприятным эффектом на выход аланина.
Конструирование штамма Е. coli QZ33, QZ60, QZ61, QZ62
Конструирование штамма проводили, как описано ранее. Кассету ygaW-cat-sacB (3091 п.н.) амплифицировали с праймерами Rec2_1_F и Rec_2_1_R. Кассету ygaW-SNP- (130 п.н.) амплифицировали со способными к самоотжигу праймерам Rec2_2_F и Rec2_2_R. Контрольные ПЦР проводили с геном-специфическими праймерами Rec2_seq_F и Rec2_seq_R. Образованный с делецией промотора ydbH-ldhA и SNP Q5H ygaW называли QZ33.
Аналогично альтернативные аминокислотные замены вводили в Е. coli QZ32. Двухцепочечную ДНК (gBlocks), содержащую представляющей интерес мутацию, заказывали в IDT Technologies и использовали для замещения маркерной кассеты cat-sacB во время рекомбинации Red/ET. Ε. coli QZ60 содержит мутацию YgaW Q5N, Ε. coli QZ61 содержит мутацию YgaW Q5R, и Ε. coli QZ62 содержит мутацию YgaW Q5Y.
Испытание ферментации Ε. coli QZ32, QZ60, QZ61 и QZ62, QZ33
Штамм QZ33 (мутант делеции Q5H ygaW, ydhB-ldha) исследовали в отношении его производительности во время ферментации по сравнению с Е. coli QZ32. Периодическую ферментацию проводили, как описано ранее.
Мутация Q5H ygaW приводила к дополнительному увеличению образования аланина Е. coli QZ33 по сравнению с Е. coli QZ32 (фигура 13). Дополнительная усиленная волюметрическая производительность аланина, составляющая 1,82±0,03 г/(л ч) достигалась Е. coli QZ33 по сравнению с 1,47±0,05 г/(л ч) для Е. coli QZ32 (фигура 14).
Штаммы с альтернативными мутациями Q5 исследовали при идентичных условиях во время периодической ферментации. Все три альтернативных мутации показали повышенную максимальную скорость образования аланина по сравнению с Е. coli QZ32 с YgaW дикого типа (фигура 15). Е. coli QZ60 (YgaW Q5N) показали волюметрическую производительность аланина, составляющую 1,56±0,004 г/(л ч), 1,68±0,02 г/(л ч) для Е. coli QZ61 (YgaW Q5R) и 1,61±0,04 г/(л ч) для QZ62 (YgaW Q5Y) по сравнению с 1,47±0,04 г/(л ч) для QZ32 (фигура 14). Соответственно, замена аргинина характеризовалась самым сильным благоприятным эффектом, за ней следовала замена тирозина и замена аспарагина. Тем не менее, Е. coli QZ33 с мутацией Q5H ygaW, обнаруженной во время адаптивной эволюции, превзошел каждый из рационально сконструированных мутантов с волюметрической производительностью аланина, составляющей 1,82±0,03 г/(л ч).
Анализ ОТ-кПЦР уровней транскрипции гена ygaW
Точный механизм, с помощью которого сигнал SNP в N-концевой области YgaW обеспечивает усиленную активность экспортера аланина, не известен. Авторы настоящего изобретения исследовали уровни генной экспрессии ygaW в образцах РНК QZ16 и QZ20 с помощью ОТ-кПЦР, как описано ранее с ген-специфическими праймерами ygaW_RT_F и ygaW_RT_R (таблица 1). Данные в отношении генной экспрессии нормировали к rrsA в качестве эталонного гена и рассчитывали в отношении к уровням генной экспрессии в Е. coli QZ16 через 8 ч в качестве калибровочного стандарта.
Не наблюдали значительной положительной или отрицательной регуляции экспрессии гена ygaW для образцов штамма из 8 ч и 11 ч ферментации (фигура 16). Указанные результаты подтверждают, что эффект мутации Q5H ygaW не связан с повышенными уровнями экспрессии ygaW, но должен напрямую влиять на активность или стабильность YgaW.
Пример 8 Подтверждение эффекта SNP в гене zipA на выход аланина
Для определения роли, которую играет SNP zipA в производительности аланина, SNP zipA вводили в штамм Е. coli QZ33 (делеция промотора ydbH-ldhA, Q5H ygaW).
Конструирование штамма
Поскольку zipA является важным геном, кассету интеграции zipA cat-sacB разрабатывали так, чтобы не прерывать zipA, а интегрировать ниже него по ходу транскрипции. Кассету амплифицировали из вектора pQZ11 (Genescript) с праймерами Rec4B_1_F7R (таблица 1). Кассету SNP zipA (197 п.н.) амплифицировали из геномной ДНК штамма QZ20 с праймерами Rec4B_2_F/R. Red/ET проводили, как описано ранее. Клоны исследовали с помощью ПЦР в геле (способ молекулярных колоний) с праймерами секвенирования Rec4_seq_F/R. SNP zipA вводили в Ε. coli QZ33 с делецией промотора ldhA и ygaW SNP. Образованный штамм обозначали как QZ41.
Испытание ферментации QZ33 и QZ41
Штамм QZ41 (мутант SNP zipA, Q5H ygaW, Δldha) исследовали в отношении его производительности во время ферментации, как описано ранее. Образование аланина подвергали мониторингу по сравнению со штаммом QZ33.
SNP zipA приводил к дополнительному увеличению в образовании аланина по сравнению с штаммом - предшественником, QZ33 (фигура 17). Волюметрическая производительность аланина в отношении QZ41 составляла 2,06±0,06 г/(л ч) по сравнению с 1,82±0,03 г/(л ч) (фигура 18).
Пример 9 Подтверждение эффекта SNP в гене lpd на выход аланина
Для исследования влияния SNP lpd на производительность аланина его вводили в E. coli WZ33 ((деления ydbH-ldhA, Q5H ygaW) для создания E. coli QZ52 и в E. coli QZ41 (делеция ydbH-ldhA, Q5H ygaW, SNP zipA) для создания штамма E. coli QZ53.
Конструирование штамма
Кассету интеграции lpd cat-sacB (3087 п.н.) разрабатывали так, чтобы она не прерывала lpd, но интегрировалась выше него против хода транскрипции. Кассету амплифицировали из вектора pQZ11 (Genescript) с праймерами Rec3B_1_F7R (таблица 1) и использовали, чтобы интегрировать в штамм QZ20, который содержит SNP lpd. Кассету lpd_SNP-cat-sacB (3527 п.н.) амплифицировали из геномной ДНК штамма QZ20 с интегрированной кассетой cat-sacB с праймерами Rec3B_2_F/R и использовали для интеграции в E. coli QZ33 и E. coli QZ41, соответственно. Кассету замещения cat-sacB амплифицировали с праймерами Rec3B_F7R из генома QZ20 и использовали для удаления маркерной кассеты cat-sacB в QZ33 и QZ41. Red/ET проводили, как описано ранее. Клоны исследовали с помощью ПНР в геле (способ молекулярных колоний) с праймерами секвенирования Rec3_seq_F и Rec_3B_FR.
Испытание ферментации QZ33 по сравнению с QZ52
Штамм QZ52 (промотор ΔydbH-ldha, Q5H ygaW, SNP lpd) исследовали в отношении его производительности во время ферментации, как описано ранее, с 10 г/л глюкозы в качестве источника углерода. Образование аланина подвергали мониторингу по сравнению со штаммом QZ33.
SNP lpd оказывал значительный положительный эффект на образование аланина по сравнению с QZ33 (фигура 19). QZ33 не был способен полностью потребить 100 г/л глюкозы в среде ферментации в пределах времени мониторинга, составляющего 52 ч. QZ52 полностью потреблял доступную глюкозу в пределах 41 ч и достигал волюметрической производительности аланина, составляющей 1,79±0,160 г/(л ч) по сравнению с QZ33 с 1,45±0,007 г/(л ч) за одинаковый промежуток времени (фигура 20).
Испытание ферментации QZ41 по сравнению с QZ53
Штамм QZ53 (промотор ΔydbH-ldha, Q5H ygaW, SNP zipA, SNP lpd), в котором SNP lpd вводили в Ε. coli QZ41, исследовали в отношении его производительности во время ферментации, как описано ранее. Образование аланина подвергали мониторингу по сравнению со штаммом QZ41.
SNP lpd в QZ53 также показал свой положительный эффект на образование аланина по сравнению с QZ41 (фигура 22). Волюметрическая производительность аланина QZ53 составляла 2,21±0,004 г/(л ч) по сравнению с QZ41 с 2,06±0,06 г/(л ч) (фигура 23).
Общее улучшение волюметрических производительностей аланина в результате делеции промотора ydbH-ldhA, SNP Q5H ygaW, SNP zipA и SNP lpd представлено на фигуре 21.
Избыточная экспрессия гена lpd
Дополнительную копию lpd под контролем его нативного промотора вводили в плазмиду pACYC184. pACYC184-Lpd (р15 ori, ChlR, ~15 копий на клетку) конструировали посредством коммерческой технологии клонирования InFusion (Clontech, Маунтин-Вью, Калифорния, США). Первый вектор pACYC184 (р15 ori, chlR, tetR) получали от NEB (Ипсвич, Массачусетс, США) и линеаризировали с рестрикционными эндонуклеазами HindIII и SalI, также от NEB. Указанная обработка удаляла большинство генов устойчивости к тетрациклину. Отдельно ORF lpd амплифицировали с помощью ПЦР из ДНК Е. coli W дикого типа с помощью полимеразы Phusion (Thermo Scientific, Уолтем, Массачусетс, США) со следующими праймерами (lpd-pACYC_F SEQ ID NO: 114 и lpd-pACYC_R SEQ ID NO: 115).
Праймеры содержали дополнительные 15 п.н. липкие концы, гомологичные концам линеаризованного вектора для облегчения беспрепятственного клонирования. Затем проводили реакцию InFusion согласно протоколу производителя как с очищенными каркасом линеаризованного вектора, так и со вставкой lpd. Полученные продукты InFusion заем использовали для трансформации QZ33 (делеция промотора ydbH-ldhA, Q5H ygaW) посредством электропорации и селекции на LB планшетах с хлорамфениколом. Положительные клоны идентифицировали с помощью ПЦР, подтверждали с помощью секвенирования ДНК и использовали в ферментациях для исследований избыточной экспрессии.
Сравнение ферментации между QZ33/pACYC184 и QZ33/pACYC184-Lpd
Производительность аланина штамма, содержащего экспрессионный вектор lpd (QZ33/pACYC184-lpd) сравнивали со штаммом, содержащим пустой контрольный вектор (QZ33/pACYC184). Прекультуры выращивали во встряхиваемых колбах со средой LB, с 20% объемом заполнения при 37°С и 200 об/мин в течение ночи. Ферментацию проводили в системе параллельных 1,5 л биореакторов DASGIP с 8% глюкозы в среде NBS. Другие условия были такие же, как и ранее.
Через 33 ч QZ33/pACYC184-lpd произвел 58,4 г/л аланина по сравнению с 57,1 г/л для QZ33/pACYC184 (фигура 24).
По сравнению с QZ33/pACYC184 выход за один проход в единицу времени (производительность) QZ33/pACYC184-lpd также увеличивался от 1,63 до 1,77 г/ч/л (фигура 25).