Результат интеллектуальной деятельности: САЙТ-СПЕЦИФИЧЕСКАЯ КОНЪЮГАЦИЯ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО ПОСРЕДСТВОМ ГЛИКОИНЖЕНЕРИИ
Вид РИД
Изобретение
РОДСТВЕННЫЕ ЗАЯВКИ
По настоящей заявке испрашивается приоритет предварительной патентной заявки США 61/776724, озаглавленной «Site-Specific Antibody Drug Conjugation Through Glycoengineering», поданной 11 марта 2013 г.; предварительной патентной заявки США 61/776710, озаглавленной «Hyperglycosylated Binding Polypeptides», поданной 11 марта 2013 г., и предварительной патентной заявки США 61/776715, озаглавленной «Fc Containing Polypeptides with Измененный Glycosylation and Reduced Effector Function», поданной 11 марта 2013 г. Полное содержание вышеупомянутых заявок, таким образом, приведено в настоящем документе путем ссылки.
УРОВЕНЬ ТЕХНИКИ
Лечение злокачественных опухолей все еще является серьезной проблемой для человечества. Хотя современные терапевтические средства, включая хирургию, радиоактивное излучение и химиотерапию, спасли жизнь многих пациентов, существует огромная потребность в более эффективных терапевтических средствах, особенно специфических для мишеней терапевтических средствах в более высокой эффективностью и более широким терапевтическим окном. В одном из видов этого специфического для мишеней лечения используют конъюгаты антитело-лекарственное средство (ADC), в которых специфическое для антигена антитело нацеливает неспецифическое химиотерапевтическое средство на участок опухоли. Показано, что эти молекулы обладают эффективностью и хорошими профилями безопасности в клинических условиях. Однако, разработка таких лекарственных средств может являться сложной, поскольку многие факторы, включая стабильность собственно антитела и связей, могут оказывать значительное влияние на специфичность для опухолей, таким образом, уменьшая эффективность. При высоком неспецифическом связывании и низкой стабильности в кровотоке, ADC могут выводиться через нормальные ткани до достижения опухоли. Более того, ADC с значительными субпопуляциями с высокой нагрузкой лекарственного средства могут образовывать агрегаты, которые могут быть уничтожены макрофагами, что приводит к более короткому времени полужизни. Таким образом, существует увеличенная необходимость в контроле и улучшении критического процесса, так же как в предотвращении осложнений, таких как агрегация продукта и неспецифическая токсичность из-за IgG.
Хотя ADC, полученные в соответствии с современными способами, являются эффективными, разработка таких лекарственных средств может являться сложной, поскольку гетерогенные смеси часто являются следствием использованных химических реакций для конъюгации. Например, конъюгация лекарственного средства с остатками лизина антитела осложняется тем фактом, что существует множество остатков лизина (~30) в антителе, доступных для конъюгации. Поскольку оптимальное значение соотношения лекарственного средства к антителу (DAR) намного ниже (например, приблизительно 4:1), лизиновая конъюгация часто образует очень гетерогенный профиль. Более того, многие остатки лизина локализованы в критических антигенсвязывающих участках области CDR, и конъюгация с лекарственным средством может приводить к снижению аффинности антитела. С другой стороны, в то время как опосредованная тиолом конъюгация в основном нацелена на восемь остатков цистеина, вовлеченных в дисульфидные связи шарнира, все еще трудно предсказывать и идентифицировать, какие четыре из восьми остатков цистеина являются систематически конъюгированными среди различных препаратов. Более недавно, генетическая инженерия свободных остатков цистеина позволила сайт-специфичкескую конъюгацию с помощью химических реакция на основе тиола, но такие связи часто обладают высоко изменчивой стабильностью, где лекарственное средство-линкер подвергается реакциям обмена с альбумином и другими содержащими тиол молекулами сыворотки. Таким образом, способ сайт-специфической конъюгации, образующий ADC с определенным участком конъюгации и стабильной связью, можно широко использовать для гарантии конъюгации лекарственного средства, минимизируя в то же время неблагоприятные эффекты на структуру или функцию антитела.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее описание относится к связывающим полипептидам (например, антителам) и их конъюгатам с эффекторными группами (например, конъюгатам с лекарственными средствами). В конкретных вариантах осуществления конъюгаты содержат сайт-специфически сконструированную связь лекарственное средство-гликан на природных или сконструированных гликанах связывающего полипептида. Настоящее описание относится также к нуклеиновым кислотам, кодирующим антигенсвязывающие полипептиды, рекомбинантным экспрессирующим векторам и клеткам-хозяевам для получения таких антигенсвязывающих полипептидов. Представлены также способы использования антигенсвязывающих полипептидов, описанных в настоящем документе, для лечения заболевания.
В конкретных вариантах осуществления, связывающий полипептид по изобретению можно получать посредством присоединения эффекторной группы (например, группы лекарственного средства) через стабильные (например, оксимные) связи.
Этот способ обеспечивает высоко определенные продукты с увеличенной стабильностью in vivo и сниженной агрегацией. В других вариантах осуществления, и для обеспечения дополнительной избирательности для участка и гомогенности, конъюгат с эффекторной группой (например, конъюгат с лекарственным средством) можно получать посредством присоединения к концевому остатку сахара (например, концевому остатку сиаловой кислоты или галактозы) гликана IgG. Концевой остаток сахара можно легко переводить в реакционноспособную альдегидную форму посредством умеренного окисления (например, с помощью периодата натрия). Окисленный остаток сахара можно затем конъюгировать с реакционноспособными по отношению к альдегиду аминоокси-лекарственными средствами-линкерами для получения стабильных и гомогенных популяций конъюгатов белок-лекарственное средство (например, ADC).
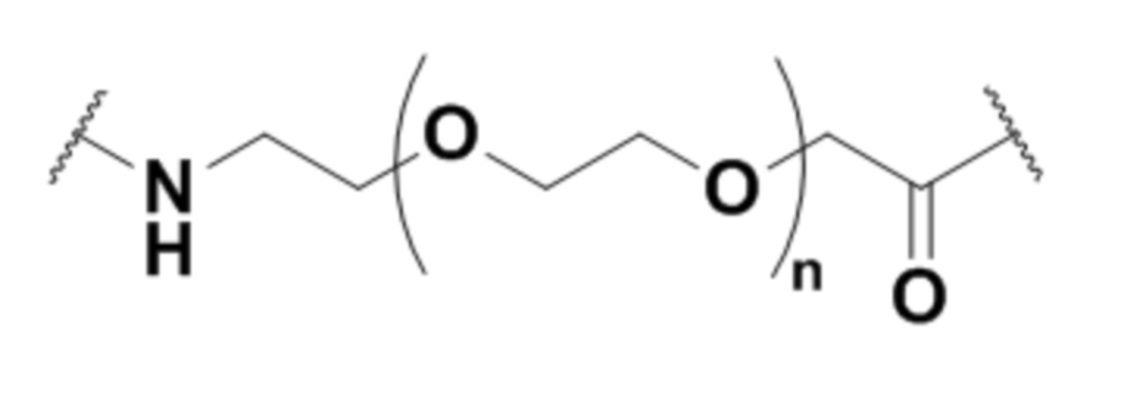
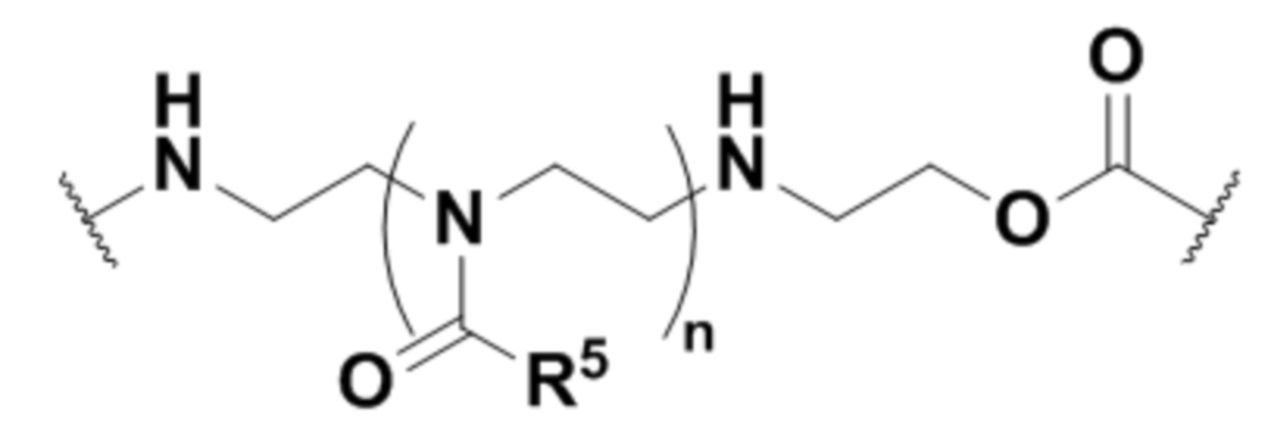
Соответственно, в одном аспекте изобретение относится к связывающему полипептиду, содержащему по меньшей мере один модифицированный гликан, содержащему по меньшей мере одну группу формулы (IV):
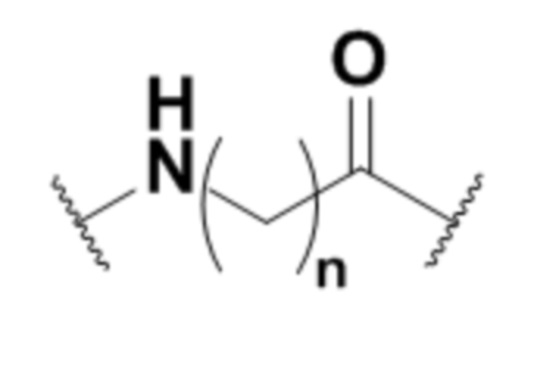
-Gal-Sia-C(H)=N-Q-CON-X
Формула (IV),
где:
A) Q представляет собой NH или O;
B) CON представляет собой соединительную группу; и
C) X представляет собой эффекторную группу (например, группу лекарственного средства или нацеливающую группу);
D) Gal представляет собой компонент, происходящий из галактозы;
E) Sia представляет собой компонент, происходящий из сиаловой кислоты; и
где Sia присутствует или отсутствует.
В одном варианте осуществления модифицированный гликан представляет собой двухантенный гликан. В другом варианте осуществления двухантенный гликан является фукозилированным или нефукозилированным. В другом варианте осуществления модифицированный гликан содержит по меньшей мере две группы формулы (IV), где Sia присутствует только на одной из двух групп. В другом варианте осуществления модифицированный гликан содержит по меньшей мере две группы формулы (IV), где Sia присутствует на обеих из двух групп. В другом варианте осуществления, модифицированный гликан является N-связанным со связывающим полипептидом.
В другом варианте осуществления связывающий полипептид содержит домен Fc. В другом варианте осуществления модифицированный гликан является N-связанным со связывающим полипептидом через остаток аспарагина в положении аминокислоты 297 домена Fc, в соответствии с нумерацией EU. В другом варианте осуществления модифицированный гликан является N-связанным со связывающим полипептидом через остаток аспарагина в положении аминокислоты 298 домена Fc, в соответствии с нумерацией EU. В другом варианте осуществления домен Fc является человеческим.
В другом варианте осуществления связывающий полипептид содержит домен CH1. В одном варианте осуществления модифицированный гликан является N-связанным со связывающим полипептидом через остаток аспарагина в положении аминокислоты 114 домена CH1, в соответствии с нумерацией Kabat. В одном варианте осуществления связывающий полипептид представляет собой антитело или иммуноадгезин.
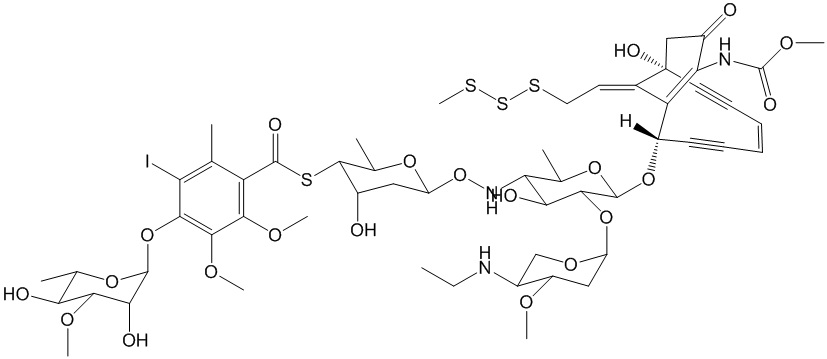
В одном варианте осуществления эффекторная группа представляет собой цитотоксин. В другом варианте осуществления цитотоксин выбран из группы, состоящей из цитотоксинов, пречисленных в таблице 1. В другом варианте осуществления эффекторная группа представляет собой средство для детекции. В конкретных вариантах осуществления эффекторная группа представляет собой нацеливающую группу. В одном варианте осуществления нацеливающая группа представляет собой углевод или гликопептид. В другом варианте осуществления нацеливающая группа представляет собой гликан.
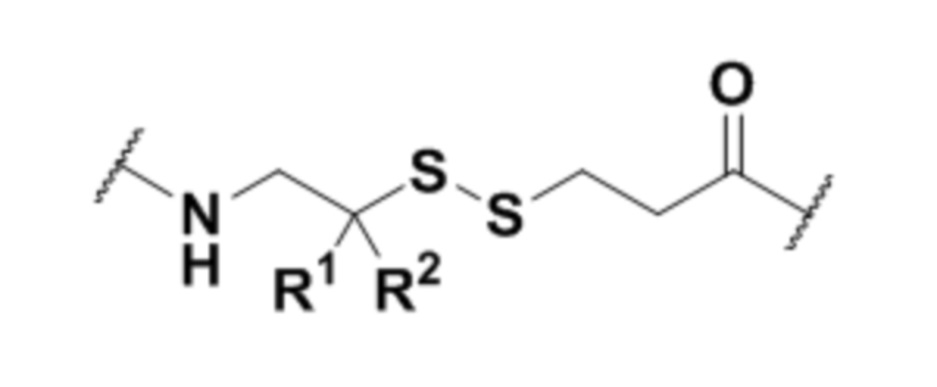
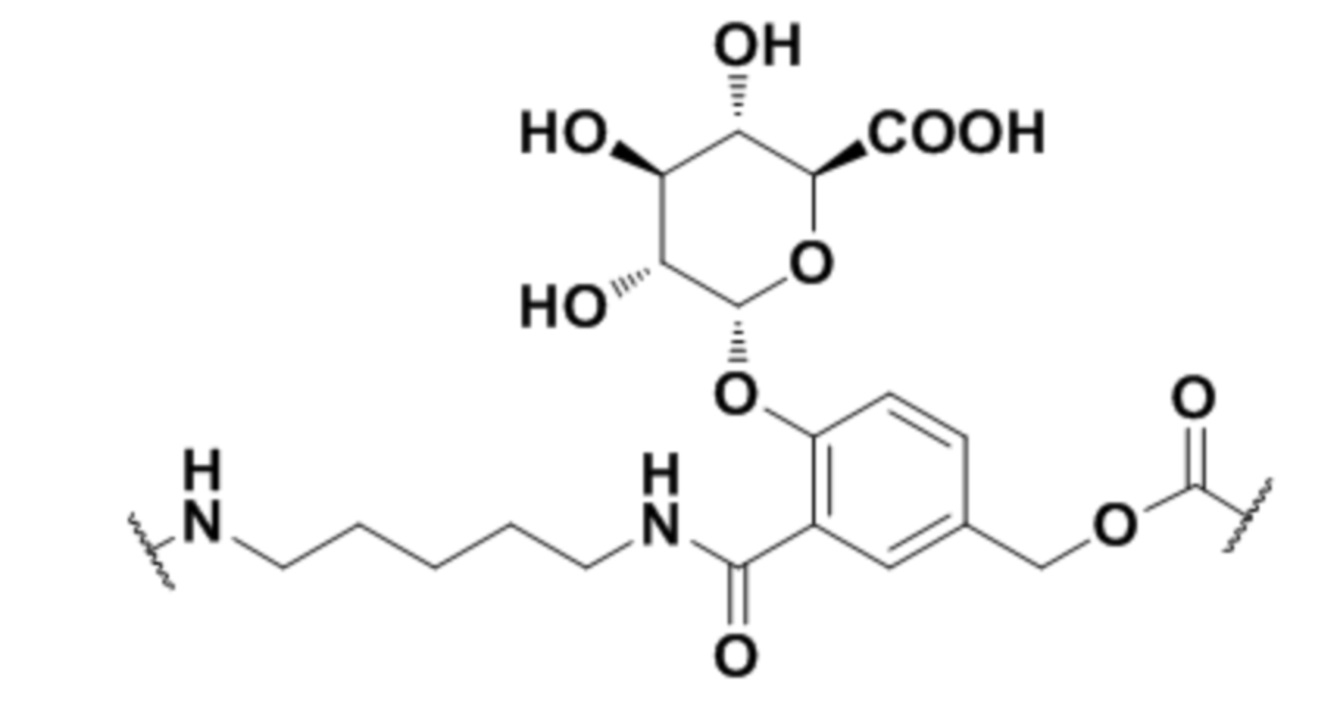
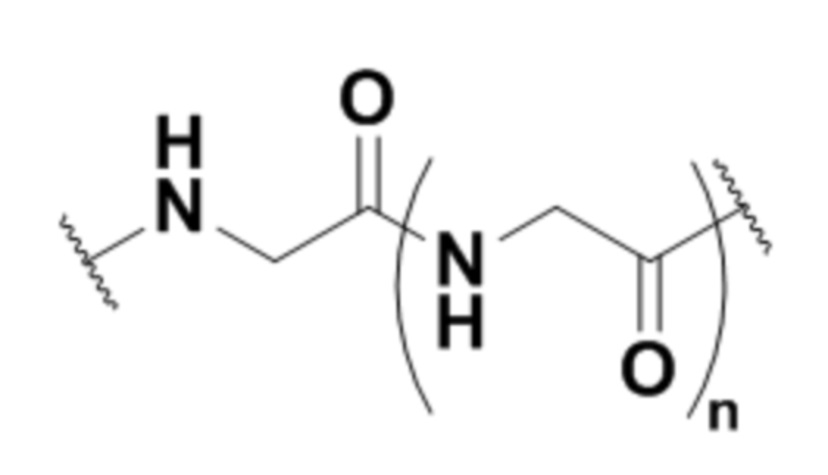
В другом варианте осуществления соединительная группа содержит pH-чувствительный линкер, дисульфидный линкер, фермент- чувствительный линкер или другую отщепляемую линкерную группу. В другом варианте осуществления соединительная группа содержит линкерную группу, выбранную из группы линкерных групп, показанных в таблице 2 или 14.
В других аспектах, изобретение относится к композиции, содержащей связывающий полипептид по изобретению и фармацевтически приемлемый носитель или наполнитель. В одном варианте осуществления соотношение терапевтической или диагностической эффекторной группы к связывающему полипептиду составляет менее 4. В другом варианте осуществления соотношение терапевтической или диагностической эффекторной группы к связывающему полипептиду составляет приблизительно 2.
В других аспектах, изобретение относится к способу лечения нуждающегося в этом пациента, включающему введение эффективного количества композиции по изобретению.
В других аспектах, изобретение относится к выделенному полинуклеотиду, кодирующему связывающий полипептид по изобретению. В других аспектах изобретение относится к вектору, содержащему полинуклеотид. В других аспектах, изобретение относится к клетке-хозяину, содержащей полинуклеотид или вектор.
В других аспектах изобретение относится к способу получения связывающего полипептида по изобретению, где способ включает реакцию эффекторной группы формулы (I):
NH2-Q-CON-X
Формула (I),
где:
A) Q представляет собой NH или O;
B) CON представляет собой соединительную группу; и
C) X представляет собой эффекторную группу,
с измененным связывающим полипептидом, содержащим окисленный гликан.
В одном варианте осуществления измененный связывающий полипептид содержит окисленный гликан, полученный посредством реакции связывающего полипептида, содержащего гликан, с умеренно окисляющим средством. В конкретных вариантах осуществления умеренно окисляющее средство представляет собой периодат натрия.
В конкретных вариантах осуществления используют менее, чем 1 мМ периодат натрия. В одном варианте осуществления, окисляющее средство представляет собой оксидазу галактозы. В другом варианте осуществления связывающий полипептид, содержащий гликан, содержит один или два концевых остатка сиаловой кислоты. В другом варианте осуществления концевые остатки сиаловой кислоты вводят посредством обработки связывающего полипептида с помощью сиалилтрансферазы или комбинации сиалилтрансферазы и галактозилтрансферазы.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
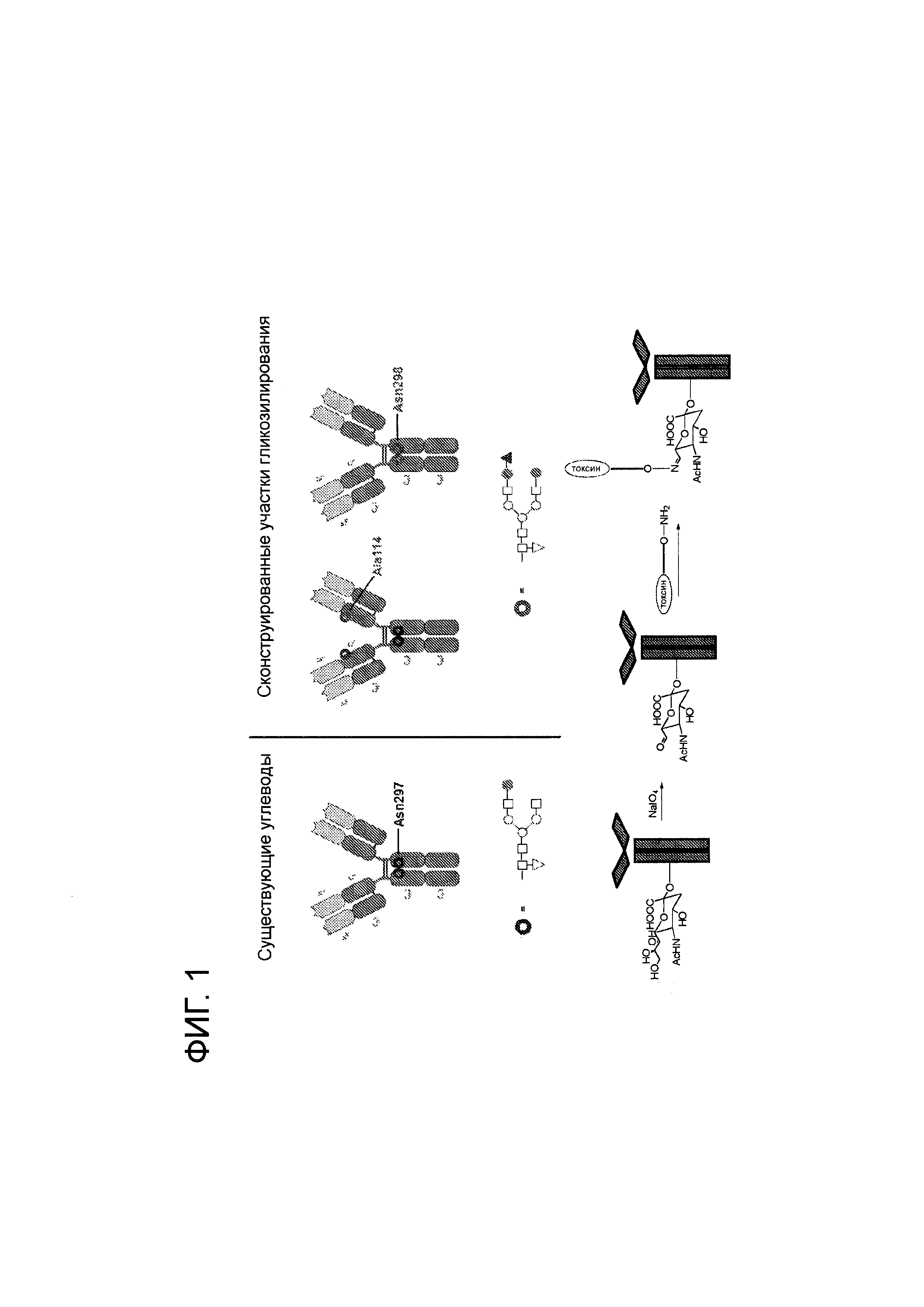
Фигура 1 представляет собой схематическую иллюстрацию синтеза конъюгата антитела с лекарственным средством, где группа токсина связана с окисленным остатком сиаловой кислоты гликана антитела с использованием оксимной связи.
Фигура 2 представляет собой окрашенный Кумасси синим гель, показывающий экспрессию и очистку мутантов по гликозилированию.
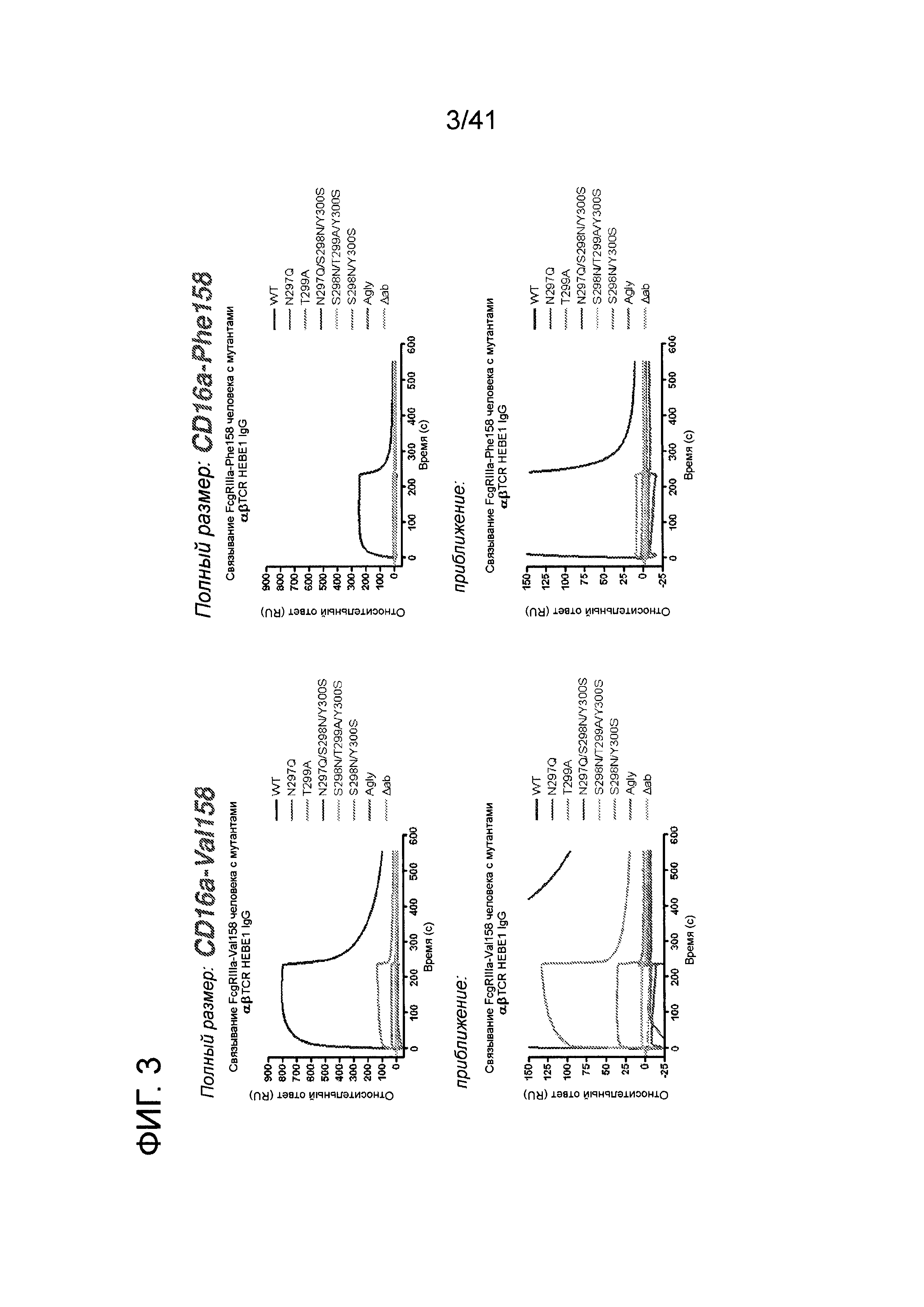
На фигуре 3 изображены результаты экспериментов поверхностного плазмонного резонанса, использованных для оценки связывания мутантов антитела αβTCR HEBE1 IgG с рекомбинантным FcγRIIIa (V158 и F158) человека.
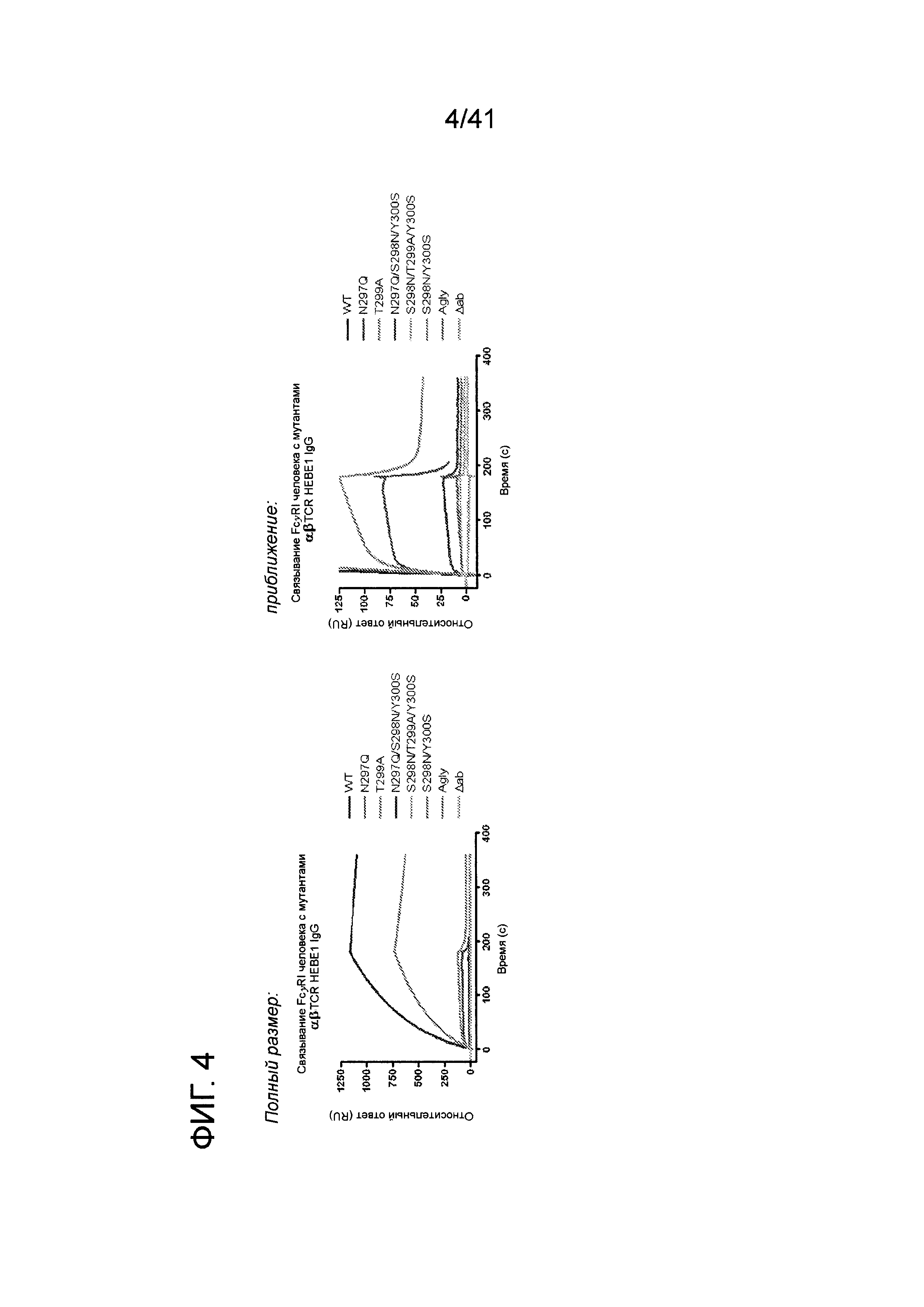
На фигуре 4 изображены результаты экспериментов поверхностного плазмонного резонанса, использованных для оценки связывания мутантов антитела αβTCR HEBE1 IgG с рекомбинантным FcγRI человека.
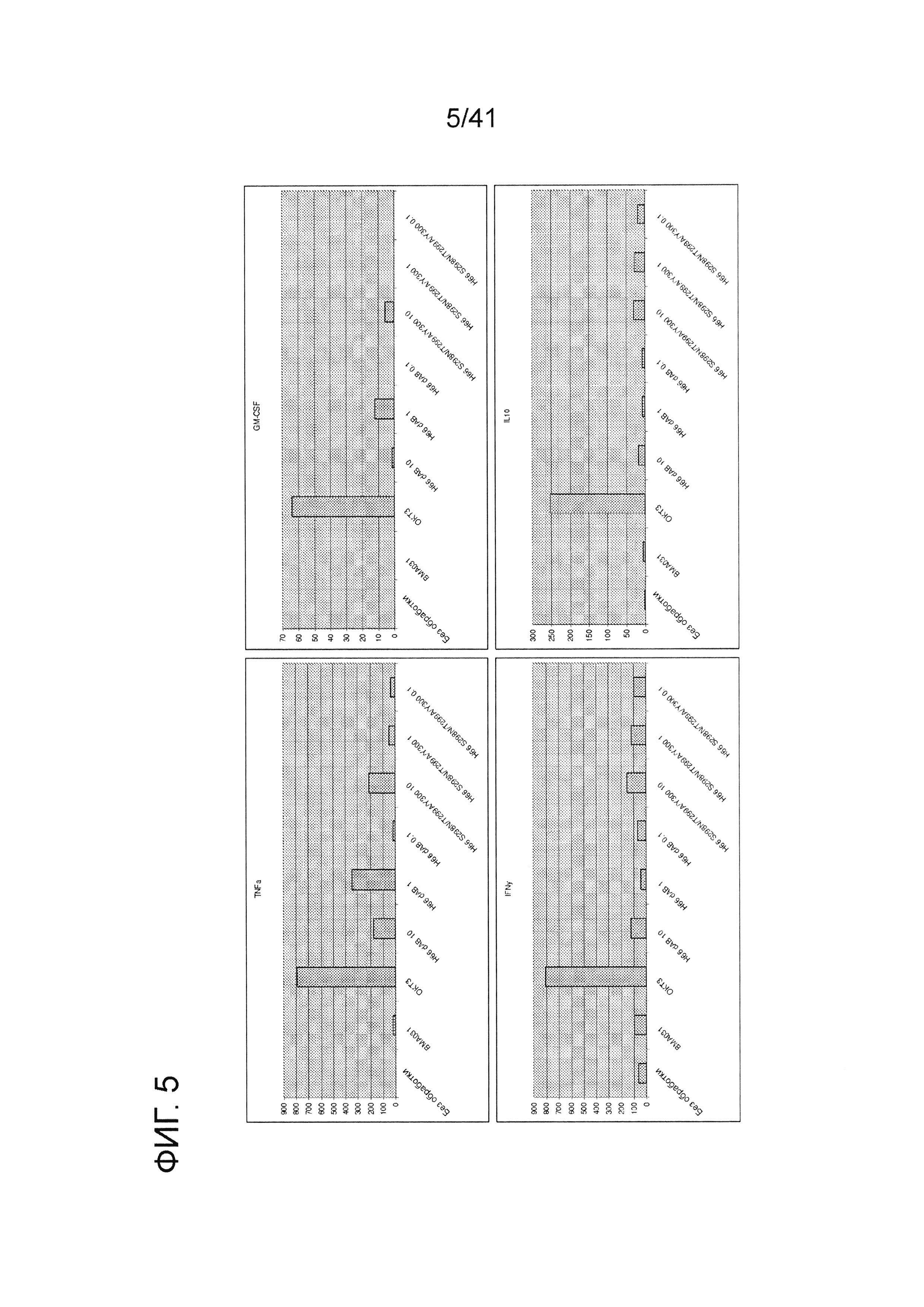
На фигуре 5 изображен профиль высвобождения цитокинов из PBMC для TNFa, GM-CSF, IFNy и IL10 в присутствии мутантных антител анти-αβTCR (сутки 2).
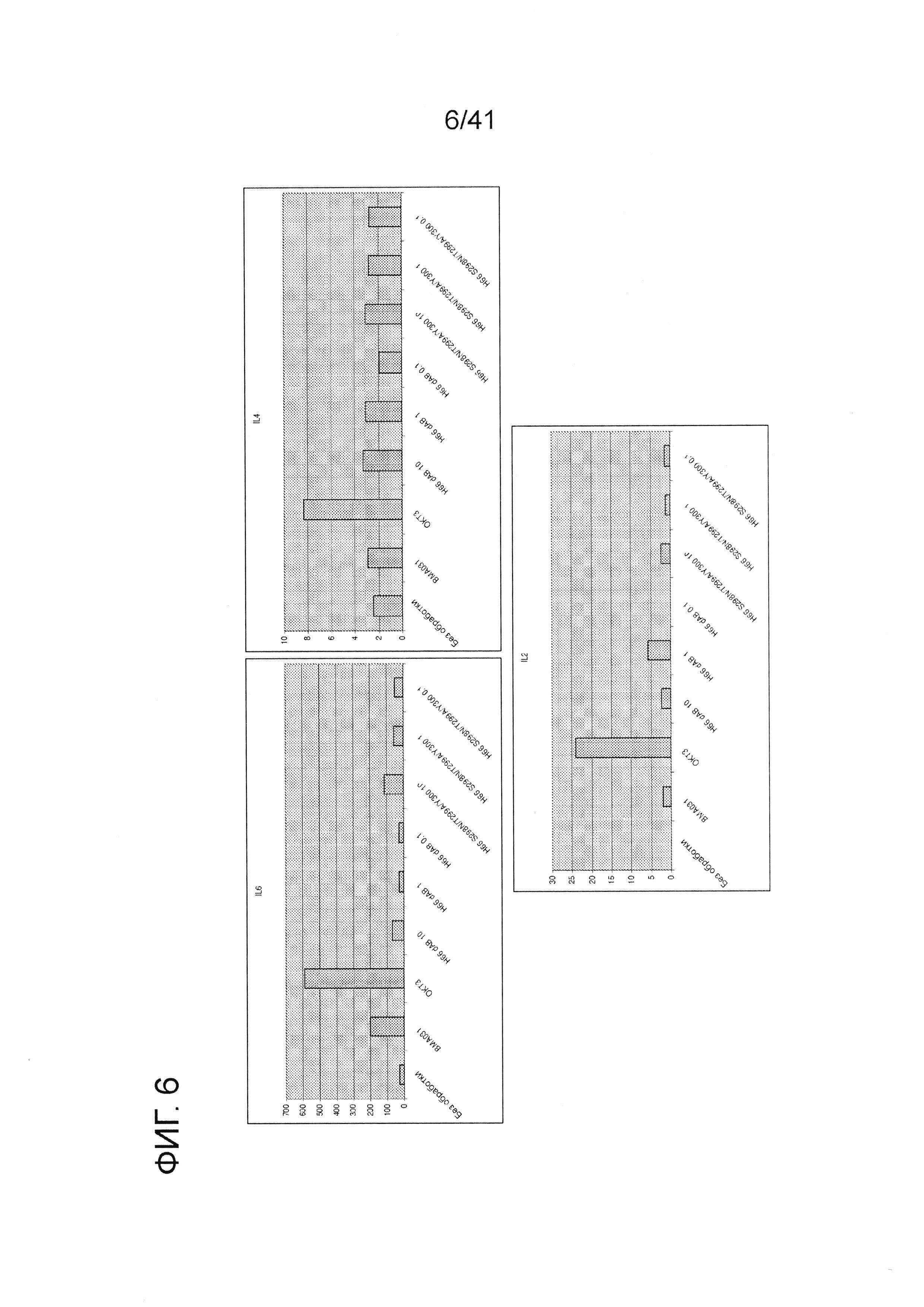
На фигуре 6 изображен профиль высвобождения цитокинов из PBMC для IL6, IL4 и IL2 в присутствии мутантных антител анти-αβTCR (сутки 2).
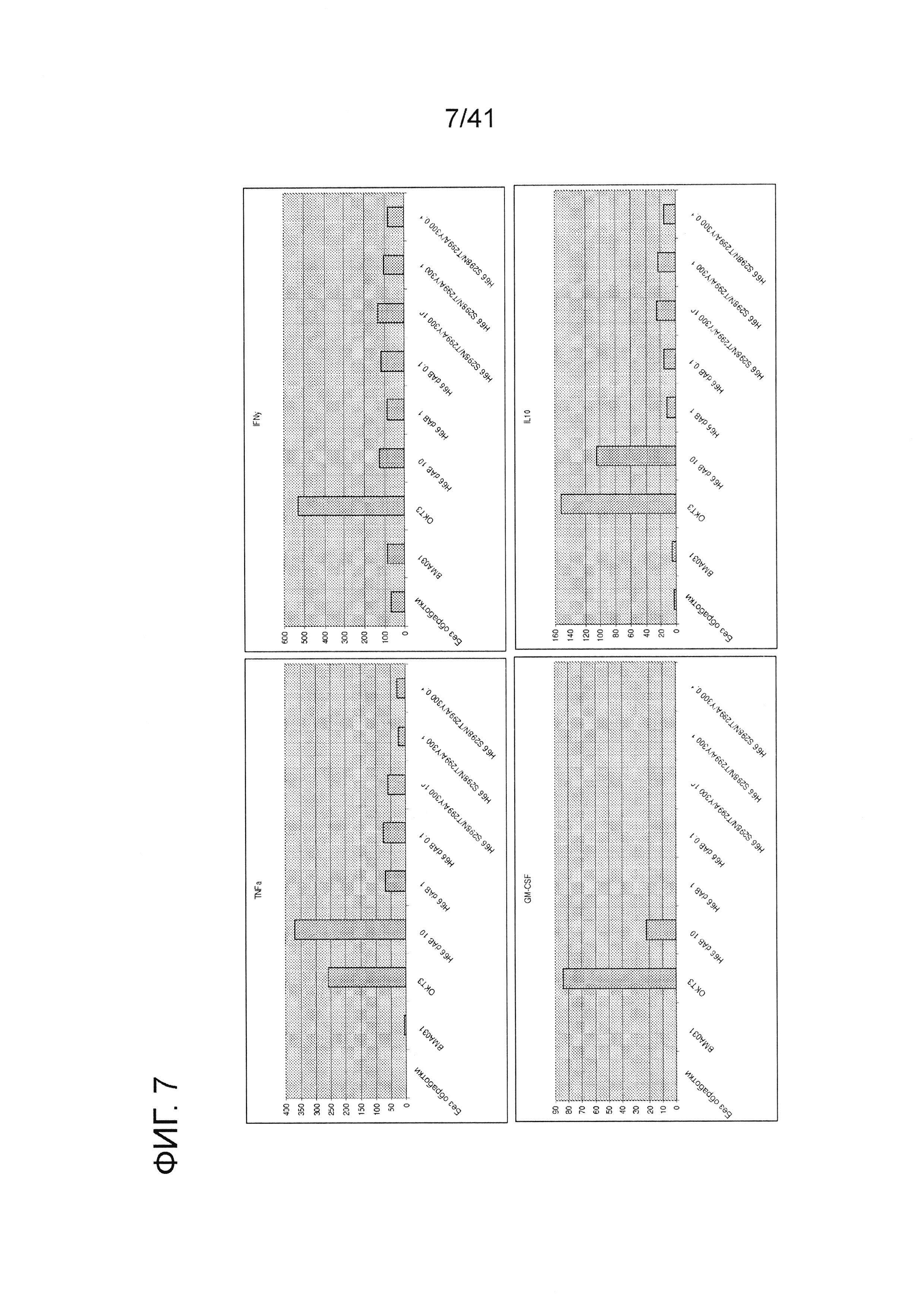
На фигуре 7 изображен профиль высвобождения цитокинов из PBMC для TNFa, GM-CSF, IFNy и IL10 в присутствии мутантных антител анти-αβTCR (сутки 4).
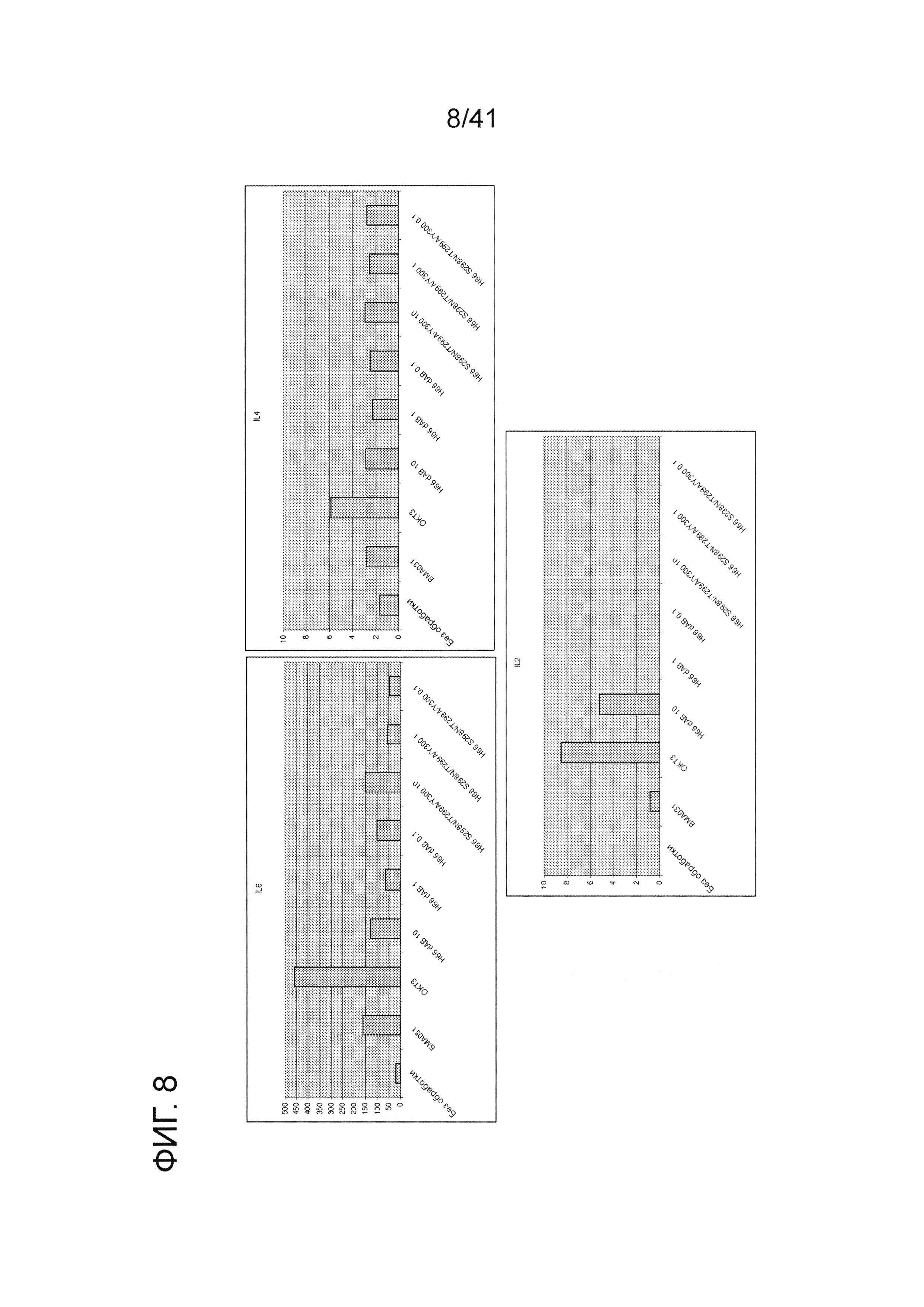
На фигуре 8 изображен профиль высвобождения цитокинов из PBMC для IL6, IL4 и IL2 в присутствии мутантных антител анти-αβTCR (сутки 4).
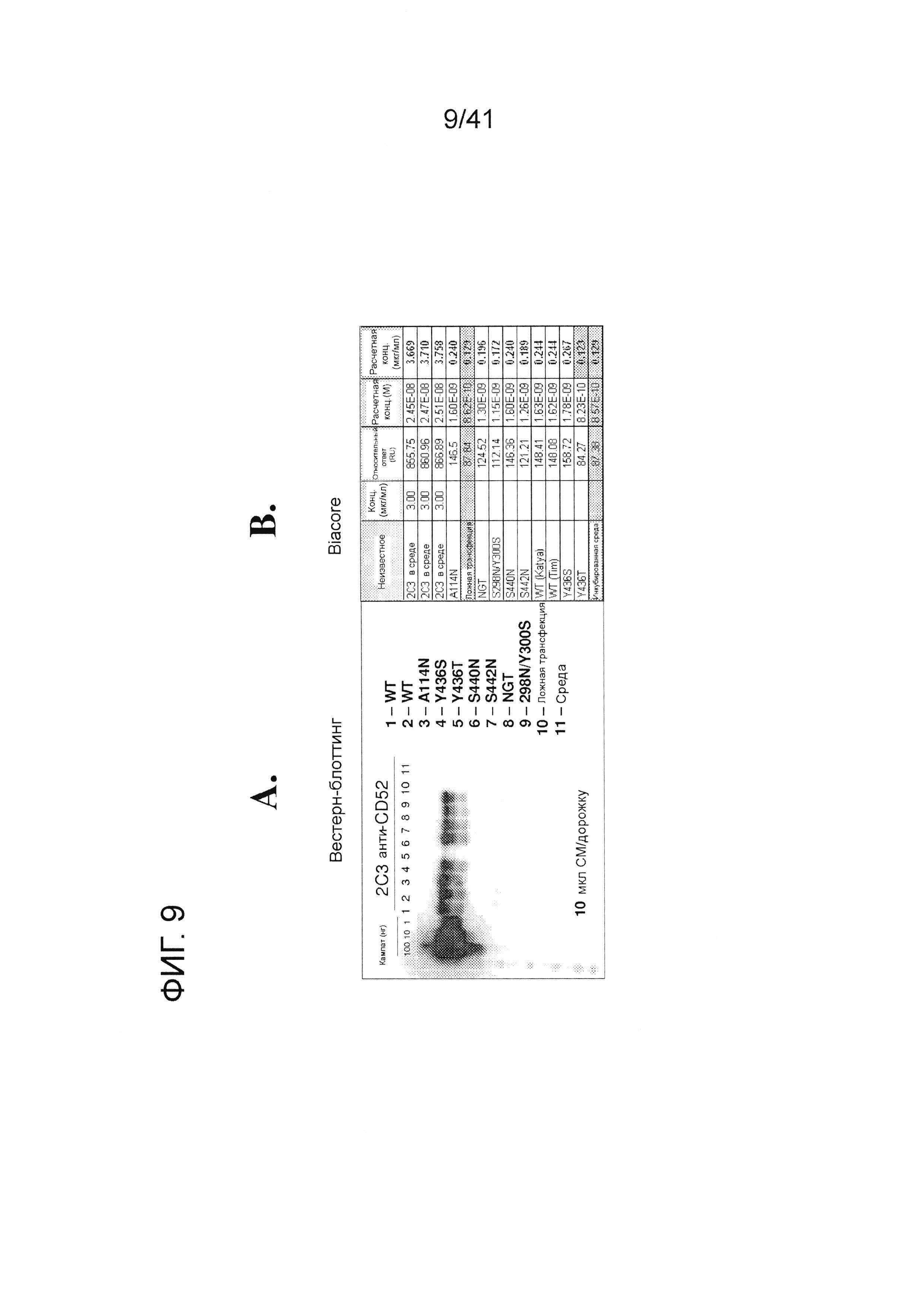
На фигуре 9 изображены результаты экспериментов, исследующих уровень экспрессии мутантов 2C3 посредством Вестерн-блоттинга и поверхностного плазмонного резонанса.
На фигуре 10 изображены результаты экспериментов, исследующих гликозилирование мутантов 2C3 до и после обработки PNGase F.
На фигуре 11 изображены результаты экспериментов в SDS-PAGE, исследующих участки гликозилирования на мутантах 2C3, выделенных из культуры клеток.
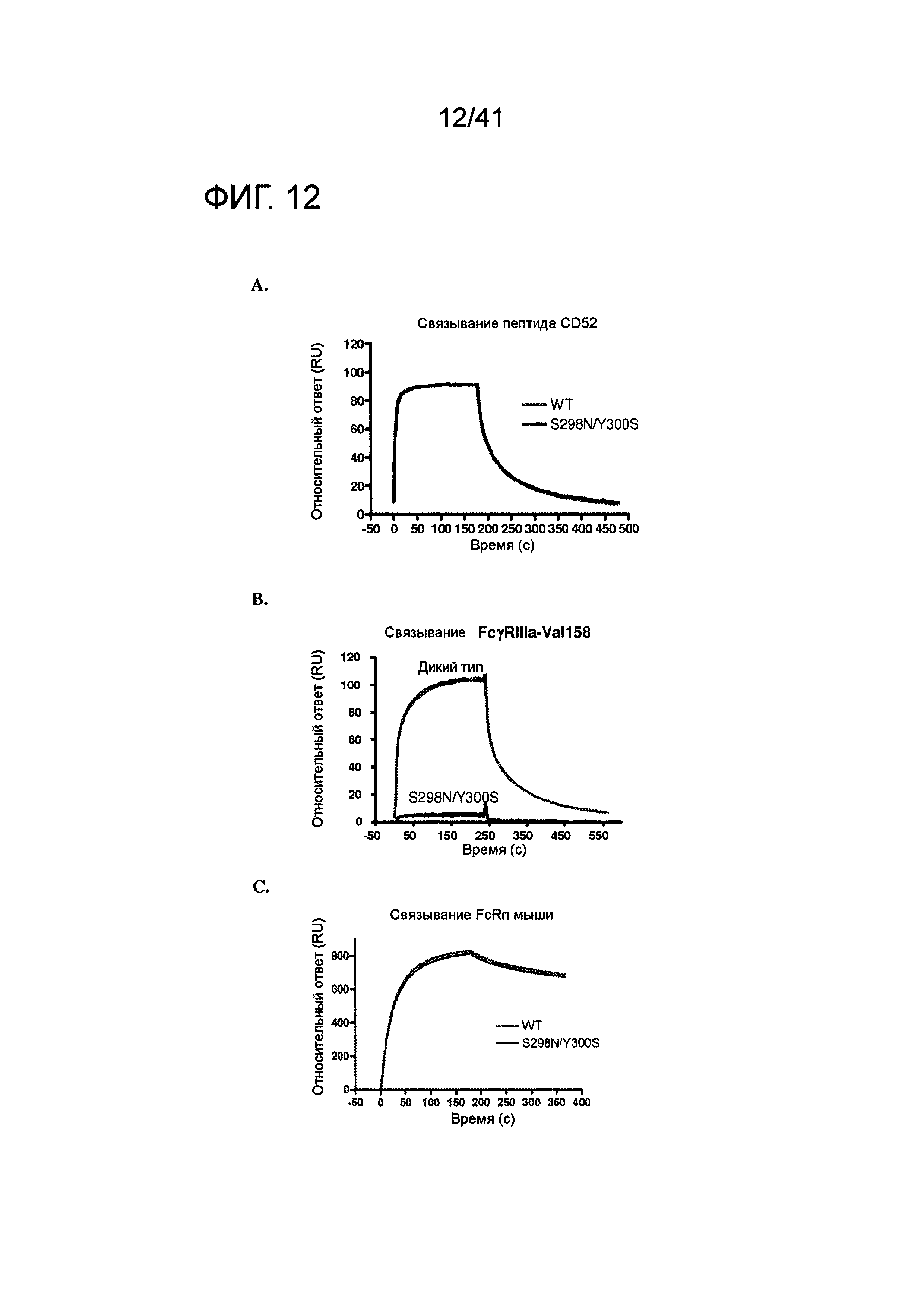
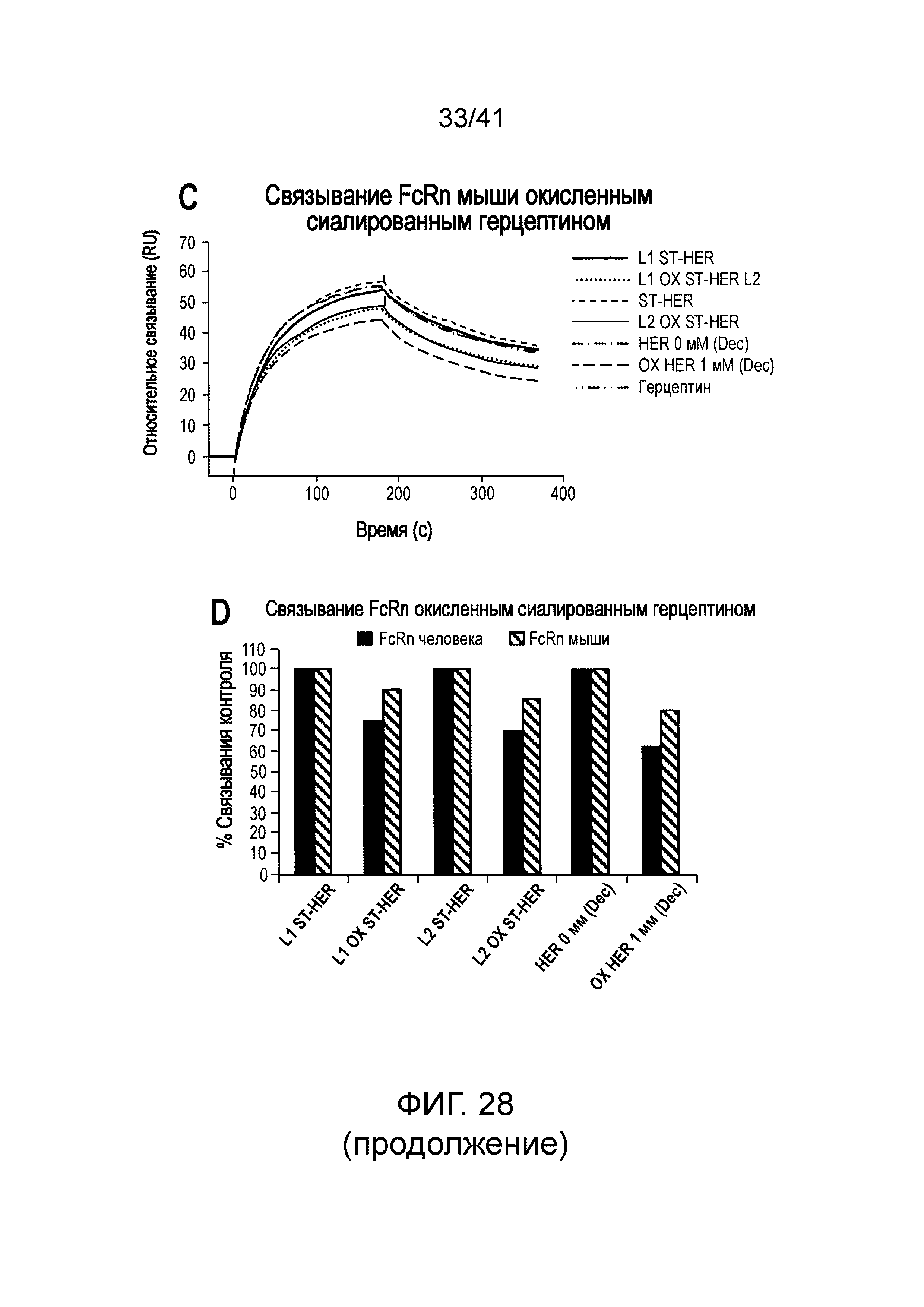
На фигуре 12 изображены результаты экспериментов поверхностного плазмонного резонанса, использованных для оценки связывания модифицированного анти-CD52 с рекомбинантным FcγRIIIa (V158) человека. Анти-CD52, содержащее мутации S298N/Y300S в домене Fc, использовали для оценки эффекторной функции модифицированной молекулы, связывания с пептидом CD52 (A), связывания с FcγRIIIa (V158, B) и контрольного связывания с FcRn (C) мыши.
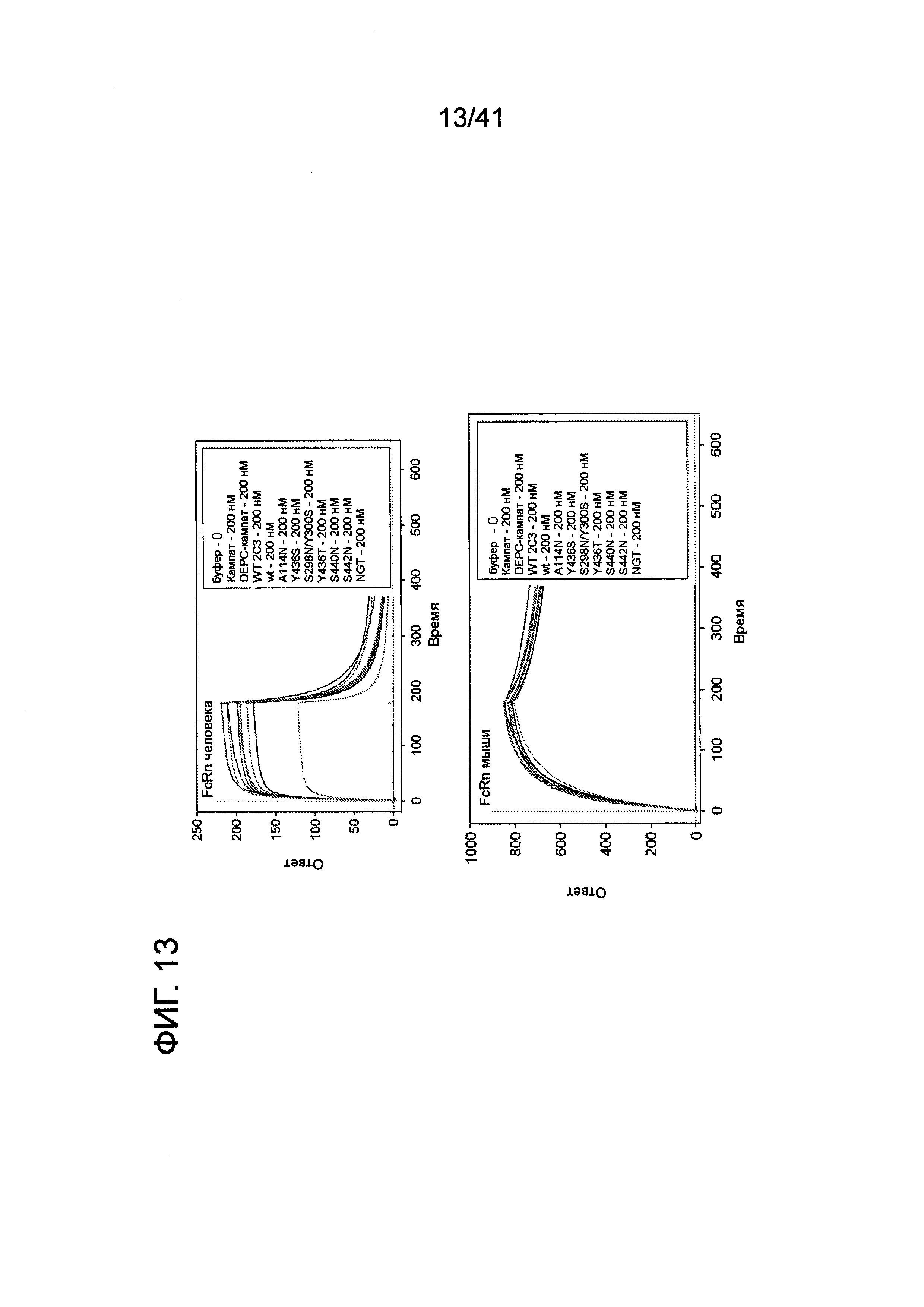
На фигуре 13 изображены результаты экспериментов поверхностного плазмонного резонанса, исследующих свойства связывания Fc мутантов 2C3.
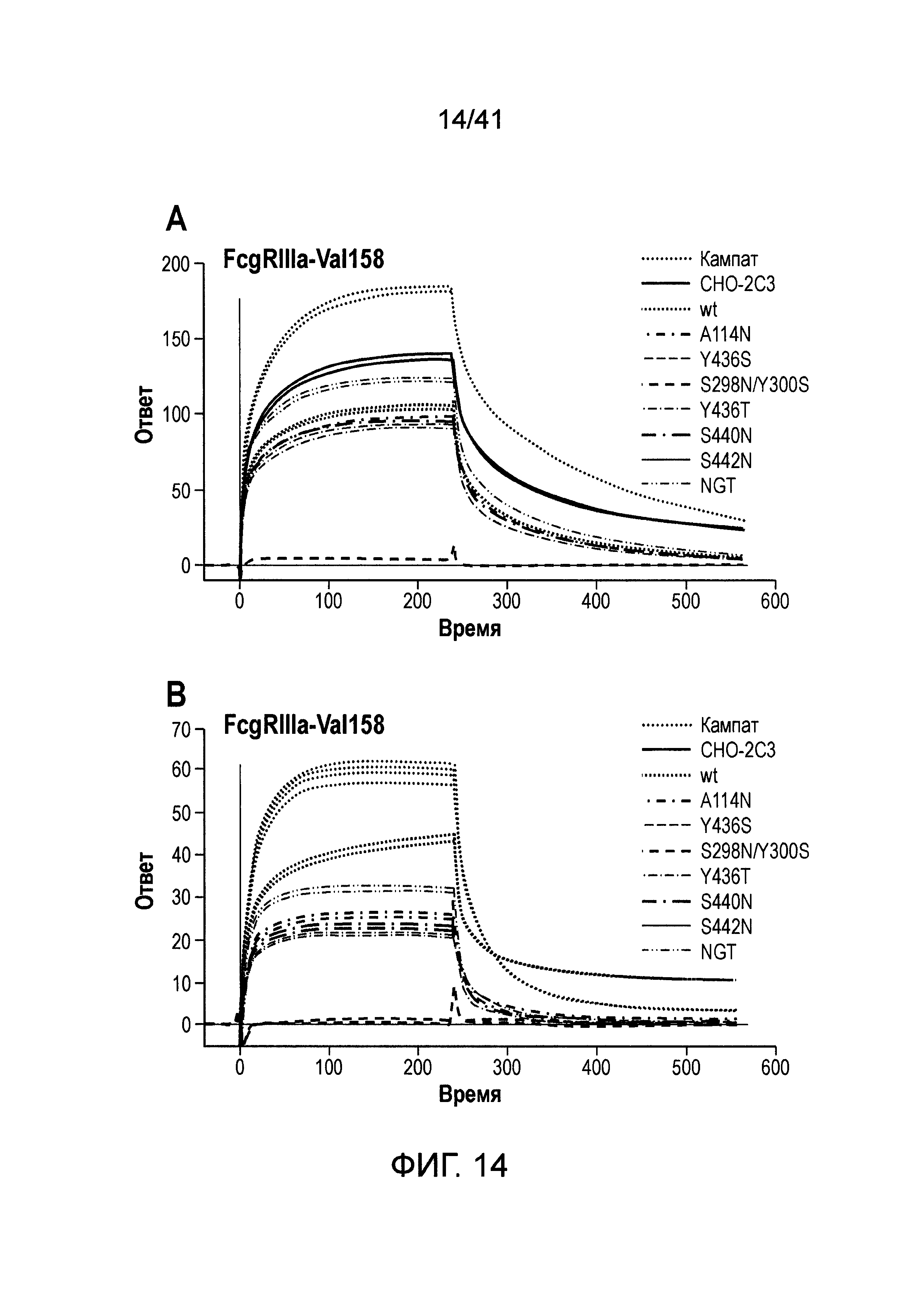
На фигуре 14 изображены результаты экспериментов поверхностного плазмонного резонанса, исследующих связывание модифицированного анти-CD52 как с FcγRIIIa (Val158) (как выше), так и с FcγRIIIa (Phe158). Антитела против CD52, содержащие мутации S298N/Y300S в домене Fc, использовали для оценки эффекторной функции модифицированной молекулы, связывающейся с FcγRIIIa (Val158, фиг. 14A) и FcγRIIIa (Phe58, фиг. 14B).
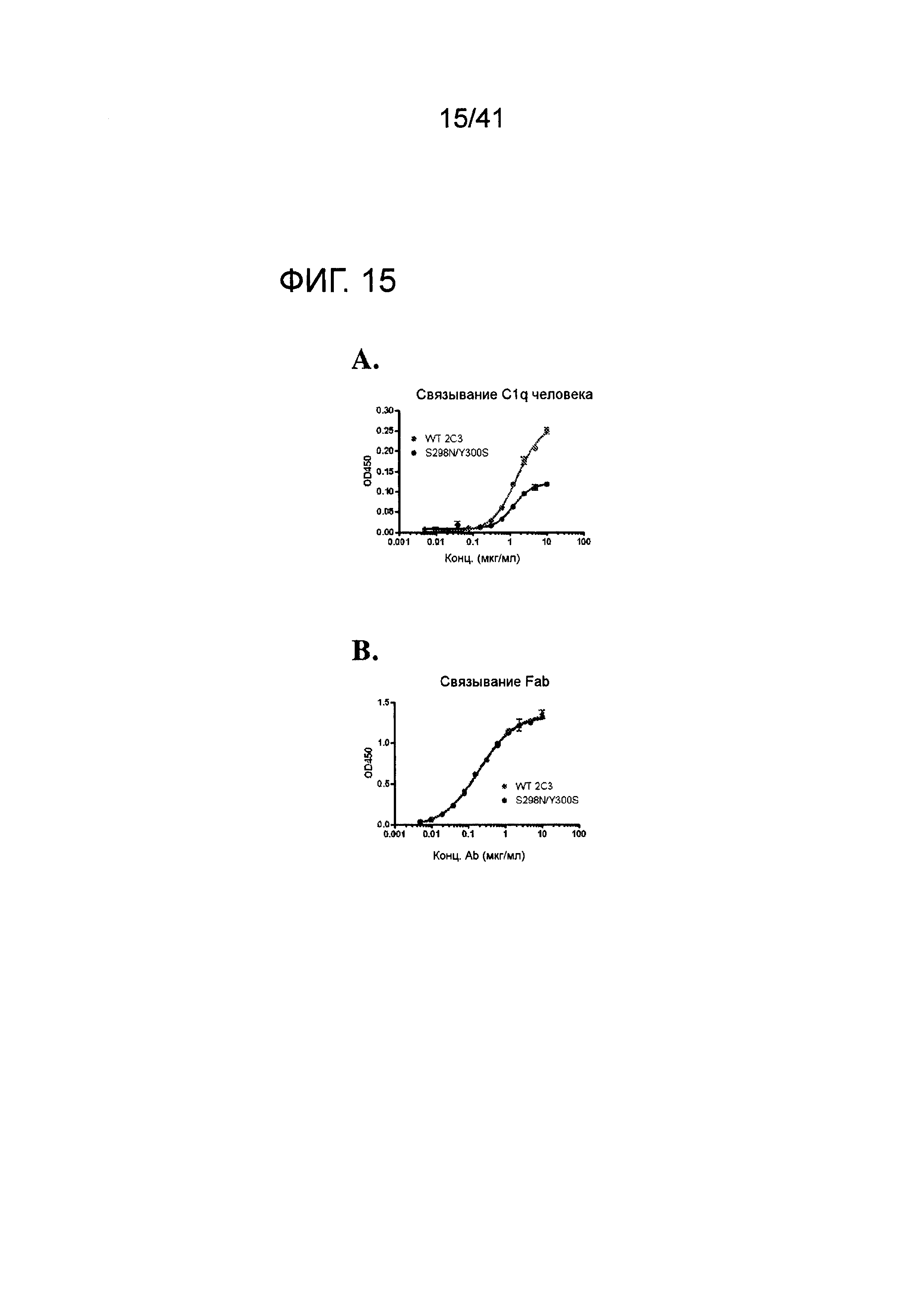
На фигуре 15 изображен анализ связывания C1q для мутанта S298N/Y300S и контроля WT 2C3 (A), и результаты анализа Eliza, подтверждающие эквивалентное покрытие лунок.
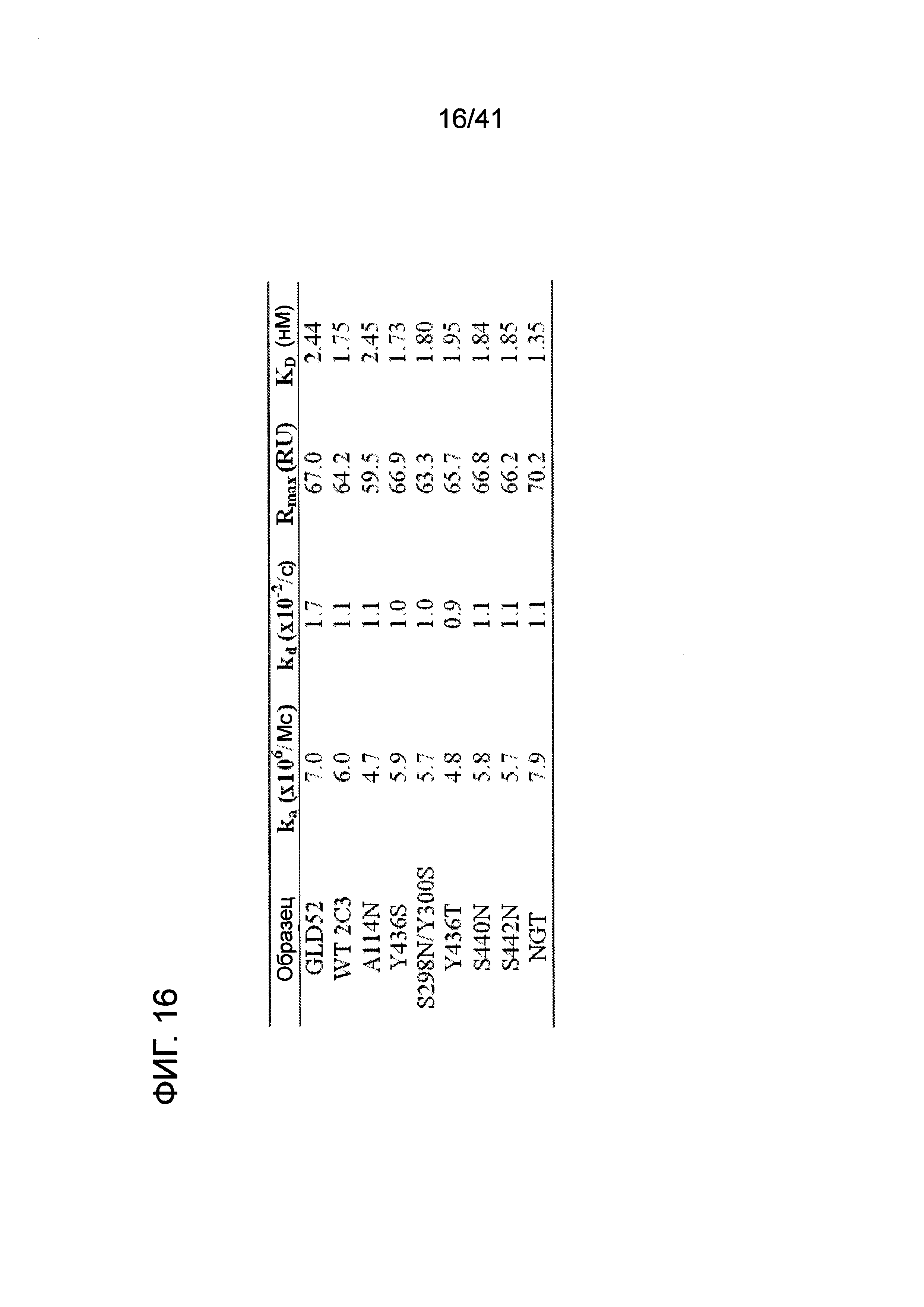
На фигуре 16 изображены результаты экспериментов плазмонного резонанса, измеряющих кинетику связывания мутантов 2C3 с пептидом 741 CD-52.
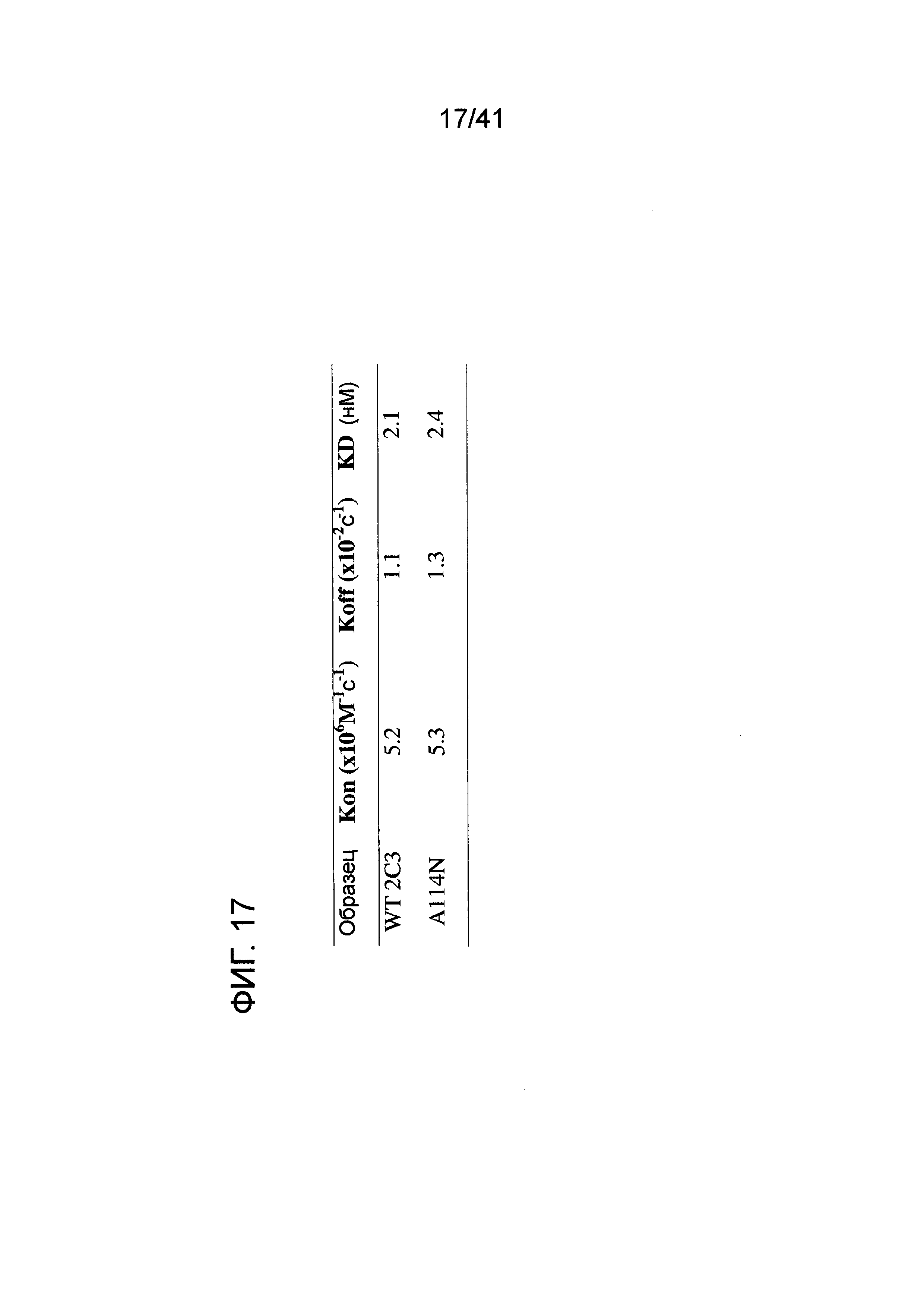
На фигуре 17 изображены результаты экспериментов плазмонного резонанса, сравнивающих аффинность связывания антигена для анти-CD-52 2C3 WT и мутанта A114N с гипергликозилированием.
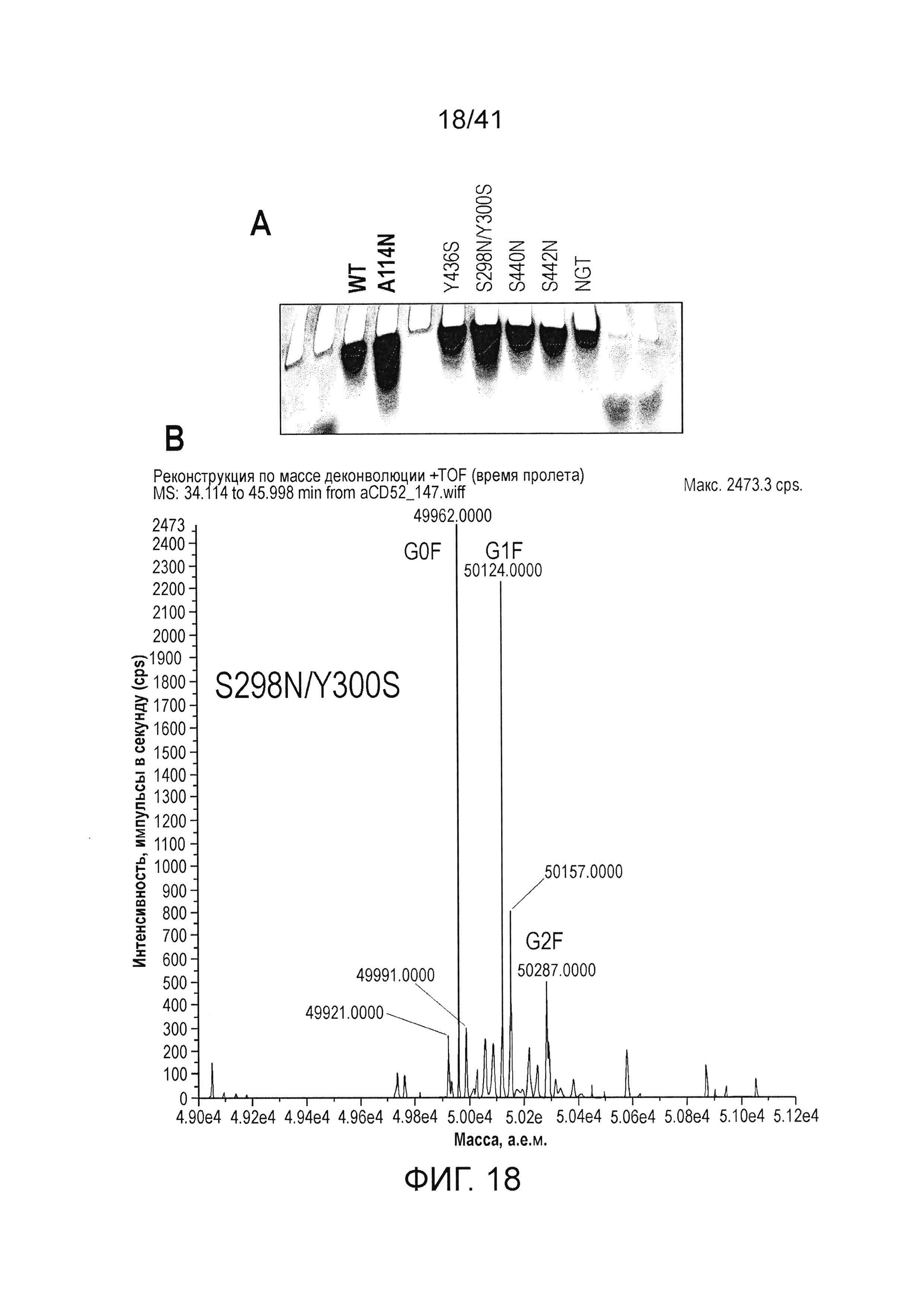
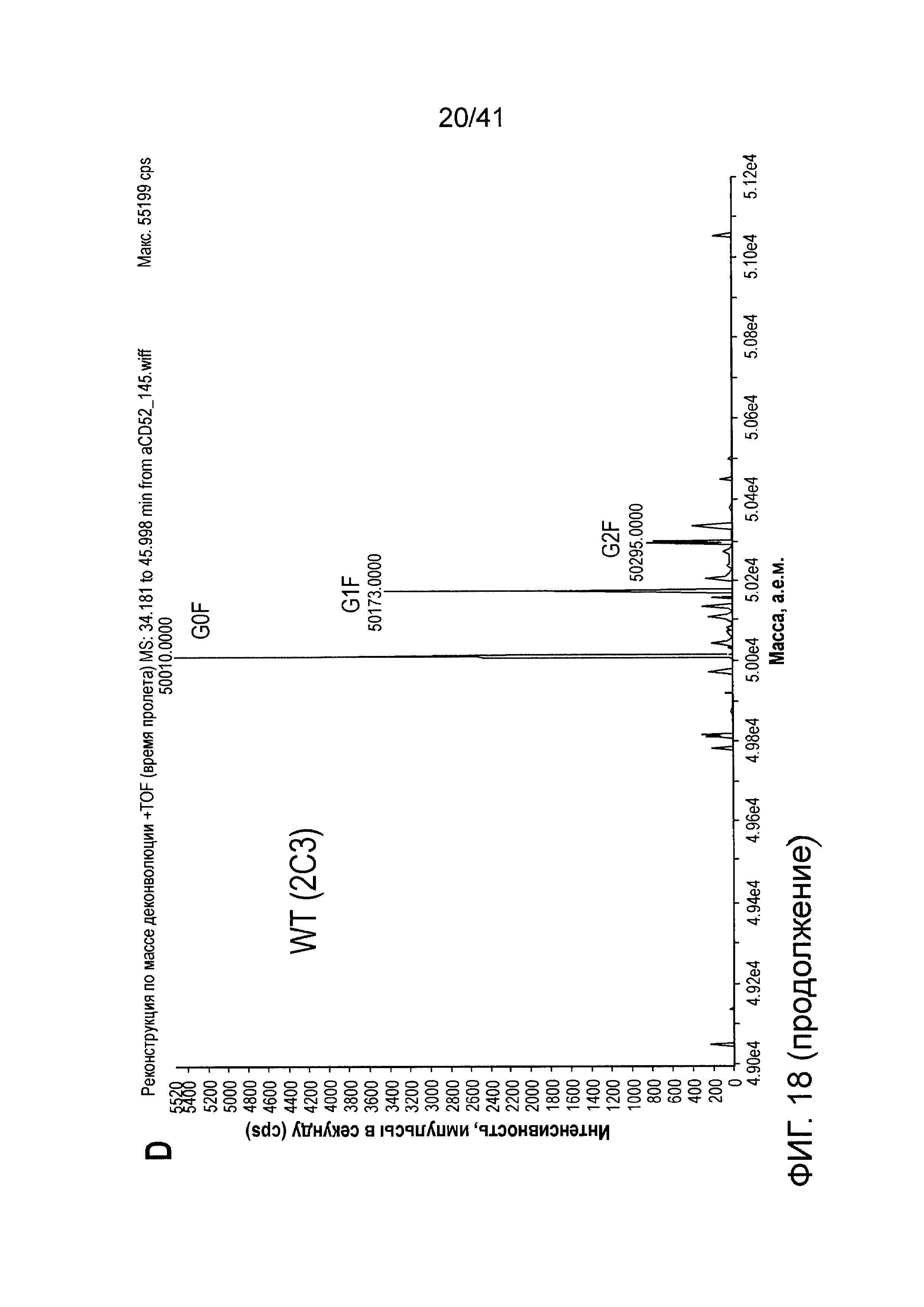
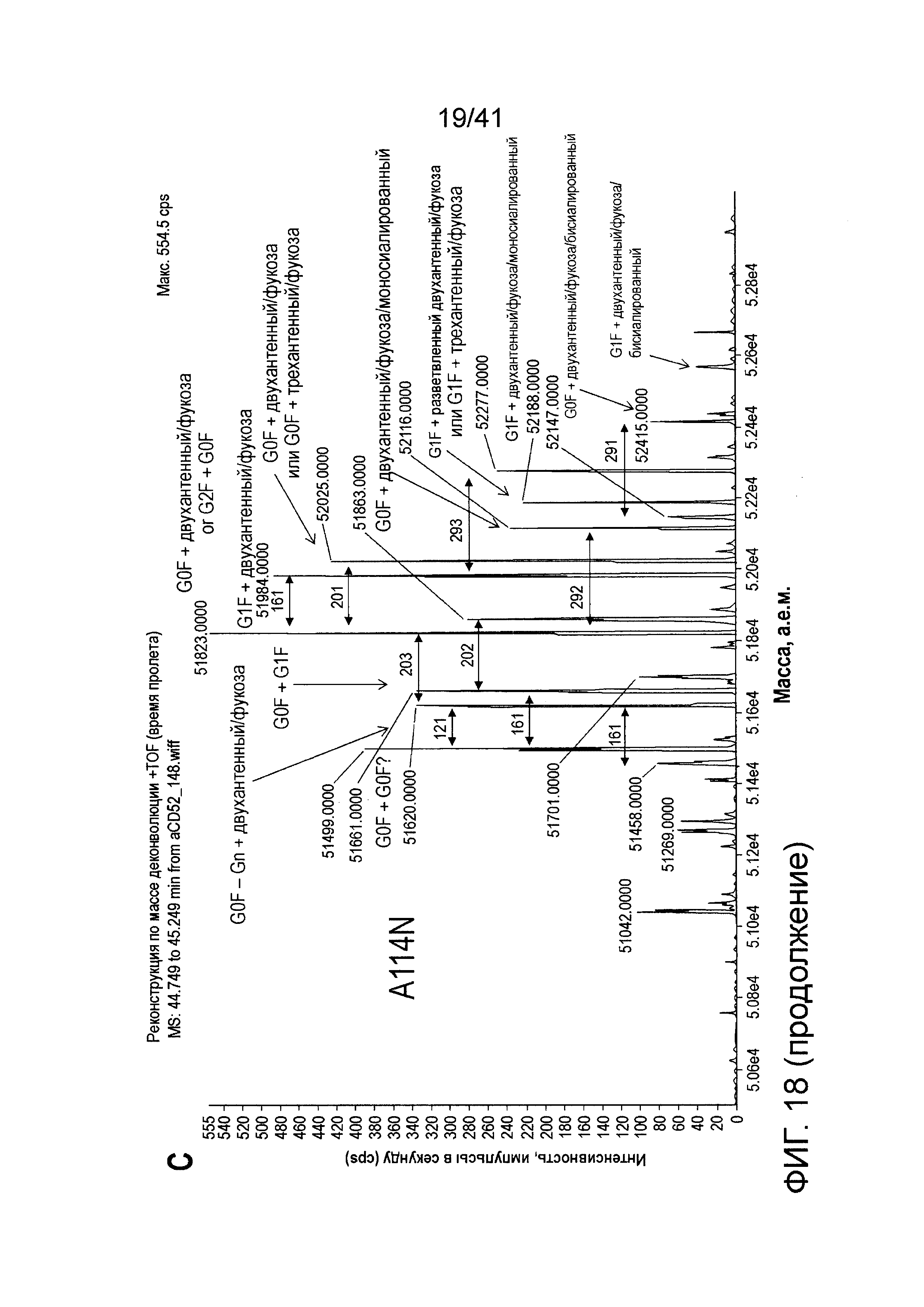
На фигуре 18 изображены результаты экспериментов характеризации заряда изоэлектрическим фокусированием и масс-спектрометрией для определения содержания гликанов мутантов 2C3.
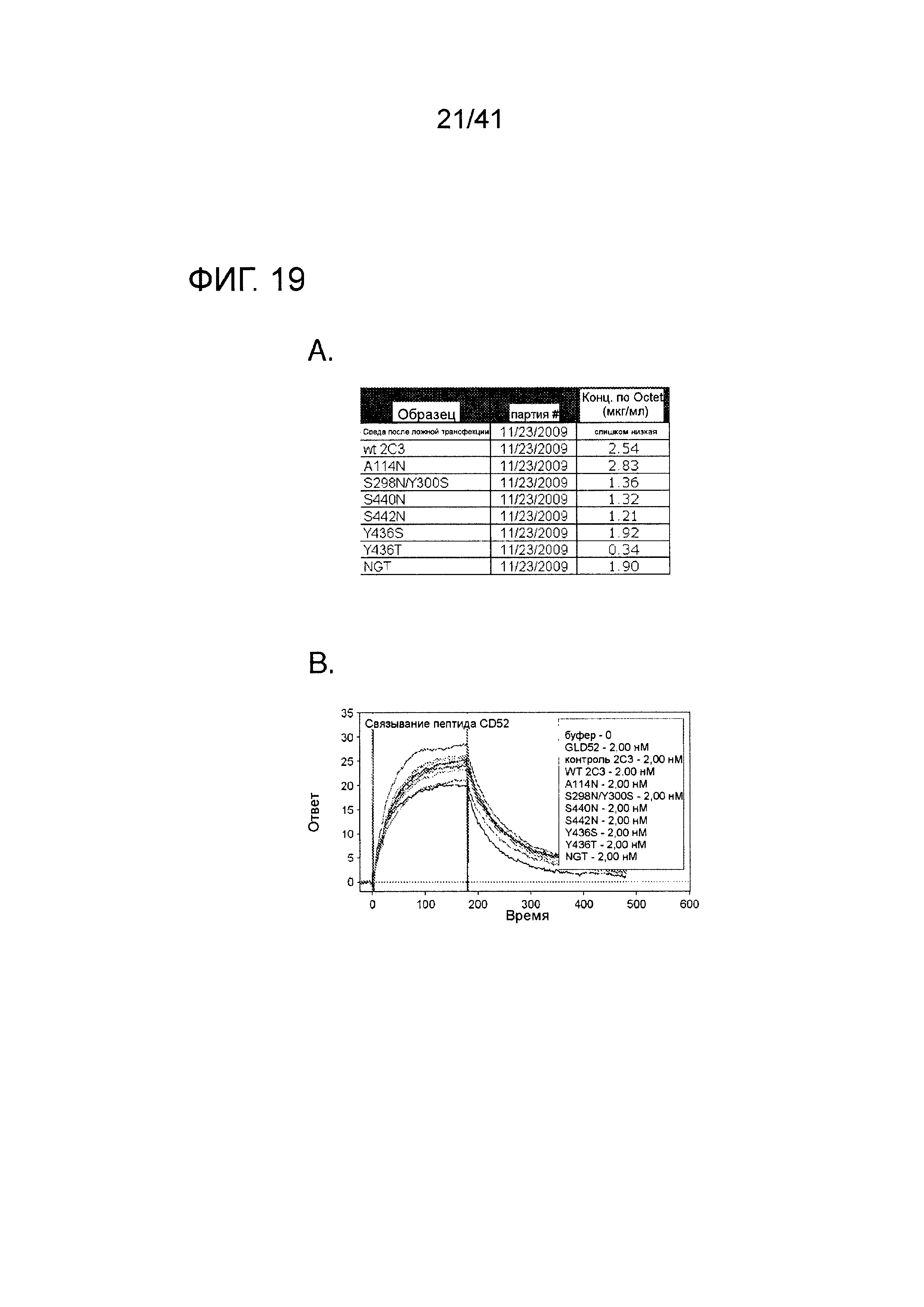
На фигуре 19 изображены результаты экспериментов определения концентрации (Octet) и плазмонного резонанса, сравнивающих аффинность связывания антигена для анти-CD52 2C3 WT и мутантов.
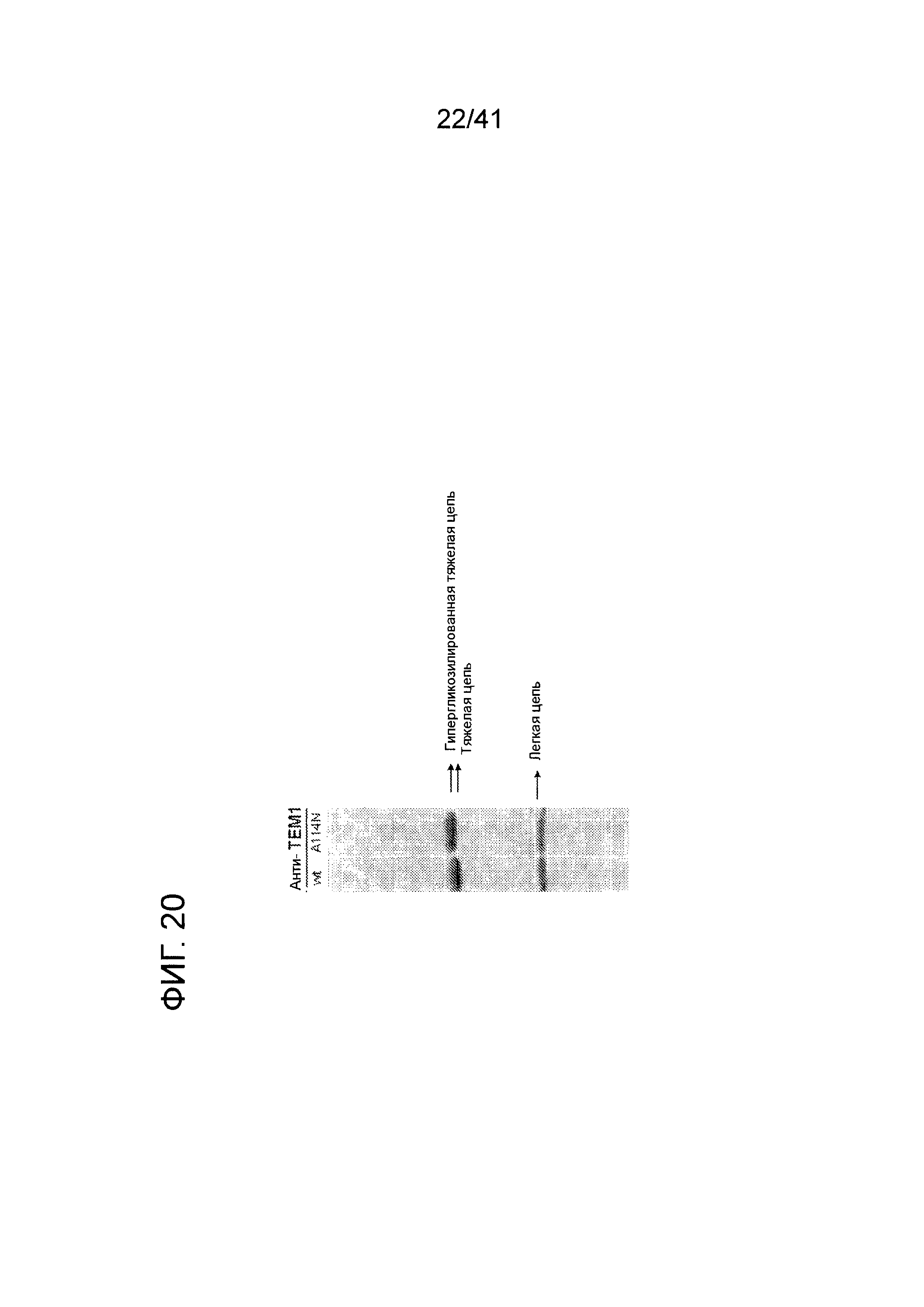
На фигуре 20 показаны результаты экспериментов SDS-PAGE, чтобы продемонстрировать дополнительное гликозилирование мутанта A114N анти-TEM1.
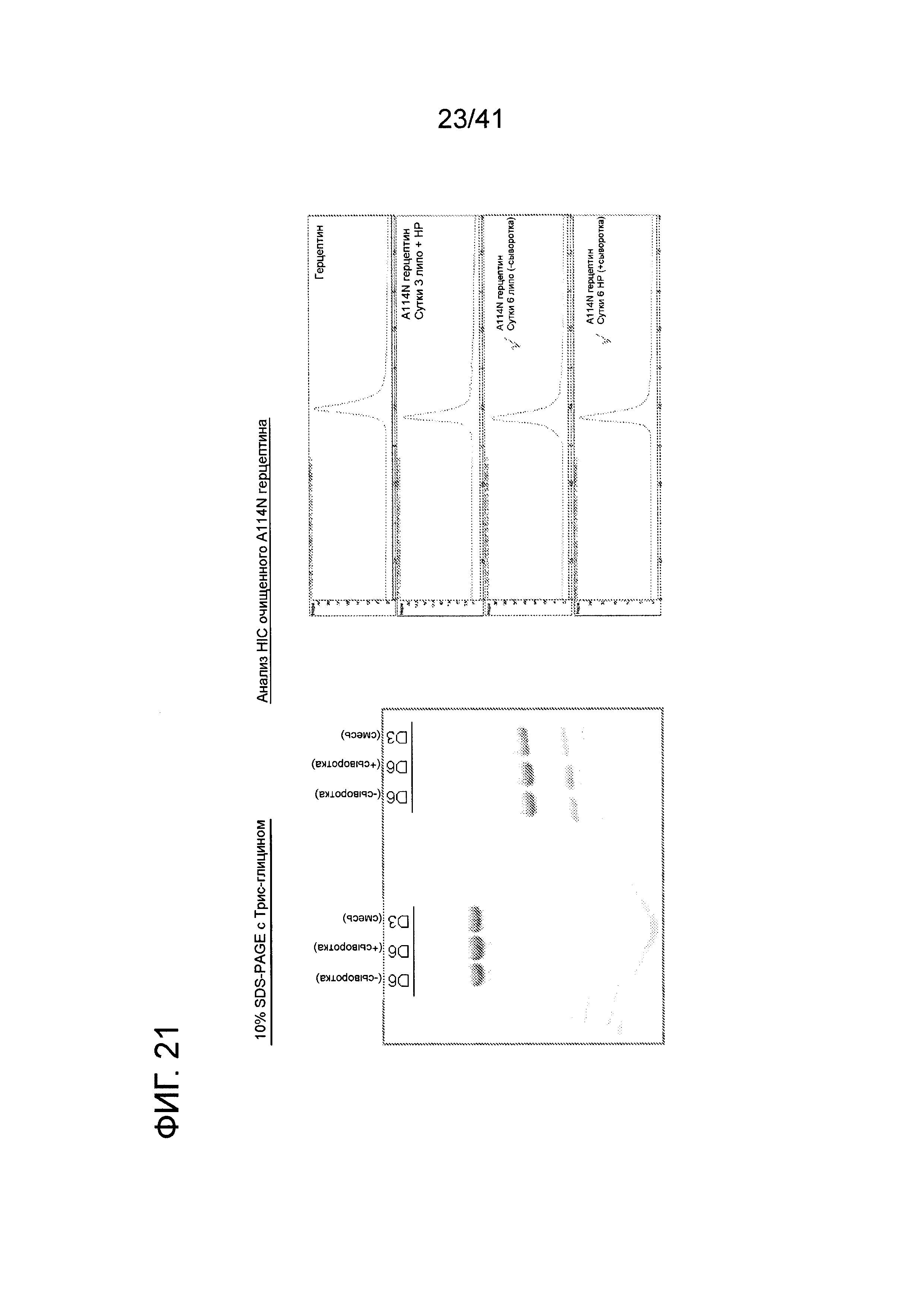
На фигуре 21 показаны результаты анализа SDS-PAGE и хроматографии гидрофобного взаимодействия мутанта A114N анти-Her2.
На фигуре 22 показаны результаты экспериментов SDS-PAGE, чтобы продемонстрировать конъюгацию PEG с мутантом A114N 2C3 через аминоокси-связь.
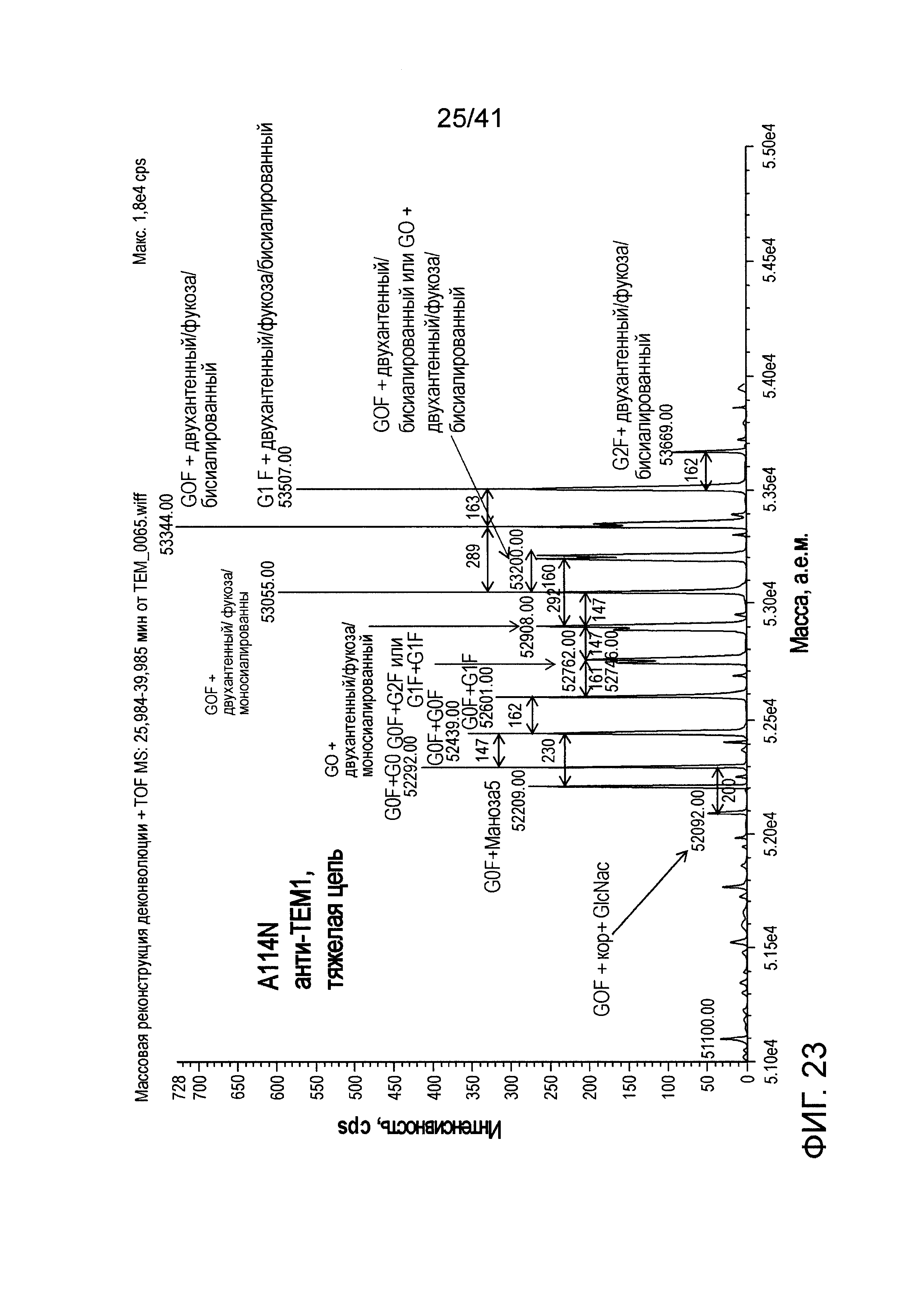
На фигуре 23 показаны результаты экспериментов LC-MS для определения содержания гликанов A114N мутанта анти-TEM1 с гипергликозилированием.
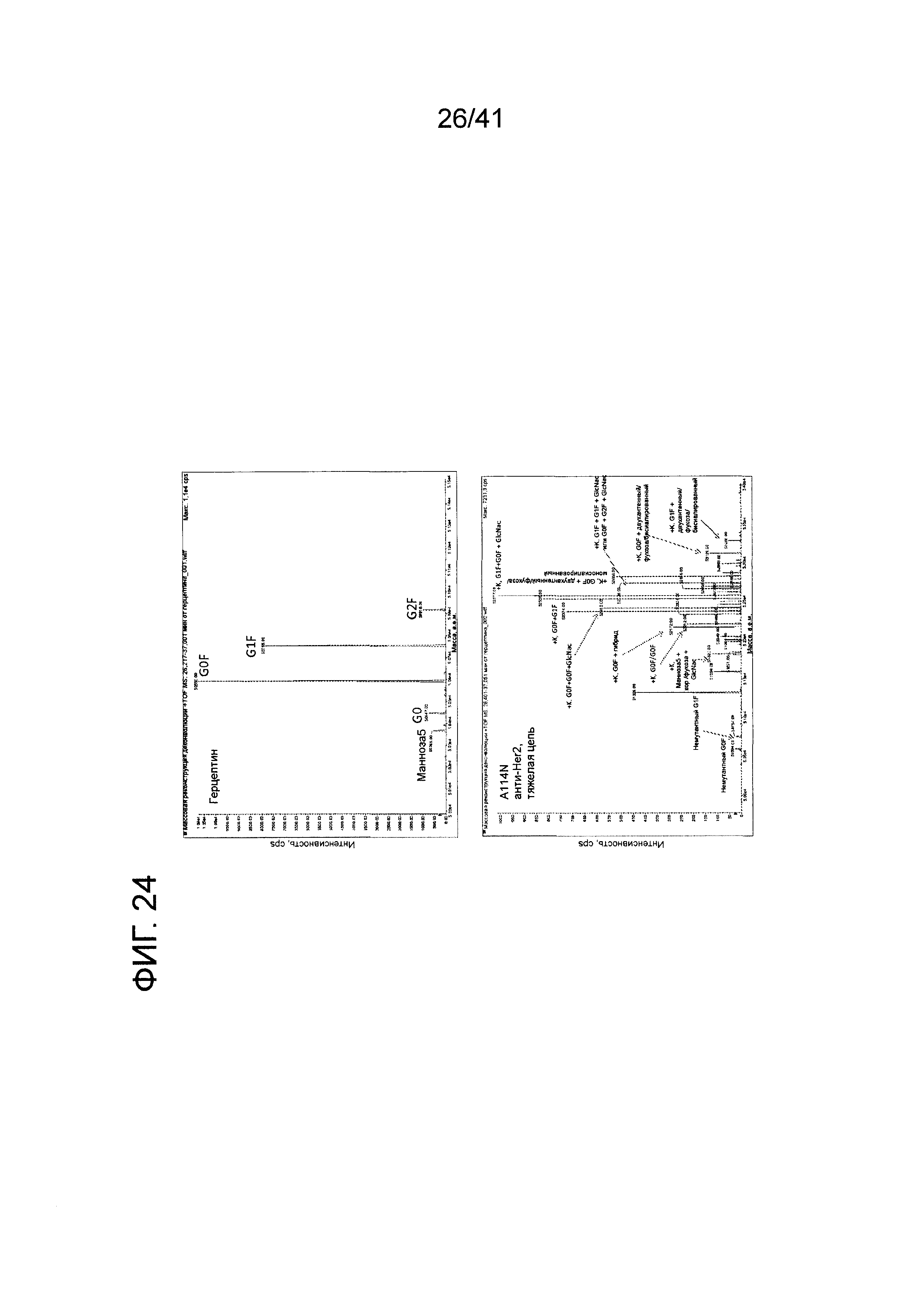
На фигуре 24 показаны результаты экспериментов LC-MS для определения содержания гликанов антитела анти-HER2 дикого типа и мутанта A114N анти-Her2 с гипергликозилированием.
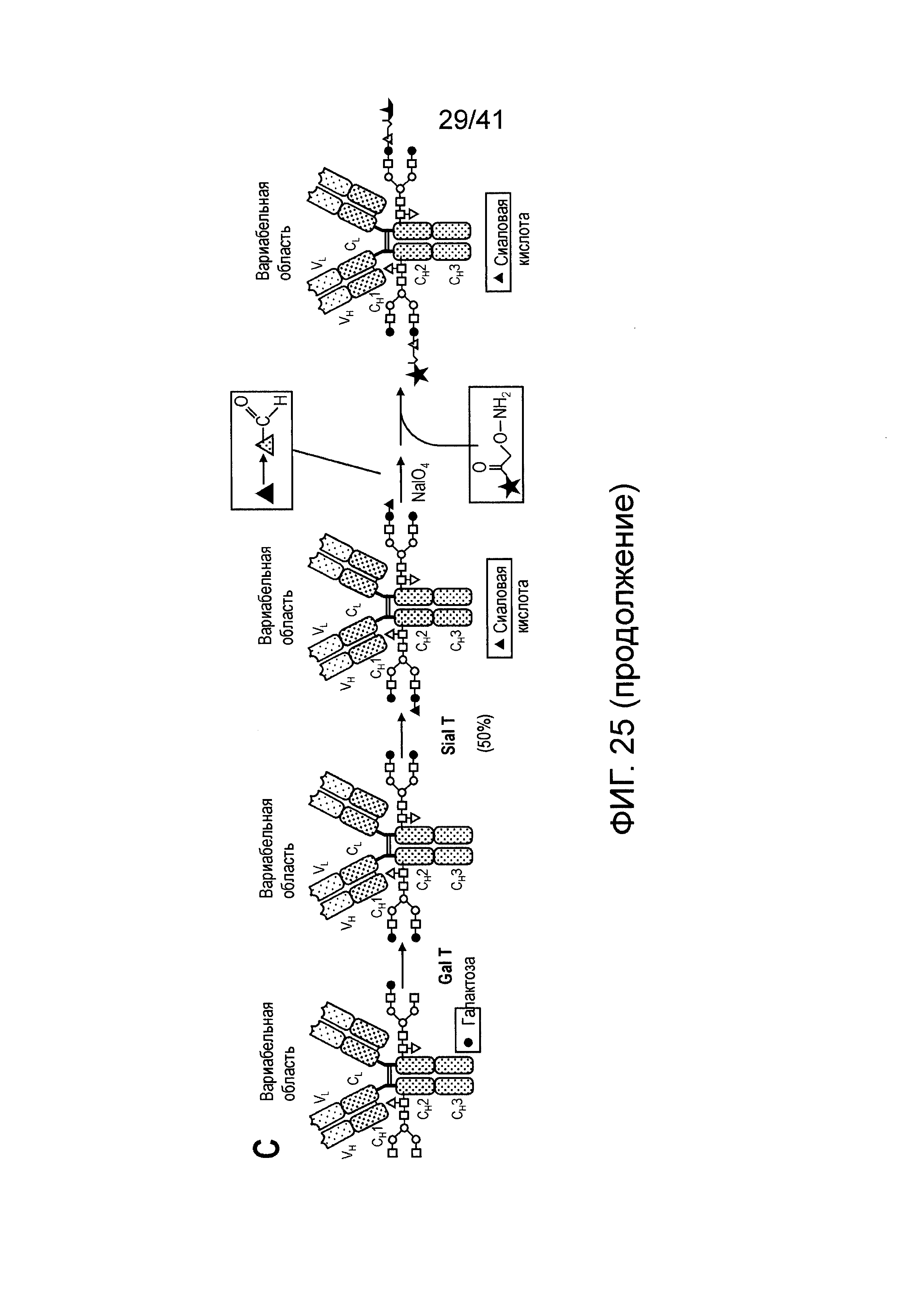
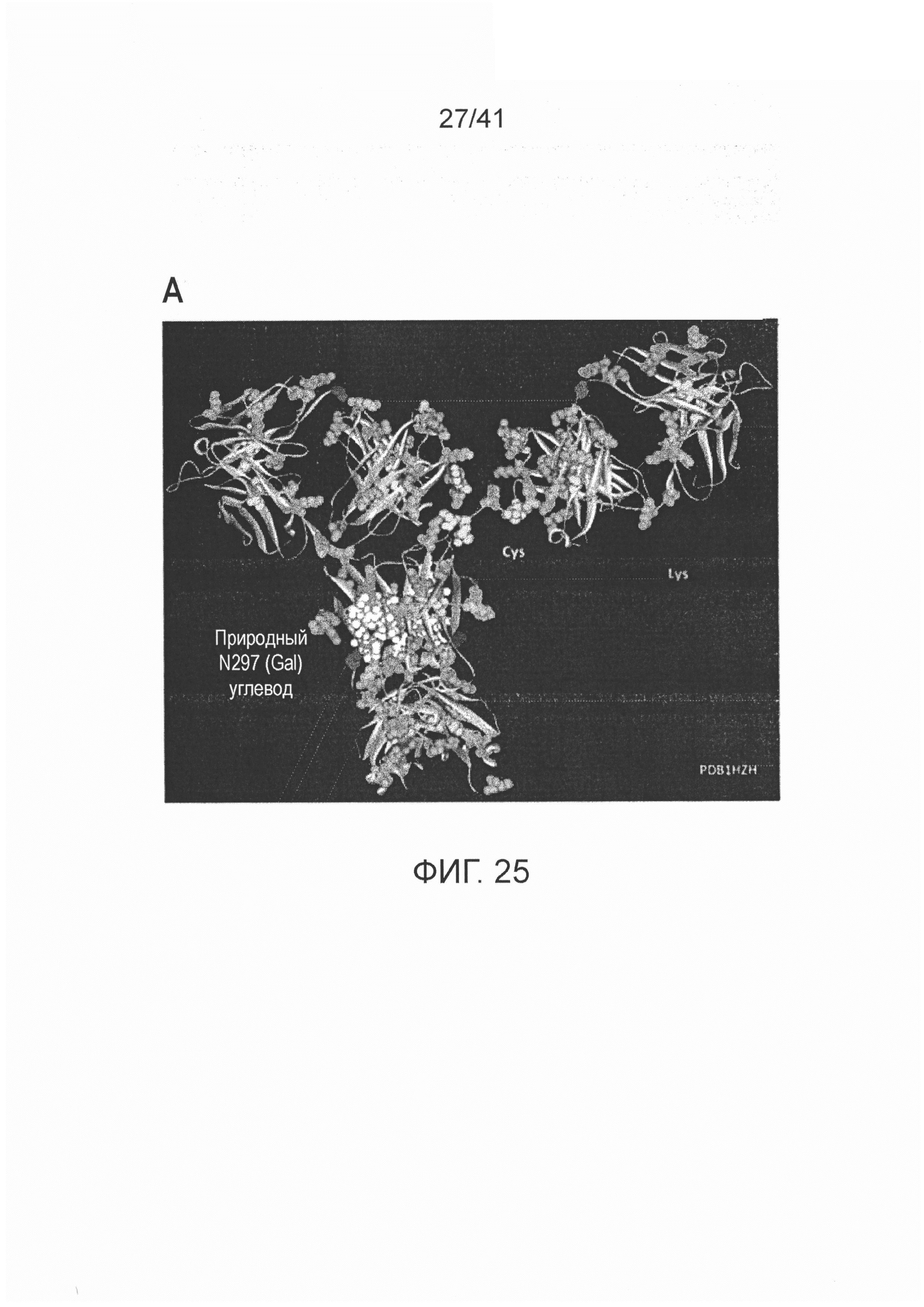
На фигуре 25 изображен иллюстративный способ осуществления сайи-специфической конъюгации антитела в соответствии со способами по изобретению.
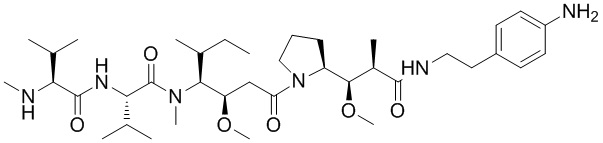
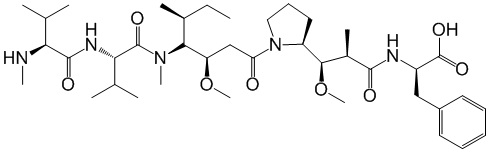
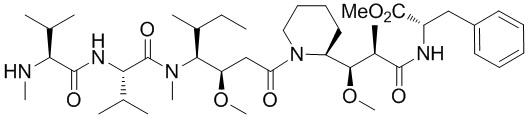
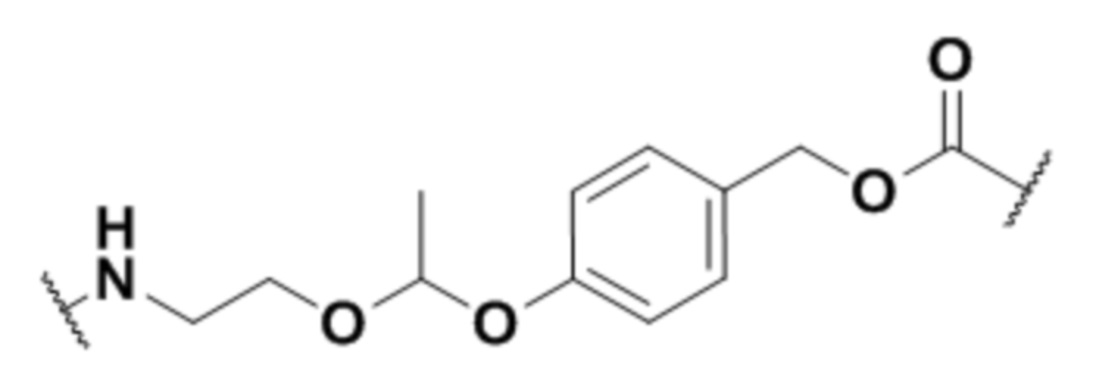
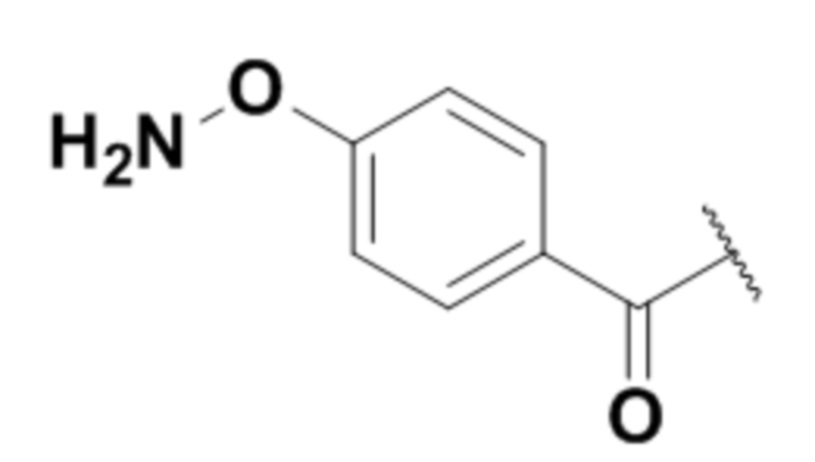
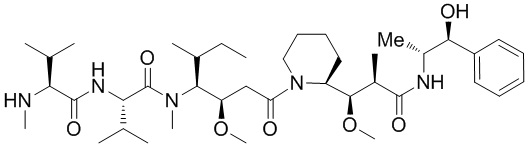
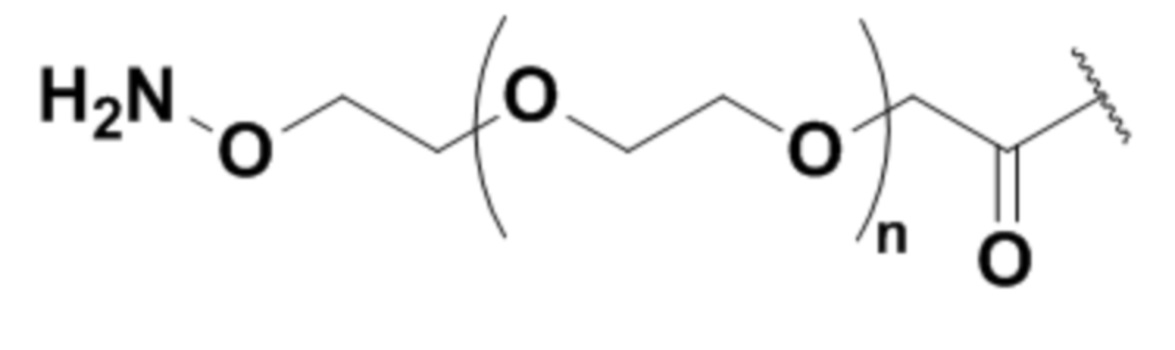
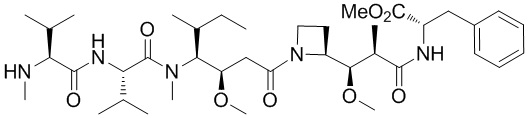
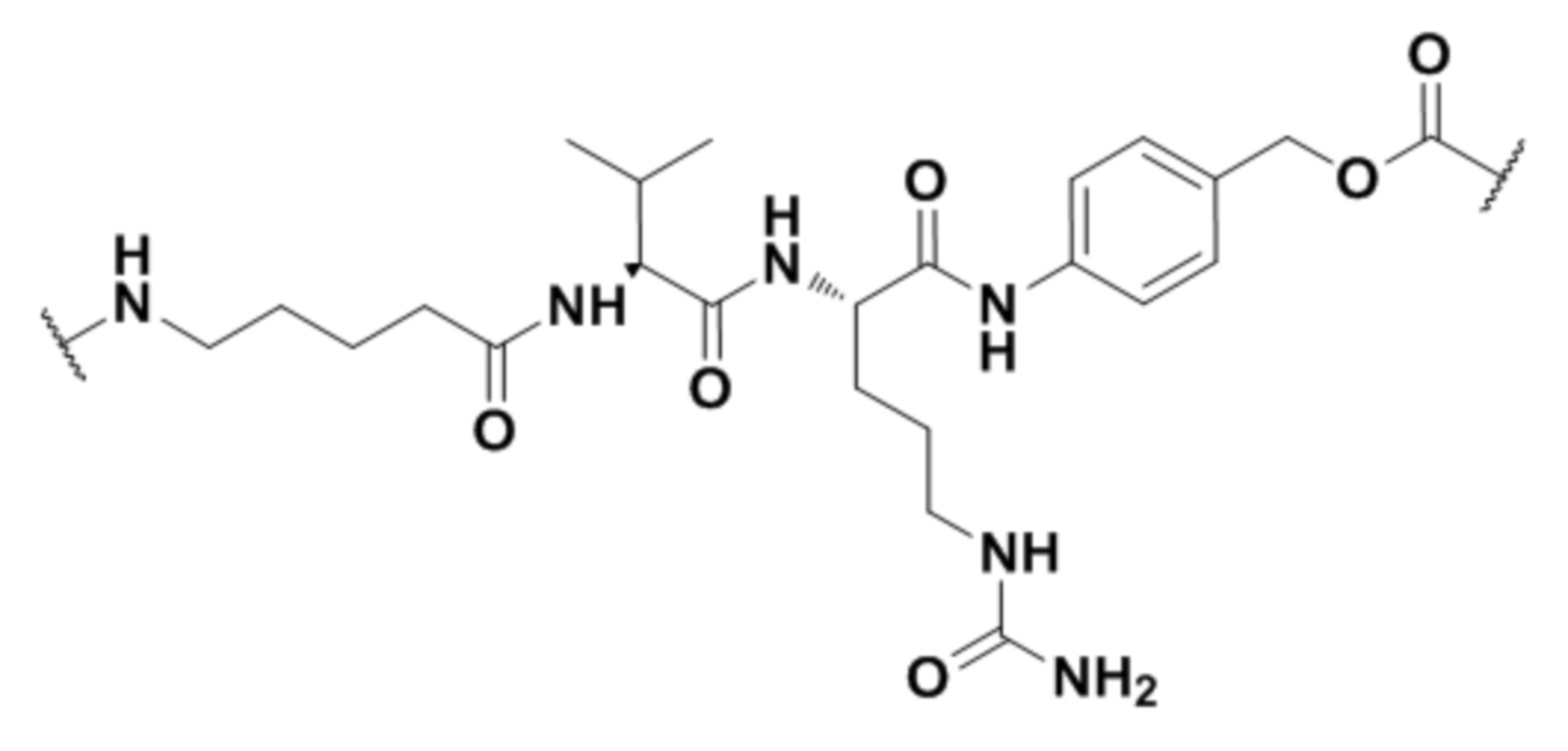
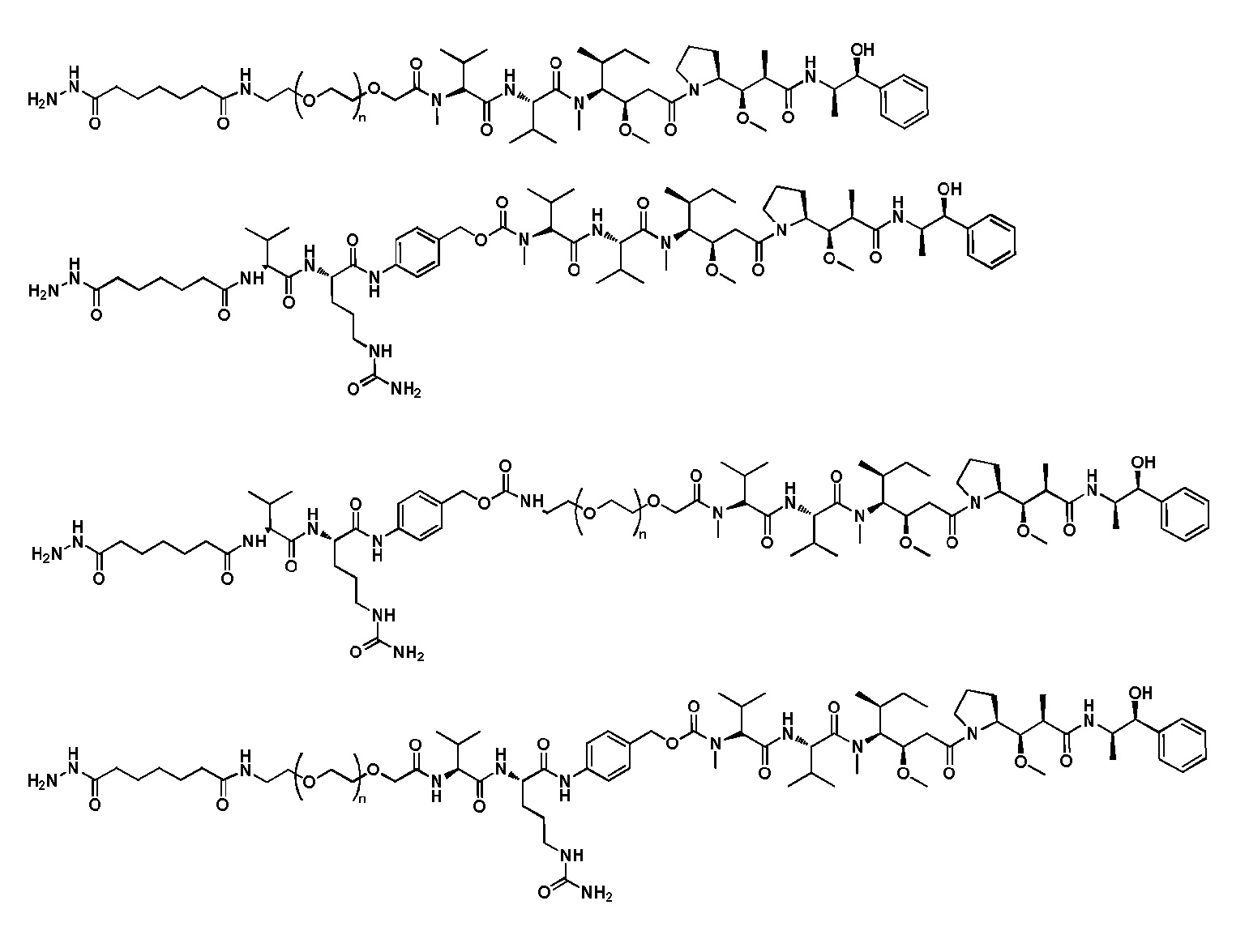
На фигуре 26 изображен синтез иллюстративных эффекторных групп по изобретению: аминоокси-Cys-MC-VC-PABC-MMAE и аминоокси-Cys-MC-VC-PABC-PEG8-Dol10.
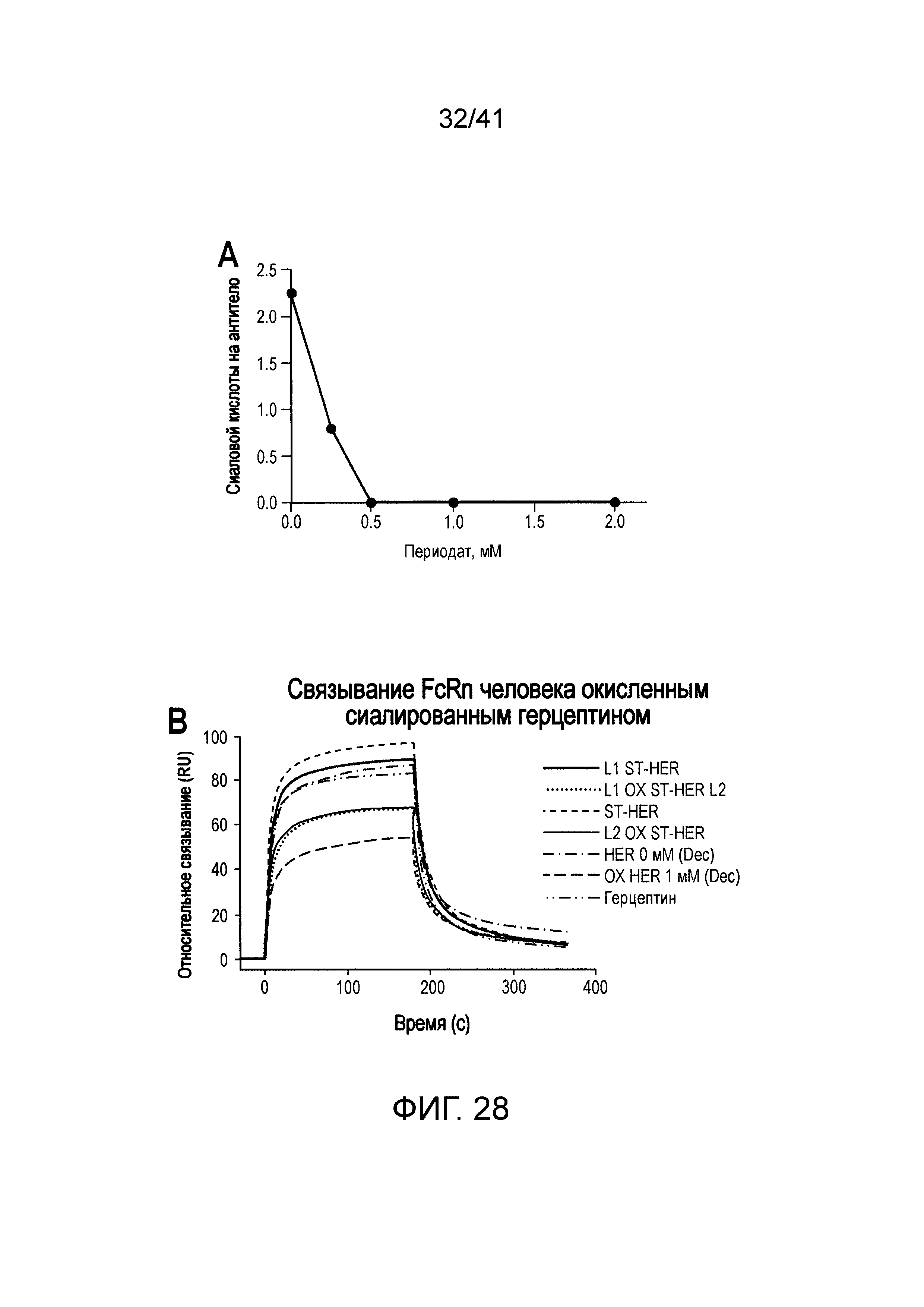
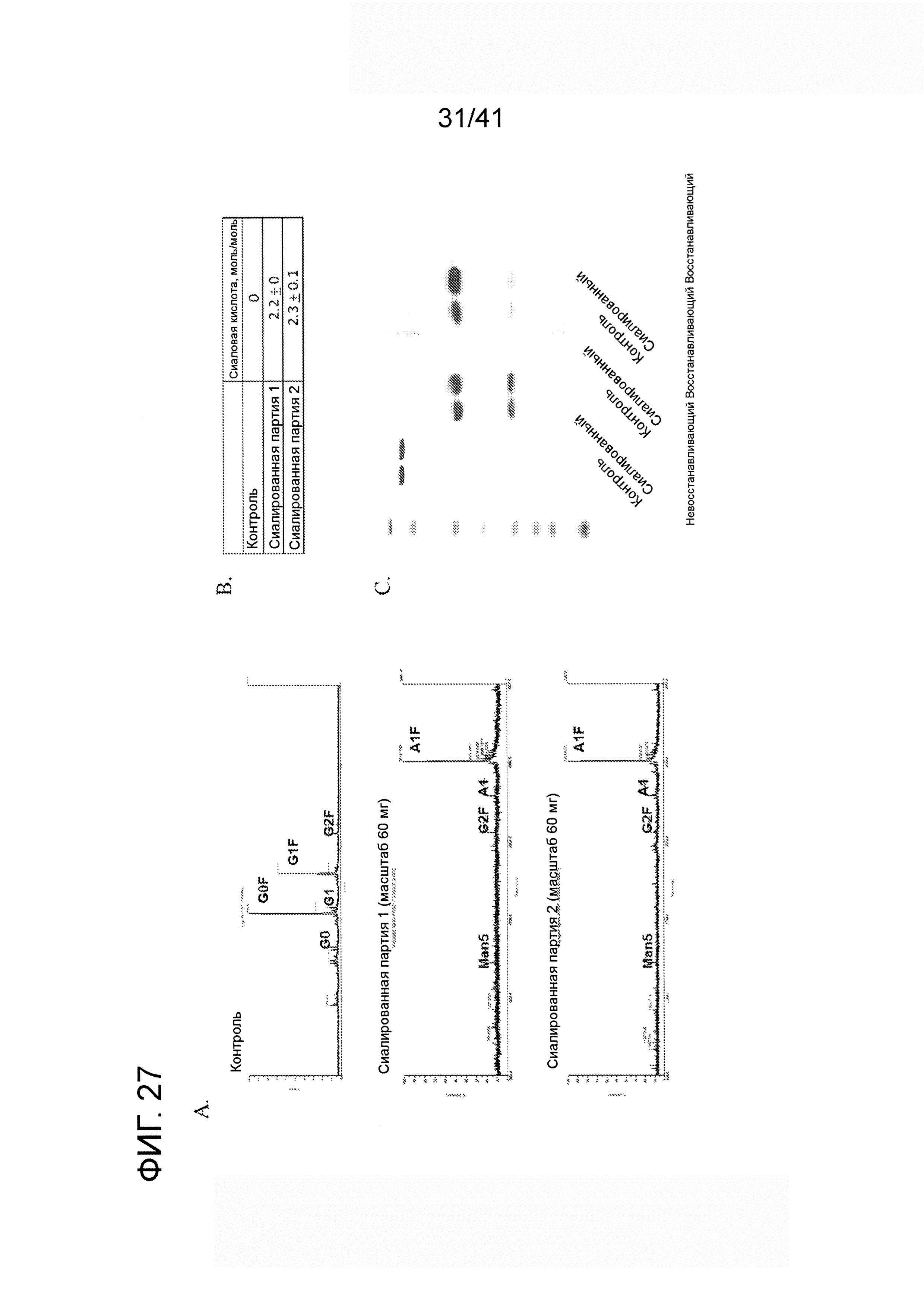
На фигуре 27 изображена информация по характеризации сиалированного антитела против HER2.
На фигуре 28 изображена информация по характеризации окисленного сиалированного антитела анти-HER2.
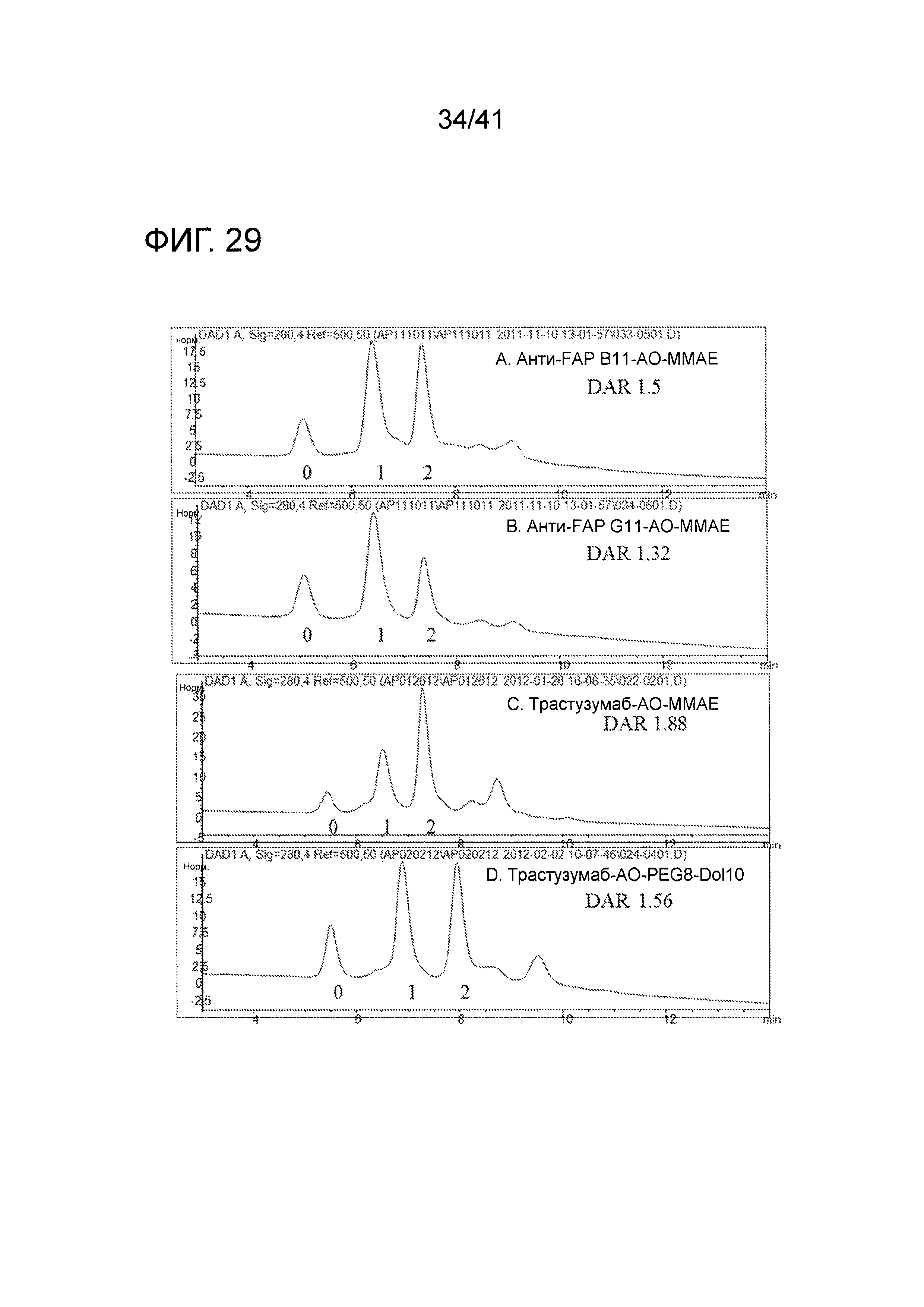
На фигуре 29 изображены хроматограммы гидрофобного взаимодействия гликоконъюгатов, полученных с тремя различными сиалированными антителами с двумя различными аминооксигруппамми.
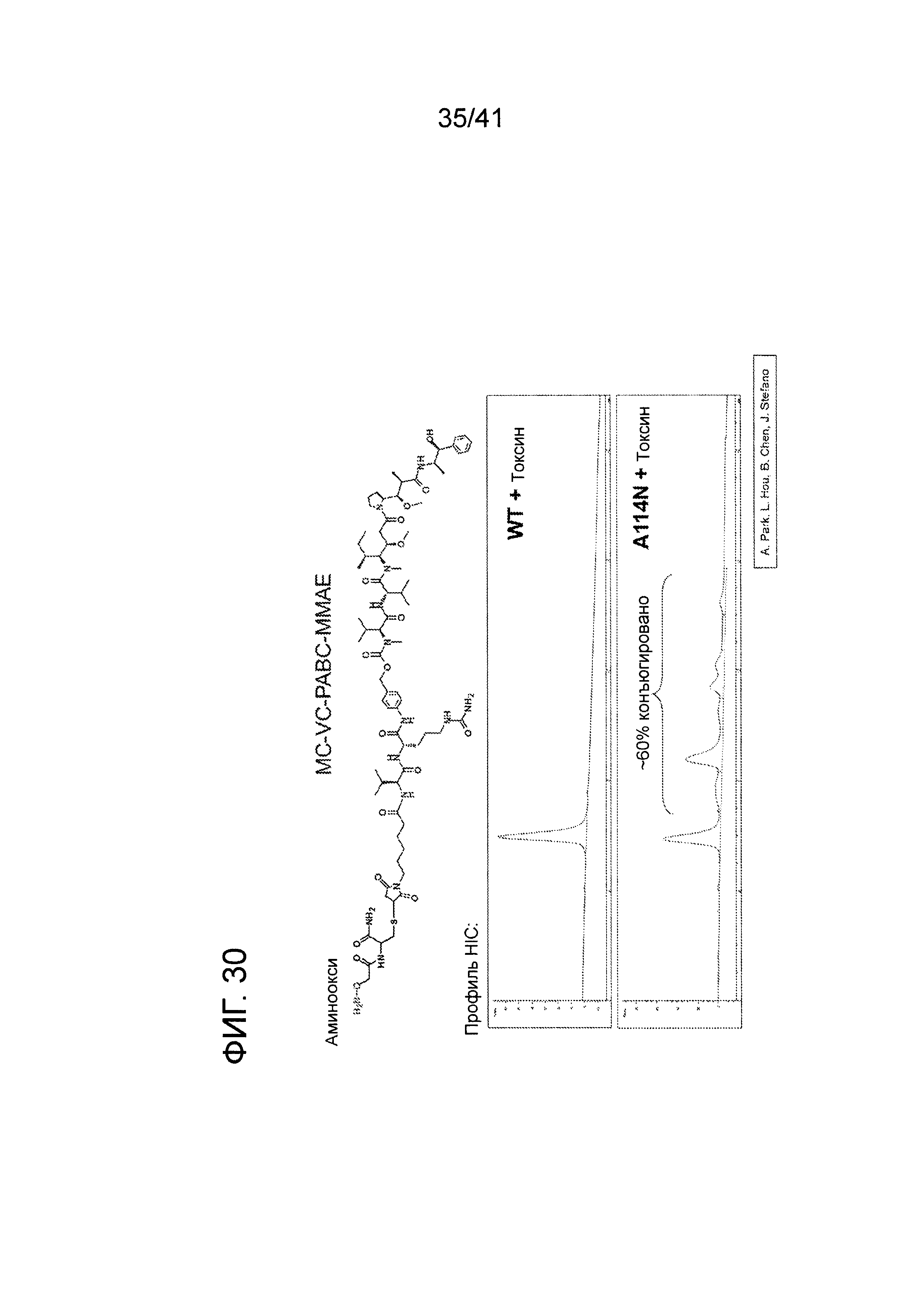
На фигуре 30 показана хроматограмма HIC конъюгата мутанта по гликозилированию A114 анти-Her2 с AO-MMAE, полученного с использованием химических реакций GAM(+).
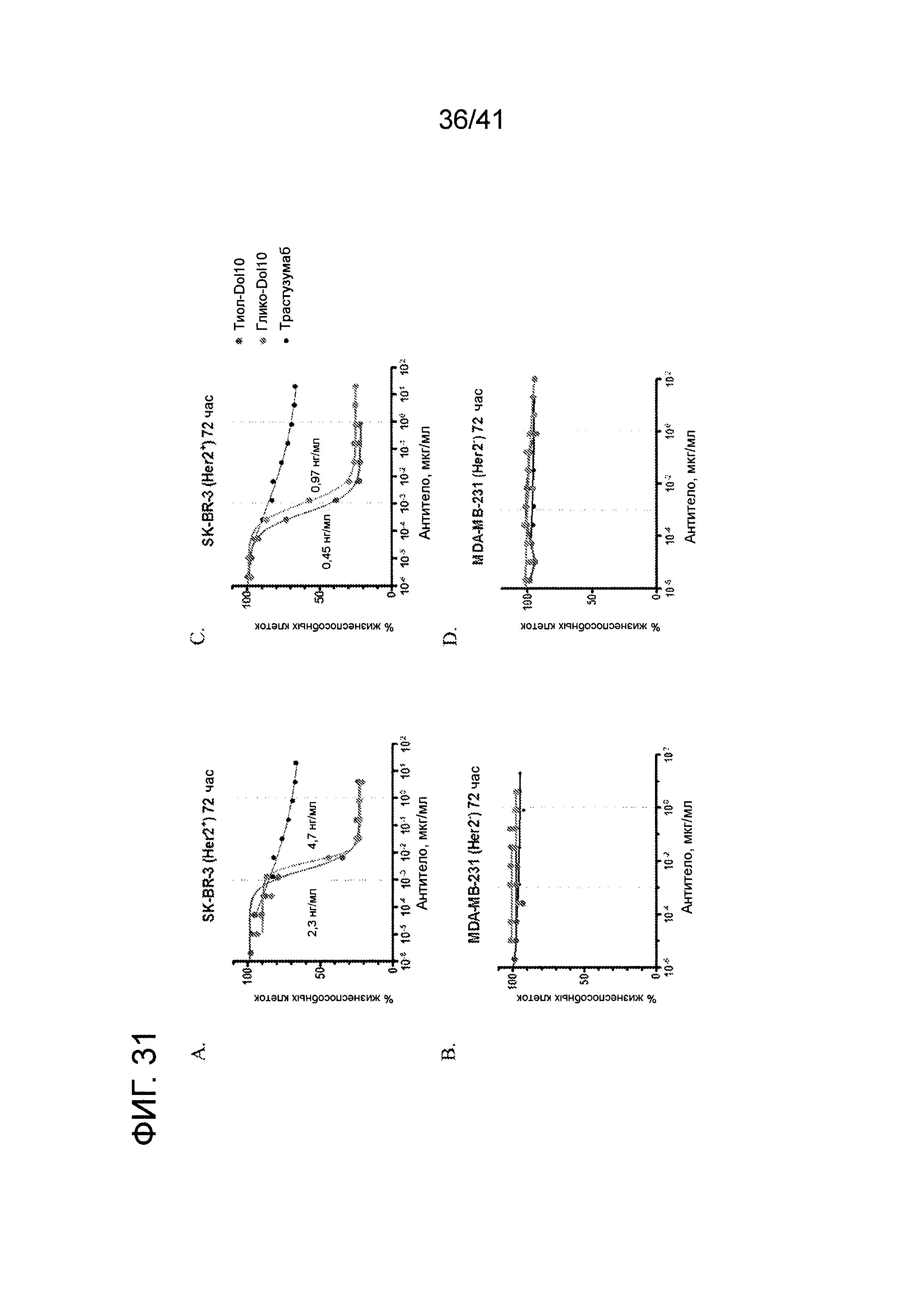
На фигуре 31 изображено сравнение активности in vitro гликоконъюгата и тиолового конъюгата анти-HER2.
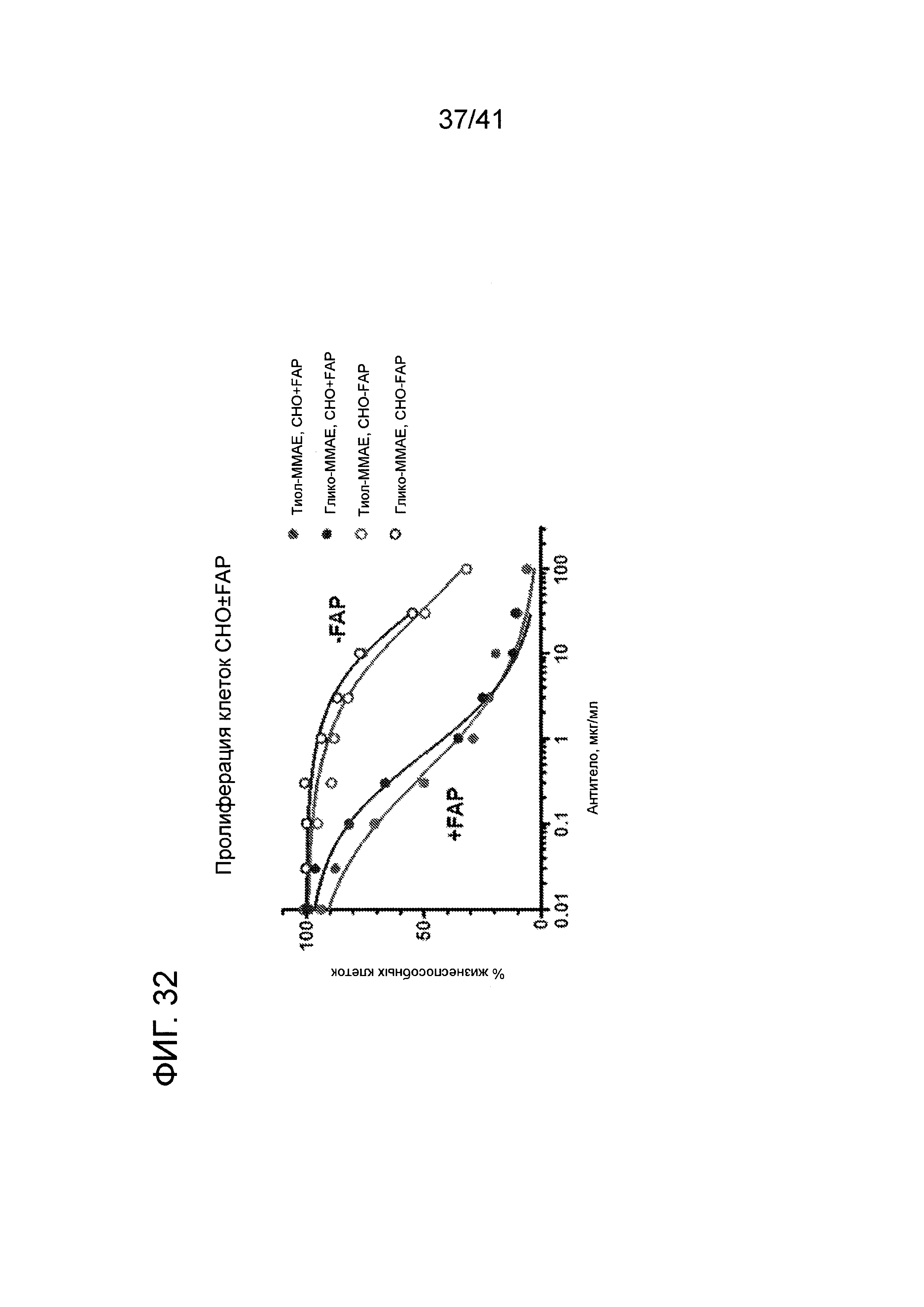
На фигуре 32 изображено сравнение активности in vitro гликоконъюгата и тиолового конъюгата анти-FAP B11.
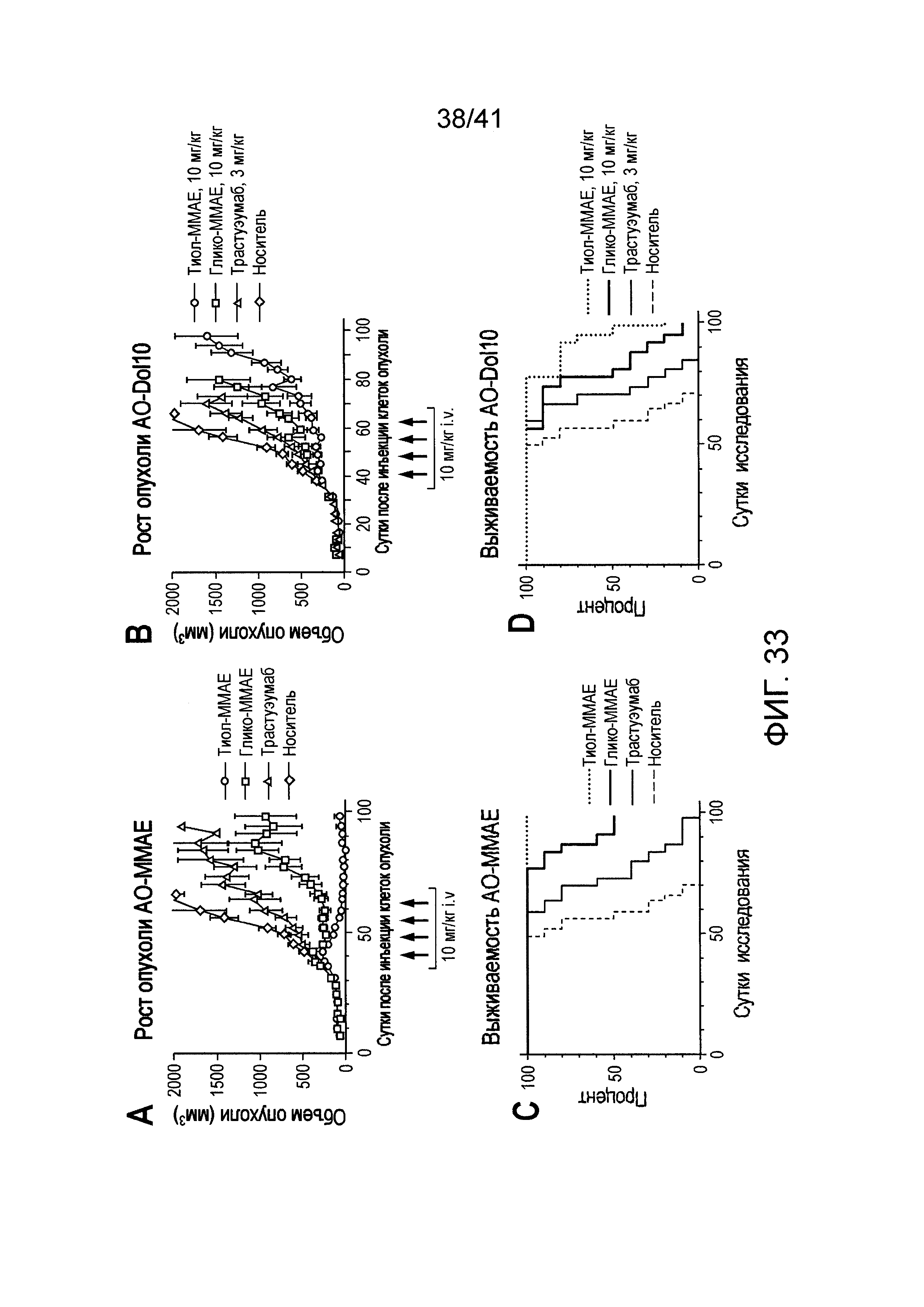
На фигуре 33 изображено сравнение эффективности in vivo гликоконъюгатов и тиоловых конъюгатов анти-HER2 в модели ксенотрансплантата Her2+ клеток опухоли.
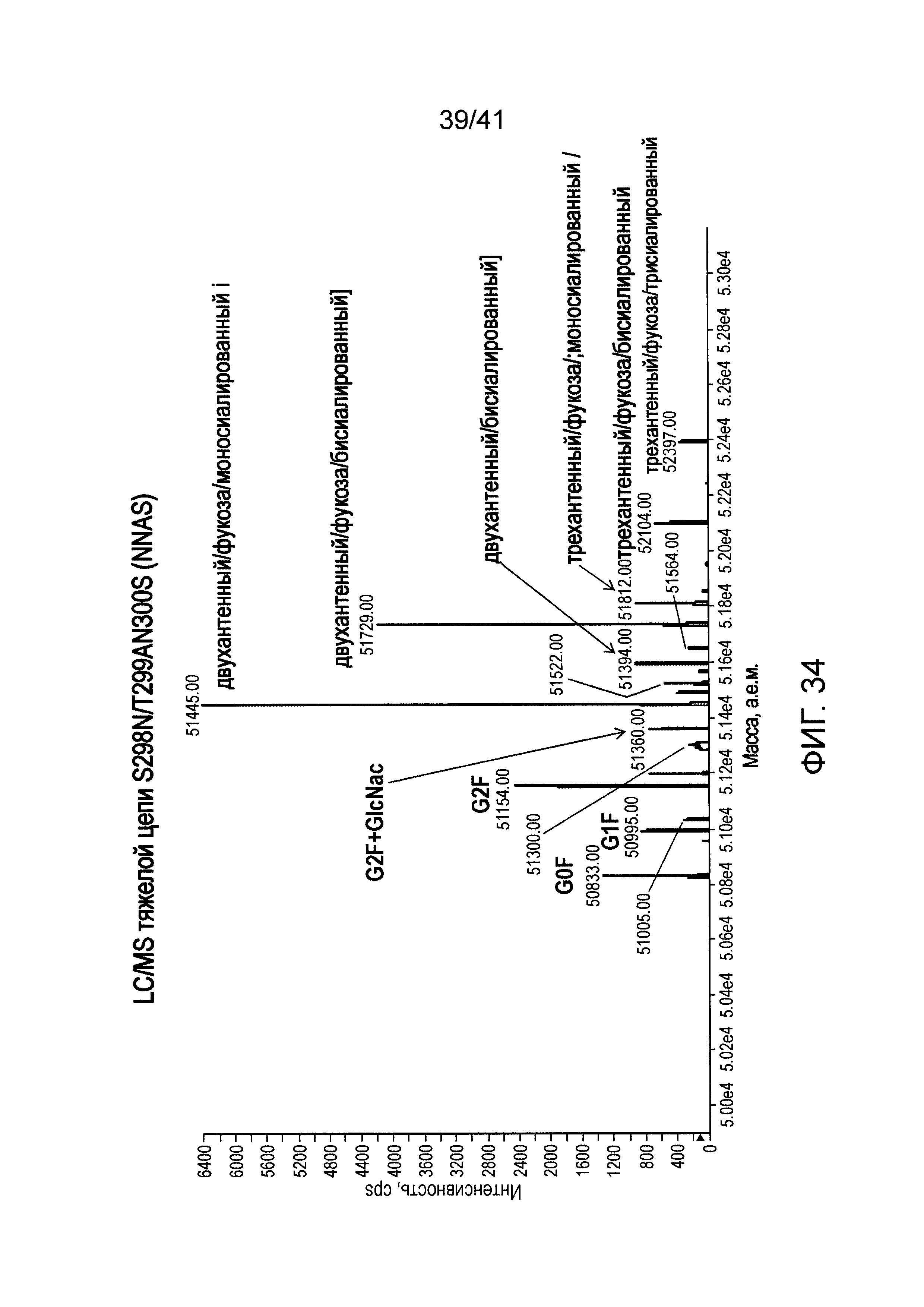
На фигуре 34 изображены результаты экспериментов LC-MS для определения содержания гликанов мутантного антитела анти-αβTCR, содержащего мутацию S298N/Y300S.
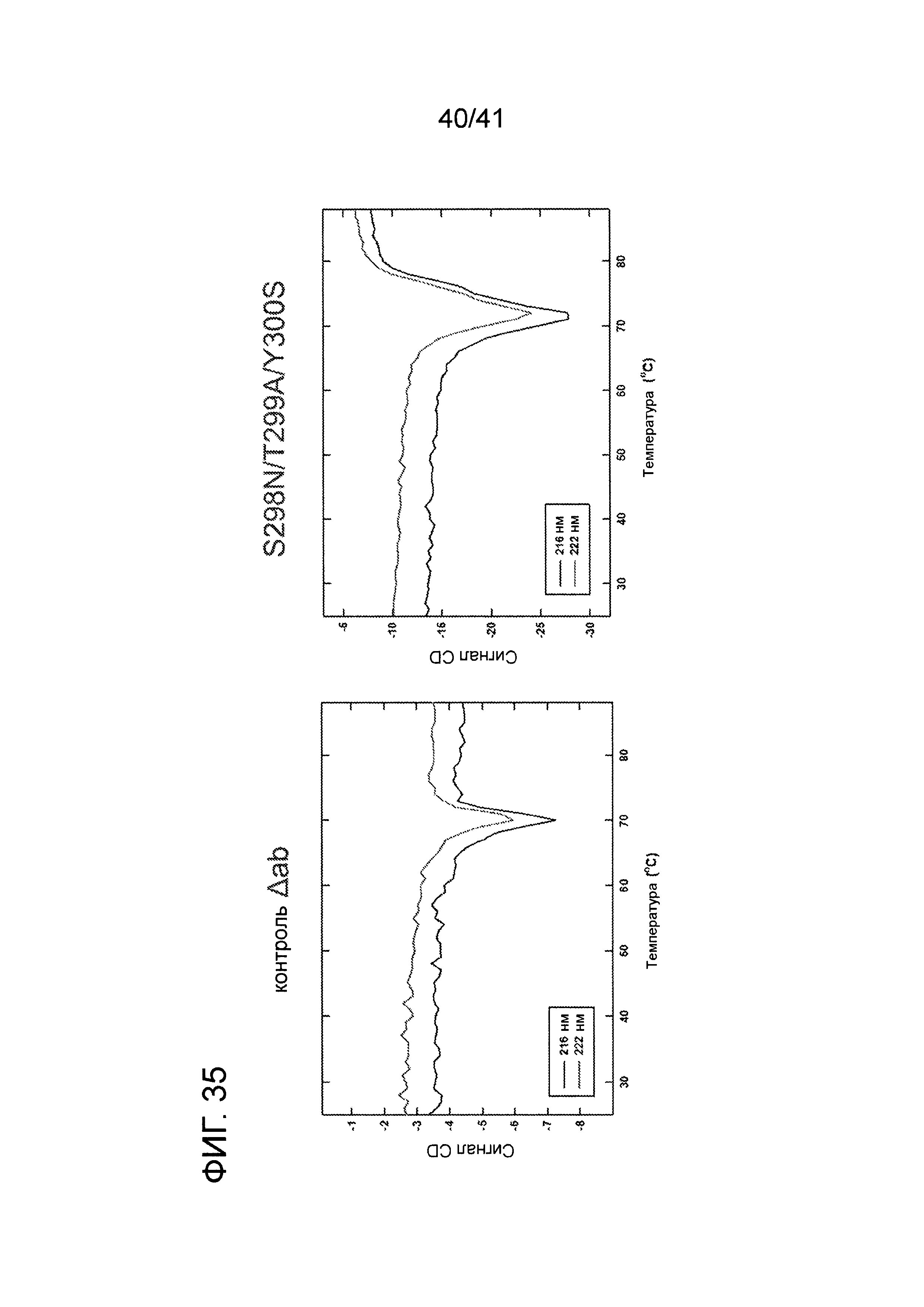
На фигуре 35 изображены результаты экспериментов кругового дихроизма для определения относительной термостабильности антитела анти-αβTCR дикого типа и мутантного антитела анти-αβTCR, содержащего мутацию S298N/Y300S.
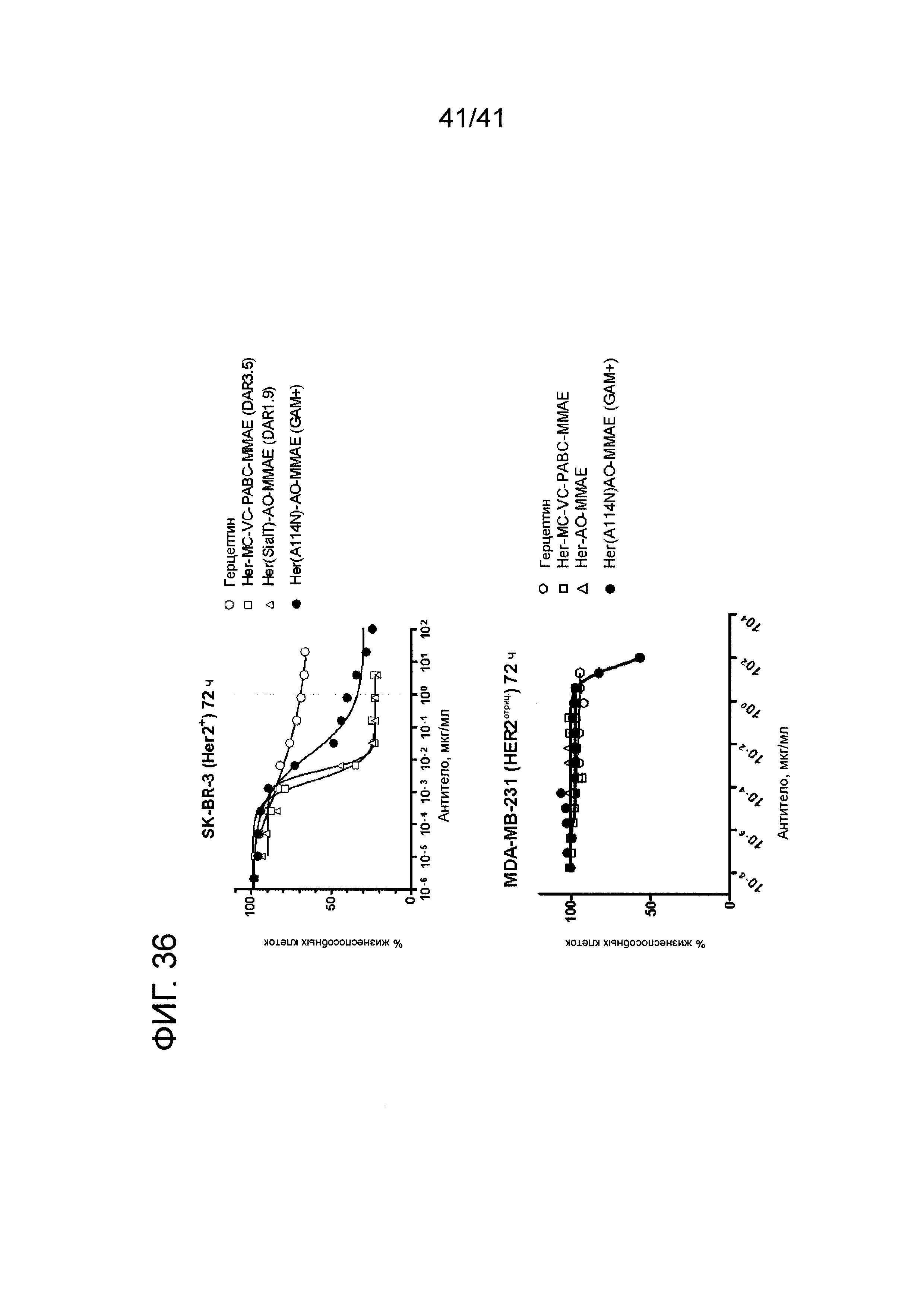
На фигуре 36 изображены результаты анализа пролиферации клеток для ADC, полученного с антителом анти-HER, несущим мутацию A114N с гипергликозилированием и AO-MMAE.
ПОДРОБНОЕ ОПИСАНИЕ
Настоящее описание относится к связывающим полипептидам (например, антителам) и их конъюгатам с эффекторной группой (например, конъюгатам с лекарственным средством). В конкретных вариантах осуществления конъюгаты содержат сайт-специфически сконструированную связь лекарственное средство-гликан в природных или сконструированных гликанах антигенсвязывающего полипептида, такого как молекула IgG. Настоящее описание относится также к нуклеиновым кислотам, кодирующим антигенсвязывающие полипептиды, рекомбинантным экспрессирующим векторам и клеткам-хозяевам для получения таких антигенсвязывающих полипептидов. Представлены также способы использования антигенсвязывающих полипептидов, описанных в настоящем документе, для лечения заболевания.
I. Определения
Как применяют в настоящем документе, термин «связывающий белок» или «связывающий полипептид» могут относится к полипептиду (например, антителу), содержащему по меньшей мере один участок связывания, являющийся ответственным за избирательное связывание с представляющим интерес антигеном-мишенью (например, антигеном человека). Иллюстративные участки связывания включают вариабельный домен антитела, участок связывания лиганда из рецептора или участок связывания рецептора из лиганда. В конкретных аспектах связывающие полипептиды по изобретению содержат множество (например, два, три, четыре или более) участков связывания.
Как применяют в настоящем документе, термин «природный остаток» может относиться к аминокислотному остатку, который встречается в природе в конкретном положении аминокислоты связывающего полипептида (например, антитела или его фрагмента) и который не был модифицирован, введен или изменен человеком. Как применяют в настоящем документе, термин «измененный связывающий белок» или «измененный связывающий полипептид» включает связывающие полипептиды (например, антитело или его фрагмент), содержащие по меньшей мере один неприродный мутантный аминокислотный остаток.
Термин «специфически связывает», как применяют в настоящем документе, относится к способности антитела или его антигенсвязывающего фрагмента связывать антиген с константой диссоциации (Kd) не более приблизительно 1 × 10-6 M, 1 × 10-7 M, 1 × 10-8 M, 1 × 10-9 M, 1 × 10-10 M, 1 × 10-11 M, 1 × 10-12 M или менее, и/или связывать антиген с аффинностью, по меньшей мере в два раза превышающей его аффинность для неспецифического антигена.
Как применяют в настоящем документе, термин «антитело» относится к таким соединениям (например, интактным молекулам антител, фрагментам антител или их вариантам), обладающим значительной известной иммунореактивной активностью для представляющего интерес антигена (например, опухолеассоциированного антигена). Антитела и иммуноглобулины содержат легкие и тяжелые цепи, с межцепьевой ковалентной связью между ними или без нее. Основные структуры иммуноглобулинов в системах позвоночных относительно хорошо известны.
Как более подробно обсуждают ниже, общий термин «антитело» включает пять различных классов антител, которые можно различать биохимически. В то время как все пять классов антител явно входят в объем настоящего описания, следующее обсуждение в основном направлено на класс IgG молекул иммуноглобулинов. В отношении IgG, иммуноглобулины содержат две идентичных легких цепи молекулярной массой приблизительно 23000 Дальтон и две идентичных тяжелых цепи молекулярной массой 53000-70000. Четыре цепи соединены дисульфидными связями в конфигурации «Y», где легкие цепи охватывают тяжелые цепи, начиная с сужения «Y» и продолжая на протяжении вариабельной области.
Легкие цепи иммуноглобулинов классифицируют как каппа либо лямбда (κ, λ). Каждый класс тяжелой цепи может быть связан либо с каппа, либо с лямбда легкой цепью. Как правило, легкие и тяжелые цепи ковалентно связаны друг с другом, и «хвостовые» части двух тяжелых цепей связаны друг с другом посредством ковалентных дисульфидных связей или нековалентных связей, когда иммуноглобулины получены посредством гибридом, B-клеток или полученных с помощью генной инженерии клеток-хозяев. В тяжелой цепи аминокислотные последовательности проходят от N-конца на раздвоенном конце конфигурации Y до C-конца внизу каждой цепи. Специалистам в данной области понятно, что тяжелые цепи классифицируют как гамма, мю, альфа, дельта или эпсилон, (γ, μ, α, δ, ε) с некоторыми подклассами среди них (например, γ1-γ4). Природа этой цепи является тем, что определяет «класс» антитела как IgG, IgM, IgA IgG или IgE, соответственно. Подклассы изотипов иммуноглобулинов (например, IgG1, IgG2, IgG3, IgG4, IgA1 и т.д.) хорошо охарактеризованы и, как известно, придают функциональную специализацию. Модифицированные варианты каждого из этих классов и изотипов легко может распознать специалист в данной области в свете настоящего описания и, соответственно, они входят в объем настоящего описания.
Как легкие, так и тяжелые цепи разделены на области структурной и функциональной гомологии. Термин «область» относится к части или порции цепи иммуноглобулина или антитела и включает константную область или вариабельные области, так же как более дискретные части или порции указанных областей. Например, вариабельные области легкой цепи включают «определяющие комплементарность области» или «CDR», вкрапленные в «каркасные области» или «FR», как определено в настоящем документе.
Области тяжелой или легкой цепи иммуноглобулина можно определять как «константную» (C) область или «вариабельные» (V) области, на основании относительного отсутствия разнообразия последовательности внутри областей различных членов класса в случае «константной области», или значительного разнообразия внутри областей различных членов класса в случае «вариабельных областей». Термины «константная область» и «вариабельная область» также можно использовать функционально. В этом отношении, следует понимать, что вариабельные области иммуноглобулина или антитела определяют узнавание антигена и специфичность. И наоборот, константные области иммуноглобулина или антитела придают важные эффекторные функции, такие как секреция, трансплацентарная подвижность, связывание Fc-рецептора, связывание комплемента и т.п. Субъединичные структуры и трехмерные конфигурации константных областей различных классов иммуноглобулинов хорошо известны.
Константные и вариабельные области тяжелых и легких цепей иммуноглобулинов свернуты в домены. Термин «домен» относится к глобулярной области тяжелой или легкой цепи, содержащей пептидные петли (например, содержащей 3-4 пептидные петли), стабилизированные, например, посредством β-складчатого листа и/или межцепьевой дисульфидной связи. Домены константной области легкой цепи иммуноглобулина обозначают взаимозаменяемо как «домены константной области легкой цепи», «области CL» или «домены CL». Константные домены на тяжелой цепи (например, шарнирном, CH1, CH2 или CH3 доменах) обозначают взаимозаменяемо как «домены константной области тяжелой цепи», домены области «CH» или «домены CH». Вариабельные домены на легкой цепи обозначают взаимозаменяемо как «домены вариабельной области легкой цепи», «домены области VL» или «домены VL». Вариабельные домены на тяжелой цепи обозначают взаимозаменяемо как «домены вариабельной области тяжелой цепи», «домены области VH» или «домены VH».
Обычно нумерация вариабельных доменов константной области увеличивается, когда они становятся более удаленными от антигенсвязывающего участка или амино-конца иммуноглобулина или антитела. N-конец каждой тяжелой и легкой цепи иммуноглобулина представляет собой вариабельную область, и на C-конце находится константная область; домены CH3 и CL действительно содержат карбокси-конец тяжелой и легкой цепи, соответственно. Соответственно, домены легкой цепи иммуноглобулина аранжированы в ориентации VL-CL, в то время как домены тяжелой цепи аранжированы в ориентации VH-CH1-шарнир-CH2-CH3.
Положения аминокислот в константной области тяжелой цепи, включая положения аминокислот в CH1, шарнирном, CH2, CH3 и CL доменах, можно нумеровать в соответствии с системой нумерации индексов Kabat (см. Kabat et al, в «Sequences of Proteins of Immunological Interest», U.S. Dept. Health and Human Services, 5th edition, 1991). Альтернативно, положения аминокислот антитела можно нумеровать в соответствии с системой нумерации индексов EU (см. Kabat et al, там же).
Как применяют в настоящем документе, термин «домен VH» включает аминоконцевой вариабельный домен тяжелой цепи иммуноглобулина, и термин «домен VL» включает аминоконцевой вариабельный домен легкой цепи иммуноглобулина.
Как применяют в настоящем документе, термин «домен CH1» включает первый (наиболее близкий к амино-концу) домен константной области тяжелой цепи иммуноглобулина, который продолжается, например, от приблизительно положений 114-223 в системе нумерации Kabat (положения EU 118-215). Домен CH1 является соседним к домену VH и находится на амино-конце от шарнирной области молекулы тяжелой цепи иммуноглобулина, и не формирует часть Fc-области тяжелой цепи иммуноглобулина.
Как применяют в настоящем документе, термин «шарнирная область» включает часть молекулы тяжелой цепи, соединяющую домен CH1 с доменом CH2. Эта шарнирная область содержит приблизительно 25 остатков и является гибкой, таким образом, позволяя двум N-концевым антигенсвязывающим областям двигаться независимо. Шарнирные области можно подразделять на три отдельных домена: верхний, средний и нижний шарнирный домены (Roux et al. J. Immunol. 1998, 161:4083).
Как применяют в настоящем документе, термин «домен CH2» включает часть тяжелой цепи молекулы иммуноглобулина, продолжающуюся, например, приблизительно от положений 244-360 в системе нумерации Kabat (положения EU 231-340). Домен CH2 является уникальным в том, что он не является близко спаренным с другим доменом. Вместо этого, две N-связанных разветвленных углеводных цепи вкраплены между двумя доменами CH2 интактной природной молекулы IgG. В одном варианте осуществления связывающий полипептид из настоящего описания содержит домен CH2, происходящий из молекулы IgG1 (например, молекулы IgG1 человека).
Как применяют в настоящем документе, термин «домен CH3» включает часть тяжелой цепи молекулы иммуноглобулина, продолжающуюся приблизительно 110 остатков от N-конца домена CH2, например, от приблизительно положений 361-476 системы нумерации Kabat (положения EU 341-445). Домен CH3, как правило, формирует C-концевую часть антитела. В некоторых иммуноглобулинах, однако, дополнительные домены могут продолжаться от домена CH3 для формирования C-концевой части молекулы (например, домен CH4 в цепи μ IgM и цепи ε IgE). В одном варианте осуществления связывающий полипептид по настоящему описанию содержит домен CH3, происходящий из молекулы IgG1 (например, молекулы IgG1 человека).
Как применяют в настоящем документе, термин «домен CL» включает домен константной области легкой цепи иммуноглобулина, продолжающийся, например, приблизительно от положения Kabat 107A-216. Домен CL является соседним с доменом VL. В одном варианте осуществления связывающий полипептид из настоящего описания содержит домен CL, происходящий из легкой цепи каппа (например, легкой цепи каппа человека).
Как применяют в настоящем документе, термин «область Fc» определяют как часть константной области тяжелой цепи, начинающуюся в шарнирной области непосредственно перед участком расщепления папаином (т.е. остатком 216 в IgG, принимая первый остаток константной области тяжелой цепи являющимся 114) и заканчивающуюся на C-конце антитела. Соответственно, полная область Fc содержит по меньшей мере шарнирный домен, домен CH2 и домен CH3.
Термин «природный Fc», как применяют в настоящем документе, относится к молекуле, содержащей последовательность не связывающего антиген фрагмента, полученную в результате расщепления антитела или полученную другими способами, либо в мономерной, либо в мультимерной форме, и могущую содержать шарнирную область. Исходный иммуноглобулиновый источник природного Fc предпочтительно имеет человеческое происхождение и может представлять собой любой из иммуноглобулинов, хотя IgG1 и IgG2 являются предпочтительными. Природные молекулы Fc состоят из мономерных полипептидов, которые могут быть связаны в димерные или мультимерные формы посредством ковалентной (т.е. дисульфидных связей) и нековалентной ассоциации. Количество межмолекулярных дисульфидных связей между мономерными субъединицами природных молекул Fc лежит в диапазоне от 1 до 4 в зависимости от класса (например, IgG, IgA и IgE) или подкласса (например, IgG1, IgG2, IgG3, IgA1 и IgGA2). Одним примером природного Fc является связанный дисульфидными связями димер, возникающий в результате расщепления папаином IgG. Термин «природный Fc», как применяют в настоящем документе, является общим для мономерных, димерных и мультимерных форм.
Термин «вариант Fc», как применяют в настоящем документе, относится к молекуле или последовательности, которая является модифицированной из природного Fc, но еще содержит участок связывания для рецептора спасения, FcRn (неонатального рецептора Fc). Иллюстративные варианты Fc и их взаимодействие с рецептором спасения известны в данной области. Таким образом, термин «вариант Fc» может включать молекулу или последовательность, являющуюся гуманизированной из не относящегося к человеку природного Fc. Более того, природный Fc содержит области, которые можно удалять, поскольку они обеспечивают структурные свойства или биологическую активность, которые не являются необходимыми для антителоподобных связывающих полипептидов по изобретению. Таким образом, термин «вариант Fc» включает молекулу или последовательность, в которой отсутствуют один или несколько природных участков или остатков Fc, или в которых модифицированы один или несколько участков или остатков Fc, которые влияют на: (1) формирование дисульфидной связи, (2) несовместимость с избранной клеткой-хозяином, (3) N-концевую гетерогенность при экспрессии в избранной клетке-хозяине, (4) гликозилирование, (5) взаимодействие с комплементом, (6) связывание рецептора Fc, отличного от рецептора спасения, или (7) антителозависимую клеточную цитотоксичность (ADCC), или вовлечены в них.
Термин «домен Fc», как применяют в настоящем документе, включает природный Fc и варианты и последовательности Fc, как определено выше. Как для вариантов Fc, так и для природных молекул Fc, термин «домен Fc» включает молекулы в мономерной или мультимерной форме, либо выщепленные из полноразмерного антитела, либо полученные другими способами.
Как указано выше, вариабельные области антитела позволяют ему избирательно узнавать и специфически связывать эпитопы на антигенах. То есть, домен VL и домен VH антитела объединяются для формирования вариабельной области (Fv), определяющей трехмерный антигенсвязывающий участок. Эта четверичная структура антитела формирует антигенсвязывающий участок, присутствующий на конце каждого плеча Y. Более конкретно, антигенсвязывающий участок определен тремя определяющими комплементарность областями (CDR) на каждой из вариабельных областей тяжелой и легкой цепи. Как применяют в настоящем документе, термин «антигенсвязывающий участок» включает участок, который специфически связывает антиген (является иммунореактивным для антигена) (например, антигена поверхности клеток или растворимого антигена). Антигенсвязывающий участок включает вариабельную область тяжелой цепи и легкой цепи иммуноглобулина, и участок связывания, сформированный этими вариабельными областями, определяет специфичность антитела. Антигенсвязывающий участок формируется вариабельными областями, которые меняются от одного антитела к другому. Измененные антитела по настоящему описанию содержат по меньшей мере один антигенсвязывающий участок.
В конкретных вариантах осуществления связывающие полипептиды по настоящему описанию содержат по меньшей мере два антигенсвязывающих домена, обеспечивающих ассоциацию связывающего полипептида с избранным антигеном. Антигенсвязывающие домены не обязательно должны происходить из одной и той же молекулы иммуноглобулина. В этом отношении, вариабельная область может происходить или происходит из любого типа животного, у которого можно индуцировать установление гуморального ответа и образование иммуноглобулинов против желательного антигена. В этой связи, вариабельная область связывающего полипептида может происходить, например, из относящегося к млекопитающим источника, например, может являться человеческой, мышиной, крысиной, козьей, овечьей, может происходить из нечеловекообразного примата (такого как яванские макаки, макаки и т.д.), волчьих или верблюдовых (например, из верблюдов, лам и родственных видов).
В природных антителах шесть CDR, присутствующих на каждом мономерном антителе, представляют собой короткие, не непрерывные последовательности аминокислот, которые специфически расположены для формирования антигенсвязывающего участка, когда антитело принимает его трехмерную конфигурацию в водном окружении. Для остальной части тяжелых и легких вариабельных доменов показана меньшая межмолекулярная изменчивость аминокислотной последовательности, и они названы каркасными областями. Каркасные области большей частью принимают конформацию β-листа, и CDR формируют петли, которые соединяют структуру β-листа, и в некоторых случаях формируют ее часть. Таким образом, эти каркасные области действуют для формирования каркаса, который обеспечивает расположение шести CDR в правильной ориентации посредством межцепьевых нековалентных взаимодействий. Антигенсвязывающий домен, сформированный расположенными CDR, определяет поверхность, комплементарную эпитопу на иммунореактивном антигене. Эта комплементарная поверхность стимулирует нековалентное связывание антитела с эпитопом иммунореактивного антигена.
Иллюстративные связывающие полипептиды по изобретению включают варианты антител. Как применяют в настоящем документе, термин «вариант антитела» включает синтетические и сконструированные формы антител, измененные таким образом, что они не встречаются в природе, например, антитела, которые содержат по меньшей мере две части тяжелой цепи, но не две полные тяжелые цепи (например, антитела с делетированным доменом или миниантитела); мультиспецифические формы антител (например, биспецифические, триспецифические и т.д.), измененные для связывания с двумя или более различными антигенами или с различными эпитопами на одном антигене); молекулы тяжелой цепи, соединенные с молекулами scFv, и т.п.. Кроме того, термин «вариант антитела» включает мультивалентные формы антител (например, трехвалентные, тетравалентные и т.д., антитела, которые связываются с тремя, четырьмя или более копиями одного и того же антигена.
Как применяют в настоящем документе, термин «валентность» относится к количеству потенциальных участков связывания мишеней в полипептиде. Каждый участок связывания мишени специфически связывает одну молекулу-мишень или специфический участок на молекуле-мишени. Когда полипептид содержит более одного участка связывания мишени, каждый участок связывания мишени может специфически связывать одинаковые или различные молекулы (например, может связываться с различными лигандами или различными антигенами, или различными эпитопами на одном и том же антигене). Рассматриваемые связывающие полипептиды предпочтительно обладают по меньшей мере одним участком связывания, специфическим для молекулы антигена человека.
Термин «специфичность» относится к способности специфически связываться с (например, вступать в иммунологическую реакцию с) данным антигеном-мишенью (например, с антигеном-мишенью человека). Связывающий полипептид может являться моноспецифическим и содержать один или несколько участков связывания, которые специфически связывают мишень, или полипептид может являться мультиспецифическим и содержать два или более участков связывания, которые специфически связывают одинаковые или различные мишени. В конкретных вариантах осуществления связывающий полипептид по изобретению является специфическим для двух различных (например, неперекрывающихся) частей одной и той же мишени. В конкретных вариантах осуществления, связывающий полипептид по изобретению является специфическим для более, чем одной мишени. Иллюстративные связывающие полипептиды (например, антитела), содержащие антигенсвязывающие участки, которые связываются с антигенами, экспрессированными на клетках опухолей, известны в данной области, и одну или несколько CDR из таких антител можно включать в антитело по изобретению.
Термин «связывающая группа» включает группы, способные связывать эффекторную группу со связывающими полипептидами, описанными в настоящем документе. Связывающую группу можно выбирать таким образом, что она является отщепляемой (например, ферментативно отщепляемой или pH-чувствительной) или неотщепляемой. Иллюстративные связывающие группы указаны в таблице 2 в настоящем документе.
Как применяют в настоящем документе, термин «эффекторная группа» включает средства (например, белки, нуклеиновые кислоты, липиды, углеводы, гликопептиды, группы лекарственного средства и их фрагменты) с биологической или другой функциональной активностью. Например, модифицированный связывающий полипептид, содержащий эффекторную группу, конъюгированную со связывающим полипептидом, обладает по меньшей мере одной дополнительной функцией или свойством по сравнению с неконъюгированным антителом. Например, конъюгация цитотоксического лекарственного средства (например, эффекторной группы) со связывающим полипептидом приводит к формированию связывающего полипептида с цитотоксичностью лекарственного средства в качестве второй функции (т.е. в дополнение к связыванию антигена). В другом примере, конъюгация второго связывающего полипептида со связывающим полипептидом может обеспечивать дополнительные связывающие свойства. В конкретных вариантах осуществления, где эффекторная группа представляет собой генетически кодированный терапевтический или диагностический белок или нуклеиновую кислоту, эффекторную группу можно синтезировать или экспрессировать посредством либо синтеза пептидов, либо способов рекомбинантной ДНК, которые хорошо известны в данной области. В другом аспекте, где эффекторная группа представляет собой негенетически кодированный пептид или группу лекарственного средства, эффекторную группу можно синтезировать искусственно или очищать из природного источника. Как применяют в настоящем документе, термин «группа лекарственного средства» включает противовоспалительные, противораковые, противоинфекционные (например, антигрибковые, антибактериальные, антипаразитические, антивирусные и т.д.), и анестетические лекарственные средства. В следующем варианте осуществления группа лекарственного средства представляет собой противораковое или цитотоксическое средство. Совместимые группы лекарственного средства могут также содержать пролекарства. Иллюстративные эффекторные группы указаны в таблице 1 в настоящем документе.
В конкретных вариантах осуществления, «эффекторная группа» включает «нацеливающую группу». Как применяют в настоящем документе, термин «нацеливающая группа» относится к эффекторной группе, которая связывается с молекулой-мишенью. Нацеливающие группы могут включать, без ограничения, белки, нуклеиновые кислоты, липиды, углеводы (например, гликаны) и их комбинации (например, гликопротеины, гликопептиды и гликолипиды).
Как применяют в настоящем документе, термин «пролекарство» относится к форме предшественника или производного фармацевтически активного средства, которая является менее активной, реакционноспособной или устойчивой к побочным эффектам по сравнению с исходным лекарственным средством и является способной подвергаться ферментативной активации или конвертации иным образом в более активную форму in vivo. Пролекарства, совместимые с композициями по настоящему описанию, включают, но без ограничения, содержащие фосфат пролекарства, содержащие аминокислоту пролекарства, содержащие тиофосфат пролекарства, содержащие сульфат пролекарства, содержащие пептид пролекарства, содержащие β-лактам пролекарства, содержащие необязательно замещенный феноксиацетамид пролекарства или содержащие необязательно замещенный фенилацетамид пролекарства, 5-фторцитозин и другие 5-фторуридиновые пролекарства, которые можно конвертировать в более активное цитотоксическое свободное лекарственное средство. Специалист в данной области может выполнять химические модификации желательной группы лекарственного средства или его пролекарства, чтобы сделать реакции этого соединения более пригодными для целей получения модифицированных связывающих полипептидов по настоящему описанию. Группы лекарственного средства включают также производные, фармацевтически приемлемые соли, сложные эфиры, амиды и простые эфиры групп лекарственного средства, описанных в настоящем документе. Производные включают модификации лекарственных средств, идентифицированных в настоящем документе, которые могут улучшать или не снижают значительно конкретную желательную терапевтическую активность лекарственного средства.
Как применяют в настоящем документе, термин «противораковое средство» включает средства, которые являются вредными для роста и/или пролиферации неопластических клеток или клеток опухолей и могут действовать для снижения, ингибирования или разрушения злокачественного новообразования. Примеры таких средств включают, но без ограничения, цитостатические средства, алкилирующие средства, антибиотики, цитотоксические нуклеозиды, связывающие тубулин вещества, гормоны, антагонисты гормонов, цитотоксические средства и т.п. Цитотоксические средства включают производные томаймицина, производные майтанзина, производные криптофицина, производные антрациклина, производные бисфосфоната, производные лептомицина, производные стрептонигрина, производные ауристатина и производные дуокармицина. Любое средство, действующее для задержки или замедления роста иммунореактивных клеток или злокачественных клеток, входит в объем настоящего описания.
Термин «антиген» или «антиген-мишень», как применяют в настоящем документе, относится к молекуле или части молекулы, способной быть связанной участком связывания связывающего полипептида. Антиген-мишень может обладать одним или несколькими эпитопами.
II. Связывающие полипептиды
В одном аспекте настоящее описание относится к связывающим полипептидам (например, антителам, фрагментам антител, вариантам антител и слитым белкам), содержащим гликозилированный домен, например, a гликозилированный константный домен. Связывающие полипептиды, описанные в настоящем документе, включают любой связывающий полипептид, содержащий домен, обладающий участком N-связанного гликозилирования. В конкретных вариантах осуществления связывающий полипептид представляет собой антитело, или его фрагмент или производное. Любое антитело из любого источника или видов можно использовать в связывающих полипептидах, описанных в настоящем документе. Пригодные антитела включают в себя, без ограничения, человеческие антитела, гуманизированные антитела или химерные антитела.
В конкретных вариантах осуществления гликозилированный домен представляет собой домен Fc. В конкретных вариантах осуществления гликозилированный домен представляет собой домен с пиродным гликозилированием на N297.
В других вариантах осуществления гликозилированный домен представляет собой сконструированный гликозилированный домен. Иллюстративные сконструированные гликозилированные домены в домене Fc содержат остаток аспарагина в положении аминокислоты 298 в соответствии с нумерацией EU; и остаток серина или треонина в положении аминокислоты 300, в соответствии с нумерацией EU.
Домены Fc из любого класса (например, IgM, IgG, IgD, IgA и IgE) и видов иммуноглобулинов можно использовать в связывающих полипептидах, описанных в настоящем документе. Химерные домены Fc, содержащие части доменов Fc из различных видов или классов Ig, также можно использовать. В конкретных вариантах осуществления домен Fc представляет собой домен Fc IgG1 человека. В случае домена Fc IgGl человека, мутация аминокислоты дикого типа в положении Kabat 298 до аспарагина и в положении Kabat 300 до серина или треонина приводит к формированию консенсусного участка N-связанного гликозилирования (т.е. сиквона N-X-T/S сиквон, где X представляет собой любую аминокислоту, кроме пролина). Однако, в случае доменов Fc из других видов, и/или классов или изотипов Ig, специалисту в данной области понятно, что может быть необходимо вносить мутации в положении Kabat 299 домена Fc, если присутствует остаток пролина, для восстановлния сиквона N-X-T/S.
В других вариантах осуществления настоящее описание относится к связывающим полипептидам (например, антителам, фрагментам антител, вариантам антител и слитым белкам), содержащим по меньшей мере один домен CH1, обладающий участком N-связанного гликозилирования. Такие иллюстративные связывающие полипептиды могут содержать, например, и сконструированный участок гликозилирования в положении 114, в соответствии с нумерацией Kabat.
Домены CH1 из любого класса (например, IgM, IgG, IgD, IgA и IgE) и видов иммуноглобулинов можно использовать в связывающих полипептидах, описанных в настоящем документе. Химерные домены CH1, содержащие части доменов CH1 из различных видов или классов Ig, также можно использовать. В конкретных вариантах осуществления домен CH1 представляет собой домен CH1 IgG1 человека. В случае домена IgG1 человека, мутация аминокислоты дикого типа в положении 114 до аспарагина приводит к формированию консенсусного участка N-связанного гликозилирования (т.е. сиквона N-X-T/S, где X представляет собой любую аминокислоту, кроме пролина). Однако, в случае других доменов CH1 из других видов, и/или классов или изотипов Ig, специалисту в данной области понятно, что может быть необходимо вносить мутации в положения 115 и/или 116 домена CH1 для получения сиквона N-X-T/S.
В конкретных вариантах осуществления связывающий полипептид по настоящему описанию может содержать антигенсвязывающий фрагмент антитела. Термин «антигенсвязывающий фрагмент» относится к полипептидному фрагменту иммуноглобулина или антитела, который связывает антиген или конкурирует с интактным антителом (т.е. с интактным антителом, из которого они происходят) за связывание антигена (т.е. специфическое связывание). Антигенсвязывающие фрагменты можно получать рекомбинантными или биохимическими способами, которые хорошо известны в данной области. Иллюстративные антигенсвязывающие фрагменты включают Fv, Fab, Fab' и (Fab')2. В предпочтительных вариантах осуществления, антигенсвязывающий фрагмент по настоящему описанию представляет собой измененный антигенсвязывающий фрагмент, содержащий по меньшей мере один сконструированный участок гликозилирования. В одном иллюстративном варианте осуществления измененный антигенсвязывающий фрагмент по настоящему описанию содержит измененный домен VH, описанный выше. В другом иллюстративном варианте осуществления измененный антигенсвязывающий фрагмент по настоящему описанию содержит измененный домен CH1, описанный выше.
В иллюстративных вариантах осуществления связывающий полипептид содержит последовательность одноцепочечной вариабельной области (ScFv). Последовательности одноцепочечной вариабельной области содержат отдельный полипептид, обладающий одним или несколькими антигенсвязывающими участками, например, доменом VL, связанным с гибким линкером с доменом VH. Молекулы ScFv можно конструировать в ориентации VH-линкер-VL или в ориентации VL-линкер-VH. Гибкий шарнир, связывающий домены VL и VH, которые составляют антигенсвязывающий участок, предпочтительно содержит от приблизительно 10 до приблизительно 50 аминокислотных остатков. Соединяющие пептиды известны в данной области. Связывающий полипептид по изобретению может содержать по меньшей мере один scFv и/или по меньшей мере одну константную область. В одном варианте осуществления связывающий полипептид по настоящему описанию может содержать по меньшей мере один scFv, связанный или слитый с антителом или фрагментом, содержащим домен CH1 (например, домен CH1, содержащий остаток аспарагина в положении Kabat 114) и/или домен CH2 (например, домен CH2, содержащий остаток аспарагина в положении EU 298, и остаток серина или треонина в положении EU 300).
В конкретных иллюстративных вариантах осуществления связывающий полипептид по настоящему описанию представляет собой мультивалентное (например, тетравалентное) антитело, которое получено слиянием последовательности ДНК, кодирующей антитело, с молекулой ScFv (например, измененной молекулой ScFv). Например, в одном варианте осуществления, эти последовательности скомбинированы так, что молекула ScFv (например, измененная молекула ScFv) связана на ее N-конце или C-конце с фрагментом Fc антитела через гибкий линкер (например, линкер gly/ser). В другом варианте осуществления тетравалентное антитело по настоящему описанию можно получать слиянием молекулы ScFv с соединительным пептидом, слитым с доменом CH1 (например, доменом CH1, содержащим остаток аспарагина в положении Kabat 114), для конструирования тетравалентной молекулы ScFv-Fab.
В другом варианте осуществления связывающий полипептид по настоящему описанию представляет собой измененное миниантитело. Измененные миниантитела по настоящему описанию представляют собой димерные молекулы, состоящие из двух полипептидных цепей, где каждая содержит молекулу ScFv (например, измененную молекулу ScFv, содержащую домен VH, описанный выше), слитую с доменом CH3 или его частью через соединительный пептид. Миниантитела можно получать посредством конструирования компонента ScFv и соединения компонентов пептид-CH3 с использованием способов, описанных в данной области (см., например, патент США 5837821 или WO 94/09817Al). В другом варианте осуществления, можно конструировать тетравалентное миниантитело. Тетравалентные миниантитела можно конструировать таким же способом, как миниантитела, за исключением того, что две молекулы ScFv связывают с использованием гибкого линкера. Связанную конструкцию scFv-scFv затем соединяют с доменом CH3.
В другом варианте осуществления связывающий полипептид по настоящему описанию содержит диатело. Диатела представляют собой димерные, тетравалентные молекуламолекулы, где каждая обладает полипептидом, сходным с молекулами scFv, но обычно обладает коротким линкером из аминокислотных остатков (менее 10 и предпочтительно 1-5), соединяющим оба вариабельных домена, так что домены VL и VH на одной и той же полипептидной цепи не могут взаимодействовать. Вместо этого, домен VL и VH одной полипептидной цепи взаимодействуют с доменом VH и VL (соответственно) на второй полипептидной цепи (см., например, WO 02/02781). Диатела по настоящему описанию содержат молекулу scFv, слитую с доменом CH3.
В других вариантах осуществления связывающие полипептиды по изобретению содержат мультиспецифические или мультивалентные антитела, содержащие один или несколько вариабельных доменов в сериях на одной и той же полипептидной цепи, например, полипептиды тандемных вариабельных доменов (TVD). Иллюстративные полипептиды TVD включают конфигурацию «двойной головки» или «двойного Fv», описанные в Патенте США № 5989830. В конфигурации двойного Fv, вариабельные домены двух различных антител экспрессированы в тандемной ориентации на двух отдельных цепях (одной тяжелой цепи и одной легкой цепи), где одна полипептидная цепь обладает двумя доменами VH в сериях, разделенных пептидным линкером (VH1-линкер-VH2), и другая полипептидная цепь состоит из комплементарных доменов VL, соединенных в сериях пептидным линкером (VL1-линкер-VL2). В конфигурации перекрестной двойной головки, вариабельные домены двух различных антител экспрессированы в тандемной ориентации на двух отдельных полипептидных цепях (одной тяжелой цепи и одной легкой цепи), где одна полипептидная цепь обладает двумя доменами VH в сериях, разделенных пептидным линкером (VH1-линкер-VH2), и другая полипептидная цепь состоит из комплементарных доменов VL, соединенных в сериях пептидным линкером в обратной ориентации (VL2-линкер-VL1). Дополнительные варианты антител на основе формата «двойного-Fv» включает биспецифическое антитело IgG с двойным-вариабельным-доменом (DVD-IgG) (см. Патент США № 7612181, и формат TBTI (см. US 2010/0226923 A1). Добавление константных доменов к соответствующим цепям двойного Fv (CH1-Fc к тяжелой цепи и константного домена каппа или лямбда - к легкой цепи) приводит к функциональным биспецифическим антителам без какой-либо необходимости дополнительных модификаций (т.е. очевидного добавления константных доменов для усиления стабильности).
В другом иллюстративном варианте осуществления связывающий полипептид содержит биспецифическое антитело IgG с перекрестным двойным вариабельным доменом (CODV-IgG) на основе конфигурации «двойной головки» (см. US20120251541 A1, приведенной в настоящем документе путем ссылки в полном объеме). Варианты антитела CODV-IgG обладают одной полипептидной цепью с доменами VL, соединенных в сериях с доменом CL (VL1-L1-VL2-L2-CL), и второй полипептидной цепью с комплементарными доменами VH, соединенными в сериях в обратной ориентации к домену CH1 (VH2-L3-VH1-L4-CH1), где полипептидные цепи формируют перекрестную пару легкая цепь-тяжелая цепь. В конкретном варианте осуществления, второй полипептид можно дополнительно соединять с доменом Fc (VH2-L3-VH1-L4-CH1-Fc). В конкретных вариантах осуществления линкер L3 по меньшей мере в два раза превышает длину линкера L1, и/или линкер L4 по меньшей мере в два раза превышает длину линкера L2. Например, L1 и L2 могут составлять в длину 1-3 аминокислотных остатка, L3 может составлять в длину 2-6 аминокислотных остатков, и L4 может составлять в длину 4-7 аминокислотных остатков. Примеры пригодных линкеров включают отдельный остаток глицина (Gly); пептид диглицина (Gly-Gly); трипептид (Gly-Gly-Gly); пептид с четырьмя остатками глицина (Gly-Gly-Gly-Gly); пептид с пятью остатками глицина (Gly-Gly-Gly-Gly-Gly); пептид с шестью остатками глицина (Gly-Gly-Gly-Gly-Gly-Gly); пептид с семью остатками глицина (Gly-Gly-Gly-Gly-Gly-Gly-Gly); пептид с восемью остатками глицина (Gly-Gly-Gly-Gly-Gly-Gly-Gly-Gly). Можно использовать другие комбинации аминокислотных остатков, такие как пептид Gly-Gly-Gly-Gly-Ser и пептид Gly-Gly-Gly-Gly-Ser-Gly-Gly-Gly-Gly-Ser.
В конкретных вариантах осуществления связывающий полипептид содержит молекулу иммуноадгезина, содержащую не относящуюся к антителу связывающую область (например, рецептор, лиганд или молекулу клеточной адгезии), слитую с константной областью антитела (см. например, Ashkenazi et al., Methods, 1995 8(2), 104-115, полное содержание которого приведено в настоящем документе путем ссылки).
В конкретных вариантах осуществления связывающий полипептид содержит иммуноглобулиноподобные домены. Пригодные иммуноглобулиноподобные домены включают, без ограничения, домены фибронектина (см., например, Koide et al. (2007), Methods Mol. Biol. 352: 95-109, полное содержание которого приведено в настоящем документе путем ссылки), DARPin (см., например, Stumpp et al. (2008) Drug Discov. Today 13 (15-16): 695-701, полное содержание которого приведено в настоящем документе путем ссылки), Z домены белка A (см., Nygren et al. (2008) FEBS J. 275 (11): 2668-76, полное содержание которого приведено в настоящем документе путем ссылки), Lipocalins (см., например, Skerra et al. (2008) FEBS J. 275 (11): 2677-83, полное содержание которого приведено в настоящем документе путем ссылки), аффилины (см., например, Ebersbach et al. (2007) J. Mol. Biol. 372 (1): 172-85, полное содержание которого приведено в настоящем документе путем ссылки), аффитины (см., например, Krehenbrink et al. (2008). J. Mol. Biol. 383 (5): 1058-68, полное содержание которого приведено в настоящем документе путем ссылки), авимеры (см., например, Silverman et al. (2005) Nat. Biotechnol. 23 (12): 1556-61, полное содержание которого приведено в настоящем документе путем ссылки), финомеры, (см., например, Grabulovski et al. (2007) J Biol Chem 282 (5): 3196-3204, полное содержание которого приведено в настоящем документе путем ссылки), и пептиды с доменом Куница (см., например, Nixon et al. (2006) Curr Opin Drug Discov Devel 9 (2): 261-8, полное содержание которого приведено в настоящем документе путем ссылки).
III. N-связанные гликаны
В конкретных вариантах осуществления в связывающих полипептидах по изобретению используют N-связанные гликаны, которые являются «N-связанными» через остаток аспарагина с участком гликозилирования в полипептидном остове связывающего полипептида. Участок гликозилирования может представлять собой природный или сконструированный участок гликозилирования. Кроме того или альтернативно, гликан может представлять собой природный гликан или сконструированный гликан, содержащий неприродные связи.
В конкретных иллюстративных вариантах осуществления связывающий полипептид по изобретению содержит природный участок гликозилирования домена Fc антитела. Этот природный участок гликозилирования содержит остаток аспарагина дикого типа в положении 297 домена Fc (N297), в соответствии с нумерацией EU. Природный N-связанный гликан, расположенный в этом положении, как правило, связан через β-гликозиламидную связь с группой азота боковой цепи N297. Однако, можно также использовать другие известные в данной области связи. В других иллюстративных вариантах осуществления связывающие полипептиды по изобретению содержат один или несколько сконструированных участков гликозилирования. Такие сконструированные участки гликозилирования содержат замену одной или нескольких аминокислот дикого типа в полипептидном остове связывающего полипептида на остаток аспарагина, способный подвергаться N-гликозилированию посредством ферментов клетки для гликозилирования. Иллюстративные сконструированные участки гликозилирования по изобретению включают введение мутации до аспарагина в положении аминокислоты 298 домена Fc (298N) или в положении аминокислоты 114 домена CH1 (114N).
Любой тип природного или синтетического (т.е. неприродного) N-связанного гликана может быть связан с участком гликозилирования связывающего полипептида по изобретению. В конкретных вариантах осуществления, гликан содержит сахарид (например, остаток сахарида, локализованный на конце олигосахарида), который можно окислять (например, посредством обработки периодатом или оксидазой галактозы) для получения группы, пригодной для конъюгации с эффекторной группой (например, реакционноспособной альдегидной группы). Пригодные поддающиеся окислению сахариды включают, без ограничения, галактозу и сиаловую кислоту (например, N-Ацетилнейраминовую кислоту). В конкретных вариантах осуществления гликан представляет собой двухантенный гликан. В конкретных вариантах осуществления гликан представляет собой природную гликоформу млекопитающих.
Гликозилирования можно достигать любыми способами, известными в данной области. В конкретных вариантах осуществления гликозилирования достигают посредством экспрессии связывающих полипептидов в клетках, способных к N-связанному гликозилированию. Можно использовать любую природную или сконструированную клетку (например, прокариотическую или эукариотическую). Как правило, клетки млекопитающих используют для эффекта гликозилирования. N-гликаны, продуцированные в клетках млекопитающих обычно обозначают как комплексные N-гликаны (см. например, Drickamer K, Taylor ME (2006). Introduction to Glycobiology, 2nd ed., полное содержание которого приведено в настоящем документе путем ссылки). Эти комплексные N-гликаны обладают структурой, которая, как правило, имеет от двух до шести внешних ветвей с последовательностью сиалиллактозамина, связанными с внутренней коровой структурой Man3GlcNAc2. Комплексный N-гликан обладает по меньшей мере одной ветвью, и предпочтительно, по меньшей мере двумя, из перемежающихся остатков GlcNAc и галактозы (Gal), заканчивающихся олигосахаридами, например, такими как: NeuNAc-; NeuAc α2,6 GalNAc α1-; NeuAc α2,3 Gal.бета.1 3 GalNAc α 1-; и NeuAc α.2,3/6 Gal β1,4 GlcNAc β1.; Кроме того, сульфатные сложные эфиры могут возникать на остатках галактозы, GalNAc и GlcNAc, и фосфаные сложные эфиры могут возникать на остатках маннозы. NeuAc может являться O-ацетилированным или замененным NeuGl (N-гликолилнейраминовая кислота). Комплексные N-гликаны могут также обладать внутрицепьевыми заменами GlcNAc в точках ветвления и коровой фукозы (Fuc).
Дополнительно или альтернативно, гликозилирование можно осуществлять или модифицировать посредством ферментативных способов, in vitro. Например, одну или несколько гликозилтрансфераз можно использовать для добавления специфических сахаридных остатков к N114, и одну или несколько гликозидаз можно использовать для удаления нежелательных сахаридов из N-связанного гликана. Такие ферментативные способы хорошо известны в данной области (см.. например, WO/2007/005786, полное содержание которого приведено в настоящем документе путем ссылки).
IV. Иммунологические эффекторные функции и модификации Fc
В конкретных вариантах осуществления связывающие полипептиды по изобретению могут содержать константную область антитела (например, константную область IgG, например, константную область IgG человека, например, константную область IgG1 или IgG4 человека), опосредующие одну или несколько эффекторных функций. Например, связывание C1-комплекса с константной областью антитела может активировать систему комплемента. Активация системы комплемента является важной в опсонизации и лизисе клеточных патогенов. Активация системы комплемента также стимулирует воспалительный ответ и может также быть вовлечена в аутоиммунную гиперчувствительность. Кроме того, антитела связываются с рецепторами на различных клетках через область Fc (участки связывания Fc-рецептора на области Fc антитела связываются с Fc-рецепторами (FcR) на клетке). Существует ряд Fc-рецепторов, которые являются специфическими для различных классов антител, включая IgG (рецепторы гамма), IgE (рецепторы эпсилон), IgA (рецепторы альфа) и IgM (рецепторы мю). Связывание антитела с Fc-рецепторами на поверхности клетки запускает ряд важных и разнообразных биологических ответов, включая поглощение и разрушение покрытых антителами частиц, вывод иммунных комплексов, лизис покрытых антителами клеток-мишеней посредством клеток-киллеров (называемый антителозависимой опосредованной клеткам цитотоксичностью, или ADCC), высвобождение медиаторов воспаления, перенос через плаценту и контроль продукции иммуноглобулинов. В предпочтительных вариантах осуществления, связывающие полипептиды (например, антитела или их антигенсвязывающие фрагменты) по изобретению связываются с рецептором Fc-гамма. В альтернативных вариантах осуществления, связывающие полипептиды по изобретению могут содержать константную область, которая лишена одной или нескольких эффекторных функций (например, активности ADCC) и/или неспособна связывать рецептор Fcγ.
Конкретные варианты осуществления изобретения включают антитела, в которых по меньшей мере одна аминокислота в одном или нескольких доменах константной области делетирована или иным образом изменена так, чтобы обеспечивать желательные биохимические характеристики, такие как сниженные или усиленные эффекторные функции, способность к нековалентной димеризации, увеличенная способность к локализации в участке опухоли, сниженное время полужизни в сыворотке или увеличенное время полужизни в сыворотке по сравнению с полноразмерным, неизмененным антителом приблизительно такой же иммуногенности. Например, конкретные антитела для использования в способах диагностики и лечения, описанных в настоящем документе, представляют собой антитела с делетированным доменом, содержащие полипептидную цепь, сходную с тяжелой цепью иммуноглобулина, но лишенной по меньшей мере части одного или нескольких доменов тяжелой цепи. Например, в конкретных антителах, один целый домен константной области модифицированного антитела может быть делетирован, например, весь или часть домена CH2 может быть делетирован.
В других конкретных вариантах осуществления связывающие полипептиды содержат константные области, происходящие из различных изотипов антител (например, константные области из двух или более IgG1, IgG2, IgG3 или IgG4 человека). В других вариантах осуществления связывающие полипептиды содержат химерный шарнир (т.е. шарнир, содержащий части шарнира, происходящие из шарнирных доменов различных изотипов антитела, например, верхнего шарнирного домена из молекулы IgG4 и среднего шарнирного домена IgG1). В одном варианте осуществления связывающие полипептиды содержат область Fc или ее часть из молекулы IgG4 человека, и мутацию Ser228Pro (нумерация EU) в коровой шарнирной области молекулы.
В конкретных вариантах осуществления часть Fc можно подвергать мутации для увеличения или уменьшения эффекторной функции с использованием способов, известных в данной области. Например, делеция или инактивация (посредством точечных мутаций или других способов) домена константной области может уменьшать связывание Fc-рецептора циркулирующего модифицированного антитела, таким образом, расширяя локализацию опухоли. В других случаях может быть, что модификации константной области, в соответствии с настоящим изобретением, смягчают связывание комплемента и таким образом, уменьшают время полужизни в сыворотке и неспецифическую ассоциацию конъюгированного цитотоксина. Другие модификации константной области можно использовать для модификации дисульфидных связей или олигосахаридных групп, позволяющих расширенную локализацию из-за увеличенной антигенной специфичности или гибкости. Полученный физиологический профиль, биодоступность и другие биохимические эффекты модификаций, такие как локализация в опухоли, биораспределение и время полужизни в сыворотке, легко можно измерять и оценивать количественно с использованием хорошо известных иммунологических способов без излишнего экспериментирования.
В конкретных вариантах осуществления домен Fc, используемый в антителе по изобретению представляет собой вариант Fc. Как применяют в настоящем документе, термин «вариант Fc» относится к домену Fc, обладающему по меньшей мере одной аминокислотной заменой относительно домена Fc дикого типа, из которого происходит указанный домен Fc. Например, когда домен Fc происходит из антитела IgG1 человека, вариант домен Fcа Fc указанного IgG1 человека содержит по меньшей мере одну аминокислотную замену относительно указанного домена Fc.
Аминокислотная замена(замены) варианта Fc может являться локализованной в любом положении (т.е. любом положении аминокислоты по конвенции EU) внутри домена Fc. В одном варианте осуществления вариант Fc содержит замену в положении аминокислоты, локализованном в шарнирном домене или его части. В другом варианте осуществления вариант Fc содержит замену в положении аминокислоты, локализованном в домене CH2 или его части. В другом варианте осуществления вариант Fc содержит замену в положении аминокислоты, локализованном в домене CH3 или его части. В другом варианте осуществления вариант Fc содержит замену в положении аминокислоты, локализованном в домене CH4 или его части.
В связывающих полипептидах по изобретению можно использовать любой известный в данной области вариант Fc, как известно, вносящий вклад в улучшении (например, снижении или усилении) эффекторной функции и/или связывания FcR. Указанные варианты Fc могут включать, например, любую из аминокислотных замен, описанных в Международных Публикациях PCT WO88/07089A1, WO96/14339A1, WO98/05787A1, WO98/23289A1, WO99/51642A1, WO99/58572A1, WO00/09560A2, WO00/32767A1, WO00/42072A2, WO02/44215A2, WO02/060919A2, WO03/074569A2, WO04/016750A2, WO04/029207A2, WO04/035752A2, WO04/063351A2, WO04/074455A2, WO04/099249A2, WO05/040217A2, WO05/070963A1, WO05/077981A2, WO05/092925A2, WO05/123780A2, WO06/019447A1, WO06/047350A2 и WO06/085967A2 или в патентах США №№ 5648260; 5739277; 5834250; 5869046; 6096871; 6121022; 6194551; 6242195; 6277375; 6528624; 6538124; 6737056; 6821505; 6998253; и 7083784, полное содержание каждого из которых приведено в настоящем документе путем ссылки. В одном иллюстративном варианте осуществления связывающий полипептид по изобретению может содержать вариант Fc, содержащий аминокислотную замену в положении EU 268 (например, H268D или H268E). В другом иллюстративном варианте осуществления связывающий полипептид по изобретению может содержать аминокислотную замену в положении EU 239 (например, S239D или S239E) и/или положении EU 332 (например, I332D или I332Q).
В конкретных вариантах осуществления связывающий полипептид по изобретению может содержать вариант Fc, содержащий аминокислотную замену, изменяющую антигеннезависимые эффекторные функции антитела, в частности, время полужизни циркулирующего связывающего полипептида. Такие связывающие полипептиды обладают либо увеличенным, либо уменьшенным связыванием с FcRn по сравнению со связывающими полипептидами с отсутствием этих замен, таким образом, обладают увеличенным или уменьшенным временем полужизни в сыворотке, соответственно. Предполагают, что варианты Fc с улучшенной аффинностью для FcRn обладают более длительными периодами полужизни в сыворотке, и такие молекулы обладают пригодными применениями в способах лечения млекопитающих, где является желательным длительное время полужизни введенного антитела, например, для лечения хронического заболевания или нарушения. В отличие от этого, ожидают, что варианты Fc с уменьшенной аффинностью связывания FcRn обладают более короткими периодами времени полужизни, и такие молекулы также можно использовать, например, для введения млекопитающему, когда более короткое время циркуляции может предоставлять преимущества, например, для получения диагностических изображений in vivo, или в ситуациях, когда исходное антитело обладает токсическими побочными эффектами при присутствии в кровотоке в течение более длительных периодов. Варианты Fc с уменьшенной аффинностью связывания FcRn также менее вероятно пересекают плаценту и, таким образом, их можо также использовать для лечения заболеваний или нарушений у беременных женщин. Кроме того, другие применения, в которых может являться желательной сниженная аффинность связывания FcRn, включают применения, локализованные в мозге, почке и/или печени. В одном иллюстративном варианте осуществления для измененных связывающих полипептидов (например, антител или их антигенсвязывающих фрагментов) по изобретению показан сниженный транспорт через эпителий гломерул почек из сосудистой сети. В другом варианте осуществления для измененных связывающих полипептидов (например, антител или их антигенсвязывающих фрагментов) по изобретению показан сниженный транспорт через гематоэнцефалический барьер (BBB) из головного мозга в просвет сосуда. В одном варианте осуществления антитело с измененным связыванием FcRn содержит домен Fc, обладающий одной или несколькими аминокислотными заменами внутри «связывающей FcRn петли» домена Fc. Связывающая FcRn петля состоит из аминокислотных остатков 280-299 (в соответствии с нумерацией EU). Иллюстративные аминокислотные замены, которые изменяют активность связывания FcRn, описаны в Международной публикации PCT № WO05/047327, полное содержание которой приведено в настоящем документе путем ссылки. В конкретных иллюстративных вариантах осуществления связывающие полипептиды (например, антитела или их антигенсвязывающие фрагменты) по изобретению содержат домен Fc, обладающий одной или несколькими из следующих замен: V284E, H285E, N286D, K290E и S304D (нумерация EU). В других иллюстративных вариантах осуществления связывающие молекулы по изобретению содержат домен Fc человека с двойной мутацией H433K/N434F (см., например, патент США № 8163881).
В других вариантах осуществления связывающие полипептиды для использования в способах диагностики и лечения, описанных в настоящем документе, обладают константной областью, например, константной областью тяжелой цепи IgG1 или IgG4, которая является измененной для уменьшения или прекращения гликозилирования. Например, связывающие полипептиды (например, антитела или их антигенсвязывающие фрагменты) по изобретению могут также содержать вариант Fc, содержащий аминокислотную замену, изменяющую гликозилирование Fc антитела. Например, указанный вариант Fc может обладать уменьшенным гликозилированием (например, N- или O-связанным гликозилированием). В иллюстративных вариантах осуществления вариант Fc может обладать уменьшенным гликозилированием N-связанного гликана, в норме обнаруживаемого в положении аминокислоты 297 (нумерация EU). В другом варианте осуществления антитело обладает аминокислотной заменой вблизи или внутри мотива гликозилирования, например, мотива N-связанного гликозилирования, содержащего аминокислотную последовательность NXT или NXS. В конкретном варианте осуществления антитело содержит вариант Fc с аминокислотной заменой в положении аминокислоты 228 или 299 (нумерация EU). В конкретных вариантах осуществления связывающий полипептид содержит константную область IgG1 или IgG4, содержащую мутацию S228P и T299A (нумерация EU).
Иллюстративные аминокислотные замены, обеспечивающие уменьшенное или измененное гликозилирование, описаны в Международной публикации PCT № WO05/018572, полное содержание которой приведено в настоящем документе путем ссылки. В предпочтительных вариантах осуществления связывающие полипептиды по изобретению модифицированы для исключения гликозилирования. Такие связывающие полипептиды можно обозначать как «agly» связывающие полипептиды (например, «agly» антитела). Без связи с теорией, считают, что «agly» связывающие полипептиды могут обладать улучшенной безопасностью и профилем стабильности in vivo. Agly связывающие полипептиды могут принадлежать к любому изотипу или его подклассу, например, IgG1, IgG2, IgG3 или IgG4. В конкретных вариантах осуществления agly связывающие полипептиды содержат агликозилированную область Fc антитела IgG4, лишенную Fc-эффекторной функции, таким образом исключая потенциал для опосредованной Fc токсичности для нормальных жизненно важных органов, экспрессирующих IL-6. В других вариантах осуществления связывающие полипептиды по изобретению содержат измененный гликан. Например, антитело может обладать уменьшенным количеством остатков фукозы на N-гликане на Asn297 области Fc, т.е. является афукозилированным. Афукозилирование увеличивает связывание FcRgII на клетках NK и сильно увеличивает ADCC. Показано, что диатело, содержащее анти-IL-6 scFv и анти-CD3 scFv индуцирует уничтожение экспрессирующих IL-6 клеток посредством ADCC. Соответственно, в одном варианте осуществления, афукозилированное антитело анти-IL-6 используют для нацеливания на экспрессирующие IL-6 клетки и для их уничтожения. В другом варианте осуществления связывающий полипептид может обладать измененным количеством остатков сиаловой кислоты на N-гликане на Asn297 области Fc. Многочисленные известные в данной области способы доступны для получения «agly» антител или антител с измененными гликанами. Например, генетически модифицированные клетки-хозяева (например, модифицированные дрожжи, например, Picchia, или клетки CHO) с модифицированными путями гликозилирования (например, делециями гликозил-трансферазы) можно использовать для продукции таких антител.
V. Эффекторные группы
В конкретных вариантах осуществления связывающие полипептиды по настоящему описанию содержат эффекторные группы (например, группы лекарственного средства и нацеливающие группы). Как правило, эти эффекторные группы конъюгированы (либо напрямую, либо через линкерную группу) с N-связанным гликаном на связывающем полипептиде, (например, N-связанным гликаном, связанным с N298 (нумерация EU) домена CH2 и/или с N114 домена CH1 (нумерация Kabat). В конкретных вариантах осуществления связывающий полипептид представляет собой полноразмерное антитело, содержащее два домена CH1 с гликаном в положении Kabat 114, где оба гликана являются конъюгированными с одной или несколькими эффекторными группами.
Любые эффекторные группы можно добавлять к связывающим полипептидам, описанным в настоящем документе. Эффекторные группы предпочтительно добавляют неприродную функцию к измененному антителу или его фрагментам, без значительного изменения присущей связывающему полипептиду активности. Эффекторная группа может представлять собой, например, но без ограничения, терапевтическое или диагностическое средство. Модифицированный связывающий полипептид (например, антитело) по настоящему описанию может содержать одну или несколько эффекторных групп, которые могут являться одинаковыми или различными.
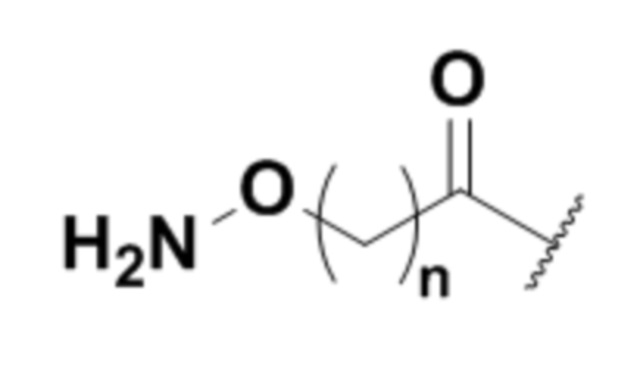
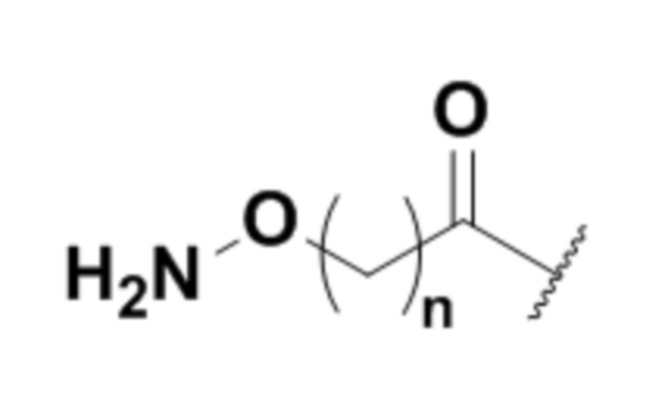
В одном варианте осуществления эффекторная группа может иметь формулу (I):
H2N-Q-CON-X
Формула (I),
где:
A) Q представляет собой NH или O; и
B) CON представляет собой соединительную группу; и
C) X представляет собой эффекторную группу (например, терапевтическое или диагностическое средство, как определено в настоящем документе).
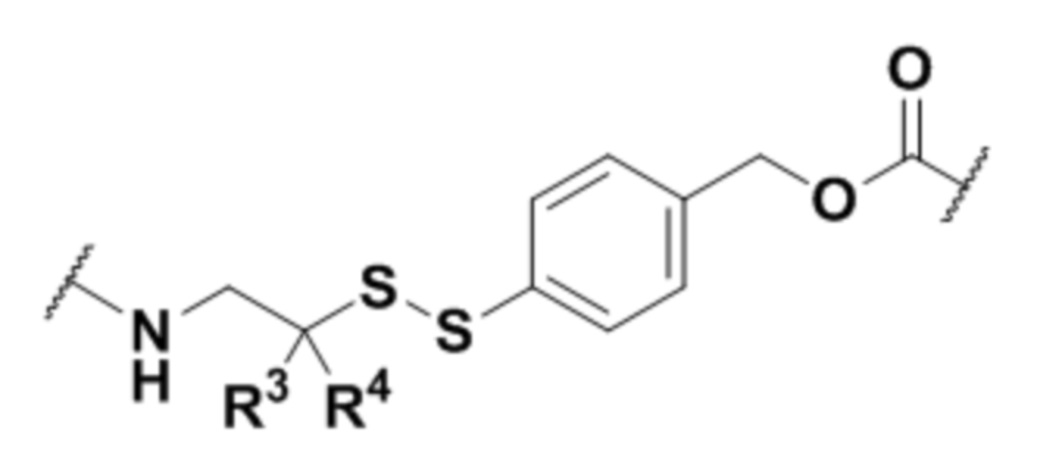
Соединительная группа соединяет лекарственное средство с H2N-Q-. Соединительная группа может включать по меньшей мере один из любых пригодных компонентов, известных специалистам в данной области, включая, например, алкиленильный компонент, полиэтиленгликолевый компонент, поли(глициновый) компонент, поли(оксазолиновый) компонент, карбонильный компонент, компонент, происходящий из цистеинамида, компонент, происходящий из валина, связанного с цитрулином, и компонент, происходящий из 4-аминобензилкарбамата, или любую их комбинациию.
В другом варианте осуществления эффекторная группа формулы (I) может иметь формулу (Ia):
H2N-Q-CH2-C(O)-Z-X
Формула (Ia),
где:
A) Q представляет собой NH или O; и
B) Z представляет собой Cys-(MC)a-(VC)b-(PABC)c-(C16H32O8C2H4)f,
где
i. Cys представляет собой компонент, происходящий из цистеинамида;
ii. MC представляет собой компонент, происходящий из малеимида;
iii. VC is a компонент, происходящий из валина, связанного с цитрулином;
iv. PABC представляет собой компонент, происходящий из 4-аминобензилкарбамата;
v. X представляет собой эффекторную группу (например, терапевтическое или диагностическое средство, как определено в настоящем документе);
vi. a представляет собой 0 или 1;
vii. b представляет собой 0 или 1;
viii.c представляет собой 0 или 1; и
ix. f представляет собой 0 или 1
«Компонент, происходящий из цистеинамида», является точкой присоединения к H2N-Q-CH2-C(O)-. В одном варианте осуществления «компонент, происходящий из цистеинамида» может относиться к одной или нескольким частям эффекторной группы, обладающей структурой:
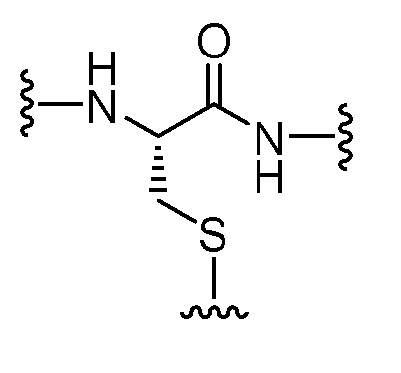
В одном варианте осуществления компонент «Cys» эффекторной группы может содержать одну такую часть. Например, следующая структура показывает эффекторную группу с одной такой частью (где компонент «Cys» обозначен рамкой из пунктирной линии):
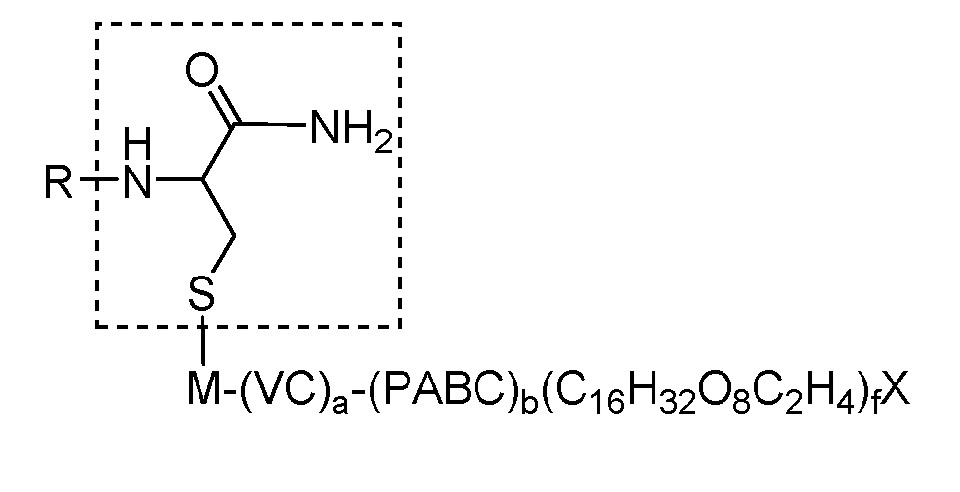
В другом варианте осуществления компонент «Cys» эффекторной группы может содержать две или более такие части. Например, следующая группа содержит две такие части:
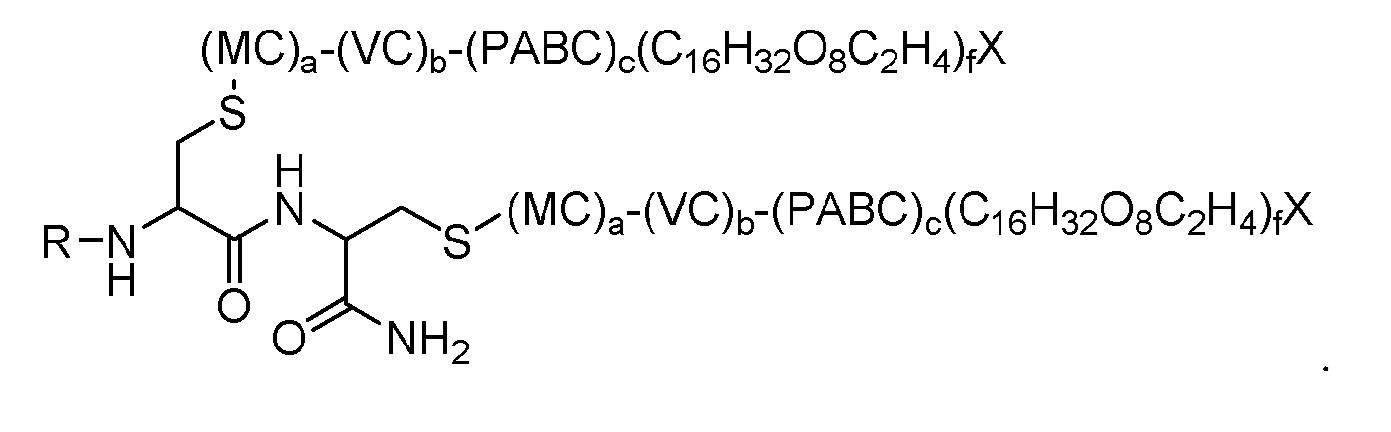
Как можно видеть из структуры, каждый компонент «Cys» несет группу -(MC)a-(VC)b-(PABC)c-(C16H32O8C2H4)f-X.
В одном варианте осуществления фраза «компонент, происходящий из малеимида», может относиться к любой части эффекторной группы, обладающей структурой:
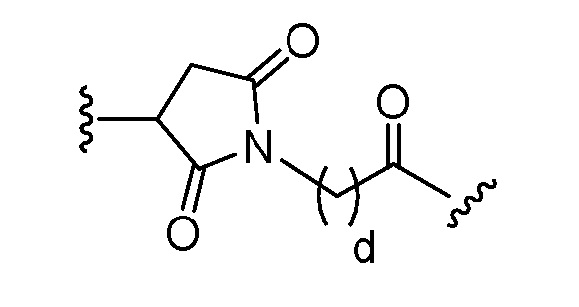 ,
,
где d представляет собой целое число от 2 до 5. Количество компонентов MC, включенных в любую группу Cys-(MC)a-(VC)b-(PABC)c-(C16H32O8C2H4)f-X в эффекторной группе, указано нижним индексом «a» и может составлять 0 или 1. В одном варианте осуществления a представляет собой 1. В другом варианте осуществления b представляет собой 0.
В одном варианте осуществления компонент «Cys» может быть соединен с компонентом «MC» через атом серы в компоненте «Cys», как обозначено рамкой из пунктирной линии в структуре ниже:
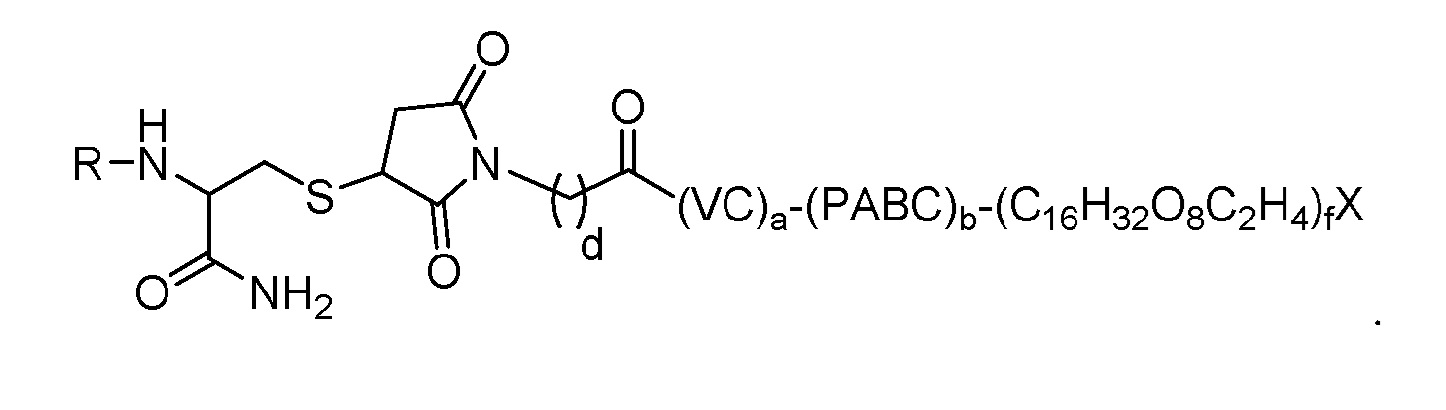
В одном варианте осуществления фраза «компонент, происходящий из валина, соединенного с цитрулином», может относиться к любой части эффекторной группы со следующей структурой:
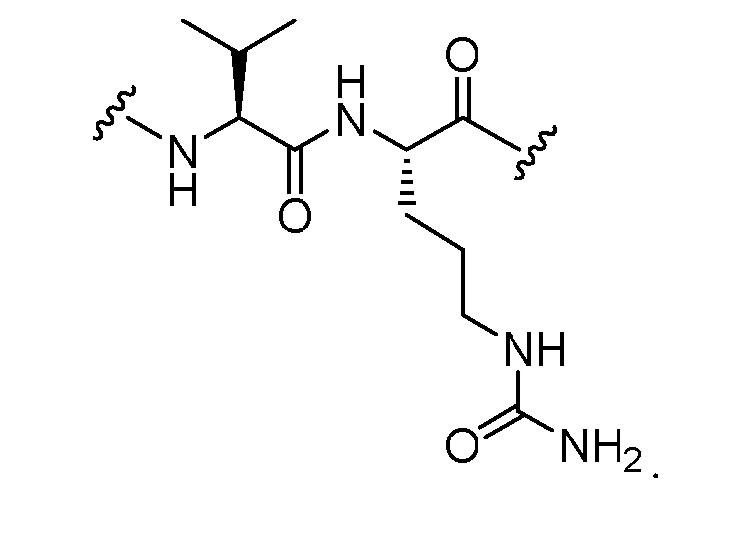
Количество компонентов VC, включенных в любую группу Cys-(MC)a-(VC)b-(PABC)c-(C16H32O8C2H4)f-X в эффекторной группе, указано нижним индексом «b» и может составлять 0 или 1. В одном варианте осуществления b представляет собой 1. В другом варианте осуществления b представляет собой 0.
В одном варианте осуществления фраза «компонент, происходящий из 4-аминобензилкарбамата», может относиться к любой части эффекторной группы со следующей структурой:
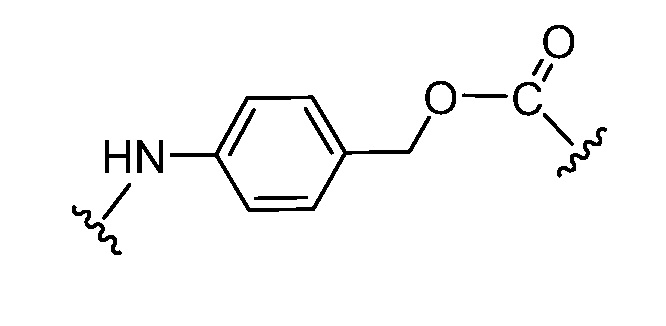
Количество компонентов PABC, включенных в любую группу Cys-(MC)a-(VC)b-(PABC)c-(C16H32O8C2H4)f-X в эффекторной группе, указано нижним индексом «c» и может составлять 0 или 1. В одном варианте осуществления c представляет собой 1. В другом варианте осуществления c представляет собой 0.
В одном варианте осуществления, «C16H32O8C2H4» относится к следующей структуре:
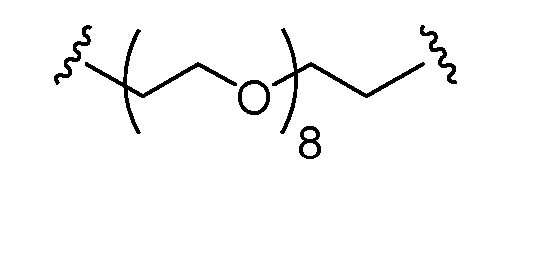
Количество единиц C16H32O8, включенных в любую группу Cys-(MC)a-(VC)b-(PABC)c-(C16H32O8C2H4)f-X в эффекторной группе, указано нижним индексом «f». В одном варианте осуществления f представляет собой 1. В другом варианте осуществления f представляет собой 0.
В одном варианте осуществления a представляет собой 1, b представляет собой 1, c представляет собой 1, и f представляет собой 0.
a) Терапевтические эффекторные группы
В конкретных вариантах осуществления связывающие полипептиды по настоящему описанию конъюгированы с эффекторной группой, содержащей лекарственное средство, например, группой лекарственного средства (или его пролекарства) или радиоактивно меченного соединения. В одном варианте осуществления лекарственное средство представляет собой цитотоксин. Иллюстративные цитотоксические лекарственные средства указаны в таблице 1 в настоящем документе.
|
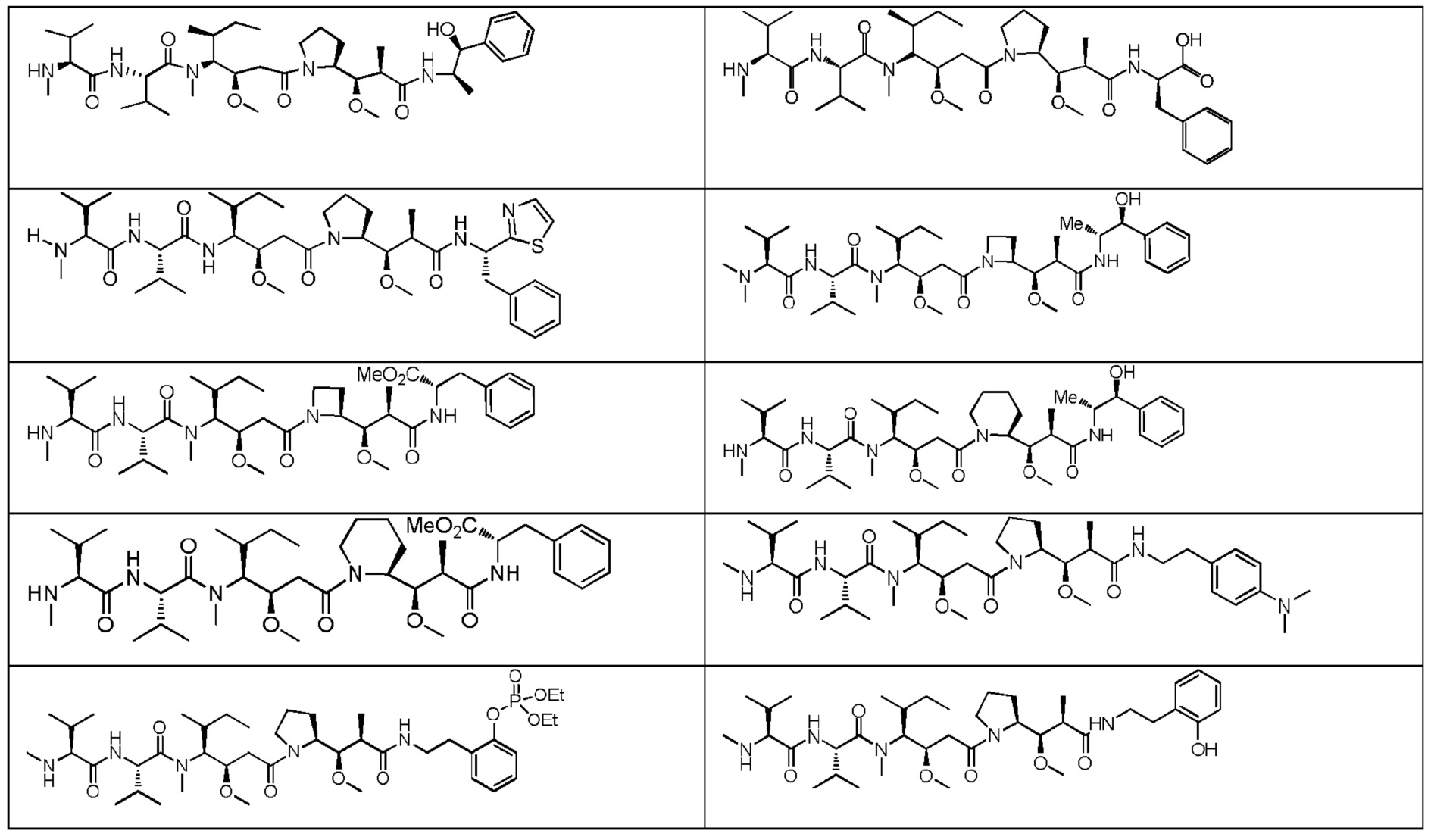
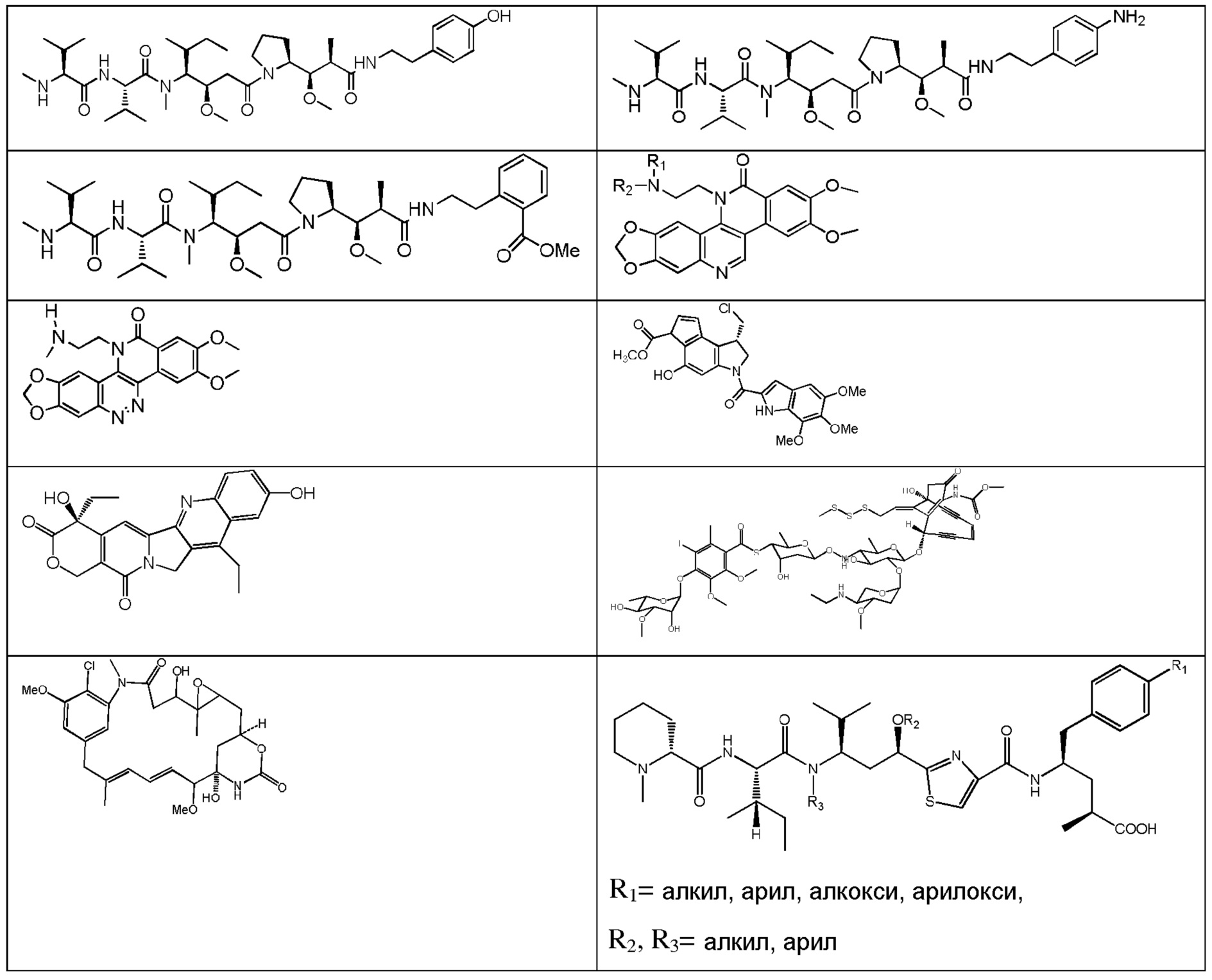
Дополнительные иллюстративные группы лекарственного средства включают противовоспалительные, противораковые, противоинфекционные (например, антигрибковые, антибактериальные, антипаразитические, антивирусные и т.д.), и анестетические лекарственные средства. В следующем варианте осуществления группа лекарственного средства представляет собой противораковое средство. Иллюстративные противораковые средства включают, но без ограничения, цитотоксические средства, ингибиторы ферментов, регуляторы генов, цитотоксические нуклеозиды, связывающие тубулин вещества или ингибиторы тубулина, ингибиторы протеасом, гормоны и антагонисты гормонов, средства против ангиогенеза и т.п. Иллюстративные цитотоксические противораковые средства включают алкилирующие средства, такие как антрациклиновое семейство лекарственных средств (например, адриамицин, карминомицин, циклоспорин-A, хлороквин, метоптерин, митрамицин, порфиромицин, стрептонигрин, порфиромицин, антрацендионы и азиридины). Другие цитотоксические противораковые средства включают ингибиторы синтеза ДНК (например, метотрексат и дихлорметотрексат, 1,4-диоксид 3-амино-1,2,4-бензотриазина, аминоптерин, цитозин-β-D-арабинофуранозид, 5-фтор-5'-дезоксиуридин, 5-фторурацил, ганцикловир, гидроксимочевину, актиномицин-D и митомицин C), интеркалирующие в ДНК или сшивающие ДНК средства (например, блеомицин, карбоплатин, кармустин, хлорамбуцил, циклофосфамид, дихлорид цис-диаминоплатины (II) (цисплатин), мелфалан, митоксантрон и оксалиплатин), и регуляторы транскрипции ДНК-РНК (например, актиномицин D, даунорубицин, доксорубицин, гомогаррингтонин и идарубицин). Другие иллюстративные цитотоксические средства, совместимые с настоящим описанием включают бензохинонансамицины, хиноидные производные (например, хинолонхинолоны, генистеин, бактациклин), бусульфан, ифосфамид, мехлорэтамин, триазиквон, диазиквон, карбазилхинон, индолoхинон EO9, диазиридинил-бензохинонметил DZQ, триэтиленфосфорамид и соединения нитрозомочевины (например, кармустин, ломустин, семустин).
Иллюстративные цитотоксические нуклеозидные противораковые средства включают, но без ограничения: арабинозид аденозина, цитарабин, арабинозид цитозина, 5-фторурацил, флударабин, флоксуридин, фторафур и 6-меркаптопурин. Иллюстративный противораковые связывающие тубулин вещества включают, но без ограничения: таксоиды (например, паклитаксел, доцетаксел, таксан), нокодазол, ризоксин, доластатины (например, доластатин-10, -11 или -15), колхицин и колхициноиды (например, ZD6126), комбретастатины (например, комбретастатин A-4, AVE-6032), и алкалоиды барвинка (например, винбластин, винкристин, виндезин и винорелбин (навелбин)). Иллюстративные противораковые гормоны и антагонисты гормонов, включают, но без ограничения: кортикостероиды (например, преднизон), прогестины (например, гидроксипрогестерон или медропрогестерон), эстрогены, (например, диэтилстилбестрол), антиэстрогены (например, тамоксифен), андрогены (например, тестостерон), ингибиторы ароматазы (например, аминоглутетимид), 17-(аллиламино)-17-деэтоксиметоксигелданамицин, 4-амино-1,8-нафталимид, апигенин, брефелдин A, циметидин, дихлорэтиленметилен-дифосфоновую кислоту, леупролид (лейпрорелин), гормон, высвобождающий лютеинизирующий гормон, пифитрин-a, рапамицин, глобулин, связывающий половые гормоны, и тапсигаргин. Иллюстративные противораковые средства против ангиогенеза, включают, но без ограничения: соединения, включающие ангиостатин Kl-3, DL-α-дифторэтилметил-орнитин, эндостатин, фумагиллин, генистеин, миноциклин, стауроспорин и (±)-талидомид.
Иллюстративные противораковые ингибиторы ферментов включают, но без ограничения, S(+)-камптотецин, куркумин, (-)-дегуелин, 5,6-дихлоробензимидазол-1-β-D-рибофуранoзид, этопозид, форместан, фостриецин, гиспидин, 2-имино-1-имидазолидинуксусную кислоту (циклокреатин), мевинолин, трихостатин A, тирфостин AG 34 и тирфостин AG 879.
Иллюстративные противораковые регуляторы генов включают, но без ограничения,: 5-аза-2'-дезоксицитидин, 5-азацитидин, хлоркальциферол (витамин D3), 4-гидрокситамоксифен, мелатонин, мифепристон, ралоксифен, транс-ретинол (альдегиды витамина A), ретиноевую кислоту, кислый витамин A, 9-цис-ретиноевую кислоту, 13-цис-ретиноевую кислоту, ретинол (витамин A), тамоксифен и троглитазон.
Другие предпочтительные классы противораковых средств включают, но без ограничения: птеридиновое семейство лекарственных средств, диинены и подофиллотоксины. Особенно пригодные члены этих классов включают, например, метоптерин, подофиллотоксин или производные подофиллотоксина, такие как этопозид или фосфат этопозида, лейрозидин, виндезин, леурозин и т.п.
Другие противораковые средства, совместимые со способами в настоящем документе, включают ауристатины (например, ауристатин E и монометилауристан E), гелданамицин, калихеамицин, грамицидин D, майтанзиноиды (например, майтанзин), неокарциностатин, топотекан, таксаны, цитохалазин B, бромид этидия, эметин, тенопозид, колхицин, дигидроксиантрациндион, митоксантрон, прокаинпрокаин, татракаин, лидокаин, пропранолол, пуромицин и их аналоги или гомологи.
Другие противораковые средства, совместимые с объяснениями в настоящем документе, включают производные томаимицина, производные майтанзина, производные криптофицина, производные антрациклина, производные бисфосфоната, производные лептомицина, производные стрептонигрина, производные ауристатина и производные дуокармицина.
Другим классом совместимых противораковых средств, которые можно использовать в качестве групп лекарственного средства, являются радиосенсибилизирующие лекарственные средства, которые можно эффективно направлять на опухоль или иммунореактивные клетки. Такие группы лекарственного средства усиливают чувствительность к ионизирующему излучению, таким образом, увеличивая эффективность радиотерапии. Без намерения быть ограниченными теорией, антитело, модифицированное с помощью группы радиосенсибилизирующего лекарственного средства и интернализированное клеткой опухоли, может доставлять радиосенсибилизирующее средство ближе к ядру, где радиосенсибилизация максимальна. Антитела, утратившие группу радиосенсибилизирующего средства, могут быстро выводиться из крови, локализуя оставшееся радиосенсибилизирующее средство в опухоли-мишени и обеспечивая минимальное поглощение в нормальных тканях. После выведения из крови, вспомогательную радиотерапию можно проводить посредством наружной дистанционной лучевой терапии, направленной специфически на опухоль, источника радиоактивности, имплантированного непосредственно в опухоль, или системной радиоиммунотерапии с помощью такого же модифицированного антитела.
В одном варианте осуществления лекарственное средство содержит радиоактивные изотопы или радиоактивные метки с высокоэнергетическим ионизирующим излучением, способным вызывать множественные разрывы цепей ядерной ДНК, приводя к гибели клетки. Иллюстративные высокоэнергетические радиоактивные изотопы включают : 90Y, 125I, 131I, 123I, 111In, 105Rh, 153Sm, 67Cu, 67Ga, 166Ho, 177Lu, 186Re и 188Re. Эти изотопы, как правило, образуют высокоэнергетические α- или β-частицы, обладающие короткой длиной пути. Такие радиоактивные изотопы уничтожают клетки, с которыми они находятся в непосредственной близости, например, неопластические клетки, к которым присоединен конъюгат или в которые вошел конъюгат. Они оказывают небольшой эффект или не оказывают эффекта на нелокализованные клетки и являются в основном неиммуногенными. Альтернативно, высокоэнергетические изотопы можно получать посредством теплового облучения в ином случае стабильного изотопа, например, в форме бор-нейтрон-захватной терапии (Guan et al., PNAS, 95: 13206-10, 1998).
В одном варианте осуществления лекарственное средство выбрано из MMAE, MMAF и PEG8-Do110.
Иллюстративные терапевтические эффекторные группы включают структуры:
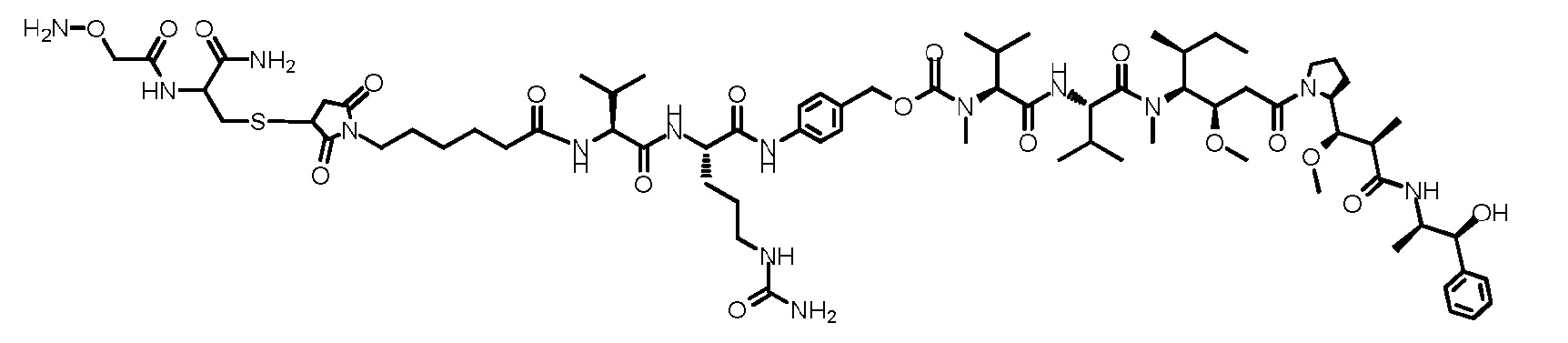
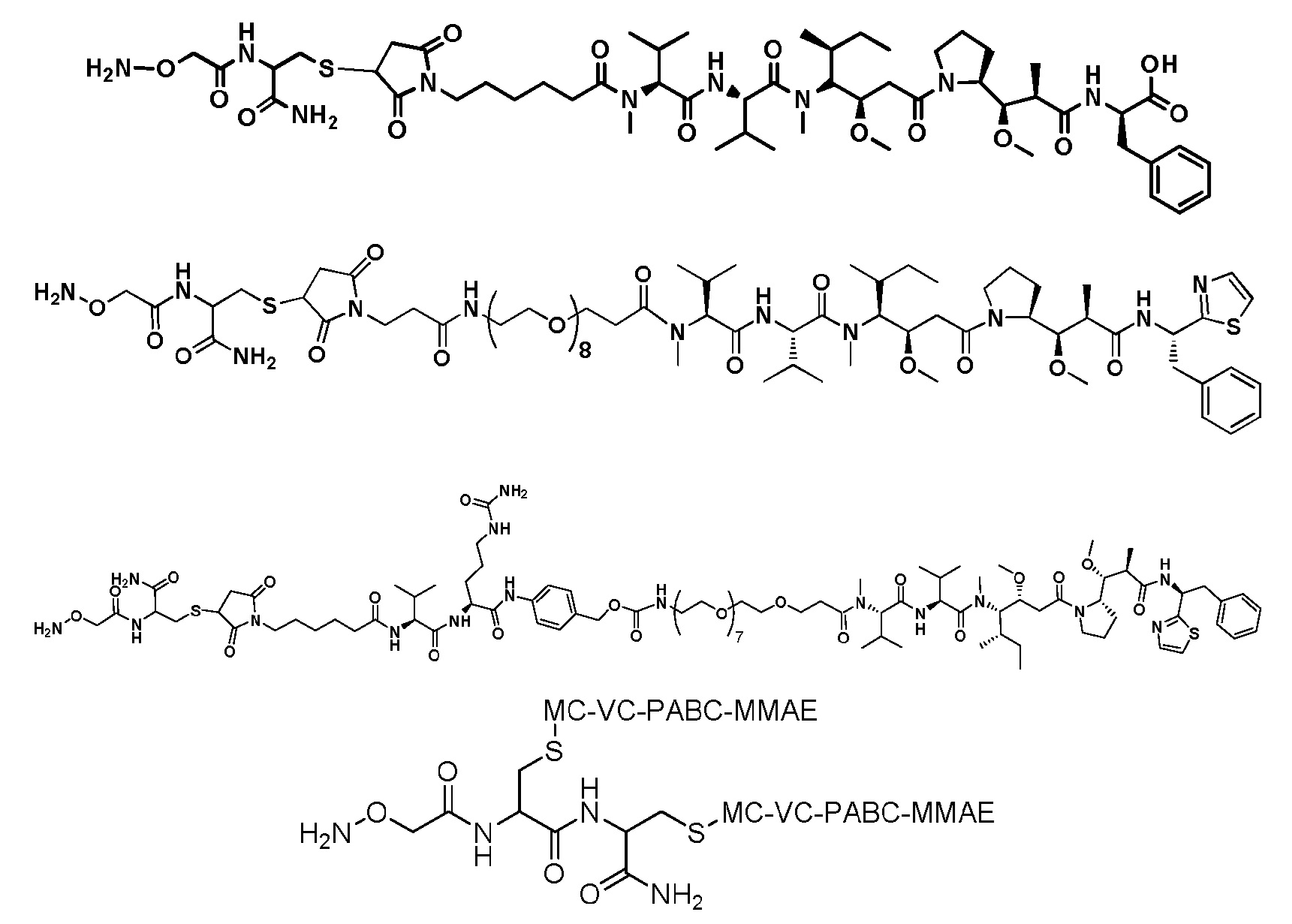
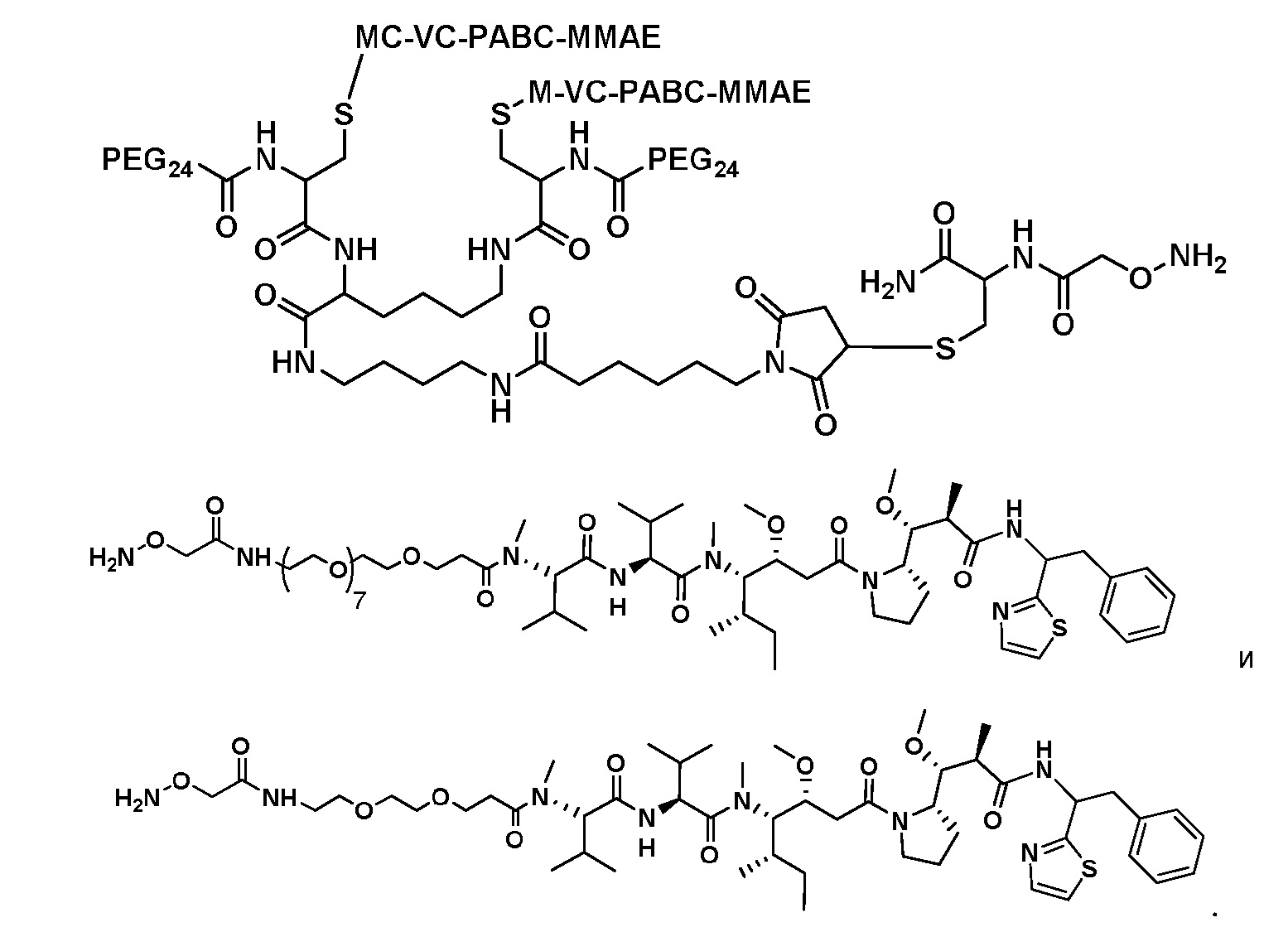
В одном варианте осуществления эффекторная группа выбрана из:
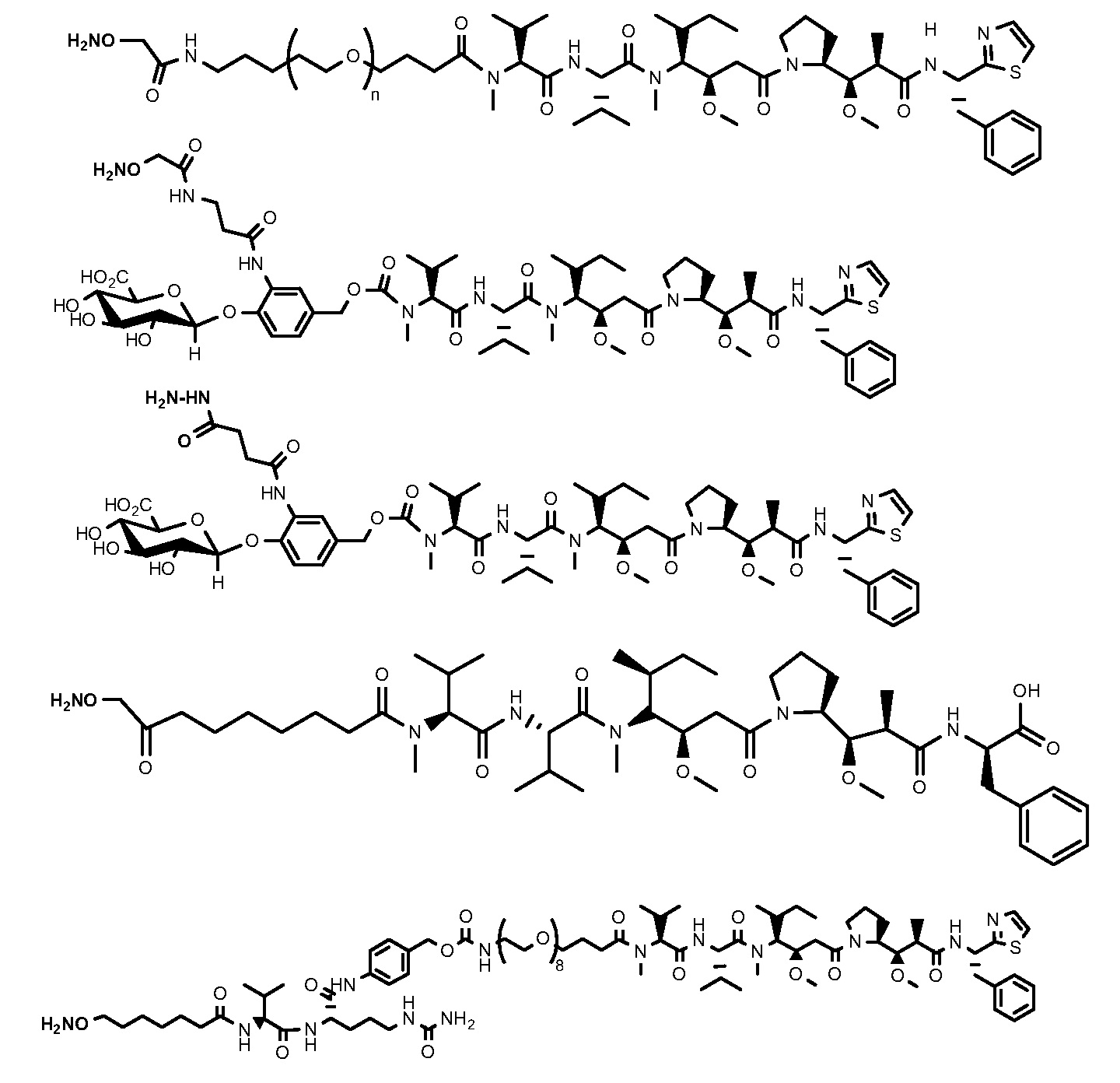
В конкретных вариантах осуществления эффекторная группа содержит более одного лекарственного средства. Эти множественные лекарственные средства могут являться одинаковыми или различными.
b) Диагностические эффекторные группы
В конкретных вариантах осуществления связывающие полипептиды по настоящему описанию конъюгированы с эффекторной группой, содержащей диагностическое средство. В одном варианте осуществления диагностическое средство представляет собой поддающуюся детекции низкомолекулярную метку, например, биотин, флуорофоры, хромофоры, спиновые резонансные зонды или радиоактивные метки. Иллюстративные флуорофоры включают флуоресцентные красители (например, флуоресцеин, родамин и т.п.) и другие люминесцентные молекулы (например, люминал). Флуорофор может являться чувствительным к окружению, так что его флуоресценция изменяется, если он локализован близко к одному или нескольким остаткам в модифицированном связывающем полипептиде, подвергающимся структурным изменениям при связывании субстрата (например, дансиловых зондов). Иллюстративные радиоактивные метки включают малые молекулы, содержащие атомы с одним или несколькими низко чувствительными ядрами (13C, 15N, 2H, 125I, 124I, 123I, 99Tc, 43K, 52Fe, 64Cu, 68Ga, 111In и т.п.). Предпочтительно, радиоактивный изотоп представляет собой испускающий гамма, фотоны или позитроны радиоактивный изотоп с временем полужизни, пригодным, чтобы позволять активность или детекцию после прошедшего времени между введением и локализацией в участке получения изображений.
В одном варианте осуществления диагностическое средство представляет собой полипептид. Иллюстративные диагностические полипептиды включают ферменты с флуорогенной или хромогенной активностью, например, способностью расщеплять субстрат, формирующий флуорофор или хромофор в качестве продукта (т.е. репортерные белки, такие как люцифераза). Другие диагностические белки могут обладать присущим им флуорогенной или хромогенной активностью (например, зеленый, красный и желтый флуоресцентные биолюминесцентные эквориновые белки из биолюминесцентных морских организмов) или они могут содержать белок, содержащий один или несколько низкоэнергетических радиоактивных ядер (13C, 15N, 2H, 125I, 124I, 123I, 99Tc, 43K, 52Fe, 64Cu, 68Ga, 111In и т.п.).
Что касается использования радиоактивно меченных конъюгатов в соответствии с настоящим описанием, связывающие полипептиды по настоящему описанию можно метить напрямую (например, посредством иодирования) или можно метить опосредованно посредством использования хелатирующего агента. Как применяют в настоящем документе, фразы «опосредованное мечение» и «способ опосредованного мечения» обе означают, что хелатирующий агент ковалентно присоединен к связывающему полипептиду, и по меньшей мере один радиоактивный изотоп ассоциирован с хелатирующим агентом. Такие хелатирующие агенты, как правило, обозначают как бифункциональные хелатирующие агенты, поскольку они связывают как полипептид, так и радиоактивный изотоп. Иллюстративные хелатирующие агенты содержат производные 1-изотиоцикматобензил-3-метилдиотелентриаминпентауксусной кислоты («MX-DTPA») и циклогексилдиэтилентриаминпентауксусной кислоты («CHX-DTPA»). Другие хелатирующие агенты содержат производные P-DOTA и EDTA. Особенно предпочтительные радиоактивные изотопы для непрямого мечения включают 111In и 90Y. В большинстве исследований с получением изображений используют 5 мКи 111In-меченного антитела, поскольку эта доза как является безопасной, так и обладает увеличенной эффективностью по сравнению с более низкими дозами, где оптимальное получение изображения происходит от трех до шести суток после введения антитела. См., например, Murray, (1985), J. Nuc. Med. 26: 3328 и Carraguillo et al, (1985), J. Nuc. Med. 26: 67. Особенно предпочтительный радиоактивный изотоп для прямого мечения представляет собой 131I. Специалистам в данной области понятно, что нерадиоактивные конъюгаты также можно собирать в зависимости от избранного средства, подлежащего конъюгации.
В конкретных вариантах осуществления диагностическая эффекторная группа представляет собой зонд с FRET (резонансным переносом энергии флуоресценции). FRET использовали для множества применений, включая диагностику злокачественных опухолей. Зонд с FRET может включать расщепляемый линкер (чувствительный к ферменту или pH линкер), соединяющий донорную и акцепторную группы зонда с FRET, где расщепление приводит в результате к усиленной флуоресценции (включая ближнюю инфракрасную) (см., например, A. Cobos-Correa et. al. Membrane-bound FRET probe visualizes MMP12 activity in pulmonary inflammation, Nature Chemical Biology (2009), 5(9), 628-63; S. Gehrig et.al. Spatially Resolved Monitoring of Neutrophil Elastase Activity with Ratiometric Fluorescent Reporters (2012) Angew. Chem. Int. Ed,., 51, 6258 -6261).
В одном варианте осуществления эффекторная группа выбрана из:
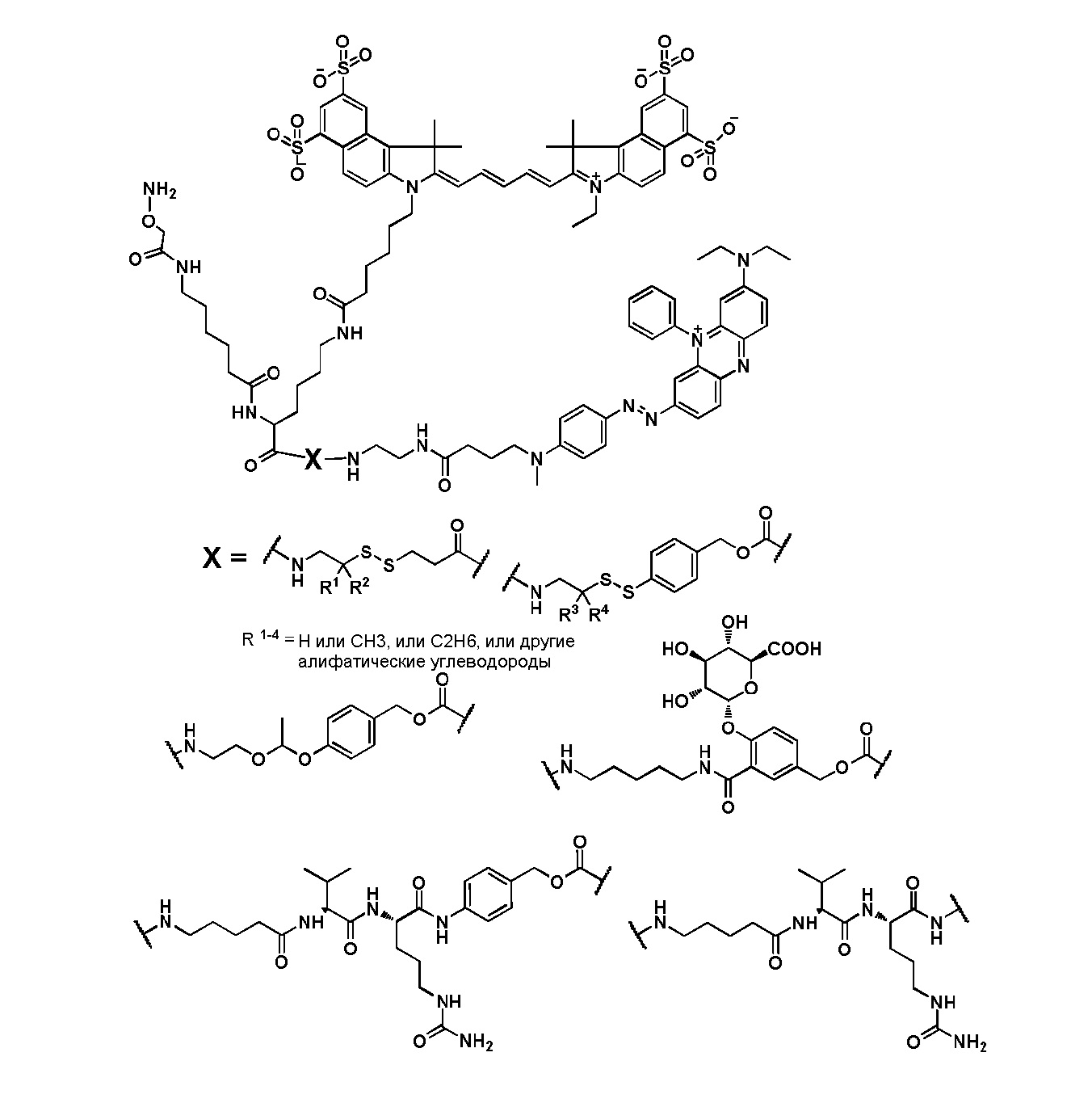
c) Функционализированные эффекторные группы
В конкретных вариантах осуществления эффекторные группы по изобретению могут являться функционализированными для содержания дополнительных групп в дополнение к собственно эффекторной группе. Например, эффекторная группа может содержать отщепляемые линкеры, которые высвобождают эффекторную группу из связывающего полипептида в конкретных условиях. В иллюстративных вариантах осуществления, эффекторная группа может содержать линкер, который поддается отщеплению клеточными ферментами и/или является чувствительным к pH. Дополнительно или альтернативно, эффекторная группа может содержать дисульфидную связь, отщепляемую внутриклеточным глутатионом при поглощении клеткой. Иллюстративные чувствительные к дисульфиду и pH линкеры представлены ниже:
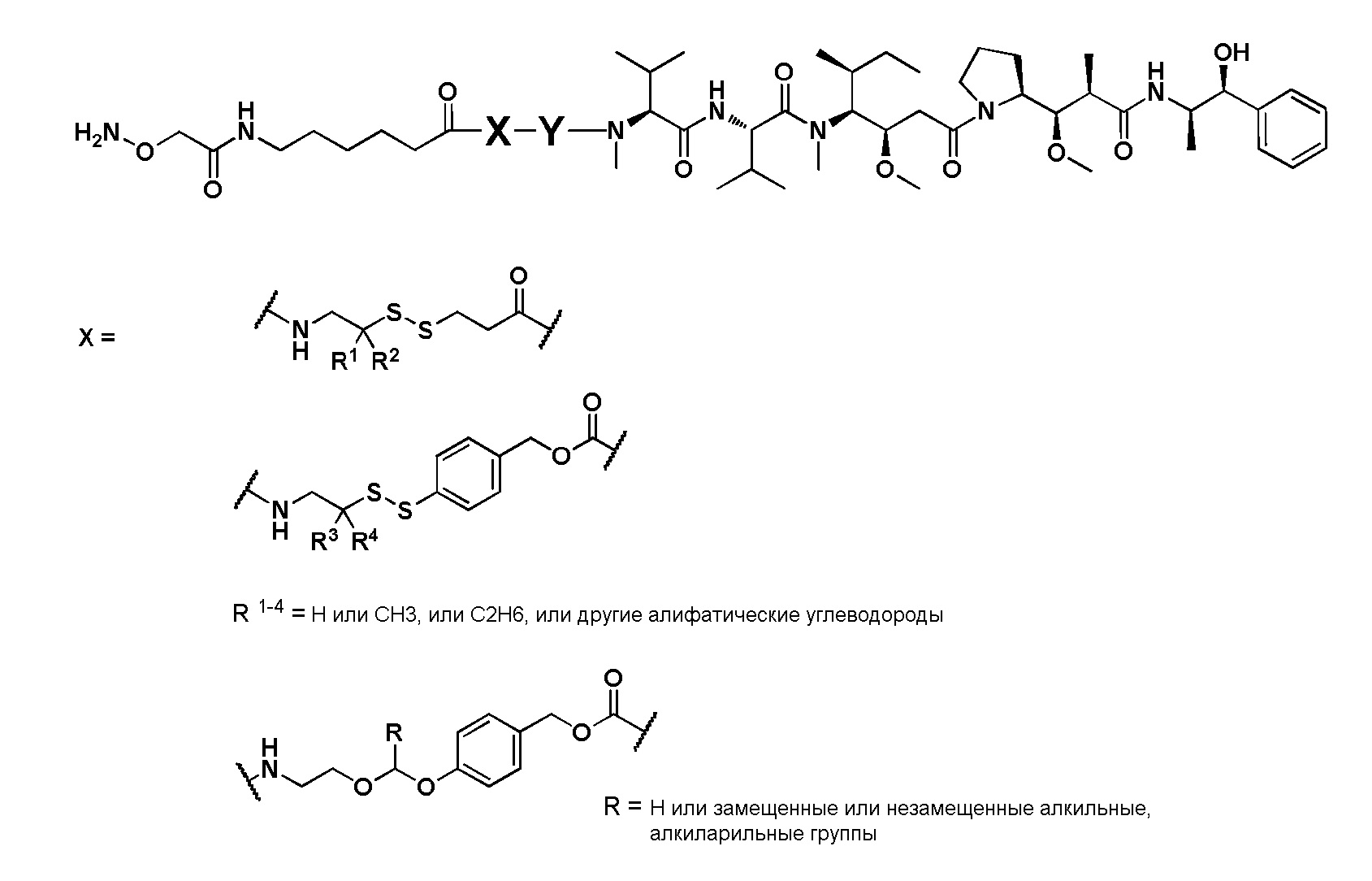
В других вариантах осуществления эффекторная группа может содержать гидрофильные и биосовместимые группы, такие как группы поли(глицина), поли(оксазолина) или PEG. Иллюстративные структуры («Y») представлены ниже:
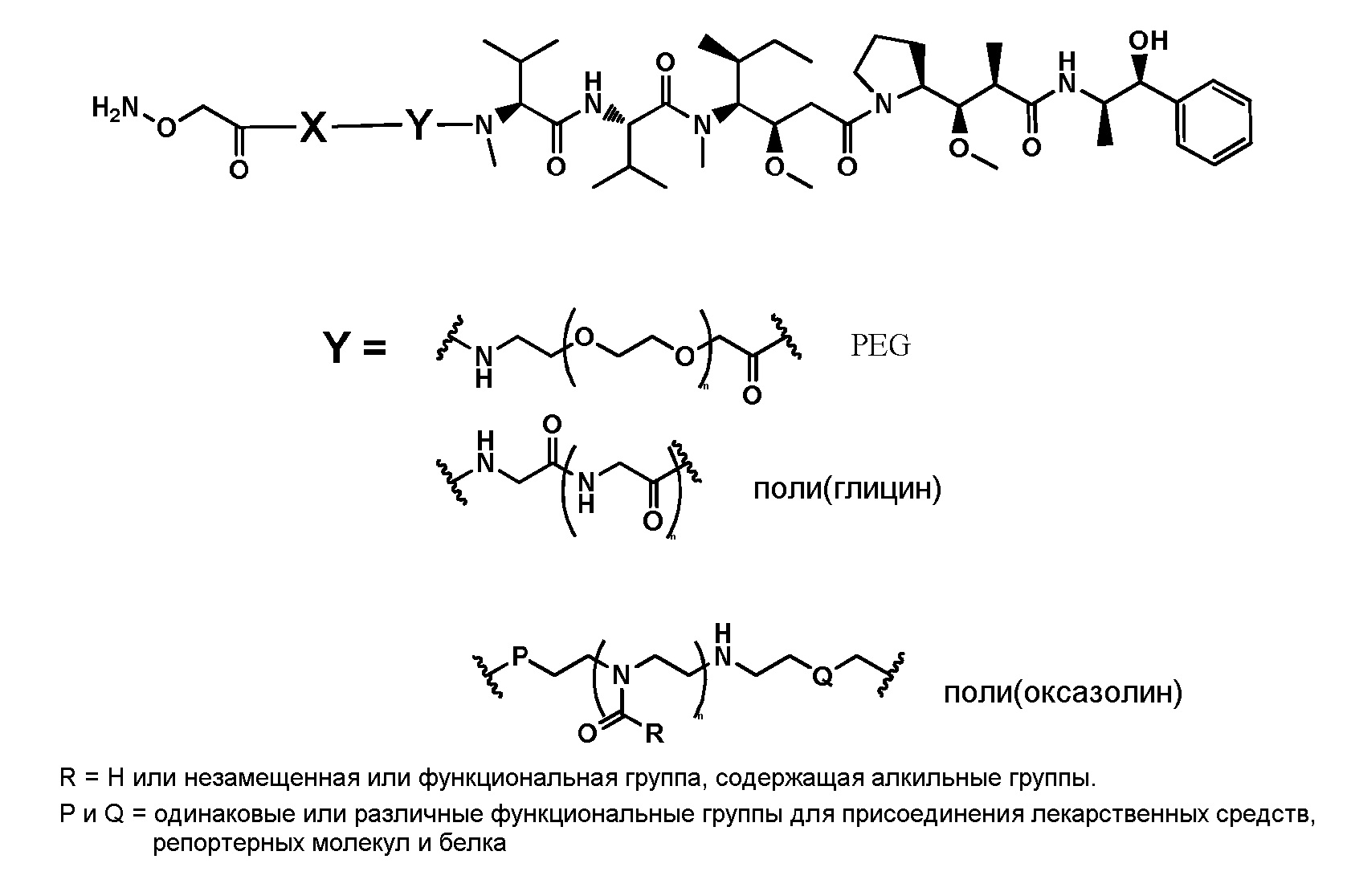
В конкретных вариантах осуществления эффекторная группа содержит аминооксигруппу, которая облегчает конъюгацию со связывающим полипептидом через стабильную оксимную связь. Иллюстративные эффекторные группы, содержащие аминооксигруппы, указаны в таблице 2 в настоящем документе.
|
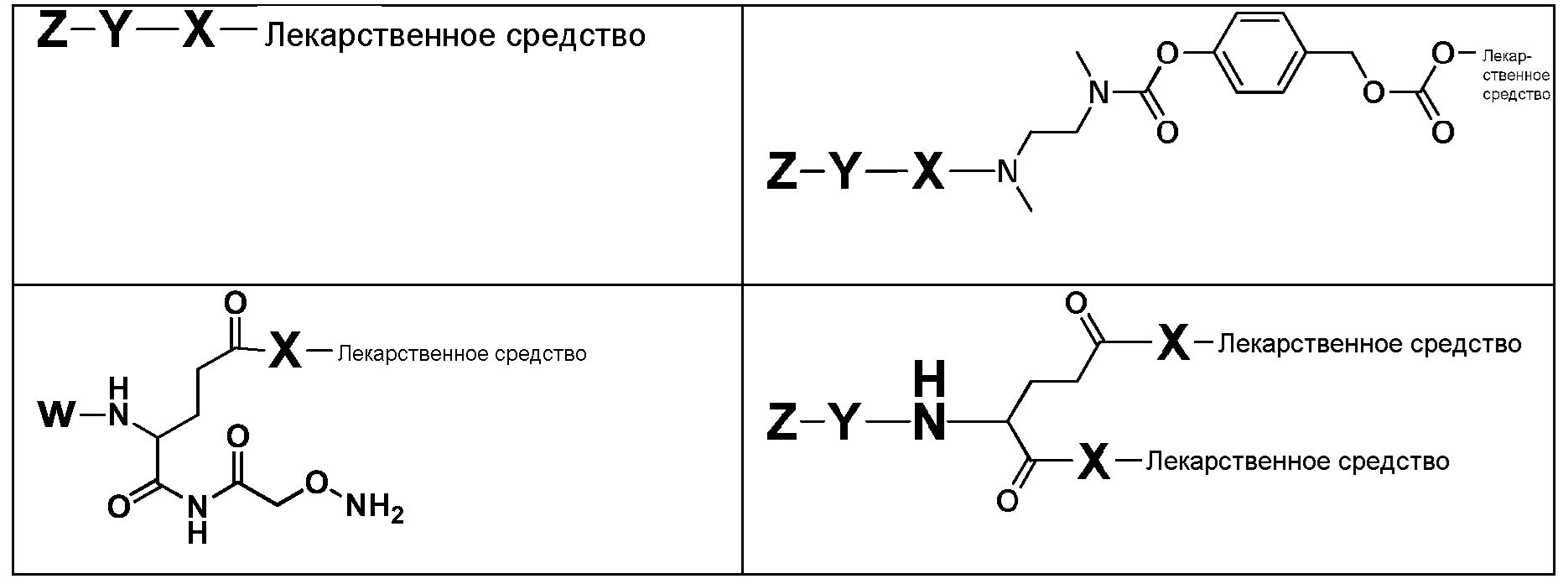
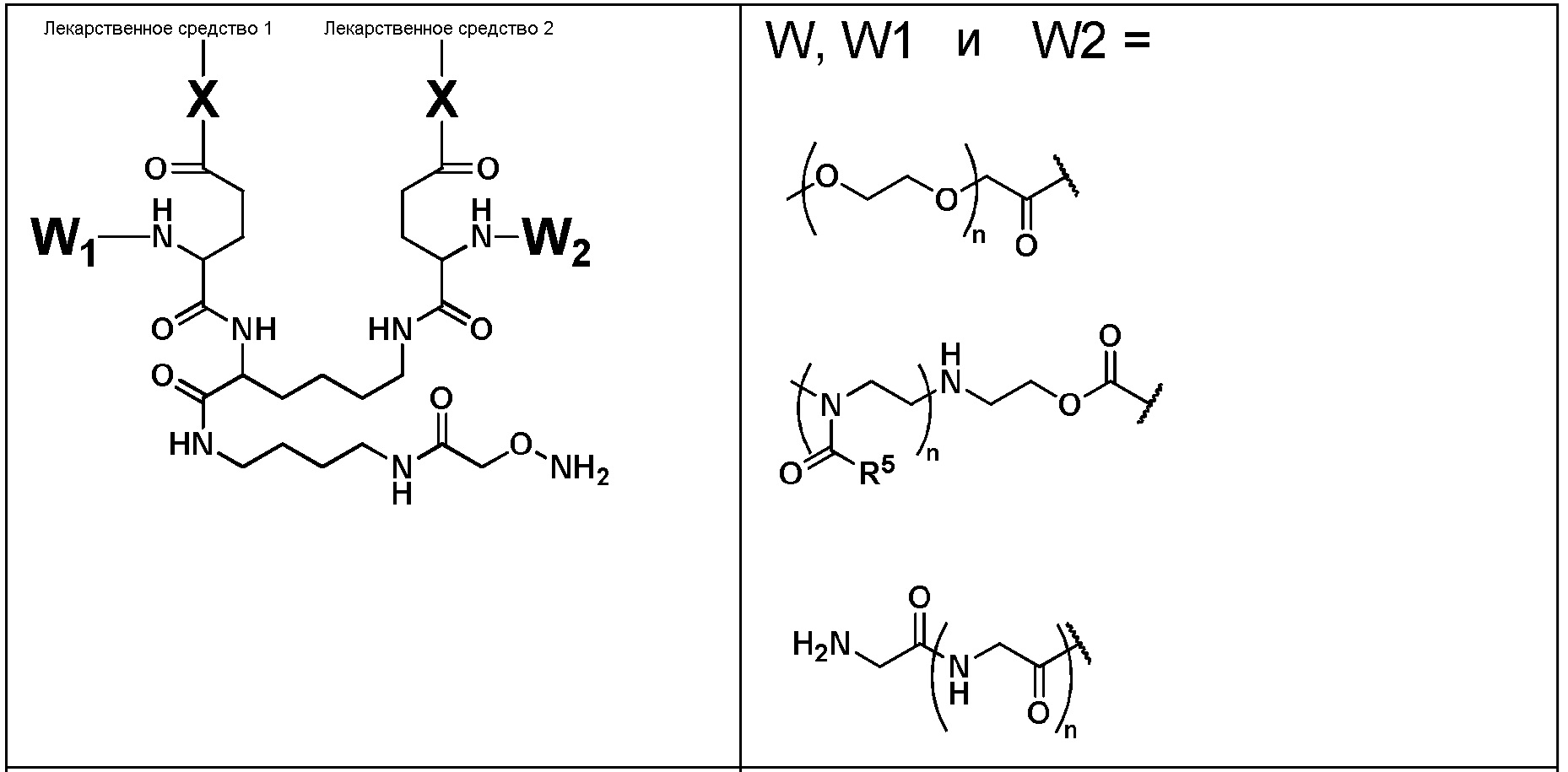
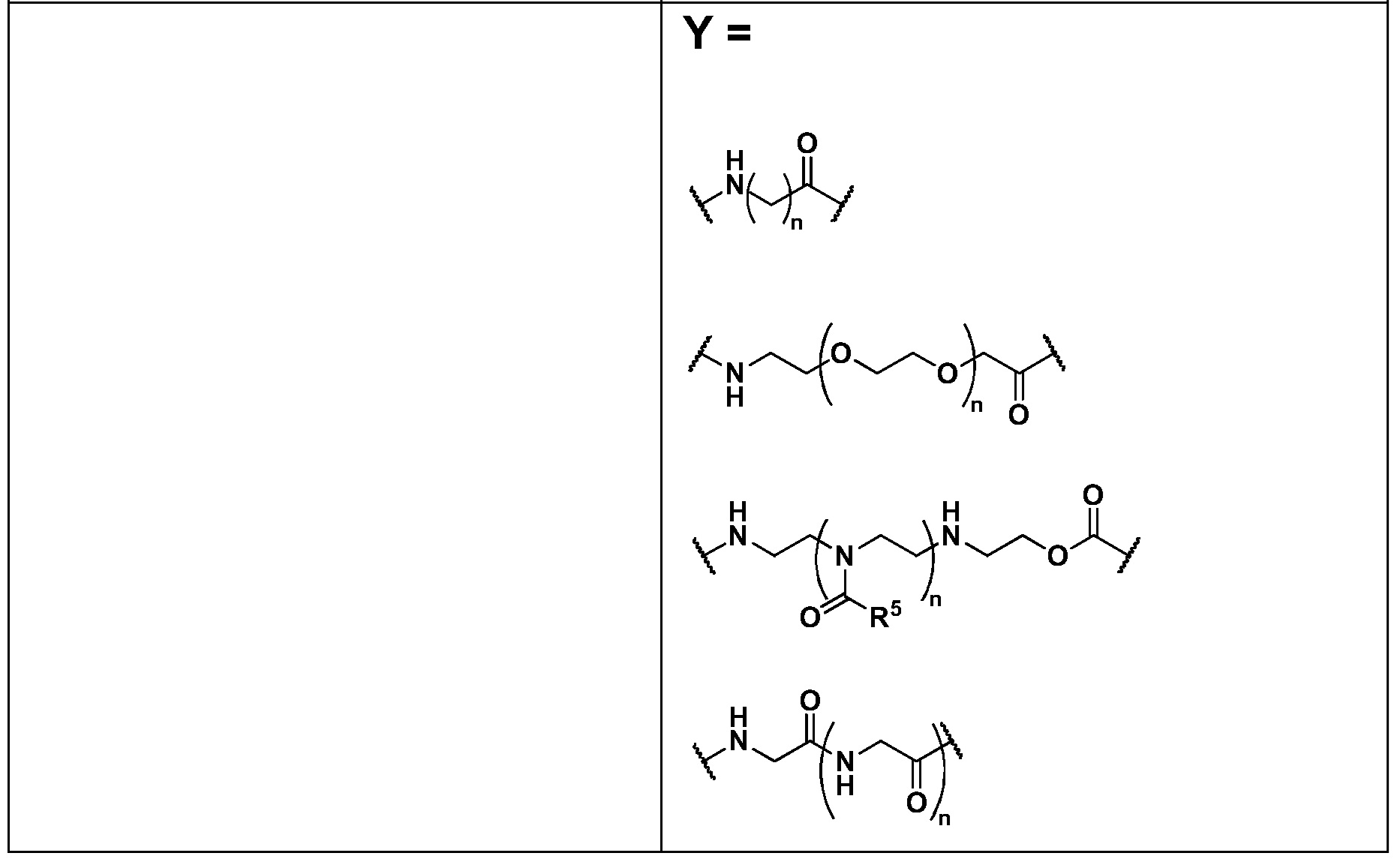
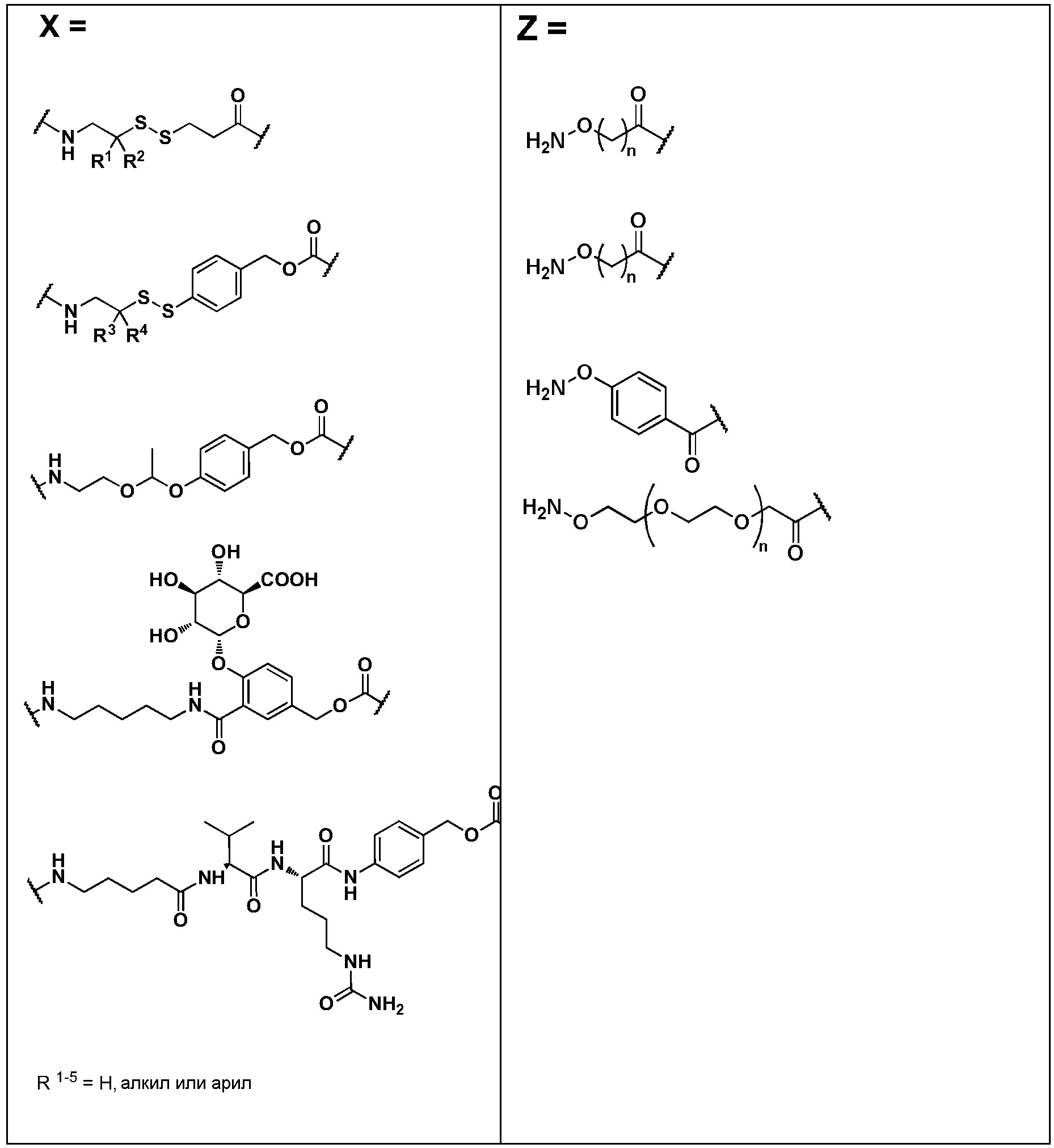
В других вариантах осуществления эффекторная группа содержит группу гидразида и/или N-алкилированного гидразина для облегчения конъюгации со связывающим полипептидом через стабильную гидразоновую связь. Иллюстративные эффекторные группы, содержащие аминооксигруппы, указаны в таблице 14 в настоящем документе.
|
d) Нацеливающие группы
В конкретных вариантах осуществления эффекторные группы содержат нацеливающие группы, которые специфически связываются с одной или несколькими молекулами-мишенями. Можно использовать любой тип нацеливающей группы, включая, без ограничения, белки, нуклеиновые кислоты, липиды, углеводы (например, гликаны) и их комбинации (например, гликопротеины, гликопептиды и гликолипиды). В конкретных вариантах осуществления нацеливающая группа представляет собой углевод или гликопептид. В конкретных вариантах осуществления нацеливающая группа представляет собой гликан. Нацеливающие группы могут представлять собой природные или неприродные молекулы.
VI. Конъюгация эффекторных групп со связывающими полипептидами
В конкретных вариантах осуществления эффекторные группы конъюгированы (либо напрямую, либо через линкерную группу) с окисленным гликаном (например, окисленным N-связанным гликаном) измененного связывающего полипептида, (например, сконструированным гликаном на N114 домена CH1 антитела или природным гликаном на N297 домена F антитела). Термин «окисленный гликан» означает, что спиртовой заместитель на гликане был окислен, предоставляя карбонильный заместитель. Карбонильный заместитель может вступать в реакцию с пригодным азотным нуклеофилом для формирования двойной связи углерод-азот. Например, реакция карбонильной группы с аминооксигруппой или гидразиновой группой образует оксим или гидразин, соответственно. В одном варианте осуществления карбонильный заместитель представляет собой альдегид. Пригодные окисленные гликаны включают окисленную галактозу и окисленную сиаловую кислоту.
В одном варианте осуществления модифицированный полипептид формулы (II) может иметь формулу (II):
Ab(Gal-C(O)H)x(Gal-Sia-C(O)H)y
Формула (II),
где
A) Ab представляет собой антитело или другой связывающий полипептид, как определено в настоящем документе;
B) Gal представляет собой компонент, происходящий из галактозы;
C) Sia представляет собой компонент, происходящий из сиаловой кислоты;
D) x составляет 0-5; и
E) y составляет 0-5,
где по меньшей мере один из x и y не составляет 0.
Любые известные в данной области химические реакции можно использовать для конъюгации эффекторной группы (например, эффекторной группы, содержащей линкерную группу) с гликаном (см. например, Hermanson, G.T., Bioconjugate Techniques. Academic Press (1996), полное содержание которого приведено в настоящем документе путем ссылки). В конкретных вариантах осуществления сахаридный остаток (например, остаток сиаловой кислоты или галактозы) гликана сначала окисляют (например, с использованием обработки периодатом натрия) для получения реакционноспособной альдегидной группы. Эта альдегидная группа вступает в реакцию с аминооксигруппой или гидразиновой группой эффекторной группы для формирования оксимного или гидразонового линкера, соответственно. Иллюстративные способы с использованием этой общей схемы реакции указаны в примерах 10-15.
В конкретных вариантах осуществления природные или сконструированные гликаны связывающего полипептида сначала предварительно обрабатывают ферментом гликозилтрансферазой in vitro для обеспечения концевого сахаридного остатка, обладающего пригодной реакционной способностью. Например, сначала можно осуществлять сиалирование с использованием комбинации галактозилтрансферазы (Gal T) и сиалилтрансферазы (Sial T). В конкретных вариантах осуществления двухантенные гликаны, которые лишены галактозы (G0F или G0) или которые содержат только одну галактозу (G1F или G1), можно переводить в галактозилированные или сиалированные структуры более высокого порядка, пригодные для конъюгации (G1F, G1, G2F, G2, G1S1F, G1S1, G2S1F, G2S1, G2S2F или G2S2).
Иллюстративная схема конъюгации для получения сиалированных гликоконъюгатов показана на фигуре 25C. Остатки сиаловой кислоты вводят ферментативно и сайт-специфически в гликан антитела (например, природный гликан на Asn-297) с использованием комбинации галактозилтрансферазы (Gal T) и сиалилтрансферазы (Sial T). Введенные остатки сиаловой кислоты затем окисляют с помощью низкой концентрации периодата натрия для получения реакционноспособных альдегидов сиаловой кислоты, пригодным образом реакционноспособных с лекарственными средствами-линкерами (например, аминоокси-линкерами лекарственными средствами) для получения конъюгатов антитела с лекарственным средством (ADC) (например, оксим-связанных ADC). Посредством контроля количества гликана и количества остатков сиаловой кислоты с помощью ремоделирования in vitro, специалист в данной области может иметь точный контроль над соотношением лекарственное средство-антитело (DAR) ADC. Например, если ~1 сиаловую кислоту добавляют на отдельный двухантенный гликан (A1F) на каждой тяжелой цепи, можно получать гомогенные антитело или связывающий полипептид с DAR 2.
VII. Модифицированные связывающие полипептиды
В конкретных вариантах осуществления изобретение относится к модифицированным полипептидам, которые являются продуктом конъюгации эффекторных групп, конъюгированных (либо напрямую, либо через линкерную группу) с окисленным гликаном (например, окисленным N-связанным гликаном) измененного связывающего полипептида (например, сконструированным гликаном на N114 домена CH1 антитела или природным гликаном на N297 домена F антитела).
В одном варианте осуществления связывающий полипептид может иметь формулу (III):
Ab-(Gal-C(H)=N-Q-CON-X)x(Gal-Sia-C(H)=N-Q-CON-X)y
Формула (III),
где:
A) Ab представляет собой антитело, как определено в настоящем документе;
B) Q представляет собой NH или O;
C) CON представляет собой соединительную группу, как определено в настоящем документе; и
D) X представляет собой терапевтическое или диагностическое средство, как определено в настоящем документе;
E) Gal представляет собой компонент, происходящий из галактозы;
F) Sia представляет собой компонент, происходящий из сиаловой кислоты;
G) x составляет 0-5; и
H) y составляет 0-5,
где по меньшей мере один из x и y не составляет 0.
В одном варианте осуществления связывающий полипептид может иметь формулу (III), может иметь формулу (IIIa):
Ab(Gal-C(H)=N-Q-CH2-C(O)-Z-X)x(Gal-Sia-C(H)=N-Q-CH2-C(O)-Z-X)y
Формула (IIIa),
где:
A) Ab представляет собой антитело;
B) Q представляет собой NH или O;
C) Z представляет собой Cys-(MC)a-(VC)b-(PABC)c-(C16H32O8C2H4)f-, где
i. Cys представляет собой компонент, происходящий из цистеинамида;
ii. MC представляет собой компонент, происходящий из малеимида;
iii. VC представляет собой компонент, происходящий из валина, соединенного с цитрулином;
iv. PABC представляет собой компонент, происходящий из 4-аминобензилкарбамата;
v. X представляет собой эффекторную группу (например, терапевтическое или диагностическое средство, как определено в настоящем документе);
vi. a составляет 0 или 1;
vii. b составляет 0 или 1;
viii. c составляет 0 или 1; и
ix. f составляет 0 или 1;
D) X представляет собой лекарственное средство, как определено в настоящем документе;
E) Gal представляет собой компонент, происходящий из галактозы;
F) Sia представляет собой компонент, происходящий из сиаловой кислоты;
G) x составляет 0-5; и
H) y составляет 0-5,
где по меньшей мере один из x и y не составляет 0.
Следует понимать, что формула (III) не предназначена, чтобы подразумевать, что антитело, заместитель Gal и заместитель Gal-Sia соединены подобным цепи образом. Вместо этого, когда такие заместители присутствуют, антитело соединено напрямую с каждым заместителем. Например, связывающий полипептид формулы (III), в которой x составляет 1, и y составляет 2, может иметь аранжировку, показанную ниже:
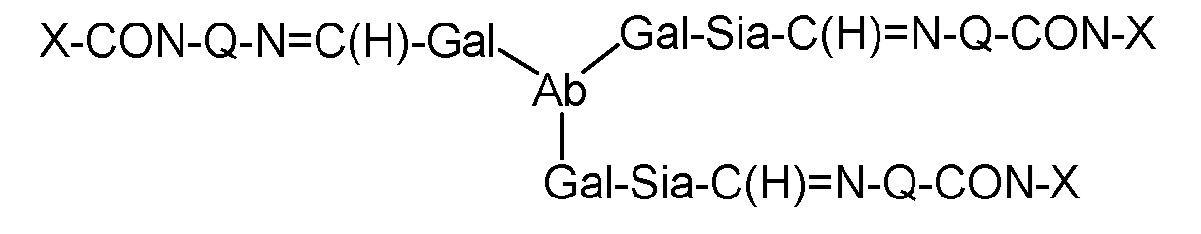
Формула (III)
Заместитель CON в формуле (III) и его компоненты являются такими, как описано по отношению к формуле (I) для эффекторных групп.
В одном варианте осуществления, Q представляет собой NH. В другом варианте осуществления Q представляет собой O.
В одном варианте осуществления x представляет собой 0.
Антитело Ab формулы (III) может представлять собой любое пригодное антитело, как описано в настоящем документе.
В одном варианте осуществления представлен способ получения связывающего полипептида формулы (III), где способ включает реакцию эффекторной группы формулы (I):
NH2-Q-CON-X
Формула (I),
где:
A) Q представляет собой NH или O;
B) CON представляет собой соединительную группу; и
C) X представляет собой эффекторную группу (например, терапевтическое или диагностическое средство, как определено в настоящем документе),
с модифицированным антителом формулы (II)
Ab(OXG)r
Формула (II),
где
A) OXG представляет собой окисленный гликан; и
B) r выбран из 0-4;
В одном варианте осуществления представлен способ получения связывающего полипептида формулы (III), где способ включает реакцию эффекторной группы формулы (I):
NH2-Q-CON-X
Формула (I),
где:
A) Q представляет собой NH или O;
B) CON представляет собой соединительную группу; и
C) X представляет собой эффекторную группу (например, терапевтическое или диагностическое средство, как определено в настоящем документе),
с модифицированным антителом формулы (IIa)
Ab(Gal-C(O)H)x(Gal-Sia-C(O)H)y
Формула (IIa),
где
A) Ab представляет собой антитело, как описано в настоящем документе;
B) Gal представляет собой компонент, происходящий из галактозы;
C) Sia представляет собой компонент, происходящий из сиаловой кислоты;
D) x составляет 0-5; и
E) y составляет 0-5,
где по меньшей мере один из x и y не составляет 0.
VII. Способы лечения с помощью модифицированных антител
В одном аспекте изобретение относится к способам лечения или диагностики нуждающегося в этом пациента, включающим введение эффективного количества связывающего полипептида, описанного в настоящем документе. Предпочтительные варианты осуществления по настоящему описанию относятся к наборам и способам для диагностики и/или лечения нарушений, например, неопластических нарушений, у субъекта-млекопитающего, нуждающегося в таком лечении. Предпочтительно, субъект представляет собой человека.
Связывающие полипептиды по настоящему описанию являются пригодными в ряде различных применений. Например, в одном варианте осуществления, рассматриваемые связывающие полипептиды являются пригодными для уменьшения количества или уничтожения клеток, несущих эпитоп, узнаваемый связывающим доменом связывающего полипептида. В другом варианте осуществления рассматриваемые связывающие полипептиды являются эффективными для уменьшения концентрации или уничтожения растворимого антигена в кровотоке. В одном варианте осуществления связывающие полипептиды могут уменьшать размер опухоли, ингибировать рост опухоли и/или продлевать время выживаемости несущих опухоли животных. Соответственно, это описание также относится к способу лечения опухолей у человека или другого животного посредством введения такому человеку или животному эффективного, нетоксичного количества модифицированного антитела. Специалист в данной области способен, посредством общепринятых экспериментов, определить то, что составляет эффективное, нетоксичное количество модифицированного связывающего полипептида для цели лечения злокачественных новообразований. Например, терапевтически активное количество модифицированного антитела или его фрагментов можно менять в зависимости от таких факторов, как стадия заболевания (например, стадия I по сравнению со стадией IV), возраст, пол, медицинские осложнения (например, иммуносупрессивные состояния или заболевания) и масса субъекта, и способность модифицированного антитела вызывать желательный ответ у субъекта. Режим дозирования можно регулировать для обеспечения оптимального терапевтического ответа. Например, несколько дробных доз можно вводить ежесуточно, или дозу можно пропорционально уменьшать, как показано по требованием терапевтической ситуации.
Как правило, композиции, представленные в настоящем описании, можно использовать для профилактического или терапевтического лечения любой неоплазии, содержащей антигенный маркер, позволяющий нацеливание на злокачественные клетки посредством модифицированного антитела.
VIII. Способы введения модифицированных антител или их фрагментов
Способы получения и введения связывающих полипептидов по настоящему описанию субъекту хорошо известны специалистам в данной области, или специалисты в данной области могут легко их определять. Способ введения связывающих полипептидов по настоящему описанию может являться пероральным, парентеральным, посредством ингаляции или местным. Термин парентеральное, как применяют в настоящем документе, включает внутривенное, внутриартериальное, внутрибрюшинное, внутримышечное, подкожное, ректальное или вагинальное введение. Внутривенная, внутриартериальная, подкожная и внутримышечная формы парентерального введения являются в основном предпочтительными. В то время как все эти формы введения явно предусматривают как входящие в объем настоящего описания, форма для введения может представлять собой раствор для инъекции, в частности для внутривенной или внутриартериальной инъекции или капельницы. Обычно пригодная фармацевтическая композиция для инъекции может содержать буфер (например, ацетатный, фосфатный или цитратный буфер), поверхностно-активное вещество (например, полисорбат), необязательно, стабилизирующее средство (например, альбумин человека) и т.д. Однако, в других способах, совместимых с объяснениями в настоящем документе, модифицированные антитела можно доставлять напрямую в участок нежелательной клеточной популяции, таким образом увеличивая воздействие лекарственного средства на пораженную заболеванием ткань.
В одном варианте осуществления связывающий полипептид, который вводят, представляет собой связывающий полипептид формулы (III):
Ab(Gal-C(H)=N-Q-CON-X)x(Gal-Sia-C(H)=N-Q-CON-X)y
Формула (III),
где:
A) Ab представляет собой антитело, как определено в настоящем документе;
B) Q представляет собой NH или O;
C) CON представляет собой соединительную группу, как определено в настоящем документе; и
D) X представляет собой эффекторную группу (например, терапевтическое или диагностическое средство, как определено в настоящем документе);
E) Gal представляет собой компонент, происходящий из галактозы;
F) Sia представляет собой компонент, происходящий из сиаловой кислоты;
G) x составляет 0-5; и
H) y составляет 0-5,
где по меньшей мере один из x и y не составляют 0.
Препараты для парентерального введения включают стерильные водные или неводные растворы, суспензии и эмульсии. Примеры неводных растворителей представляют собой пропиленгликоль, полиэтиленгликоль, растительные масла, такие как оливковое масло, и пригодные для инъекции органические сложные эфиры, такие как этилолеат. Водные носители включают воду, спиртовые/водные растворы, эмульсии или суспензии, включая солевой раствор и забуференные среды. В композициях и способах по настоящему описанию, фармацевтически приемлемые носители включают, но без ограничения, 0,01-0,1 M и предпочтительно, 0,05 M фосфатный буфер или 0,8% солевой раствор. Другие общепринятые парентеральные носители включают растворы фосфата натрия, декстрозу Рингера, декстрозу и хлорид натрия, лактат Рингера или жирные масла. Внутривенные носители включают пополняющие жидкость и питательные вещества средства, пополняющие электролиты средства, такие как средства на основе декстрозы Рингера, и т.п. Могут также присутствовать консерванты и другие добавки, например, такие как противомикробные средства, антиоксиданты, хелатирующие агенты и инертные газы, и т.п. Более конкретно, фармацевтические композиции, пригодные для применения для инъекций, включают стерильные водные растворы (когда они водорастворимы) или дисперсии и стерильные порошки для приготовления для немедленного введения стерильных пригодных для инъекции растворов или дисперсий. В таких случаях, композиция должна являться стерильной и должна являться жидкой до такой степени, что существует возможность легкого введения через шприц. Она должна являться стабильной в условиях изготовления и хранения и предпочтительно является защищенной от контаминирующего действия микроорганизмов, таких как бактерии и грибы. Носитель может представлять собой растворитель или диспергирующую среду, содержащую, например, воду, этанол, полиол (например, глицероглицерин, пропиленгликоль и жидкий полиэтиленгликоль, и т.п.), и их пригодные смеси. Надлежащую текучесть можно поддерживать, например, посредством использования покрытия, такого как лецитин, посредством поддержания требуемого размера частиц в случае дисперсии и посредством использования поверхностно-активных веществ.
Предотвращения действия микроорганизмов можно достигать посредством различных антибактериальных и противогрибковых средств, например, парабенов, хлорбутанола, фенола, аскорбиновой кислоты, тимеросала и т.п. Во многих случаях, является предпочтительным включать изотонические средства, например, сахара, полиспирты, такие как маннит, сорбит или хлорид натрия, в композицию. Продленная абсорбция пригодных для инъекции композиций может быть обусловлена включением в композицию средства, замедляющего абсорбцию, например, моностеарата алюминия и желатина.
В любом случае, стерильные пригодные для инъекции растворы можно получать посредством включения активного соединения (например, модифицированного связывающего полипептида, отдельно или в комбинации с другими активными средствами) в требуемое количество пригодного растворителя с одним или комбинацией ингредиентов, перечисленных в настоящем документе, по необходимости, с последующей стерилизацией фильтрацией. Как правило, дисперсии получают посредством включения активного соединения в стерильный носитель, содержащий базовую диспергирующую среду и другие требуемые ингредиенты из перечисленных выше. В случае стерильных порошков для получения стерильных пригодных для инъекции растворов, предпочтительными способами получения являются вакуумная сушка и лиофилизация, которыми получают порошок активного ингредиента плюс любого дополнительного желательного ингредиента из его предварительно стерилизованного фильтрацией раствора. Препараты для инъекций перерабатывают, заполняют в контейнеры, такие как ампулы, мешки, бутыли, шприцы или флаконы, и герметично закрывают в асептических условиях в соответствии со способами, известными в данной области. Далее препараты можно упаковывать и продавать в форме набора, такого как набор, описанный в находящихся одновременно на рассмотрении U.S.S.N. 09/259337 и U.S.S.N. 09/259338, содержание каждого из которых приведено в настоящем документе путем ссылки. Такие изделия предпочтительно имеют ярлыки или вкладыши в упаковку, указывающие на то, что прилагаемые композиции являются пригодными для лечения субъекта, страдающего от аутоиммунных или неопластических нарушений или предрасположенного к ним.
Эффективные дозы композиций по настоящему описанию для лечения вышеописанных состояний варьируют в зависимости от множества различных факторов, включая способы введения, участок-мишень, физиологическое состояние пациента, где пациент представляет собой человека или животного, другие введенные лекарственные средства, и то, является ли лечение профилактическим или терапевтическим. Как правило, пациент представляет собой человека, но не относящихся к человеку млекопитающих, включая трансгенных млекопитающих, также можно лечить. Дозы для лечения можно титровать с использованием общепринятых способов, известных специалистам в данной области, для оптимизации безопасности и эффективности.
Для пассивной иммунизации с помощью связывающего полипептида, доза может лежать в диапазоне, например, от приблизительно 0,00001 до 100 мг/кг, и более обычно, от 0,001 до 5 мг/кг (например, 0,002 мг/кг, 0,25 мг/кг, 0,5 мг/кг, 0,75 мг/кг, 1 мг/кг, 2 мг/кг и т.д.), массы тела хозяина. Например, дозы могут составлять 1 мг/кг массы тела или 10 мг/кг массы тела, или лежать в диапазоне 1-10 мг/кг, предпочтительно, по меньшей мере 1 мг/кг. Промежуточные дозы в вышеуказанных диапазонах также предназначены для включения в объем настоящего описания. Субъектам можно вводить такие дозы ежесуточно, в чередующиеся сутки, еженедельно или в соответствии с любым другим расписанием, определенным эмпирическим анализом. Иллюстративное лечение предусматривает введение в множественных дозах в течение продолжительного периода, например, по меньшей мере шесть месяцев. Дополнительные иллюстративные режимы лечения предусматривают введение раз в каждые две недели или раз в месяц, или раз в каждые 3-6 месяцев. Иллюстративные расписания дозирования включают 1-10 мг/кг или 15 мг/кг в последовательные сутки, 30 мг/кг в чередующиеся сутки или 60 мг/кг еженедельно. В некоторых способах два или более моноклональных антитела с различной специфичностью связывания вводят одновременно, в этом случае доза каждого введенного антитела попадает в указанные диапазоны.
Связывающие полипептиды по настоящему описанию можно вводить неоднократно. Интервалы между однократными дозами могут представлять собой еженедельные, ежемесячные или ежегодные. Интервалы могут также являться нерегулярными, как показано по измерению уровней в крови модифицированного связывающего полипептида или антигена у пациента. В некоторых способах, дозу регулируют для достижения концентрации в плазме модифицированного связывающего полипептида 1-1000 мкг/мл и в некоторых способах 25-300 мкг/мл. Альтернативно, связывающие полипептиды можно вводить в форме состава с замедленным высвобождением, в этом случае необходимо менее частое введение. Для антител, доза и частота меняется в зависимости от времени полужизни антитела у пациента. Как правило, для гуманизированных антител показано наиболее длительное время полужизни, со следующими за ними химерными антителами и не относящимися к человеку антителами.
Дозу и частоту введения можно менять в зависимости от того, является ли лечение профилактическим или терапевтическим. В профилактических применениях композиции, содержащие настоящие антитела или их смесь, вводят пациенту, еще не находящемуся в состоянии заболевания, для увеличения устойчивости пациента. Такое количество определяют как являющееся «профилактически эффективной дозой». В этом применении, точные количества снова зависят от состояния здоровья пациента и общего иммунитета, но в общем лежат в диапазоне от 0,1 до 25 мг на дозу, особенно от 0,5 до 2,5 мг на дозу. Относительно низкую дозу вводят в относительно нечастые интервалы в течение длительного периода времени. Некоторым пациентам продолжают проводить лечение в течение их оставшейся жизни. В терапевтических применениях, относительно высокая доза (например, приблизительно от 1 до 400 мг/кг антитела на дозу, где дозы от 5 до 25 мг являются наиболее часто используемыми для радиоиммуноконъюгатов, и более высокие дозы - для модифицированных цитотоксином-лекарственным средством антител) в относительно короткие интервалы иногда необходимы до тех пор, пока прогрессирование заболевания не уменьшится или не прекратится, и предпочтительно, пока для пациента не будет показано частичное или полное облегчение симптомов заболевания. После этого пациенту можно осуществлять введение в профилактическом режиме.
Связывающие полипептиды по настоящему описанию можно, необязательно, вводить в комбинации с другими средствами, которые являются эффективными в лечении нарушения или состояния, нуждающееся в лечении (например, профилактическом или терапевтическом). Эффективные однократные дозы для лечения (т.е. терапевтически эффективные количества) 90Y-меченных модифицированных антител по настоящему описанию лежат в диапазоне между приблизительно 5 и приблизительно 75 мКи, более предпочтительно, между приблизительно 10 и приблизительно 40 мКи. Эффективные однократные не разрушающие костный мозг дозы для лечения 131I-модифицированных антител лежат в диапазоне между приблизительно 5 и приблизительно 70 мКи, более предпочтительно, между приблизительно 5 и приблизительно 40 мКи. Эффективные однократные разрушающие дозы для лечения (т.е. могущие требовать аутологичной трансплантации костного мозга) 131I-меченных антител лежат в диапазоне между приблизительно 30 и приблизительно 600 мКи, более предпочтительно, между приблизительно 50 и менее чем приблизительно 500 мКи. В сочетании с химерным антителом, благодаря более длительному времени полужизни в кровотоке по сравнению с мышиными антителами, эффективные однократные не разрушающие костный мозг дозы для лечения меченных иодом-131 химерных антител лежат в диапазоне между приблизительно 5 и приблизительно 40 мКи, более предпочтительно, менее чем приблизительно 30 мКи. Критерии получения изображений, например, для метки 111In, составляют, как правило, менее чем приблизительно 5 мКи.
В то время как связывающие полипептиды можно вводить, как описано непосредственно выше, необходимо подчеркнуть, что в других вариантах осуществления связывающие полипептиды можно вводить в остальном здоровым пациентам в качестве терапии первой линии. В таких вариантах осуществления связывающие полипептиды можно вводить пациентам, обладающим нормальными или средними ресурсами красного костного мозга, и/или пациентам, которых не подвергали и не подвергают. Как применяют в настоящем документе, введение модифицированных антител или их фрагментов в сочетании или в комбинации с вспомогательной терапией обозначает последовательное, одновременное, одинаковое по протяженности, параллельное, сопутствующее или совпадающее по времени введение или применение терапии и описанных антител. Специалистам в данной области понятно, что введение или применение различных компонентов режима комбинированной терапии можно регулировать по времени для увеличения общей эффективности лечения. Например, химиотерапевтические средства можно вводить в стандартных, хорошо известных курсах лечения с последующими несколькими неделями с радиоиммуноконъюгатами по настоящему описанию. И наоборот, ассоциированные с цитотоксином связывающие полипептиды можно вводить внутривенно с последующей локализованной в опухоли наружной дистанционной лучевой терапией. В других вариантах осуществления модифицированный связывающий полипептид можно вводить параллельно с одним или несколькими избранными химиотерапевтическими средствами за одно посещение клиники. Специалист в данной области (например, опытный онколог) легко может определять эффективные режимы комбинированной терапии без излишнего экспериментирования на основании избранной вспомогательной терапии и объяснений в настоящем описании.
В этой связи следует понимать, что комбинацию связывающих полипептидов и химиотерапевтического средства можно вводить в любом порядке и внутри любых временных рамок, обеспечивающих терапевтическое преимущество для пациента. То есть, химиотерапевтическое средство и связывающие полипептиды можно вводить в любом порядке или параллельно. В избранных вариантах осуществления связывающие полипептиды по настоящему описанию вводят пациентам, которых ранее подвергали химиотерапии. В других вариантах осуществления лечение связывающими полипептидами и химиотерапевтическим средством можно проводить по существу одновременно или параллельно. Например, пациенту можно вводить связывающие полипептиды при подвергании курсу химиотерапии. В предпочтительных вариантах осуществления модифицированное антитело вводят в пределах одного года от любого химиотерапевтического средства или лечения. В других предпочтительных вариантах осуществления связывающие полипептиды вводят в пределах 10, 8, 6, 4 или 2 месяцев от любого химиотерапевтического средства или лечения. В других предпочтительных вариантах осуществления связывающий полипептид вводят в пределах 4, 3, 2 или 1 недели(недель) от любого химиотерапевтического средства или лечения. В других вариантах осуществления связывающие полипептиды вводят в пределах 5, 4, 3, 2 или 1 суток от избранного химиотерапевтического средства или лечения. Кроме того, следует понимать, что два средства или способа терапии можно применять для пациента в пределах часов или минут (т.е. по существу одновременно).
Кроме того, следует понимать, что связывающие полипептиды по настоящему описанию можно использовать в сочетании или в комбинации с любыми химиотерапевтическими средствами или агентами (например, для обеспечения режима комбинированной терапии), которые прекращают, уменьшают, ингибируют или контролируют рост неопластических клеток in vivo. Иллюстративные химиотерапевтические средства, совместимые с настоящим описанием, включают алкилирующие средства, алкалоиды барвинка (например, винкристин и винбластин), прокарбазин, метотрексат и преднизон. Комбинация из четырех лекарственных средств MOPP (мехлетамин (азотистый иприт), винкристин (онковин), прокарбазин и преднизон) является очень эффективной для лечения различных типов лимфомы и составляет предпочтительный вариант осуществления по настоящему описанию. У устойчивых к MOPP пациентов можно использовать комбинации ABVD (например, адриамицин, блеомицин, винбластин и декарбазин), ChIVPP (хлорамбуцил, винбластин, прокарбазин и преднизон), CABS (ломустин, доксорубицин, блеомицин и стрептозотоцин), MOPP плюс ABVD, MOPP плюс ABV (доксорубицин, блеомицин и винбластин) или BCVPP (кармустин, циклофосфамид, винбластин, прокарбазин и преднизон). См. в Arnold S. Freedman and Lee M. Nadler, Malignant Lymphomas, in HARRISON'S PRINCIPLES OF INTERNAL MEDICINE 1774-1788 (Kurt J. Isselbacher et al, eds., 13th ed. 1994) и V. T. DeVita et al, (1997) и процитированных в них ссылках на стандартные дозы и расписание. Эти способы терапии можно использовать без изменений или изменять, как необходимо для конкретного пациента, в комбинации с одним или несколькими связывающими полипептидами по настоящему описанию, как описано в настоящем документе.
Дополнительные режимы, которые можно использовать в контексте настоящего описания, включают отдельные алкилирующие средства, такие как циклофосфамид или хлорамбуцил, или комбинации, такие как CVP (циклофосфамид, винкристин и преднизон), CHOP (CVP и доксорубицин), C-MOPP (циклофосфамид, винкристин, преднизон и прокарбазин), CAP-BOP (CHOP плюс прокарбазин и блеомицин), m-BACOD (CHOP плюс метотрексат, блеомицин и лейковорин), ProMACE-MOPP (преднизон, метотрексат, доксорубицин, циклофосфамид, этопозид и лейковорин плюс стандартный MOPP), ProMACE-CytaBOM (преднизон, доксорубицин, циклофосфамид, этопозид, цитарабин, блеомицин, винкристин, метотрексат и лейковорин) и MACOP-B (метотрексат, доксорубицин, циклофосфамид, винкристин, фиксированная доза преднизона, блеомицин и лейковорин). Специалисты в данной области могут легко определять стандартные дозы и расписание для каждого из этих режимов. CHOP также комбинируют с блеомицином, метотрексатом, прокарбазином, азотистым ипритом, арабинозидом цитозина и этопозидом. Другие совместимые химиотерапевтические средства включают, но без ограничения, 2-хлордезоксиаденозин (2-CDA), 2'-дезоксикоформицин и флударабин.
Для пациентов с NHL со средней и высокой степенью злокачественности, для которых не удалось достичь ремиссии, или с рецидивом, можно использовать терапию спасения. В способах терапии спасения используют такие лекарственные средства, как арабинозид цитозина, карбоплатин, цисплатин, этопозид и ифосфамид, введенные по отдельности или в комбинации. При рецидивирующих или агрессивных формах конкретных неопластических нарушений часто используют следующие протоколы: IMVP-16 (ифосфамид, метотрексат и этопозид), MIME (этилметил-gag, ифосфамид, метотрексат и этопозид), DHAP (дексаметазон, высокая доза цитарабина и цисплатин), ESHAP (этопозид, метилпреднизолон, HD цитарабин, цисплатин), CEPP(B) (циклофосфамид, этопозид, прокарбазин, преднизон и блеомицин) и CAMP (ломустин, митоксантрон, цитарабин и преднизон), где для каждого хорошо известны частоты и расписания дозирования.
Количество химиотерапевтического средства для использования в комбинации с модифицированными антителами по настоящему описанию можно изменять для субъекта или можно вводить в соответствии с тем, что известно в данной области. См. например, Bruce A Chabner et al, Antineoplastic Agents, in GOODMAN & GILMAN'S THE PHARMACOLOGICAL BASIS OF THERAPEUTICS 1233-1287 ((Joel G. Hardman et al, eds., 9th ed. 1996).
Как обсуждали ранее, связывающие полипептиды по настоящему описанию, их иммунореактивные фрагменты или рекомбинантные варианты можно вводить в фармацевтически эффективном количестве для лечения in vivo нарушений у млекопитающих. В этой связи, следует понимать, что описанные связывающие полипептиды можно составлять для облегчения введения и повышения стабильности активного средства.
Предпочтительно, фармацевтические композиции в соответствии с настоящим описанием содержат фармацевтически приемлемый, нетоксичный, стерильный носитель, такой как физиологический солевой раствор, нетоксичные буферы, консерванты и т.п.. Для целей по настоящей заявке, фармацевтически эффективное количество модифицированного связывающего полипептида, его иммунореактивного фрагмента или рекомбинантного варианта, конъюгированного или неконъюгированного с лекарственным средством, следует поддерживать в среднем количестве, достаточном для достижения эффективного связывания с антигеном и для достижения преимущества, например, для облегчения симптомов заболевания или нарушения, или для детекции вещества или клетки. В случае клеток опухолей, модифицированный связывающий полипептид предпочтительно способен взаимодействовать с избранными иммунореактивными антигенами на неопластических или иммунореактивных клетках и обеспечивать увеличение гибели этих клеток. Разумеется, фармацевтические композиции по настоящему описанию можно вводить в однократной или множественных дозах для предоставления фармацевтически эффективного количества модифицированного связывающего полипептида.
В соответствии с объемом настоящего описания, связывающие полипептиды из описания можно вводить человеку или другому животному в соответствии с вышеупомянутыми способами лечения в количестве, достаточном для оказания терапевтического или профилактического эффекта. Связывающие полипептиды из описания можно вводить такому человеку или другому животному в общепринятой лекарственной форме, полученной комбинацией антитела из описания с общепринятым фармацевтически приемлемым носителем или разбавителем в соответствии с известными способами. Специалисту в данной области известно, что форма и характер фармацевтически приемлемого носителя или разбавителя продиктованы количеством активного ингредиента, с которым его следует комбинировать, способом введения и другими хорошо известными переменными. Специалистам в данной области, кроме того, известно, что можно доказать, что смесь, содержащая один или несколько видов связывающих полипептидов, описанных в настоящем описании, является особенно эффективной.
IX. Экспрессия связывающих полипептидов
В одном аспекте изобретение относится к полинуклеотидам, кодирующим связывающие полипептиды, описанные в настоящем документе. Представлен также способ получения связывающего полипептида, включающий экспрессию этих полинуклеотидов.
Полинуклеотиды, кодирующие связывающие полипептиды, описанные в настоящем документе, как правило, вставляют в экспрессирующий вектор для введения в клетки-хозяева, которые можно использовать для продукции желательного количества заявленных антител или их фрагментов. Соответственно, в конкретных аспектах, изобретение относится к экспрессирующим векторам, содержащим полинуклеотиды, описанные в настоящем документе, и к клеткам-хозяевам, содержащим эти векторы и полинуклеотиды.
Термин «вектор» или «экспрессирующий вектор» применяют в настоящем документе для целей описания и формулы изобретения, для обозначения векторов, используемых в соответствии с настоящим изобретением в качестве носителя для введения желаемого гена в клетку и экспрессии желаемого гена в клетке. Как известно специалистам в данной области, такие векторы можно легко выбирать из группы, состоящей из плазмид, фагов, вирусов и ретровирусов. Как правило, векторы, совместимые с настоящим изобретением, обладают селективным маркером, подходящими участками рестрикции для облегчения клонирования желательного гена и способностью входить в эукариотические или прокариотические клетки, и/или реплицироваться в них.
Многочисленные системы экспрессирующих векторов можно использовать для целей по этому изобретению. Например, в одном классе векторов используют элементы ДНК, происходящие из вирусов животных, таких как вирус папилломы крупного рогатого скота, вирус полиoмы, аденовирус, вирус осповакцины, бакуловирус, ретровирусы (RSV, MMTV или MOMLV) или вирус SV40. Другие включают использование полицистронных систем с внутренними участками связывания рибосом. Кроме того, клетки, обладающие ДНК, интегрированной в их хромосомы, можно отбирать посредством введения одного или нескольких маркеров, позволяющих отбор трансфицированных клеток-хозяев. Маркер может придавать прототрофность ауксотрофному хозяину, устойчивость к биоцидам (например, антибиотикам) или устойчивость к тяжелым металлам, таким как медь. Ген селективного маркера можно либо напрямую связывать с последовательностями ДНК, подлежащими экспрессии, либо вводить в одну и ту же клетку посредством совместной трансформации. Дополнительные элементы также могут потребоваться для оптимального синтеза мРНК. Эти элементы могут включать сигнальные последовательности, сигналы сплайсинга, так же как транскрипционные промоторы, энхансеры и сигналы терминации. В особенно предпочтительных вариантах осуществления клонированные гены вариабельной области вставляют в экспрессирующий вектор вместе с генами константной области тяжелой и легкой цепи (предпочтительно, человеческими), синтезированными, как обсуждали выше.
В других предпочтительных вариантах осуществления связывающие полипептиды по изобретению можно экспрессировать с использованием полицистронных конструкций. В таких системах экспрессии множество представляющих интерес продуктов генов, таких как тяжелые и легкие цепи антител, можно получать с одной полицистронной конструкции. В этих системах преимущественно используют внутренний участок связывания рибосомы (IRES) для обеспечения относительно высоких уровней полипептидов по изобретению в эукариотических клетках-хозяевах. Совместимые последовательности IRES описаны в Патенте США № 6193980, содержание которого приведено в настоящем документе путем ссылки. Специалистам в данной области понятно, что такие системы экспрессии можно использовать для эффективного получения полного диапазона полипептидов, описанных в настоящем описании.
В более общем смысле, после получения вектора или последовательности ДНК, кодирующей антитело или его фрагмент, экспрессирующий вектор можно вводить в подходящую клетку-хозяина. То есть, клетки-хозяева можно трансформировать. Введение плазмиды в клетку-хозяина можно осуществлять различными способами, хорошо известными специалистам в данной области. Они включают, но без ограничения, трансфекцию (включая электрофорез и электропорацию), слияние протопластов, преципитацию фосфатом кальция, слияние клеток с покрытой оболочкой ДНК, микроинъекцию и инфекцию интактным вирусом. См., Ridgway, A. A. G. «Mammalian Expression Vectors» Chapter 2422, pp. 470-472 Vectors, Rodriguez and Denhardt, Eds. (Butterworths, Boston, Mass. 1988). Наиболее предпочтительно, введение плазмиды в хозяина происходит посредством электропорации. Трансформированные клетки выращивают в условиях, подходящих для продукции легких цепей и тяжелых цепей, и анализируют синтез белка для тяжелой и/или легкой цепи. Иллюстративные способы анализа включают твердофазный иммуноферментный анализ (ELISA), радиоиммунный анализ (RIA) или анализ сортировки клеток с активацией флуоресценции (FACS), иммуногистохимию и т.п.
Как применяют в настоящем документе, термин «трансформация» следует использовать в широком смысле для обозначения введения ДНК в клетку-хозяина - реципиента, которое изменяет генотип и впоследствии приводит к изменению в клетке-реципиенте.
Среди одних и тех же линий, «клетки-хозяева» относятся к клеткам, трансформированным векторами, конструированными с использованием способов рекомбинантной ДНК и кодирующими по меньшей мере один гетерологичный ген. В описаниях способов выделения полипептидов из рекомбинантных хозяев, термины «клетка» и «культура клеток» используют взаимозаменяемо для обозначения источника антитела, если явно не указано иначе. Иными словами, выделение полипептида из «клеток» может означать выделение либо из осажденных центрифугированием цельных клеток, либо из культуры клеток, содержащих как среду, так и суспендированные клетки.
В одном варианте осуществления линия клеток-хозяев, использованная для экспрессии антитела, происходит из млекопитающих; специалисты в данной области могут определять конкретные линии клеток-хозяев, лучше всего подходящие для желательного продукта гена, подлежащего экспрессии в настоящем документе. Иллюстративные линии клеток-хозяев включают, но без ограничения, DG44 и DUXB11 (линии яичников китайского хомяка, DHFR минус), HELA (карцинома шейки матки человека), CVI (линия почек человека), COS (производное CVI с T-антигеном SV40), R1610 (фибробласты китайского хомяка) BALBC/3T3 (фибробласты мыши), HAK (линия почек хомяка), SP2/O (миелома мыши), BFA-1c1BPT (бычьи эндотелиальные клетки), RAJI (лимфоциты человека), 293 (почка человека). В одном варианте осуществления линия клеток обеспечивает измененное гликозилирование, например, афукозилирование, экспрессированного из нее антитела (например, PER.C6.RTM. (Crucell) или линии клеток CHO с нокаутом FUT8 (клетки Potelligent.RTM.) (Biowa, Princeton, N.J.)). В одном варианте осуществления можно использовать клетки NS0. Клетки CHO являются особенно предпочтительными. Линии клеток-хозяев, как правило, доступны из коммерческих организаций, из Американской коллекции типовых культур или из опубликованной литературы.
Продукция in vitro позволяет масштабирование для получения более крупных количеств желательных полипептидов. Способы культивирования клеток млекопитающих в условиях культивирования тканей известны в данной области и включают культивирование в гомогенной суспензии, например, в аэролифтном реакторе или в реакторе с непрерывным перемешиванием, или в иммобилизованной или связанной культуре клеток, например, в полых волокнах, микрокапсулах, на агарозных микробусинах или в керамических картриджах. Если необходимо и/или желательно, растворы полипептидов можно очищать общепринятыми способами хроматографии, например, гель-фильтрацией, ионообменной хроматографией, хроматографией на DEAE-целлюлозе и/или (иммуно-)аффинной хроматографией.
Гены, кодирующие связывающие полипептиды по изобретению, можно также экспрессировать в не относящихся к млекопитающим клеткам, таких как бактерии или дрожжи, или в клетках растений. В этой связи следует понимать, что различные одноклеточные не относящиеся к млекопитающим микроорганизмы, такие как бактерии, также можно трансформировать; т.е. микроорганизмы, способные к росту в культурах или к ферментации. Бактерии, чувствительные к трансформации, включают члены enterobacteriaceae, такие как штаммы Escherichia coli или Salmonella; Bacillaceae, такие как Bacillus subtilis; Pneumococcus; Streptococcus и Haemophilus influenzae. Кроме того, следует понимать, что при экспрессии в бактериях, полипептиды могут становиться частью телец включения. Полипептиды можно выделять, очищать и затем собирать в функциональные молекулы.
В дополнение к прокариотам, можно использовать также эукариотические микроорганизмы. Saccharomyces cerevisiae, или общепринятые пекарские дрожжи, наиболее часто используют среди эукариотических микроорганизмов, хотя ряд других штаммов является общедоступным. Для экспрессии в Saccharomyces обычно используют например, плазмиду YRp7 (Stinchcomb et al., Nature, 282:39 (1979); Kingsman et al., Gene, 7:141 (1979); Tschemper et al., Gene, 10:157 (1980)). Эта плазмида уже содержит ген TRP1, обеспечивающий селективный маркер для мутантного штамма дрожжей с отсутствием способности расти на триптофане, например, ATCC № 44076 или PEP4-1 (Jones, Genetics, 85:12 (1977)). Присутствие локуса trpl в качестве характеристики генома клетки-хозяина дрожжей обеспечивает эффективное окружение для детекции трансформации по росту в отсутствие триптофана.
ПРИМЕРЫ
Настоящее изобретение далее проиллюстрировано следующими примерами, которые не следует рассматривать как дополнительно ограничивающие. Содержание списка последовательностей, фигур и всех ссылок, патентов и опубликованных патентных заявок, процитированных на протяжении этой заявки, явным образом приведено в настоящем документе путем ссылки.
Пример 1. Разработка, получение и характеризация мутантов антитела 2C3 анти-CD-52 с гипергликозилированием
Множество мутаций с гипергликозилированием разработаны в тяжелой цепи антитела анти-CD-52, 2C3, для цели добавления объемной группы на поверхности взаимодействия (например, участка связывания FcRn для модуляции фармакокинетики антитела), для модуляции эффекторной функции антитела посредством изменения его взаимодействия с FcγR или для введения нового участка сшивки для последующей химической модификации для конъюгации эффекторной группы, включая, но без ограничения, лекарственные средства, токсины, цитотоксические средства и радионуклеотиды. Гипергликозилированные мутанты 2C3 указаны в таблице 3.
|
|
1A. Получение мутантов антитела 2C3 анти-CD-52 с гипергликозилированием
Мутацию A114N, обозначенную на основе системы нумерации Kabat, вводили в домен CH1 2C3 посредством мутагенной ПЦР. Для получения полноразмерного антитела домен VH плюс мутантный остаток A114N вставляли посредством независимого от лигирования клонирования (LIC) в вектор pENTR-LIC-IgG1, кодирующий домены CH 1-3 антитела. Все другие мутации вводили в pENTR-LIC-IgG1 посредством сайт-направленного мутагенеза с помощью набора для сайт-направленного мутагенеза QuikChange (Agilent Technologies, Inc., Santa Clara, CA, USA). VH 2C3 WT клонировали в мутантные векторы посредством LIC. Полноразмерные мутанты клонировали в экспрессирующий вектор pCEP4(-E+I)Dest посредством клонирования Gateway. Мутации Fc обозначены на основании системы нумерации EU. Мутации подтверждали посредством секвенирования ДНК. Аминокислотные последовательности тяжелых и легких цепей 2C3 WT и мутантных тяжелых цепей 2C3 указаны в таблице 4. Мутантные аминокислоты выделены серым, и консенсусные участки-мишени гликозилирования, полученные посредством мутации, подчеркнуты.
|
|
|
|
Мутанты и контроль WT трансфицировали в клетки HEK293-EBNA в формате 6-луночного планшета. Как показано на фигуре 9, обнаружено, что уровень экспрессии составляет ~0,1 мкг/мл, как анализировали посредством SDS-PAGE и Вестерн-блоттинга. Экспрессию мутантов в кондиционированных средах измеряли также по связыванию белка A на Biacore. Концентрацию определяли с использованием ответа диссоциации через 6 минут после инъекции на иммобилизованный белок A. Продуцированное в CHO 2C3 WT, серийно разведенное в среде от 90 мкг/мл до 1,5 нг/мл, использовали в качестве стандартной кривой. Концентрации рассчитывали ниже до ~0,2 мкг/мл посредством калибровочной кривой с использованием 4-параметрического соответствия. Как показано на фигуре 9, относительные уровни экспрессии являлись низкими и в основном соответствовали результатам Вестерн-блоттинга.
1B. Верификация гипергликозилирования
Для определения того, введены ли дополнительные участки гликозилирования посредством мутации, белки 2C3 мутантного и дикого типа обрабатывали универсальным дегликозилирующим ферментом PNGase F, и образцы белка анализировали посредством SDS-PAGE и Вестерн-блоттинга. Как показано на фигуре 10, только мутант A114N обладал увеличенной кажущейся молекулярной массой, что указывает на присутствие дополнительного N-связанного углевода.
Препараты антитела в малом масштабе получали для очистки мутантов 2C3 для дальнейшей верификации введения участка гликозилирования. Как показано на фигуре 11, посредством SDS-PAGE подтвердили, что только мутант A114N обладал дополнительными введенными участками гликозилирования.
1C. Свойства связывания мутантов анти-CD-52 2C3
Biacore использовали для сравнения свойств связывания очищенных белков. Мышиный и очищенный SEC FcRn-HPC4 человека иммобилизовали на чипе CM5 посредством присоединения амина. Каждое антитело разводили до 200, 50 и 10 нМ, и инъецировали поверх Fc-рецепторов. Кампат, продуцированное в CHO 2C3 WT и обработанный DEPC кампат включали в качестве положительного и отрицательного контроля. Как показано на фигуре 13, для мутанта Y436S показано приблизительно 2-кратное уменьшение связывания с FcRn человека. Интересно, что связывание этого мутанта с FcRn мыши не было затронуто. Ни одна из других мутаций 2C3 не оказывала какого-либо значительного влияния на связывание с FcRn человека или мыши.
Biacore использовали для сравнения антигенсвязывающих свойств очищенных белков с использованием анализа связывания Biacore пептида 741 CD-52. Пептид 741 CD-52 и контрольный пептид 777 иммобилизовали на чипе CM5. Антитела серийно разводили в 2 раза от 60 до 0,2 нМ в HBS-EP и инъецировали в двух повторах в течение 3 мин с последующими 5 мин диссоциации в буфере при скорости потока 50 мкл/мин. Партию 17200-084 GLD52 включали в качестве контроля. Поверхность регенерировали с помощью 1 импульса 40 мМ HCl. Модель связывания 1:1 использовали для подбора кривых от 7,5 до 0,2 нМ. Как показано на фигуре 16, мутант A114N обладал немного более низкой аффинностью связывания CD-52, в то время как мутант NGT обладал немного более высокой аффинностью, чем остальные мутанты в этом анализе. Анализ связывания Biacore пептида 741 CD-52 повторяли с белком, очищенным из препарата более крупного масштаба. Как показано на фигуре 17, для мутанта A114N показано связывание пептида CD-52, сравнимое с WT 2C3.
1D. Характеризация заряда мутанта A114N
Изоэлектрическое фокусирование (IEF) проводили для характеризации заряда мутантов 2C3. Очищенный белок разделяли в акриламидных гелях с фиксированным градиентом pH (pH3-10) (IPG). Как показано на фигуре 18A, обнаружено, что A114N обладает более отрицательным зарядом, вероятно, из-за остатков сиаловой кислоты. Данные интактной MS подтвердили комплексную структуру с сиаловыми кислотами на мутанте A114N. В отличие от этого, показано, что 2C3 WT обладает G0F и G1F в качестве доминантных видов гликозилирования (фигуры 18C и 18D, соответственно).
Пример 2. Получение мутантов с гипергликозилированием в остовах нескольких антител
В дополнение к антителу 2C3 против CD-52, мутацию A114N конструировали в остовах нескольких других антител для подтверждения того, что уникальный участок гипергликозилирования можно вводить в неродственные последовательности вариабельного домена тяжелой цепи. Гипергликозилированные мутанты анти-TEM1, анти-FAP, и анти-Her2 указаны в таблице 5.
|
2A. Получение мутантов антител анти-TEM1 и анти-FAP с гипергликозилированием
Мутацию A114N, обозначенную на основе системы нумерации Kabat, вводили в домен CH1 анти-TEM1 и анти-FAP посредством мутагенной ПЦР. Для получения полноразмерного антитела мутантный VH плюс остаток 114 вставляли посредством независимого от лигирования клонирования (LIC) в вектор pENTR-LIC-IgG1, кодирующий домены CH 1-3 антитела. Затем полноразмерные мутанты клонировали в экспрессирующий вектор pCEP4(-E+I)Dest посредством клонирования Gateway. Мутации подтверждали посредством секвенирования ДНК. Аминокислотные последовательности анти-TEM1 дикого типа и мутантных тяжелых и легких цепей указаны в таблице 6. Мутантные аминокислоты выделены серым, и консенсусные участки-мишени гликозилирования, полученные посредством мутации, подчеркнуты.
|
|
Мутанты и контроль дикого типа трансфицировали в клетки HEK293-EBNA в формате трех повторов флаконов и очищали на колонках HiTrap с белком A (GE Healthcare Biosciences, Pittsburgh, PA, USA). Как анализировано по A280 на спектрофотометре NanoDrop, экспрессия анти-FAP A114N и анти-FAP A114C составляла приблизительно 3 мкг/мл и приблизительно 1 мкг/мл, соответственно. Экспрессия анти-TEM1 A114N составляла приблизительно 0,04 мкг/мл.
2B. Верификация гипергликозилирования
Для подтверждения того, что дополнительный участок гликозилирования введен в мутанты A114N, очищенный белок из мутантов A114N анализировали в восстанавливающем SDS-PAGE вместе с контрольным белком дикого типа. Один дополнительный участок гликозилирования может добавлять 2000-3000 Дальтон к молекулярной массе тяжелой цепи. Как показано на фигуре 20, SDS-PAGE показал, что полосы мутантов A114N тяжелой цепи анти-FAP и анти-TEM1 обладали увеличенной кажущейся молекулярной массой, согласующейся с успешным введением дополнительного участка гликозилирования в оба антитела.
2C. Получение мутантов антитела анти-Her2 с гипергликозилированием
Антитела против Her-2 A114N, Her-2 A114N/NNAS и Her-2 WT получали посредством независимого от лигирования клонирования. Синтезировали домен VH герцептина и амплифицировали ПЦР с двумя LIC-совместимыми наборами праймеров, либо WT, либо несущими мутацию A114N. Для получения полноразмерного антитела, амплифицированные вставки VH (WT или A114N) клонировали в два вектора pENTR, кодирующих домены CH 1-3, pENTR-LIC-IgG1 WT и pENTR-LIC-IgG1 NNAS, получая три полноразмерных мутанта (A114N, NNAS, A114N/NNAS) и контроль WT в качестве исходных клонов в pENTR. Эти мутанты клонировали в экспрессирующий вектор pCEP4(-E+I)Dest, посредством клонирования Gateway. Мутации подтверждали посредством секвенирования ДНК. Аминокислотные последовательности анти-Her-2 дикого типа и мутантных тяжелых и легких цепей указаны в таблице 7. Мутантные аминокислоты выделены серым, и консенсусные участки-мишени гликозилирования, полученные посредством мутации, подчеркнуты.
|
|
|
2D. Экспрессия мутанта A114N антитела анти-Her2 с гипергликозилированием
Конструкции анти-Her2 A114N и дикого типа трансфицировали с помощью липофектамина-2000 (соотношение реагента к ДНК 2,5:1) и XtremeGene HP (соотношение реагента к ДНК 3:1) в клетки HEK293-EBNA в 12 флаконах в трех повторах. Измерение в Octet аликвот кондиционированной среды (CM) с суток 3 показало, что экспрессия белка являлась согласующейся среди 6 флаконов как для липофектамина-2000, так и для XtremeGene HP. Как показано в таблице 8, общая эффективность трансфекции была приблизительно на 30% выше с XtremeGene HP. Кондиционированные среды, собранные на сутки 3, пулировали вместе для обоих условий трансфекции и очищали на колонке с белком A. Измерение Octet показало 1,8 мкг/мл антитела в содержащих сыворотку средах после ложной трансфекции по сравнении с 0 мкг/мл в не содержащих сыворотку средах после ложной трансфекции.
|
Кондиционированные среды с суток 6 собирали и очищали отдельно для каждых условий трансфекции. Оба элюата подвергали замене буфера в PBS, pH 7,2, и концентрировали в ~15 раз с использованием колонок Amicon-4 (отсечение 50 кДа). Для CM на сутки 6 показан более высокий уровень экспрессии по сравнению с CM на сутки 3. Как показано в таблице 8, всего 3 мг герцептина A114N 15,59 мг/мл (после трансфекции липофектамином) и 6 мг герцептина A114N 16,86 мг/мл (после трансфекции XtremeGene HP) получено из кондиционированной среды на сутки 6 для дополнительных последующих применений, таких как конъюгация антитела-лекарственного средства.
2E. Анализ SDS-PAGE и HIC мутанта A114N анти-Her2
Перед конъюгацией, очищенный герцептин A114N характеризовали посредством SDS-PAGE и HIC (хроматографии гидрофобного взаимодействия). Как показано на фигуре 21, определили, что количество очищенного герцептина A114N являлось пригодным для дальнейших последующих применений.
2F. Конъюгация со сконструированным гликозилированием
Показано, что: a) участок гликозилирования введен в участок положения Kabat 114 на анти-TEM1; b) мутант A114N обладал гипергликозилированием на тяжелой цепи по восстанавливающему SDS-PAGE; и c) гипергликозилированный мутант A114N обладал комплексной углеводной структурой по интактной LC/MS, включая концевые сиаловые кислоты и галактозу, которые являются идеальными для конъюгации SAM и GAM. Чтобы подтвердить, что сконструированный участок гликозилирования являлся пригодным для конъюгации, анти-TEM1 A114N конъюгировали с 5 кДа PEG посредством химических реакций аминооксигруппы. Как показано на фигуре 22, PEG успешно конъюгировали с анти-TEM1 A114N через аминоокси-связь. Этот мутант также успешно получали на остовах анти-FAP и анти-CD-52 2C3 (не показано). Эти данные показывают, что участок гликозилирования на N114 можно использовать для конъюгации эффекторных групп.
Пример 3: Получение мутантов S298N/Y300S Fc
Разрабатывали и получали сконструированные варианты Fc, в которых новый участок гликозилирования вводили в положении EU Ser 298, радом с природным участком Asn297. Гликозилирование на Asn297 либо сохраняли, либо удаляли посредством мутации. Мутации и желательные результаты гликозилирования указаны в таблице 9.
|
|
3A. Получение вариантов антитела H66 αβ-TCR с измененным гликозилированием
Мутации вводили в тяжелую цепь антитела против αβ T-клеточного рецептора клона #66 посредством Quikchange с использованием матрицы pENTR_LIC_IgG1. Домен VH HEBE1 Δab IgG1 #66 амплифицировали с помощью праймеров LIC перед клонированием в pENTR_LIC_IgG1 мутантного или дикого типа посредством LIC для получения полноразмерных антител мутантного или дикого типа. Субклонирование верифицировали с помощью двойного расщепления DraIII/XhoI, образующего вставку размером приблизительно 1250 п.о. в успешных клонах. Эти полноразмерные мутанты затем клонировали в экспрессирующий вектор, pCEP4(-E+I)Dest, посредством клонирования Gateway. Мутации подтверждали посредством секвенирования ДНК. Аминокислотные последовательности тяжелых и легких цепей анти-αβTCR H66 WT и мутантных тяжелых цепей H66 указаны в таблице 10. Мутантные аминокислоты выделены серым, и консенсусные участки-мишени гликозилирования, полученные посредством мутации, подчеркнуты.
|
|
|
Мутантные конструкции, конструкции дикого типа и две агликозилированные контрольные конструкции (HEBE1 Agly IgG4 и HEBE1 Δab IgG1 в pCEP4) трансфицировали в клетки HEK293-EBNA в трех повторах флаконов для экспрессии. Белки очищали из 160 мл кондиционированной среды (CM) с помощью колонок 1 мл HiTrap с белком A (GE) с использованием многоканального перистальтического насоса. Пять микрограмм каждого полученного супернатанта анализировали в 4-20% восстанавливающих с Трис-глицином и невосстанавливающих гелях для SDS-PAGE (см. фигуру 2). Тяжелые цепи агликозилиронных мутантов (N297Q, T299A и контроли Agly), мигрировали дальше (конец стрелки), в соответствии с потерей гликанов в этих антителах. Однако, тяжелые цепи сконструированных гликозилированных антител (NSY, STY, SY, Δab и контроля wt, стрелки), мигрировали сходным образом с контролем дикого типа. Этот результат согласуется с существованием сконструированного участка гликозилирования в положении EU 298. Анализ SEC-HPLC показал, что все мутанты экспрессированы в форме мономеров.
3B. Анализ гликозилирования посредством LC-MS
Сконструированные варианты Fc H66 IgG1 были частично восстановлены с помощью 20 мМ DTT при 37°C в течение 30 мин. Затем образцы анализировали посредством капиллярной LC/MS в системе для капиллярной HPLC Agilent 1100 с присоединенной гибридной системой QSTAR qq TOF (Applied Biosystems). Байесовскую реконструкцию белка с фоновой коррекцией и компьютерным моделированием на Analyst QS 1.1 (Applied Bisoystem) использовали для анализа данных. В мутанте S298N/T299A/Y300S антитела H66, один участок гликозилирования наблюдали на аминокислоте 298, где двухантенные и трехантенные гликаны комплексного типа детектированы как главные виды наряду с G0F, G1F и G2F (см. фигуру 34). Этот измененный профиль гликозилирования согласуется со сдвинутым гликозилированием на N298 вместо участка гликозилирования дикого типа на N297.
3C. Свойства связывания мутантов антитела αβTCR с FcγRIIIa и FcγRI человека с использованием Biacore
Biacore использовали для оценки связывания рекомбинантного FcγRIIIa (V158 и F158) и FcγRI человека. Во всех четырех проточных ячейках на чипе CM5 иммобилизовали антитело анти-HPC4 посредством общепринятого способа связывания амина, предоставленного Biacore. Антитело анти-HPC4 разводили до 50 мкг/мл в 10 мМ ацетате натрия, pH 5,0, для реакции связывания и инъецировали в течение 25 мин при 5 мкл/мин. Приблизительно 12000 RU антитела иммобилизовали на поверхности чипа. Рекомбинантные FcγRIIIa-V158 и FcγRIIIa-F158 человека разводили до 0,6 мкг/мл в буфере для связывания (HBS-P с 1 мМ CaCl2) и инъецировали в проточные ячейки 2 и 4, соответственно, в течение 3 мин при 5 мкл/мин для связывания 300-400 RU рецептора на чипе анти-HPC4. Для установления различий между веществами с низким связыванием, в три раза больше rhFcγRIIIa связывали на поверхности анти-HPC4, чем обычно использовали в этом анализе. Проточные ячейки 1 и 3 использовали в качестве эталонных контролей. Каждое антитело разводили до 200нМ в буфере для связывания и инъецировали поверх всех четырех проточных ячеек в течение 4 мин, с последующими 5 мин диссоциации в буфере. Поверхности регенерировали с помощью 10 мМ ЭДТА в буфере HBS-EP в течение 3 мин при 20 мкл/мин. Результаты этих экспериментов показаны на фигуре 3.
Biacore также использовали для сравнения связывания FcγRI. Антитело анти-тетра-His подвергали замене буфера в 10 мМ ацетате натрия pH 4,0, с использованием обессоливающей колонки Zeba и разводили до 25 мкг/мл в ацетатном буфере для связывания амина. В двух проточных ячейках чипа CM5 иммобилизовали ~9000 RU антитела анти-Тетра-His после 20 мин инъекции при 5 мкл/мин. Как в предыдущем эксперименте, в десять раз больше FcγRI связывали на поверхности с анти-тетра-His для сравнения образцов со слабым связыванием. Рекомбинантный FcγRI человека разводили до 10 мкг/мл в буфере для связывания HBS-EP и инъецировали в проточную ячейку 2 в течение 1 мин при 5 мкл/мин для связывания ~1000 RU рецептора с чипом анти-тетра-His. Одну концентрацию антитела, 100 нМ, инъецировали в течение 3 мин при 30 мкл/мин поверх связанного рецептора и контрольной поверхности. Затем диссоциацию мониторировали в течение трех минут. Затем поверхность регенерировали с помощью 30-секундных инъекций 10 мМ глицина pH 2,5 при 20 мкл/мин. Результаты этих экспериментов показаны на фигуре 4.
Эти результаты показывают явное увеличение связывания мутантов с модифицированным гликозилированием с FcγRIIIa или FcγRI. H66 S298N/T299A/Y300S, в частности, обладает почти полностью уничтоженным связыванием с обоими рецепторами. Этот мутант выбрали для более подробного анализа.
3D. Характеризация стабильности с использованием кругового дихроизма (CD)
Стабильность мутантного антитела S298N/T299A/Y300S мониторировали посредством эксперимента термоплавления Far-UV CD, в котором сигнал CD при 216 нм и 222 нм мониторировали при увеличенной температуре, приводящей к разворачиванию антитела (денатрурации).
Температуру контролировали посредством термоэлектрического элемента Пельтье (Jasco модели AWC100) и увеличивали со скоростью 1°C/мин от 25-89°C. Спектры CD собирали на спектрофотометре Jasco 815 при концентрации белка приблизительно 0,5 мг/мл в буфере PBS в кварцевой кюветы (Hellma, Inc) с длиной пути 10 мм. Скорость сканирования составляла 50 нм/мин, и шаг данных 0,5 нм. Использовали ширину полосы 2,5 нм с установкой чувствительности на среднюю. Сигнал CD и вольтаж HT собирали при 210-260 нм с интервалами данных 0,5 нм и интервалами температуры 1°C, и четыре повтора сканирований проводили для каждого образца. Результаты показывают, что как дельта AB H66, так и мутант S298N/T299A/Y300S H66 обладают сходным термическим поведением и обладают приблизительно одинаковой начальной температурой для деградации (приблизительно 63°C) (фигура 35), что позволяет далее предполагать, что они обладают сравнительной стабильностью.
Пример 4: Функциональный анализ Fc-модифицированных мутантов
Fc-модифицированные мутанты оценивали посредством анализа пролиферации PBMC и анализа высвобождения цитокинов. В анализе пролиферации PBMC, PBMC человека культивировали с увеличивающимися концентрациями терапевтического антитела в течение 72 часов, добавляли 3H-тимидин, и клетки собирали через 18 часов. Для анализа истощения T-клеток/высвобождения цитокинов, PBMC человека культивировали с увеличивающимися концентрациями терапевтического антитела и анализировали ежесуточно количества и жизнеспособность клеток (Vi-Cell, Beckman Coulter) до суток 7. Супернатанты клеток также собирали, хранили при -20°C и анализировали на 8-плексную панель цитокинов (Bio-Rad).
PBMC нормального донора размораживали и обрабатывали в следующих условиях (все в среде, содержащей комплемент): без обработки; BMA031, moIgG2b 10 мкг/мл; OKT3, moIgG2a 10 мкг/мл; H66, huIgG1 дельтаAB 10 мкг/мл, 1 мкг/мл и 0,1 мкг/мл; H66, huIgG1 S298N/T299A/Y300S 10мкг/мл, 1мкг/мл и 0,1 мкг/мл.
Цитокины собирали на сутки 2 (D2) и сутки 4 (D4) для анализа Bioplex (IL2, IL4, IL6, IL8, IL10, GM-CSF, IFNg, TNFa). Клетки окрашивали на D4 по экспрессии CD4, CD8, CD25 и abTCR.
Результаты, показанные на фигурах 5-8, показывают, что поведение H66 S298N/T299A/Y300S было сходным с поведением H66 дельтаAB во всех проведенных анализах на основе клеток, показывая минимальную активацию T-клеток по экспрессии CD25, связывание с abTCR (с немного различной кинетикой для дельтаAB), и минимальное высвобождение цитокинов в обоих временных точках D2 и D4. У мутанта S298N/T299A/Y300S, таким образом, уничтожали эффекторную функцию так эффективно, как мутация дельтаAB.
Пример 5: Получение и характеризация сконструированного варианта Fc в остове антитела анти-CD52.
В дополнение к антителу H66 анти-αβTCR, мутацию S298N/Y300S также конструировали в остове антитела анти-CD52 (клон 2C3). Затем этот мутант исследовали, чтобы определить, являлась ли обнаруженная модуляция эффекторной функции, наблюдаемая в антителе S298N/Y300S H66 анти-αTCR, согласованной в остове другого антитела.
5A. Получение вариантов антитела 2C3 анти-CD52 с измененным гликозилированием
Сначала вариант ДНК 2C3 S298N/Y300S получали посредством мутагенеза с быстрым изменением с использованием pENTR_LIC_IgG1, и VH 2C3 WT клонировали в мутантный вектор посредством LIC. Полноразмерные мутанты клонировали в экспрессирующий вектор pCEP4 (-E+I)Dest с использованием способа Gateway. Мутации затем подтверждали посредством секвенирования ДНК, и последовательности указаны в таблице 11. Затем мутанты трансфицировали в клетки HEK293-EBNA в формате 6-луночного планшета, и белок очищали из кондиционированной среды. Антитело анти-CD52 2C3 дикого типа получали параллельно в качестве контроля. Обнаружили, что уровень экспрессии составляет 0,1 мкг/мл с использованием анализов SD-PAGE и Вестерн-блоттинга (фигура 9A). Экспрессию мутантов в чистых кондиционированных средах также измеряли по связыванию с белком A на Biacore. Концентрацию определяли с использованием ответа диссоциации после шести минут инъекции на иммобилизованный белок A. Продуцированное в CHO 2C3 WT, серийно разведенное в среде от 90 мкг/мл до 1,5 нг/мл, использовали в качестве стандартной кривой. Концентрации рассчитывали около приблизительно 0,2 мкг/мл посредством калибровочной кривой с использованием 4-параметрического соответствия. Относительные уровни экспрессии являлись низкими и в основном соответствовали данным Вестерн-блоттинга (фигура 9B).
|
|
5B. Анализ гликозилирования с использованием PNGaseF
Для оценки дополнительных участков гликозилирования, введенных посредством мутации, обогащенный мутант S298N/Y300S дегликозилировали с помощью PNGase F. Не показано какого-либо кажущегося изменения молекулярной массы, что не присутствовало дополнительного углевода (фигура 10). Проводили выделения в малом масштабе для очистки этих мутантов для дальнейшей характеризации, и результаты повторно подтвердили, что не существовало дополнительного углевода, присутствующего на мутанте S298N/Y300S (фигура 11).
5C. Свойства связывания мутантов антитела анти-CD52 2C3 с FcγRIIIa человека с использованием Biacore
Biacore использовали также характеризации связывания антигена, FcγRIII и свойств связывания очищенных антител (см. фигуры 12, 13 и 14). Вариант S298N/Y300S 2C3 прочно связывался с пептидом CD52, и сенсограмма связывания являлась неотличимой от контроля дикого типа, показывая, что эта мутация не влияет на его связывание антигена (фигура 12A).
Для анализа эффекторной функции Fc, рецептор FcγRIII (Val158) использовали в исследованиях связывания. Мутантное антитело и контрольное антитело дикого типа разводили до 200 нМ и инъецировали на связанный с HPC4-tag FcγRIIIa. Связывание FcγRIII являлось почти не поддающимся детекции для мутанта S298N/Y300S, что указывает на потерю эффекторной функции этим вариантом (фигура 12B и фигура 14A). Для дальнейшего анализа эффекторной функции Fc, рецептор FcγRIII (Phe158) также использовали в исследованиях. Мутантное антитело и контрольное антитело дикого типа разводили до 200 нМ и инъецировали на связанный с HPC4-tag FcγRIIIa. Связывание FcγRIII являлось почти не поддающимся детекции для мутанта S298N/Y300S, что указывает на потерю эффекторной функции вариантом Phe158 (фигура 14B). Наконец, Biacore использовали для сравнения свойств связывания с FcRn очищенных белков. Мышиный и очищенный SEC FcRn-HPC4 человека иммобилизовали на чипе CM5 посредством присоединения амина. Каждое антитело разводили до 200, 50 и 10 нМ, и инъецировали поверх рецепторов. Кампат, продуцированное в CHO 2C3 WT и обработанный DEPC кампат включали в качестве положительного и отрицательного контроля. Эти данные показывают, что мутант связывается с рецептором FcRn как человека, так и мыши, с такой же аффинностью, как контрольное антитело дикого типа, и что вероятно не присутствует изменений времени полужизни в кровотоке или других фармакокинетических свойств. (см. фигуру 12C, фигуру 13A и B). Соответственно, мутация S298N/Y300S является применимой для антител в общем, для уменьшения или уничтожения нежелательной эффекторной функции Fc, например, посредством вовлечения рецепторов Fcγ человека.
Пример 6: Детекция циркулирующего иммунного комплекса для мутанта S298N/Y300S.
Детекцию циркулирующего иммунного комплекса также исследовали с использованием анализа связывания C1q для мутанта S298N/Y300S и контроля WT. 96-луночные планшеты Costar с высоким связыванием покрывали в течение ночи при 4°C 100 мкл 2C3 Ab в 2-кратном серийным разведении в концентрациях, лежащих в диапазоне 10-0,001 мкг/мл в буфере для покрытия (0,1 М NaCHO3 pH 9,2). Анализ ELISA показал, что связывание C1q уменьшено для мутанта S298N/Y300S по сравнению с WT (фигура 15A). Связывание анти-Fab Ab с покрытием 2C3 Ab подтвердило эквивалентное покрытие лунок (фигура 15B).
Пример 7: Разделение и анализ мутанта S298N/Y300S с использованием изоэлектрического фокусирования.
Изоэлектрическое фокусирование (IEF) в геле pH 3-10 проводили для характеризации мутантов S298N/Y300S. Обнаружено, что S298/Y300S обладает более отрицательными зарядами, и таким образом, вероятно, большим количеством молекул сиаловой кислоты (фигура 18A). По интактной MS показано, что как мутант S298N/Y300S, так и WT 2C3 обладают G0F и G1F в качестве доминантных видов гликозилирования (фигура 18 B и D, соответственно).
Пример 8: Аффинность связывания антигена S298N/Y300S.
Biacore использовали для сравнения аффинности связывания антигена для анти-CD52 Ab 2C3 WT и мутанта S298N/Y300S, которые получали и очищали после экспрессии как в более малом (фигура 16), так и более крупном масштабе (фигура 17). Получали чипы CM5 с иммобилизованным пептидом 741 CD52 и контрольным пептидом 777. Получали серийные 2-кратные разведения антитела от 60 до 0,2 нМ в HBS-EP и затем инъецировали поверх поверхности чипа в течение 3 мин с последующей 5 мин диссоциацией в буфере при скорости потока 50 мкл/мин. Затем поверхность регенерировали с помощью импульса 40 мМ HCl. Эти анализы проводили в двух повторах и показали, что мутант S298N/Y300S и WT антитела 2C3 обладают сравнимым связыванием пептида CD52.
Разработали платформу для скрининга среды для тестирования функциональных свойств связывания перед очисткой, чтобы проводить скрининг антител, полученных в ходе трансфекций в малом масштабе. Эти тесты проводили с использованием Octet (фигура 19A) для определения концентрации и использовали биосенсоры с белком A и стандартную кривую GLD52. Образцы разводили до 7,5 и 2 нМ в HBS-Ep для сравнения связывания CD52 с использованием Biacore (фигура 19B). Результаты анализы связывания пептида показали, что как мутант S298N/Y300S, так и WT антитела 2C3 обладают сравнимым связыванием пептида CD52. Более того, эти анализы показали, что Octet и Biacore хорошо действуют для предсказания связывания антигена антителами из трансфекций малого масштаба.
Пример 9: Получение мутантов S298N/Y300S, S298N/T299A/Y300S и N297Q/S298N/Y300S с измененным гликозилированием в остовах дополнительных антител.
В дополнение к антителу анти-αβ-TCR и антителу анти-CD-52 2C3, мутации S298/Y300S, S298N/T299A/Y300S и N297Q/S298N/Y300S конструировали в остовах других антител для подтверждения того, что дополнительный тандемный участок гликозилирования можно вводить в неродственные последовательности вариабельного домена тяжелой цепи. Мутанты анти-CD-52 12G6 и анти-Her2 c альтернативным гликозилированием указаны в таблицах 12 и 13.
|
|
|
|
|
Пример 10. Получение измененных антител, содержащих реакционноспособные группы гликана
Для получения антител, содержащих группы гликана, способные вступать в реакцию с дериватизированными эффекторными группами, антитело анти-HER сначала гликозилировали in vitro с использованием гликозилтрансферазы и соответствующих доноров UDP-сахара. Например, для введения сиаловой кислоты, донорные антитела сначала галактозилировали с помощью β-галактозилтрансферазы, с последующим сиалированием с помощью α2,6-сиалилтрансферазы в соответствии со способами Kaneko et al. (Kaneko, Y., Nimmerjahn, F., and Ravetch, J. V. (2006) Anti-inflammatory activity of immunoglobulin G resulting from Fc sialylation. Science 313, 670-3). Реакцию проводили на стадии синтеза в одном реакторе с использованием β-галактозилтрансферазы (50 мЕд./мг, Sigma) и α2,6-сиалилтрансферазы (5 мкг/мг, R&D system) с субстратами - донорами сахарных нуклеотидов, UDP-галактозы (10 мМ) и CMP-сиаловой кислоты (10 мМ) в буфере 50 мМ MES (pH 6,5), содержащем 5 мМ MnCl2. Реакционную смесь, содержащую 5 мг/мл антитела анти-HER2, инкубировали в течение 48 часов при 37°C. Сиалирование верифицировали с использованием анализа MALDI-TOF MS перметилированных гликанов, высвобожденных из антитела с помощью PNGase F, анализа содержания сиаловой кислоты с использованием Dionex HPLC и блоттинга с лектином SNA, лектином, специфическим для α2,6-сиаловой кислоты.
Анализ MALDI-TOF гликанов, высвобожденных посредством обработки PNGase F сиалированного антитела анти-HER2, показал, что нативные гликаны были полностью ремоделированы с в основном моносиалированной двухантенной структурой, A1F (фигура 27A) вместе с небольшим количеством дисиалированных видов. Обработкой антитела более высокими количествами α2,6-сиалилтрансферазы получали более гомогенные популяции гликоформы A1F, что позволяет предполагать, что либо активность фермента, либо локализация гликана может предотвращать полное сиалирование. Определили, что содержание сиаловой кислоты составляло ~2 моль на моль антитела, что согласуется с гликаном A1F в качестве главных видов гликоформ (фигура 27B). Лектиновый блоттинг с лектином SAN, агглютинином Sambucus nigra, специфическим для α2,6-связанной сиаловой кислоты, подтвердил, что сиаловая кислота присутствует в конфигурации с α2,6-связью (фигура 27C).
В заключение, хотя гликаны природного белка являются несколько гетерогенными, ремоделирование посредством галактозил- и сиалилтрансфераз приводит к почти гомогенному антителу с моносиалированными, но полностью галактозилированными двухантенными гликанами (A1F). Введение только ~1 сиаловой кислоты на два галактозных акцептора на каждом разветвленном гликане может быть обусловлено ограниченной доступностью одной из галактоз из гликанов, которые часто углублены в антитело, или нековалентными взаимодействиями гликанов с поверхностью белка.
Пример 11. Окисление измененных антител, содержащих реакционноспособные группы гликанов
После верификации сиалирования, исследовали окисление в ходе процесса сиалированного антитела анти-HER2 с помощью различных концентраций периодата (0,25-2 мМ). Сиалированное антитело сначала подвергали замене буфера в 25 мМ Tris-HCl (pH 7,5), содержащем 5 мМ ЭДТА, с последующей заменой буфера с помощью буфера PBS. Затем забуференную смесь антител наносили колонку с сефарозой с белком A, предварительно уравновешенной с помощью буфера PBS. После промывки колонки 15 объемами колонки PBS, 15 объемами колонки PBS, содержащим 5 мМ ЭДТА, и 30 объемами колонки PBS, затем проводили элюцию 25 мМ цитратно-фосфатным буфером (pH 2,9). Элюаты немедленно нейтрализовали с помощью двухосновного фосфатного буфера, и антитело концентрировали с использованием Amicon ultra из Millipore. После очистки сиалированное антитело анти-HER2 затем окисляли с помощью периодата натрия (Sigma) в буфере 100 мМ ацетате натрия (pH 5,6) на льду в темноте в течение 30 минут, и реакцию останавливали с помощью 3% глицерина на льду в течение 15 минут. Продукт подвергали обессоливанию и смене буфера на 100 мМ ацетат натрия (pH 5,6) посредством 5 циклов ультрафильтрации через 50 кДа Amicons. На фигуре 28A показан анализ содержания сиаловой кислоты сиалированного антитела, титрованной с различными количествами периодата. Полного окисления остатков сиаловой кислоты достигали при концентрации периодата выше 0,5 мМ. Действительно, концентрация периодата, настолько низкая, как 0,5 мМ, являлась достаточной для полного окисления введенной сиаловой кислоты. Соответственно, концентрацию периодата 1 мМ выбрали для окисления сиалированного антитела для конъюгации лекарственного средства.
Окисление может оказывать неблагоприятные эффекты на целостность антитела. Для окисления остатков метионина, включая Met-252 и Met-428, локализованные в области CH3 Fc, близко к участкам связывания FcRn, известно влияние на связывание FcRn, которое является критическим для продления времени полужизни антитела в сыворотке (Wang, W., et al. (2011) Impact of methionine oxidation in human IgG1 Fc on serum half-life of monoclonal antibodies. Mol Immunol 48, 860-6). Соответственно, для оценки потенциальных побочных эффектов окисления периодатом на остатки метионина (например, Met-252), критические для взаимодействия с FcRn, состояние окисления сиалированного антитела определяли по анализу LC/MS расщепления пептидов трипсином. Этот анализ выявил ~30% окисление Met-252 и <10% окисление Met-428 после обработки сиалированного трастузумаба 1 мМ периодатом. Для определения вклада этой степени окисления метионина в связывание FcRn, кинетику связывания FcRn для каждого антитела оценивали с использованием поверхностного плазмонного резонанса (BIACORE). Этот анализ выявил, что состояние окисления коррелировало с незначительной потерей связывания FcRn (12% и 26% уменьшение Ka для FcRn мыши и человека, см. фигуры 28B и 28C, соответственно). Следует отметить, опубликовано, что ~25% уменьшение Ka для FcRn человека не оказывает эффект на время полужизни в сыворотке в трансгенной мыши с FcRn человека, поскольку отдельный интактный участок FcRn на каждом антителе является достаточным для обеспечения функциональности и преимуществ PK (Wang et al., там же).
В общем, эти данные показывают, что введение чувствительных к периодату остатков сиаловой кислоты посредством обработки сиалилтрансферазой позволяет использование намного более низких концентраций периодата, приводя к минимальным побочным эффектам на взаимодействия антитело-FcRn и целостность антитела, как оценивали по агрегации (≤1%). Таким образом, использование сиалированных антител в соответствии со способами по изобретению обеспечивает более широкое окно условий окисления, позволяющее воспроизводимое получение активных гликоконъюгатов без эффекта на время полужизни в сыворотке.
Галактозу в мутанте антитела с гипергликозилированием можно также окислять специфически с использованием оксидазы галактозы для получения альдегидной группы для конъюгации. Для подтверждения этого способа, антитело анти-TEM1 A114N концентрировали до 13-20 мг/мл и затем обрабатывали с помощью 20 мЕд./мг сиалидазы в PBS в течение 6 часов при 37°C. Десиалированный продукт затем окисляли с помощью оксидазы галактозы («GAO»), сначала с 5 мкг GAO/мг белка в течение ночи при 37°C с последующим добавлением 2 мкг GAO/мг белка и инкубацией в течение дополнительных 5 часов. Ацетат натрия добавляли для доведения pH до 5,6 (0,1 об./об., pH5,6), и DMSO добавляли для достижения конечной концентрации в реакционной смеси 16%, добавляли до конъюгации. Мутант A114N антитела анти-HER с гипергликозилированием (15 мг/мл) сходным образом десиалировали с помощью сиалидазы (20 мЕд./мг) и окисляли с помощью 5 мкг GAO на мг белок в одной реакционной смеси в течение ночи при 37°C.
Пример 12. Синтез реакционноспособных эффекторных групп
Для облегчения конъюгации с дериватизированных альдегидом гликоформ антитела по изобретению, эффекторные группы лекарственных средств-кандидатов (например, монометилауристатин E (MMAE) и доластатин 10 (Dol10)) дериватизировали с помощью аминооксицистамида, чтобы они содержали функциональные группы (например, аминоокси-цис) со специфической реакционной способностью для альдегида.
Кратко, для получения аминооксицистамида в качестве исходного материала, S-тритил-L-цистеинамид (362 мг, 1 ммоль) добавляли к 3 мл раствора в DMF N-гидроксисукцинимидного сложного эфира т-BOC-аминооксиуксусной кислоты (289 мг, 1 ммоль). Реакция завершалась через 3 час, как очевидно из анализа HPLC. Затем реакционную смесь разводили с помощью 30 мл дихлорметанэтана и промывали раствором 0,1 M бикарбоната натрия (2 × 20 мл), водой (2 × 20 мл), и рассолом (2 × 20 мл). Раствор сушили над безводным сульфатом натрия, фильтровали и концентрировали до сухости. К этому высушенному осадку добавляли 3 мл TFA с последующими 150 мкл триэтилсилана. Полученный раствор преципитировали из т-бутилметилового эфира, и процесс повторяли три раза. После фильтрации осадок сушили под пониженным давлением с получением 205 мг грязно-белого твердого вещества (выход 67%). Соединение использовали для следующей стадии без дополнительной очистки.
Для получения аминоокси-дериватизированного MMAE (аминоокси-Cys-MC-VC-PABC-MMAE), 30,1 мг аминооксицистамида (0,098 ммоль, 2 экв.) объединяли с 64,6 мг MC-VC-PABC-MMAE (0,049 ммоль) и 100 мкл триэтиламина в 3 мл DMF. Полученную реакционную смесь перемешивали при комнатной температуре в течение 15 минут, времени, за которое реакция завершалась согласно анализу HPLC. Соединение очищали препаративной HPLC с получением 45 мг (62%) желательного продукта в форме грязно-белого твердого вещества. Анализ обращеннофазовой HPLC позволял предполагать, что чистота соединения составляет >96%. ESI, рассчитано для C73H116N14O18S (MH)+ 1509,8501; обнаружено, m/z 1509,8469.
Для получения аминоокси-дериватизированного Dol10 (аминоокси-Cys-MC-VC-PABC-PEG8-Dol10), 7,4 мг (0,024 ммоль, 3 экв.) аминооксицистамида, 12 мг (0,008 ммоль) MC-VC-PABC-PEG8-Dol10 и 30 мкл триэтиламина объединяли в 3 мл DMF. Реакция завершалась в течение 15 минут согласно анализу HPLC. Очисткой препаративной HPLC получили 6,2 мг (46%) желательного продукта в форме грязно-белого твердого вещества. Анализ обращеннофазовой HPLC позволяет предполагать, что чистота соединения составляет >96%. ESI, рассчитано для C80H124N16O19S2 (MH)+ 1678,0664; обнаружено, m/z 1678,0613.
Пример 13. Опосредованная сиаловой кислотой (SAM) конъюгация реакционноспособных эффекторных групп
После обессоливания, лекарственные средства-линкеры из примера 11 объединяли с окисленными, сиалированными антителами из примера 10 в 75% DMSO при концентрации 25 мМ для достижения молярного соотношения лекарственного средства-линкера с антителом 24:1 и конечной концентрации антитела 5 мг/мл. Смесь инкубировали в течение ночи при комнатной температуре. Невключенные лекарственные средства-линкеры и любые свободные лекарственные средства выводили с использованием BioBeads. Продукт подвергали замене буфера в гистидиновом-Твин буфере с использованием колонок PD-10 и стерилизовали фильтрацией. Определяли уровни эндотоксинов, и менее 0,1 ЕЭ/мг ADC достигали для исследования in vivo.
На фигуре 29A-C показана хроматография гидрофобного взаимодействия (HIC) различных сиалированных антител (анти-FAP B11 и G11, и антитело анти-HER2 из примера 11), гликоконъюгированных с AO-MMAE. Сиалированное антитело против HER2 также конъюгировали с лекарственным средством-линкером, AO-Cys-MC-VC-PABC-PEG8-Dol10 (фигура 29D). Этот анализ выявил, что присутствовали в основном один или два конъюгата лекарственных средства на антитело с соотношением лекарственного средства к антителу (DAR) в диапазоне 1,3-1,9. Увеличенное время удержания гликоконъюгата Dol10 (фигура 29D) по сравнению с гликоконъюгатом MMAE (фигура 29C), по-видимому, обусловлено большей гидрофобностью Dol10.
Анализ LC-MS проводили также с антителом анти-HER, конъюгированным с двумя различными лекарственными средствами-линкерами (AO-MMAE или AO-PEG8-Dol10) в масштабе 30 мг. Этот анализ показал сходные значения DAR 1,7 и 1,5 после конъюгации, что является сравнимым с анализом HIC. Эксклюзионная хроматография (SEC) показала очень низкие уровни (1%) агрегатов в этих конъюгатах.
Пример 14. Опосредованная галактозой (GAM) конъюгация реакционноспособных эффекторных групп
Галактозный альдегид, полученный с помощью оксидазы галактозы на мутантном антителе A114N анти-TEM1 с гипергликозилированием, как описано в примере 11, конъюгировали с 24 молярным избытком аминоокси-MC-VC-PABC-MMAE-лекарственного средства-линкера по отношению к антителу посредством инкубации в течение ночи при 25°C, с получением конъюгата ADC с DAR 1,72.
К обработанному оксидазой галактозы антителу анти-HER, полученному, как описано в примере 11, одну десятую объема реакционной смеси 1M ацетата натрия, pH5,6, добавляли для доведения pH до 5,6, и DMSO добавляли для получения конечной концентрации 14% перед добавлением 24 экв. аминоокси-MC-VC-PABC-MMAE-лекарственного средства-линкера. Реакционные смеси инкубировали в течение ночи при комнатной температуре. Свободное лекарственное средство и лекарственное средство-линкер удаляли с помощью Biobeads, и продукт подвергали замене буфера посредством SEC (выход 65%). Конъюгат продукта анализировали посредством HIC. Как показано на фигуре 30, AO-MMAE был конъюгирован с ~60% молекул.
Пример 15. Анализы ADC пролиферации клеток in vitro
Активность in vitro молекул гликоконъюгата анти-HER и анти-FAP по изобретению сравнивали также с соответствующими тиоловыми конъюгатами, содержащими такую же группу лекарственного средства, связанную посредством тиоловых связей с цистеинами шарнирной области такого же донорного антитела. Тиоловые конъюгаты содержали приблизительно двойное количество лекарственного средства на антитело (DAR), чем гликоконъюгаты. Конъюгацию на основе тиола проводили, как описано в Stefano et al (Methods in Molecular Biology 2013, in press). Затем линии клеток Her2+ SK-BR-3 и Her2-MDA-MB-231 использовали для оценки относительной эффективности каждого ADC. Результаты этого анализа представлены в таблице 15 ниже.
|
На фигуре 31 показано сравнение активности in vitro гликоконъюгата анти-HER и соответствующего ему тиолового конъюгата. Жизнеспособность клеток определяли после 72 час воздействия конъюгатов на экспрессирующие антиген Her2 клетки (SK-BR-3) (фигура 31A и C) или не экспрессирующие антиген Her2 клетки (MDA-MB-231) (фигура 31B и D). ADC содержали либо MMAE, либо PEG8-Dol10, связанные с гликанами («глико») или, посредством общепринятых химических реакций, с остатками цистеина шарнирной области («тиол»). Как показано на фигуре 30A и C, ~ в 2 раза более низкую EC50 наблюдали для тиоловых конъюгатов по сравнению с гликоконъюгатами, что согласуется с в 2 раза более высоким DAR в первых, чем в последних. Не наблюдали токсичности для линии Her2-клеток с любым антителом вплоть до 100 мкг/мл.
Сходные тенденции наблюдали также при пролиферации клеток для ADC, полученных с антителами против антигена опухоли (FAP), который на высоком уровне экспрессируют реакционноспособные стромальные фибробласты в эпителиальных злокачественных опухолях, включая злокачественные опухоли ободочной кишки, поджелудочной железы и молочной железы (Teicher, B. A. (2009) Antibody-drug conjugate targets. Curr Cancer Drug Targets 9, 982-1004). Эти конъюгаты снова получали посредством конъюгации либо аминоокси-MMAE-лекарственного средства-линкера, либо малеимидо-MMAE лекарственного средства-линкера с гликанами или тиоловой группой. Анализы пролиферации клеток для этих конъюгатов показали, что EC50 тиолового конъюгата обладала в ~100 раз более высокой активностью на клетках CHO, трансфицированных FAP человека, чем на таких же клетках, лишенных экспрессии FAP, как изображено на фигуре 32, на которой показано сравнение активности in vitro гликоконъюгата и тиолового конъюгата анти-FAP B11. Жизнеспособность клеток определяли после воздействия конъюгатов на трансфицированные клетки CHO с антигеном FAP или без него. ADC содержали MMAE, связанные с гликанами («глико») или, посредством общепринятых химических реакций, с остатками цистеина шарнирной области («тиол»). Следует отметить, что в ~2 раза более низкая EC50 тиоловых конъюгатов по сравнению с гликоконъюгатами согласуется с относительными количествами лекарственного средства, доставляемыми на антитело, при условии сходной эффективности для связывания мишени и интернализации в экспрессирующих антиген клетках CHO. Параллельно, анализировали гликоконъюгат анти-FAP (B11) ADC с DAR 1,5, как описано ранее, и показали в ~2 раза более высокую EC50, чем у сравнительного тиолового конъюгата (DAR 3,3).
Как показано на фигуре 36, сходные тенденции наблюдали также в анализе пролиферации клеток для ADC, полученных с антителом анти-HER, несущим мутацию A114N с гипергликозилированием и AO-MMAE, как описано в примере 14, при анализе на экспрессирующих SK-BR-3 клетках или клетках MDA-MB-231. Для гликоконъюгата A114N ясно показана увеличенная клеточная токсичность против экспрессирующей Her2 линии клеток по сравнению с не экспрессирующей линией. Относительная токсичность по сравнению с гликоконъюгатом SialT, полученным с таким же антителом, согласуется с более низкой нагрузкой лекарственного средства в этом препарате.
Анализ пролиферации клеток проводили также для ADC, полученного с антителом анти-TEMl, несущим мутацию A114N с гипергликозилированием и AO-MMAE, полученного, как описано в примере 14. Более высокую токсичность наблюдали для экспрессирующих ТЕМ 1 линий клеток SJSA-1 и A673 по сравнению с не экспрессирующей линией MDA-MB-231. Уровень токсичности по сравнению с общепринятым тиоловым конъюгатом такого же антитела был согласован с нагрузкой лекарственного средства (DAR) в этом препарате.
|
В общем, сайт-специфической конъюгацией лекарственных средств через гликаны с помощью отщепляемых линкеров, получили ADC с токсичностью и эффективностью in vitro, эквивалентными общепринятым конъюгатам на основе тиола, как показано с использованием различных антител и различных лекарственных средств-линкеров. Более того, при ниже 2 мМ периодата, уровень лекарственного средства коррелирует с восстановлением сиаловой кислоты. Увеличение концентрации периодата выше 2 мМ предоставляет небольшое преимущество, как ожидают из полного перевода сиаловой кислоты в окисленную форму. Однако, при всех условиях, количество лекарственного средства на антитело было немного ниже, чем содержание сиаловой кислоты, что указывает на то, что некоторые из окисленных сиаловых кислот могут сходным образом не являться доступными для присоединения, либо из-за заглубления, либо иным образом из-за стерических затруднений, возникающих из-за объема лекарственного средства-линкера.
Пример 16. Характеризация in vivo конъюгатов антитела с лекарственным средством
Эффективность гликоконъюгатов анти-HER оценивали также в способах ксенотрансплантации Her2+ клеток опухоли и сравнивали с сравнительным тиоловым конъюгатом, обладающим в ~2 раза более высоким DAR. Мышам nude имплантировали SK-OV-3 Her2+ клетки опухолей, которым позволяли развить опухоли ~150 мм3 до начала лечения. ADC в дозах 3 или 10 мг/кг инъецировали через хвостовую вену на сутки 38, 45, 52 и 59. Присутствовали ~10 мышей на группу. Объем опухоли у мышей в различных группах измеряли, и их выживаемость регистрировали. Кривую выживаемости строили на основании способа Каплана-Мейера.
На фигуре 33 показано сравнение эффективности in vivo гликоконъюгатов и тиоловых конъюгатов анти-HER в модели ксенотрансплантата Her2+ клеток опухоли. Мышам Beige/SCID с имплантированными SK-OV-3 Her2+ клетками опухолей вводили дозы MMAE (фигура 33 A и B) и PEG8-Dol10 (фигура 33 C и D), содержащие гликоконъюгаты или сравнительные тиоловые конъюгаты с в ~2 раза более высоким DAR. Кинетика роста опухолей для конъюгатов MMAE показана на фигуре 33A. В этом случае, для гликоконъюгата показана значительно более высокая эффективность, чем для голого антитела отдельно (черный), но меньшая, чем для сравнительного тиолового конъюгата, обладающего в ~2 раза более высоким DAR (зеленый). Для гликоконъюгата MMAE показаны значительная регрессия опухоли и задержка роста опухоли на ~20 суток (фигура 33A), и ~2-кратное увеличение времени выживаемости от первой дозы (фигура 33B). Для тиолового конъюгата MMAE показана почти полная супрессия опухоли при такой же дозе ADC (10 мг/кг).
Эффективность in vivo гликоконъюгата PEG8-Dol10 («глико-Dol10») и сравнительного тиолового конъюгата с в ~2 раза более высоким DAR («тиол-Dol10») также определяли в той же модели ксенотрансплантата Her2+ клеток опухоли. Для обоих конъюгатов показана более низкая эффективность, чем для конъюгатов MMAE, как описано ранее. Однако, для гликоконъюгата аминоокси-PEG8-Dol10 («глико-Dol10») при 10 мг/кг показана 15-суточная задержка роста опухоли (фигура 33C) и ~20-суточное (1,7-кратное) увеличение времени выживаемости после первого введения (фигура 33D). Тиоловый конъюгат являлся более эффективным в такой же дозе, с показанным 2-кратным увеличением выживаемости. В более низкой дозе (3 мг/кг), для тиолового конъюгата показана меньшая эффективность, чем для гликоконъюгата при 10 мг/кг. Эта доза соответствует дозе 80 мкмоль лекарственного средства PEG8-Dol10 на кг, по сравнению с дозой 110 мкмоль лекарственного средства PEG8-Dol10 на кг для гликоконъюгата.
Эти данные показывают, что сайт-специфическая конъюгация лекарственных средств на сиаловой кислоте гликанов антитела приводит к молекулам с активностью, сравнимой с активностью ADC, полученных посредством химических реакций на основе тиола. Несколько более низкая эффективность in vivo, по-видимому, обусловлена меньшим количеством лекарственных средств, которое каждое антитело переносит в клетки опухолей посредством интернализации каждого связанного с антителом антигена. Хотя авторы настоящего изобретения не сравнивали эти гликоконъюгаты с тиоловыми конъюгатами с таким же DAR, эффективность, наблюдаемая при различных дозах двух ADC, представляющих сравнимые уровни введенного лекарственного средства, показывает, что гликоконъюгаты обладают присущей им эффективностью, сравнимой с эффективностью их тиоловых эквивалентов, указывая на отсутствие неблагоприятного эффекта конъюгации в этом участке. Более того, доза 10 мг/кг гликоконъюгата Dol10, которая вводила только на 28% более лекарственного средства, обеспечивала 2-кратное увеличение выживаемости по сравнению с тиоловым конъюгатом (при 3 мг/кг), что позволяет предполагать, что эти конъюгаты могут даже обеспечивать эффективность, превосходящую эффективность при таком же DAR. Принимая во внимание очевидное ограничение включения сиаловой кислоты в природные гликаны, более высокой нагрузки лекарственного средства, можно достигать посредством ряда различных способов, включая использование разветвленных линкеров для лекарственного средства или введение дополнительных участков гликозилирования, и с использованием такого же способа.