Результат интеллектуальной деятельности: ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ТЕРАПИИ ХРОНИЧЕСКИХ РАН
Вид РИД
Изобретение
Область техники
Изобретение относится к медицине и фармакологии, а именно к лекарственным средствам для терапии хронических ран и язв кожи, обладающим многофакторным воздействием на процессы регенерации и воспаления, и может быть использовано в хирургии.
Уровень техники
Известен способ профилактики и лечения инфекций роговицы глаз с использованием липополисахаридов Pseudomonas aeruginosa (Патент США №6984622). Недостатком указанного способа является ограниченная область применения (офтальмология). Кроме того, к недостаткам данного способа можно отнести недостаточную эффективность, связанную с особенностями химической структуры липополисахаридов Pseudomonas aeruginosa.
Известно лекарственное средство «Пирогенал», содержащее бактериальный липополисахариды Salmonella typhi, предназначенное для системного введения и выпускаемое в виде растворов для инъекций, а также в виде ректальных свечей, применяемое для терапии хронических заболеваний печени, хронических простатитов и уретритов, воспалительных процессов придатков матки, бесплодия, спаечной болезни брюшной полости, псориаза и других заболеваний (патент РФ 2139043). Механизм действия препарата связан с активацией врожденного иммунного ответа, что сопровождается пирогенным эффектом (гипертермией, повышением температуры тела). При терапии раневых дефектов кожи и/или слизистых оболочек системный способ введения не является целесообразным, т.к. невозможно при системном введении, учитывая высокую скорость метаболизма данного соединения, обеспечить достижение терапевтических концентраций липополисахаридов в области раневого дефекта. К недостаткам также относится наличие пирогенного эффекта.
Известно лекарственное средство, предназначенное для стимуляции регенерации раневых дефектов кожи и слизистых оболочек в форме геля, содержащая в качестве активного компонента бактериальные липополисахариды, а также, в качестве вспомогательных веществ водорастворимое производное целлюлозы, многоатомный спирт, консерванты и воду очищенную (Патент РФ 2447082). Недостатком изобретения является то, что данный препарат селективно таргетирует только один рецептор системы врожденного иммунного ответа, а именно, Толл-подобный рецептор 4 (TLR4), что исключает возникновения эффекта синергизма, наблюдаемого при одновременной активации нескольких рецепторов врожденного иммунного ответа.
Раскрытие изобретения
Задачей изобретения является повышение эффективности терапии хронических ран, в том числе трофических язв различной локализации, путем использования высокоэффективного с точки зрения биологической доступности лекарственного средства, способного одновременно таргетировать два рецептора системы врожденного иммунного ответа, а именно, рецепторы TLR4 и Mincle (CLEC4E).
Указанная задача решается за счет того, что лекарственное средство для терапии хронических ран содержит бактериальный липополисахарид, трегалозу дибегенат, водорастворимое производное целлюлозы, многоатомный спирт, консерванты и воду очищенную в эффективных соотношениях. При этом лекарственное средство выполнено в виде геля при следующем соотношении компонентов в граммах на 100 г геля:
|
В качестве водорастворимого производного целлюлозы используют натриевую соль карбоксиметилцеллюлозы, в качестве многоатомного спирта используют глицерин, в качестве консерванта используют нипагин и/или нипазол.
Перечень фигур
На фигуре 1
представлены данные, показывающие изменение остаточной площади раны, в процентах, для всех экспериментальных групп; значения в формате: «среднее значение ± стандартное отклонение». *p<0.05 по сравнению с группой плацебо, вычислено с использованием критерия Стьюдента.
На фигуре 2
представлены данные, характеризующие количество (A) F4/80 положительных клеток (макрофагов) и (Б) Ly6G положительных клеток (нейтрофилов) в области раневого дефекта; значения представлены в формате: «среднее значение ± стандартное отклонение». *p<0.05 по сравнению с группой плацебо, вычислено с использованием критерия Стьюдента.
Реализация изобретения
Одним из наиболее перспективных направлений фармацевтической разработки ранозаживляющих средств является местное использование лигандов рецепторов врожденного иммунного ответа, играющих ключевую роль в процессах репарации.
Рецепторы врожденного иммунитета, в том числе Toll-подобные рецепторы и C-лектиновые рецепторы, экспрессируются широким спектром клеток, образующихся или присутствующих в коже: фибробластами, адипоцитами, кератиноцитами, эндотелиальными клетками, включая клетки иммунной системы, такие как моноциты, макрофаги, нейтрофилы, дендритные клетки, клетки Лангерганса, тучные клетки, Т- и В-лимфоциты.
Активация рецепторов врожденного иммунитета приводит к запуску биохимических каскадов, приводящих к активации ряда транксрипционных факторов (NF-κВ, IRF3, 5, 7, АР-1), регулирующих секрецию спектра цитокинов, хемокинов, антимикробных пептидов, молекул адгезии и других факторов, регулирующих процесс репарации.
Авторами была изучена экспрессия рецепторов врожденного иммунного ответа на модели раны методом полногеномного анализа экспрессии генов, RNA microarray (Kostarnoy А.V. et al. Receptor Mincle promotes skin allergies and is capable of recognizing cholesterol sulfate // Proceedings of the National Academy of Sciences. - 2017. - T. 114. - №. 13. - С. E2758-E2765). Из поврежденной кожи, а так же из интактной кожи была выделена общая РНК. Из всех генов, экспрессия которых в поврежденной коже по сравнению с интактной увеличивалась в три и более раз, были отобраны гены рецепторов врожденной иммунной системы. Как следует из полученных результатов, в ответ на повреждения кожи повышается экспрессия генов врожденного иммунного ответа, относящихся к семействам: Toll-подобных рецепторов, в том числе гена рецептора TLR4, NOD-подобных рецепторов, RIG-I-like рецепторов. Было определено, что в наибольшей степени повышается экспрессия двух генов, относящихся к семейству С-лектиновых рецепторов врожденного иммунного ответа, а именно, рецепторов Clec4e (Mincle) и Clec4d (MCL). В связи с полученными результатами, рецептор Clec4e (Mincle) был выбран в качестве одного из таргетов при создании лекарственного средства.
Заявленное лекарственное средство содержит в качестве активного вещества два высокоочищенных компонента: липополисахарид энтеробактерий и трегалозы дибегенат. Липополисахарид обладает способностью активировать транскрипционный фактор NF-κВ через Toll-подобный рецептор 4. Трегалозы дибегенат получен методом химического синтеза, и представляет собой синтетический аналог корд-фактора микобактерий (трегалозы димиколята), является лигандом С-лектинового рецептора Mincle (CLEC4E).
Биомишенью лекарственного средства являются рецепторы TLR-4 (представитель семейства Toll-подобных рецепторов врожденного иммунного ответа) и Mincle (CLEC4E, представитель семейства С-лектиновых рецепторов врожденного иммунного ответа, CLRs). Совместная активация С-лектиновых и Toll-подобных рецепторов врожденного иммунного ответа приводит к выраженному синергетическому эффекту активации транскрипционного фактора NF-κВ, что способствует значительному ускорению процессов репарации.
Действующие компоненты лекарственногого средства, бактериальный липополисахарид и трегалозы дибегенат, таргетируя рецепторы врожденного иммунного ответа TLR4 и Mincle (CLEC4E), соответственно, вызывают активацию транскрипционного фактора NF-кВ ряда клеток, присутствующих в коже (моноциты, макрофаги, фибробласты, кератиноциты, эндотелиальные клетки), что приводит к секреции провоспалительных цитокинов и хемокинов - хемоаттрактантов макрофагов. Количество макрофагов в тканях раны значительно увеличивается. Известно, что макрофаги играют ключевую роль в раневом процессе и являются его регуляторами, секретируя спектр ростовых факторов и других регуляторных молекул, что приводит к интенсивному ангиогенезу, коллагенообразованию, эпителизации, и в конечном итоге к значительному ускорению процесса репарации.
Таким образом, местное применение комбинированного лекарственного средства оказывает комплексное терапевтическое воздействие на раневый процесс, за счет синергетического эффекта, возникающего при таргетирования двух рецепторов системы врожденного иммунного ответа, а именно, рецепторов TLR4 и Mincle (CLEC4E), что способствует значительному ускорению процессов репарации.
В качестве терапевтических концентраций бактериального липополисахарида в лекарственной форме выбран диапазон 0,02-5,00 г в 100 г формы. Диапазон определен на основании экспериментальных данных и литературных сведений (Крайцеров Б.В. Концептуальный подход к пиротерапии с позиции теории стресса. М.: Лабиринт, 2001. - 560 с.).
Для терапии хронических ран, в том числе трофических язв, используют гель на гидрофильной основе, содержащий в качестве активного компонента трегалозу дибегенат и бактериальный липополисахрид. В качестве гидрофильной основы используют водорастворимые производные целлюлозы, например натриевая соль карбоксиметилцеллюлозы (натрия кармеллоза). Преимущества данных основ:
- обладают ранозаживляющим действием;
- создают на поверхности раны пленку, защищающую рану от воздействия факторов окружающей среды, в том числе от микробной контаминации;
- обладают слабым осмотическим действием;
- не препятствуют газообмену;
- гипоаллергенны.
Пример 1.
Предварительно взвешенные активные вещества (трегалозы дибегенат и бактериальный липополисахарид) и вспомогательные вещества (воду очищенную (ФС. 2.20020.15), нипагин (Eur.Ph.) и нипазол (Eur.Ph.)) загружают в реактор из нержавеющей стали, снабженный якорной мешалкой, нагревают до температуры 80°С и выдерживают при постоянном перемешивании в течение 20 минут.
Затем в реактор при перемешивании загружают отвешенный глицерин (Eur.Ph. или ГОСТ 6824-96) и предварительно приготовленную суспензию натриевой соли карбоксиметилцеллюлозы (Eur.Ph.) в воде. Осуществляют гомогенизацию геля в реакторе с помощью съемного погружного гомогенизатора. Проводят перемешивание геля при температуре 80°С в течение 45 минут. По истечении времени перемешивания, охлаждают холодной водопроводной воды и включают вакуумный насос, регулируя давление по манометру - 0,5-0,7 кгс/см2. Гель охлаждают под вакуумом до температуры +20-25°С. Гель фасуют в тубы алюминиевые по 10 г.
Полученный гель сохраняет стабильность в течение 24 месяцев по ряду показателей: внешний вид (описание), специфическая активность, количественное определение, подлинность, масса содержимого упаковки, рН водного извлечения, однородность геля, аномальная токсичность, микробиологическая чистота и т.д.
Пример 2.
Оценка эффективности предлагаемого лекарственного средства. Планиметрические исследования.
В качестве интегрального показателя, характеризующего эффективность процесса репарации, была выбрана динамика в изменении площади раны. Площадь раны является интегральным показателем, отражающим эффективность процесса регенерации, косвенно характеризующим процессы воспаления, неоваскуляризации, пролиферации фибробластов и коллагенообразования. Моделирование раны проведено с использованием биопсийного инструмента по известной методике (Khanna S, Biswas S, Shang Y, Collard E, Azad A, Kauh C, Bhasker V, Gordillo GM, Sen CK, Roy S. Macrophage dysfunction impairs resolution of inflammation in the wounds of diabetic mice // PLoS One. - 2010. - 5(3). - C. 9539).
Для моделирования условий трофической труднозаживающей раны на фоне диабета, предварительно было осуществлено субхроническое введение стрептозоцина. Для этого стрептозоцин вводился подопытным животным внутрибрюшинно, ежедневно, в течение 5 дней, в количестве 50 мг/кг веса.
В эксперименте использованы мыши-аутбреды линии ICR, самцы весом 23-27 г, в количестве 60 особей. Животные прошли акклиматизацию в течение 10 дней. Механическая депиляция была проведена триммером для животных "Oster Mark-N". Животные были анестезированы с помощью золетило-ксилазинового наркоза (45 мг/кг золетила и 7,5 мг/кг ксилазина внутримышечно). Операционное поле было обработано 70% этанолом. Моделирование раны проведено в соответствии с общеизвестной методикой. На спине животных с использованием биопсийного инструмента диаметром 8 мм были созданы раны, путем оттягивание кожи и последующего штампования. Биопсийный инструмент проникал через эпидермис, дерму и подкожную клетчатку, при этом фасция сохранялась интактной. Введение лекарственных средств животным осуществлялось путем накожного нанесения на область раневого дефекта, ежедневно в течение семи дней, в объеме 150 мкл, в одно и то же время (в пределах 4 ч). Первое нанесение проводили через 24 часа после моделирования раны. На рану накладывали пластинку простерилизованного в автоклаве целлофана и на ней маркером обрисовывали площадь раны. Затем целлофан с нанесенным контуром накладывали на миллиметровую бумагу и путем подсчета квадратных миллиметров внутри контура определяли площадь раны.
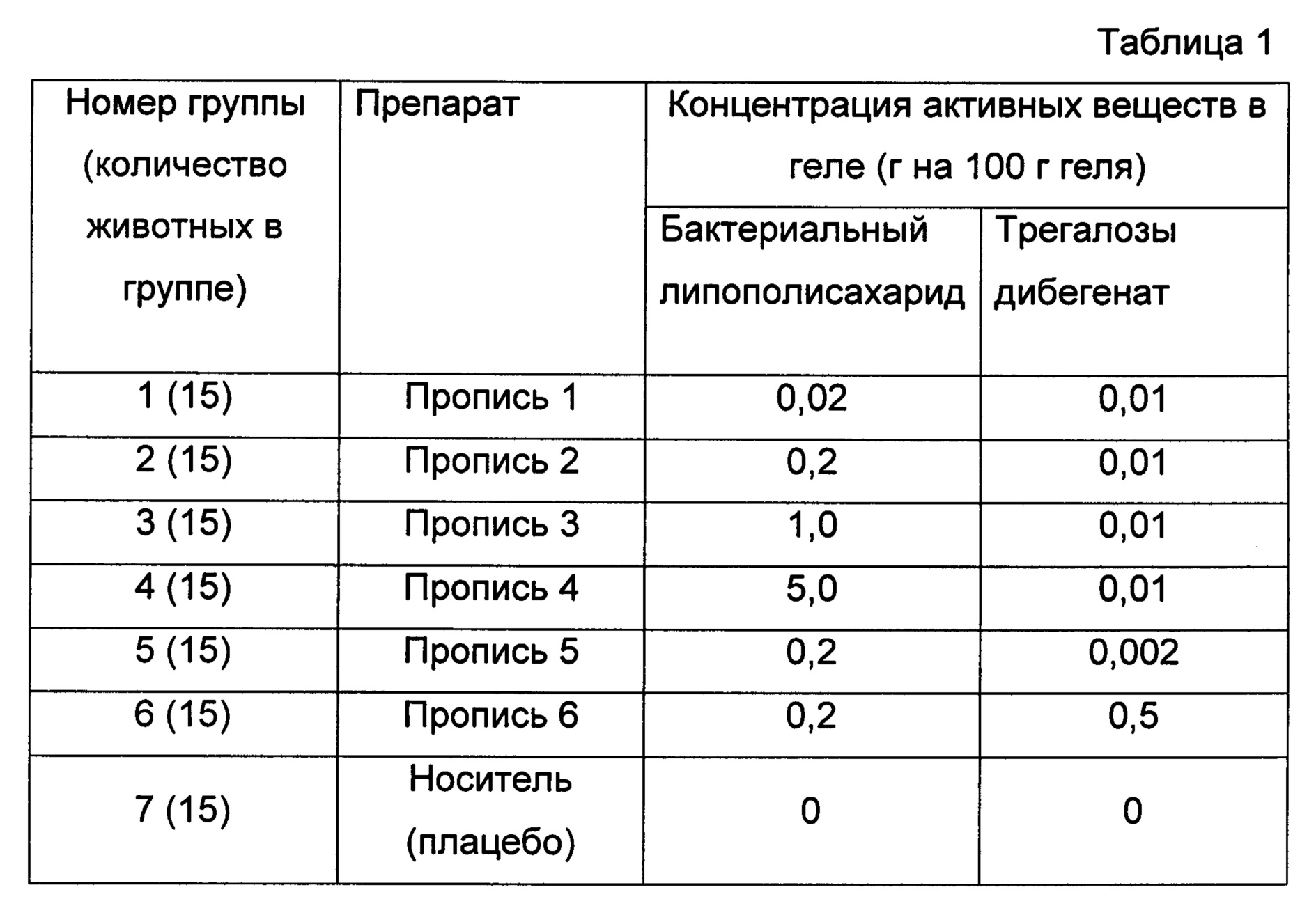
Статистическую обработку проводили, используя программу Statistica 6.0. Значимость отличий значений контрольной и экспериментальной групп оценивали с использованием дисперсионного анализа (ANOVA), различия считались значимыми при p<0.05. В таблице 1 представлен дизайн эксперимента.
В ходе исследования на 7, 14, 21 день эксперимента площадь каждой раны была измерена планиметрически, полученные данные были подвергнуты статистической обработке.
На фигуре 1 представлены данные, показывающие изменение остаточной площади раны, в процентах, для всех экспериментальных групп; значения в формате: «среднее значение ± стандартное отклонение». *p<0.05 по сравнению с группой плацебо, вычислено с использованием критерия Стьюдента.
В ходе исследования показано, что при местном нанесении исследуемого лекарственного средства, происходит статистически значимое уменьшение площади раны в динамике, по сравнению с группой плацебо (контрольной группой). Для дальнейших исследований выбрана пропись 2, поскольку эффективность этой прописи превосходит эффективность прописей 1 и 5, и при этом в прописи 2 используется меньшая дозировка активных компонентов, по сравнению с прописями 3, 4 и 6. Причем снижение дозировки при хорошей эффективности очень важно, так как позволяет максимально снизить побочный эффект при использовании лекарственного средства, а также выгодно с экономической точки зрения
Пример 3.
Оценка эффективности предлагаемого лекарственного средства. Определение влияния местного нанесения лекарственного средства на область раневого дефекта на процессы воспаления, инфильтрации лейкоцитов, коллагенообразования и эпителизации раневых дефектов кожи
В эксперименте использованы мыши-аутбреды линии ICR, самцы весом 23-27 г, в количестве 50 особей. Животные прошли акклиматизацию в течение 10 дней. Механическая депиляция была проведена триммером для животных "Oster Mark-N". Животные были анестезированы с помощью золетило-ксилазинового наркоза (45 мг/кг золетила и 7,5 мг/кг ксилазина внутримышечно). Операционное поле было обработано 70% этанолом. Моделирование раны проведено в соответствии с методикой, опубликованной в работе The effect of topical tretinoin on tissue strength and skin components in a murine incisional wound model. Muehlberger Т., Moresi J.M., Schwarze H, Hristopoulos G., Laenger F., Wong L. // Journal of the American Academy of Dermatology, 2005 Apr 52(4):583-588. На спине животных вдоль линии хребта при помощи скальпеля были иссечены эпидермис, дермис и подкожная клетчатка до фасции так, чтобы создать разрез длиной 4 см. Раневый дефект был зашит двумя швами при помощи полиамидного шовного материала «Поликон».
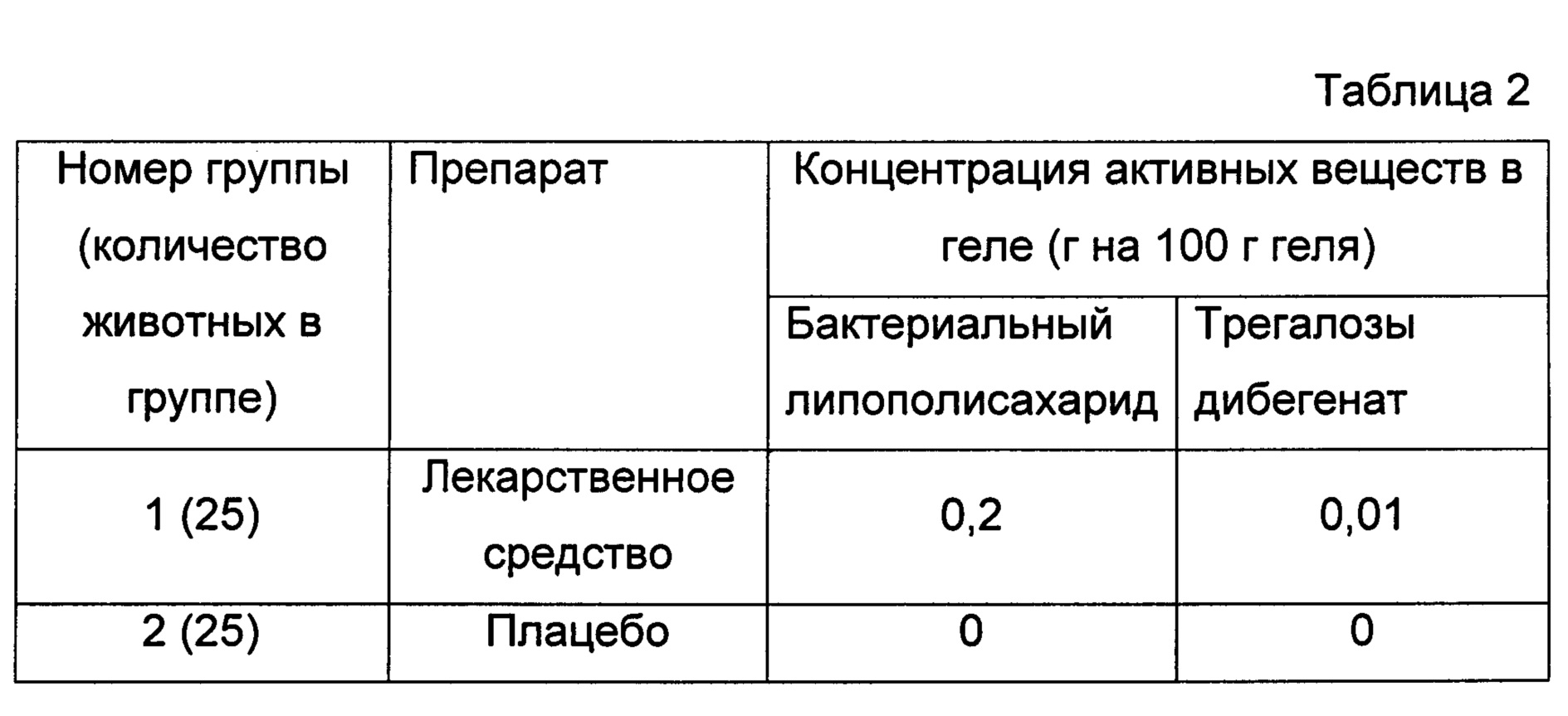
Введение лекарственного средства и плацебо животным осуществлялось путем накожного нанесения на область раневого дефекта ежедневно в течение семи дней, в объеме 150 мкл, в одно и то же время. Первое нанесение проводили через 24 часа после моделирования раны. В таблице 2 представлен дизайн эксперимента.
В ходе исследования на 1, 3, 7, 14, 21 день эксперимента из каждой группы было выведено по пять животных. У животных были взяты полоски кожи 1×3 см, содержащие раневый дефект, для дальнейшей обработки и проведения гистологических, иммуногистологических и морфометрических исследований.
Материалом для гистологического исследования являлись полоски кожи мышей размерами 2×1 см с наличием раневого дефекта, расположенного в центре полоски перпендикулярно наибольшему размеру. Материал был подвергнут гистологическому и иммуногистологическому исследованию. Полоски кожи были фиксированы в 10% формалине. Проводка образцов осуществлялась по стандартной методике. При изготовлении парафиновых блоков материал был ориентирован так, чтобы поверхность среза была перпендикулярна раневому дефекту. Гистологическое исследование образцов осуществлялось на парафиновых срезах толщиной 4 мкм, окрашенных гематоксилином и эозином по стандартной методике.
С тем, чтобы оценить интенсивность и кинетику лейкоцитарной инфильтрации в области раневого дефекта, гистологические срезы были иммуногистохимически окрашены с использованием моноклональных антител к Ly-6G (маркеру нейтрофилов) или F4/80 (маркеру макрофагов). Гистологическое исследование микропрепаратов осуществлялось на микроскопе Leica DM, снабженного цифровой фотокамерой Leica D300. Численная плотность Ly6G и F4/80 положительных клеток была определена в пяти произвольно выбранных полях зрения для каждого раневого дефекта при увеличении ×400. Из полученных данных были определены средние арифметические значения, которые были подвергнуты статистической обработке. Статистическую обработку данных морфометрии проводили, используя программу Statistica 6.0. Значимость отличий значений контрольной и экспериментальной групп оценивали с использованием дисперсионного анализа (ANOVA), различия считались значимыми при p<0.05.
В соответствии с полученными результатами, местное нанесение лекарственного средства способствовало более быстрому завершению процесса воспаления (по сравнению с группой плацебо). Так, через семь дней после начала терапии, в группе плацебо наблюдалась более интенсивная инфильтрация полиморфноядерных клеток, отмечались отечные явления.
Местное применение исследуемого лекарственного средства положительно влияло на процесс эпителизации. Так, уже через неделю после нанесения ран в экспериментальной группе отмечалась полная эпителизация раневого дефекта акантотически утолщенным эпидермисом, в то время как в группе плацебо наблюдались язвенные дефекты эпидермиса. К концу второй недели эксперимента в экспериментальной группе количество слоев эпидермиса составляло 2-3 слоя, что соответствует толщине эпидермиса интактных животных, тогда как в группе плацебо отмечалось наличие акантотически утолщенного эпидермиса. К третьей неделе количество слоев эпидермиса во всех группах составляло 2-3 слоя, что соответствовало толщине эпидермиса интактных животных.
Морфометрический анализ состоял в оценке численной плотности F4/80 и Ly-6G положительных клеток в пяти полях зрения в области раневого дефекта при увеличении ×400. В соответствии с полученными результатами, местное применение исследуемого лекарственного средства стимулировало раннюю инфильтрацию макрофагов в края раны. Через сутки после первого нанесения препаратов количество макрофагов в поле зрения в экспериментальной группе было статистически значимо больше, чем в контрольной. К 3-ему и 7-му дням инфлюкс макрофагов в обеих группах был сходным. Пик инфильтрации нейтрофилами приходился на первые сутки. В экспериментальной группе количество нейтрофилов начало уменьшаться на 3-й день, а к 7-му дню их количество было незначительным. В контрольной группе инфильтрация области раны нейтрофилами на 3-й и 7-й день была более интенсивной, при этом различия между группами были статистически значимыми.
На фигуре 2 представлены данные, характеризующие количество (A) F4/80 положительных клеток (макрофагов) и (Б) Ly6G положительных клеток (нейтрофилов) в области раневого дефекта; значения представлены в формате: «среднее значение ± стандартное отклонение». *p<0.05 по сравнению с группой плацебо, вычислено с использованием критерия Стьюдента.
Пример 4.
Оценка безопасности предлагаемого лекарственного средства. Изучение острой и хронической токсичности.
Исследования были проведены по стандартным методикам (Руководство по проведению доклинических исследований лекарственных средств, ред. А.Н. Миронов, М., «Гриф и К», 2012).
Острую токсичность изучали на мышах и крысах (самцах и самках). Исследуемое лекарственное средство наносили животным на раневую поверхность и на неповрежденную кожу, фиксировали окклюзионной повязкой и оставляли на 24 часа. Для выявления токсических эффектов использовали тестируемое лекарственное средство с 35-кратным увеличением активных веществ. Максимально нанесенные дозы мышам и крысам превысили предполагаемую терапевтическую дозу для человека в 10000 и 5000 раз, соответственно. Из-за низкой токсичности исследуемого лекарственного средства вычислить ЛД50 биометрическим методом не представилось возможным. Проведенное экспериментальное исследование острой токсичности показало, что лекарственное средство на основе трегалозы дибегената и модифицированного липополисахарида энтеробактерий в условиях однократного нанесения на область раневого дефекта и на неповрежденную кожу не оказывает токсического действия на организм животных.
Хроническую токсичность изучали на крысах и кроликах (самцах и самках). Исследуемое лекарственное средство наносили животным на неповрежденную кожу 1 раз в сутки в течение 28 дней. Животным наносили предполагаемую терапевтическую дозу и десятикратную дозу, с учетом межвидовых коэффициентов пересчета. При исследовании использовали общепринятые методы: интегральные и физиологические показатели, исследования клинических и биохимических показателей крови, исследование мочи, морфометрическую и гистологическую оценку внутренних органов и тканей. Было показано, что многократные накожные аппликации тестируемого лекарственного средства, применяемые на крысах и кроликах, как в терапевтической дозе, так и в 10 раз ее превышающей, не вызывают значимых патологических процессов в организме животных.
Пример 5.
Оценка безопасности предлагаемого лекарственного средства. Изучение местно-раздражающего действия.
Исследования были проведены по стандартным методикам (Руководство по проведению доклинических исследований лекарственных средств, ред. А.Н. Миронов, М., «Гриф и К», 2012).
Местно-раздражающее действие изучали на крысах и кроликах (самцах и самках). Исследуемое лекарственное средство наносили животным на неповрежденную кожу 1 раз в сутки в течение 28 дней. Животным наносили предполагаемую терапевтическую дозу и десятикратную дозу, с учетом межвидовых коэффициентов пересчета. Оценку проводили визуально и гистологически. Было установлено, что многократные накожные аппликации тестируемого лекарственного средства, применяемые на крысах и кроликах в течение 28 суток, как в терапевтической дозе, так ив 10 раз ее превышающей, не вызывают у животных изменений кожного покрова: не отмечено покраснения кожи, утолщения кожной складки и изъязвлений; гистологические исследования не показали каких-либо изменений кожи, свидетельствующих о негативном побочном действии.
Пример 6.
Оценка безопасности предлагаемого лекарственного средства. Изучение мутагенности.
Исследования были проведены по стандартным методикам (Руководство по проведению доклинических исследований лекарственных средств, ред. А.Н. Миронов, М., «Гриф и К», 2012).
Оценку мутагенных свойств тестируемого лекарственного средства проводили в тестах на индукцию генных мутаций in vitro (тест Эймса) и в тесте на индукцию хромосомных повреждений in vivo (учет хромосомных аберраций в клетках костного мозга мышей). В тесте Эймса лекарственное средство на основе трегалозы дибегената и модифицированного липополисахарида энтеробактерий было испытано в виде раствора 10 мг/мл, приготовленного путем внесения 50 мг лекарственного средства в 5 мл диметилсульфоксида (ДМСО) и четырех 10-кратных разведений в ДМСО. Тест учета хромосомных аберраций проводили на клетках костного мозга мышей-гибридов (CBA×C57BI/6) F1 (самцов и самок), которым наносили лекарственное средство однократно и четырехкратно на область спины в терапевтической дозе (с учетом пересчета доз по поверхности тела с человека на мышь) и однократно максимально возможную дозу. В рамках данного исследования было установлено, что лекарственное средство на основе трегалозы дибегената и модифицированного липополисахарида энтеробактерий не индуцирует генные мутации на тестерных штаммах Salmonella typhimurium и не вызывает повышения частоты хромосомных аберраций в клетках костного мозга мышей. Таким образом, проведенные исследования позволяют сделать вывод, что лекарственное средство на основе трегалозы дибегената и модифицированного липополисахарида энтеробактерий не обладает мутагенным действием.
Пример 7.
Оценка безопасности предлагаемого лекарственного средства. Изучение иммунотоксичности.
Для изучения иммунотоксических свойств тестируемого средства использовали стандартные методы исследования. Эксперименты проводили на здоровых половозрелых мышах линий СВА, мышах-гибридах первого поколения (СВА × C57BL/6)F1, мышах линии Balb/c. Использовали две дозы тестируемого препарата: терапевтическая доза с учетом межвидовых коэффициентов пересчета доз, и на порядок выше. Контрольным животным наносили основу лекарственного средства (плацебо). Исследование включало в себя оценку гуморального иммунного ответа, клеточного иммунного ответа, фагоцитарной активности перитонеальных макрофагов и определение массы и клеточности органов иммунной системы, оценку аллергизирующего действия. Результаты исследования иммунотоксичности показали, что лекарственное средство на основе трегалозы дибегената и модифицированного липополисахарида энтеробактерий для терапии хронических ран и трофических язв, не изменяет титр гемагглютининов в сыворотке крови мышей, не оказывает влияния на показатели клеточного иммунного ответа и не влияет на массу и клеточность органов иммунной системы, не обладает аллергизирующим действием. Таким образом, по полученным данным можно сделать вывод, что лекарственное средство для местного применения на основе трегалозы дибегената и модифицированного липополисахарида энтеробактерий не оказывает иммунотоксического действия на организм животных.
Пример 8.
Оценка безопасности предлагаемого лекарственного средства. Изучение репродуктивной токсичности.
Исследования были проведены по стандартным методикам (Руководство по проведению доклинических исследований лекарственных средств, ред. А.Н. Миронов, М., «Гриф и К», 2012).
Работы включали в себя изучение влияния тестируемого лекарственного средства на репродуктивную (генеративную) функцию животных и изучение эмбриотоксического действия, регистрируемого в антенатальном и постнатальном периодах развития. Эксперименты проводили на половозрелых аутбредных крысах. Использовали две дозы тестируемого препарата: терапевтическая доза с учетом межвидовых коэффициентов пересчета доз, и на порядок выше. При проведении исследований оценивали показатели эмбриотоксичности (количество мест имплантации, количество живых и мертвых плодов, количество резорбций, предимплантационную и постимплантанционную гибель), состояние плодов к концу антенатального периода развития, развитие плодов в постнатальном периоде (физическое развитие, скорость созревания сенсорно-двигательных рефлексов). В процессе исследования было установлено, что нанесение лекарственного средства на основе трегалозы дибегената и модифицированного липополисахарида энтеробактерий для терапии хронических ран и трофических язв как до спаривания животных, так и во время гестации, не приводит к нарушению репродуктивной функции, не вызывает эмбриотоксического и тератогенного действия, не нарушает развитие потомства в постнатальном периоде. Таким образом, проведенные исследования позволяют сделать вывод, что исследуемое лекарственное средство не оказывает отрицательного действия на репродуктивную функцию и не вызывает эмбриотоксического действия.
Представленные данные свидетельствуют об эффективности и безопасности использования предлагаемого лекарственного средства.
В предлагаемом лекарственном средстве, по сравнению с прототипом, комбинированное лекарственное средство оказывает комплексное терапевтическое воздействие на раневый процесс, за счет синергетического эффекта, возникающего при таргетирования двух рецепторов системы врожденного иммунного ответа, а именно, рецепторов TLR4 и Mincle (CLEC4E), что способствует ускорению процессов репарации.
Таким образом, задача изобретения, а именно повышение эффективности терапии хронических ран, в том числе трофических язв различной локализации, путем использования высокоэффективного лекарственного средства, способного одновременно таргетировать два рецептора системы врожденного иммунного ответа, а именно, рецепторы TLR4 и Mincle (CLEC4E), реализована в заявленном изобретении.
В заявленном способе по сравнению с другими препаратами, например пирогеналом, - во-первых, при местном введении существует возможность достижения терапевтических концентраций липополисахаридов в области раневого дефекта, что невозможно при системном введении, учитывая высокую скорость метаболизма данного соединения. Во-вторых, местное применение позволяет воздействовать на процессы регенерации при отсутствии пирогенного эффекта, так как в данном случае препарат не попадает в системный кровоток. В-третьих, местное применение лекарственного средства в виде терапевтически приемлемой лекарственной формы в виде геля увеличивает эффективность препарата также за счет того, что на поверхности раны создается пленка, защищающая рану от воздействия факторов окружающей среды, в том числе от микробной контаминации; а также обеспечивается отток экссудата.