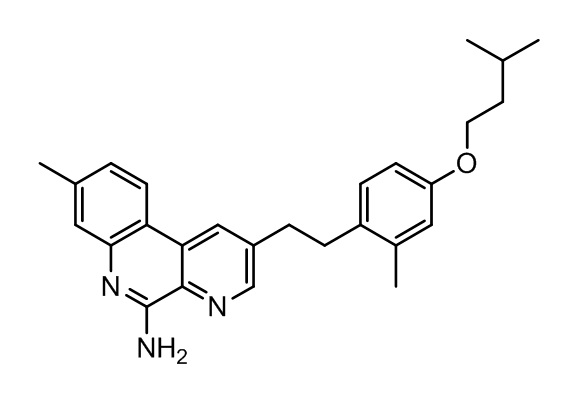
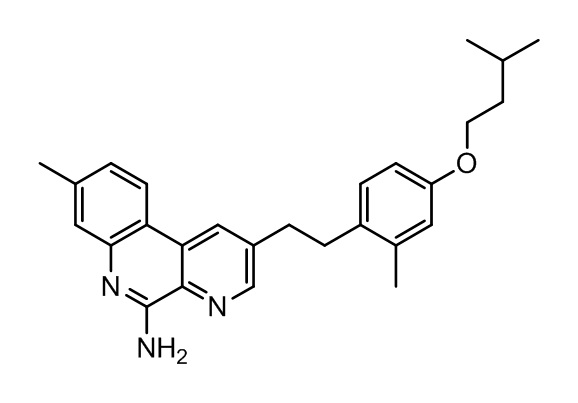
Результат интеллектуальной деятельности: ГАЛЕНОВАЯ КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ МЕСТНОГО ПРИМЕНЕНИЯ
Вид РИД
Изобретение
Настоящее изобретение относится к фармацевтическим композициям, включающим лекарственное средство для местного применения, например, модулятор TLR7 (Toll-подобного рецептора). Более конкретно, настоящее изобретение относится к фармацевтической композиции, включающей производное бензо[f][1,7]нафтиридина.
Предпосылки создания изобретения
В случае мощных фармацевтически эффективных соединений, которые разработаны для местного применения, зачастую наблюдается их низкая местная переносимость. В этой связи, жизненно важно иметь композицию для местного применения, которая могла бы решить проблему местной непереносимости и которая не оказывала бы при этом отрицательного влияния на эффективность соответствующего соединения.
Краткое описание сущности изобретения
Галеновые композиции по настоящему изобретению относятся к очень мощным фармацевтически эффективным соединениям, таким как модулятор TLR7, которые адаптированы для применения в местном режиме, например, таким как крем, гель или др., которые характеризуются стабильностью и хорошей переносимостью при контакте с кожей.
В частности, настоящее изобретение относится к фармацевтической композиции, подходящей для местного применения, которая включает фармацевтически приемлемое средство, например, модулятор TLR7, такое как, например, производное бензо[f][1,7]нафтиридина, например, соединение, описываемое одной из указанных ниже формул (I), (II), (III) и/или (IV), растворитель, эмульгатор, загуститель или гелеобразователь, буфер, подщелачивающий агент, консервант и необязательно антиоксидант.
Подробное описание изобретения
В типичном случае, фармацевтические композиции по настоящему изобретению представляют собой стабильные и в основном хорошо переносимые при нанесении на кожу препараты.
В целях настоящего изобретения, модулятор TLR7 может иметь химическую структуру, указанную ниже, т.е. представлять собой соединение формулы (I):
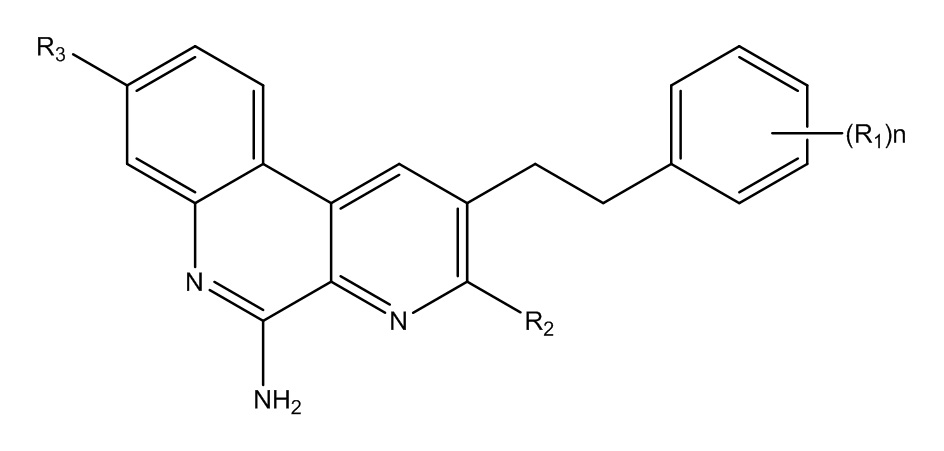
где каждый из R1, R2 и R3 независимо выбран из H, -CH3, -CH2CH3, -CF3, CH2OH -OCH3, -COOCH3, -COOCH2CH3, F, Cl, Br, -CH2OCH3, -CH2OCH2CH3, -N(CH3)2, ((O(CH2)2)2-OH, -O(CH2)2-OH, -O(CH2)2-(PO3H2), -O(CH2)2-COOH, -O(CH2)2-CH(CH3)2, -C2-C6-алкила, замещенного 1-3 заместителями, выбранными из -OH, -CH3, циклопропила, -O(CH2)2-COOH, -O(CH2)2-(PO3H2), -COOH, -COOCH3 и -COOCH2CH3, и n равен 0, 1, 2 или 3; или может представлять собой его фармацевтически приемлемую соль.
Более конкретно, модулятор TLR7 может представлять собой соединение с химической структурой, показанной ниже и описываемой формулами (II), (III) и/или (IV), или его фармацевтически приемлемую соль.
(II)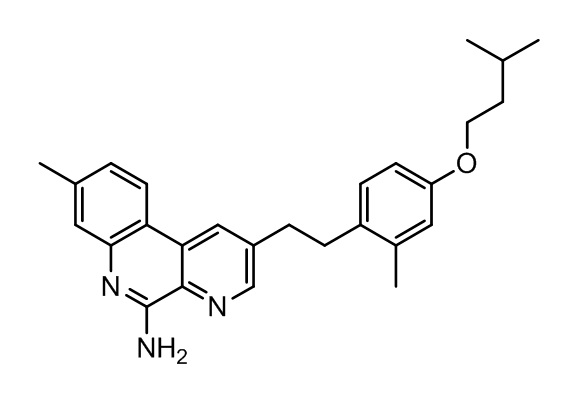
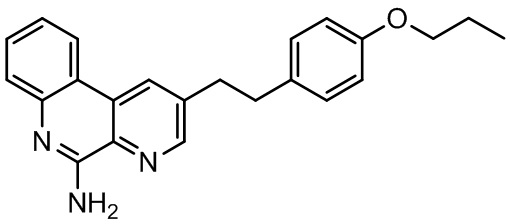 (III)
(III)
 (IV)
(IV)
Примеры фармацевтически приемлемых солей соединений формул I-IV включают соли, полученные с использованием неорганических кислот, такие как гидрохлорид, гидробромид или сульфат, соли, полученные с использованием органических кислот, такие как ацетат, фумарат, малеат, бензоат, цитрат, малат, а также метансульфонатные и бензолсульфонатные соли, или, где это приемлемо, соли, полученные с использованием металлов, таких как натрий, калий, кальций, алюминий, соли, полученные с использованием аминов, таких как триэтиламин, и соли, полученные с использованием двухосновных аминокислот, таких как лизин. Одной из таких приемлемых солей может быть гидрохлорид.
Фармацевтическая композиция по настоящему изобретению содержит в типичном случае модулятор TLR7, в количестве от 0,001 до 5 вес.%, или от 0,001 до 1 вес.%, или от 0,01 до 0,5 вес.%, или, например, от 0,003 до 0,1 вес.% от общего веса всей композиции.
Фармацевтическая композиция по настоящему изобретению включает в типичном случае один или несколько эксципиентов, таких как растворитель, эмульгатор, загуститель или гелобразователь, буфер, подщелачивающий агент, консервант и/или антиоксидант.
Определения
Используемый в настоящем изобретении растворитель может быть в типичном случае выбран из воды, этанола, изопропанола, н-пропанола, пропиленгликоля, этиленгликоля, диэтиленгликоля, моноэтилового эфира диэтиленгликоля (Транскутол® HP (Transcutol® HP)), диэтилового эфира диэтиленгликоля, кукурузного масла или бензилового спирта. В одном варианте осуществления настоящего изобретения, вода, этанол, пропиленгликоль, моноэтиловый эфир диэтиленгликоля и/или бензиловый спирт могут использоваться по отдельности или любом их сочетании.
Растворитель присутствует в настоящей композиции в типичном случае в количестве, составляющем примерно 0,1-95 вес.%, или в количестве 1-95 вес.%, или в количестве 5-95 вес.%, или в количестве 15-95 вес.%, или в количестве 25-95 вес.%, или в количестве 35-95 вес.%, или в количестве 45-95 вес.%, или в количестве 55-95 вес.% от общего веса всей композиции.
Используемый в настоящем изобретении эмульгатор выполняет обычную для него функцию, препятствуя разделению компонентов в составе фармацевтической композиции, а также применение эмульгатора определяется его способностью продлевать срок действия препарата (длительность хранения). Одним из примеров такого эмульгатора является лецитин, также известный как фосфатидилхолин, а также фосфатидилэтаноламин, холестерин, цетиловый спир, полиоксилстеариловый эфир (например, Бридж® S2 (Brij® S2), Бридж® S721 (Brij® S721)) или каприлкапроилполиоксилглицерид (Лабрасол® (Labrasol®)). В одном варианте осуществления настоящего изобретения, лецитин, полиоксилстеариловый эфир, каприлкапроилполиоксилглицерид и/или холестерин могут использоваться по отдельности или в любом их сочетании.
Эмульгатор присутствует в настоящей композиции в типичном случае в количестве, составляющем примерно 0,05-15 вес.%, или в количестве 0,1-10 вес.%, или в количестве 0,1-8 вес.% от общего веса всей композиции.
Используемый в настоящем изобретении загуститель или гелеобразующий агент может вводиться в состав данной композиции для разных целей, таких как загущение, образование геля, эмульгирование и/или стабилизация, и может быть выбран, например, из целлюлозы, такой как карбоксиметилцеллюлоза или гидроксиэтилцеллюлоза; полиакрилатов, таких как, например, карбомер или карбопол (например, Carbopol® 974), поликарбофилов, таких как, например, Noveon® AA-1, поливинилового спирта, такого как Mowiol® 26-88; поливинилпирролидона, такого как повидон® K30; сополимера натрий-акриламида/акроилдиметилтаурата, такого как Сепинео® P600 (Sepineo® P600), и ксантановой камеди. В одном варианте осуществления настоящего изобретения, Сепинео® P600 (Sepineo® P600) и ксантановая камедь могут использоваться по отдельности или в сочетании.
Такой загуститель или гелеобразующий агент присутствует в настоящей композиции в типичном случае в количестве, составляющем примерно 0,05-10 вес.%, или в количестве 0,1-7 вес.%, или в количестве 0,1-5 вес.% от общего веса всей композиции.
Используемый в настоящем изобретении буфер может вводиться в состав данной композиции для целей корректировки с течением времени уровня pH, предпочтительно до физиологического значения pH. Примеры буферных веществ включают ацетатный, аскорбатный, боратный, гидрокарбонатный/карбонатный, цитратный, глюконатный, лактатный, фосфатный, пропионатный и Трис (TRIS) (трометаминовый) буферы. В одном варианте осуществления настоящего изобретения, используется цитратный буфер. Количество добавляемого буферного вещества представляет собой, в типичном случае, такое количество, которое необходимо для создания и поддержания показателя рН в физиологически приемлемом диапазоне значений. Указанный физиологически приемлемый диапазон значений рН составляет в основном от 4 до 9, или от 4,5 до 8,5, или от 5,0 до 8,2.
Используемый в настоящем изобретении подщелачивающий агент может вводиться в состав данной композиции для целей корректировки уровня pH, предпочтительно до физиологического значения pH. Примеры подщелачивающих агентов включают гидроксид натрия, гидроксид аммония, триэтиламин или трис(2-гидроксиэтил)амин. Количество добавляемого подщелачивающего агента представляет собой, в типичном случае, количество, необходимое для корректировки и поддержания показателя рН в физиологически приемлемом диапазоне значений. Указанный физиологически приемлемый диапазон значений рН составляет в основном от 4 до 9, или от 4,5 до 8,5, или от 5,0 до 8,2.
Консервант , вводимый, при наличии такой потребности, может представлять собой, например, четвертичное аммониевое соединение, такое как хлорид бензалкония (N-бензил-N-(C8-C18алкил)-N,N-диметиламмония хлорид), хлорид бензоксония, или консерванты, отличные от четвертичных аммониевых солей, типа парабенов, такие как, например, метилпарабен или пропилпарабен, спирты, такие как, например, хлорбутанол, бензиловый спирт, феноксиэтанол или фенилэтанол, производные гуанидина, такие как, например, хлоргексидин или полигексаметиленбигуанид, перборат натрия, Гермал ®II (Germal®II) или сорбиновая кислота. В одном варианте осуществления настоящего изобретения, может использоваться феноксиэтанол.
Количество присутствующего в композиции консерванта представляет собой такое количество, которое позволяет эффективно сохранять композицию. Настоящая композиция может содержать консервант в количестве, составляющем в типичном случае от 0,01 до 10% вес.%, или в количестве от 0,1 до 10 вес.%, или в количестве от 0,1 to 5 вес.%, или в количестве от 0,1 to 2 вес.% от общего веса всей композиции.
Для целей применения в настоящем изобретении, антиоксидант может быть выбран, например, из аскорбиновой кислоты, ацетилцистеина, цистеина, гидросульфита натрия, бутилгидроксианизола, бутилгидрокситолуола или ацетата альфа-токоферола.
В одном варианте осуществления настоящего изобретения, в качестве антиоксиданта может быть выбран бутилгидроксианизол и/или бутилгидрокситолуол. Количество и тип добавляемого антиоксиданта зависит от конкретных потребностей, и в основном его количество может составлять примерно от 0,001 до 5 вес.%, или от 0,01 до 4 вес.%, или от 0,1 до 2 вес.%, или от 0,1 to 1 вес.%, от общего веса всей композиции.
Другие репрезентативные количества и типы эксципиентов, присутствующих в фармацевтической композиции по настоящему изобретению, представлены в приведенных ниже конкретных примерах.
Другие варианты осуществления настоящего изобретения включают следующие:
Вариант 1 относится к фармацевтической композиции, подходящей для местного применения, которая включает:
(a) модулятор TLR7, включающий производное бензо[f][1,7]нафтиридина;
(b) растворитель,
(c) эмульгатор, выбранный из лецитина (фосфатидилхолина), полиоксилстеарилового эфира, каприлкапроилполиоксилглицерида, цетилового спирта и холестерина;
(d) загуститель или гелеобразующий агент, выбранный из полиакрилатов, например, карбомера или карбопола, сополимера на основе акрилоилдиметилтаурата, например, Сепинео® P600 (Sepineo® P600), и ксантановой камеди;
(e) буфер,
(f) подщелачивающий агент,
(g) консервант и необязательно
(h) антиоксидант.
Вариант 2 относится к композиции согласно варианту 1, где модулятор TLR7 представляет собой соединение формулы (I):
 (I)
(I)
где каждый из R1, R2 и R3 независимо выбран из H, -CH3, -CH2CH3, -CF3, CH2OH -OCH3, -COOCH3, -COOCH2CH3, F, Cl, Br, -CH2OCH3, -CH2OCH2CH3, -(CH3)2, -((O(CH2)2)2-OH, -O(CH2)2-OH, -O(CH2)2-(PO3H2), -O(CH2)2-COOH, -O(CH2)2-CH(CH3)2, C2-C6-алкила, замещенного 1-3 заместителями, выбранными из -OH, -CH3, циклопропила, -O(CH2)2-COOH, -O(CH2)2-(PO3H2), -COOH, -COOCH3 и -COOCH2CH3; и n равно 0, 1, 2 или 3; или представляет собой его фармацевтически приемлемую соль.
Вариант 3 относится к композиции согласно любому указанному выше варианту осуществления настоящего изобретения (варианты 1-2), где указанный растворитель выбран из воды, этанола, пропиленгликоля, моноэтилового эфира диэтиленгиколя и бензилового спирта.
Вариант 4 относится к композиции согласно любому указанному выше варианту осуществления настоящего изобретения (варианты 1-3), где указанный буфер представляет собой цитрат натрия.
Вариант 5 относится к композиции согласно любому указанному выше варианту осуществления настоящего изобретения (варианты 1-4), где указанный консервант представляет собой феноксиэтанол.
Вариант 6 относится к композиции согласно любому указанному выше варианту осуществления настоящего изобретения (варианты 1-5), где указанный подщелачивающий агент представляет собой гидроксид натрия.
Вариант 7 относится к композиции согласно любому указанному выше варианту осуществления настоящего изобретения (варианты 1-6), где указанный антиоксидант представляет собой бутилгидроксианизол.
Вариант 8 относится к композиции согласно любому указанному выше варианту осуществления настоящего изобретения (варианты 1-7), где указанный модулятор TLR7 представляет собой соединение формулы (II), (III) или (IV) или его фармацевтически приемлемую соль:
(II) 
 (III)
(III)
 (IV)
(IV)
Вариант 9 относится к композиции согласно любому указанному выше варианту осуществления настоящего изобретения (варианты 1-8), которая представляет собой крем или гель.
Вариант 10 относится к композиции согласно варианту 1, которая включает следующие компоненты:
Соединение формулы (II) 0,0075 мг
Вода очищенная 19,235 мг Этанол, безводный 2,5 мг
Моноэтиловый эфир диэтиленгликоля 1,0 мг
Лецитин 1,0 мг
Сепинео® P600 (Sepineo® P600) 1,0 мг
Феноксиэтанол 0,125 мг
Цитрат натрия 0,0725 мг
Холестерин 0,03 мг; и Лимонная кислота, безводная 0,03 мг.
Вариант 11 относится к композиции согласно варианту 1, которая включает следующие компоненты:
Соединение формулы (II) 0,0375 мг
Вода очищенная 11,1625 мг
Пропиленгликоль 4,0 мг
Моноэтиловый эфир диэтиленгликоля 2,5 мг
Кукурузное масло 1,250 мг
Бензиловый спирт 0,750 мг
Каприлкапроилполиоксилглицериды 1,250 мг
Полиоксилстеариловый эфир 1,75 мг
(Бридж® S2 (Brij® S2) и Бридж® S721 (Brij® S721) в соотношении 4: 3)
Цетиловый спирт 0,750 мг
Феноксиэтанол 0,250 мг
Карбомер 0,250 мг
Ксантановая камедь 0,05 мг и
NaOH (2N водный раствор) 1,0 мг.
Вариант 12 относится к композиции согласно варианту 1, состоящей из следующих компонентов:
Соединение формулы (II) 0,03%
Вода очищенная 76,94%
Этанол, безводный 10%
Моноэтиловый эфир диэтиленгликоля 4%
Лецитин 4%
Сепинео® P600 (Sepineo® P600) 4% Феноксиэтанол 0,5%
Цитрат натрия 0,29%
Холестерин 0,12%;
и Лимонная кислота, безводная 0,12%;
где % относится к весовому % от общего количества всей композиции.
Вариант 13 относится к композиции согласно варианту 1, состоящей из следующих компонентов:
Соединение формулы (II) 0,15%
Вода очищенная 44,65%
Пропиленгликоль 16%
Моноэтиловый эфир диэтиленгликоля 10%
Кукурузное масло 5%
Бензиловый спирт 3%
Каприлкапроилполиоксилглицериды 5%
Полиоксилстеариловый эфир 7%
где указанный полиоксилстеариловый эфир состоит из Бриджа® S2 (Brij® S2) и Бриджа® S721 (Brij® S721) в соотношении 4: 3
Цетиловый спирт 3%
Феноксиэтанол 1%
Карбомер 1%
Ксантановая камедь 0,2% и
NaOH (2N водный раствор) 4%;
где % относится к весовому % от общего количества всей композиции.
Вариант 14 относится к композиции согласно варианту 1, состоящей из следующих компонентов:
Соединение формулы (II) 0,0125 мг
Вода очищенная 11,1625 мг
Пропиленгликоль 4,0 мг
Моноэтиловый эфир диэтиленгликоля 2,5 мг
Кукурузное масло 1,250 мг
Бензиловый спирт 0,750 мг
Каприлкапроилполиоксилглицериды 1,250 мг
Полиоксилстеариловый эфир 1,750 мг
Гидроксид натрия 1,0 мг
Цетиловый спирт 0,750 мг
Феноксиэтанол 0,250 мг
Карбомер 0,250 мг
Необязательно бутилгидроксианизол 0,0250 мг; и
Ксантановая камедь 0,05 мг.
Пример 1
В процедуре получения крема для местного применения, следующие количества компонентов (в граммах) присутствуют в партии, состоящей из 25 г (общее количество). Так, соответственно, 1 грамм крема включает 0,3 мг соединения формулы (II). В варианте крема, в котором концентрация соединения формулы (II) соответствует 1 мг активного ингредиента на 1 грамм крема, соединение No. (II) присутствует в количестве 0,025 г на 25 г общего количества крема.
Соединение формулы (II) 0,0075 (соответствует 0,3 мг/г крема) Вода очищенная 19,235
Этанол, безводный 2,5
Моноэтиловый эфир диэтиленгликоля 1,0
Лецитин 1,0
Сепинео® P600 (Sepineo® P600) 1,0
Феноксиэтанол 0,125
Цитрат натрия 0,0725
Холестерин 0,03
Лимонная кислота, безводная 0,03
Описание процесса производства (указанный процесс был масштабирован до партии размером примерно 25 кг):
1. Безводную лимонную кислоту и цитрат натрия растворяют в очищенной воде (= водная фаза).
2. Соединение формулы (II) суспендируют в этаноле (= липофильная фаза, часть 2) в сосуде.
3. Моноэтиловый эфир диэтиленгликоля, лецитин, холестерин и феноксиэтанол объединяют при перемешивании и нагревании (= липофильная фаза, часть 1).
4. Далее, липофильную фазу, часть 2 переносят в липофильную фазу, часть 1 при перемешивании и нагревании. Сосуд, который использовался на стадии 2, ополаскивают оставшимся количеством безводного этанола.
5. Затем материал со стадии 4 добавляют к материалу со стадии 1, т.е. к водной фазу, при перемешивании и гомогенизации в условиях охлаждения.
6. После этого, Сепинео® P600 (Sepineo® P600) добавляют к материалу со стадии 5, при перемешивании и гомогенизации. Перемешивание продолжают до получения гомогенного крема.
7. Затем полученный крем переносят в подходящий сосуд.
8. После этого крем вводят в алюминиевые тубы (например, тубы, включающие 10 г крема), и затем тубы закрывают.
Оценка стабильности
Стабильность композиции крема, описанной в примере 1, оценивают, проводя анализы в течение 12 месяцев при температуре 25°C. В этих условиях, в указанный период времени не было выявлено неприемлемых количеств продуктов деградации (одного или нескольких).
Пример 2
В процедуре получения крема для местного применения, используют партию, состоящую из 25 г (общее количество), в которой содержатся следующие количества компонентов (в граммах). Соответственно, в 1 грамме крема содержится 0,5 соединения No (II).
Соединение формулы (II) 0,0125 (соответствует 0,5 мг/г крема)
Очищенная вода 11,1625
Пропиленгликоль (ПГ) 4,0
Моноэтиловый эфир диэтиленгликоля 2,5
(=Транскутол® HP (Transcutol® HP))
Кукурузное масло 1,250
Бензиловый спирт 0,750
Каприлкапроилполиоксилглицериды 1,250
(Лабрасол® (Labrasol®))
Полиоксилстеариловый эфир 1,750
(Бридж® S2 (Brij® S2) и Бридж® S721 (Brij® S721) в соотношении 4: 3)
Гидроксид натрия 1,0
Цетиловый спирт 0,750
Феноксиэтанол 0,250
Карбомер 0,250
Необязательно бутилгидроксианизол 0,0250
Ксантановая камедь 0,05
Описание процесса производства (указанный процесс был масштабирован до партии размером примерно 25 кг):
1. Ксантановую камедь диспергируют в пропиленгликоле с получением премикса на основе ксантановой камеди. Указанный премикс на основе ксантановой камеди переносят затем в воду и добавляют карбомер с получением водной фазы.
2. Указанную смесь перемешивают при нагревании до образования гомогенного геля.
3. Соединение формулы (II) суспендируют в моноэтиловом эфире диэтиленгликоля.
4. Затем формируют липофильную фазу путем смешивания следующих компонентов: полиоксилстеариловый эфир, кукурузное масло, цетиловый спирт, каприлкапроилполиоксилглицерид, бензиловый спирт, феноксиэтанол, бутилированный гидроксианизол и суспензия соединения формулы (II) со стадии 3. Сосуд, который использовался на стадии 3, промывают оставшимся количеством моноэтилового эфира диэтиленгликоля и добавляют полученный после промывания материал к указанной липофильной фазе.
5. Затем смесь со стадии 4 перемешивают до образования прозрачного раствора.
6. Далее, раствор со стадии 5 добавляют к гелю, полученному на стадии 2, при этом смесь вначале подвергают только перемешиванию, а затем проводят гомогенизацию смеси при перемешивании.
7. Затем добавляют 2 N раствор NaOH к материалу со стадии 6, продолжая при этом перемешивание и гомогенизацию.
8. Объемный материал, полученный на стадии 7, согласно приведенному описанию, переносят затем в подходящий сосуд.
9. Затем крем, полученный на стадии 7, вводят в алюминиевые тубы, которые плотно закрывают.
Пример 3
Используя процедуру, аналогичную описанной в примере 2, получают следующую композицию, состоящую из следующих компонентов:
Соединение формулы (II) 0,0375 мг
Вода очищенная 11,1625 мг
Пропиленгликоль 4,0 мг
Моноэтиловый эфир диэтиленгликоля 2,5 мг
Кукурузное масло 1,250 мг
Бензиловый спирт 0,750 мг
Каприлкапроилполиоксилглицериды 1,250 мг
Полиоксилстеариловый эфир 1,75 мг
(Бридж® S2 (Brij® S2) и Бридж® S721 (Brij® S721) в соотношении 4: 3)
Цетиловый спирт 0,750 мг
Феноксиэтанол 0,250 мг
Карбомер 0,250 мг
Ксантановая камедь 0,05 мг, и
NaOH (2N водный раствор) 1,0 мг.
Оценка стабильности
Стабильность композиции крема, описанной в примере 2, исследуют, проводя анализы в течение 12 месяцев при температуре 25°C. В этих условиях, в указанный период времени не было выявлено неприемлемых количеств продуктов деградации (одного или нескольких).
Оценка переносимости
Галеновые композиции, описанные в примерах No. 1 и No. 2 (в каждой из них концентрация активного ингредиента составляла 0,25% и некоторые ингредиенты были откорректированы по количеству), исследовали при местном нанесении на кожу домашних свиней и регистрировали в течение 16 дней средний балльный показатель воспаления. Указанные балльные показатели определяли путем вычисления суммы очков, характеризующих степень воспаления (изменения в гитопатологии). В качестве препарата сравнения, использовали коммерчески доступный крем Альдара® (Aldara®) (5%) (соединение формулы (II) примерно в 100 раз более мощный агонист TLR7, чем Альдара® (Aldara®)), и стандартную галеновую композицию (далее по тексту ʺстандартный гельʺ), имеющую следующие характеристики:
Стандартный гель:
Соединение формулы (II) 0,5%
Полиэтиленгликоль 400 28,75%
Пропиленгликоль 30%
Сепинео® P 600 (Sepineo® P 600) 5%
Транскутол® HP (Transcutol® HP) 10%
Бензиловый спирт 3%
Феноксиэтанол 1%
Олеиловый спирт 1%
Диметилизосорбид 10%
(Лабрасол® (Labrasol®)) 10,5%
БГТ (BHT) 0,1%
БГА (BHA) 0,1%
Токоферол 0,05%
Общее количество 100% (по весу)
Были получены следующие результаты при проведении рейтинговой оценки переносимости:
|
Композиции из примеров 1 и 2 очень хорошо переносились при нанесении на кожу домашних свиней, тогда как стандартный гель и Альдара® (Аldara®) вызывали заметные раздражения на коже, что видно из указанных выше балльных показателей раздражения.
Аналогично процедуре, описанной в примере 1, были приготовлены другие стабильные и хорошо воспринимаемые кожей кремы согласно принципам и объему настоящего изобретения, в соответствии с указанными ниже данными (где % обозначает весовой % и относится к общему весу всей композиции):
|