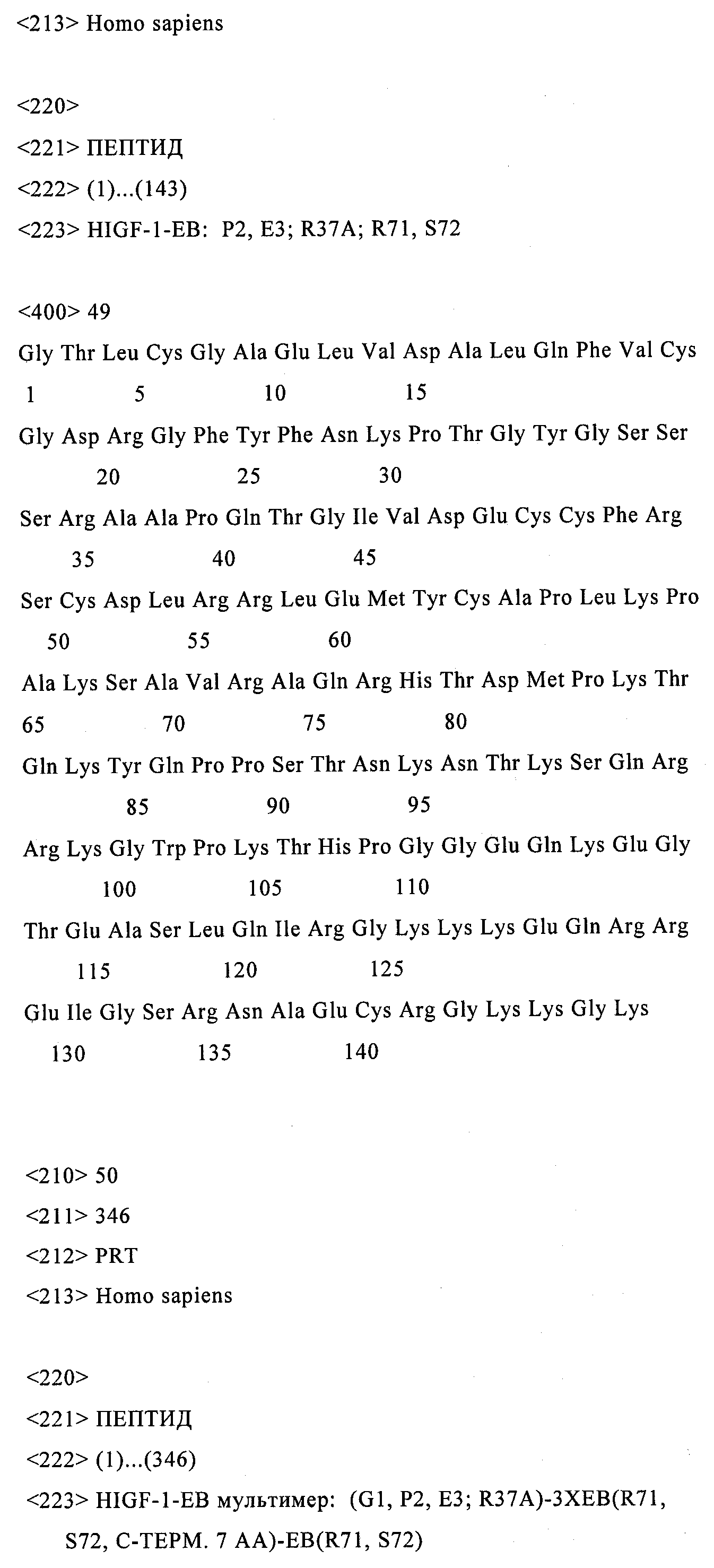Результат интеллектуальной деятельности: СТАБИЛИЗИРОВАННЫЕ ПОЛИПЕПТИДЫ ИНСУЛИНОПОДОБНОГО ФАКТОРА РОСТА
Вид РИД
Изобретение
Предпосылки создания изобретения
Инсулиноподобные факторы роста (IGF) являются частью комплексной системы, которую клетки используют для связи с их физиологическим окружением. Эта комплексная система (которую часто называют осью инсулиноподобных факторов роста) состоит из двух расположенных на клеточной поверхности рецепторов (IGF-1R и IGF-2R), двух лигандов (IGF-1 и IGF-2), семейства, состоящего из шести обладающих высокой аффинностью к связыванию IGF белков (IGFBP 1-6), и ассоциированных с IGFBP расщепляющих ферментов (протеаз). Эта система важна не только для регуляции нормальной физиологической функции, она участвует также в некоторых патологических состояниях (Glass, Nat Cell Biol 5, 2003, с.87-90).
Установлено, что ось IGF играет роль в усилении клеточной пролиферации и ингибировании клеточной гибели (апоптоз). IGF-1 секретируется главным образом печенью в результате стимуляции человеческим гормоном роста (hGH). IGF-1 оказывает воздействие почти на все клетки в человеческом организме, прежде всего на клетки в мышцах, хрящах, костях, печени, почках, нервах, коже и легких. Помимо инсулиноподобного действия, IGF-1 может регулировать также рост клеток. IGF-1 и IGF-2 регулируются семейством генных продуктов, которые известны как IGF-связывающие белки. Эти белки способствуют модуляции действия IGF сложными путями, которые включают как ингибирование действия IGF в результате предотвращения связывания с IGF-рецепторами, так и усиление действия IGF благодаря «помощи» в переносе к рецепторам и удлинению времени полужизни IGF в кровотоке. Существует по меньшей мере шесть обладающих способностью к связыванию с IGF белков (IGFBP1-6).
В своей зрелой форме человеческий IGF-1 (gpetlcgaelvdalqfvcgdrgfyfnkptgygsssrrapqtgivdeccfrscdlrrlemycaplkpaksa; SEQ ID NO:1), который называют также соматомедином, представляет собой небольшой состоящий из 70 аминокислот белок, который, как установлено, стимулирует рост широкого разнообразия клеток в культуре. Кодирование зрелого белка инициируется тремя известными полученными в результате сплайсинга вариантами мРНК. Открытая рамка считывания каждой мРНК кодирует белок-предшественник, содержащий 70 аминокислот IGF-1 и конкретный Е-пептид на С-конце, в зависимости от конкретной мРНК IGF-1. Эти Е-пептиды, которые обозначены как Еа-пептид (rsvraqrhtdmpktqkevhlknasrgsagnknyrm; SEQ ID NO:2), Eb-пептид (rsvraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk; SEQ ID NO:3) и Ес-пептид (rsvraqrhtdmpktqkyqppstnkntksqrrkgstfeerk; SEQ ID NO:4), состоят из 35-87 аминокислот и содержат общую последовательность на N-конце и вариабельную последовательность на С-конце. Например, открытая рамка считывания дикого типа IGF-1-Ea кодирует состоящий из 105 аминокислот полипептид (gpetlcgaelvdalqfvcgdrgfyfhkptgygsssrrapqtgivde cfrscdirrlemycaplkpaksarsvraqrhtdmpktqkevhlknasrgsagnknyrm; SEQ ID NO:5). При экспрессии в физиологических условиях Е-пептиды отщепляются от предшественника с помощью эндогенных протеаз с образованием зрелого состоящего из 70 аминокислот IGF-1, который, как известно, обладает биологической активностью. Установлено, что в определенных ситуациях 1-3 N-концевых аминокислот IGF-1 отщепляются в физиологических условиях с образованием активного IGF-1, который состоит из 67-70 аминокислот. Экспрессия и процессинг гена IGF-2 характеризуются сходными особенностями за исключением наличия только одного Е-пептида (rdvstpptvlpdnfprypvgkffqydtwkqstqrlrrglpallrarrghvlakeleafreakrhrplialptqdpahggap pemasnrk; SEQ ID NO:6), который был идентифицирован в состоящем из 156 аминокислот предшественнике IGF-2 (ayrpsetlcggelvdtlqfvcgdrgfyfsrpasrvsrrsrgiveeccfrscdlalletycatpakserdvstpptvlpdnfprypvgkffqydtwkqstqrlrrglpallrarrghvlakeleafreakrhrplialptqdpahggappemasnrk; SEQ ID NO:7). Как IGF-1, так и IGF-2, по-видимому, обладают неудовлетворительными свойствами в качестве лекарственных средств-кандидатов, поскольку эти белки быстро расщепляются эндогенными протеазами в сыворотке пациентов. Одной из возможных стратегий является стабилизация IGF-1 с получением лекарственного средства путем образования комплекса с одним из связывающихся с ним белков.
Краткое изложение сущности изобретения
Настоящее изобретение основано на открытии того факта, что белок-предшественник IGF-1 или IGF-2, который содержит практически соответствующий ему Е-пептид, является биологическим активным и стабилизированным в присутствии сыворотки, что приводит к образованию полипептида IGF-1 или IGF-2, который можно применять в качестве фармацевтического средства. В композициях, предлагаемых в изобретении, не происходит имеющее место в естественных условиях (нормальное) отщепление Е-пептида от IGF-1, например, в результате мутации или делеции либо аргинина в положении 1, либо серина в положении 2 Е-пептидов (что соответствует положениям 71 и 72 в предшественнике IGF-1 дикого типа). В IGF-2 отщепление не происходит, например, в результате мутации или делеции или аргинина в положении 1, или аспарагиновой кислоты в положении 2 Е-пептида (что соответствует положениям 68 и 69 в предшественнике IGF-2 дикого типа). Другие модификации в белке-предшественнике IGF могут приводить к аннулированию или снижению указанного расщепления.
Кроме того, дополнительные модификации аминокислотой последовательности предшественника IGF-1 могут придавать дополнительные ценные фармацевтические свойства. Например, полипептиды, предлагаемые в изобретении, могут обладать повышенной аффинностью к рецептору IGF-1 или пониженной способностью к связыванию с ингибирующим IGF-1 или IGF-2 связывающимся белком.
Для ясности и единообразия нумерация аминокислотных остатков в предшественниках или зрелых белках IGF-1 или IGF-2 в контексте настоящего описания и в формуле изобретения основана на нумерации в последовательности белка-предшественника дикого типа без сигнального пептида.
Таким образом, изобретение относится к полипептиду, содержащему человеческий белок-предшественник IGF-1, в котором отщепление Е-пептида от IGF-1 протеазой снижено в результате модификации белка-предшественника. Е-пептид может представлять собой Еа-, Eb- или Ес-пептид. На N-конце предшественника аминокислоты G1, P2 или Е3 белка-предшественника могут быть удалены в результате делеции или изменены в результате мутации, например, могут представлять собой R36 (например, R36A) и R37 (например, R37A).
Белок-предшественник может дополнительно включать консенсусную последовательность N-связанного гликозилирования NXS/T, например, в результате встраивания аминокислот 93-102, характерных для Еа-пептида, между аминокислотами N95 и Т96 Eb-пептида. В целом, белок-предшественник может включать олигосахарид, ковалентно связанный с боковой цепью аминокислоты белка-предшественника, такой как боковая цепь аргинина белка-предшественника.
Кроме того, остатки белка-предшественника можно заменять на не встречающиеся в естественных условиях аминокислоты (например, на аминокислоты, которые содержат ацетиленовую группу или азидогруппу). Такие не встречающиеся в естественных условиях аминокислоты могут облегчать связывание поли(этиленгликольного) звена с боковой цепью белка-предшественника, хотя в данной области хорошо известны общепринятые стратегии пэгилирования белков.
Белок-предшественник может включать также один или несколько дополнительных Е-пептидов, сцепленных с С-концом белка-предшественника. Например, полипептид может включать в направлении от N-конца к С-концу (1) белок-предшественник IGF-1, который несет первый Eb-пептид, в котором G1, Р1 и Е1 удалены в результате делеции либо R36, либо R37, либо обе аминокислоты изменены в результате мутации, R71 и S72 удалены в результате делеции и последние семь С-концевых аминокислот первого Eb-пептида удалены в результате делеции; (2) второй Eb-пептид, при этом R71, S72 и последние семь С-концевых аминокислот второго Eb-пептида удалены в результате делеции; (3) третий Eb-пептид, при этом R71, S72 и последние семь С-концевых аминокислот третьего Eb-пептида удалены в результате делеции; и (4) четвертый Eb-пептид, в котором R71 и S72 удалены в результате делеции.
Эффективным путем предупреждения отщепления Е-пептида от IGF-1 является делеция или мутация R71 или S72.
Аналогично этому изобретение относится к человеческому белку-предшественнику IGF-2, в котором отщепление Е-пептида от IGF-2 протеазой снижают путем модификации белка-предшественника. В частности, делеция или мутация R68 или D69 могут представлять собой эффективные пути аннулирования протеазного расщепления белка-предшественника GF-2.
Кроме того, любой Е-пептид IGF-1 можно объединять с IGF-2 и любой Е-пептид IGF-2 можно объединять с IGF-1 с получением указанных в настоящем описании благоприятных действий.
Изобретение относится также к способу лечения заболеваний костно-мышечной системы, диабета, гибели нейронов, заключающемуся в том, что вводят в эффективном количестве полипептид, предлагаемый в изобретении. Изобретение относится также к применению полипептида, предлагаемого в изобретении, для приготовления лекарственного средства, которое предназначено для лечения заболеваний костно-мышечной системы, диабета, гибели нейронов или анемии.
Другим вариантом осуществления изобретения является пэгилированный IGF-1, который не содержит Е-пептид, но в который интродуцирована не встречающаяся в естественных условиях аминокислота в качестве сайта пэгилирования. Под объем изобретения подпадает также любой модифицированный, пэгилированный IGF-1, который содержит не встречающуюся в естественных условиях аминокислоту, указанную в настоящем описании, без Е-пептида.
В изобретении описаны также применяемые в ветеринарии способы и варианты введения полипептида, предлагаемого в изобретении, в эффективном количестве для получения требуемого действия.
Применение в ветеринарии включает (I) увеличение скорости роста и/или размера животного, (II) повышение эффективности превращения корма в ткани организма, (III) увеличение производства молока у животных на стадии лактации, (IV) лечение животного, имеющего симптомы, связанные с кахексией, травмой или другими ассоциированными с истощением заболеваниями, и (V) лечение находящихся на стадии лактации животных для улучшения здоровья новорожденных.
Все процитированные ссылки или документы включены в настоящее описание в качестве ссылки.
Краткое описание чертежей
На чертежах показано:
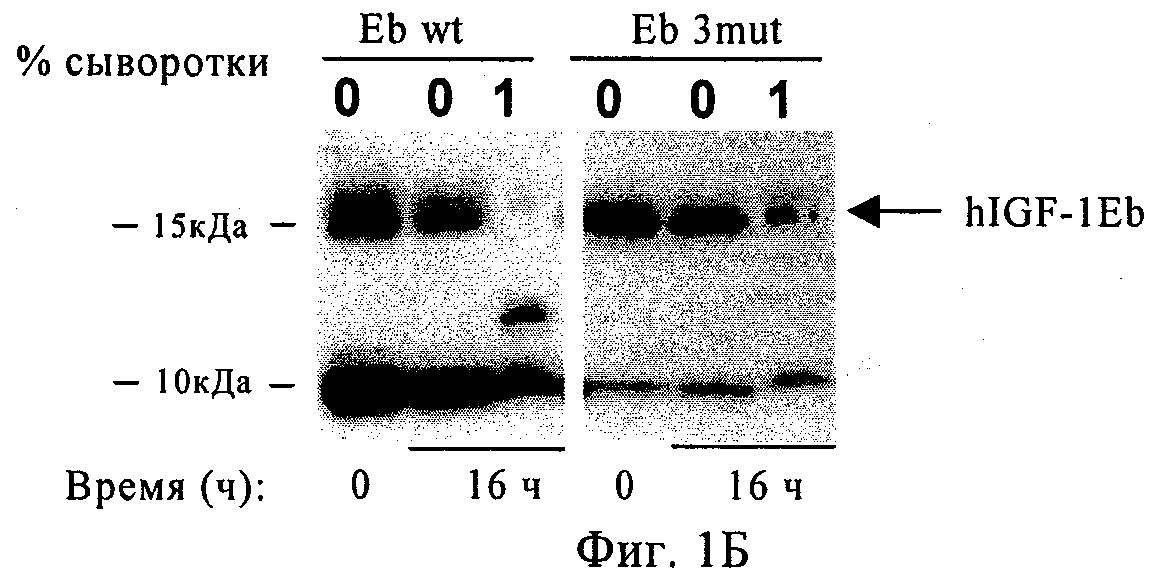
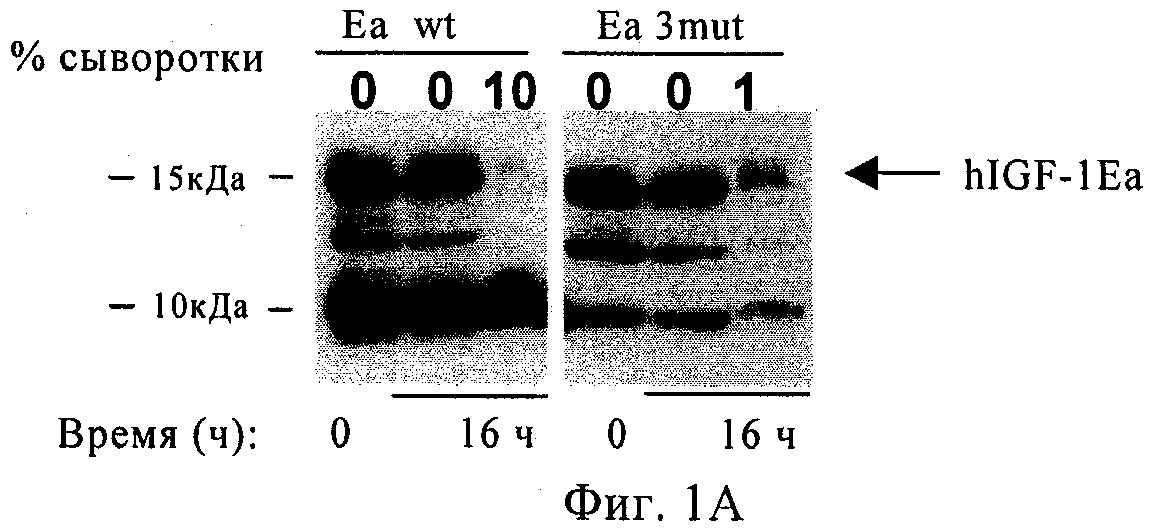
на фиг.1А-1В - результаты Вестерн-блоттинга полипептидов, предлагаемых в изобретении, и предшественника IGF-1 дикого типа после отсутствия инкубации (0 ч) или 16-часовой инкубации в присутствии 10% человеческой сыворотки или без нее при 37°С. Экспрессионными векторами, кодирующими различные конструкции IGF-1, трансфектировали клетки линии Cos7 и получали кондиционированную среду. Обозначение «3mut» относится к предшественнику, представляющему собой hIGF-1-Е-пептид, который имеет следующие три набора модификаций: делецию G1, P2 и Е3; мутацию, приводящую к замене Arg 37 на Ala (R37A); и делецию R71 и S72. На фиг.1А показаны результаты Вестерн-блоттинга (с использованием антитела к IGF-1) полипептида дикого типа и 3mut-предшественника, который содержит Еа. На фиг.1Б показаны результаты Вестерн-блоттинга (с использованием антитела к hIGF-1) полипептида дикого типа и 3mut-предшественника, который содержит Eb. На фиг.1В показаны результаты Вестерн-блоттинга (с использованием антитела к hIGF-1) полипептида дикого типа и 3mut-предшественника, который содержит Ее;
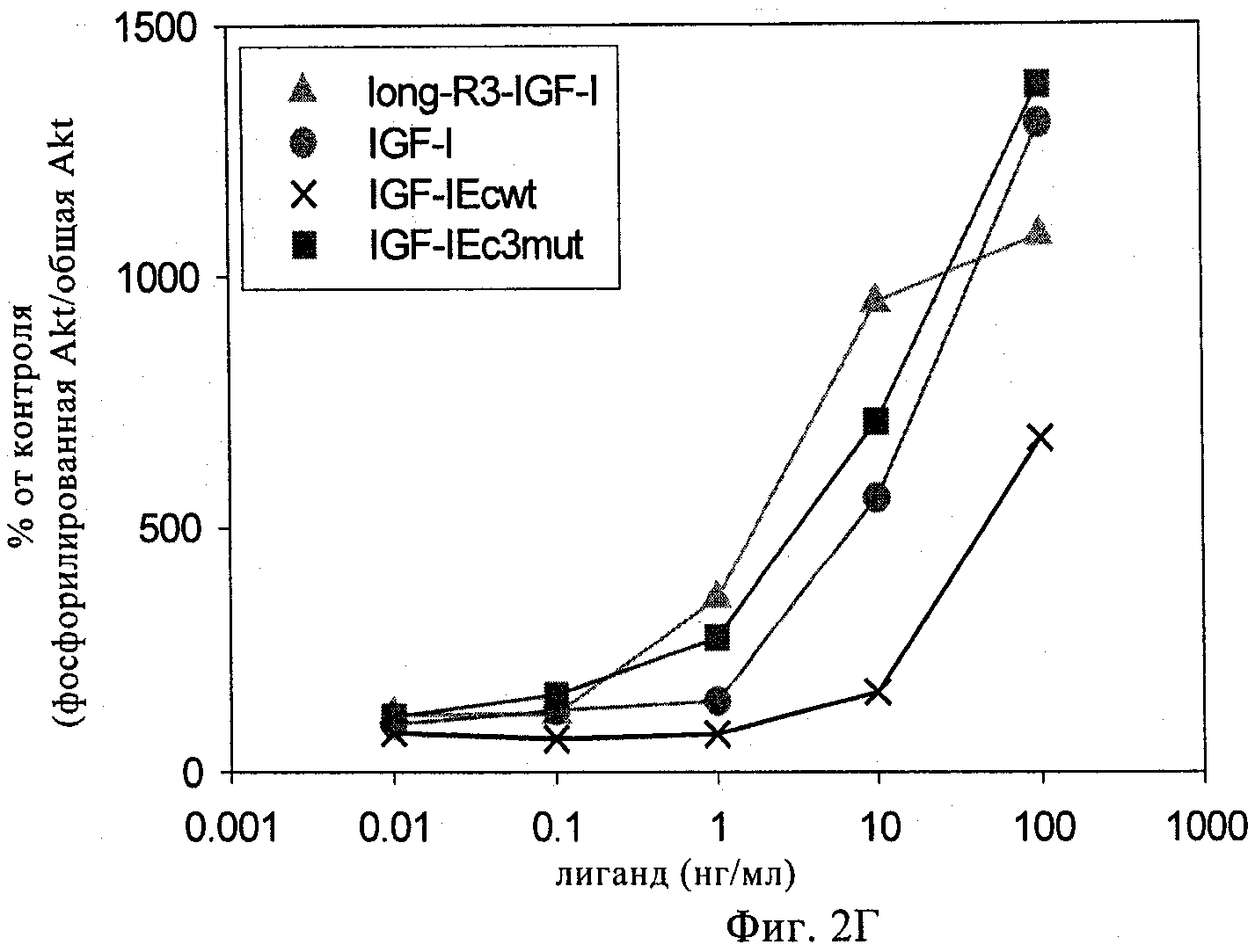
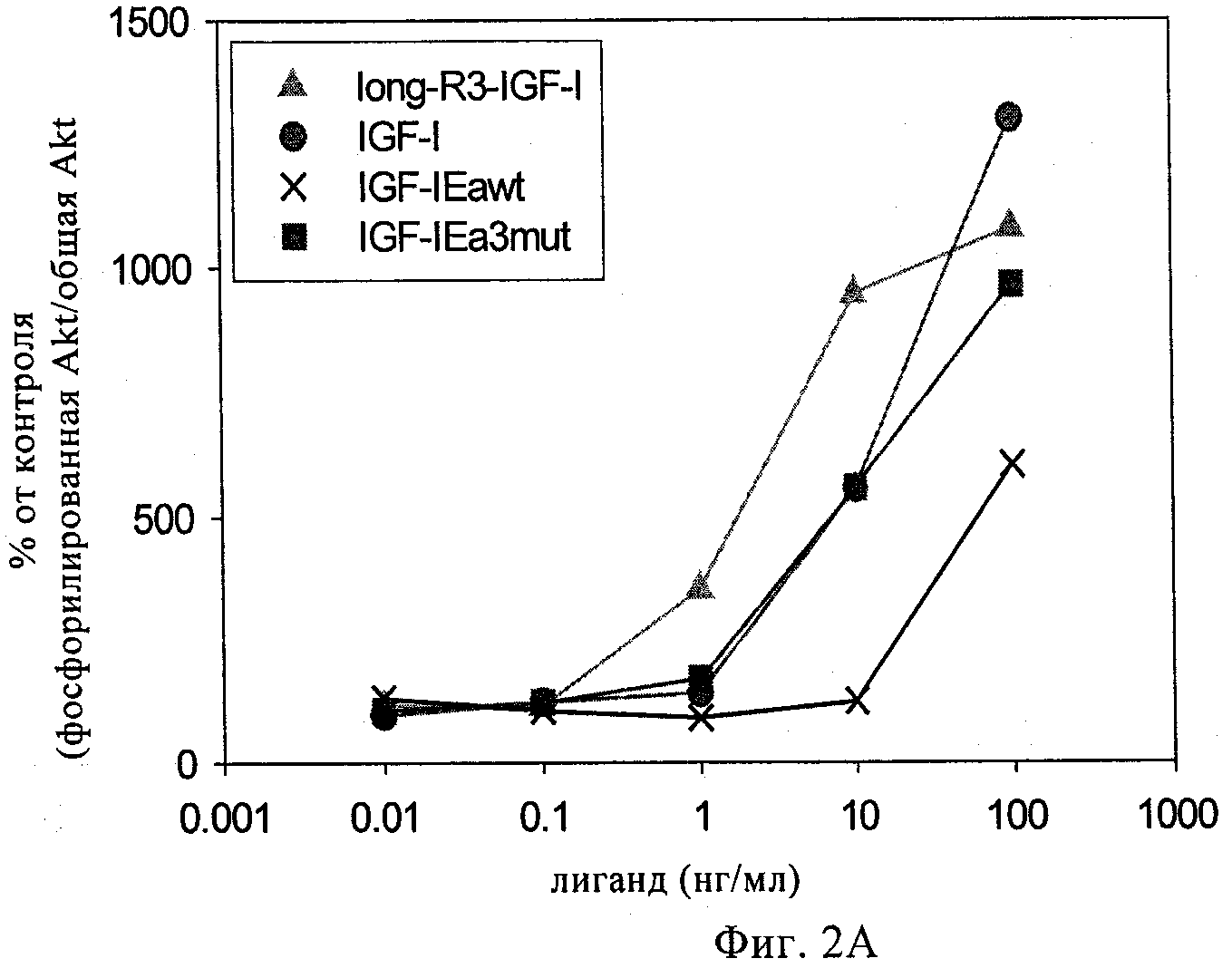
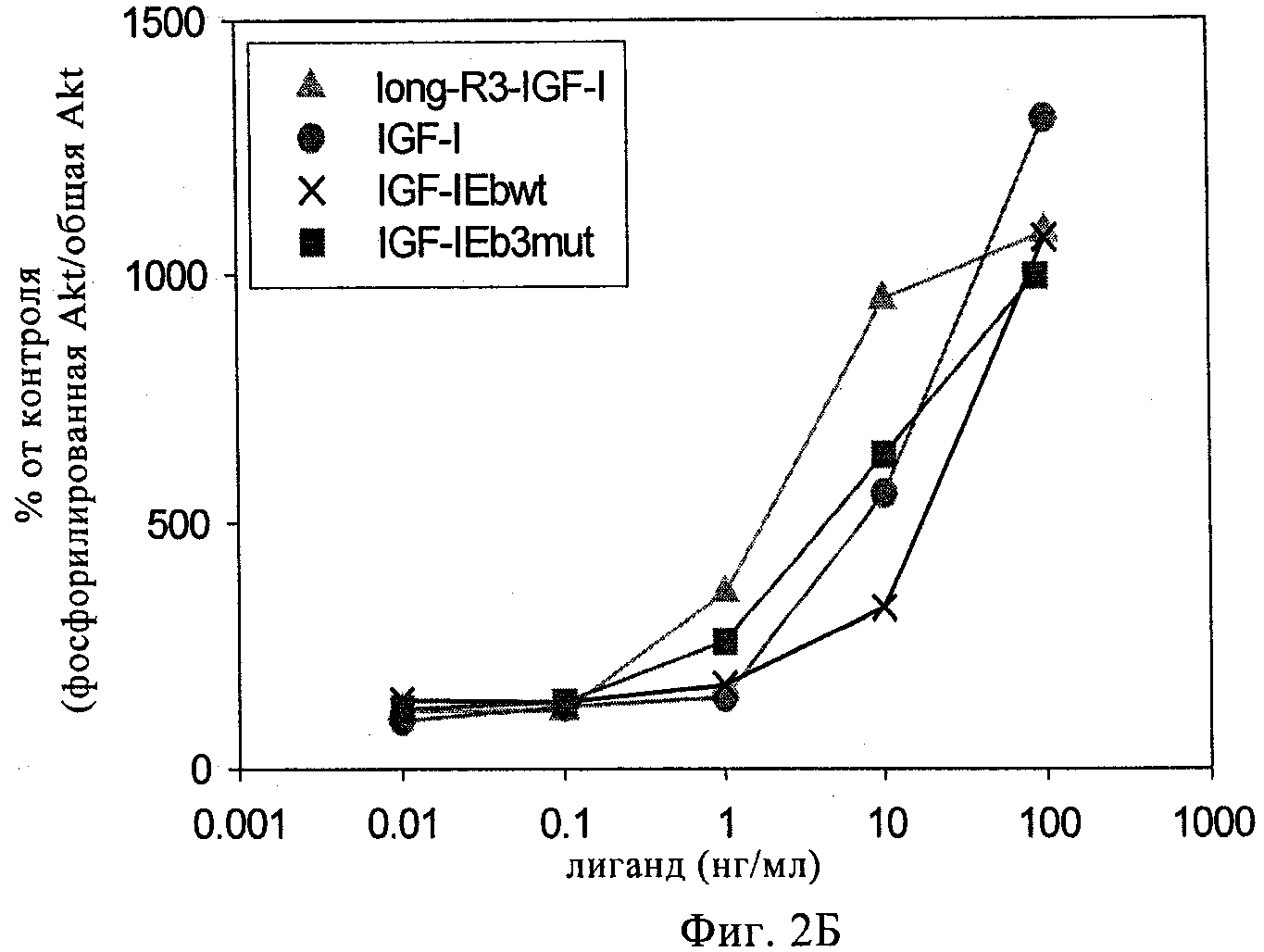
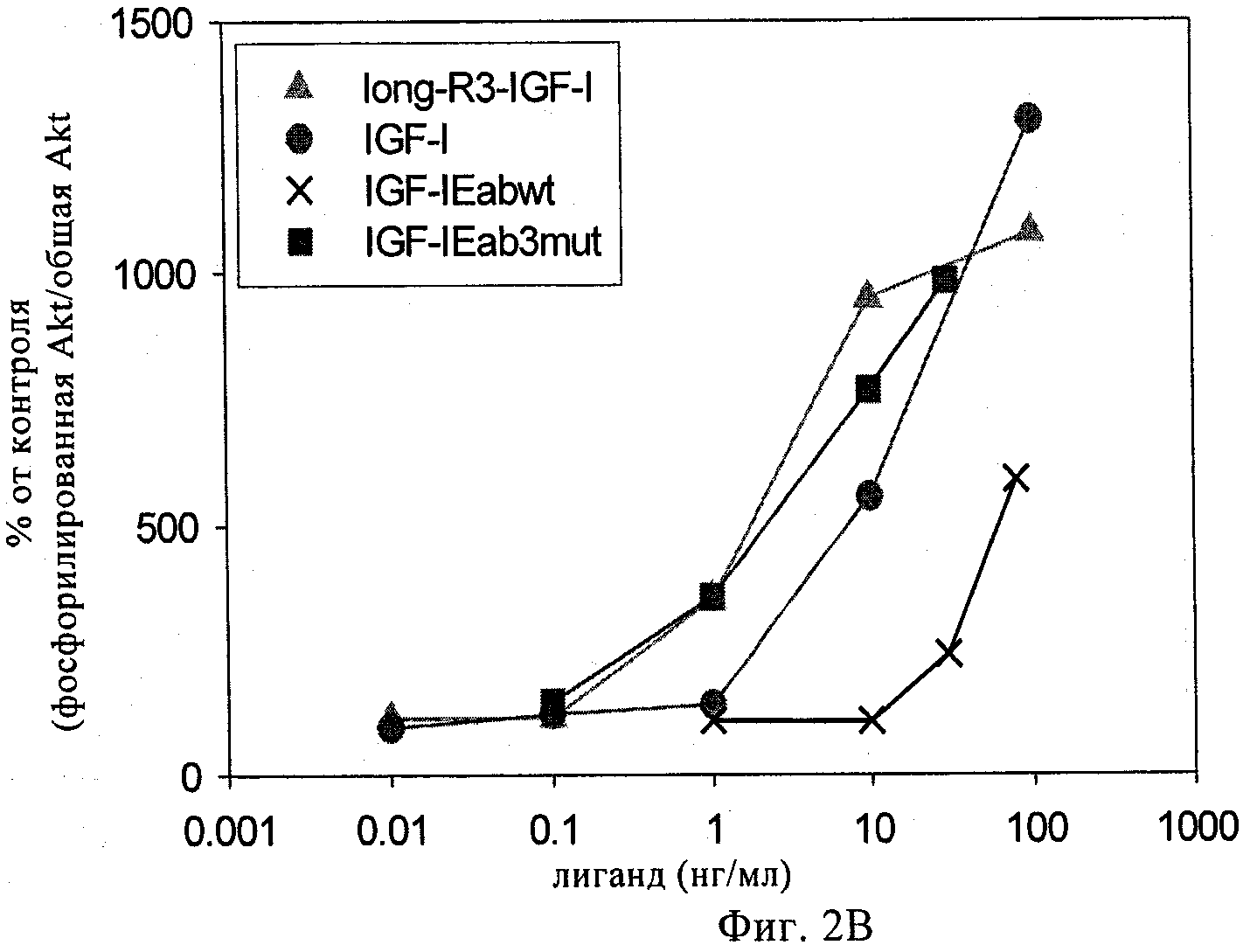
на фиг.2А-2Г - линейные графики, демонстрирующие биологическую активность различных полипептидов IGF-1 («лиганды»). Биологическую активность оценивали путем стимуляции миобластов С2С12 полипептидами, экспрессируемыми Cos7-клетками. Затем в стимулированных С2С12-клетках анализировали относительные количества общей АКТ и фосфорилированной АКТ. Long-R3-IGF-1 представляет собой поступающий в продажу реагент (фирма Sigma, продукт №1-1271), который состоит из зрелой человеческой аминокислотой последовательности IGF-1 с мутацией E3R и с добавлением N-концевого состоящего из 13 аминокислот удлиняющего пептида. На фиг.2А показаны данные об активности IGF-1-Ea3mut. На фиг.2Б показаны данные об активности IGF-1-Eb3mut. На фиг.2В приведены данные об активности IGF-1-Eab3mut, представляющего собой несущую 3mut конструкцию, в которой аминокислоты 93-102 Еа встроены между аминокислотами 95 и 96 Eb. На фиг.2Г показаны данные об активности IGF-1-Ec3mut;
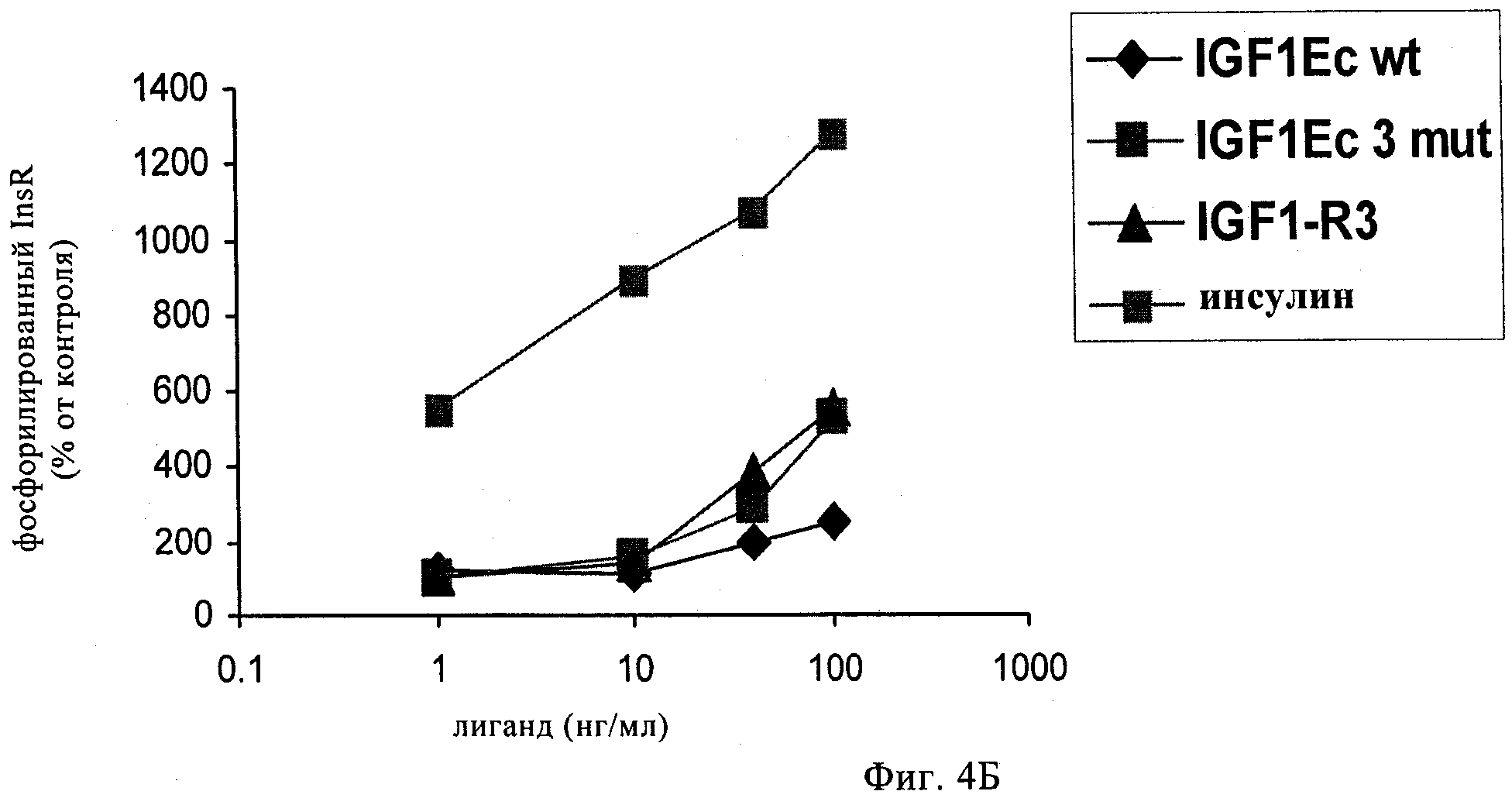
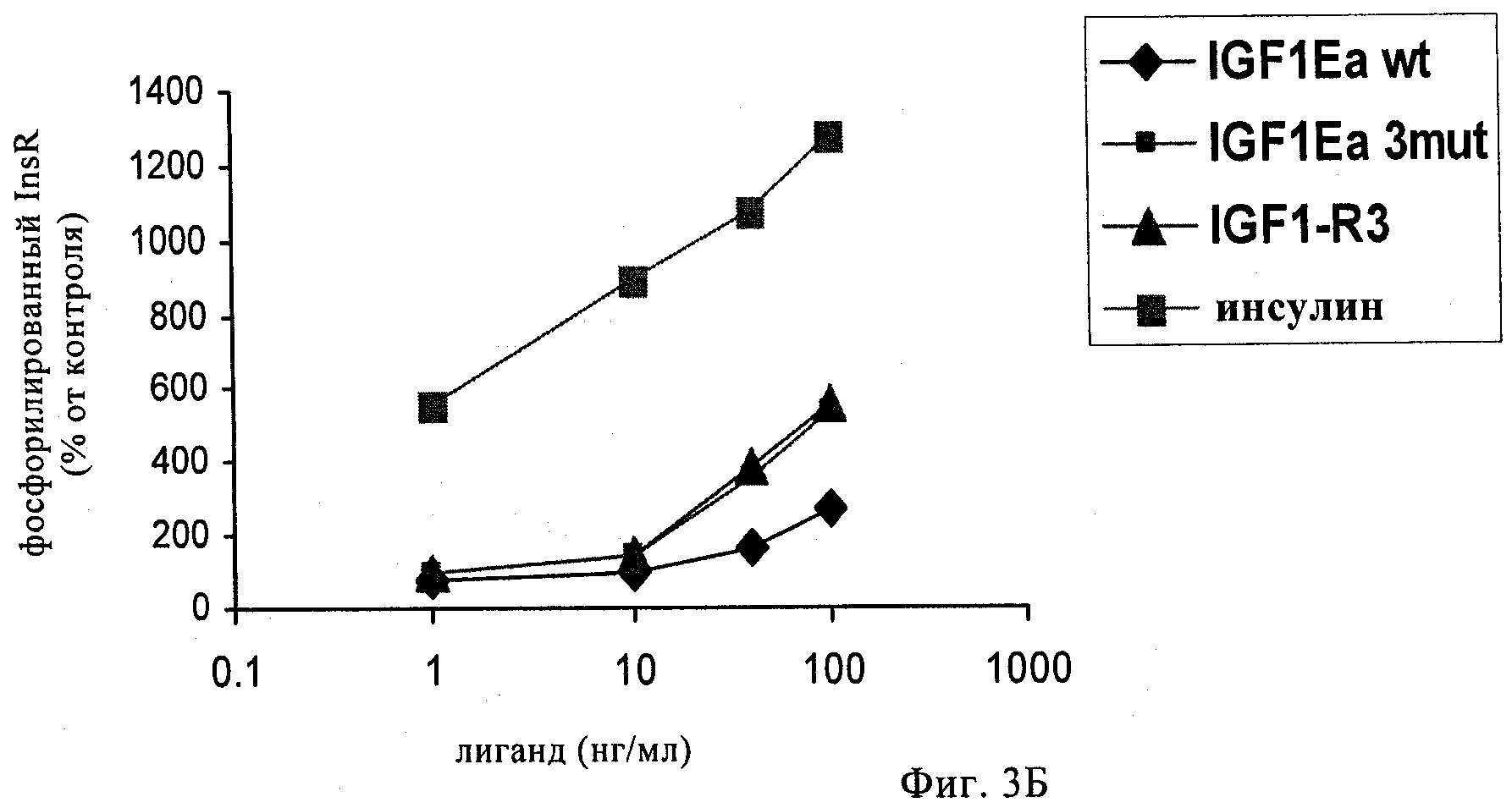
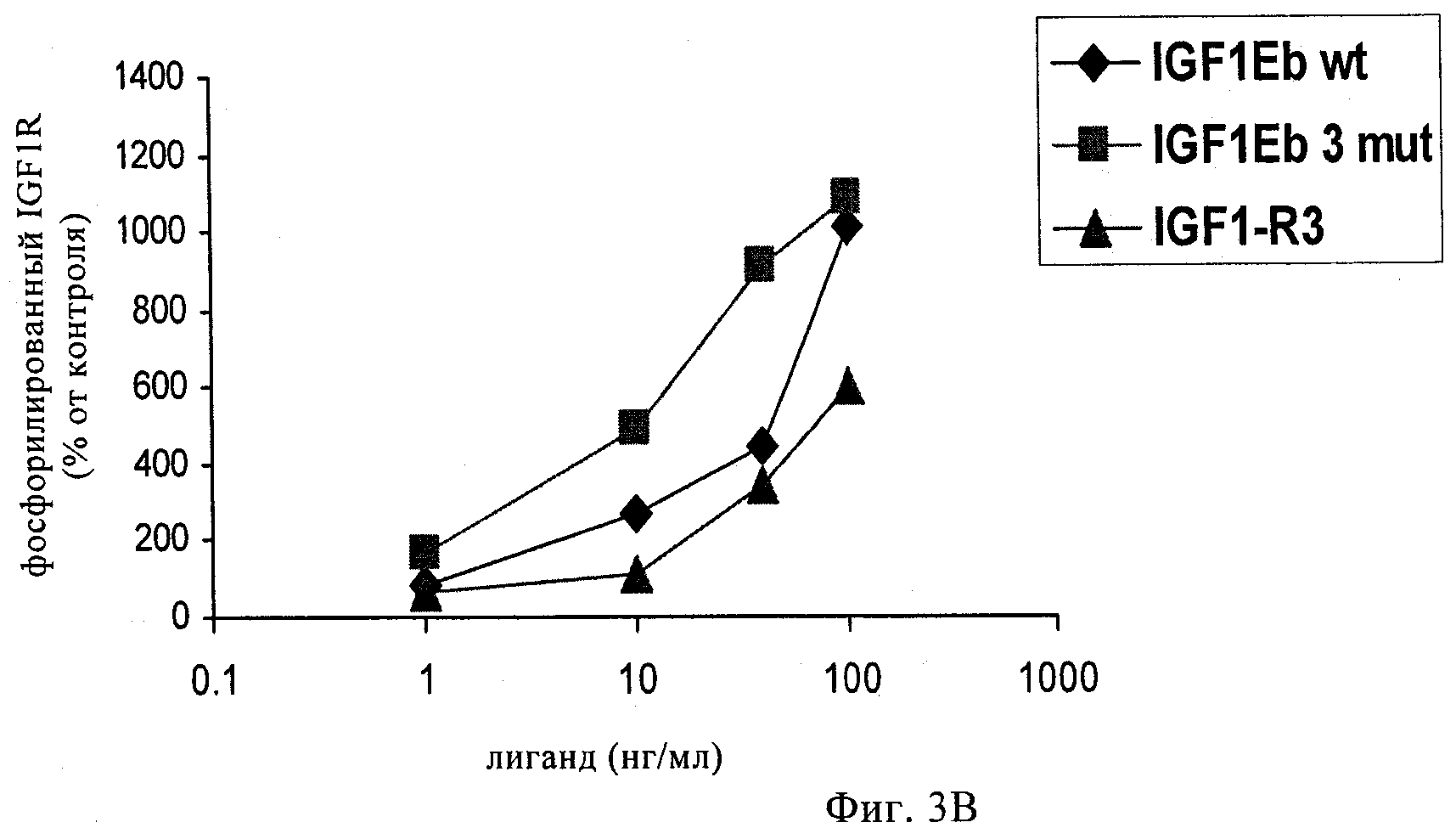
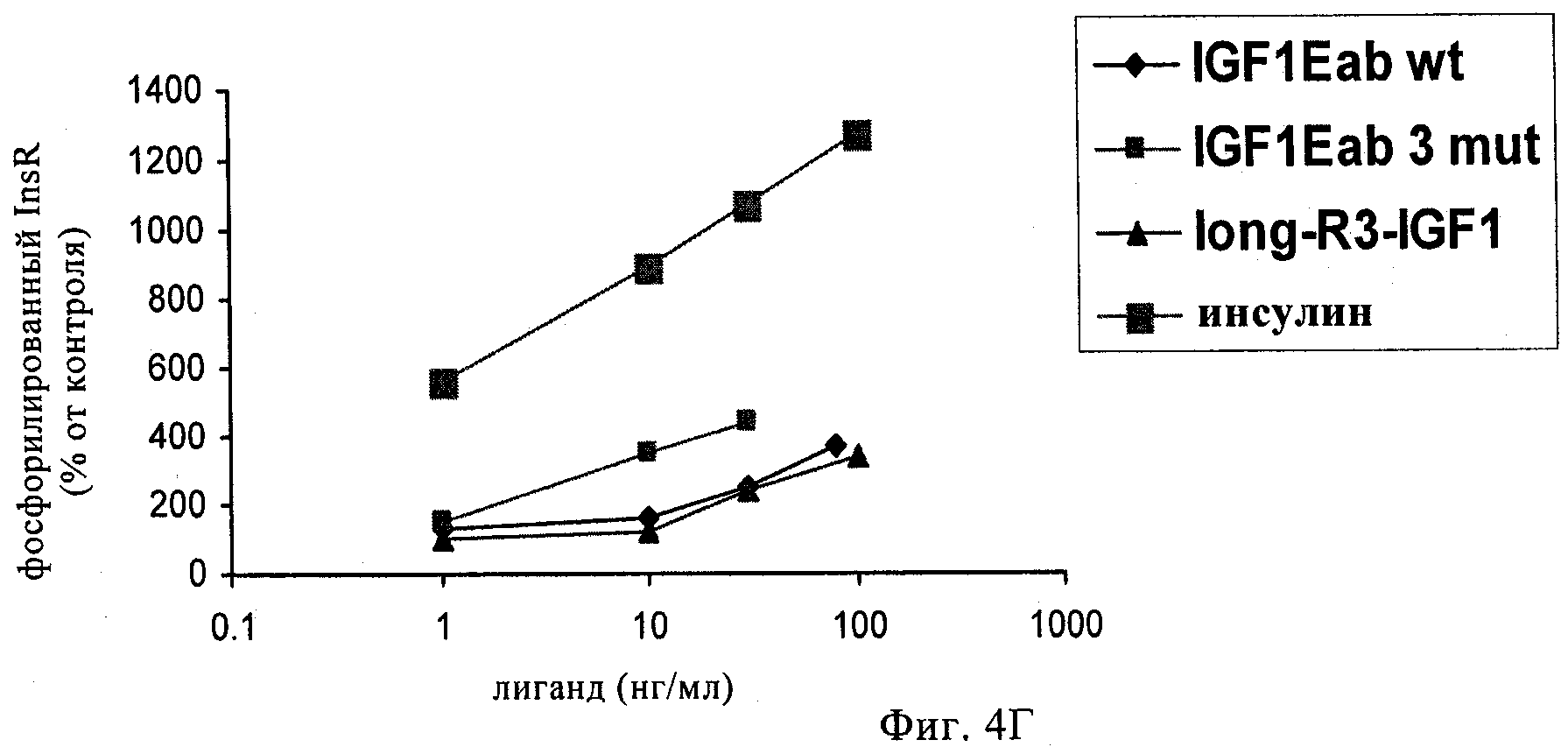
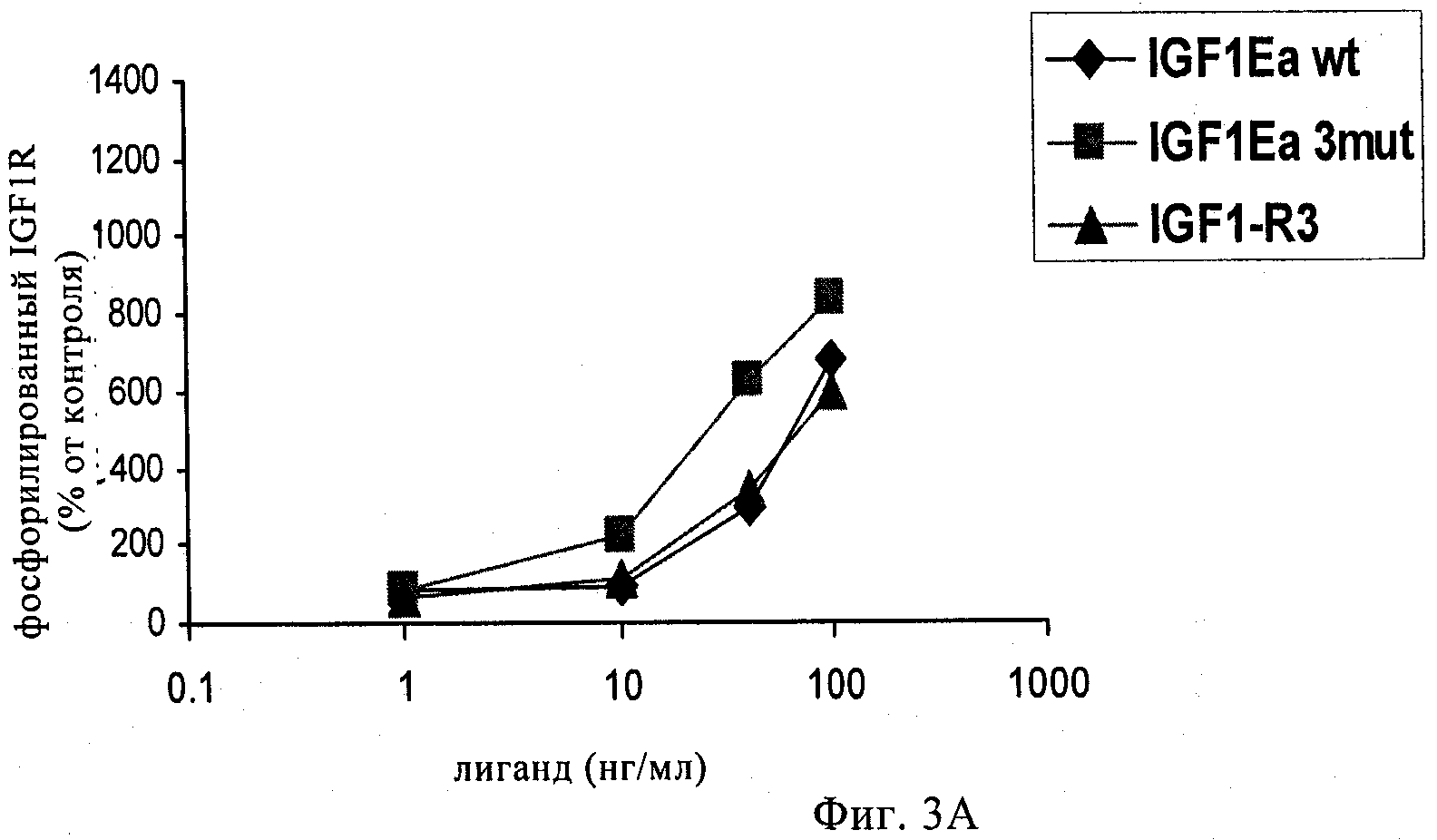
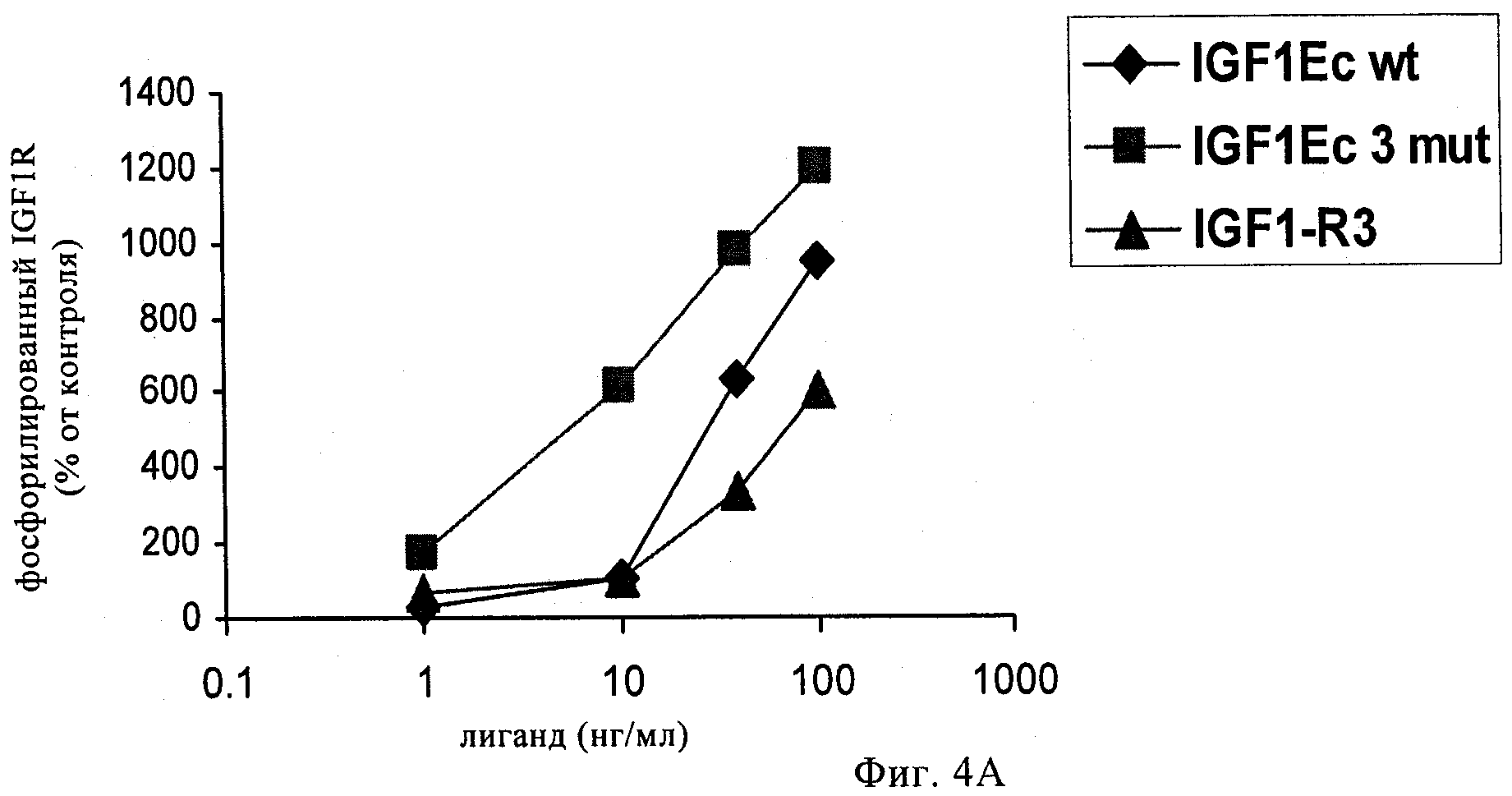
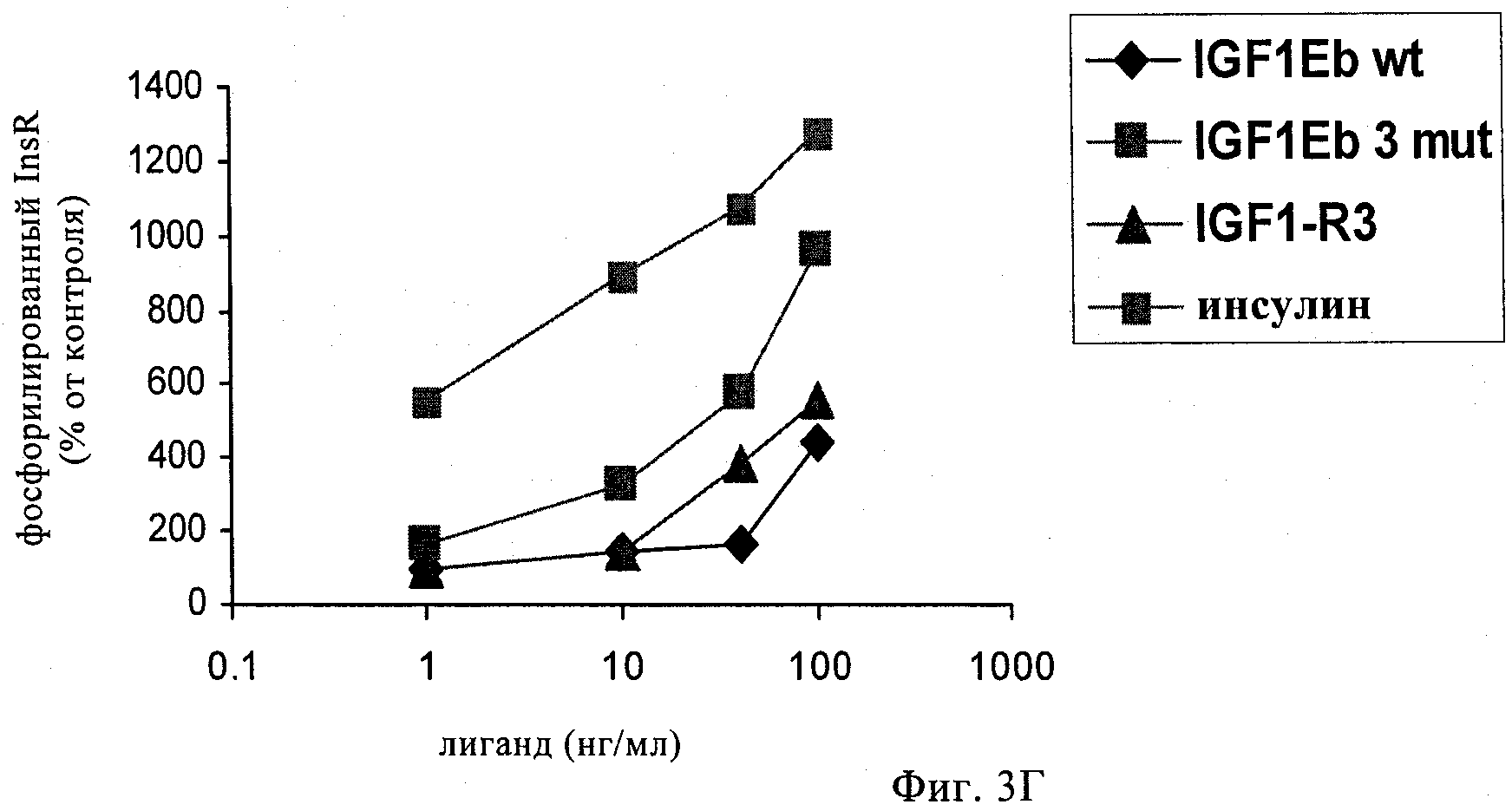
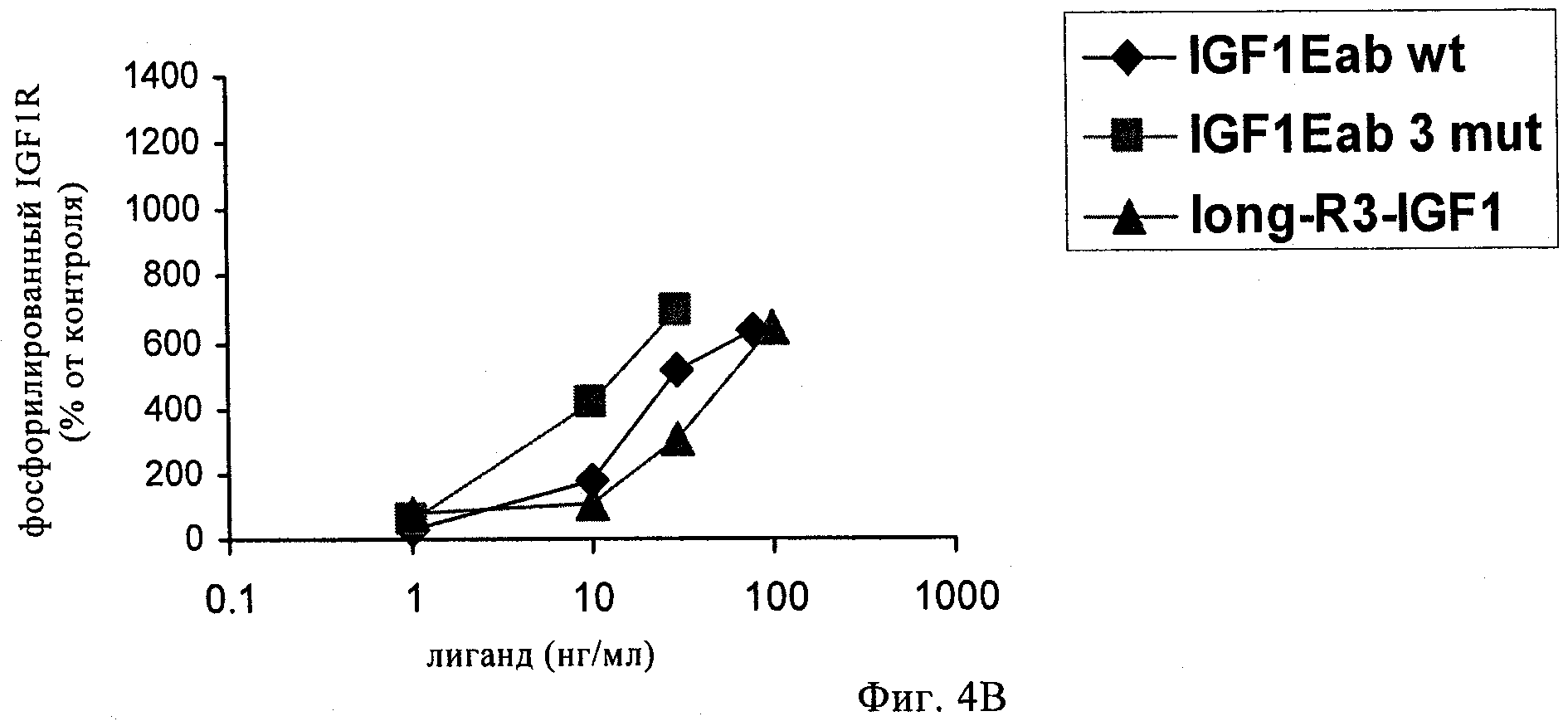
на фиг.3А-3Г и 4А-4Г - линейные графики, позволяющий определять сохраняют ли полипептиды-предшественники IGF-1, предлагаемые в изобретении, селективность по отношению к соответствующему рецептору при анализе фосфорилирования рецептора в ответ на связывание с лигандом. На фиг.3А и 3Б представлены результаты оценки селективности к рецептору IGF-1-Ea3mut по сравнению с рецептором IGF-1 (фиг.3А) и инсулиновым рецептором (фиг.3Б). На фиг.3В и 3Г представлены результаты оценки селективности к рецептору IGF-1-Eb3mut по сравнению с рецептором IGF-1 (фиг.3 В) и инсулиновым рецептором (фиг.3Д). На фиг.4А и 4Б представлены результаты оценки селективности к рецептору IGF-1-Ec3mut по сравнению с рецептором IGF-1 (фиг.4А) и инсулиновым рецептором (фиг.4Б). На фиг.4В и 4Г представлены результаты оценки селективности к рецептору IGF-1-Eab3mut по сравнению с рецептором IGF-1 (фиг.4В) и инсулиновым рецептором (фиг.4Д). «IGF1-R3» обозначает описанный выше Long-R3-IGF-1. Полипептид, обозначенный как «IGF1Eab», представляет собой конструкцию, в которой аминокислоты 93-102 Еа встроены между аминокислотами 95 и 96 Eb;
на фиг.5 - результаты Вестерн-блоттинга, демонстрирующие относительное фосфорилирование АКТ после стимуляции мышечных трубочек линии С2С12 (в результате дифференцировки в течение 3-4 дней миоцитов С2С12) различными лигандами. Понятие «мультимеры IGF-1Eb» используют для обозначения конструкции, изображенной схематически на фиг.6А;
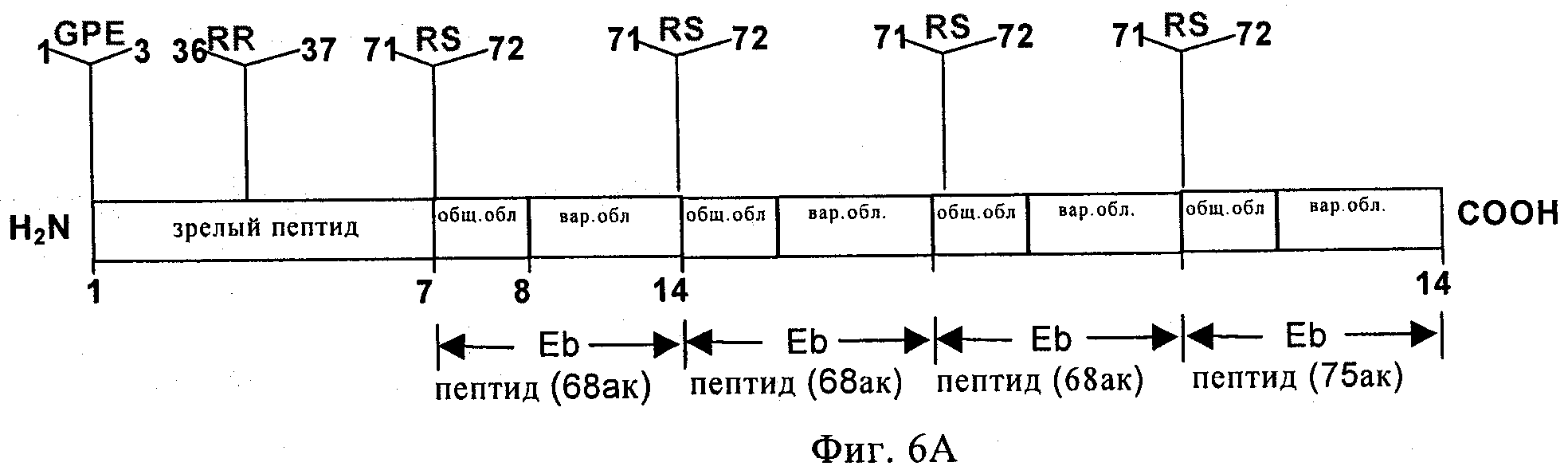
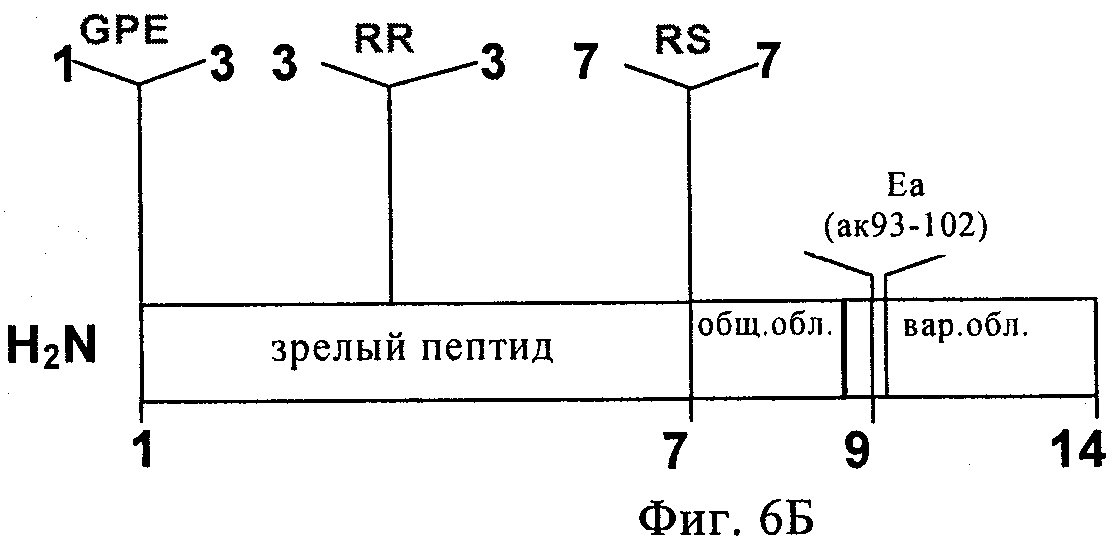
на фиг.6А и 6Б - схематические изображения двух полипептидов, предлагаемых в изобретении. На фиг.6А показан полипептид-предшественник IGF-1-Eb с 4 наборами модификаций: делеция G1, P2 и Е3; мутация, приводящая к замене R37 на А; делеция R71 и S72 и делеция последних семи С-концевых аминокислот. Кроме того, полипептид удлинен путем добавления еще двух Eb-пептидов (но без R71 и S72 и без последних семи С-концевых аминокислот) и добавления последнего Eb-пептида (но без R71 и S72) на С-конец полипептида. Эту конструкцию часто обозначают как мультимер IGF-1-Eb. На фиг.6Б показан полипептид-предшественник IGF-1-Eab с 4 наборами модификаций: делеция Gl, P2 и Е3; мутация, приводящая к замене R37 на А; делеция R71 и S72 и инсерция аминокислот 93-102 Еа между аминокислотами 95 и 96 Eb;
на фиг.7А - сравнительный анализ последовательности человеческого IGF-1 (SEQ ID NO:1) и последовательности IGF-1 соответствующего животного. Представлены все проанализированные виды животных и регистрационные номера в GenBank соответствующих им последовательностей. G1, P2, Е3 являются консервативными для всех проанализированных видов, кроме стерляди (в последовательности этого вида S2 заменен на P2). R36 и R37 являются консервативными для всех проанализированных видов;
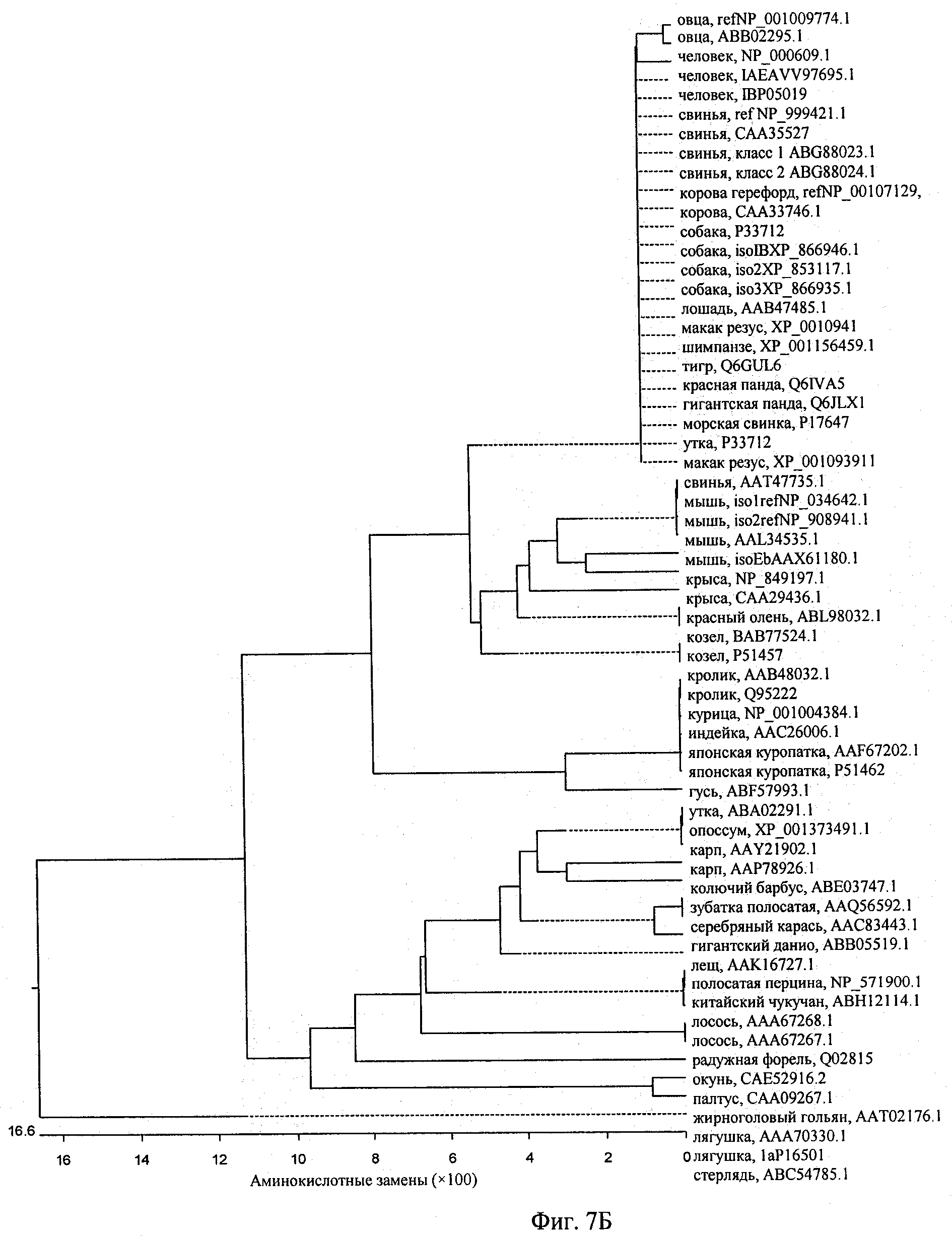
на фиг.7Б - график, демонстрирующий филогению проанализированных аминокислотных последовательностей относительно человеческого IGF-1 (SEQ ID NO:1). Под филогенетическим деревом изображена шкала, на которой указано количество «аминокислотных замен» на 100 остатков белковых последовательностей. Для расчета величин расстояний используют предназначенную для этой цели формулу Кимура (Kimura), полученную на основе данных о количестве не входящих в брешь ошибочных спариваний и скорректированную с учетом молчащих замен. Полученные с помощью компьютерной обработки величины представляют собой среднее значение различий на сайт и находятся в диапазоне от 0 до 1. Ноль обозначает полную идентичность, а 1 обозначает отсутствие идентичности. На шкале филогенетического дерева эти величины умножены на 100;
на фиг.8А - сравнительный анализ последовательностей человеческого Еа-пептида (SEQ ID NO:2) и Еа-пептидов различных животных. Представлены все проанализированные виды животных и регистрационные номера в GenBank соответствующих им последовательностей. R71 и S72 являются консервативными для всех проанализированных видов;
на фиг.8Б - график, демонстрирующий филогению проанализированных аминокислотных последовательностей относительно человеческого Еа-пептида IGF-1 (SEQ ID NO:2);
на фиг.9А - сравнительный анализ последовательностей человеческого Eb-пептида (SEQ ID NO:3) и Eb-пептидов различных животных. Представлены все проанализированные виды животных и регистрационные номера в GenBank соответствующих им последовательностей. R71 и S72 являются консервативными для всех проанализированных видов;
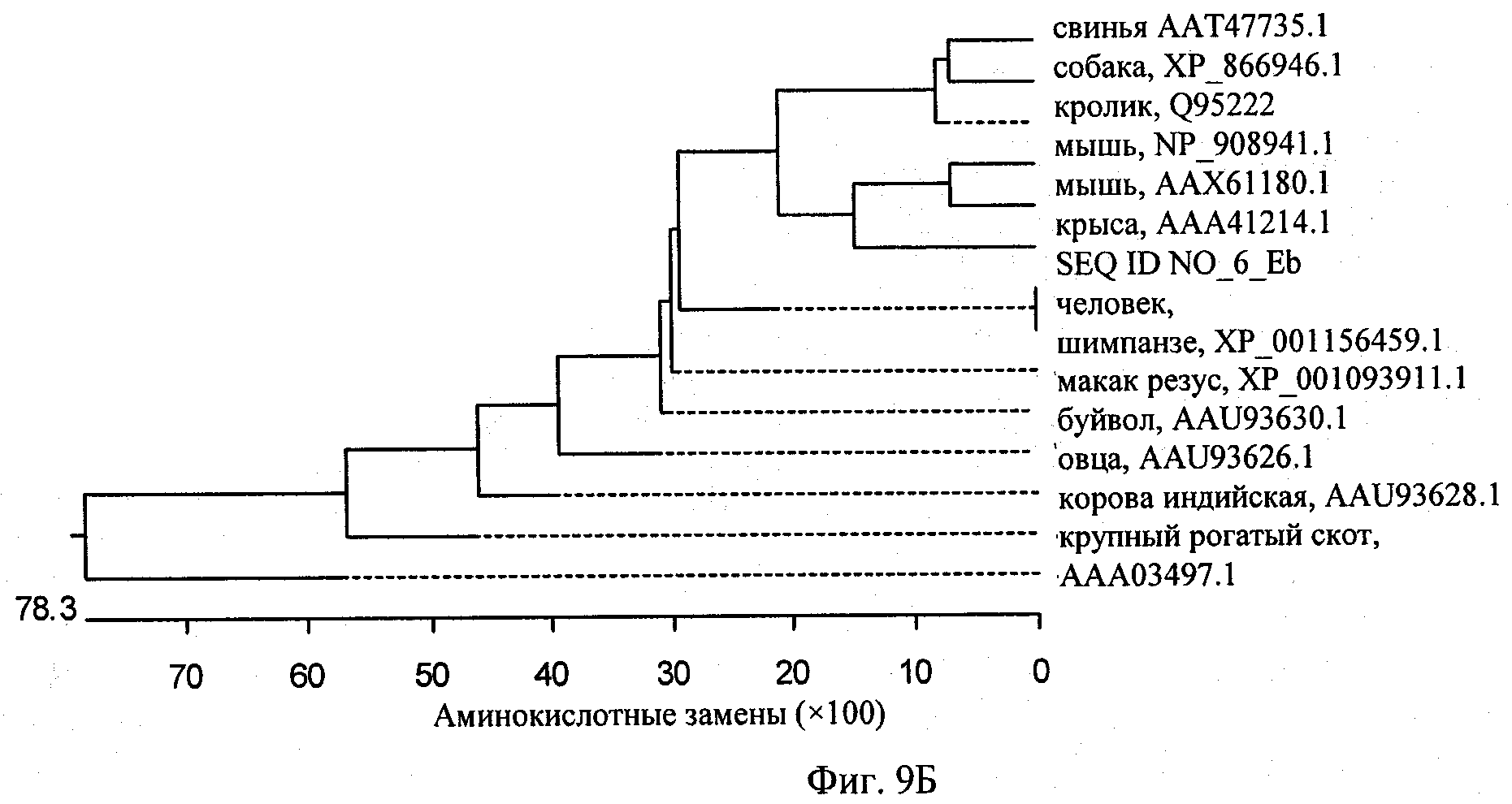
на фиг.9Б - график, демонстрирующий филогению проанализированных аминокислотных последовательностей относительно человеческого Eb-пептида IGF-1 (SEQ ID NO:3);
на фиг.10А - сравнительный анализ последовательностей человеческого Ес-пептида (SEQ ID NO:4) и Ес-пептидов различных животных. Представлены все проанализированные виды животных и регистрационные номера в GenBank соответствующих им последовательностей, R71 и S72 являются консервативными для всех проанализированных видов;
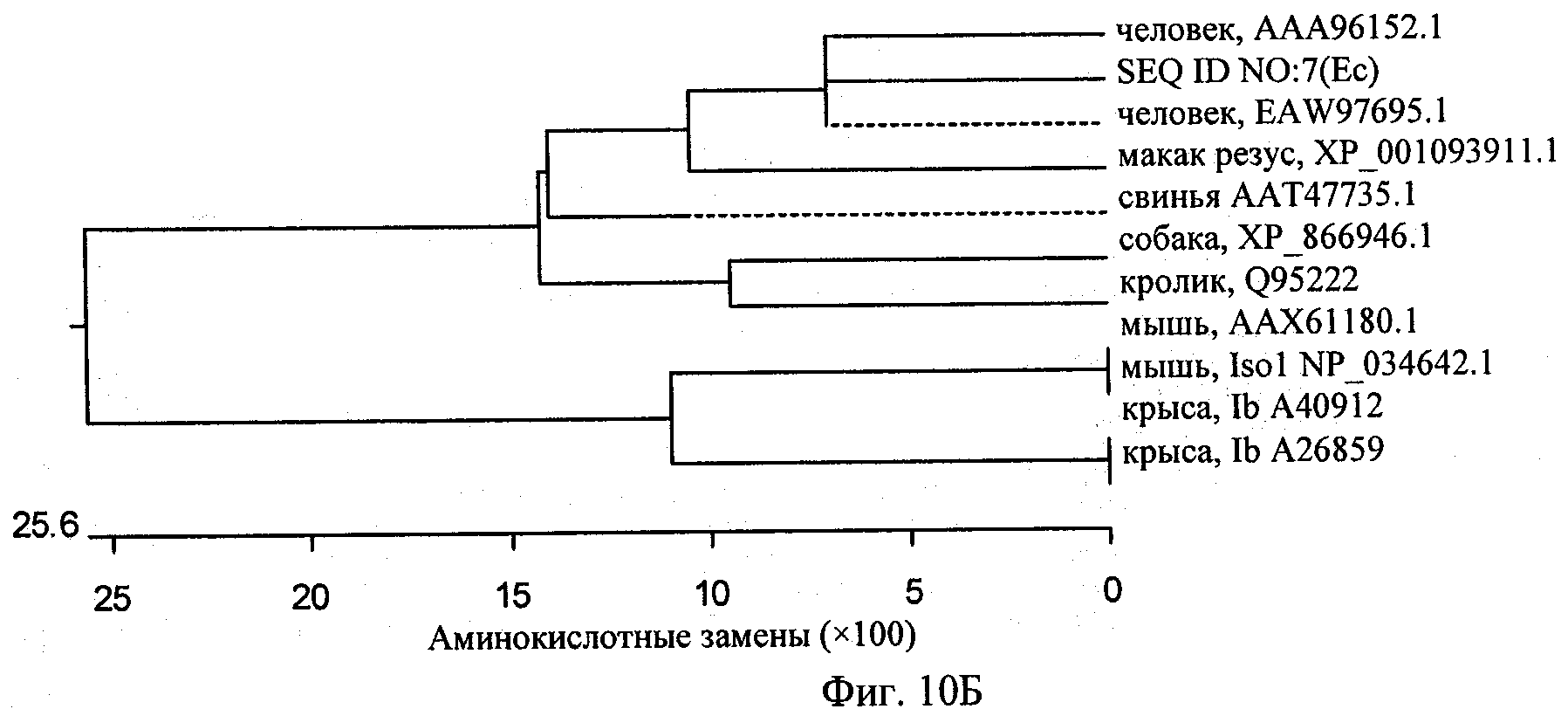
на фиг.10Б - график, демонстрирующий филогению проанализированных аминокислотных последовательностей относительно человеческого Ес-пептида IGF-1 (SEQ ID NO:4);
на фиг.11А - сравнительный анализ последовательности человеческого IGF-2 (SEQ ID NO:7) и соответствующих последовательностей IGF-2 различных видов животных. Представлены все проанализированные виды животных и регистрационные номера в GenBank соответствующих им последовательностей. R68 является консервативным для всех проанализированных видов; D69 является консервативным для всех видов, кроме шимпанзе, в последовательности этого вида в этом положении находится остаток гистидина;
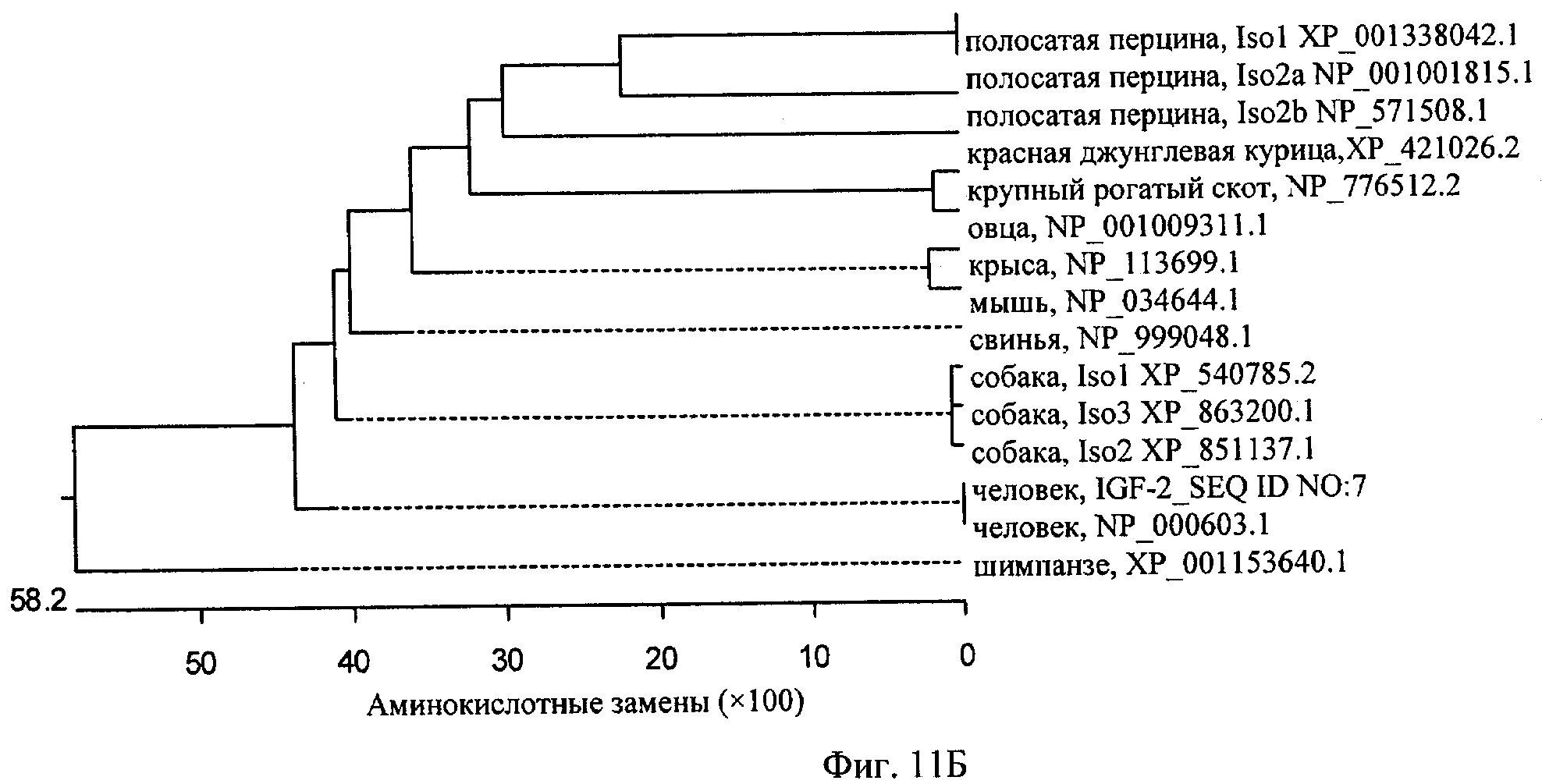
на фиг.11Б - график, демонстрирующий филогению проанализированных аминокислотных последовательностей относительно человеческого IGF-2 (SEQ IDNO:7);
на фиг.12А - сравнительный анализ последовательности человеческого Е-пептида IGF-2 (SEQ ID NO:6) и Е-пептидов IGF-2 различных видов животных. Представлены все проанализированные виды животных и регистрационные номера в GenBank соответствующих им последовательностей. R68 является консервативным для всех проанализированных видов; D69 является консервативным для всех видов, кроме шимпанзе, в последовательности этого вида в этом положении находится остаток гистидина;
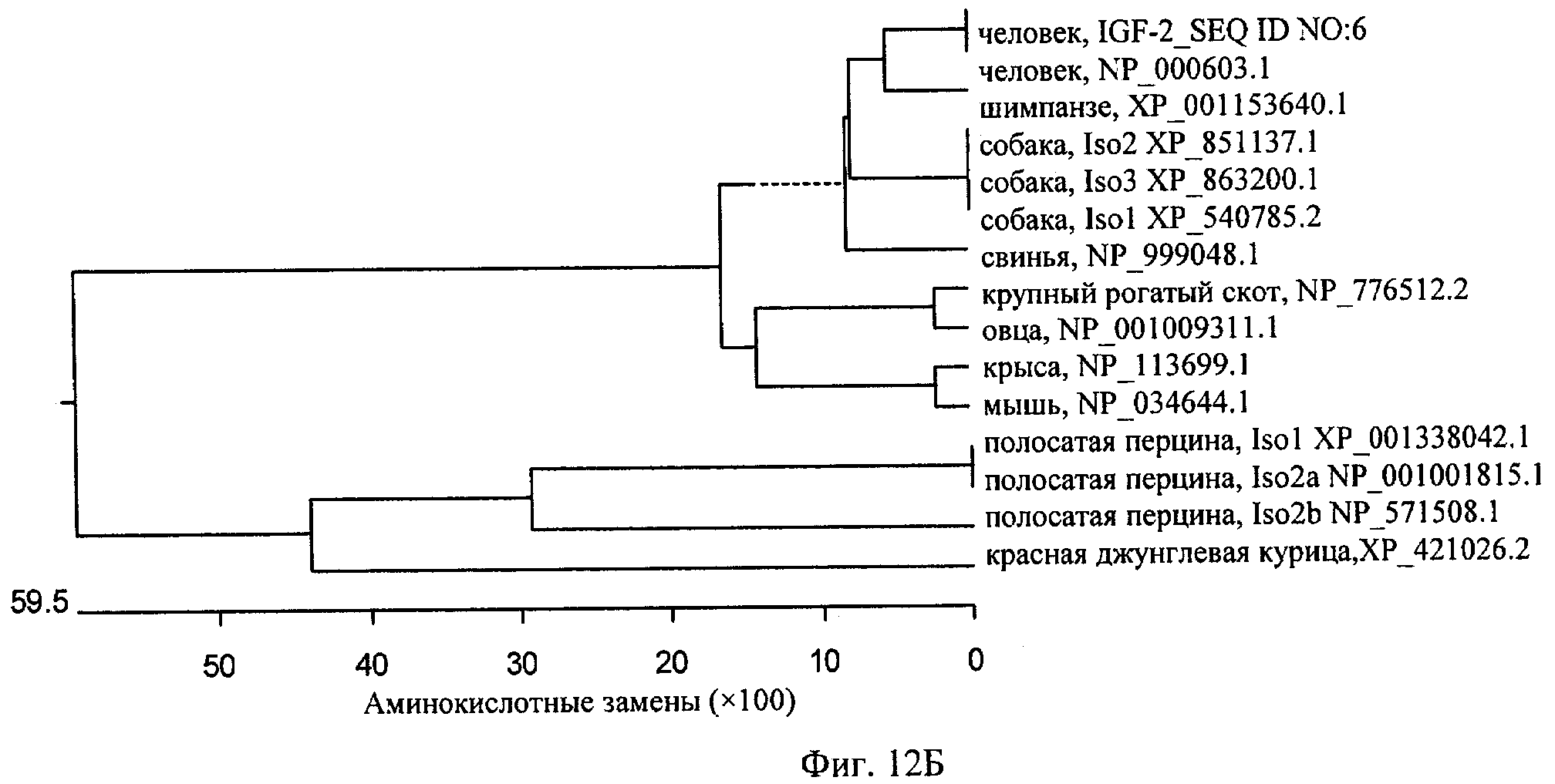
на фиг.12Б - график, демонстрирующий филогению проанализированных аминокислотных последовательностей относительно человеческого Е-пептида IGF-2 (SEQ ID NO:6).
Подробное описание изобретения
Настоящее изобретение относится к новым полипептидам-предшественникам IGF-1 и IGF-2, которые содержат практически соответствующий им Е-пептид, модифицированный для предупреждения, снижения или аннулирования типичного протеазного расщепления, ответственного за отделение активной формы IGF-1 или IGF-2 от ее Е-пептидов. Возможность применения полипептидов, предлагаемых в изобретении, основана на неожиданно установленном при создании изобретения факте, что такие полипептиды-предшественники обладают биологической активностью, стабильностью и благоприятным действием в качестве фармацевтических средств.
Скрининг полипептидов-предшественников IGF в отношении биологической активности
Возможность применения любого полипептида, предлагаемого в изобретении, можно оценивать с помощью следующих анализов.
Стабильность - Полипептид, предлагаемый в изобретении, должен обладать достаточной стабильностью в присутствии эндогенных протеаз, таких как протеазы, входящие в состав человеческой сыворотки, для того чтобы представлять собой эффективное лекарственное средство. Для оценки стабильности экспрессионным вектором, который кодирует полипептид, можно трансфектировать клетки линии Cos7 (ATCC) в среде DMEM, содержащей 10% фетальной телячьей сыворотки, 100 ед./мл пенициллина и 100 мкг/мл стрептомицина. Культуральную среду, содержащую секретируемые полипептиды, можно применять для дополнительных анализов, или в другом варианте экспрссионный вектор может кодировать легко доступные метки, такие как гекса-гистидиновую метку, вместе с полипептидом для облегчения эффективной очистки экспрессируемых полипептидов в культурах Cos7-клеток. Вне зависимости от пути получения образец полипептида инкубируют в сыворотке здорового человека (фирма Sigma) или в ЗФР в течение различных промежутков времени (например, 0, 1, 5, 10 и 16 ч), анализируют с помощью электрофореза в полиакриламидном геле, блоттируют на нитроцеллюлозу и соответствующие белки, визуализируют с помощью первичного антитела к IGF-1 или IGF-2 и вторичного антитела, например, конъюгированного с пероксидазой из хрена. Можно использовать любые многочисленные аналогичные методы блоттинга и обнаружения, в некоторых из которых используются флуоресцентные красители или даже радионуклиды. Интенсивность полосы, соответствующей предшественнику, по сравнению с интенсивностью полосы, соответствующей IGF-1 или IGF-2, должна свидетельствовать о степени расщепления предшественника в различных условиях. Полипептид, предлагаемый в изобретении, обработанный человеческой сывороткой в течение 16 ч при 37°С, может характеризоваться соотношением нерасщепленного предшественника и расщепленного зрелого IGF, составляющим примерно от 1:2 до 1:0,1, например примерно от 1:1 до 1:0,5, в частности соотношением примерно 1:1 или соотношением примерно 1:0,5. Как правило, предшественник должен присутствовать в соотношении, составляющем по меньшей мере 1:1.
Фосфорилирование АКТ - Полипептид, предлагаемый в изобретении, должен сохранять способность передавать сигнал через рецептор IGF-1 (сигналы и IGF-1, и IGF-2 передаются через рецептор IGF-1). Для определения указанной способности осуществлять передачу сигнала можно оценивать фосфорилирование находящейся по ходу передачи сигнала внутриклеточной мишени, т.е. АКТ, в ответ на связывание лиганда на поверхности клетки. Для анализа фосфорилирования АКТ биобласты линии С2С12 выращивают в условиях «голодания» в бессывороточной среде, а затем стимулируют различными лигандами. Клетки лизируют и осветляют центрифугированием. Фосфорилирование АКТ и уровни общей АКТ анализируют с помощью ELISA с использованием набора для двухвалентного (сэндвич) ELISA PathScan phospho АКТ (Ser473) и набора для двухвалентного ELISA PathScan АКТ (фирма Cell Signaling) соответственно.
Специфичность в отношении рецептора IGF-1 - Полипептид, предлагаемый в изобретении, предпочтительно сохраняет специфичность в отношении рецептора IGF-1 и должен связываться с родственным инсулиновым рецептором с низкой аффинностью. Для оценки специфичности в отношении рецептора образцы полипептида добавляют к выращенным в бессывороточной среде NIH3T3-клеткам, сверхэкспрессирующим рецептор IGF-1 или инсулиновый рецептор, и уровни фосфорилирования рецептора IGF-1 или фосфорилирования инсулинового рецептора определяют, лизируя клетки и подвергая лизаты анализу с помощью ELISA с использованием человеческого фосфорилированного IGF-1-рецептора и ELISA-набора для инсулинового рецептора (фирма R&D Systems).
Оценка гипертрофии in vivo на мышиных моделях - Для решения вопроса о том, может ли полипептид, предлагаемый в изобретении, повышать массу скелетных мышц в условиях, которые уже приводят к мышечной гипертрофии, можно подвергать обработанных и необработанных животных физической нагрузке и определять будет ли у обрабатываемых полипептидом животных образовываться больше мышечной массы по сравнению с необработанными животными.
Модели физической нагрузки
Одна из известных в данной области моделей основана на применении вращающегося колеса, движение которого определяется той нагрузкой, которую прикладывает к нему животное без дополнительного принуждения (см., например, Konhilas и др. Am J Physiol Heart Circ Physiol 289, 2005, с.455-465). Находящееся в клетке колесо, которое животное вращает без дополнительного принуждения, позволяет устранять инсульты, связанные с физическим и психологическим состоянием, которые характерны для моделей с принудительной нагрузкой, и поэтому является приемлемой моделью для оценки лекарственных средств-кандидатов, которые можно применять для относительно здоровых особей, для которых повышение мышечной массы является желательным.
Можно применять любую пригодную линию мышей. Например, можно произвольно разделять самцов мышей линии C57B1/6J на экспериментальную (например, получающую полипептид-предшественник IGF) и контрольную группы. Животных помещают по отдельности в клетку с колесом для физических упражнений; ведущих «малоподвижный образ жизни» контрольных животных помещают в идентичные клетки без колеса. Колесо для физических упражнений описано у Allen и др. J Appl Physiol 90, 2001. с.1900-1908. В целом, система состоит их колеса диаметром 11,5 см с поверхностью для пробега шириной 5,0 см (модель 6208, фирма Petsmart, Феникс, шт. Аризона), которая снабжена цифровым магнитным счетчиком (модель ВС 600, фирма Sigma Sport, Олни, шт. Иллинойс), который активируется при вращении колеса. Кроме того, каждое колесо снабжено обеспечивающим сопротивление механизмом, который позволяет регулировать нагрузку. Для этой цели присоединяют леску из нержавеющей стали к верхней части клетки и наматывают проволоку на неподвижный шкив, который закрепляют на находящемся в клетке колесе на оси вращения, так что это не влияет на прилагаемую к колесу нагрузку. Проволоку снова закрепляют в верхней части клетки с помощью пружины и винта. Такая конструкция позволяет осуществлять точную регулировку нагрузки на колесо, которая равномерно распределяется во время вращения колеса. Ежедневно регистрируют продолжительность физической нагрузки и расстояние, которое пробегает каждое животное, находящееся в условиях, позволяющих осуществлять физическую нагрузку, в течение всего периода выдерживания в указанных условиях. Все животные имели свободный доступ к воде и стандартному твердому корму для грызунов. Во всех группах пробег без дополнительного принуждения (нахождение в клетке с колесом) можно начинать с использованием мышей, возраст которых составляет в среднем примерно 12 недель. Каждая группа животных продолжала бегать в условиях различного сопротивления в зависимости от экспериментальной группы в течение 50 дней до достижения животными возраста примерно 19 недель. Нагрузку колеса определяли путем подвешивания на колесо грузов известной массы до тех пор, пока колесо слегка не смещалось. Все группы, находящиеся в условиях физической нагрузки, сначала в течение первой недели имели колесо в клетке без дополнительной нагрузки. Однако условия «без нагрузки» фактически представляли собой нагрузку в 2 г, которую определяли как нагрузку, необходимую для поддержания в колесе силы инерции и трения. Учитывая, что период акклиматизации к колесу составлял 1 неделю, нагрузку колеса можно было изменять с интервалами в одну неделю за исключением более высоких нагрузок, которые можно было изменять через 2 недели. Изменение нагрузок может составлять от 2 г вплоть до 12 г. Находящихся в условиях нагрузки и контрольных ведущих «малоподвижный образ жизни» животных умерщвляли под ингаляционным наркозом путем смещения шеи сразу после окончания конкретного периода нахождения в условиях нагрузки. Определяли вес тела и определенные мышцы быстро вырезали, промывали и замораживали для гистологического или биохимического анализа, которые осуществляли позднее.
Специалистам в данной области известны также альтернативные модели связанной с физической нагрузкой гипертрофии (см., например, модель физической нагрузки с использованием педального вращающегося устройства, которое описано у Lerman и др. J Appl Physiol 92, 2002, с.2245-2255).
Модель, созданная путем инъекции кленбутерола
Кленбутерол представляет собой β2-адренергический агонист, обладающий усиливающими рост свойствами, который, как установлено, вызывает увеличение мышечной массы. Точный механизм действия кленбутерола пока не известен, хотя предполагается снижение расщепления мышечных белков при его применении. В клинических условиях кленбутерол применяют в качестве противоастматического средства, но им, по-видимому, наиболее широко злоупотребляют в качестве структурообразующего агента (агента для бодибилдинга) для повышения мышечной массы как у людей, так и у шоу-животных.
Пяти мышам вводили ежедневно путем инъекции кленбутерол (3 мг/кг, подкожно (s.c.)) в течение 3, 7 или 14 дней для индукции мышечной гипертрофии. Мыши, которым инъецировали ЗФР, служили в качестве отрицательного контроля. Животных обследовали ежедневно (визуальный осмотр) в отношении любых побочных реакций (т.е. неопрятность шерстяного покрова, сонливость) на обработку. Обработка кленбутеролом потенциально может делать мышей более пугливыми или агрессивными, поэтому за мышами, если они помещены в клетки группами, необходимо особенно тщательно следить с позиций из драк друг с другом. Мыши могли свободно двигаться и могли нормально есть и пить. Мышей обследовали ежедневно до их умерщвления в день 3, 7 или 14 и отбирали ткани для дополнительного анализа.
Оценка на моделях мышечной атрофии in vivo - Способность полипептида-предшественника IGF, предлагаемого в изобретении, поддерживать мышечную массу в условиях, которые обычно приводят к снижению мышечной массы, можно оценивать на различных моделях атрофии скелетных мышц. При использовании примеров моделей, описанных ниже, специалист в данной области легко может создавать и осуществлять контролируемые эксперименты, включающие введение и применение полипептидов-предшественников IGF для решения вопроса о том, могут ли указанные полипептиды приводить к увеличению мышечной массы.
Например, самцов мышей линии С57 В16/2 покупали у фирмы The Jackson Laboratories. В начале каждого эксперимента мыши должны были иметь возраст примерно 9 недель. Как правило, мышей помещали в клетки-микроизоляторы с обычным кормом для грызунов. В начале каждого эксперимента мышей взвешивали. В конце каждого эксперимента мышей обычно умерщвляли ингаляционным наркозом с последующим смещением шеи и мышечные ткани собирали для дополнительной обработки. Мышей взвешивали для определения «конечного веса тела». Скелетные мышцы, которые можно получать, представляли собой переднюю большеберцовую мышцу, длинный разгибатель пальцев стопы, камбаловидную мышцу и икроножную мышцу. Произвольно собирали другие ткани, такие как сердце, печень, селезенка, почки, яички и головной мозг. Все мышцы и ткани полностью иссекали и взвешивали на весах, нижний предел которых составлял 0,0001 г. Затем ткани быстро замораживали в жидком азоте для последующей экстракции РНК и белков или быстро замораживали погружением в ОСТ (орто-хлортолуол) на корковом диске. Мышцы, замороженные на корковом диске для последующего получения криосрезов, погружали в изопентан, охлажденный с помощью жидкого азота до образования густой суспензии. Все образцы хранили при -80°С.
Обработка дексаметазоном
Фармакологический метод индукции мышечной кахексии у мышей предусматривает ежедневную внутрибрюшинную инъекцию дексаметазоном в дозе 20 мг/кг. Дексаметазон является синтетическим представителем класса глюкокортикоидных гормонов. Он обладает противовоспалительной и иммуносупрессорной активностью, превышающей по активности гидрокортизон примерно в 40 раз. Дексаметазон применяют для лечения воспаления и аутоиммунных состояний, например ревматоидного артрита. Его дают также страдающим раком пациентам, подвергающимся химиотерапии, для снижения некоторых побочных действий противоопухолевого лечения. Дексаметазон вызывает мышечную атрофию как у мышей, так и у людей.
Мышам инъецировали внутрибрюшинно (ip) дексаметазон в течение 3, 7 или 14 дней. В день окончания опыта животных умерщвляли с помощью CO2 и выделяли мышцы лап. Животных обследовали ежедневно (визуальный осмотр) в отношении любых побочных реакций (т.е. неопрятность шерстяного покрова, сонливость) на обработку. Мыши, как правило, были подвижными и могли нормально есть и пить. Для создания отрицательного контроля мышам инъецировали ЗФР.
Иммобилизация с помощью повязки
Физическое неупотребление различных групп мышц приводит к атрофии этих мышц. Доказано, что фиксация голеностопного сустава («закрепленная пятка» или наложение повязки) является очень эффективным и позволяющим получать воспроизводимые результаты средством индукции физической иммобилизации мускулатуры задних конечностей крыс и мышей.
Для иммобилизации мышей анестезировали изофлуораном. Голеностопный и коленный сустав фиксировали под углом 90° путем наложения повязки из легкого перевязочного материала (VET-LITE) вокруг суставов. Материал замачивали в теплой воде и затем оборачивали конечность, оставляя свободными суставы пальцев стопы и тазобедренный сустав. Суставы поддерживали в положении под углом 90° до высыхания перевязочного материала. Контралатеральные конечности служили в качестве контроля. Мышам давали отойти от наркоза и помещали в обычные клетки-микроизоляторы. Как установлено, перевязка не приводила к повышенному стрессу и животные свободно передвигались в клетке к корму и питью. Однако мышей ежедневно обследовали в отношении побочных действий, которые могут влиять на вес тела, активность и возбудимость.
После наложения на мышей повязки животных ежедневно обследовали для получения гарантий того, что повязка сохраняется на месте, поскольку мыши могут ее изжевывать. Животные могли двигаться, пить и есть после отхода от наркоза, и они не нуждались в специальном ложе, клетках или другой помощи.
Денервация
Как правило, мышей для осуществления денервации анестезировали с помощью газа изофлуорана. С помощью асептических хирургических процедур (три промывки бетадином и конечная промывка этанолом) обнажали правый седалищный нерв в середине бедра и вырезали кусок размером 2-5 мм. Контралатеральная конечность служила в качестве контроля.
Более конкретно, разрез на коже закрывали с помощью кожного зажима и животным инъецировали одну дозу бупренорфина перед тем, как дать им отойти от наркоза. Через 3, 7 или 14 дней после операции животных умерщвляли ингаляционным наркозом с последующим смещением шеи и мышцы (комплекс икроножных мышц, переднюю большеберцовую мышцу, длинный разгибатель пальцев стопы, камбаловидную мышцу) выделяли для гистологических и биохимических анализов.
Поскольку седалищный нерв был рассечен, то соответствующая иннервируемая им конечность становилась неподвижной, индуцируя атрофию скелетных мышц. Несмотря на это, животные могли двигаться, пить и есть после отхода от наркоза, и они не нуждались в специальном ложе, клетках или другой помощи.
Тем не менее, животных обследовали сразу после операции и их отхода от наркоза (1-2 ч). Кроме того, области разреза и общее состояние здоровья животных оценивали в течение 3 дней после операции. Кожный зажим удаляли через 7-10 дней после операции.
Генетические модели
В качестве моделей мышечной атрофии можно использовать также генетически измененных трансгенных мышей. Например, так называемые мини-мыши (Mini Mice) (фирма The Jackson Laboratory, линия №003258) содержат выключающую мутацию («knock out»-мутацию) в гене IGF-1, которая приводит к аномально пониженному постнатальному росту, а также низкому весу тела и росту. Дополнительную информацию можно почерпнуть у Powetl-Braxton и др. Genes Dev 7, 1993, сс.2609-2617. Кроме того, так называемые миди-мыши (Midi Mice) (фирма The Jackson Laboratory, линия №003259) содержат другую мутацию в гене, которая приводит к получению гипоморфного гена, обусловливающего низкий вес взрослых особей и другие сердечно-сосудистые фенотипы. Дополнительную информацию можно почерпнуть у Lembo и др. J Clin Invest 98, 1996, с.2648-2655.
Имеющие решающее значение и необязательные мутации или модификации предшественников IGF
Имеющие решающее значение мутации - Настоящее изобретение основано, в частности, на полученных данных о том, что полипептид-предшественник IGF, который содержит практически соответствующий ему Е-пептид, сохраняет биологическую активность и стабильность в присутствии сыворотки. Для гарантии того, что Е-пептид не отщепляется эндогенными протеазами, мишенью которых является двухосновный протеазный сайт, обычно любую из двух N-концевых двухосновных аминокислот Е-пептида в предшественнике удаляют путем делеции, изменяют путем мутации или маскируют иным образом. В случае MGF-1 эти две аминокислоты представляют собой R71 и S72, а в случае MGF-2 эти первые две аминокислоты представляют собой R68 и D69.
Указанное расщепление могут предупреждать различные модификации:
(1) делеция одного или обоих двухосновных остатков,
(2) мутация одного или обоих двухосновных остатков, приводящая к замене на неосновную аминокислоту, такую как аланин,
(3) инсерция одного или двух неосновных аминокислот между двухосновными остатками,
(4) встраивание сайта гликозилирования около двухосновных остатков, что является достаточным для маскировки протеазного сайта,
(5) сайтнаправленное пэгилирование с применением замены любого из двухосновных остатков или встраивания вблизи или между двухосновными остатками с использованием не встречающейся в естественных условиях аминокислоты, как будет описано ниже.
Кроме того, остатки К68 и К65, вероятно, играют роль в расщеплении IGF-1/Е-пептида; таким образом, мутации или делеции указанных остатков можно применять в сочетании с любой указанной выше тактикой, применяемой в отношении двухосновных аминокислот.
Мутации на N-конце зрелого IGF - В некоторых вариантах осуществления изобретения полипептиды-предшественники IGF имеют делеции или мутации нескольких первых N-концевых аминокислот. В случае IGF-1 любые первые три N-концевые аминокислоты можно изымать путем делеции или подвергать мутации, в то время как в случае IGF-2 любые первые шесть N-концевых аминокислот можно изымать путем делеции или подвергать мутации. Было установлено, что определенные N-концевые аминокислоты отщепляются в естественных условиях in vivo, и интродукция указанных мутаций или делеции минимизирует in vivo ассоциации полипептидов, предлагаемых в изобретении, с IGF-связывающими белками (IGFBP). Взаимодействие IGF-1 и IGF-2 с рецептором IGF-1 регулируется IGFBP-белками. Установлено, что все шесть IGFB ингибируют действие IGF (прежде всего IGFBP5), но в некоторых случаях обнаружено стимулирующее действие. По меньшей мере 99% IGF в кровотоке в норме связано с IGFBP. IGFBP, имеющий наиболее высокий уровень в кровотоке в посленатальный период, представляет собой IGFBP3, который может связываться с одинаковой аффинностью и с IGF-1, и с IGF-2. Встречающийся в естественных условиях укороченный IGF-1 (имеющий делецию G1, P2 и Е3) связывается с IGFBP3 в несколько раз с более низкой аффинностью по сравнению с встречающемся в естественных условиях IGF-1. Кроме того, G3 является важным для связывания с IGFBP, a G6 играет аналогичную роль в IGF-2-пептиде.
Таким образом, в случае предшественника hIGF-1 любой из остатков G1, P2 и Е3 можно изымать путем делеции или подвергать мутации либо индивидуально, либо в комбинации. Когда требуется мутация, то можно интродуцировать мутацию, приводящую к замене на аланин. В другом примере в случае предшественника hIGF-2 любой из остатков Р4, S5 и Е6 можно изымать путем делеции или подвергать мутации либо индивидуально, либо в комбинации. Когда требуется мутация, то можно интродуцировать мутацию, приводящую к замене на аланин.
Мутации на остатках 36 и 37 IGF-1 можно расщеплять с помощью сериновых протеаз, присутствующих в человеческой сыворотке. Мутация либо R36, либо R37, приводящая к замене на А, может предупреждать расщепление IGF-1 в этом предсказанном сайте расщепления, находящемся между R36 и R37. В случае hIGF-2 R38 можно подвергать мутации или изымать путем делеции для предупреждения этого оказывающего неблагоприятное воздействие расщепления.
Применение гликозилирования - Время полужизни in vivo полипептидов, предлагаемых в изобретении, можно повышать, добавляя N-связанные сайты гликозилирования либо в IGF, либо во фрагменты Е-пептида-предшественника при экспрессии в клетках млекопитающих или других эукариотических клетках, в которых может проходить N-связанное гликозилирование. Было установлено in vivo, что человеческий IGF-1-Ea является гликозилированным на N92 и N100, поскольку эти фрагменты Еа соответствуют консенсусной последовательности N-связанного сайта гликозилирования N-X-S/T, где Х может обозначать любую аминокислоту, а третья аминокислота триплета представляет собой либо S, либо Т. Известно также, что примыкающий к консенсусу аминокислотный контекст должен оказывать влияние на то, насколько сильно гликозилируется аспарагин. Таким образом, одной из стратегий интродукции сайта гликозилирования в Eb или Ее является встраивание аминокислот Еа вблизи консенсусной последовательности примерно в тот же участок Eb или Ее. Конкретное применение указанной стратегии проиллюстрировано ниже в примерах. В любом случае любую другую консенсусную последовательность N-связанного сайта гликозилирования, включая окружающие контекстные аминокислоты, которая известна специалистам в данной области, можно встраивать в полипептид-предшественник, предлагаемый в изобретении. Кроме того, можно осуществлять O-связанное гликозилирование полипептида, предлагаемого в изобретении, путем выбора конкретного хозяина, применяемого для получения полипептида. Например, применение определенных линий дрожжей для экспрессии IGF-1 приводит к добавлению олигосахаридов к остаткам серина или треонина (см., например, US 5273966).
Добавление поли(этиленгликоля) - Доказано, что конъюгация с поли(этиленгликолем) (ПЭГ; пэгилирование) оказывает благоприятное действие в отношении удлинения времени полужизни терапевтических лекарственных средств. Можно ожидать, что пэгилирование полипептидов-предшественников IGF, предлагаемых в изобретении, может обладать аналогичным преимуществом с позиций фармации. Методы пэгилирования IGF-1 хорошо известны в данной области (см., например, опубликованную заявку на патент США 2006/0154865, в которой описано благоприятное действие конъюгата лизин-монопэгилированный IGF-1). Такое лизин-монопэгилирование можно адаптировать для полипептидов-предшественников IGF, предлагаемых в изобретении. Кроме того, пэгилирование можно осуществлять в любой части полипептида, предлагаемого в изобретении, путем интродукции не встречающихся в естественных условиях аминокислот. Некоторые не встречающиеся в естественных условиях аминокислоты можно интродуцировать с помощью технологии, описанной у Deiters и др. J Am Chem Soc 125, 2003, с.11782-11783; Wang и Schultz, Science 301, 2003, с.964-967; Wang и др. Science 292, 2001, с.498-500; Zhang и др. Science 303, 2004, с.371-373 или в US 7083970. В целом, для некоторых из указанных систем экспрессии применяли сайтнаправленный мутагенез для интродукции нонсенс-кодона, такого как амбер-кодон TAG, в открытую рамку считывания, которая кодирует полипептид, предлагаемый в изобретении. Такие экспрессионные векторы затем интродуцируют в хозяина, который может использовать тРНК, специфическую для интродуцированного нонсенс-кодона, и «загружают» выбранной не встречающейся в естественных условиях аминокислотой. Конкретные не встречающиеся в естественных условиях аминокислоты, которые обладают благоприятным действием при их применении в качестве компонентов для конъюгации с полипептидами, предлагаемыми в изобретении, представляют собой аминокислоты с боковыми цепями, которые несут ацетиленовые группы и азидогруппы. Полипептиды-предшественники IGF, которые содержат эти новые аминокислоты, затем можно пэгилировать на указанных выбранный сайтах в белке. Кроме того, такие пэгилированные молекулы IGF, не содержащие Е-пептид, можно применять также в качестве терапевтических агентов.
Мультимеры Е-пептидов - В определенных фармакологических контекстах может требоваться увеличивать размер пептидного или белкового лекарственного средства для гарантии того, что лекарственное средство сохраняется на одной или другой стороне гематоэнцефалического барьера. Поскольку зрелые молекулы IGF представляют собой относительно короткие пептиды, даже в случае, когда в них сохраняется Е-пептид, может оказаться важным увеличивать размер полипептидов, предлагаемых в изобретении. Одним из путей достижения этого является создание мультимеров Е-пептидов на С-конце полипептида-предшественника IGF, что проиллюстрировано в некоторых описанных ниже примерах
С-концевая делеция Е-пептидов - Можно предположить, что наличие свободного цистеина в положении 81 Eb может приводить к гомодимеризации или другим действиям, которые могут приводить к снижению активности полипептидов, предлагаемых в изобретении, в качестве лекарственных средств. Так, делеция или мутация С81 в Eb может оптимизировать активность лекарственного средства. В конкретном варианте благоприятное действие оказывает делеция последних семи аминокислот Eb (т.е. аминокислот 81-87).
Другие мутации или модификации - Дополнительные мутации или модификации IGF, которым можно подвергать полипептиды-предшественники IGF, предлагаемые в изобретении, описаны в US 5077276 и в опубликованных заявках на патент США 2005/0287151, 2006/0211606 и 2006/0166328.
Под объем изобретения подпадают, помимо человеческих IGF-1 и IGF-2, все известные или пока неизвестные последовательности предшественников IGF-1 или IGF-2 животных, кроме человека, которые содержат практически соответствующий им Е-пептид, если имеющее место в естественных условиях отщепление Е-пептида аннулировано или снижено в результате модификаций, предлагаемых в настоящем изобретении.
Предпочтительный для применения тип IGF зависит от видов, подлежащих лечению.
Предпочтительно, чтобы IGF соответствовал виду, для лечения которого его применяют, например, когда лечению подлежат коровы, то предпочтительным типом IGF является бычий IGF.
Хотя, по-видимому, все формы IGF оказывают воздействие на различных индивидуумов благодаря высокой гомологии их последовательностей, в соответствующих видах можно избегать потенциальных нежелательных иммунологических осложнений, которые являются результатом индукции иммунного ответа на IGF из других видов.
Одним из вариантов осуществления изобретения являются модифицированные последовательности предшественников IGF-1 из животных, кроме человека.
Предпочтительными являются последовательности предшественников IGF-1 из позвоночных животных, которые содержат практически соответствующий им Е-пептид, в которых имеющее место в естественных условиях отщепление Е-пептида аннулировано или снижено в результате модификаций, предлагаемых в настоящем изобретении.
Примерами таких последовательностей являются (но, не ограничиваясь только ими) последовательности мышей, крыс, коров, свиней, лошадей, овец, коз, птиц, собак, кошек, рыб и т.п., полученные из любого источника, в том числе естественного, синтетического или рекомбинантного.
Другим вариантом осуществления изобретения являются модифицированные последовательности предшественников IGF-2 из животных, кроме человека.
Предпочтительными являются последовательности предшественников IGF-2 из позвоночных животных, которые содержат практически соответствующий им Е-пептид, в которых имеющее место в естественных условиях отщепление Е-пептида аннулировано или снижено в результате модификаций, предлагаемых в настоящем изобретении.
Примерами таких последовательностей являются (но не ограничиваясь только ими) последовательности мышей, крыс, коров, свиней, лошадей, овец, коз, птиц, собак, кошек, рыб и т.п., полученные из любого источника, в том числе естественного, синтетического или рекомбинантного.
Терапевтическое применение полипептидов-предшественников IGF
Показания - Изобретение относится также к применению полипептида-предшественника IGF, предлагаемого в изобретении, для приготовления лекарственного средства, предназначенного для лечения или предупреждения заболеваний костно-мышечной системы. Кроме того, изобретение относится также к применению полипептидов-предшественников IGF для повышения мышечной или костной массы у индивидуума вне зависимости от того, имеет или не имеет индивидуум риск развития заболевания костно-мышечной системы или имеет или не имеет заболевание костно-мышечной системы.
В частности, заболевание костно-мышечной системы может представлять собой мышечную атрофию. Известно много типов мышечной атрофии, в том числе являющейся результатом лечения глюкокортикоидами, такими как кортизол, дексаметазон, бетаметазон, преднизон, метилпреднизолон или преднизолон. Мышечная атрофия может являться результатом денервации, вызванной травмой нерва или дегенеративной, метаболической или воспалительной невропатии (например, синдром Гийена-Барре, периферическая невропатия или воздействие находящихся в окружающей среде токсинов или лекарственных средств). Кроме того, мышечная атрофия может быть результатом заболевания моторных нейронов у взрослых, детской атрофии спинных мышц, юношеской атрофии спинных мышц, аутоиммунной моторной невропатии с многоочаговой проводниковой блокадой, паралича, связанного с «ударом» или повреждением спинного мозга, скелетной иммобилизацией из-за травмы, пролонгированного пребывания на постельном режиме, добровольной пониженной активности, принудительной пониженной активности, метаболического стресса или недостаточности питательных веществ, рака, СПИДа, голодания, острого некроза скелетных мышц, заболевания щитовидной железы, диабета, доброкачественной врожденной гипотонии, заболевания центрального ядра, немалиновой (непрогрессирующей врожденной нитеобразной) миопатии, миопатии (центронуклеарной) мышечных трубочек, ожогового повреждения, хронического обструктивного заболевания легких, болезни печени, сепсиса, почечной недостаточности, застойной сердечной недостаточности или старения.
Заболевание костно-мышечной системы может быть связано с синдромом мышечной дистрофии, таким как симптом Дюшенна, симптом Беккера, миотония, плече-лопаточно-лицевая мышечная дистрофия, мышечная дистрофия Эмери-Дрейфуса, глазофарингеальная мышечная дистрофия, лопаточно-лицевая мышечная дистрофия, тазово-плечевая мышечная дистрофия, врожденная мышечная дистрофия или приобретенная дистальная миопатия. Заболевание костно-мышечной системы может представлять собой также остеопороз, перелом кости, низкий рост или карликовость.
Предполагается, что IGF-1 можно применять для лечения нечувствительного к инсулину диабета, поскольку IGF-1 может связываться также с гетеродимерами рецептора IGF-1 и инсулинового рецептора. Таким образом, полипептиды, предлагаемые в изобретении, можно применять для лечения диабета.
IGF-1 обладает нейротрофным действием и удлиняет продолжительность существования нейронов. Было высказано предположение о том, что IGF-1 можно применять для лечения случаев гибели моторных нейронов, что характерно для амиотрофического бокового склероза (ALS), атрофии головного мозга, старения и деменции. Таким образом, полипептиды, предлагаемые в изобретении, можно применять для лечения состояний, ассоциированных с гибелью нейронов, таких как ALS, атрофия головного мозга или деменция.
IGF-1 повышает популяции как лейкоцитов, так и эритроцитов и обладает аддитивным действием при введении в сочетании с эритропоэтином. Таким образом, полипептиды, предлагаемые в изобретении, можно применять для лечения анемии.
Поскольку IGF-1 и IGF-2 являются широко распространенными и основными регуляторами деления клеток и роста позвоночных животных, может оказаться целесообразным применять их в различных ветеринарных методах для экзогенного усиления или поддержания роста животных. Примерами такого применения являются (но не ограничиваясь только ими):
(I) увеличение скорости роста и/или размера животного, например ускорение увеличение мышечной ткани у свиней, крупного рогатого скота, домашней птицы и рыбы;
(II) повышение эффективности превращения корма в ткани организма (соотношение тощей массы и жировой массы), например, у свиней, крупного рогатого скота, овец, домашней птицы и рыбы; и
(III) увеличение производства молока у животных на стадии лактации, например молочного крупного рогатого скота, овец, коз.
Другие ветеринарные терапевтические применения включат (но не ограничиваясь только ими):
(IV) лечение животного, имеющего симптомы, связанные с кахексией, травмой или другими связанными с истощением заболеваниями, например животных-компаньонов, таких как собаки, кошки и лошади; и
(V) лечение находящихся на стадии лактации животных для улучшения здоровья новорожденных, например находящихся на стадии лактации свиноматок для улучшения характеристик новорожденных.
Методы введения - Полипептиды, предлагаемые в изобретении, можно вводить различными путями, включая применение носителей для введения генов. Для введения в терапевтических целях полипептида, предлагаемого в изобретении, можно применять методы, известные в данной области для терапевтического введения таких агентов, как белки или нуклеиновые кислоты, например такие методы, как трансфекция клеток, генная терапия, непосредственное введение в помощью наполнителя, применяемого для введения, или фармацевтически приемлемого носителя, непрямое введение с помощью рекомбинантных клеток, которые содержат нуклеиновую кислоту, кодирующую полипептид.
В данной области известны различные системы введения и их можно применять для введения полипептида, предлагаемого в изобретении, такие, например, как капсулирование в липосомы, микрочастицы, микрокапсулы, рекомбинантные клетки, обладающие способностью экспрессировать белок, опосредуемый рецептором эндоцитоз (см., например, Wu и Wu, J Biol Chem 262, 1987, с.4429-4432), конструирование нуклеиновых кислот в качестве части векторов на основе ретровирусов, аденоассоциированных вирусов, аденовирусов, поксивирусов (например, птичьего поксивируса, прежде всего поксивируса домашней птицы) или других векторов и т.д. Методы интродукции могут быть энтеральные или парентеральные и представляют собой (но не ограничиваясь только ими) внутрикожный, внутримышечный, внутрибрюшинный, внутривенный, подкожный, легочный, интраназальный, внутриглазной, эпидуральный и оральный пути. Полипептиды можно вводить с помощью любого удобного пути, например путем инфузии или болюсной инъекции, путем абсорбции через эпителиальную или слизисто-кожную выстилку (например, слизистую оболочку рта, ректальную или кишечную слизистую оболочку и т.д.) и можно вводить вместе с другими биологически активными агентами. Введение может быть системным или местным. Кроме того, может оказаться желательным интродуцировать фармацевтические композиции, предлагаемые в изобретении, в центральную нервную систему с помощью любого приемлемого пути, включая внутрижелудочковую и подоболочечную инъекцию; внутрижелудочковую инъекцию можно облегчать, используя внутрижелудочковый катетер, например, прикрепленный к резервуару, такому как резервуар Оммайя. Легочное введение можно осуществлять также с помощью, например, ингалятора или распылителя и в виде препаративной формы, содержащей пропеллент.
В конкретном варианте осуществления изобретения может требоваться местное введение фармацевтических композиций, предлагаемых в изобретении, в область, подлежащую лечению; для этой цели можно использовать (но не ограничиваясь только ими) местную инфузию в процессе хирургической операции, местное нанесение, например, путем инъекции, с помощью катетера или с помощью имплантата, имплантат можно изготавливать из пористого, непористого или желеобразного материала, включая мембраны, такие как сиаластические мембраны, волокна или поступающие в продажу заменители кожи.
В другом варианте осуществления изобретения действующее вещество можно вводить в пузырьке, прежде всего в липосоме (см. Langer, Science 249, 1990, с.1527-1533). Еще в одном варианте осуществления изобретения действующее вещество можно вводить с помощью системы с контролируемым высвобождением. В одном из вариантов осуществления изобретения можно использовать насос. В другом варианте осуществления изобретения можно использовать полимерные материалы (см. Howard и др. J Neurosurg 71, 1989, с.105). В другом варианте осуществления изобретения, в котором действующее вещество, предлагаемое в изобретении, представляет собой нуклеиновую кислоту, которая кодирует полипептид, предлагаемый в изобретении, нуклеиновую кислоту можно вводить in vivo для усиления экспрессии кодируемого ею белка, создавая ее в качестве части соответствующего нуклеотидного экспрессионного вектора и вводя его так, чтобы он становился внутриклеточным, например применяя ретровирусный вектор (см., например, US 4980286), или путем непосредственной инъекции, или путем применения бомбардировки микрочастицами (например, с помощью генной пушки; Biolistic, фирма Dupont), или нанося покрытие с использованием липидов, или с помощью находящихся на клеточной поверхности рецепторов, или с помощью трансфектирующих агентов, или путем введения в сочетании с гомеобокс-подобным пептидом, для которого известна способность проникать в ядро (см., например, Joliot и др. Proc. Natl. Acad. Sci. USA 88, 1991, c.1864-1868) и т.д. В другом варианте нуклеиновую кислоту можно интродуцировать внутрь клетки и включать в ДНК клетки-хозяина для экспрессии путем гомологичной рекомбинации.
Трансфекция клеток и генная терапия - Настоящее изобретение относится к применению нуклеиновых кислот, которые кодируют полипептиды, предлагаемые в изобретении, для трансфекции клеток in vitro и in vivo. Эти нуклеиновые кислоты можно встраивать в любой из хорошо известных векторов для трансфекции клеток- или организмов-мишеней. Нуклеиновыми кислотами также трансфектируют клетки ex vivo и in vivo посредством взаимодействия вектора и клетки-мишени. Композиции вводят (например, путем инъекции в мышцу) индивидууму в количестве, достаточном для того, чтобы вызвать терапевтический ответ.
Другим объектом изобретения является способ лечения области-мишени, т.е. клетки- или ткани-мишени, у человека или другого животного, заключающийся в том, что трансфектируют клетку нуклеиновой кислотой, которая кодирует полипептид, предлагаемый в изобретении, где нуклеиновая кислота включает индуцибельный промотор, функционально связанный с нуклеиновой кислотой, которая кодирует обеспечивающий направленный перенос слитый полипептид. Процедуры генной терапии, которые применяют для лечения или предупреждения болезней человека, см., например, у Van Brunt, Biotechnology 6, 1998, с.1149-1154.
Комбинированные терапии - Согласно нескольким вариантам осуществления изобретения полипептиды, предлагаемые в настоящем изобретении, можно вводить в сочетании с одним или несколькими дополнительными соединениями или видами терапии. Например, несколько полипептидов можно вводить в сочетании с одним или несколькими терапевтическими соединениями. Комбинированная терапия может предусматривать одновременное или чередующееся введение. Кроме того, комбинацию можно использовать для острого или постоянного применения. Полипептиды, предлагаемые в изобретении, можно вводить в сочетании с анаболическими агентами, такими как тестостерон или специфические модуляторы андрогенного рецептора (SARM). К другим анаболическим агентам относятся гормон роста (GH) или молекулы, которые индуцируют высвобождение GH. Грелин представляет собой особенно ценный агент для комбинированной терапии кахексии, поскольку грелин может вызывать усиление аппетита. Аналогично этому полипептиды, предлагаемые в изобретении, можно объединять с белковыми добавками для усиления анаболизма или объединять с физиотерапией для повышения веса тела. Любая молекула, которая ингибирует миостатин, также является кандидатом для комбинированной терапии.
Фармацевтические композиции - Настоящее изобретение относится также к фармацевтическим композициям, которые содержат белок-предшественник IGF, предлагаемый в изобретении, и фармацевтически приемлемый носитель. Под понятием «фармацевтически приемлемый» подразумевают разрешенный регулирующим органом федерального или государственного управления или включенный в список Фармакопеи США или другой общепринятой фармакопеи как разрешенный для применения на животных или человеке. Понятие «носитель» относится к разбавителю, адъюванту, эксципиенту или наполнителю, с которым осуществляют введение терапевтического средства. Указанные фармацевтически приемлемые носители могут представлять собой стерильные жидкости, такие как вода и масла, включая вазелин, масла животного, растительного происхождения или синтетические масла, такие как арахисовое масло, соевое масло, минеральное масло, кунжутное масло и т.п. Приемлемыми фармацевтическими эксципиентами являются крахмал, глюкоза, лактоза, сахароза, желатин, солод, рис, мука, мел, силикагель, стеарат натрия, моностеарат глицерина, тальк, хлорид натрия, обезжиренное сухое молоко, глицерин, пропиленгликоль, вода, этанол и т.п. При необходимости композиция может содержать также минорные количества смачивающих или эмульгирующих агентов или рН-забуферивающих агентов. Такие композиции могут иметь форму растворов, суспензий, эмульсии, таблеток, пилюль, капсул, порошков, форм с пролонгированным высвобождением и т.п. Композицию можно приготавливать в форме суппозитория с использованием традиционных связующих веществ и носителей, таких как триглицериды. В состав формы для орального применения могут входить стандартные носители, такие как имеющие фармацевтическую чистоту маннит, лактоза, крахмал, стеарат магния, сахарин натрия, целлюлоза, карбонат магния и т.д. Примеры приемлемых фармацевтических носителей приведены в «Remington's Pharmaceutical Sciences» под ред. Е.W.Martin.
Согласно некоторым вариантам осуществления изобретения композицию приготавливают с помощью общепринятых процедур в виде фармацевтической композиции, адаптированной для внутривенного введения человеку. При необходимости в состав композиции можно включать солюбилизатор и местный анестетик, такой как лидокаин, для ослабления боли в месте инъекции. Если композиция подлежит введению путем инфузии, ее можно приготавливать и выпускать вместе с флаконом для инфузии, содержащим стерильные имеющие фармацевтическую чистоту воду или физиологический раствор. Когда композицию вводят путем инъекции, то можно поставлять ампулу со стерильной водой для инъекций или физиологическим раствором так, чтобы ингредиенты можно было смешивать перед введением.
Полипептиды, предлагаемые в изобретении, можно включать в препаративную форму в нейтральном виде или в виде соли. Фармацевтически приемлемые соли представляют собой соли, образованные со свободными аминогруппами, являющиеся производными соляной, фосфорной, уксусной, щавелевой, винной кислот и т.д., и соли, образованные со свободными карбоксильными группами, являющиеся производными натрия, калия, аммония, кальция, гидроксидов железа, изопропиламина, триэтиламина, 2-этиламиноэтанола, гистидина, прокаина и т.д.
Количество полипептида, предлагаемого в изобретении, которое должно обладать эффективностью при лечении состояния или заболевания, можно определять стандартными клиническими методиками на основе предписания лечащего врача. Кроме того, необязательно можно проводить анализы in vitro, которые способствуют определению оптимальных диапазонов доз. Точная доза, которую следует вводить в препаративную форму, зависит также от пути введения и серьезности состояния и должна выбираться согласно решению лечащего врача и в зависимости от индивидуального состояния индивидуума. Однако приемлемые диапазоны доз для внутривенного введения составляют, как правило, примерно 20-5000 мкг действующего вещества на кг веса тела. Приемлемые диапазоны доз для интраназального введения составляют, как правило, примерно от 0,01 пг/кг веса тела до 1 мг/кг веса тела. Эффективные дозы можно определять путем экстраполяции из кривых зависимости ответа от дозы, полученных in vitro или с использованием для оценки смоделированных на животных систем. В частности, возможная схема приема лекарственного средства может составлять от 60 до 120 мкг/кг веса тела путем подкожной инъекции дважды в день.
Применение в ветеринарии
Помимо вышеуказанных методов введения людям, можно рассматривать также применение в ветеринарии.
Дозы, которые вводят здоровому животному и страдающему заболеванием животному, могут отличаться. Выбор соответствующей дозы легко могут осуществлять специалисты в данной области на основе анализов, известных в данной области, например на основе описанного ниже анализа пролиферации миобластов (пример 79) или анализа эпителиальной ткани молочной железы (пример 80). Общие анализы для оценки IGF также хорошо известны в данной области, например анализы, описанные в примере 81.
Специалистам в данной области должно быть очевидно, что для некоторых видов животных может быть характерна сезонная фертильность, которая зависит от длины фотопериода. В любых вариантах ветеринарного метода или его применения необязательно можно начинать лечение в конкретный момент репродуктивного цикла животного для того, чтобы достигать требуемого действия. Специалистам в данной области должно быть очевидно, что репродуктивный статус и цикл легко определять и при необходимости синхронизировать с помощью соответствующего режима.
При применении при ветеринарных показаниях, помимо ранее описанных методов, применяемых на людях, пептид IGF-1 или IGF-2, предлагаемый в настоящем изобретении, можно использовать путем вливания в ротовую полость животного или в виде добавки к оральным или твердым кормам для животных.
Ниже изобретение описано дополнительно с помощью примеров, не ограничивающих его объем.
Примеры
Пример 1
Конструировали экспрессионный ДНК-вектор, который кодирует полипептид-предшественник hIGF-1-Ea, содержащий следующие модификации: делеция G1, делеция Р2 и делеция ЕЗ; мутация, приводящая к замене R37 на А; и делеция R71 и делеция S72. Указанные мутации иногда обозначают как «3mut» в настоящем описании. В результате получали следующую секретируемую белковую последовательность: tlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemyeaplkpaksavraqrhtdmpktq kevhiknasrgsagnknyrm (SEQ ID NO:8)
Клетки линии Cos7 (полученные из АТСС) поддерживали в среде DMEM, содержащей 10% фетальной бычьей сыворотки, 100 ед./мл пенициллина и 100 мкг/мл стрептомицина, и высевали с плотностью 1×106 клеток на 10-сантиметровый планшет. Эти клеточные культуры трансфектировали 8 мкг экспрессионной плазмиды с помощью Fugene (фирма Roche) согласно инструкциям производителя. Через 24 ч после трансфекции клетки однократно промывали и культивировали в бессывороточной среде в течение 48 ч. Супернатанты собирали и хранили при -80°С.
Для оценки стабильности полипептида в человеческой сыворотке супернатанты, собранные после культивирования клеток линии Cos7, трансфектированных hIGF-1Ea дикого типа (wt) и hIGF-1Ea3mut, инкубировали в течение 16 ч при 37°С либо в присутствии 10% человеческой сыворотки (фирма Sigma), либо без нее. Образцы анализировали с помощью 18% ДСН-ПААГ и осуществляли иммуноблоттинг, используя козье поликлональное антитело к человеческому IGF-1. Результаты, представленные на фиг.1, свидетельствуют о том, что hIGF-1Ea wt в значительной степени расщеплялся после инкубации с сывороткой в течение 16 ч, a hIGF-1Ea3mut оказался стабильным. Денситометрический анализ показал, что отношение нерасщепленного к расщепленному IGF-1 составляло примерно 1:6,2, а в случае hIGF-1Ea3mut указанное отношение составляло примерно 1:0,68, что свидетельствует о том, что указанные мутации привели к получению стабилизированного полипептида.
Для подтверждения того, что hIGF-1Ea3mut обладал способностью передавать сигнал через IGF-1R, оценивали фосфорилирование АКТ в клетках при контакте с полипептидом. Клетки линии С2С12 получали из АТСС и поддерживали в модифицированной по методу Дульбекко среде Игла (DMEM) с высоким содержанием глюкозы (фирма Invitrogen), содержащей 10% фетальной бычьей сыворотки (фирма AMIMED), 100 ед./мл пенициллина(фирма Invitrogen), 100 мкг/мл стрептомицина (фирма Invitrogen) и 2 мМ глутамина (фирма Invitrogen). Для анализа фосфорилирования АКТ клетки линии С2С12 высевали с плотностью 0,15×106 клеток на лунку 6-луночного планшета и культивировали в среде для роста в течение 72 ч. Клетки выдерживали в течение 4 ч в условиях «голодания» в бессывороточной среде и затем стимулировали различными лигандами при 37°С в течение 30 мин. Клетки лизировали с помощью буфера PhosphoSafe (фирма Cell Signaling), содержащего различные ингибиторы протеаз, и осветляли центрифугированием при 14000×g в течение 15 мин при 4°С. Фосфорилирование АКТ и общие уровни АКТ анализировали с помощью ELISA с использованием набора для двухвалентного ELISA PathScan phospho АКТ (Ser473) и набора для двухвалентного ELISA PathScan АКТ (фирма Cell Signaling) соответственно. Данные о фосфорилировании АКТ обобщены на фиг.2А, из которой видно, что hIGF-1Ea3mut обладал способностью активировать клеточный путь IGF-1R аналогично применяемому в качестве положительного контроля реагента long-R3-IGF-1 и рекомбинантному IGF-1. Кроме того, данные, представленные на фиг.5, убедительно свидетельствуют о том, что hIGF-1Ea3mut приводит к фосфорилированию АКТ.
Далее для гарантии того, что рецепторная специфичность hIGF-1Ea3mut в отношении IGF-1R сохранялась, добавляли различные лиганды в культуры NIH3T3-клеток, сверхэкпрессирующих либо IGF-1R, либо инсулиновый рецептор (InsR). Эти клетки культивировали в таких же условиях, что и описанные выше для Со87-клеток. Для анализа фосфорилирования IGF-1R и InsR клетки линий NIH3T3-IGF1R и NIH3T3-InsR высевали с плотностью 0,2×106 клеток на лунку 6-луночного планшета и культивировали в среде для роста в течение 24 ч. Клетки выдерживали в течение 16 ч в условиях «голодания» в бессывороточной среде и затем стимулировали различными лигандами при 37°С в течение 10 мин. Клетки лизировали согласно процедуре, описанной в эксперименте с использованием АКТ, и уровни фосфорилирования IGF-1R и InsR анализировали с помощью ELISA, используя набор DuoSet 1C human phosphor-IGFIR и -InsR ELISA (фирма R&D Systems). Результаты, которые обобщены на фиг.3А и 3Б, свидетельствуют о том, что указанный полипептид-предшественник IGF-1 сохраняет специфичность в отношении рецептора IGF-1 и может связываться с родственным инсулиновым рецептором с более низкой аффинностью.
Пример 2
Конструировали экспрессионный ДНК- вектор, который кодирует полипептид-предшественник hIGF-1-Eb, содержащий следующие мутации: делеция G1, делеция Р2 и делеция ЕЗ; мутация, приводящая к замене R37 на А; и делеция R71 и делеция S72 (т.е. «3mut»). В результате получали следующую секретируемую белковую последовательность: tlcgaelvdalqfvcgdrgfyfnkptgygsssarapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:9)
Полипептид анализировали с помощью процедур, описанных выше в примере 1. Данные, представленные на фиг.1Б и полученные с помощью денситометрии, демонстрируют, что отношение нерасщепленного к расщепленному IGF-1 составляло примерно 1:9, в то время как в случае hIGF-1Eb3mut указанное отношение составляло примерно 1:1, что свидетельствует о том, что указанные модификации приводили к получению стабилизированного полипептида. Данные, представленные на фиг.2Б, свидетельствуют о том, что hIGF-1Eb3mut обладал способностью активировать клеточный путь IGF-1R аналогично применяемому в качестве положительного контроля реагенту long-R3-IGF-1 и рекомбинантному IGF-1. Кроме того, данные, представленные на фиг.5, убедительно свидетельствуют о том, что hIGF-1Eb3mut приводил к фосфорилированию АКТ. Результаты, обобщенные на фиг.3В и 3Г, свидетельствуют, что указанный полипептид-предшественник IGF-1 сохраняет специфичность в отношении рецептора IGF-1 и может связываться с родственным инсулиновым рецептором с более низкой аффинностью.
Пример 3
Конструировали экспрессионный ДНК-вектор, который кодирует полипептид-предшественник hIGF-1-Ec, содержащий следующие мутации: делеция G1, делеция Р2 и делеция Е3; мутация, приводящая к замене R37 на А; и делеция R71 и делеция S72 (т.е. «3mut»). В результате получали следующую секретируемую белковую последовательность: tlcgaelvdalqfvcgdrgfyfnkptgygsssrapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkyqppstnkntksqrrkgstfcerk (SEQ ID NO:10)
Полипептид анализировали с помощью процедур, описанных выше в примере 1. Данные, представленные на фиг.1В и полученные с помощью денситометрии, демонстрируют, что отношение нерасщепленного к расщепленному IGF-1 составляло примерно 1:5, в то время как в случае hIGF-1Ec3mut указанное отношение составляло примерно 1:0,96, что свидетельствует о том, что указанные модификации приводили к получению стабилизированного полипептида. Данные, представленные на фиг.2Г, свидетельствуют о том, что hIGF-1Ec3mut обладал способностью активировать клеточный путь IGF-1 R аналогично применяемому в качестве положительного контроля реагенту long-R3-IGF-1 и рекомбинантному IGF-1. Кроме того, данные, представленные на фиг.5, убедительно свидетельствуют о том, что hIGF-1Ec3mut приводил к фосфорилированию АКТ. Результаты, обобщенные на фиг.4А и 4Б, свидетельствуют о том, что указанный полипептид-предшественник IGF-1 сохраняет специфичность в отношении рецептора IGF-1 и может связываться с родственным инсулиновым рецептором с более низкой аффинностью.
Пример 4
Конструировали экспрессионный ДНК-вектор, который кодирует полипептид-предшественник hIGF-1-Eab, содержащий следующие мутации: делеция G1, делеция Р2 и делеция Е3; мутация, приводящая к замене R37 на А; и делеция R71 и делеция S72 (т.е. «3mut»); и вставку аминокислот Еа-пептида 93-102 между аминокислотами 95 и 96 Eb-пептида. Вставка создаст возможный N-связанный сигнал гликозилирования N92. В результате получали следующую секретируемую белковую последовательность: tlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkyqppstnknasrgsagnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:11)
Полипептид анализировали с помощью процедур, описанных выше в примере 1. Данные, представленные на фиг.2В, свидетельствуют о том, что hIGF-1Eab3mut обладал способностью активировать клеточный путь IGF-1R аналогично применяемому в качестве положительного контроля реагенту long-R3-IGF-1 и рекомбинантному IGF-1. Результаты, обобщенные на фиг.4В и 4Г, свидетельствуют о том, что указанный полипептид-предшественник IGF-1 сохраняет специфичность в отношении рецептора IGF-1 и не активирует инсулиновый рецептор.
Пример 5
Конструировали экспрессионный ДНК-вектор, который кодирует мультимерный полипептид-предшественник hIGF-1-Eb, содержащий следующие мутации: делеция G1, делеция Р2, делеция Е3, делеция R36, делеция R37, делеция R71, делеция S72, делеция последних семи С-концевых аминокислот Eb и вставка на С-конец указанного предшественника двух дополнительных Eb-пептидов, которые оба не имели R71 и S72 и последних семи С-концевых аминокислот, и четвертого и последнего Eb-пептида, который не имел R71 и S72. На фиг.6А представлено схематическое изображение указанной конструкции. В результате получали следующую секретируемую белковую последовательность: tlcgaelvdalqfvcgdrgfyfnkptgygsssapqtgivdeccfrscdlrrlemycaplkpaksavraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaersvraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsmaersvraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaersvraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:12)
Этот полипептид оценивали с помощью анализа фосфорилирования АКТ, который описан в примере 1. На фиг.5 показано, что указанный мультимер hIGF-1-Eb обладает способностью осуществлять передачу сигнала через IGF-1R-путь.
Пример 6
Можно экспрессировать полипептид-предшественник hIGF-1-Eb, предлагаемый в изобретении, который схематически изображен на фиг.6Б. Эта конструкция содержала следующие модификации: делеция G1, делеция Р2, делеция Е3, делеция R36, делеция R37, делеция R71, делеция S72 и инсерция аминокислот 93-102 Еа между аминокислотами 95 и 96 Eb, что позволяло создавать N-связанный сайт гликозилирования в положении N92 и N100. В результате получали следующую секретируемую белковую последовательность: tlcgaelvdalqfvcgdrgfyfnkptgygsssapqtgivdeccfrscdirrlcmycaplkpaksavraqrhtdmpktqkyqppstnknasrgsagnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:13)
Пример 7
Можно экспрессировать полипептид-предшественник hIGF-2-E, предлагаемый в изобретении, который содержал следующие модификации: делеция Р4, делеция S5 и делеция Е6; мутация, приводящая к замене R38 на А; и делеция R68 и делеция D69. В результате получали следующую секретируемую белковую последовательность: ayrtlcggelvdtlqfvcgdrgfyfsrpasrvsrasrgiveeccfrscdialletycatpaksevstpptvlpdnfprypvgkffqydtwkqstqrirrglpallrarrghvlakeleafreakrhrplialptqdpahggappemasnrk (SEQ ID NO:14)
Пример 8
Можно экспрессировать полипептид-предшественник hIGF-1-Ea, предлагаемый в изобретении, который содержал следующие мутации: делеция G1 и делеция Р2; мутация, приводящая к замене Е3 на X, где Х обозначает не встречающуюся в естественных условиях аминокислоту, которую пэгилируют; мутация, приводящая к замене R37 на А; и делеция R71 и делеция S72. В результате получали следующую секретируемую белковую последовательность: Xtlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkevhiknasrgsagnknyrm (SEQ ID NO:15)
Примеры 9-78 (Δ = стирание)
9) hIGF-1-Ea: ΔG1, ΔР2, ΔЕ3; R36A; ΔR71
tlcgaelvdalqfvcgdrgfyfnkptgygsssarapqtgivdeccfrscdirrlemycaplkpaksasvraqrhtdmpktqkevhiknasrgsagnknyrm (SEQ ID NO:16).
10) hIGF-1-Ea: ΔG1, ΔP2, ΔE3; R36A; ΔS72
tlcgaelvdalqfvcgdrgfyfhkptgygsssarapqtgivdeccfrscdirrlemycaplkpaksarvraqrhtdmpktqkevhiknasrgsagnknyrm (SEQ ID NO:17).
10) hIGF-1-Ea: ΔG1, ΔP2, ΔE3; R36A; ΔR71, ΔS72
tlcgaelvdalqfvcgdrgfyfhkptgygsssarapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkevhiknasrgsagnknyrm (SEQ ID NO:18).
11) hIGF-1-Ea: ΔG1, ΔP2, ΔE3; R37A; ΔR71
tlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdecc&scdlrrlemycaplkpaksasvraqrhtdmpktqkevhiknasrgsagnknyrm (SEQ ID NO:19).
12) hIGF-1-Ea: AG1, AP2, ΔE3; R37A; ΔS72
tlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdlrrlemycaplkpaksarvraqrhtdmpktqkevhiknasrgsagnknyrm (SEQ ID NO:20).
13) hIGF-1-Ea: ΔG1, ΔP2, ΔE3, ΔR37; ΔR71
tlcgaelvdalqfvcgdrgfyfnkptgygsssrapqtgivdeccfrscdirrlemycaplkpaksasvraqrhtdmpktqkevhiknasrgsagnknyrm (SEQ ID NO:21).
14) hIGF-1-Ea: ΔG1, ΔP2, ΔE3, ΔR37; ΔS72
tlcgaelvdalqfvcgdrgfyfnkptgygsssrapqtgivdeccfrscdirrlemycaplkpaksarvraqrhtdmpktqkevhiknasrgsagnknyrm (SEQ ID NO:22).
15) hIGF-1-Ea: ΔG1, ΔP2, ΔE3; ΔR37; ΔR71, ΔS72
tlcgaelvdalqfvcgdrgfyfnkptgygsssrapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkevhlknasrgsagnknyrm (SEQ ID NO:23).
16) hIGF-1-Eb: ΔG1, ΔP2, ΔE3; R36A; ΔR71
tlcgaelvdalqfvcgdrgfyfnkptgygsssarapqtgivdeccfrscdirrlemycaplkpaksasvraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk(SEQ ID NO:24).
17) hIGF-1-Eb: ΔG1, ΔP2, ΔE3; R36A; ΔS72
tlcgaelvdalqfvcgdrgfyfnkptgygsssarapqtgivdeccfrscdirrlemycaplkpaksarvraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:25).
18) hIGF-1-Eb: ΔG1, ΔP2, ΔE3; R37A; ΔR71
tlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdlrrlemycaplkpaksasvraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk(SEQ ID NO:26).
19) hIGF-1-Eb: ΔG1, ΔP2, ΔE3; R37A; ΔS72
tlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksarvraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:27).
20) hIGF-1-Eb: ΔG1, ΔP2, ΔE3; R37A; ΔR71, ΔS72
tlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrrcigsrnaecrgkkgk (SEQ ID NO:28).
21) hIGF-1-Eb: ΔG1, ΔP2, ΔE3, ΔR37; ΔR71
tlcgaelvdatqfvcgdrgfyfnkptgygsssrapqtgivdeccfrscdirrlemycaplkpaksasvraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:29).
22) hIGF-1-Eb: ΔG1, ΔP2, ΔE3, ΔR37; ΔS72
tlcgaelvdalqfvcgdrgiyfhkptgygsssrapqtgivdeccfrscdirrlemycaplkpaksarvraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegtcaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:30).
23) hIGF-1-Eb: ΔG1, ΔP2, ΔE3, ΔR37; ΔR71, ΔS72
tlcgaelvdalqfvcgdrgfyfhkptgygsssrapqtgivdecc&scdlrrlemycaplkpaksavraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggcqkegteaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:31).
24) hIGF-1-Ec: ΔG1, ΔP2, ΔE3; R36Δ; ΔR71
tlcgaelvdalqfvcgdrgfyfnkptgygsssarapqtgivdeccfrsedlrrlemycaplkpaksasvraqrhtdmpktqkyqppstnkntksqrrkgstfeerk (SEQ ID NO:32).
25) hIGF-1-Ec: ΔG1, ΔP2, ΔE3; R36Δ; ΔS72
tlcgaelvdalqfvcgdrgfyfhkptgygsssarapqtgivdeccfrscdirrlcmycaplkpaksarvraqrhtdmpktqkyqppstnkntksqrrkgstfeerk (SEQ ID NO:33).
26) hIGF-1-Ec: ΔG1, ΔP2, ΔE3; R36Δ; ΔR71, ΔS72
tlcgaelvdalqfvcgdrgfyfnkptgygsssarapqtgivdecc&scdlrrlemycaplkpaksavraqrhtdmpktqkyqppstnkntksqrrkgstfeerk (SEQ ID NO:34).
27) hIGF-1-Ec: ΔG1, ΔP2, ΔE2; R37Δ; ΔR71
tlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksasvraqrhtdmpktqkyqppstnkntksqrrkgstfeerk (SEQ ID NO:35).
28) hIGF-1-Ec: ΔG1, ΔP2, ΔE3; R37Δ; ΔS72
tlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksarvraqrhtdmpktqkyqppstnkntksqrrkgstfeerk (SEQ ID NO:36).
29) hIGF-1-Ec: ΔG1, ΔP2, ΔE3; R37Δ; ΔR71, ΔS72
tlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdecc&scdlrrlemycaplkpaksavraqrhtdmpktqkyqppstnkntksqrrkgstfeerk (SEQ ID NO:37).
30) hIGF-1-Ec: ΔG1, ΔP2, ΔE3, ΔR37, ΔR71
tlcgaelvdalqfvcgdrgfyfnkptgygsssrapqtgivdeccfrscdirrlemycaplkpaksasvraqrhtdmpktqkyqppstnkntksqrrkgstfeerk (SEQ ID NO:38).
31) hIGF-1-Ec: ΔG1, ΔP2, ΔE3, ΔR37, ΔS72
tlcgaelvdalqfvcgdrgfyfnkptgygsssrapqtgivdeccfrscdirrlemycaplkpaksarvraqrhtdmpktqkyqppstnkntksqrrkgstfeerk (SEQ ID NO:39).
32) hIGF-1-Eab: ΔG1, ΔP2, ΔE3; R36Δ; ΔR71; инсерция ак 93-102 Еа между ак 95 и 96 Eb (т.е. «Eab»).
tlcgaelvdalqfvcgdrgfyfnkptgygsssarapqtgivdeccfrscdirrlemycaplkpaksasvraqrhtdmpktqkyqppstnknasrgsagnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:40)
33) hIGF-1-Eab: ΔG1, ΔP2, ΔE3; R37Δ; ΔR71
tlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksasvraqrhtdmpktqkyqppstnknasrgsagnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:41).
34) hIGF-1-Eab: ΔG1, ΔP2, ΔE3, ΔR37, ΔR71
tlcgaelvdalqfvcgdrgfyfnkptgygsssrapqtgivdeccfrscdirrlemycaplkpaksasvraqrhtdmpktqkyqppstnknasrgsagnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:42).
35) hIGF-1-Eab: ΔG1, ΔP2, ΔE3; R36Δ; ΔS72
tlcgaelvdalqfvcgdrgfyfnkptgygsssarapqtgivdeccfrscdlrrlemycaplkpaksarvraqrhtdmpktqkyqppstnknasrgsagnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:43).
36) hIGF-1-Eab: ΔG1, ΔP2, ΔE3; R37Δ; ΔS72
tlcgaelvdalqfvcgdrgfyfhkptgygsssraapqtglvdeccfrscdirrlemycaplkpaksarvraqrhtdmpktqkyqppstnknasrgsagnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:44).
37) hIGF-1-Eab: ΔG1, ΔP2, ΔE3, ΔR37, ΔS72
tlcgaelvdalqfvcgdrgfyfnkptgygsssrapqtgivdeccfrscdirrlemycaplkpaksarvraqrhtdmpktqkyqppstnknasrgsagnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:45).
38) hIGF-1-Eab: ΔG1, ΔP2, ΔE3; R36Δ; ΔR71, ΔS72
ttcgaelvdalqfvcgdrgfyfnkptgygsssarapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkyqppstnknasrgsagnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:46).
39) hIGF-1-Eab: ΔG1, ΔP2, ΔE3, ΔR37, ΔR71, ΔS72
tlcgaelvdalqfvcgdrgfyfnkptgygsssrapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkyqppstnknasrgsagnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaccrgkkgk (SEQ ID NO:47).
40) hIGF-1-Ea: ΔP2, ΔE3; R37Δ; ΔR71, ΔS72
gtlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkevhlknasrgsagnknyrm (SEQ ID NO:48).
41) hIGF-1-Eb: ΔP2, ΔE3; R37Δ; ΔR71, ΔS72
gtlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:49).
42) Мультимер hIGF-1-Eb: (ΔG1, ΔP2, ΔE3; R37Δ) - 3×Eb (ΔR71, ΔS72, ΔC-конц. 7 ак) - Eb (ΔР71, ΔS72)
tlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdecc&scdlrrlemycaplkpaksavraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkcgteaslqirgkkkeqrreigsrnaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegtcaslqirgkkkeqrreigsrnaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:50)
43) Мультимер hIGF-1-Ebr: (ΔP2, ΔE3; R37Δ) - 3×Eb (ΔR71, ΔS72, АС-конц. 7 ак) - Eb (ΔR71, ΔS72)
gtlcgaclvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsmaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrrcigsrnaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteastqirgkkkeqrreigsrnaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:51).
44) hIGF-1-Ec: ΔP2, ЛЕЗ; R37Δ; ΔR71, ΔS72
gtlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkyqppstnkntksqrrkgstfeerk (SEQ ID NO:52).
45) hIGF-1-Ea: ΔE3; R37Δ; ΔR71, ΔS72
gptlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkevhlknasrgsagnknyrm (SEQ ID NO:53).
46) hIGF-1-Eb: ΔE3; R37Δ; ΔR71, ΔS72
gptlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk(SEQ ID NO:54).
47) Мультимер hIGF-1-Eb: (ΔG1, ΔP2, ΔE3; R37Δ) - 3×Eb (ΔR71, ΔS72, ΔC-конц. 7 ак) - Eb (ΔР71, ΔS72)
tlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsmaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:55).
48) Мультимер hIGF-1-Eb: (ΔE3; R37Δ) - 3×Eb (ΔR71, ΔS72, ΔС-конц.7 ак) - Eb (ΔR71, ΔS72)
gptlcgaelvdalqfvcgdrgfyfhkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsmaecrgkkgk (SEQ ID NO:56).
49) hIGF-1-Ec: ΔE3; R37Δ; ΔR71, ΔS72
gptlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgtvdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkyqppstnkntksqrrkgstfeerk (SEQ ID NO:57).
50) hIGF-1-Ea: ΔE3; R37Δ; ΔR71, ΔS72
gptlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkevhlknasrgsagnknyrm (SEQ ID NO:58).
51) hIGF-1-Eb: ΔE3; R37Δ; ΔR71, ΔS72
gptlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:59).
52) hIGF-1-Ec: ΔE3; R37A; ΔR71, ΔS72
gptlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkyqppstnkntksqrrkgstfeerk (SEQ ID NO:60).
53) hIGF-1-Eab: ΔЕ3; R37A; ΔR71, ΔS72 gptlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkyqppstnknasrgsagnkntksqrrkgwpkthpggeqkegteaslqirgkkkcqrreigsrnaecrgkkgk (SEQ ID NO:61).
54) Мультимер hIGF-1-Eb: (ΔE3; R37A) - 3×Eb (ΔR71, ΔS72, ΔС-конц. 7 ак) - Eb (ΔR71, ΔS72)
gptlcgaelvdalqfvcgdrgfyfhkptgygsssraapqtgivdeccfrscdirrtemycaplkpaksavraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteastqirgkkkeqrreigsrnaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsruaecrgkkgk (SEQ ID NO:62).
55) hIGF-1-Ea: E3Δ; R37A; ΔR71, ΔS72
gpatlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkevhlknasrgsagnknyrm (SEQ ID NO:63).
56) hIGF-1-Eb: E3Δ; R37A; ΔR71, ΔS72
gpatlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:64).
57) hIGF-1-Ec: E3Δ; R37A; ΔR71, ΔS72
gpatlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaptkpaksavraqrhtdmpktqkyqppstnkntksqrrkgstfeerk (SEQ ID NO:65).
58) hIGF-1-Eab: E3Δ; R37A; ΔR71, ΔS72
gpatlegaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdcccfrscdirrlemyeaplkpaksavraqrhtdmpktqkyqppstnknasrgsagnkntksqrrkgwpkthpggcqkegteaslqirgkkkeqrrcigsrnaecrgkkgk (SEQ ID NO:66).
59) Мультимер hIGF-1-Eb: (E3Δ; R37A) - 3×Eb (ΔR71, ΔS72, ΔС-конц. 7 ак) - Eb (ΔR71, ΔS72)
gpatlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:67).
60) hIGF-1-Ea: ΔP2, ΔЕ3; R37A; ΔR71, ΔS72
gtlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkevhlknasrgsagnknyrm (SEQ ID NO:68).
61) hIGF-1-Eb: ΔP2, ΔE3; R37A; ΔR71, ΔS72
gtlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdecc&scdlrrlemycaplkpaksavraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsmaecrgkkgk (SEQ ID NO:69).
62) hIGF-1-Ec: ΔP2, ΔE3; R37A; ΔR71, ΔS72
gtlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkyqppstnkntksqrrkgstfeerk (SEQ ID NO:181).
63) hIGF-1-Eab: ΔP2, ΔE3; R37A; ΔR71, ΔS72
gtlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkyqppstnknasrgsagnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsmaecrgkkgk (SEQ ID NO:70).
64) Мультимер hIGF-1-Eb: (ΔP2, ΔE3; R37A) - 3×Eb (ΔR71, ΔS72, АС-конц. 7 aK) - Eb (ΔR71, ΔS72)
gtlcgaelvdalqfvcgdrgfyRikptgygsssraapqtgivdeccfrscdIrrlemycaplkpaksavraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsmaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:71).
65) hIGF-1-Eb: ΔG1, ΔP2; E3X; R37A; ΔR71, ΔS72
Xtlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:72).
66) hIGF-1-Ec: ΔG1, ΔP2; E3X; R37A; ΔR71, ΔS72
Xtlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkyqppstnkntksqrrkgstfeerk (SEQ ID NO:73).
67) hIGF-1-Eab: ΔG1, ΔP2; E3X; R37A; ΔR71, ΔS72
Xtlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkyqppstnknasrgsagnkntksqrrkgwpkthpggeqkcgteaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:74).
68) Мультимер hIGF-1-Eb: (ΔG1, ΔP2; E3X; R37A) - 3×Eb (ΔR71, ΔS72, ΔC-конц. 7 ак) - Eb (ΔР71, ΔS72)
Xtlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:75).
69) hIGF-1-Ea: ΔG1, ΔP2, ΔE3; R37A; ΔR71; S72X
tlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdlrrlemycaplkpaksaXvraqrhtdmpktqkevhlknasrgsagnknyrm (SEQ ID NO:76).
70) hIGF-1-Eb: ΔG1, ΔP2, ΔE3; R37A; ΔR71; S72X
tlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdlrrlemycaplkpaksaXvraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:77).
71) hIGF-1-Ec: ΔG1, ΔP2, ΔE3; R37A; ΔR71; S72X
tlcgaclvdaIqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdIrrlemycaplkpaksaXvraqrhtdmpktqkyqppstnkntksqrrkgstfeerk (SEQ ID NO:78).
72) hIGF-1-Eab: ΔG1, ΔP2, ΔE3; R37A; ΔR71; S72X
tlcgaelvdalqfvcgdrgfyfhkptgygsssraapqtgivdeccfrsedlrrlemycaplkpaksaXvraqrhtdmpktqkyqppstnknasrgsagnkntksqrrkgwpkthpggeqkegtcaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:79).
73) Мультимер hIGF-1-Eb: (ΔG1, ΔP2, ΔE3; R37A) - Eb (ΔR71; S72X; ΔC-конц. 7 ак) - 2×Eb (ΔР71, ΔS72, АС-конц. 7 ак) - Eb (ΔР71, ΔS72)
tlcgaelvdatqfvcgdrgfyfnkptgygsssraapqtgivdcccfrscdlrrlemycaplkpakXsavraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkcgteaslqirgkkkeqrreigsrnaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaecrgkkgk (SEQ ID NO:80).
74) hIGF-1-Ea: ΔG1, ΔP2, ΔE3; R37A; ΔR71, ΔS72; N92X
tlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkevhlkXasrgsagnknyrm (SEQ ID NO:81).
75) hIGF-1-Eb: ΔG1, ΔP2, ΔE3; R37A; ΔR71, ΔS72; C142X
tlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsmaeXrgkkgk (SEQ ID NO:82).
76) hIGF-1-Eab: ΔG1, ΔP2, ΔE3; R37A; ΔR71, ΔS72; C151X
tlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkyqppstnknasrgsagnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsmaeXrgkkgk (SEQ ID NO:83).
78) Мультимер hIGF-1-Eb (ΔG1, ΔP2, ΔE3; R37A) - 3×Eb (ΔR71, ΔS72, ΔC-конц.7 ак) - Eb (ΔР71, ΔS72; C71X)
tlcgaelvdalqfvcgdrgfyfnkptgygsssraapqtgivdeccfrscdirrlemycaplkpaksavraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsmaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaevraqrhtdmpktqkyqppstnkntksqrrkgwpkthpggeqkegteaslqirgkkkeqrreigsrnaeXrgkkgk (SEQ ID NO:84)
Пример 79: Анализ пролиферации миобластов
Анализ пролиферации миобластов представляет собой достоверный индикаторный метод оценки in vitro активности IGF, его применяли в качестве модели для факторов, оказывающих влияние на эмбриональные миобласты и клетки-сателлиты взрослых особей. Факторы, обладающие активностью в этой системе, проявляют свое действие так же, как и в первичных культурах миобластов. Усиление пролиферации миобластов in vitro пептидом, предлагаемым в настоящем изобретении, свидетельствует об активности, повышающей пролиферацию миобластов и вследствие этого повышающей в конце концов количество миофибрилл в матке. Кроме того, аналогичное усиление пролиферации миобластов свидетельствует о том, что пептиды, предлагаемые в настоящем изобретении, можно применять для повышения мышечной гипертрофии у взрослых особей, например, путем стимуляции клеточной пролиферации в мышце-сателлите.
Пример 80: Анализ эпителиальной ткани молочной железы
У животного на стадии лактации количество эпителиальной ткани молочной железы является лимитирующим фактором производства молока, поскольку эта ткань содержит клетки, которые продуцируют и секретируют молоко. При использовании в системах in vitro эпителиальные клетки, полученные из молочных желез животных, можно стимулировать модифицированными IGF-1 или IGF-2, предлагаемыми в настоящем изобретении, в отношении пролиферации и производства повышенных количеств компонентов молока. Можно продемонстрировать также, что эпителиальные клетки молочных желез, пролиферация которых стимулирована в одной из таких систем in vitro, можно повторно имплантировать в очищенные скопления жировой ткани молочной железы и стимулировать пролиферацию и/или производство молока у животных на стадии лактации.
Пример 81: Оценка уровней IGF-1 или IGF-2 в крови или других жидкостях организма
Эффективное количество введенного парентерально пептида в дозе можно оценивать с помощью кривых зависимости доза-ответ. Например, уровни модифицированных пептидов IGF, предлагаемых в изобретении, можно определять в крови или в общей воде организма индивидуума, подлежащего лечению, с целью определения дозировки. В другом варианте можно вводить возрастающие количества пептида индивидууму и оценивать уровни модифицированного IGF-1 и IGF-2 в сыворотке индивидуума. Количество пептида, которое следует применять, можно рассчитывать в молях на основе данных об уровнях модифицированного IGF-1 или IGF-2 в сыворотке.
Один из методов определения соответствующей дозировки пептида предусматривает оценку пептида IGF, предлагаемого в изобретении, в биологической жидкости, такой как общая вода организма или плазма крови. Оценку указанных уровней можно осуществлять любыми методиками, включая РИА и ELISA. После определения уровней IGF жидкость приводят в контакт с одной или несколькими дозами пептида. После указанной стадии контакта в жидкости повторно оценивают уровни IGF. Если уровни IGF в жидкости находятся ниже количества, достаточного для достижения требуемой эффективности, с целью получения которой молекулу вводят, то дозу молекулы можно регулировать для достижения максимальной эффективности. Этот метод можно осуществлять in vitro или in vivo. Предпочтительно указанный метод осуществляют in vivo, т.е. после экстракции жидкости из организма индивидуума и оценки уровней IGF пептид вводят млекопитающему в виде одной или нескольких доз (это означает, что путем введения животному достигают стадии контакта) и затем уровни IGF повторно оценивают в экстрагированной жидкости, полученной из животного.
Другой метод определения дозировки предусматривает применение антител к пептиду или представляет собой другой метод определения в LIFA-формате.
Пример 82: Фармакокинетические характеристики hIGF-1-Ec 3mut in vivo
Взрослым самцам мышей (n=3/группу) вводили путем внутривенной (i.v.) болюсной инъекции rhIGF-1 в дозе 1 мг/кг и hIGF-l-Ec3mut (описанный в примере 3) в дозе 1,55 мг/кг. Брали серийные образцы крови через 5, 15, 30 и 60 мин после введения тестируемой субстанции. Концентрации в сыворотке rhIGF-1 и hIGF-1-Ec3mut определяли с помощью ELISA. Этот анализ является специфическим для hIGF-1.
Эквимолярные дозы rhIGF-1 и hIGF-1-Ec3mut вводили мышам i.v. Результаты свидетельствуют о существенно более высоких уровнях белка hIGF-l-Ec3mut по сравнению с rhIGF-1 во все изученные моменты времени, что демонстрирует, что hIGF-1-Ec3mut является более стабильным в отношении метаболизма, чем состоящий из 70 аминокислот IGF-1.
|