Результат интеллектуальной деятельности: АНТИМУТАГЕННОЕ СРЕДСТВО
Вид РИД
Изобретение
Изобретение относится к области использования средств растительного происхождения, к медицине и фармакологии, а именно - для снижения мутагенного эффекта антибластомного препарата. Предложено применение пентациклического тритерпеноида милиацина в качестве средства для снижения мутагенного эффекта антибластомного химиопрепарата-циклофосфана.
Технический результат. Предварительное введение милиацина обеспечивало 10-кратное снижение относительного содержания (%) метафазных пластинок с аберрациями и 16-кратное снижение количества аберраций (на 100 метафазных пластинок) в клетках костного мозга животных при внутрибрюшинном введении циклофосфана, а также трехкратное снижение относительного содержания аберрантных пластинок и 4,5-кратное снижение аберраций при его внутривенном введении. 5 ил.
Изобретение относится к области использования средств растительного происхождения, снижающих мутагенный эффект ксенобиотика - циклофосфана.
Настоящее изобретение относится к области лекарственных средств, в частности, к применению милиацина в качестве средства для снижения мутагенного эффекта циклофосфана.
Изобретение относится к медицине и может найти применение в качестве средства, снижающего мутагенный эффект циклофосфана, как проявления его побочного отрицательного действия на организм при использовании в клинической практике.
Актуальность проблемы антимутагенеза связана прежде всего с воздействием на организм неблагоприятных экологических факторов, вызывающих хромосомные повреждения и нарушения структуры ДНК, способствуя, тем самым, росту онкологических заболеваний населения (Гончарова Р.И., Кужир Т.Д., 2005; Домрачева Е.В. и соавт., 2012). Вместе с тем, эта проблема весьма значима и в клинической практике, связанной с использованием химиопрепаратов, мутагенный эффект которых является одним из распространенных и тяжелых осложнений в лечении онкологических больных (Репин М.В. и соавт., 2002; Иванова А.А., 2010). Данное обстоятельство служит серьезным препятствием к достижению должного лечебного эффекта, поскольку определяет необходимость увеличения интервалов между курсами терапии и снижения дозы препаратов, вплоть до их отмены. В связи с этим, разработка средств, предупреждающих и (или) ограничивающих мутагенные последствия побочных воздействий ксенобиотиков, включая химиопрепараты, имеет отчетливое прикладное значение.
Существует обширный арсенал таких средств, которые обладают антимутагенной активностью (Середин С.Б., Дурнев А.Д., 1992; Дурнев А.Д., Середин С.Б., 1998; Гончарова Р.И., Кужир Т.Д., 2005). Анализ молекулярных механизмов этой активности свидетельствует об их полифункциональной направленности, включающей антиоксидантное действие, подавление системы метаболической активации ксенобиотиков и стимуляцию их детоксикации, модуляцию репарации ДНК, влияние на транскрипционные факторы и сигнальные пути, вовлеченные в апоптоз и в регуляцию клеточного цикла.
Наиболее близким патентом по теме данной заявки является:
Антимутагенное средство: патент № 2189232; А61К 31/415, А61Р 43/00.
Предварительное внутрижелудочное введение синтетического препарата-йодантипирина (1-фенил-2,3-диметил-4 йодпиразолон) приводило к снижению мутагенного эффекта циклофосфана по показателям хромосомных аберраций в клетках костного мозга мышей.
В настоящее время скрининг антимутагенов, в основном, сосредоточен на соединениях растительного происхождения (Бириляк И.Р., Исаева А.В., 1994; Vanisree V., Tsay H.S., 2004; Неупокоева О.В., 2015), характеризующихся наряду с генопротекторным эффектом низкой токсичностью. В этом отношении обращают на себя внимание тритерпеноиды, обладающие выраженной антиоксидантной активностью (Карачурина Л.Г. и соавт., 2003; Tang X.H. at al., 2004; Gayathri K. et al., 2009), что особенно важно, исходя из представлений о роли активных форм кислорода и продуктов перекисного окисления липидов (ПОЛ) в механизмах мутагенеза (Дурнев А.Д., Середин С.Б., 1998; Зиновьева В.Н., Спасов А.А., 2003). Тритерпеноиды (тритерпены) относится к терпеноидным (или изопреноидным) соединениям. Последние представляют собой самый многочисленный класс низкомолекулярных соединений, построенных из развлетвленных С5 единиц (Лукнер М., 1979; Т. Гудвин, Мерцер Э., 1986). Они объединяются в один класс по биогенетическому признаку, поскольку все эти соединения образуются из продукта восстановления 3-окси-3-метилглютаровой (мевалоновой) кислоты. Большая часть известных к настоящему времени терпеноидов относится к веществам специализированного обмена растений, где они участвуют в процессах сигнализации, защите от фитопатогенов и т.д. Многие антибиотики, фитоалексины, реппеленты также имеют терпеноидную структуру (Пасешниченко В.А., 1998).
К числу тритерпеноидов, нашедших практическое применение в медицине, относится и милиацин, входящий в состав просяного масла (Олифсон Л.Е. с соавт., 1991), используемого для лечения трофический язв, инфицированных ран и некоторых других заболеваний (Нузов Б.Г. с соавт., 2001). Экпериментально показано, что обладая широким спектром биологической активности, милиацин стимулирует факторы неспецифической защиты и предотвращает их выраженную депрессию в условиях токсического поражения организма тетрахлорметаном (Павлова М.М., 1984), вызывает гиперцеллюлярность лимфоидных органов, стимулирует иммунный ответ (патент №2244548 (RU)), обладает антиоксидантной (Панфилова Т.В. с соавт., 2006), мембранопротекторной (патент №1043860 (RU)) и антиапоптотической (Панфилова Т.В. с соавт., 2003) активностью, демонстрирует способность регулировать экспрессию генов, контролирующих редокс-баланс клетки (Калинина О.В. с соавт., 2013), предотвращает структурно-функциональные нарушения органов иммуногенеза и печени при действии ксенобиотика (Железнова А.Д., 2010; Калинина О.В., 2013; Фролов Б.А. с соавт., 2013), снижает системную патологическую эндотоксинемию при бактериальной инфекции (патент №2564918 (RU)); Фролов Б.А. и соавт., 2013), повышая выживаемость зараженных животных и уменьшая выраженность гипоплазии центральных органов иммуногенеза: тимуса и красного костного мозга. В этой связи закономерным является интерес к исследованию способности милиацина ограничивать мутагенное действие ксенобиотиков.
Задачей изобретения является расширение арсенала природных лекарственных средств, обладающих антимутагенным действием.
Новизной изобретения является свойство растительного тритерпеноида милиацина ограничивать мутагенный эффект антибластомного химиопрепарата - циклофосфана.
Существенным отличием предлагаемого изобретения является то, что применяют милиацин в качестве средства, ограничивающего мутагенный эффект антибластомного химиопрепарата - циклофосфана.
Технический результат, обеспечиваемый изобретением, заключается в создании нового средства, снижающего мутагенный эффект антибластомного химиопрепарата - циклофосфана.
Экспериментально установлено, что заявляемое средство снижает мутагенный эффект при действии циклофосфана.
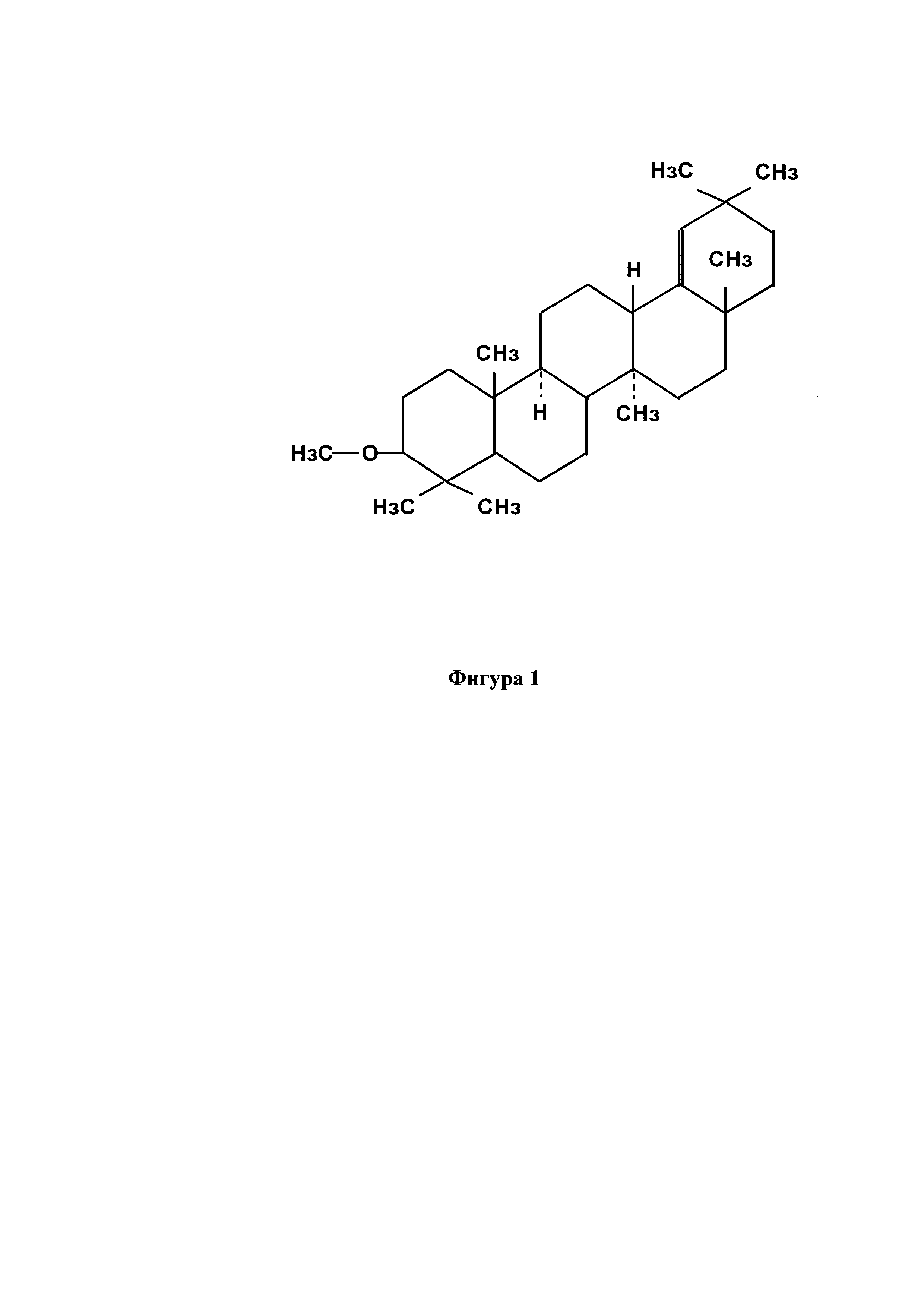
Предложенное средство 3-β-метокси-Δ18 - олеанен (милиацин) относится к группе природных циклических тритерпеноидов, содержится в просяном масле и представляет собой вещество белого цвета с температурой плавления 285-286°C. Он оптически активен, нерастворим в воде, слабо растворим в этиловом спирте, диэтиловом эфирацетоне, хорошо растворим в хлороформе. Милиацин обладает хорошей переносимостью в диапазоне доз от 2 до 1000 мг/кг. ЛД50 этого соединения больше 1000 мг/кг (Олифсон Л.Е. с соавт., 1991), что свидетельствует об отсутствии у него токсических свойств.
Химическая структура пентациклического тритерпеноида-милиацина (3-β-метокси-Δ18 - олеанена) представлена на фигуре 1.
Описание эксперимента.
Исследования выполнены на 81 особи беспородных белых мышей массой 25-30 гр., разделенных на девять групп. Животных содержали в стандартных пластмассовых клетках при комнатной температуре, двухразовом питании натуральным кормом в количестве, соответствующем суточным нормам при неограниченном доступе к воде. Эксперимент проведен в соответствии с этическими нормами и рекомендациями по гуманизации работы с лабораторными животными, отраженными в «Европейской конвенции по защите позвоночных животных, используемым для экспериментальных и других научных целей» (Страсбург, 1985). Эвтаназию животных осуществляли дислокацией шейных позвонков под эфирным наркозом.
В качестве исследуемого объекта использованы клетки костного мозга животных, исходя из представлений о том, что «исследование мутагенной активности химических соединений по выходу аберраций хромосом в костном мозге мелких грызунов является общепризнанным, надежным и весьма доступным методом» (Поздышкина О.В., 2013).
Хромосомные аберрации в клетках костного мозга индуцировали однократным внутрибрюшинным (группа IV) или внутривенным (группа V) введением циклофосфана (ЦФ)-20 мг/кг (положительные группы сравнения). Животным опытных групп милиацин вводился трехкратно внутрибрюшинно в разовой дозе 4 мг/кг в объеме 0,5 мл с суточными интервалами между введениями, завершавшимися за 24 часа до внутрибрюшинного (группа VII) или внутривенного (группа IX) применения циклофосфана. Соответствующими контролями служили группы мышей (группа VI и группа VIII), подвергавшиеся перед использованием циклофосфана трехкратному внутрибрюшинному введению растворителя для милиацина: твина 21 (1,6×10-7 моль/кг) по аналогичной схеме. В качестве отрицательных групп сравнения использовали интактных мышей (группа I), а также животных с трехкратным внутрибрюшинным введением только растворителя (группа II) или только милиацина (группа III). Количество мышей в контрольных и опытных группах составляло от 8 до 17, в группах сравнения - от 5 до 8 особей.
Животных IV-IX групп выводили из эксперимента через 24 часа после введения циклофосфана; мышей II и III группа - через 48 часов после прекращения введения растворителя или тритерпеноида. В эти же сроки забивали интактных мышей (группа I). За 1 час до забоя животным всех групп внутрибрюшинно вводился колхицин (0,04% раствор по 0,1 мл на каждые 10 грамм массы животных). Суспензию клеток костного мозга получали их вымыванием из бедренных костей 0,56% раствором KCl с последующим подсчетом количества миелокариоцитов и изготовлением препаратов. Клетки костного мозга фиксировали четырехкратно (по 20 минут) охлажденной смесью метанола и ледяной уксусной кислоты (3:1), после чего наносили на охлажденные предметные стекла, подсушивали над пламенем горелки и окрашивали красителем Гимза. Анализ хромосомных нарушений выполняли общепринятым методом световой микроскопии (10×10). В препаратах отбирали клетки округлой формы с хорошим разбросом хромосом, без наложений с модульным числом 40. Учитывались фрагменты хромосом после их разрывов, отражающие особенности мутагенного действия циклофосфана. В препаратах от каждого животного подсчитывалось не менее 100 метафазных пластинок. Определялись показатели относительного количества метафазных пластинок с аберрациями (%), количество аберраций, приходящихся на одну аберрантную пластинку и суммарное количество аберраций на 100 метафазных пластинок.
Статистическую обработку полученных данных проводили с использованием пакета прикладных программ Microsoft Excel и Statistica 10. Статистические результаты выражали в виде Медианы (Ме), нижних (Q25) и верхних(Q75) квартилей. Уровни статистической значимости различий определяли непрямым дисперсионным анализом с помощью непараметрического критерия Манна-Уитни и критерия Краскела-Уоллиса.
На фигуре 2 обозначены достоверные различия (p<0,05) количественных параметров относительного содержания аберрантных клеток при внутрибрюшинном введении циклофосфана в костном мозге у животных VII группы по сравнению с показателями VI и IV групп; • - обозначены достоверные различия (p<0,05) групп VII и IV;  - обозначены достоверные различия (p<0,05) групп VII и VI. На этой же фигуре обозначены достоверные различия (p<0,05) количественных параметров относительного содержания аберрантных клеток при внутривенном введении циклофосфана в костном мозге у животных IX группы по сравнению с показателями V и VIII групп; * - обозначены достоверные различия (p<0,05) групп IX и V;
- обозначены достоверные различия (p<0,05) групп VII и VI. На этой же фигуре обозначены достоверные различия (p<0,05) количественных параметров относительного содержания аберрантных клеток при внутривенном введении циклофосфана в костном мозге у животных IX группы по сравнению с показателями V и VIII групп; * - обозначены достоверные различия (p<0,05) групп IX и V;  - обозначены достоверные различия (p<0,05) групп IX и VIII.
- обозначены достоверные различия (p<0,05) групп IX и VIII.
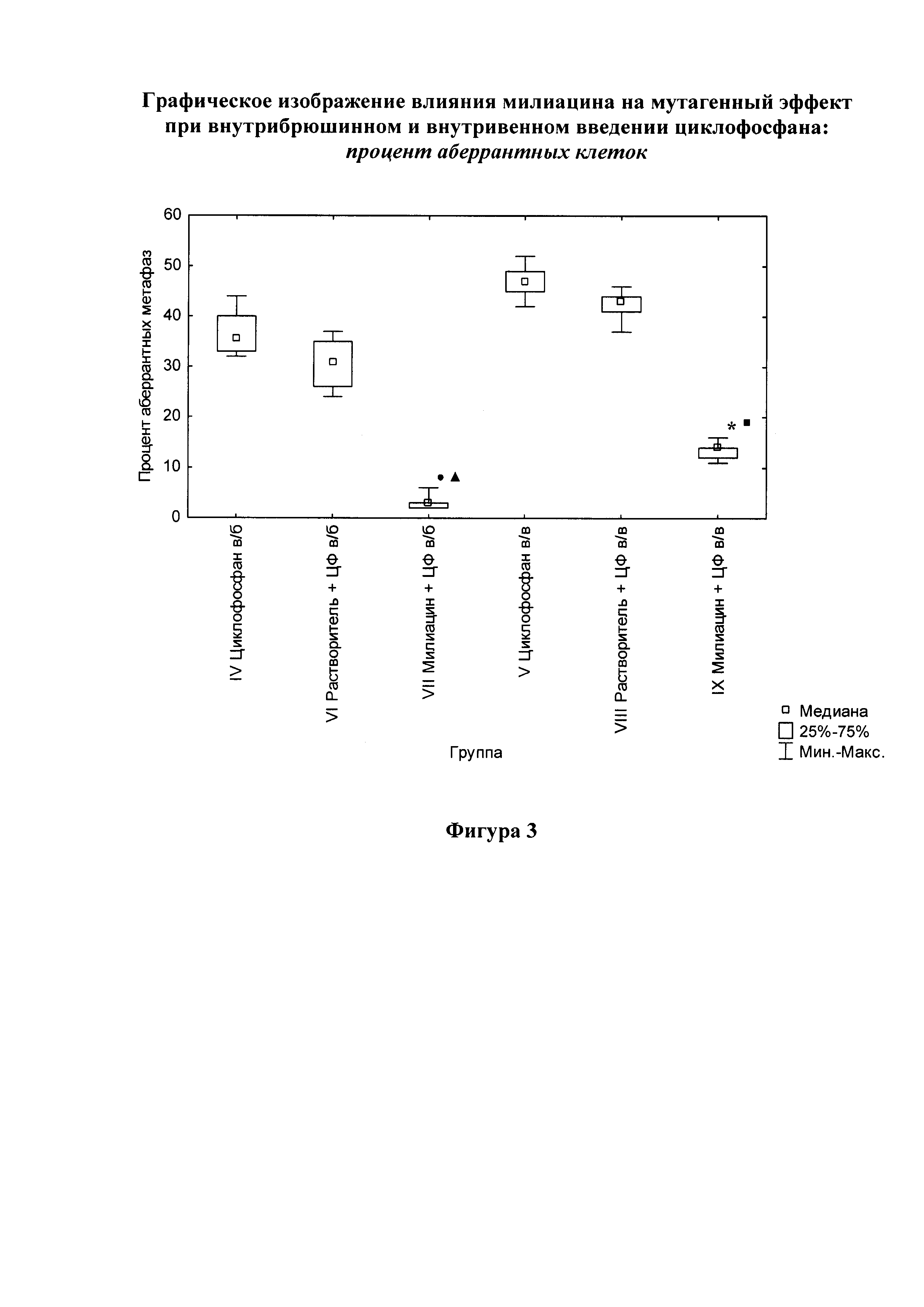
На фигуре 3 представлены графические изображения достоверности различий (p<0,05) показателей относительного содержания аберрантных клеток в сравниваемых группах.
На фигуре 4 обозначены достоверные различия (p<0,05) показателей количества аберраций на 100 метафазных пластинок при внутрибрюшинном введении циклофосфана в костном мозге у животных VII группы по сравнению с показателями VI и IV групп; • - обозначены достоверные различия (p<0,05) групп VII и IV;  - обозначены достоверные различия (p<0,05) групп VII и VI. На этой же фигуре обозначены достоверные различия (p<0,05) показателей количества аберраций на 100 метафазных пластинок при внутривенном введении циклофосфана в костном мозге у животных IX группы по сравнению с показателями V и VIII групп; * - обозначены достоверные различия (p<0,05) групп IX и V;
- обозначены достоверные различия (p<0,05) групп VII и VI. На этой же фигуре обозначены достоверные различия (p<0,05) показателей количества аберраций на 100 метафазных пластинок при внутривенном введении циклофосфана в костном мозге у животных IX группы по сравнению с показателями V и VIII групп; * - обозначены достоверные различия (p<0,05) групп IX и V;  - обозначены достоверные различия (p<0,05) групп IX и VIII.
- обозначены достоверные различия (p<0,05) групп IX и VIII.
На фигуре 5 представлены графические изображения достоверности различий (p<0,05) показателей количества аберраций на 100 метафазных пластинок в сравниваемых группах.
Установлено, что интактные мыши (I) характеризовались незначительным относительным содержанием аберрантных клеток (0,22%) и количеством аберраций на 100 метафазных пластинок (0,45). Введение растворителя (группа II) или милиацина (группа III) не приводило к существенным изменениям этих величин. В группе II относительное содержание метафазных пластинок в аберрациями составило 0,75% при количестве аберраций на 100 метафазных пластинок 0,75. В группе III относительное содержание метафазных пластинок было равно 0,37% при количестве аберраций на 100 метафазных пластинок 0,56.
Циклофосфан оказывал выраженный мутагенный эффект, проявлявшийся резким возрастанием исследуемых показателей до значений, соответственно 35,5% (33,0-40,0%) аберрантных клеток и 42,0 (40,0-56,0) аберраций на 100 метафазных пластинок при внутрибрюшинном введении (группа IV) и 47,0% (45,0-49,0%) и 127,0 (100,0-160,0) на 100 метафазных пластинок при внутривенном введении препарата (группа V).
Предварительное использование растворителя не ослабляло мутагенной активности последующего внутрибрюшинного (группа VI) или внутривенного (группа VIII) введения циклофосфана. Частота аберрантных клеток составляла 31,0% (26,0-35,0%) при количестве аберраций на 100 метафазных пластинок 49,0 (43,0-56,0) при внутрибрюшинном введении циклофосфана, а также 43,0% (41,0-44,0%) и 77,0 (82,0-93,0) при его внутривенном введении. Некоторое снижение количества мутаций на 100 метафазных пластинок в VIII группе животных не было статистически значимым по сравнению с группой V.
Предварительное введение милиацина оказывало антимутагенное действие при последующих как внутрибрюшинном (группа VII) введении циклофосфана, так и при его внутривенном (группа IX) введении. Относительное содержание аберрантных клеток снижалось, соответственно до 3,0% (2,0-3,0%) при внутрибрюшинном введении циклофосфана (группа VII) и 14,0% (12,0-14,0%) при его внутривенном введении (группа IX) при значениях числа аберраций на 100 метафазных пластинок, соответственно, - до 3,0 (2,0-4,0) и 17,0 (14,0-17,0).
Подобный протективный эффект милиацина может быть обусловлен его антиоксидантной активностью, а также прямым мембранопротективным действием. Результаты исследования расширяют представления о диапазоне биологических эффектов милиацина как перспективного средства для ограничения побочных отрицательных эффектов химиотерапии.
Таким образом, установленная в работе способность милиацина ослаблять мутагенную активность циклофосфана в экспериментальной модели на животных служит обоснованием дальнейшей разработки тритерпеноида в качестве возможного средства, снижающего мутагенный эффект химиотерапии и повышающего ее эффективность.
Литература
1. Бириляк, И.Р. Антимутагенные и генопротекторные свойства препаратов растительного происхождения / И.Р. Бириляк, А.В. Исаева// Цитология и генетика. - 1994. - Т. 28. - №3. - С. 3-17.
2. Гончарова, Р.И. Молекулярные основы применения антимутагенов в качестве антиканцерогенов / Р.И. Гончарова, Т.Д. Кужир // Экологическая генетика. - 2005. - Т. III. - №3. - С. 19-32.
3. Гудвин Т., Мерцер Э. Введение в биохимию растений // М.: Мир, 1986. - Т. 2. - С. 42-106.
4. Домрачева, Е.В. Цитогенетика индуцированных лейкозов: клональные нарушения, эффекты хромосомной нестабильности, генетическая предрасположенность/ Е.В. Домрачева, Е.А. Асеева, А.И. Удовиченко // Медицинская генетика. - 2012. - №7. - С. 4-12.
5. Дурнев, А.Д. Мутагены (скрининг и фармакологическая профилактика воздействий): монография. - М., Медицина, 1998. - 328 с.
6. Железнова А.Д. Экспериментальное обоснование применения милиацина для коррекции иммуносупрессии, индуцированной метотрексатом / А.Д. Железнова // Автореф. дисс. канд. мед. наук. - Пермь, 2010. - 22 с.
7. Зиновьева, В.Н. Коррекция мутагенного эффекта кверцетина природными и синтетическими антиоксидантами / В.Н. Зиновьева, А.А. Спасов // Вопросы биологической и фармацевтической химии. - 2005. - №1. - С. 45-48.
8. Иванова, А.А. Влияние модифицированных витаминов с антиоксидантым действием на эффективность и токсичность противоопухолевой терапии в эксперименте / А.А. Иванова // Автореф. дисс. на соиск. степ. канд. мед. наук .- Томск, 2010. - 25с.
9. Калинина О.В. Гепатопротеторная активность милиацина при метотрексат-индуцированном повреждении печени / О.В. Калинина // Автореф. дисс. канд. мед. наук. - М., 2013. - 24 с.
10. Калинина О.В. Природный тритерпеноид милиацин предотвращает вызванный метотрексатом окислительный стресс и нормализует экспрессию генов Syp 2e1 и глутатионредуктазы в печени / О.В. Калинина, Е.С. Колотова, Т.В. Панфилова, А.А. Штиль, Б.А. Фролов // Патол. физиол. и экспер. терапия, 2013а. - № 1. - С. 70-74.
11. Карачурина, Л.Г. Исследование некоторых фармакологических свойств бисгемифталата бетулина / Л.Г. Карачурина, Т.А. Сапожникова, Ф.С. Зарудий и др. // Экспер. и клин. фармакология. - 2003. - Т. 6. - №4. - С. 56-59.
12. Лукнер М. Вторичный обмен у микроорганизмов, растений и животных // М.: Мир, 1979. - С. 194-252.
13. Неупокоева, О.В. Влияние тиофана и экстракта трансформированных корней шлемника байкальского на индуцированный мутагенез / О.В.Неупокоева // Автореф. дисс. на соиск. степ. канд. биол. наук. - Томск, 2010. - 25 с.
14. Нузов Б.Г. Пути улучшения результатов лечения острого тромбофлебита поверхностных вен нижних конечностей / Б.Г. Нузов, А.А. Стадников, В.И. Бородин // Анн. травм. и ортопедии, 2001. - № 2. - С. 50-51.
15. Олифсон Л.Е. Химическая природа и биологическая активность милиацина / Л.Е. Олифсон, Н.Д. Осадчая, Б.Г. Нузов, К.Г. Галкович, М.М. Павлова // Вопросы питания, 1991. - № 2. - С. 37-59.
16. Павлова М.М. Изучение влияния активного стероида проса 3-β-метокси-Δ18 - олеанена при токсическом поражении печени CCl4 в эксперименте / М.М. Павлова // Автореф. дисс. канд. биол. наук. - Оренбург, 1984. - 21 с.
17. Панфилова Т.В. Влияние тритерпеноида милиацина на чувствительность лимфоцитов тимуса и селезенки к апоптозу, индуцированному дексаметазоном / Т.В. Панфилова, А.А. Штиль, Е.Р. Полосухина, А.Ю. Барышников, Б.А. Фролов // Бюлл. экспер. биол. и мед., 2003. - Т. 136. - № 10. - С. 382-385.
18. Панфилова Т.В. Тритерпеноид милиацин снижает индуцированное стрессом ПОЛ / Т.В. Панфилова, А.А. Штиль, Б.А. Фролов // Бюлл. экспер. биол. и мед., 2006. - Т. 141. - № 6. - С. 633-635.
19. Пасешниченко В.А. Новый альтернативный путь биосинтеза изопреноидов у эубактерий и растений // Биохимия, 1998. - Т. 63. - Вып. 2. - С. 171-182.
20. Патент № 1043860 (RU).
21. Патент № 2189232 (RU).
22. Патент № 2244548 (RU).
23. Патент № 2564918 (RU).
24. Поздышкина О.В. Количественное определение выхода аберрации хромосом в костном мозге мыши при воздействиях ионизирующей радиации и радиомодификаторов // Радиация и риск, 2013. - Т. 22. - № 1. - С. 70-74.
25. Репин, М.В. Хромосомные нарушения в лимфоцитах человека при действии ускоренных заряженных частиц / М.В. Репин, Р.О. Говорун, Е.А. Красавин // Физика элементарных частиц и атомного ядра. - 2002. - Т. 33. - №3. - С. 747-766.
26. Серединин, С.Б. Фармакологическая защита генома / С.Б. Серединин, А.Д. Дурнев / /М.:ВИНИТИ, 1992. - 160 с.
27. Фролов Б.А. Защитный эффект милиацина при экспериментальной сальмонеллезной инфекции / Б.А. Фролов, И.Н. Чайникова, А.Д. Железнова, Т.В. Панфилова, И.П. Медведева, Ю.В. Филиппова, А.И. Смолягин // ЖМЭИ, 2013б. - № 6. - С. 3-8.
28. Фролов Б.А. Преодоление гепатотоксичности метотрексата: роль тритерпеноидов / Б.А. Фролов, О.В. Калинина, А.В. Кириллова, А.А. Штиль // Клин. Онкогематология, 2013а. - Т. 6. - № 1. - С. 1-10.
29. Gayathri, R. Ursolic acid attenuates oxidative stress-mediated hepatocellular carcinoma induction by diethylnitrosamine in male Wistar rats / R. Gayathri, D.K. Priya, G.R. Gunassekaran et al. // Asian Pac. J. Cancer Prev. - 2009. - 10(5). - р. 933-938.
30. Tang, X.H. Mechanisms of hepatoprotection of Terminalia catappa L. extract on D-Galactosamine-induced liver damage / X.H. Tang, L. Gao, J. Gao et al. // Am. J. Chin. Med. - 2004. - 32(4). - р. 509-519.
31. Vanisree, M. Plant cell cultures-an alternative and efficient source for the production of biologically important secondary metabolites / M. Vanisree, H.S. Tsay // International Journal of Applied Science and Engineering. - 2004. - V.2. - р. 29-48.
Применение милиацина в качестве средства, снижающего мутагенный эффект циклофосфана.