Результат интеллектуальной деятельности: ПИТАТЕЛЬНАЯ КОМПОЗИЦИЯ ДЛЯ ПРИМЕНЕНИЯ ПРИ АКТИВАЦИИ ФОРМИРОВАНИЯ И/ИЛИ РЕГЕНЕРАЦИИ КИШЕЧНИКА И/ИЛИ ПЕЧЕНИ
Вид РИД
Изобретение
Область техники
Настоящее изобретение относится к искусственным питательным композициям, применяемым для активации формирования и/или регенерации кишечника и/или печени, и/или для лечения, и/или профилактики, и/или уменьшения риска заболеваний печени, кишечника и/или нарушения обмена веществ. Композиции в соответствии с изобретением имеют низкое содержание среднецепочечных жирных кислот (СЦЖК) и низкое содержание пальмитиновой кислоты.
Предпосылки создания изобретения
Для выздоровления от заболевания требуется полноценное питание, но у пациентов в критическом состоянии может развиваться пищевая непереносимость. Как правило, чтобы обеспечить пациента необходимым питанием, медицинские работники прекращают энтеральное кормление пациента и переводят его на парентеральное питание.
Однако парентеральное питание не лишено недостатков. Оно повышает риск катетер-ассоциированных инфекций и сепсиса, заболевания печени и других сопутствующих заболеваний.
Пищевая непереносимость может также развиваться у восприимчивых младенцев и/или детей младшего возраста, например у младенцев и/или детей младшего возраста с низким весом при рождении, находящихся в критическом состоянии, родившихся преждевременно, переживших задержку внутриутробного развития и/или страдающих задержками роста вследствие заболевания и/или неполноценного питания.
В случае восприимчивых младенцев, в частности недоношенных младенцев, пищевая непереносимость по существу связана с недоразвитием желудочно-кишечного тракта. Недоразвитая моторика желудочно-кишечного тракта приводит к медленному транзиту, задержке опорожнения желудка, приводящей к накоплению пищевого комка в желудке (например, остатков в желудке), в результате чего продолжение энтерального питания становится затруднительным. У этих младенцев также имеются особенно низкие концентрации пищеварительных ферментов и желчных солей, а также ограниченная способность к всасыванию. Вследствие этого переваривание и всасывание питательных веществ, в частности жиров, становится неоптимальным, и большая доля потребляемой энергии и поглощаемых питательных веществ выводится с калом.
У недоношенных младенцев функция печени недоразвита, и дисфункция печени часто встречается у недоношенных младенцев, поражая вплоть до 50% младенцев с крайне низким весом при рождении. Как недоношенные младенцы, так и пациенты более старшего возраста, получающие парентеральное питание в течение более чем нескольких недель, подвержены самому высокому риску заболевания угрожающими жизни гепатобилиарными расстройствами, начиная с холестаза и заканчивая терминальной стадией заболевания печени.
Следовательно, требуется улучшенная питательная композиция, которая обеспечивает удобную, безопасную и правильную доставку наиболее полноценного питания, в частности, пациентам, у которых развилась пищевая непереносимость, или подверженных риску ее развития, и особым преимуществом обладали бы, в частности, питательные композиции, позволяющие избежать рисков, связанных с парентеральным питанием, и/или ускорить период времени до перехода к полностью энтеральному питанию при одновременном обеспечении энтеральным и парентеральным питанием.
Изложение сущности изобретения
Авторами настоящего изобретения было неожиданно обнаружено, что искусственные питательные композиции в соответствии с изобретением быстрее покидают желудок, несмотря на высокое содержание в них длинноцепочечных жирных кислот (ДЦЖК) относительно среднецепочечных жирных кислот (СЦЖК). Таким образом, искусственные питательные композиции настоящего изобретения дают возможность обеспечить преимущества ДЦЖК, при этом не замедляя опорожнение желудка.
Кроме того, композиции в соответствии с изобретением проявляют повышенную способность к стимуляции переваривающей способности кишечника, а также гормонов кишечника [например, фактора роста фибробластов 19 (FGF-19) и холецистокинина (CCK)].
Таким образом, изобретение в одном аспекте относится к искусственным питательным композициям, содержащим относительно общего содержания жирных кислот:
- среднецепочечные жирные кислоты, в основном в форме триглицеридов, в количестве, находящемся в диапазоне от 0 до 50 мас.%,
- по меньшей мере одну ненасыщенную жирную кислоту, в основном в форме триглицеридов, в количестве по меньшей мере 15 мас.%, предпочтительно по меньшей мере 20 мас.%,
- пальмитиновую кислоту, в основном в форме триглицеридов, в количестве, находящемся в диапазоне не более 7%, применяемом для увеличения у индивида скорости опорожнения желудка.
Краткое описание фигур
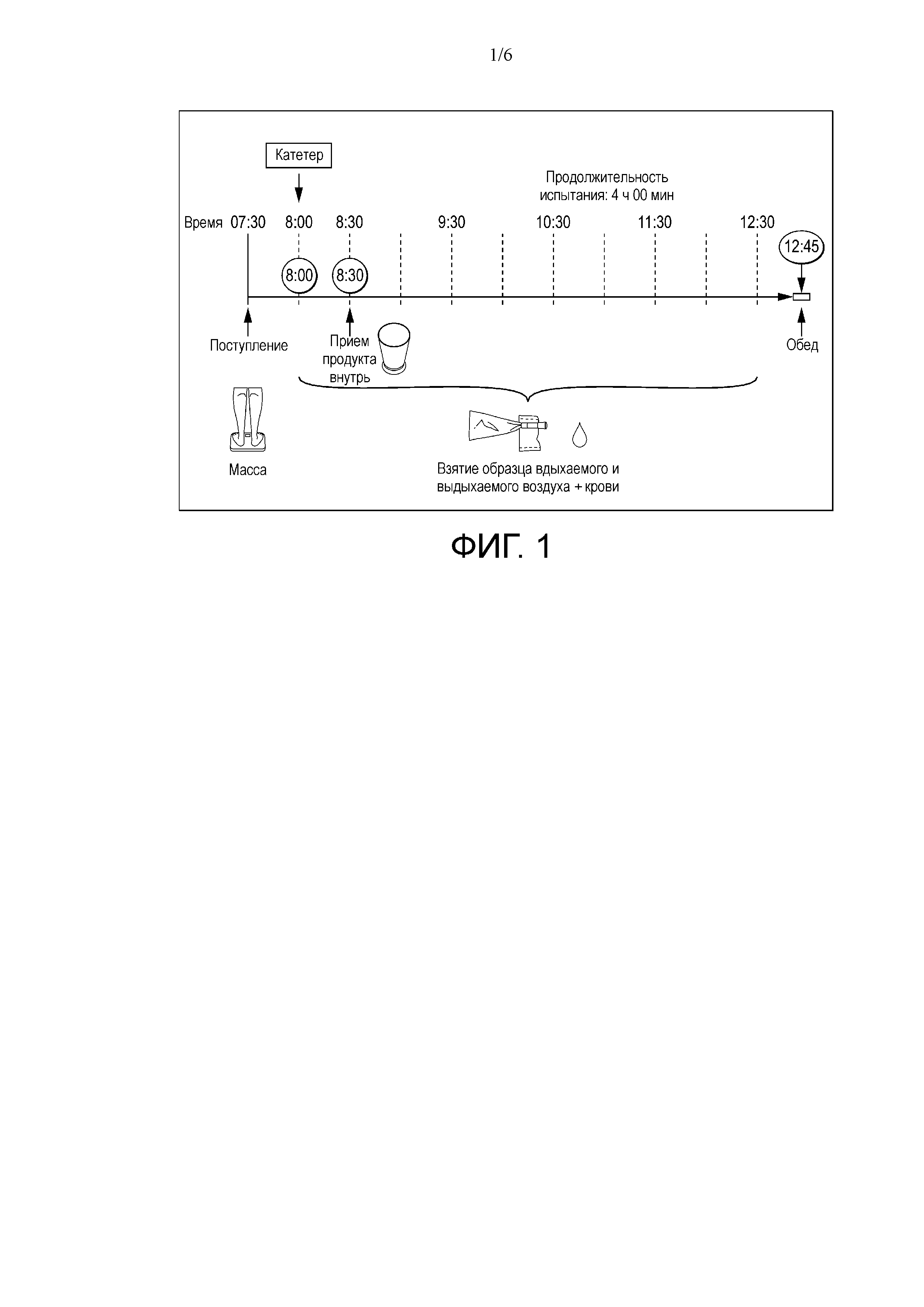
На фиг. 1 показан обзор исследования, описанного в примере 1.
На фиг. 2 показаны результаты количественных определений времени опорожнения желудка в примере 1. Заштрихованными кружками представлены оценки среднего арифметического значения, а полосами — 95% доверительный интервал половинных значений времени опорожнения желудка после потребления различных видов питания. М = питание (композицию см. в таблице 1 и таблицах 2–6); * обозначает P < 0,0001; ** обозначает P = 0,0003. Половинное значение времени (t50/мин)
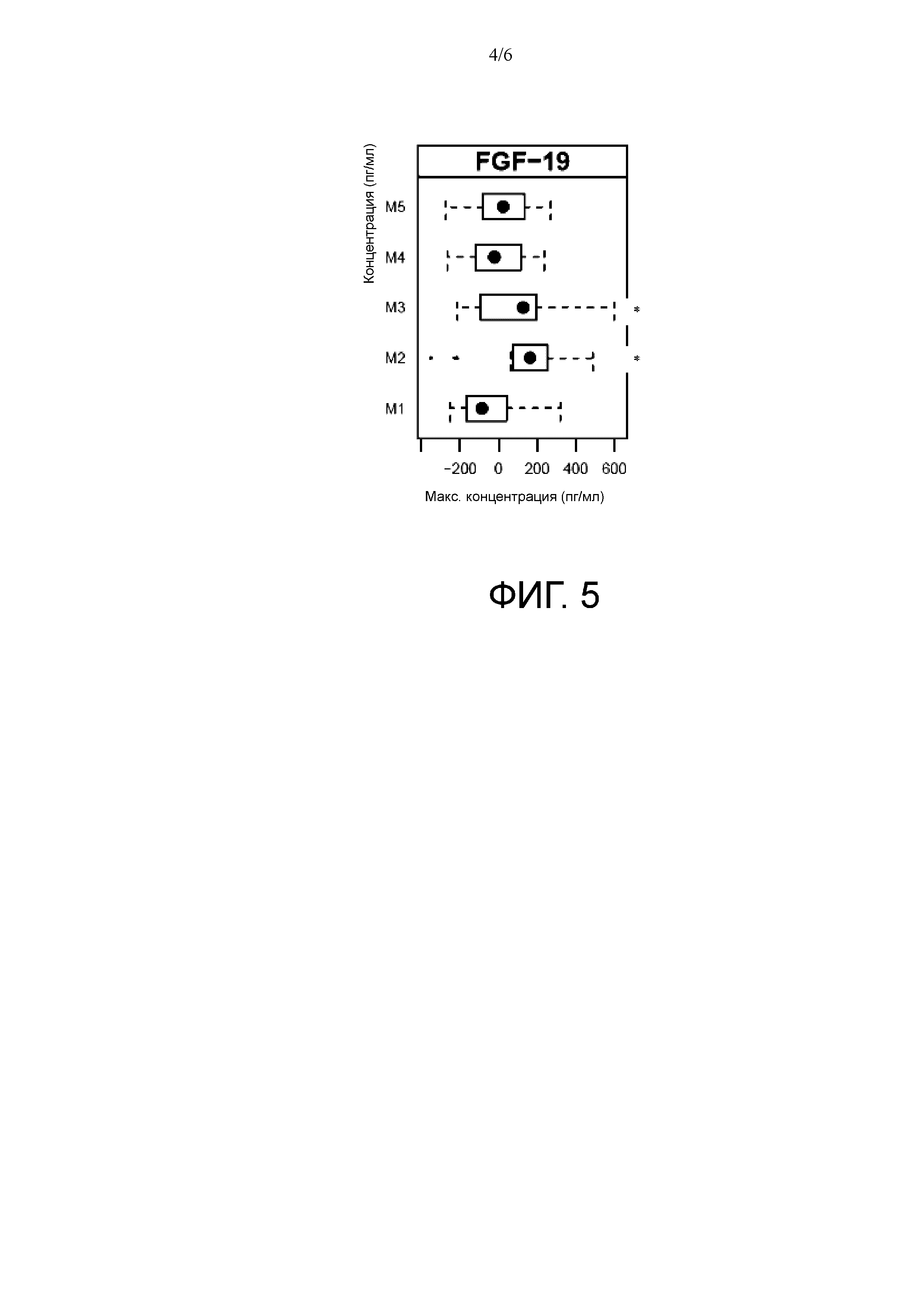
На фиг. 3 и фиг. 5 показаны результаты количественных определений фактора FGF 19 в образцах крови, отобранных во время экспериментов, описанных в примере 1. На фиг. 3 заштрихованными кружками представлены оценки среднего арифметического значения, а полосами — 95% доверительный интервал площади под кривой кинетики секреции FGF 19, скорректированной на исходные значения FGF19. М = питание (композицию см. в таблице 1 и таблицах 2–6); ** обозначает P = 0,001. Площадь над кривой исходного уровня (AOB) (пикограмм/мл мин). На фиг. 5 представлена блочная диаграмма максимальных концентраций FGF19 (пикограмм/мл) после корректировки на исходные значения FGF19. * обозначены виды пищи, где Mx > M1, p < 0,05.
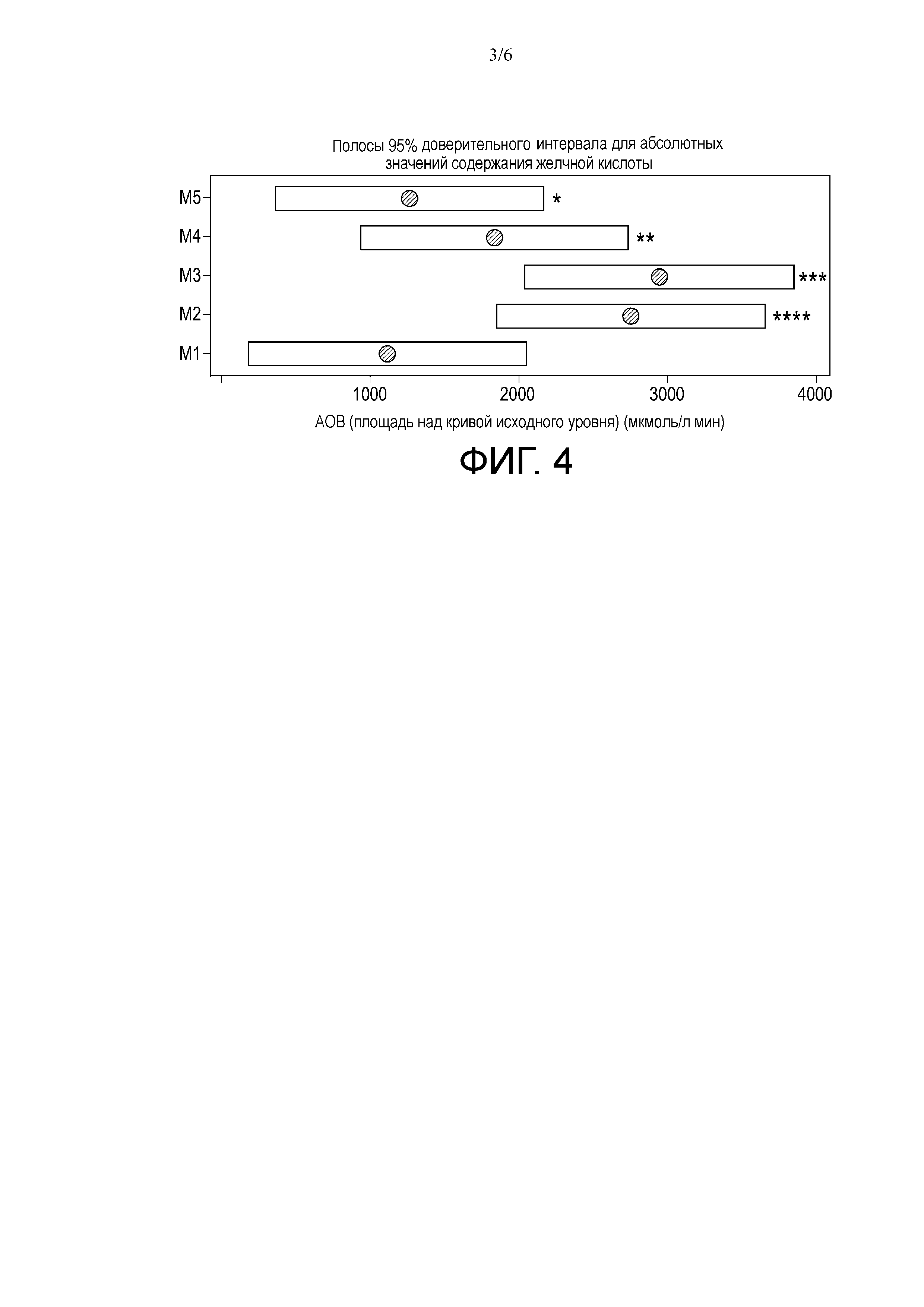
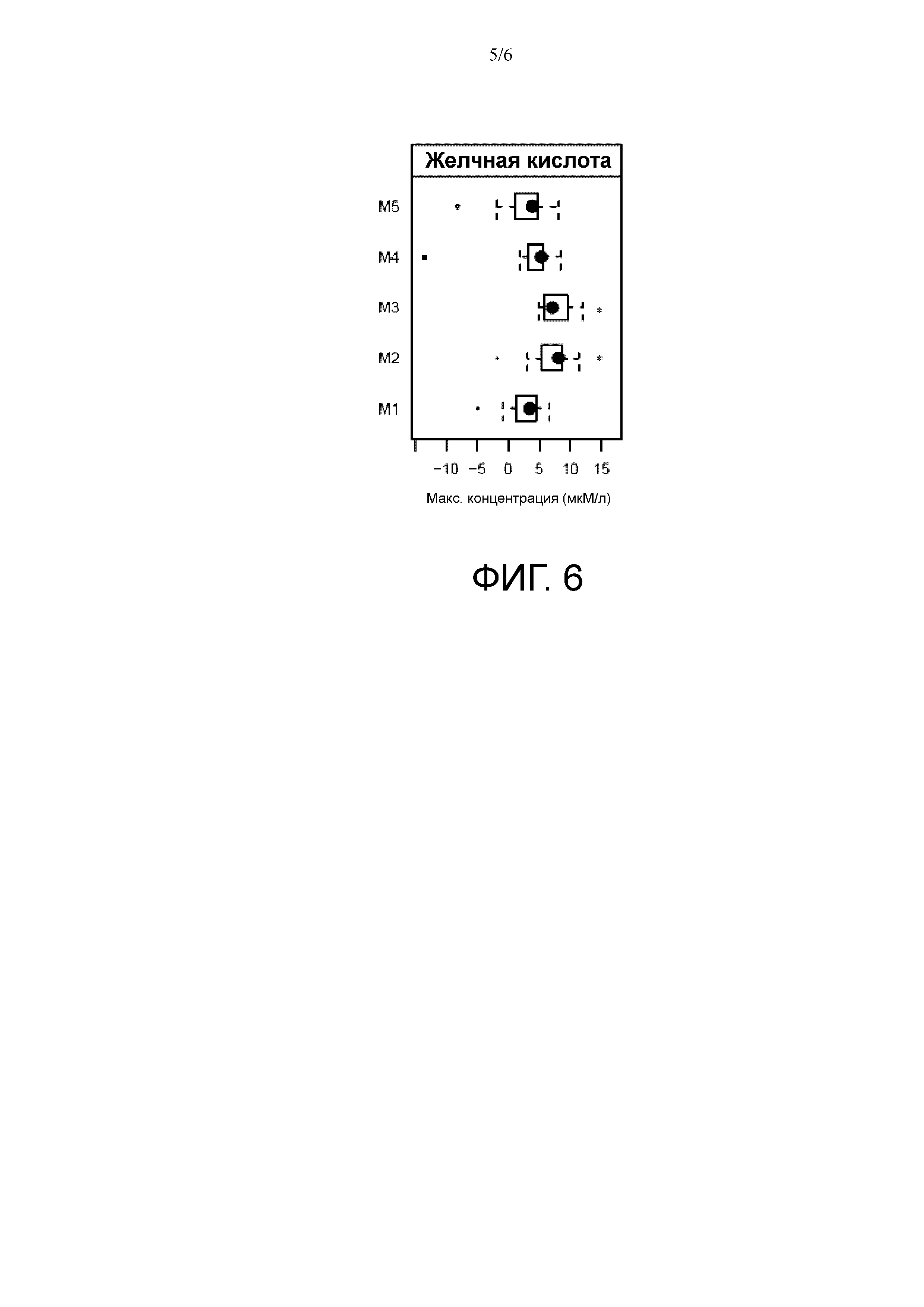
На фиг. 4 и фиг. 6 показаны результаты количественного определения желчных кислот в образцах крови, отобранных во время эксперимента, описанного в примере 1. На фиг. 4 заштрихованными кружками представлены оценки среднего арифметического значения, а полосами — 95% доверительный интервал площади под кривой кинетики секреции желчной кислоты, скорректированной на исходные значения желчной кислоты. Площадь над кривой исходного уровня (AOB) (микромоль/л мин). * обозначает P = 0,9; ** обозначает P = 0,3; *** обозначает P = 0,0003; **** обозначает P = 0,0001. На фиг. 6 представлена блочная диаграмма максимальных концентраций желчной кислоты (микромоль/л) после корректировки на исходные значения концентраций желчной кислоты; * обозначены виды пищи, где Mx > M1, p < 0,05.
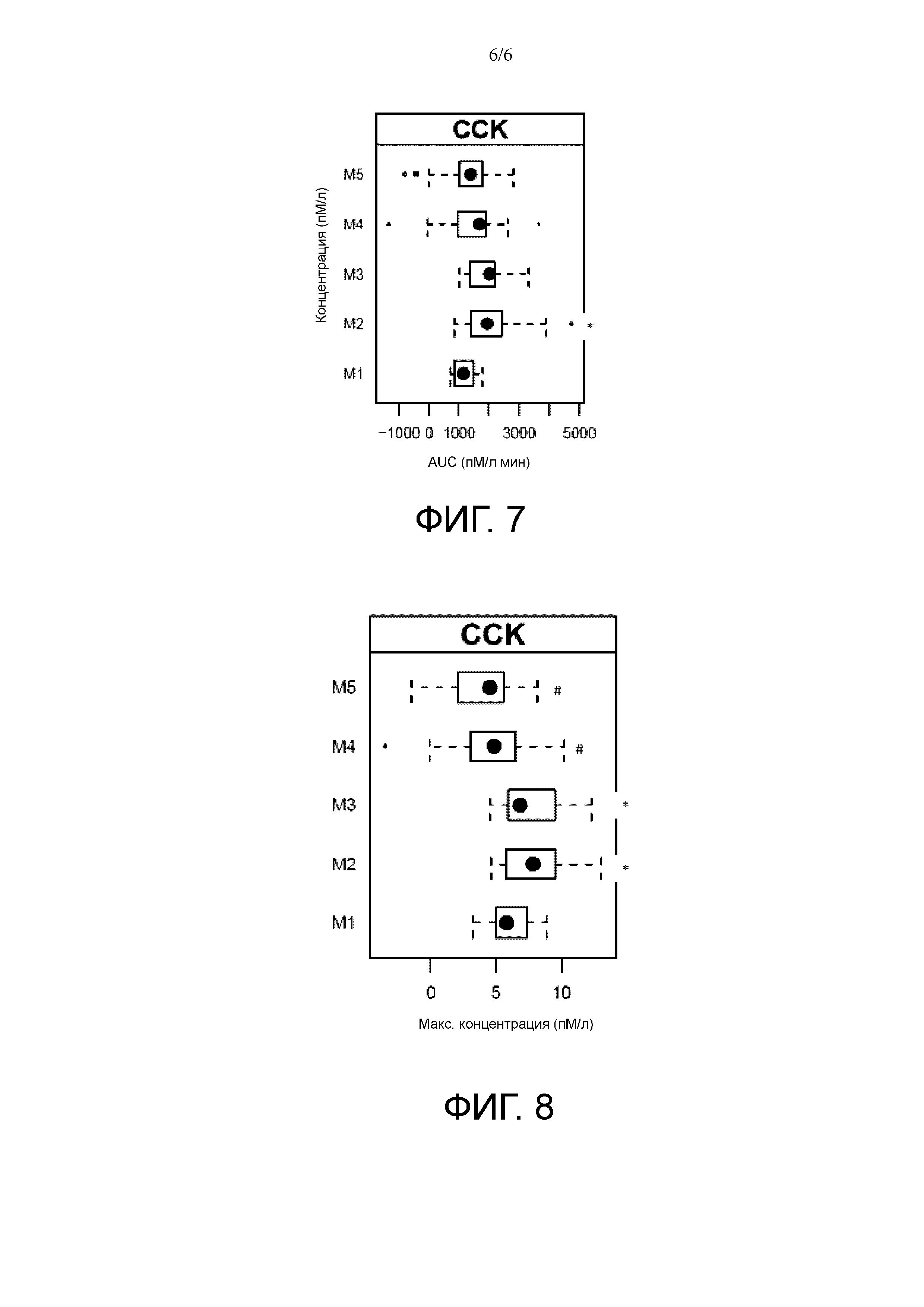
На фиг. 7 и 8 показаны результаты количественного определения холецистокинина (CCK) в образцах крови, взятых во время эксперимента, описанного в примере 1. На фиг. 7 представлена блочная диаграмма площади под кривой кинетики секреции CCK, скорректированной на исходные значения концентраций желчной кислоты (пикомоль/л мин), после корректировки на исходные значения концентраций CCK. * обозначены виды пищи, где Mx > M1, p < 0,05. На фиг. 8 представлена блочная диаграмма максимальных концентраций CCK (пикомоль/л) после корректировки на исходные значения концентраций CCK. * обозначены виды пищи, где Mx > M1, p < 0,05; # обозначены виды пищи, где Mx < M1, p < 0,05.
Подробное описание изобретения
Определения
Перед более подробным обсуждением настоящего изобретения сначала будут приведены определения указанных ниже терминов и условных обозначений.
Термин «искусственный» означает «полученный химическими и/или биологическими средствами», в противоположность «натуральному (обнаруживаемому в природе)», например, нечеловеческого происхождения (например, нечеловеческое грудное молоко).
Термин «питательная» означает композицию, которой вскармливают субъекта. Искусственные питательные композиции в соответствии с изобретением, как правило, следует принимать посредством энтерального, орогастрального или назогастрального кормления, и они могут включать источник углевода и/или белка.
Искусственные питательные композиции в соответствии с изобретением могут быть предназначены для младенцев и/или детей младшего возраста, и их можно готовить, например, в виде детской смеси, молочной смеси для детей от 1 до 3 лет, любой другой питательной композиции на молочной основе, добавки (или дополнения), обогатителя, такого как обогатитель молока (например, обогатитель человеческого грудного молока). Питательные композиции могут быть в виде порошка или в жидком виде.
Термин «добавка» означает питательную композицию, которая, как правило, обеспечивает субъекта отдельными питательными веществами и при этом не составляет значительную долю общих потребностей субъекта в питании. Как правило, они представляют не более 0,1%, 1%, 5%, 10% или 20% суточной потребности субъекта в энергии. Добавки могут быть представлены, например, в форме пилюли, таблетки или порошкообразной добавки, которую можно, например, растворять в воде или посыпать ею пищевой продукт. Наиболее предпочтительна порошкообразная добавка, которую можно растворять в жидкости или посыпать ею пищевой продукт, наиболее предпочтительно растворять ее в воде.
Термин «дополнение» означает то же, что и добавка, и эти термины используют взаимозаменяемо.
Выражение «детская смесь» означает продукт питания, специально предназначенный для употребления в пищу младенцами в течение первых шести месяцев жизни и сам по себе удовлетворяющий потребности в питании этой категории лиц (ст. 2(c) Директивы Европейской комиссии 91/321/EEC 2006/141/EC от 22 сентября 2006 г. о детских смесях и смесях для прикармливаемых детей). Оно также относится к питательной композиции, предназначенной для младенцев, как определено в Codex Alimentarius (Codex STAN 72–1981) и стандарте «Специальные продукты для младенцев» (включая статью «Продукты питания для специальных медицинских целей»). Необходимо понимать, что младенцев можно вскармливать исключительно детскими смесями или можно применять детскую смесь в качестве дополнения к грудному молоку.
Детские смеси могут включать начальные детские смеси и смеси последующего уровня или смеси для прикармливаемых детей. Обычно начальная смесь в качестве заменителя грудного молока предназначена для младенцев с рождения. Смесь последующего уровня или смесь для прикармливаемых детей, как правило, дают, начиная с 6-го месяца. Она составляет главный жидкий элемент в постепенно увеличивающемся разнообразии рациона для лиц данной категории.
Выражение «смесь для недоношенных детей» означает детскую смесь, предназначенную для недоношенного младенца.
Термин «молочная смесь для детей от 1 до 3 лет» означает смесь, которую дают после одного года и далее. Обычно это напиток на основе молока, адаптированный для конкретных потребностей в питании детей младшего возраста.
Термин «обогатитель» означает питательную композицию для младенцев, предназначенную для добавления в детскую смесь или грудное молоко или для разведения в них.
Искусственная питательная композиция в соответствии с настоящим изобретением может быть гипоаллергенной питательной композицией. Выражение «гипоаллергенная питательная композиция» означает питательную композицию, которая с малой вероятностью может вызывать аллергические реакции.
В соответствии с Директивой Комиссии EC 2006/141/EC от 22 декабря 2006 г. о детских смесях и смесях для прикармливаемых детей, статьи 1.2 (a) и (b), термин «младенец» означает ребенка младше 12 месяцев.
Выражение «ребенок младшего возраста» означает ребенка в возрасте от одного до трех лет (также называемого «ребенком, начинающим ходить»).
Термин «недоношенный» или «преждевременно родившийся» относится к младенцу или ребенку младшего возраста, который родился не в срок. Обычно этот термин относится к младенцу или к ребенку младшего возраста, который родился в гестационном возрасте менее 37 недель. Выражения «младенец (-цы)/ребенок (дети) младшего возраста, родившийся (-еся) преждевременно», «младенец (-цы)/ребенок (дети) младшего возраста, который (-ые) родился (-ись) преждевременно», «недоношенный (-ые) младенец (-цы)/ребенок (дети) младшего возраста» и «недоношенные» могут использоваться взаимозаменяемо.
«Доношенный младенец/ребенок младшего возраста» относится к младенцу или к ребенку младшего возраста, родившемуся в срок. Обычно, этот термин относится к младенцу или ребенку младшего возраста, который родился на 37 неделе беременности или позже.
Под выражением «маленький для своего гестационного возраста» или «МГВ» подразумевают младенца или ребенка младшего возраста, который имеет размеры меньше нормы для своего гестационного возраста при рождении, что чаще всего определяют как массу тела ниже 10-го процентиля для данного гестационного возраста. В некоторых вариантах осуществления изобретения состояние МГВ может быть связано с задержкой внутриутробного развития (ЗВУР), относящейся к состоянию, при котором плод неспособен достичь своего потенциального размера.
Под выражением «низкий вес при рождении» следует понимать любую массу тела менее 2500 г при рождении. Таким образом, этот термин включает:
- младенца или ребенка младшего возраста, который имеет/имел массу тела от 1800 до 2500 г при рождении (обычно называемую «низкий вес при рождении» или НВР);
- младенца или ребенка младшего возраста, который имеет/имел массу тела от 1000 до 1800 г при рождении (обычно называемую «очень низкий вес при рождении» или ОНВР);
- младенца или ребенка младшего возраста, который имеет/имел массу тела менее 1000 г при рождении (обычно называемую «крайне низкий вес при рождении» или КНВР).
Младенцы или дети младшего возраста с низким весом при рождении могут быть недоношенными или доношенными, и, таким же образом, младенцы или дети младшего возраста, маленькие для своего гестационного возраста, могут быть недоношенными или доношенными.
Термин «восприимчивые младенцы и/или дети младшего возраста» используют в настоящей заявке по отношению к младенцам и/или детям младшего возраста, которые имеют или имели проблемы развития, таким как младенцы и/или дети младшего возраста с по меньшей мере одним из следующих признаков: НВР, находящиеся в критическом состоянии, родившиеся преждевременно, маленькие для данного гестационного возраста, перенесшие задержку внутриутробного развития и/или страдающие (страдавшие) задержками роста в связи с заболеванием и/или неполноценным питанием.
Термин «в критическом состоянии» относится к индивидам с угрожающим жизни заболеванием или повреждением. Таким индивидам, например, младенцу или ребенку младшего возраста, может требоваться энтеральное, орогастральное или назогастральное питание через внутрижелудочный, интрадуоденальный или энтеральный зонд, и они могут подвергаться риску необходимости обеспечения парентерального питания.
Выражение «среднецепочечная жирная кислота» (или СЦЖК) относится к н-карбоновым кислотам насыщенных нормальных алифатических цепей, состоящих, в целом, из 6–12 атомов углерода. Среднецепочечные жирные кислоты настоящего изобретения могут представлять собой гексановую кислоту (содержащую 6 атомов углерода, C6:0, также известную как капроновая кислота), октановую кислоту (содержащую 8 атомов углерода, C8:0, также известную как каприловая кислота), декановую кислоту (содержащую 10 атомов углерода, или C10:0, также известную как каприновая кислота) и/или додекановую кислоту (содержащую 12 атомов углерода, или C12:0, также известную как лауриновая кислота).
В искусственных питательных композициях изобретения среднецепочечные жирные кислоты присутствуют, в основном (т.е. по меньшей мере 98%, например более 98,5%, или более 99%, или более 99,5%) в форме триглицеридов. Термин «среднецепочечные триглицериды» (или СЦТ) означает сложные эфиры среднецепочечных жирных кислот и глицерина, иначе говоря, соединение, образованное из глицеринового каркаса и трех жирных кислот. В случае СЦТ две или три из цепей жирных кислот, присоединенных к глицерину, представляют собой цепи средней длины. В контексте настоящей заявки термины «триглицерид», «триацилглицерид» и «триацилглицерин» используются взаимозаменяемо и обозначают одно и то же соединение.
Термин «масло СЦТ» относится к произведенному продукту, содержащему среднецепочечные триглицериды.
Выражение «длинноцепочечная жирная кислота» (или ДЦЖК) относится к н-карбоновым кислотам насыщенных или (поли)ненасыщенных разветвленных или нормальных алифатических цепей, в целом, состоящих из более 12 атомов углерода. Примеры длинноцепочечных жирных кислот включают пальмитиновую кислоту (содержащую 16 атомов углерода, или C16:0) и олеиновую кислоту (18:1 цис-9). Подобным образом, длинноцепочечные жирные кислоты настоящего изобретения находятся, в основном (т.е. по меньшей мере 98%, например более 98,5%, или более 99%, или более 99,5%) в форме триглицеридов. Термин «длинноцепочечные триглицериды» (или ДЦТ) означает сложные эфиры длинноцепочечных жирных кислот и глицерина, иначе говоря, соединение, образованное из глицеринового каркаса и трех жирных кислот, две или три из цепей жирных кислот, присоединенных к глицерину, представляют собой длинные цепи.
Выражение «длинноцепочечная полиненасыщенная жирная кислота» (или ДЦ-ПНЖК) означает полиненасыщенную жирную кислоту (ПНЖК), имеющую C20 или C22 атомов углерода. Полиненасыщенные жирные кислоты (ПНЖК) представляют собой ненасыщенные жирные кислоты, которые содержат в своем каркасе более одной двойной связи.
Под выражением «пальмитиновая кислота sn 1,3» подразумевают пальмитиновую кислоту, этерифицированную в положении sn 1,3.
Под выражением «пальмитиновая кислота sn 2» подразумевают пальмитиновую кислоту, этерифицированную в положении sn 2.
Термин «мас.%» означает процентное содержание по массе. Если не указано иное, все процентные соотношения общего содержания жиров даются в мас.%.
Термин «пребиотик» означает неперевариваемые углеводы, которые благоприятно влияют на организм-хозяин, выборочно стимулируя рост и/или активность полезных для здоровья бактерий, таких как бифидобактерии, в толстом кишечнике человека [Gibson GR, Roberfroid MB. Dietary modulation of the human colonic microbiota: introducing the concept of prebiotics. J Nutr. 1995; 125:1401–12).
Термин «пробиотик» означает препараты из клеток микроорганизмов или компоненты клеток микроорганизмов, которые оказывают благоприятное воздействие на здоровье или хорошее самочувствие организма-хозяина (Salminen S, Ouwehand A. Benno Y. et al. “Probiotics: how should they be defined” Trends Food Sci. Technol. 1999:10, 107–10).
Выражение «состоит по существу из» означает, что дополнительно к тем компонентам, которые являются обязательными, в композиции могут также присутствовать другие компоненты, при условии, что их присутствие фактически не влияет на существенные характеристики композиции.
В данном описании слова «содержит», «содержащий» и аналогичные слова не следует интерпретировать в исключительном или исчерпывающем смысле. Иными словами, под ними подразумевается «включая, без ограничений».
Выражение «остатки в желудке» относится к пище от предшествующего кормления, оставшейся в желудке к началу следующего кормления.
Искусственные питательные композиции
Питательные композиции изобретения проявляют повышенную скорость опорожнения желудка, несмотря на содержание в них больших количеств ДЦЖК (см. результаты в примере 1 и на фиг. 2).
Кроме того, ДЦЖК имеют многие описанные преимущества, которые также неожиданно достигаются композицией изобретения. Внутрижелудочное содержание липазы выше у недоношенных детей, которых кормят детской смесью, обогащенной ДЦЖК, чем у тех, которых кормят детской смесью с СЦЖК (Hamosh, 1991). Дополнительно, в отличие от ДЦЖК, виды питания, обогащенного СЦЖК, не стимулируют секрецию холецистокинина (CCK), экзокринную секрецию поджелудочной железы и секрецию желчи (Vu, 1999). Кроме того, кровоток верхней брыжеечной артерии (ВБА) в большей степени стимулируется ДЦЖК, чем СЦЖК (Vu, 2001). Нарушенный кровоток ВБА связан с непереносимостью энтерального кормления у недоношенных детей (Fang, 2001; Robel-Tillig, 2004).
Тем не менее, ДЦЖК также связаны с более длительными периодами времени опорожнения желудка.
Некоторые младенцы страдают недоразвитой желудочно-кишечной моторикой системы кишечника, которая приводит к медленному транзиту, отсроченному опорожнению желудка и накоплению пищевого комка в желудке (т.е. остатков в желудке).
Таким образом, на основании предположения, что ДЦЖК могут приводить к дальнейшему уменьшению моторики и/или к дополнительному увеличению накопления остатков в желудке, кажется, что питательные композиции на основе ДЦЖК должны быть противопоказаны. Действительно, в традиционных питательных смесях для младенцев во избежание возникновения этих проблем широко применяют СЦТ.
Настоящее изобретение основано на неожиданном результате, что некоторые питательные композиции, содержащие относительно большие количества ДЦЖК, в основном в форме ДЦТ, в действительности повышают скорость опорожнения желудка. Следовательно, композиции изобретения обеспечивают путь к получению питательной ценности ДЦЖК даже у индивидов, у которых нарушена работа кишечника, например у восприимчивых младенцев и/или детей младшего возраста; пациентов в критическом состоянии любого возраста, таких как взрослые пациенты в критическом состоянии, или пожилых людей. Любой пациент, получавший парентеральное питание, либо частично получающий парентеральное питание, либо подверженный риску получения парентерального питания, может получить пользу от композиций для применения в соответствии с изобретением. Всасывание ДЦЖК сопровождалось повышением переваривающей способности кишечника (что отражалось в повышении секреции желчных солей), а также концентрации кишечных гормонов (т.е. холецистокинина (CCK)). Повышенное всасывание ДЦЖК также сопровождалось повышением концентрации фактора роста фибробластов 19 (FGF-19). FGF 19 представляет собой кишечный гормон, который может уменьшать риск стеатоза печени и холестаза, а также активировать развитие печени. Кишечный FGF-19 может также оказывать положительное воздействие на метаболизм глюкозы посредством повышения чувствительности к инсулину и индукции синтеза гликогена. Кроме того, FGF-19 может также активировать синтез белков и приводить к росту безжировой массы тела (Schaap, 2012; Reue, 2014).
Жирные кислоты — СЦЖК
Настоящее изобретение в одном аспекте относится к искусственной питательной композиции, содержащей относительно общего содержания жирных кислот:
- среднецепочечные жирные кислоты, в основном в форме триглицеридов, в количестве, находящемся в диапазоне от 0 до 50 мас.%,
- по меньшей мере одну ненасыщенную жирную кислоту, в основном в форме триглицеридов, в количестве по меньшей мере 15 мас.%, предпочтительно по меньшей мере 20 мас.%,
- пальмитиновую кислоту, в основном в форме триглицеридов, в количестве, находящемся в диапазоне не более 13%, для применения для увеличения скорости опорожнения желудка.
В одном варианте осуществления настоящее изобретение относится к искусственной питательной композиции, содержащей относительно общего содержания жирных кислот:
- среднецепочечные жирные кислоты, в основном в форме триглицеридов, в количестве, находящемся в диапазоне от 0 до 20 мас.%,
- по меньшей мере одну ненасыщенную жирную кислоту, в основном в форме триглицеридов, в количестве по меньшей мере 15 мас.%, предпочтительно по меньшей мере 20 мас.%,
- пальмитиновую кислоту, в основном в форме триглицеридов, в количестве, находящемся в диапазоне не более 13%, для применения для увеличения скорости опорожнения желудка.
Композиции изобретения могут содержать СЦЖК в количестве, находящемся в диапазоне от 0 до 50 мас.%, от 0 до 40 мас.%, от 0 до 35 мас.%, от 0 до 30 мас.%, от 0 до 25 мас.%, от 0 до 20 мас.%, от 0 до 15 мас.%, от 0 до 10 мас.%, от 0 до 8 мас.%, от 0 до 5 мас.% или может по существу не содержать СЦЖК.
В некоторых вариантах осуществления изобретения искусственная питательная композиция содержит среднецепочечные жирные кислоты, в основном в форме триглицеридов, в общем количестве, находящемся в диапазоне от 10 до 15 мас.% относительно общего содержания жиров, таком как, например, от 10,1 до 15%, от 10,5 до 15%, от 11 до 15%, от 12 до 15%, от 13 до 15%, от 14 до 15%, или, например, от 10,1 до 14%, от 10,5 до 14%, или от 10,5 до 13%, или от 11 до 15%, или от 12 до 15%, все процентные содержания по массе.
Дополнительные варианты осуществления относятся к искусственной питательной композиции в соответствии с изобретением, в которой:
• гексановая кислота находится в количестве в диапазоне от 0 до 1% относительно общего содержания жиров, таком как, например, от 0,05 до 0,5 мас.%, от 0,05 до 0,4, от 0,06 до 0,4 или от 0,07 до 0,3 мас.%;
• октановая кислота находится в количестве в диапазоне от 0 до 10%, например, относительно общего содержания жиров, таком как, например, от 2 до 8%, от 1,55 до 2 мас.%, от 1,6 до 2, от 1,65 до 2, от 1,7 до 2 мас.%;
• декановая кислота находится в количестве в диапазоне от 0 до 10 мас.% относительно общего содержания жиров; таком как, например, от 0 до 1,8, от 0,1 до 1,8, от 1 до 1,7, от 1 до 1,5 или от 1,2 до 1,8 мас.%; и
• додекановая кислота находится в количестве в диапазоне от 0 до 12,0 мас.% относительно общего содержания жиров, таком как, например, от 0 до 10%, от 0 до 8%, от 0 до 6%, от 0 до 4% или, например, от 1 до 12%, от 2 до 12%, от 4 до 12%, от 6 до 12%, от 8 до 12%, от 10 до 12%.
Дополнительный вариант осуществления относится к искусственной питательной композиции в соответствии с изобретением, содержащей среднецепочечные жирные кислоты, в основном в форме триглицеридов, в общем количестве, находящемся в диапазоне от 10,1 до 15 мас.%, таком как, например, от 10,5 до 15%, от 11 до 15%, от 12 до 15%, от 13 до 15%, от 14 до 15% или, например, от 10,1 до 14%, от 10,5 до 14%, или от 10,5 до 13%, или от 11 до 15%, или от 12 до 15%, относительно общего содержания жиров, и длинноцепочечные жирные кислоты, в основном в форме триглицеридов, в общем количестве, находящемся в диапазоне от 85 до 89,9 мас.% относительно общего содержания жиров, в которой:
• гексановая кислота находится в количестве в диапазоне от 0 до 0,5 мас.% относительно общего содержания жиров;
• октановая кислота находится в количестве в диапазоне от 1,55 до 2 мас.% относительно общего содержания жиров;
• декановая кислота находится в количестве в диапазоне от 1 до 1,8 мас.% относительно общего содержания жиров; и
• додекановая кислота находится в количестве в диапазоне от 8,0 до 12,0 мас.% относительно общего содержания жиров.
Еще один дополнительный вариант осуществления относится к искусственной питательной композиции в соответствии с изобретением, содержащей среднецепочечные жирные кислоты, в основном в форме триглицеридов, в общем количестве, находящемся в диапазоне от 10,1 до 15 мас.%, таком как, например, от 10,5 до 15%, от 11 до 15%, от 12 до 15%, от 13 до 15%, от 14 до 15% или, например, от 10,1 до 14%, от 10,5 до 14%, или от 10,5 до 13%, или от 11 до 15%, или от 12 до 15%, относительно общего содержания жиров, и длинноцепочечные жирные кислоты, в основном в форме триглицеридов, в общем количестве, находящемся в диапазоне от 85 до 89,9 мас.% относительно общего содержания жиров, в которой:
• гексановая кислота находится в количестве в диапазоне от 0,05 до 0,5 мас.% относительно общего содержания жиров;
• октановая кислота находится в количестве в диапазоне от 1,55 до 2 мас.% относительно общего содержания жиров;
• декановая кислота находится в количестве в диапазоне от 1 до 1,8 мас.% относительно общего содержания жиров; и
• додекановая кислота находится в количестве в диапазоне от 8,0 до 12,0 мас.% относительно общего содержания жиров.
Жирные кислоты
Композиция изобретения содержит по меньшей мере одну ненасыщенную жирную кислоту, в основном в форме триглицеридов, в количестве по меньшей мере 15 мас.%, по меньшей мере 20 мас.%, таком как, например, по меньшей мере 35%, таком как, например, по меньшей мере 38%, таком как, например, от 40% до 90%, таком как, например, от 50 до 80, от 50 до 75, от 50 до 70% или, например, от 55 до 70% по массе относительно общего содержания жиров.
Примеры ненасыщенных жирных кислот включают олеиновую кислоту, а также полиненасыщенные жирные кислоты (ПНЖК), например линолевую кислоту, альфа-линолевую и эйкозеновую кислоту.
В одном преимущественном варианте осуществления изобретения композиция изобретения содержит олеиновую кислоту в количестве по меньшей мере 35%, таком как, например, по меньшей мере 38%, таком как от 40% до 90%, таком как, например, от 50 до 80, от 50 до 75, от 50 до 70% или, например, от 55 до 70% олеиновой кислоты по массе относительно общего содержания жиров.
В одном варианте осуществления композиция содержит длинноцепочечную жирную кислоту в количестве, составляющем между 75 и 95 мас.% общего содержания жиров, например, между 75 и 90 мас.% общего содержания жиров.
Жирные кислоты — ПНЖК
В особенно преимущественном варианте осуществления изобретения композиция изобретения дополнительно содержит по меньшей мере одну полиненасыщенную жирную кислоту (ПНЖК), где ПНЖК присутствует (-ют) в количестве обычно по меньшей мере 0,1%, таком как, например, по меньшей мере 8%, предпочтительно по меньшей мере 10% относительно общего содержания жирных кислот.
Полиненасыщенные жирные кислоты могут быть классифицированы по различным группам по их химической структуре. Среди этих ПНЖК можно выделить омега-3 и омега-6 ПНЖК.
Полиненасыщенные омега-3 (ω-3 или n-3) жирные кислоты представляют собой альфа-линоленовую кислоту (ALA) 18:3, стеаридоновую кислоту (SDA) 18:4, эйкозатриеновую кислоту (ETE) 20:3, n-3 эйкозатетраеновую кислоту (ETA) 20:4, эйкозапентаеновую кислоту (EPA) 20:5, n-3 докозапентаеновую кислоту (DPA) 22:5 и докозагексаеновую кислоту (DHA) 22:6. В особенно преимущественном варианте осуществления ПНЖК в соответствии с изобретением представляют собой альфа-линоленовую кислоту, которая представляет собой незаменимую жирную кислоту.
Полиненасыщенные омега-6 (ω-6 или n-6) жирные кислоты представляют собой линолевую кислоту 18:2, гамма-линоленовую кислоту (GLA) 18:3, n-6 эйкозадиеновую кислоту 20:2, дигомо-гамма-линоленовую кислоту (DGLA) 20:3, арахидоновую кислоту (AA или ARA) 20:4, n-6 докозадиеновую кислоту 22:2 и докозапентаеновую кислоту 22:5. В особенно преимущественном варианте осуществления ПНЖК в соответствии с изобретением представляют собой линолевую кислоту, которая представляет собой незаменимую жирную кислоту.
В особенно преимущественном варианте осуществления композиция изобретения дополнительно содержит по меньшей мере одну ПНЖК, которая предпочтительно представляет собой n-3 и/или n-6-ПНЖК (иначе говоря, n-3-ПНЖК, n-6-ПНЖК или более предпочтительно смесь n-3- и n-6-ПНЖК), где ПНЖК присутствует (-ют) в количестве, обычно составляющем по меньшей мере 0,8 мас.%, предпочтительно по меньшей мере 1,0 мас.% относительно общего содержания жирных кислот. Это приводит (с учетом того, что общее содержание жиров включает от 90 до 96 мас.% жирных кислот, см. выше) к количеству, составляющему по меньшей мере около 0,8 мас.%, предпочтительно по меньшей мере около 1,0 мас.% относительно общего содержания жиров.
Соединение n-3-ПНЖК может представлять собой C20 или C22 n-3 жирную кислоту. C20 или C22 n-3-ПНЖК преимущественно присутствует в количестве по меньшей мере 0,4 мас.% относительно всех жирных кислот в композиции. Это приводит к количеству по меньшей мере около 0,4 мас.% относительно общего содержания жиров в композиции. Предпочтительно n-3-ПНЖК представляет собой докозагексаеновую кислоту (DHA, C22:6).
Соединение n-6-ПНЖК может представлять собой C20 или C22 n-6 жирную кислоту. C20 или C22 n-6-ПНЖК преимущественно присутствуют в количестве по меньшей мере 0,4 мас.% всех жирных кислот в композиции. Это приводит к количеству по меньшей мере 0,4 мас.% относительно общего содержания жиров в композиции. Предпочтительно n-6-ПНЖК представляет собой арахидоновую кислоту (ARA, C20:4).
В особенно преимущественном варианте осуществления ПНЖК содержат по меньшей мере 0,4 мас.% докозагексаеновой кислоты и по меньшей мере 0,4 мас.% арахидоновой кислоты относительно общего содержания жирных кислот.
Источником ПНЖК могут быть, например, липиды куриного яйца, масло из грибов, рыбий жир с низким содержанием EPA или масло из водорослей. ПНЖК для композиции изобретения можно добавлять в виде небольших количеств масел, содержащих большие количества арахидоновой кислоты и докозагексаеновой кислоты в готовом виде, таких как рыбьи жиры или масла из микроорганизмов.
Как известно в данной области, присутствие ПНЖК обладает особым преимуществом для нескольких важных аспектов пользы для здоровья, таких как польза для когнитивной функции, развитие зрения и познавательной способности, противовоспалительные свойства.
В литературе существует много сообщений с предположением о том, что эти жирные кислоты могут быть незаменимыми для оптимального развития когнитивной функции. Среди множества ролей DHA влияет на функционирование гематоэнцефалического барьера, активность мембраносвязанных ферментов и ионных каналов, дофаминергическую и серотонинергическую нейротрансмиссию и сигнальную трансдукцию (Yaboob, P Annu. Rev. Nutr. 2009, 29:257–282).
Жирные кислоты — пальмитиновые кислоты
Особым преимуществом обладает присутствие пальмитиновой кислоты, в основном в форме триглицеридов, где пальмитиновая кислота этерифицирована в положении sn-2 триглицеридов.
Однако в некоторых искусственных питательных композициях, например, в стандартной детской смеси, часто в большом количестве присутствует пальмитиновая кислота, этерифицированная в положении sn-1,3 триглицеридов. При расщеплении sn-1,3-пальмитиновой кислоты высвобождаются свободные жирные кислоты, которые образуют комплексы с минеральными веществами, т.е. мыла. Эти мыла не всасываются и выводятся с калом. Это приводит к истощению минеральных веществ, а также к недостаточному всасыванию питательных веществ. Поэтому желательно иметь более низкие концентрации sn-1,3-пальмитиновой кислоты.
В искусственной питательной композиции настоящего изобретения общие концентрации sn-1,3-пальмитиновой кислоты снижены отчасти за счет снижения общего количества пальмитиновой кислоты, присутствующей в композициях изобретения.
Не желая ограничиваться какой-либо теорией, авторы считают, что при попадании в кишечник невсосавшиеся мыла пальмитиновой кислоты могут стимулировать высвобождение L-клетками гормона GLP1, который, как известно, замедляет скорость опорожнения желудка. Таким образом, уменьшение количества мыл пальмитиновой кислоты может вносить вклад в повышенную скорость опорожнения желудка.
Питательная композиция изобретения содержит пальмитиновую кислоту, в основном (т.е. по меньшей мере 98%, например более 98,5%, или более 99%, или более 99,5%) в форме триглицеридов, в количестве, находящемся в диапазоне не более 13% относительно общего содержания жиров, таком как, например, от 0 до 12, от 0 до 10, от 0 до 9, от 1 до 8, от 2 до 6, от 2 до 5, от 2 до 4, от 2 до 3,5 мас.% пальмитиновой кислоты.
В некоторых вариантах осуществления пальмитиновая кислота присутствует в количестве от 2 до 5 мас.%, от 2 до 4 мас.% или от 2,5 до 3,5 мас.% относительно общего содержания жиров.
Дополнительные конкретные варианты осуществления питательной композиции изобретения содержат не более 7 мас.% пальмитиновой кислоты sn 1,3 относительно общего содержания жиров.
Дополнительный вариант осуществления относится к питательной композиции изобретения, где пальмитиновая кислота sn-2 составляет от 15 до 30 мас.% общего содержания пальмитиновой кислоты и где пальмитиновая кислота sn-1,3 составляет от 70 до 75 мас.% общего содержания пальмитиновой кислоты.
В некоторых вариантах осуществления питательная композиция изобретения содержит пальмитиновую кислоту sn-1,3 в количестве не более 7 мас.% относительно общего содержания жиров, таком как, например, в количестве от 0 до 7%, от 1 до 7%, от 1 до 6,5%, от 1 до 6%, или таком как от 2 до 7, от 2 до 5, от 2 до 4 мас.%, или, например, от 3 до 7, от 4 до 7, от 5 до 7, или от 6 до 7 мас.% относительно общего содержания жиров.
Кокосовое масло
Дополнительные варианты осуществления относится к искусственной питательной композиции в соответствии с изобретением, где композиция содержит кокосовое масло в количестве, находящемся в диапазоне от 10 до 25% относительно общего содержания жиров.
Один конкретный вариант осуществления относится к искусственной питательной композиции в соответствии с изобретением, содержащей кокосовое масло в количестве, находящемся в диапазоне от 10 до 25% относительно общего содержания жиров, таком как, например, от 10 до 22, от 10 до 20, от 10 до 18, от 10 до 16, от 10 до 14, от 10 до 12 мас.%; или, например, от 12 до 24, от 14 до 24, от 16 до 24, от 18 до 24, от 20 до 24 или от 22 до 24 мас.%; или, например, от 16 до 20, от 18 до 20 мас.% относительно общего содержания жиров.
Кокосовое масло содержит смесь среднецепочечных жирных кислот, близкую к обнаруживаемой в грудном молоке.
Рецептуры — жировые смеси
Один конкретный вариант осуществления изобретения представляет собой вариант осуществления, в котором питательная композиция в соответствии с изобретением состоит по существу из жиров и, следовательно, представляет собой жировую смесь. Эта жировая смесь полезна для получения дополнительных питательных композиций, таких как детские смеси, в частности детские смеси, подходящие для младенцев, родившихся преждевременно или с низким весом при рождении, или переживших задержку внутриутробного развития, или страдающих задержками роста вследствие заболевания и/или неполноценного питания, и/или младенцев, страдающих или подверженных риску заболевания кишечника и/или печени.
Жировая смесь может быть единственным источником жиров в детской смеси.
Рецептуры
В других конкретных вариантах осуществления композиция в соответствии с изобретением дополнительно содержит источник белка и/или источник углевода.
Детская смесь
В преимущественных вариантах осуществления изобретения композиция в соответствии с изобретением представляет собой детскую смесь, в частности детскую смесь для недоношенных младенцев.
Искусственные питательные композиции в соответствии с изобретением могут представлять собой, например, детскую смесь; обогатитель, такой как обогатитель молока; начальную смесь, смесь для прикармливаемых детей; молочную смесь для детей от 1 до 3 лет; либо добавку или дополнение. Искусственная питательная композиция изобретения может быть в форме порошка, жидкости или концентрированной жидкости. Искусственная питательная композиция изобретения, например детская смесь, может представлять собой питательную композицию на основе коровьего молока, козьего молока или молока буйволиц.
В некоторых преимущественных вариантах осуществления искусственная питательная композиция изобретения представляет собой детскую смесь. Детская смесь может быть начальной детской смесью, обычно для младенцев, которые младше 6 месяцев, или смесью для прикармливаемых детей, обычно для младенцев или детей младшего возраста, которые старше 6 месяцев. Композиция изобретения также может представлять собой молочную смесь для детей от 1 до 3 лет или обогатитель, такой как обогатитель человеческого грудного молока.
В соответствии с особенно преимущественным вариантом осуществления искусственная питательная композиция в соответствии с изобретением специально адаптирована для младенцев, или для восприимчивого младенца, или ребенка младшего возраста, например, для младенцев и/или детей младшего возраста с НВР, находящихся в критическом состоянии, родившихся преждевременно, переживших задержку внутриутробного развития и/или страдающих задержками роста вследствие заболевания и/или неполноценного питания. В дополнительных вариантах осуществления искусственная питательная композиция специально адаптирована для младенцев и/или детей младшего возраста, получавших парентеральное питание или подверженных риску стать кандидатами на парентеральное питание.
В одном конкретном варианте осуществления искусственная питательная композиция в соответствии с изобретением адаптирована для энтерального введения, например энтерального, орогастрального или назогастрального введения. Введение смеси энтеральным путем вносит вклад в стимуляцию формирования кишечника и позволяет избежать рисков, связанных с парентеральным питанием, таких как катетер-ассоциированные инфекции, атрофия кишечника и гепатобилиарные расстройства.
Количества всех компонентов, выраженные в данном документе в виде процентов по массе (мас.%) относительно общего содержания жиров, отражают количества некоторых компонентов жиров, присутствующих в искусственной питательной композиции для потребления младенцем или ребенком младшего возраста. Например, композиция может быть порошковой детской смесью, которую разбавляют водой с получением готового жидкого продукта. Композиция в соответствии с изобретением также может быть концентрированной жидкостью, которую разбавляют водой для получения готового жидкого продукта. Композиция изобретения может представлять собой жидкий продукт, который потребляется младенцем непосредственно как есть. Композиция в соответствии с изобретением может представлять собой обогатитель грудного молока, который добавляют к грудному молоку или разбавляют грудным молоком. В этом случае значения концентрации компонентов, уже присутствующих в грудном молоке (к которому добавляют обогатитель грудного молока), нужно принимать как средние значения для кормящих матерей, которые известны или предсказаны по опубликованным клиническим данным.
Композиция в соответствии с настоящим изобретением содержит источник липидов. Источником липида может быть любой липид или жир, который подходит для применения в детских смесях, если содержание конкретных долей СЦЖК и ДЦЖК соответствует требованиям изобретения. Предпочтительные источники жира включают пальмовый олеин, подсолнечное масло с высоким содержанием олеиновой кислоты и подсолнечное масло с высоким содержанием олеиновой кислоты. Также можно добавлять незаменимые жирные кислоты, линолевую и α-линоленовую кислоту. В композиции соотношение жирных кислот n-6 и n-3 в источнике жира (в том числе ДЦ-ПНЖК, таких как арахидоновая кислота (ARA) и/или докозагексаеновая кислота (DHA)) предпочтительно составляет от приблизительно 1 : 2 до приблизительно 10 : 1, предпочтительно от приблизительно 5 : 1 до 10 : 1, еще более предпочтительно от приблизительно 7 : 1 до приблизительно 9 : 1.
Композиция в соответствии с изобретением предпочтительно является такой, что жиры состоят по существу из смеси от 0 до 20% молочного жира; от 10 до 30% кокосового масла; от 10 до 40% масла канолы; от 10 до 25% подсолнечного масла; от 10 до 30% подсолнечного масла с высоким содержанием олеиновой кислоты; от 2 до 10% пальмитиновой кислоты, в основном в форме триглицеридов; и от 1,5 до 2,5% смеси полиненасыщенных жирных кислот ARA и DHA (такой как смесь в соотношении 1 : 1 ARASCO® и DHASCO® от компании Martek), предпочтительно в соотношении ARA : DHA около 1 : 1 относительно общего содержания жиров.
Молочный жир можно эффективно заменять Betapol® или Infat® от компании AAK/Enzymotec.
Каждый из этих источников жира представляет собой рафинированное масло, подходящее для применения в детском питании.
В композициях настоящего изобретения также могут присутствовать другие стандартные ингредиенты, известные специалистам в данной области, для приготовления детской смеси, обогатителя или молочной смеси для детей от 1 до 3 лет.
Таким образом, композиция изобретения может содержать другие ингредиенты, действие которых может подкреплять технический эффект компонентов, в частности, в соответствии с Директивой Комиссии ЕС 2006/141/ЕС от 22 декабря 2006 г. в отношении детской смеси и смеси для прикармливаемых детей.
Композиция в соответствии с настоящим изобретением может также содержать источник углевода, предпочтительно в качестве пребиотиков или дополнительно к пребиотикам. Можно использовать любой источник углевода, традиционно присутствующий в детских смесях, такой как лактоза, сахароза, мальтодекстрин, крахмал и их смеси, хотя предпочтительным источником углевода является лактоза.
Пребиотики, которые можно использовать в соответствии с настоящим изобретением, не имеют конкретных ограничений и включают в себя все пищевые вещества, которые активируют в кишечнике рост пробиотиков или полезных для здоровья микроорганизмов. Предпочтительно их можно выбирать из группы, состоящей из олигосахаридов, необязательно содержащих фруктозу, галактозу и маннозу; пищевые волокна, в частности растворимые волокна, волокна сои; инулин или их смеси. Некоторыми примерами пребиотиков являются фруктоолигосахариды (FOS), галактоолигосахариды (GOS), изомальтоолигосахариды (IMO), ксилоолигосахариды (XOS), арабиноксилоолигосахариды (AXOS), маннанолигосахариды (MOS), инулин, полидекстрозные соевые олигосахариды, гликозилсахароза (GS), лактосахароза (LS), лактулоза (LA), палатинозоолигосахариды (PAO), мальтоолигосахариды, камеди и/или их гидролизаты, пектины и/или их гидролизаты. В конкретном варианте осуществления пребиотики могут представлять собой фруктоолигосахариды и/или инулин. В конкретном варианте осуществления пребиотики представляют собой комбинацию FOS с инулином, такую как продукт, продаваемый компанией BENEO-Orafti под товарным знаком олигофруктоза Orafti® (прежде Raftilose®), или продукт, продаваемый компанией BENEO-Orafti под товарным знаком инулин Orafti® (прежде Raftiline®). Другим примером является комбинация 70% короткоцепочечных фруктоолигосахаридов и 30% инулина, зарегистрированная компанией Nestle под товарным знаком «Prebio 1».
В одном варианте осуществления искусственная питательная композиция в соответствии с изобретением не содержит каких-либо пробиотических олигосахаридов.
Пребиотик также может представлять собой BMO (олигосахарид коровьего молока) и/или ОГМ (олигосахарид грудного молока), например N-ацетилированные олигосахариды, сиалилированные олигосахариды, фукозилированные олигосахариды и любые их смеси.
Конкретным примером пребиотика является смесь галактоолигосахарида (-ов), N-ацетилированного (-ых) олигосахарида (-ов) и сиалилированного (-ых) олигосахарида (-ов), в которой N-ацетилированный (-ые) олигосахарид (-ы) составляет (-ют) от 0,5 до 4,0% олигосахаридной смеси, галактоолигосахарид (-ы) составляет (-ют) от 92,0 до 98,5% олигосахаридной смеси, а сиалилированный (-ые) олигосахарид (-ы) составляет (-ют) от 1,0 до 4,0% олигосахаридной смеси. Далее по тексту эта смесь называется CMOS-GOS. Например, композиция для применения в соответствии с изобретением может содержать от 2,5 до 15,0 мас.% CMOS-GOS в пересчете на сухое вещество с условием, что композиция содержит по меньшей мере 0,02 мас.% N-ацетилированного олигосахарида, по меньшей мере 2,0 мас.% галактоолигосахарида и по меньшей мере 0,04 мас.% сиалилированного олигосахарида. В документах WO2006087391 и WO2012160080 приведено несколько примеров производства CMOS-GOS.
В частности, в композицию в соответствии с изобретением могут быть включены олигосахариды грудного молока, например сиалилированные олигосахариды, описанные в документе WO 2012/069416, опубликованном 31 мая 2012 г.
В композицию в соответствии с изобретением можно добавлять пробиотики. Дополнительно могут быть добавлены все пробиотические микроорганизмы. Предпочтительно пробиотик для этой цели можно выбирать из группы, состоящей из Bifidobacterium, Lactobacillus, Lactococcus, Enterococcus, Streptococcus, Kluyveromyces, Saccharoymces, Candida, в частности выбирать из группы, состоящей из Bifidobacterium longum, Bifidobacterium lactis, Bifidobacterium animalis, Bifidobacterium breve, Bifidobacterium infantis, Bifidobacterium adolescentis, Lactobacillus acidophilus, Lactobacillus casei, Lactobacillus paracasei, Lactobacillus salivarius, Lactobacillus lactis, Lactobacillus rhamnosus, Lactobacillus johnsonii, Lactobacillus plantarum, Lactobacillus salivarius, Lactococcus lactis, Enterococcus faecium, Saccharomyces cerevisiae, Saccharomyces boulardii или их смесей. Некоторые конкретные примеры пробиотиков выбирают из группы, состоящей из Bifidobacterium longum NCC3001 (ATCC BAA-999), Bifidobacterium longum NCC2705 (CNCM I-2618), Bifidobacterium longum NCC490 (CNCM I-2170), Bifidobacterium lactis NCC2818 (CNCM I-3446), Bifidobacterium breve штамм A, Lactobacillus paracasei NCC2461 (CNCM I-2116), Lactobacillus johnsonii NCC533 (CNCM I-1225), Lactobacillus rhamnosus GG (ATCC53103), Lactobacillus rhamnosus NCC4007 (CGMCC 1.3724), Enterococcus faecium SF 68 (NCC2768; NCIMB10415) и их смесей.
Композиция в соответствии с изобретением также может содержать источник белка. Тип белка не считается критическим для настоящего изобретения при условии, что соблюдены минимальные требования по содержанию незаменимых аминокислот и обеспечивается удовлетворительный рост. Таким образом, можно использовать источники белка на основе молочной сыворотки, казеина и их смесей, а также источники белка на основе сои. Что касается белков молочной сыворотки, источник белка может быть основан на кислой сыворотке или сладкой сыворотке, либо на их смесях, и может включать альфа-лактальбумин и бета-лактальбумин в любых желаемых соотношениях. Белки могут быть по меньшей мере частично гидролизованы с целью усиления пероральной толерантности к аллергенам, особенно к пищевым аллергенам. В таком случае композиция может представлять собой гипоаллергенную композицию.
В предпочтительном варианте осуществления композиция может представлять собой детскую смесь на основе молочной сыворотки коровьего молока. Смесь может также представлять собой гипоаллергенную (ГА) детскую смесь, в которой белки коровьего молока гидролизованы (частично или сильно). Смесь также может быть смесью на основе соевого молока или неаллергенной смесью, например смесью на основе свободных аминокислот.
Композиция изобретения может также содержать все витамины и минералы, а также другие питательные микроэлементы, которые, как известно, являются обязательными в повседневном пищевом рационе, в значимых с точки зрения питания количествах. Для некоторых витаминов и минеральных веществ установлены минимальные требования. Примеры минеральных веществ, витаминов и других питательных веществ, необязательно присутствующих в композиции изобретения, включают витамин А, витамин В1, витамин В2, витамин В6, витамин В12, витамин Е, витамин К, витамин С, витамин D, фолиевую кислоту, инозит, ниацин, биотин, пантотеновую кислоту, холин, кальций, фосфор, йод, железо, магний, медь, цинк, марганец, хлор, калий, натрий, селен, хром, молибден, таурин и L-карнитин. Минеральные вещества обычно добавляют в форме соли. Присутствие и количества конкретных минеральных веществ и других витаминов будут варьировать в зависимости от предполагаемой популяции.
При необходимости композиция изобретения может содержать эмульгаторы и стабилизаторы, такие как соя, лецитин, сложноэфирные моно- и диглицериды лимонной кислоты и т.п.
Композиция изобретения может также содержать другие вещества, которые могут оказывать благоприятное воздействие, такие как лактоферрин, нуклеотиды, нуклеозиды, ганглиозиды, полиамины и т.п.
Теперь получение композиции в соответствии с изобретением будет описано посредством примера.
Данную смесь можно получить любым подходящим способом. Например, ее можно приготовить перемешиванием вместе источника белка, источника углевода и источника жира, например смеси липидов в соответствии с изобретением, включающей в себя СЦЖК и ДЦЖК в надлежащих соотношениях. На данном этапе можно включать эмульгаторы в случае их применения. На данном этапе можно добавлять витамины и минеральные вещества, но обычно их добавляют позднее во избежание термического разложения. Перед перемешиванием в источнике жира можно растворять любые липофильные витамины, эмульгаторы и т.п. Затем можно примешивать воду, предпочтительно воду, очищенную обратным осмосом, с образованием жидкой смеси. Температура воды для удобства находится в диапазоне между приблизительно 50°С и приблизительно 80°С, чтобы облегчить диспергирование ингредиентов. Для образования жидкой смеси можно использовать доступные в продаже разжижители. Затем жидкую смесь гомогенизируют, например, в две стадии.
Затем жидкую смесь можно термически обрабатывать для снижения бактериальной нагрузки путем быстрого нагрева жидкой смеси до температуры в диапазоне от приблизительно 80°C до приблизительно 150°C в течение периода времени, например, от приблизительно 5 секунд до приблизительно 5 минут. Это можно осуществлять путем нагнетания пара или с помощью автоклава или теплообменника, например пластинчатого теплообменника.
Затем жидкую смесь можно охлаждать до температуры от приблизительно 60°C до приблизительно 85°C, например, путем мгновенного охлаждения. Затем жидкую смесь можно снова гомогенизировать, например, в две стадии: под давлением в диапазоне от приблизительно 10 МПа до приблизительно 30 МПа на первой стадии и от приблизительно 2 МПа до приблизительно 10 МПа на второй стадии. Затем гомогенизированную смесь можно дополнительно охлаждать для добавления любых термочувствительных компонентов, таких как витамины и минеральные вещества. На данном этапе удобно регулировать рН и содержание твердых веществ в гомогенизированной смеси.
Гомогенизированную смесь переносят в подходящий сушильный аппарат, такой как распылительная сушилка или сублимационная сушилка, и превращают в порошок. Влагосодержание порошка должно составлять менее приблизительно 5 мас.%. Некоторые из углеводов можно добавлять на этой стадии путем сухого смешивания параллельно с необязательным добавлением пробиотического (-их) бактериального (-ых) штамма (-ов) или путем смешивания в форме сиропа, полученного из кристаллических веществ, параллельно с необязательным добавлением пробиотического (-их) бактериального (-ых) штамма (-ов) и сушить с помощью распылительной сушки (или сублимационной сушки).
Если предпочтительна жидкая композиция, то гомогенизированную смесь можно стерилизовать, а затем асептически разливать в подходящие контейнеры или можно сначала разливать в контейнеры, а затем стерилизовать в автоклаве.
В другом варианте осуществления композиция изобретения может представлять собой добавку в количестве, достаточном для достижения у младенца требуемого эффекта. Эта форма введения обычно больше подходит для недоношенных младенцев.
Количество СЦЖК и ДЦЖК, которые нужно включить в добавку, будет выбрано в соответствии с предусмотренным способом введения добавки.
Добавка может быть, например, в форме порошка, таблеток, капсул, пастилок или жидкости, насколько она подходит в качестве питательной композиции для младенца. Добавка может дополнительно содержать защитные гидроколлоиды (такие как камеди, белки, модифицированные крахмалы), связующие вещества, пленкообразующие агенты, инкапсулирующие агенты/материалы, материалы стенок/оболочек, матричные соединения, покрытия, эмульгаторы, поверхностно-активные агенты, солюбилизирующие агенты (масла, жиры, воски, лецитины и т.п.), адсорбенты, носители, наполнители, вспомогательные соединения, диспергирующие агенты, увлажняющие агенты, технологические добавки (растворители), антислеживающие агенты, маскирующие вкус агенты, утяжеляющие агенты, желирующие агенты и гелеобразующие агенты. Добавка может также содержать традиционные фармацевтические добавки и адъюванты, эксципиенты и разбавители, включая, без ограничений, воду, желатин любого происхождения, растительные камеди, лигнинсульфонат, тальк, сахара, крахмал, гуммиарабик, растительные масла, полиалкиленгликоли, ароматизирующие агенты, консерванты, стабилизаторы, эмульгирующие агенты, буферы, смазывающие вещества, красители, увлажняющие агенты, наполнители и т.п.
Добавку можно вводить в приемлемый для потребителя (представляющего собой младенца) продукт, например в съедобный носитель или основу соответственно. Примерами таких носителей или основ является фармацевтическая композиция или пищевая композиция. Примерами таких композиций являются детские смеси, включающие смеси для недоношенных детей.
Дополнительно добавка может содержать органический или неорганический материал-носитель, подходящий для энтерального или парентерального введения, а также витамины, минеральные вещества, микроэлементы и другие питательные микроэлементы в соответствии с рекомендациями государственных органов, таких как Директива Европейской комиссии 2006/141/EC от 22 декабря 2006 г. о детских смесях и смесях для прикармливаемых детей.
Другие рецептуры
Искусственная питательная композиция изобретения, в основном, обсуждается в контексте детской смеси. Тем не менее рецептура питательной композиции может быть составлена таким образом, чтобы она подходила для других групп, таких как взрослые, пациенты в критическом состоянии, пожилые пациенты (в возрасте 60 лет и старше) и/или пациенты, подверженные риску парентерального кормления или получавшие парентеральное кормление. Такие питательные композиции могут содержать компоненты, обсуждаемые выше в контексте детской смеси. Однако для искусственных питательных композиций изобретения, не предназначенных для введения младенцам и/или детям младшего возраста, не требуется соблюдение руководств для детских смесей.
Целевые группы
Изобретение относится к искусственной питательной композиции в соответствии с изобретением, применяемой для введения индивиду.
В некоторых вариантах осуществления искусственную питательную композицию изобретения можно преимущественно вводить младенцам или детям младшего возраста. В конкретном варианте осуществления ее применяют для младенца младше 12 месяцев, младше 6 месяцев или младше 3 или менее месяцев. В конкретном варианте осуществления композиция представляет собой детскую смесь для недоношенных младенцев.
В одном варианте осуществления искусственная питательная композиция предназначена для применения у индивида в соответствии с изобретением.
В преимущественных вариантах осуществления искусственная питательная композиция предназначена для применения в соответствии с изобретением у младенца и/или ребенка младшего возраста, в частности у восприимчивого младенца и/или ребенка младшего возраста, такого как младенец и/или ребенок младшего возраста с НВР, находящийся в критическом состоянии, маленький для своего гестационного возраста, переживший задержку внутриутробного развития и/или страдающий (страдавший) задержками роста в связи с заболеванием и/или неполноценным питанием.
В дополнительных вариантах осуществления индивид представляет собой ребенка, взрослого и/или пожилого человека.
В дополнительных вариантах осуществления индивид может представлять собой пациента в критическом состоянии, в частности пациента, у которого развилась пищевая непереносимость или который подвержен риску ее развития, например ребенка, взрослого и/или пожилого индивида, находящихся в критическом состоянии.
В одном из вариантов осуществления настоящего изобретения композиция настоящего изобретения представляет собой детскую смесь, предназначенную и/или специально разработанную для недоношенных младенцев.
В одном варианте осуществления искусственная питательная композиция изобретения предназначена для употребления младенцами от рождения до одного года. В некоторых вариантах осуществления она специально предназначена для соответствия потребностям недоношенных младенцев в питании.
В одном варианте осуществления искусственная питательная композиция изобретения предназначена для употребления младенцами или детьми младшего возраста, имеющими уменьшенную моторику кишечника, которая может быть следствием, например, недоразвития кишечника. Например, недоношенные дети могут страдать недоразвитием кишечника и уменьшенной моторикой кишечника.
В одном варианте осуществления искусственная питательная композиция изобретения предназначена для употребления младенцами или детьми младшего возраста, имеющими ослабленное состояние здоровья печени или подверженными риску развития заболевания печени. В частности, у младенцев НВР (и особенно КНВР) часто проявляется заболевание печени, и, следовательно, в одном конкретном варианте осуществления изобретение относится к искусственной питательной композиции, предназначенной для таких младенцев.
В некоторых вариантах осуществления искусственная питательная композиция изобретения предназначена для применения у младенцев или детей младшего возраста во время болезни. В некоторых вариантах осуществления ее можно применять у младенцев или детей младшего возраста, находящихся в критическом состоянии, т.е. с угрожающим жизни заболеванием или повреждением.
В некоторых вариантах осуществления искусственная питательная композиция в соответствии с изобретением адаптирована для перорального введения. В некоторых вариантах осуществления композиция в соответствии с изобретением адаптирована для внутрижелудочного (например, орогастрального, назогастрального), интрадуоденального или энтерального введения.
Возраст для требующей введения (применения) композиции, а также продолжительность такого введения может зависеть от потребностей.
Например, композицию можно давать младенцам сразу после рождения. Композицию изобретения также можно давать в течение первой недели жизни младенца, или в течение первых 2 недель жизни, или в течение первых 3 недель жизни, или в течение первого месяца жизни, или в течение первых 2 месяцев жизни, или в течение первых 3 месяцев жизни, или в течение первых 4 месяцев жизни, или в течение первых 6 месяцев жизни, или в течение первых 8 месяцев жизни, или в течение первых 10 месяцев жизни, или в течение первого года жизни, или в течение первых двух лет жизни, или даже дольше. В некоторых других вариантах осуществления композицию изобретения дают несколько дней, или несколько недель, или несколько месяцев после рождения.
В одном варианте осуществления композицию изобретения дают младенцу или ребенку младшего возраста в качестве композиции, дополнительной к материнскому молоку. В одном варианте осуществления композицию дают младенцу или ребенку младшего возраста в качестве единственной или основной питательной композиции в течение по меньшей мере одного периода времени, например, после 1-го, 2-го или 4-го месяца, в течение по меньшей мере 1, 2, 4 или 6 месяцев. В некоторых вариантах осуществления младенец или ребенок младшего возраста получает материнское молоко в течение по меньшей мере первых 2 недель, первых 1, 2, 4 или 6 месяцев. В одном варианте осуществления композицию изобретения дают младенцу или ребенку младшего возраста после такого периода питания материнским молоком или дают во время такого периода питания материнским молоком.
Пациенты, не являющиеся младенцами
В некоторых других вариантах осуществления настоящего изобретения искусственные питательные композиции настоящего изобретения предназначены для пациентов независимо от возраста, особенно для пациентов в критическом состоянии независимо от возраста, в частности таких пациентов, у которых развилась пищевая непереносимость или подверженных риску ее развития, например, для пациентов в критическом состоянии, получавших энтеральное питание и/или подверженных риску энтерального питания. В конкретных вариантах осуществления изобретение относится к взрослым, особенно к взрослым в критическом состоянии. Взрослых определяют как индивидов от 13 лет или старше. Другие конкретные варианты осуществления относятся к детям, особенно к детям в критическом состоянии. Детей определяют как индивидов старше 3 и младше 13 лет. Дополнительные варианты осуществления относятся к пожилым людям, особенно к пожилым людям, находящимся в критическом состоянии, и/или с пищевой непереносимостью. Пожилых людей определяют как людей в возрасте 60 лет и старше.
Применение питательной композиции
Изобретение в одном варианте осуществления относится к применению в соответствии с изобретением, где применение предназначено для повышения скорости опорожнения желудка и/или повышения продукции FGF19. FGF-19 (фактор роста фибробластов 19) представляет собой кишечный гормон, который может уменьшать риск стеатоза печени и холестаза, а также активирует развитие печени. Кишечный FGF19 может также оказывать положительное воздействие на метаболизм глюкозы посредством повышения чувствительности к инсулину и индукции синтеза гликогена. Этот гормон может также активировать синтез белка и приводить к росту безжировой массы тела (Schaap, 2012; Reue, 2014).
В дополнительном варианте осуществления изобретение относится к композиции в соответствии с изобретением для применения для активации формирования и/или регенерации печени и/или кишечника и/или для уменьшения риска заболевания печени и/или кишечника.
Недоношенные младенцы, младенцы и дети младшего возраста в критическом состоянии страдают непереносимостью энтерального питания. Пищевая непереносимость побуждает медицинских работников к тому, чтобы прекращать энтеральное кормление и обеспечивать питание посредством парентерального питания.
Таким образом, настоящее изобретение относится к искусственной питательной композиции, соответствующей применению при активации и/или обеспечении формирования кишечника или уменьшения риска атрофии кишечника у младенца или ребенка младшего возраста, и/или уменьшении накопления остатков в желудке, и/или улучшении переносимости энтерального питания, и/или уменьшении риска отрыгивания и/или рвоты у младенцев или детей младшего возраста, в частности у восприимчивых младенцев или детей младшего возраста, таких как младенцы и/или дети младшего возраста с НВР, и/или находящиеся в критическом состоянии, и/или родившиеся преждевременно, и/или пережившие задержку внутриутробного развития, и/или страдавшие задержками роста вследствие заболевания и/или неполноценного питания, и/или получавшие парентеральное питание, и/или частично получавшие парентеральное питание, и/или подверженные риску стать кандидатами на парентеральное питание. Конкретные варианты осуществления относятся к питательной композиции для применения в соответствии с изобретением, где применение предназначено для недоношенных младенцев, даже более конкретно у младенцев с НВР. В одном варианте осуществления младенец или ребенок младшего возраста может находиться в критическом состоянии.
Недоношенные младенцы подвержены повышенному риску инсулинорезистентности, гипергликемии, недостаточной усвояемости питательных веществ, нарушения роста безжировой массы тела, накопления жира в области внутренних органов и расстройства метаболизма в дальнейшей жизни.
Таким образом, в другом варианте осуществления изобретение относится к искусственной питательной композиции в соответствии с изобретением для применения при активации чувствительности к инсулину, и/или при улучшении контроля уровня глюкозы в крови, и/или улучшении усвояемости питательных веществ, и/или при улучшении роста безжировой массы тела, и/или при уменьшении висцерального ожирения, и/или риска нарушения обмена веществ в дальнейшей жизни у младенца или ребенка младшего возраста, таких как младенцы и/или дети младшего возраста с НВР, находящиеся в критическом состоянии, родившиеся преждевременно, пережившие задержку внутриутробного развития и/или страдавшие задержками роста вследствие заболевания и/или неполноценного питания, получавшие парентеральное питание или подверженные риску стать кандидатами на энтеральное питание. В конкретном варианте осуществления искусственная питательная композиция в соответствии с изобретением предназначена для применения у недоношенных младенцев, даже более конкретно у недоношенных младенцев с НВР и/или КНВР.
У недоношенных младенцев функция печени недоразвита, и дисфункция печени часто встречается у недоношенных младенцев, поражая вплоть до 50% младенцев с крайне низким весом при рождении (КНВР).
Таким образом, в другом варианте осуществления изобретение относится к искусственной питательной композиции в соответствии с изобретением для применения при активации и/или обеспечении формирования печени или при уменьшении риска заболевания печени у младенца или ребенка младшего возраста, таких как младенцы и дети младшего возраста с НВР, находящиеся в критическом состоянии, родившиеся преждевременно, пережившие задержку внутриутробного развития и/или страдавшие задержками роста вследствие заболевания и/или неполноценного питания, получавшие парентеральное питание или подверженные риску стать кандидатами на энтеральное питание. В конкретном варианте осуществления искусственная питательная композиция в соответствии с изобретением предназначена для применения у недоношенных младенцев, даже более конкретно у недоношенных младенцев с НВР.
В альтернативном варианте изобретения данный аспект изобретения может быть описан в отношении применения искусственной питательной композиции в соответствии с изобретением, в частности жировой смеси в соответствии с изобретением, при получении искусственной питательной композиции в соответствии с изобретением, в частности при получении питательной композиции для активации и/или обеспечения формирования кишечника или уменьшения риска атрофии кишечника у младенца или ребенка младшего возраста, и/или уменьшения накопления остатков в желудке, и/или у младенца или ребенка младшего возраста, в частности у недоношенных младенцев, даже более конкретно у младенцев с НВР.
В другом варианте осуществления изобретение относится к искусственной питательной композиции в соответствии с изобретением для применения при повышении скорости опорожнения желудка, или для улучшения моторики желудка, и/или для улучшения переносимости энтерального питания, в частности, у младенца или ребенка младшего возраста, в частности у недоношенных младенцев, даже более конкретно у новорожденных младенцев с НВР.
Пациенты, не являющиеся младенцами
Другие группы пациентов могут также страдать сниженной моторикой желудка и/или уменьшенной способностью к всасыванию в кишечнике, и поэтому им может быть полезно применение искусственной питательной композиции данных изобретений. Примеры включают пациентов в критическом состоянии и пожилых пациентов.
Любую ссылку на документы предшествующего уровня техники в данном описании не следует рассматривать как признание того, что такой предшествующий уровень техники является широко известным или составляет часть общеизвестных знаний в области.
Следует отметить, что варианты осуществления и элементы, описанные в контексте одного из аспектов настоящего изобретения, также применимы к другим аспектам изобретения. В частности, следует отметить, что варианты осуществления и элементы, описанные в контексте младенца и детей младшего возраста, также могут применяться к другим группам, таким как взрослые, дети, пожилые пациенты и пациенты в критическом состоянии.
Хотя изобретение описано при помощи примера, следует понимать, что возможно внесение изменений и модификаций без отклонения от объема изобретения, определяемого пунктами формулы изобретения. Кроме того, если существуют известные эквиваленты конкретных элементов, такие эквиваленты включены так, как если бы они конкретно были упомянуты в данном описании.
Примеры
Пример 1
Перекрестное исследование разработано так, чтобы каждый субъект получал все испытуемые виды питания. Субъектам случайным образом назначали в одну из 10 возможных рандомизированных последовательностей из 5 испытуемых продуктов. Каждый субъект получал 5 исследуемых продуктов во время 5 различных визитов, разделенных периодом вымывания по меньшей мере в 1 неделю и максимум 4 недели. Каждый визит длился в течение двух дней (D-1 и D0):
• день –1 для получения стандартизованных видов питания;
• день 0 для:
– взятия исходных образцов плазмы крови;
– приема внутрь исследуемого продукта;
– взятия образцов плазмы крови — проб вдыхаемого и выдыхаемого воздуха.
Субъектами были здоровые мужчины в возрасте от 20 до 40 лет с ИМТ от 19 до 24,9 кг м-2 и имеющие нормогликемию натощак.
Описание исследования
Пять исследуемых продуктов содержали одно и то же количество мальтодекстринов и белка молочной сыворотки, но различались по композиции жирных кислот. Все исследуемые продукты содержат треть общего суточного потребления калорий каждого субъекта, определенного на основании определения по уравнению Харриса-Бенедикта, умноженного на коэффициент 1,5 для учета физической активности.
1. Мальтодекстрин (43% TEI) + белки молочной сыворотки (БМС, 12% TEI)
2. Мальтодекстрин (43% TEI + БМС (12% TEI) + МНЖК (39% TEI) + ПНЖК (6% TEI)
3. Мальтодекстрин (43% TEI) + БМС (12% TEI) + МНЖК (27% TEI) + СЦТ (12% TEI) + ПНЖК (6% TEI)
4. Мальтодекстрин (43% TEI) + БМС (12% TEI) + МНЖК (12% TEI) + СЦТ (27% TEI) + ПНЖК (6% TEI)
5. Мальтодекстрин (43% TEI) + БМС (12% TEI) + СЦТ (39% TEI) + ПНЖК (6% TEI)
(TEI= общее потребление калорий; БМС = белки молочной сыворотки; МНЖК = мононенасыщенные жирные кислоты; ПНЖК = полиненасыщенные жирные кислоты; СЦТ = среднецепочечные триглицериды). Композицию видов питания также см. в таблице 1.
Для мониторинга опорожнения желудка к каждому исследуемому продукту добавляли 100 мг 13C-октаноата (Eurisotope, г. Сент-Обен, Франция).
Таблица 1. Профиль жирных кислот исследуемых продуктов
Виды питания содержат одинаковое количество калорий для каждого субъекта, за исключением M1, который представляет собой рацион сравнения, не содержащий жиров, и имеет содержание углеводов и белков, аналогичное другим видам питания, но не содержит липидов. Все другие виды питания содержат одну треть суточного потребления калорий каждого субъекта, в M2 и V3 преобладает олеиновая кислота, а в M4 и M5 — СЦТ.
Таблица 1
|
Таблица 2. Композиция питания 1 (M1)
|
Таблица 3. Композиция пищи 2 (M2)
|
Таблица 4. Композиция пищи 3 (M3)
|
Таблица 5. Композиция пищи 4 (M4)
|
Таблица 6. Композиция пищи 5 (M5)
|
Исследование
В день исследования кинетики участники приходили натощак. Другие ограничения рациона отсутствовали.
Напиток подавали при комнатной температуре в непрозрачной чашке с крышкой для приема внутрь в течение 5–10 минут.
Образцы крови брали в моменты времени, начиная с 1 ч до приема напитка внутрь и в течение 4 часов исследования (обзор исследования см. дополнительно на фиг. 1).
Опорожнение желудка
Кратко, 100 мг 13C-октаноата растворяли в испытуемых видах пищи вечером накануне испытания, чтобы обеспечить полное гомогенное растворение метки. В день исследования метаболизма две исходных пробы вдыхаемого и выдыхаемого воздуха собирали в 3 стеклянные вакуумные контейнеры в моменты времени –30 и –15 мин до приема пищи. Все испытуемые виды питания принимали внутрь в течение менее 10 минут и нулевой момент времени определяли как окончание приема пищи. Пробы вдыхаемого и выдыхаемого воздуха собирали в моменты времени 15, 30, 45, 60, 75, 90, 105, 120, 150, 180, 210 и 240 минут с помощью простого пробоотборника и гофрированных трубок от компании QuinTron (г. Милуоки, штат Висконсин, США)
Пробы вдыхаемого и выдыхаемого 13CO2 анализировали на обогащение 13C с помощью масс-спектрометра для измерения соотношений стабильных изотопов (IRMS, Delta V Advantage, компания Thermo, г. Бремен, Германия), соединенного с системой газовой хроматографии (GC Trace, компания Thermo, г. Бремен, Германия). Выполняли анализы по оценке соотношения 13CO2/12CO2 (выраженного в виде δ13C, ‰). Стандартный газ CO2 калибровали против внутреннего международного стандарта, что позволяло соотнести отношение 13C/12C со стандартом Vienna Pee De Belemnite (VPDB).
Данные преобразовывали с помощью нелинейных уравнений в соответствии с работой Ghoos et al (2) и использовали программное обеспечение R для вычисления соответствия нелинейной кривой. Из этих уравнений выводят параметр T50Meas, который представляет собой период времени в минутах до момента опорожнения половины содержимого желудка.
На фиг. 2 показаны результаты T50Meas для различных исследованных видов питания. Как и ожидалось, быстрее выходящей из желудка пищей было питание M1, поскольку оно не содержало жиров. Интересно, что из видов питания, содержащих жиры, M2 и M3, т.е. виды питания, не содержащие или содержащие низкие количества СЦТ, имели более высокую скорость выхода из желудка, чем M4 и M5.
FGF-19
FGF-19 (фактор роста фибробластов 19) представляет собой кишечный гормон, который может уменьшать риск стеатоза печени и холестаза, а также активирует развитие печени. Этот гормон может также оказывать положительное воздействие на метаболизм глюкозы посредством повышения чувствительности к инсулину и индукции синтеза гликогена. Кроме того, FGF-19 может также активировать синтез белков и приводить к росту безжировой массы тела (Schaap, 2012; Reue, 2014).
FGF19 количественно определяли с помощью твердофазного иммуносорбентного ферментного анализа (ELISA), используя коммерческий набор от компании R&D Systems.
Результаты показывают, что более значительная стимуляция FGF-19 происходит при приеме M3 и M2, т.е. тех видов питания, которые содержат низкое количество или не содержат масла СЦТ, индуцируют существенно более высокие уровни FGF-19 по сравнению с контролем. Виды питания M4 и M5 статистически несущественно отличались от контроля.
См. также фиг. 3 и 5.
CCK и желчные кислоты
Холецистокинин (CCK) — это ключевой кишечный гормон для пищеварительного процесса, поскольку он индуцирует секрецию желчных кислот и панкреатических ферментов, необходимых для переваривания пищи. Оказалось также, этот гормон стимулирует формирование экзокринной части поджелудочной железы.
CCK количественно определяли с помощью радиоиммунологического анализа (РИА), используя коммерческий набор от компании Ray Biotech. Общее содержание желчных кислот количественно определяли колориметрическим ферментативным количественным анализом, используя коммерческий набор от компании Bio Supply.
Результаты показывают, что более значительная стимуляция CCK происходит при приеме M3 и M2, т.е. тех видов питания, которые содержат низкое количество или не содержат масла СЦТ, индуцируют существенно более высокие уровни CCK по сравнению с контролем. Напротив, виды питания M4 и M5 индуцировали более низкую секрецию CCK по сравнению с контролем. Соответственно, концентрации желчных кислот были также статистически значимо повышены только в результате приема M2 и M3. См. фиг. 4, 6 и 7, 8.
Эксперименты по отстаиванию
Эксперименты проводили для валидации методики определения опорожнения желудка.
Метод: образцы каждого испытуемого продукта (M1–M5) смешивали в равном соотношении с искусственным желудочным соком (ИЖС), который состоял из 2 мг/мл NaCl и 4,5 мг/мл пепсина, при 37°C и pH 1,9. Физическое распределение жира по всему объему каждой смеси оценивали путем измерения оптической мутности в зависимости от высоты образца (каждые 30 мкм) с течением времени при 37oC с помощью прибора TurbiscanTM LAB.
Результаты представлены ниже в таблице 7. Питание 3 разводили для испытания его стабильности (питание 3 (–10%)).
Таблица 7. Результаты испытания на коагуляцию пищи in vitro
|
Выводы. Виды питания 2 и 5 не проявляли разделения фаз. Виды питания 3 и 4 проявляли умеренное отстаивание, что было связано с агрегацией частиц жира. Такое разделение в желудке будет относительно незначительным и лишь умеренно влияет на опорожнение желудка. Предполагается, что питание 2, 4, 5 не влияет на опорожнение желудка.
Пример 2A
Таблица 8. Пример смеси липидов в соответствии с изобретением
|
Пример 2B
Таблица 9. Пример смеси липидов в соответствии с изобретением
|
Пример 3
Ниже в таблице 11 приведен пример композиции детской смеси в соответствии с изобретением.
Таблица 11. Пример детской смеси в соответствии с изобретением
|