Результат интеллектуальной деятельности: Микроорганизм, продуцирующий L-лейцин, и способ получения L-лейцина с использованием этого микроорганизма
Вид РИД
Изобретение
Область изобретения
Настоящее изобретение относится к микроорганизму, продуцирующему L-лейцин, и способу получения L-лейцина с использованием указанного микроорганизма. Предшествующий уровень техники
К аминокислотам с разветвленной цепью относятся три типа аминокислот (то есть L-валин, L-лейцин и L-изолейцин), и известно, что они метаболизируются в основном в мышцах и используются в качестве источника энергии во время физической активности. Наряду с увеличением информированности в отношении важных ролей этих аминокислот с разветвленной цепью в поддержании и увеличении мышечной массы во время физической активности, их применение также увеличивается. В частности, L-лейцин представляет собой незаменимую аминокислоту и широко применяется лекарственных средствах, пищевых продуктах, пищевых добавках, химических соединениях для производственных нужд и так далее.
Между тем, эти аминокислоты с разветвленной цепью продуцируются в основном микроорганизмами рода Escherichia или рода Corynebacterium, и известно, что их биосинтез осуществляется из 2-кетоизокапроновой кислоты, предшественника, после прохождения нескольких стадий от пировиноградной кислоты (патенты Кореи №№10-0220018 и 10-0438146). Однако, проблема с ферментами, вовлеченными в биосинтез лейцина, заключается в том, что они подвержены ингибированию по типу обратной связи, вызванному конечным продуктом, то есть L-лейцином или его производным, что затрудняет крупномасштабное промышленное получение L-лейцина.
Техническая задача
Авторы настоящего изобретения приложили усилия для разработки микроорганизмов, продуцирующих L-лейцин с высоким выходом по сравнению со стандартными штаммами. В результате они открыли, что мутанты, полученные с использованием микроорганизма, продуцирующего глутаминовую кислоту, проявляют устойчивость к норлейцину (NL) (то есть производному лейцина), и что эти мутанты свободны от ингибирования по типу обратной связи L-лейцином или его производным, и таким образом L-лейцин продуцируется с высоким выходом, тем самым выполняя настоящее изобретение.
Техническое решение
Задача настоящего изобретения заключается в том, чтобы предложить мутант Corynebacterium glutamicum, обладающий новой L-лейцин-продуцирующей способностью.
Другая задача настоящего изобретения заключается в том, чтобы предложить способ получения L-лейцина с использованием этого мутанта Corynebacterium glutamicum.
Полезные эффекты изобретения
Микроорганизм рода Corynebacterium glutamicum представляет собой микроорганизм, обладающий устойчивостью к L-лейцину или его производному, и, следовательно, может предотвращать ингибирование по типу обратной связи и обладает улучшенной продуктивностью по L-лейцину по сравнению с его родительским штаммом. Соответственно, способ получения L-лейцина с использованием микроорганизма по настоящему изобретению позволяет получать L-лейцин с высокой эффективностью и высоким выходом.
Краткое описание графических материалов
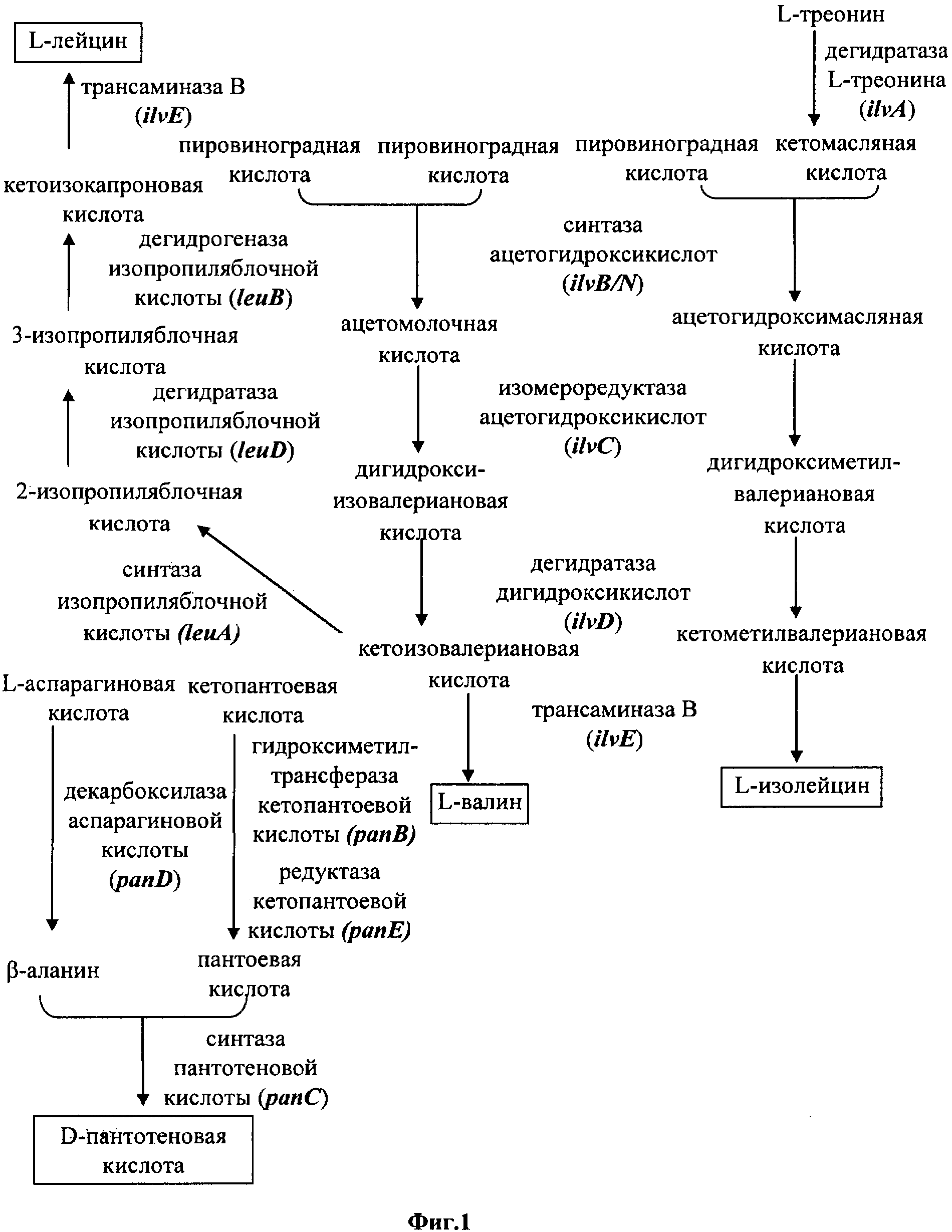
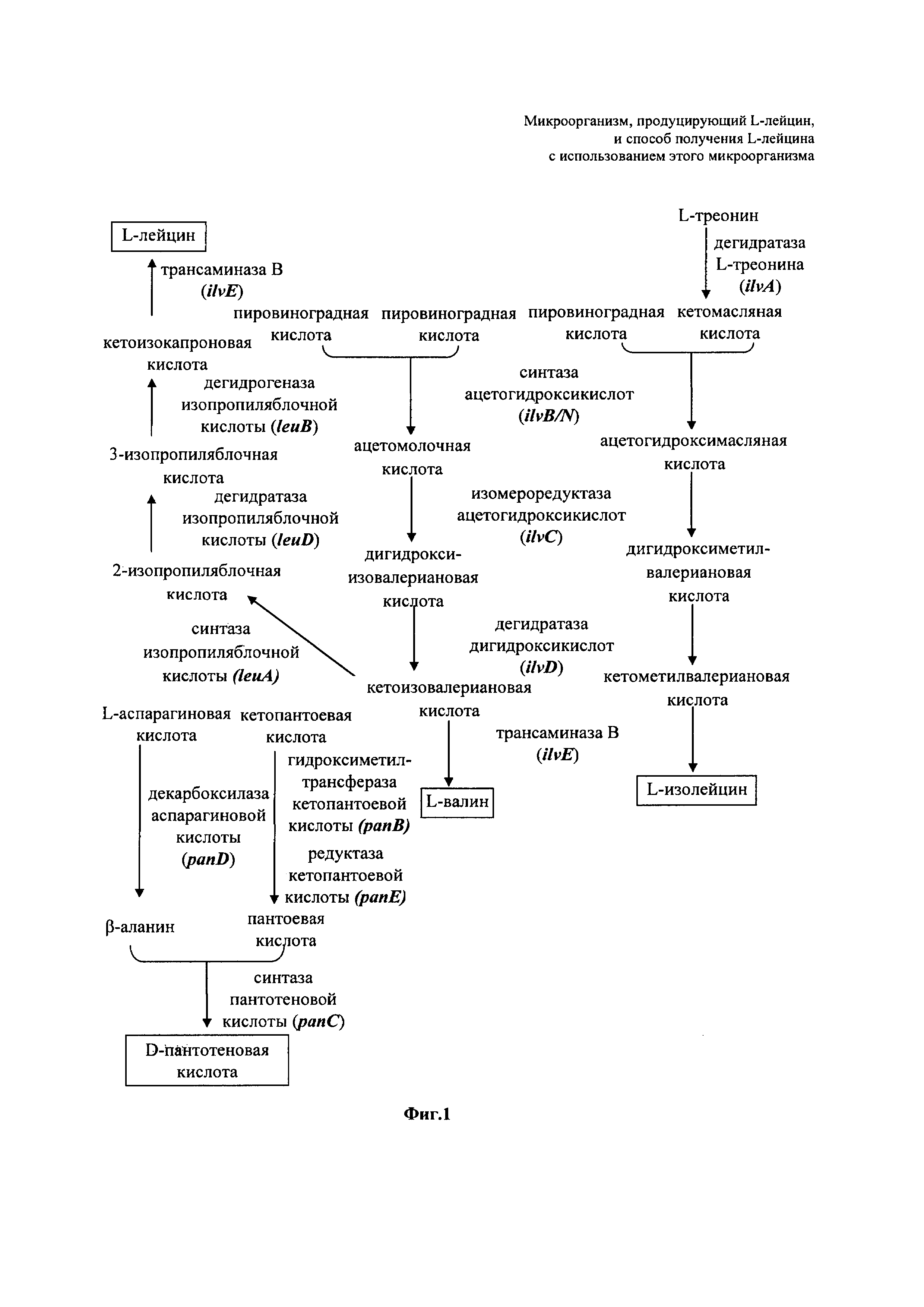
На Фиг. 1 представлена блок-схема, иллюстрирующая путь биосинтеза L-лейцина, который представляет собой конечный продукт по настоящему изобретению. Наилучшее воплощение изобретения
В одном аспекте настоящего изобретения предложен новый мутант Corynebacterium glutamicum (модифицированный штамм Corynebacterium glutamicum), продуцирующий L-лейцин, и, в частности, мутант, депонированный с номером доступа KCCM11661P, и мутант, депонированный с номером доступа KCCM11662P, для получения L-лейцина.
Как его используют здесь, термин "L-лейцин", который представляет собой незаменимую аминокислоту, относится к L-аминокислоте, представленной формулой HO2CCH(NH2)СН2СН(СН3)2, которая структурно соответствует аминокислотам с разветвленной цепью, наряду с L-валином и L-изолейцином.
Между тем, в отношении биосинтеза L-лейцина у микроорганизмов известно, что биосинтез L-лейцина осуществляется из пировиноградной кислоты через ацетомолочную кислоту, дигидроксиизовалериановую кислоту, кетоизовалериановую кислоту, 2-изопропиляблочную кислоту, 3-изопропиляблочную кислоту и кетоизокапроновую кислоту путем биосинтетического процесса, показанного на Фиг. 1. Дополнительно, биосинтез L-лейцина осуществляется путем катализа биосинтетического процесса с использованием таких ферментов как синтаза ацетогидроксикислот, изомероредуктаза ацетогидроксикислот, дегидратаза дигидроксикислот, синтаза изопропиляблочной кислоты, дегидратаза изопропиляблочной кислоты, дегидрогеназа изопропиляблочной кислоты и трансаминаза В. Однако трудно промышленным путем производить только один тип аминокислоты с разветвленной цепью путем ферментации, потому что ферменты, используемые в этих путях, являются такими же, как в процессе биосинтеза аминокислот с разветвленной цепью (то есть L-валина, L-изолейцина и L-лейцина). Дополнительно, вследствие наличия ингибирования по типу обратной связи конечным продуктом (то есть L-лейцином или его производным), существует проблема с промышленным крупномасштабным производством L-лейцина. В этом отношении мутант по настоящему изобретению может обладать устойчивостью к L-лейцину или его производному.
Как его используют здесь, термин "производное" может относиться к соединениям, о которых известно, что они обладают способностью ингибировать способность микроорганизмов продуцировать L-лейцин путем индуцирования ингибирования по типу обратной связи в отношении биосинтеза L-лейцина, конечного продукта по настоящему изобретению. Примеры соединений могут включать изолейцин, терлейцин, норлейцин, циклолейцин и так далее, но без ограничения этим. В частности, мутант может обладать устойчивостью к по меньшей мере одному веществу, выбранному из группы, состоящей из лейцина, изолейцина, терлейцина, норлейцина и циклолейцина, и более конкретно к норлейцину. В целом, известно, что биосинтез L-лейцина ингибируется, когда L-лейцин накапливается выше определенного уровня в клетке. Следовательно, любой штамм, обладающий устойчивостью к этому производному, может освободиться от ингибирования L-лейцином и может продуцировать L-лейцин даже при высокой концентрации L-лейцина.
Желаемый мутант микроорганизма, продуцирующий L-лейцин, по настоящему изобретению может быть получен путем мутагенеза его родительского штамма. В частности, мутагенез микроорганизма может быть выполнен различными способами, хорошо известными в данной области техники, и можно использовать либо физический, либо химический мутагенез. Например, примеры химических мутагенов, подходящих для настоящего изобретения, могут включать N-метил-N'-нитро-N-нитрозогуанидин (NTG), диэпоксибутан, этилметансульфонат, соединения иприта, гидразин и нитрит, но химические мутагены не ограничиваются этим. Дополнительно, примеры физических мутагенов могут включать ультрафиолет и гамма-излучение, но физические мутагены не ограничены этим.
При индуцировании мутагенеза родительский штамм подвергается воздействию мутагена в концентрации, при которой может оставаться выжившая популяция родительского штамма определенного размера. Размер варьирует в зависимости от типа мутагена и зависит от количества индуцированной мутации в выжившей популяции при постоянном уровне гибели. Например, в случае NTG уровень гибели может оставлять жизнеспособными приблизительно от 10% до 50% от начальной популяции. При мутагенезе с помощью азотистой кислоты могут оставаться жизнеспособными приблизительно от 0,01% до 0,1% от начальной популяции, и при мутагенезе с помощью ультрафиолетового света может оставаться жизнеспособным приблизительно 1,0% начальной популяции, но мутагены не ограничены этими.
В другом аспекте настоящего изобретения предложен способ получения L-лейцина, включающий культивирование мутанта Corynebacterium glutamicum и выделение L-лейцина из мутанта Corynebacterium glutamicum или из его культуры.
Как его используют здесь, термин "культивирование" обозначает, что микроорганизмы выращивают в подходящим образом искусственно контролируемых условиях окружающей среды. Культивирование микроорганизма по настоящему изобретению может быть выполнено с использованием способа культивирования Corynebacterium glutamicum, широко известного в данной области техники. В частности, примеры способов культивирования могут включать периодическое культивирование, непрерывное культивирование и периодическое культивирование с подпиткой, но способы культивирования не ограничены этим. Эти различные способы раскрыты, например, в "Biochemical Engineering" (James М. Lee, Prentice-Hall International Editions, стр. 138-176, 1991) и тому подобных.
Как его используют здесь, термин "культура" относится к материалу, содержащему среду, в которой выращивают или вырастили микроорганизм в подходящим образом искусственно контролируемых условиях окружающей среды. Культура не включает выращенный микроорганизм в узком смысле слова, но может включать его в широком смысле. Термин "культура" включает различные вещества, которые были высвобождены в среду микроорганизмом во время его роста вместе с компонентами среды, включенными для культивирования микроорганизма, и в частности, лейцина, который представляет собой целевой материал.
Среда, используемая для культивирования, должна соответствовать требованиям для культивирования определенного штамма соответствующим образом. Примеры культуральных сред для Corynebacterium раскрыты (например, Manual of Methods for General Bacteriology. American Society for Bacteriology. Washington D.C., U.S.A., 1981). Примеры источников углерода для использования могут включать сахариды и углеводы, такие как глюкоза, сахароза, лактоза, фруктоза, мальтоза, крахмал и целлюлоза; масла и жиры, такие как соевое масло, подсолнечное масло, касторовое масло и кокосовое масло; жирные кислоты, такие как пальмитиновая кислота, стеариновая кислота и линолевая кислота; спирты, такие как глицерин и этанол, и органические кислоты, такие как уксусная кислота, но источники углерода не ограничены ими. Эти вещества можно использовать по отдельности или в комбинации. Примеры источников азота для использования могут включать пептон, дрожжевой экстракт, мясной экстракт, солодовый экстракт, жидкий кукурузный экстракт, соевую муку и мочевину; или неорганические соединения, такие как сульфат аммония, хлорид аммония, фосфат аммония, карбонат аммония и нитрат аммония, но источники азота не ограничены этим. Источники азота можно использовать по отдельности или в комбинации. Примеры источников фосфора для использования могут включать дигидроортофосфат калия, гидроортофосфат калия или соответствующие их натрийсодержащие соли, но источники фосфора не ограничены ими. Дополнительно, культуральные среды могут включать соли металлов, такие как сульфат магния и сульфат железа, которые необходимы для роста. Дополнительно к вышеперечисленным веществам могут быть включены необходимые для роста вещества, такие как аминокислоты и витамины. Также в культуральной среде могут быть использованы подходящие предшественники. Вышеупомянутые вещества можно добавлять в культуральные среды подходящим образом при периодическом культивировании или непрерывном культивировании во время культивирования.
Между тем, рН культуры может быть подходящим образом отрегулирован с использованием основных соединений, таких как гидроксид натрия, гидроксид калия и аммиак, или кислотных соединений, таких как фосфорная кислота и серная кислота. Дополнительно, образование пузырей воздуха можно предупредить, используя пеногаситель, такой как полигликолевый сложный эфир жирной кислоты. Для поддержания аэробных условий в культуру вводят кислород или кислородсодержащий газ (например, воздух). Обычно температура культуральных сред может находиться в диапазоне от 20°С до 45°С. Культивирование продолжают до тех пор, пока продукция L-лейцина не достигнет ее максимального уровня, который обычно достигается через 10-160 часов. L-лейцин может высвобождаться в культуральные среды или содержаться внутри клеток.
Выделение L-лейцина из клеток или из культуральных сред может быть выполнено традиционным способом, известным в данной области техники, например центрифугированием, фильтрованием, анионообменной хроматографией, кристаллизацией, HPLC (высокоэффективная жидкостная хроматография) и так далее, но способ не ограничен ими.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Здесь и далее настоящее изобретение будет раскрыто подробно с помощью примеров воплощений. Однако эти примеры воплощений предназначены исключительно для иллюстративных целей и не предназначены ограничивать объем настоящего изобретения.
Пример 1: Отбор мутантов путем искусственного мутагенеза
Для получения мутантных микроорганизмов, продуцирующих L-лейцин, у микроорганизмов были индуцированы модификации с помощью следующих способов.
В частности, родительские штаммы (то есть продуцирующие глутаминовую кислоту Corynebacterium glutamicum АТСС 14067 и Corynebacterium glutamicum АТСС 13869), которые были активированы путем культивирования в активирующей среде в течение 16 часов, инокулировали в посевную среду, стерилизованную при 121°С в течение 15 минут, и культивировали в ней в течение 14 часов. Затем 5 мл культуральной среды отбирали и промывали 100 мМ цитратным буфером и затем к ней добавляли N-метил-N'-нитро-N-нитрозогуанидин (NTG) до конечной концентрации 200 мг/л. После обработки в течение 20 минут культуральную среду промывали 100 мМ фосфатным буфером. Штаммы, обработанные NTG, распределяли по минимальной среде и измеряли уровень гибели. В результате было подтверждено, что уровень гибели составил 85%. Для отбора модифицированных штаммов, обладающих устойчивостью к норлейцину (NL), который соответствует производному L-лейцина, штаммы, обработанные NTG, распределяли на минимальной среде, содержащей NL в конечной концентрации 20 мМ, 30 мМ, 40 мМ и 50 мМ, соответственно. Затем штаммы культивировали при 30°С в течение 5 суток и затем получали мутанты, обладающие устойчивостью к NL.
Полученные таким образом мутанты были обозначены как Corynebacterium glutamicum KCJ-24 и Corynebacterium glutamicum KCJ-28, соответственно, и были депонированы в Корейском Центре Культур Микроорганизмов (KCCM), который представляет собой международный орган депонирования согласно Будапештскому договору, 22 января 2015 года с номерами доступа KCCM11661P и KCCM11662P, соответственно.
Состав культуральных сред, используемых в Примерах 1 и 2, был следующим:
Активирующая среда
Мясной экстракт 1%, полипептон 1%, хлорид натрия 0,5%, дрожжевой экстракт 1%, агар 2%, рН 7,2;
Посевная среда
Глюкоза 5%, бактопептон 1%, хлорид натрия 0,25%, дрожжевой экстракт 1%, мочевина 0,4%, рН 7,2;
Минимальная среда
Глюкоза 1,0%, сульфат аммония 0,4%, сульфат магния 0,04%, дигидроортофосфат калия 0,1%, мочевина 0,1%, тиамин 0,001%, биотин 200 мкг/л, агар 2%, рН 7,0.
Пример 2: Исследование L-лейцин-продуцирующей способности мутантов
Corynebacterium glutamicum KCJ-24 и Corynebacterium glutamicum KCJ-28, которые были получены в Примере 1, и для которых была подтверждена их устойчивость к NL в высоких концентрациях, культивировали следующим способом, для того, чтобы подтвердить их L-лейцин-продуцирующую способность.
Каждый из Corynebacterium glutamicum АТСС 14067 и Corynebacterium glutamicum АТСС 13869 (то есть родительских штаммов) и двух мутантов инокулировали в колбы на 250 мл с угловыми перегородками, содержащие 25 мл посевной среды, описанной ниже, и культивировали при 30°С в течение 20 часов при встряхивании при 200 об/мин для получения посевных культуральных сред. После этого 1 мл каждой из посевных культуральных сред инокулировали в колбу на 250 мл с угловыми перегородками, содержащую 24 мл следующей продукционной среды и культивировали при 30°С в течение 72 часов со встряхиванием при 200 об/мин для получения L-лейцина.
Состав продукционной среды, использованной в настоящем Примере 2, был следующим.
Продукционная среда
Глюкоза 5%, сульфат аммония 2%, дигидроортофосфат калия 0,1%, гептагидрат сульфата магния 0,05%, жидкий кукурузный экстракт (CSL) 2,0%, биотин 200 мкг/л, рН 7,2.
После завершения культивирования уровень продукции L-лейцина измеряли посредством высокоэффективной жидкостной хроматографии (HPLC). Концентрации L-лейцина в культуральных средах для каждого штамма для экспериментов приведены в Таблице 1 ниже.
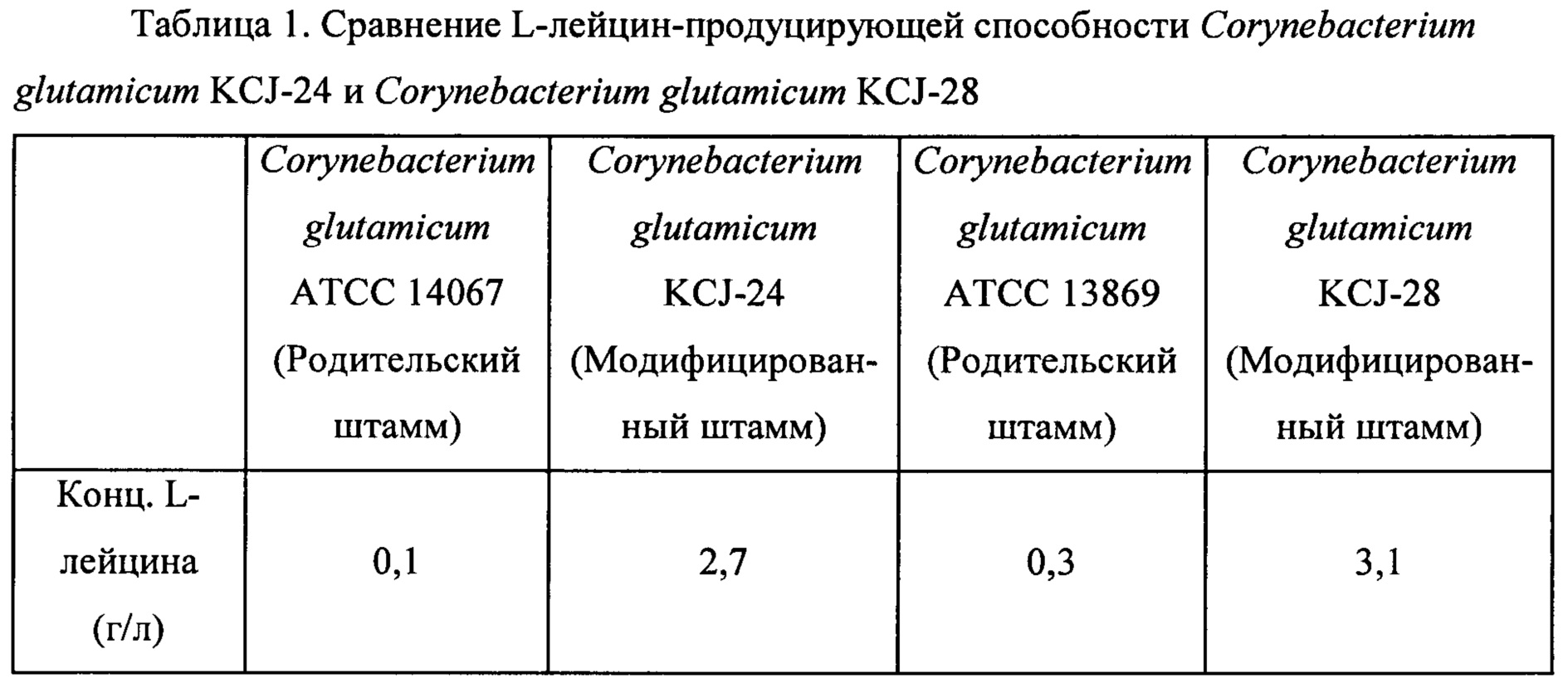
В результате, как показано в Таблице 1, родительские штаммы (то есть Corynebacterium glutamicum АТСС 14067 и Corynebacterium glutamicum АТСС 13869) продуцировали 0,1 г/л и 0,3 г/л L-лейцина, соответственно, а мутанты (то есть Corynebacterium glutamicum KCJ-24 и Corynebacterium glutamicum KCJ-28) согласно настоящему изобретению продуцировали 2,7 г/л и 3,1 г/л L-лейцина, соответственно, что подтверждает то, что L-лейцин-продуцирующая способность мутантов увеличивалась по меньшей мере примерно в 10 раз по сравнению с таковой родительских штаммов.
Приведенные выше результаты позволяют предположить, что мутанты, обладающие устойчивостью к L-лейцину и норлейцину, не подвержены ингибированию лейцином или его производным по типу обратной связи и, следовательно, могут продуцировать L-лейцин с высокой эффективностью и с высоким выходом.