Результат интеллектуальной деятельности: СПОСОБ ФОРМИРОВАНИЯ КУЛЬТУРЫ ОПУХОЛЕВЫХ КЛЕТОК, РЕЗИСТЕНТНОЙ К ПРОТОНАМ
Вид РИД
Изобретение
Изобретение относится к онкологии и лучевой терапии и направлено на получение фундаментальных и прикладных данных по реакции опухолевых клеток рецидивов и метастазов, сформированных после ранее проведенного неэффективного курса лучевой терапии к повторному курсу лучевой терапии протонами.
Успех лучевой терапии злокачественных новообразований напрямую зависит от степени радиочувствительности опухолевых клеток. Поэтому исследования, направленные на изучение радиорезистентности опухолевых клеток, имеют решающее значение для разработки более эффективных методов лечения.
Известен способ получения резистентных клеточных линий (Jing, Z. et al. Reverse resistance to radiation in KYSE-150R esophageal carcinoma cell after epidermal growth factor receptor signal pathway inhibition by cetuximab / Z. Jing, L. Gong, C.Y. Xie, L. Zhang, H.F. Su, X. Deng, S.X. Wu // Radiotherapy and Oncology. 2009. V. 93. P. 468-473), где облучение опухолевых клеток карциномы пищевода человека проводили рентгеновским излучением, после чего обновляли питательную среду и культивировали клетки. Процедуру облучения повторяли 12 раз (1 Гр 3 раза, 2 Гр 3 раза и 4 Гр 3 раза) два раза в неделю до общих доз 21 Гр в течение 1,5 месяцев до образования радиорезистентных клеток.
Известен еще один вариант получения резистентных клеток (Xie, L. et al. Fractionated irradiation induced radio-resistant esophageal cancer EC 109 cells seem to be more sensitive to chemotherapeutic drugs / L. Xie, X. Song, J. Yu, L. Wei, B. Song, X. Wang // Journal of Experimental & Clinical Cancer Research. 2009), где клеточную линию сначала выращивали примерно до 60% монослоя, затем клетки подвергали воздействию рентгеновского излучения в дозе 10 Гр, после чего культивировали примерно до 60% монослоя и снова облучали в дозе 10 Гр. Фракционированное облучение продолжались до суммарной дозы 80 Гр. После чего была установлена радиоустойчивая клеточная сублиния.
Похожая методика описана еще в одном исследовании (Fukuda K, Sakakura С, Miyagawa K, Kuriu Y, Kin S, Nakase Y, Hagiwara A, Mitsufuji S, Okazaki Y, Hayashizaki Y, Yamagishi H. Differential gene expression profiles of radioresistant oesophageal cancer cell lines established by continuous fractionated irradiation. Br J Cancer. 2004 Oct 18; 91(8): 1543-50), где линии клеток рака пищевода выращивали примерно до 50% монослоя и подвергали воздействию рентгеновского излучения в дозе 2 Гр и культивировали до 90% монослоя, затем пересевали в новые флаконы. Процедура повторялась до суммарной дозы 60 Гр.
Известен способ получения радиорезистентных опухолевых клеток человека (Shimura, Т. et al. Acquired radioresistance of human tumor cells by DNA-PK/AKT/GSK3b mediated cyclin Dl overexpression / T. Shimura, S. Kakuda, Y. Ochiai, H. Nakagawa, Y. Kuwahara, Y. Takai, J. Kobayashi, K. Komatsu, M. Fukumoto // Oncogene. 2010. N. 29. P. 4826-4837), где клетки подвергали воздействию фракционированного облучения рентгеном в дозе 0,5 Гр каждые 12 ч, 6 дней в неделю.
Общим недостатком представленных выше способов является тип воздействия к которому вырабатывается резистентность - рентгеновское излучение.
Известны и другие способы получения радиорезистентных клеток, так в работе Y. Kuwahara et al. (Kuwahara Y, Li L, Baba T, Nakagawa H, Shimura T, Yamamoto Y, Ohkubo Y, Fukumoto M. Clinically relevant radioresistant cells efficiently repair DNA double-strand breaks induced by X-rays. Cancer Sci. 2009 Apr; 100(4):747-52. doi: 10.1111/j.1349-7006.2009.01082.x. Epub 2009 Feb 2), облучение клеток карциномы печени проводили в дозе 0,5 Гр каждые 12 ч в течение более 6 лет; суммарная доза составляла более 1600 Гр. В другом исследовании (Qing, Y. et al. Microarray analysis of DNA damage repair gene expression profiles in cervical cancer cells radioresistant to 252Cf neutron and X-rays / Y. Qing, X.Q. Yang, Z.Y. Zhong, X. Lei, J.Y. Xie, M.X. Li, D.B. Xiang, Z.P. Li, Z.Z. Yang, G. Wang, D. Wang // BMC Cancer. 2010) для получения двух радиорезистентных клеток линии HeLa в течение 8 месяцев подвергали их непрерывному сублетальному облучению общей дозой 75 Гр с помощью нейтронного излучения 252Cf и рентгеновского излучения. Так же известно исследование, где в режиме фракционирования с дозой 2 Гр в день и 5 дней в неделю в течение 7 месяцев получали резистентные клетки (Wei, K. et al. Radioresistant cell strain of human fibrosarcoma cells obtained after long-term exposure to x-rays / K. Wei, R Kodym., J. Cui-Zheng // Radiat Environ Biophys. 1998. N. 37. P. 133-137).
Среди недостатков данных методов не только тип воздействия к которому вырабатывается резистентность, но и большие временные затраты для достижения результата.
Наиболее близким к заявляемому изобретению - прототипом, является способ предложенный K. Sato и др., где для выработки резистентных клонов использовали клетки плоскоклеочной карциномы NR-S1, которые облучали рентгеновским излучением в дозе 10 Гр 1 раз в две недели (6 Гр⋅экв в неделю) до суммарной дозы 60 Гр (72 Гр⋅экв). После окончательного облучения клетки культивировали в течение 4 недель до тестирующего воздействия рентгеновским излучением и ионами углерода (Sato, K. et al. Heterochromatin domain number correlates with X-ray and carbon-ion radiation resistance in cancer cells / K. Sato, T. Imai, R. Okayasu, T. Shimokawa // Radiation Research. 2014).
Как и в случае выше описанных подходов недостатком данного способа является факт выработки резистентности к ионам углерода. Указанный вид воздействия, так же как и протоны относится к тяжелым заряженным частицам, но обладает значительно более высоким значением относительной биологической эффективности, что не позволяет считать данные для ионов углерода, пригодными для прогнозирования биологических эффектов облучения протонами.
В результате поиска по источникам патентной и научно-технической информации не выявлено сведений о способе формирования радиорезистентной культуре опухолевых клеток, аналогичной заявляемой.
Технический результат направлен на создание культуры клеток с резистентностью к протонам, сформированной длительным фракционированным облучением протонами.
Указанный технический результат при осуществлении изобретения достигается за счет того, что также как и в известном способе проводят облучение в дозе 6 Гр⋅экв, с учетом величины относительной биологической эффективности.
Особенность заявляемого способа заключается в том, что культуру клеток подвергают облучению электронами 1 раз в неделю до суммарной дозы 60 Гр или протонами 1 раз в неделю до суммарной дозы 70 Гр (84 Гр⋅экв).
Изобретение поясняется подробным описанием, примерами исполнения и иллюстрациями, на которых изображено:
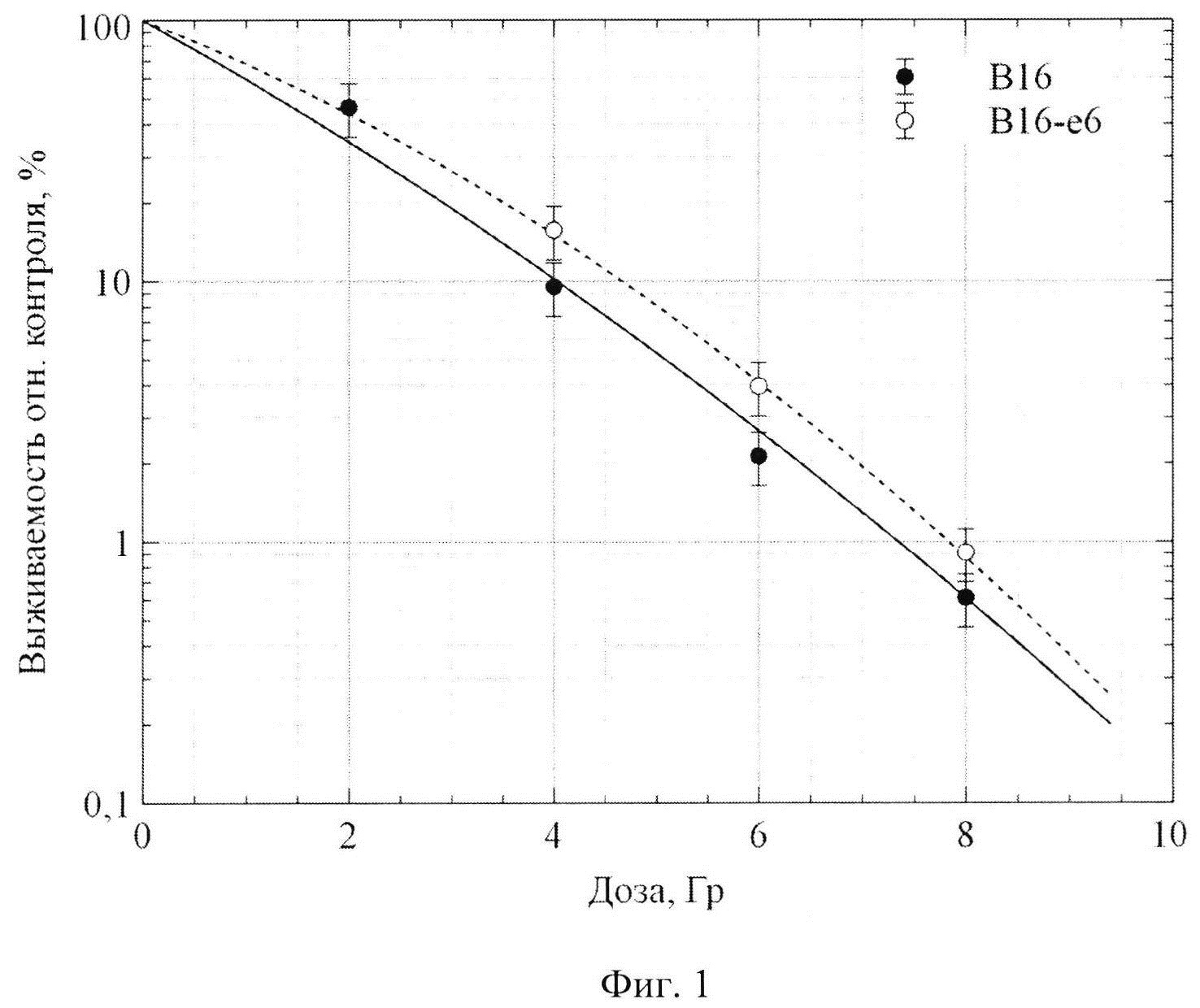
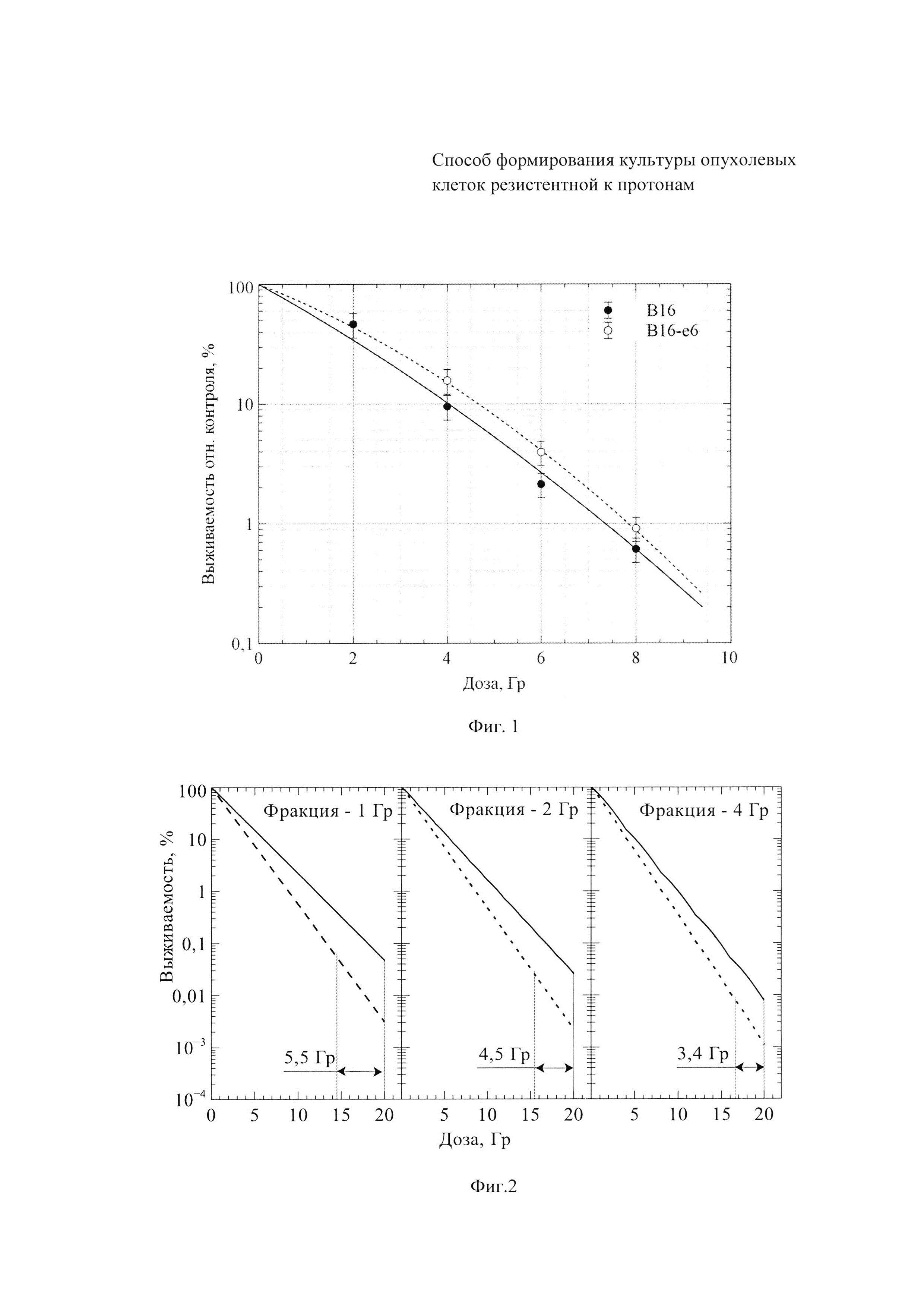
Фиг. 1 - Зависимость выживаемости клеток В16 после облучения протонами: В16 - родительская культура клеток; В16-е6 - сублиния, подвергнутая предварительному фракционированному облучению электронами.
Фиг. 2 - Моделирование облучения фракциями по 1, 2 и 4 Гр на основе полученных данных для родительской линии В-16 (пунктирная линия, «p») и ее радиорезистентной сублинии (сплошная линия, «e6-p»).
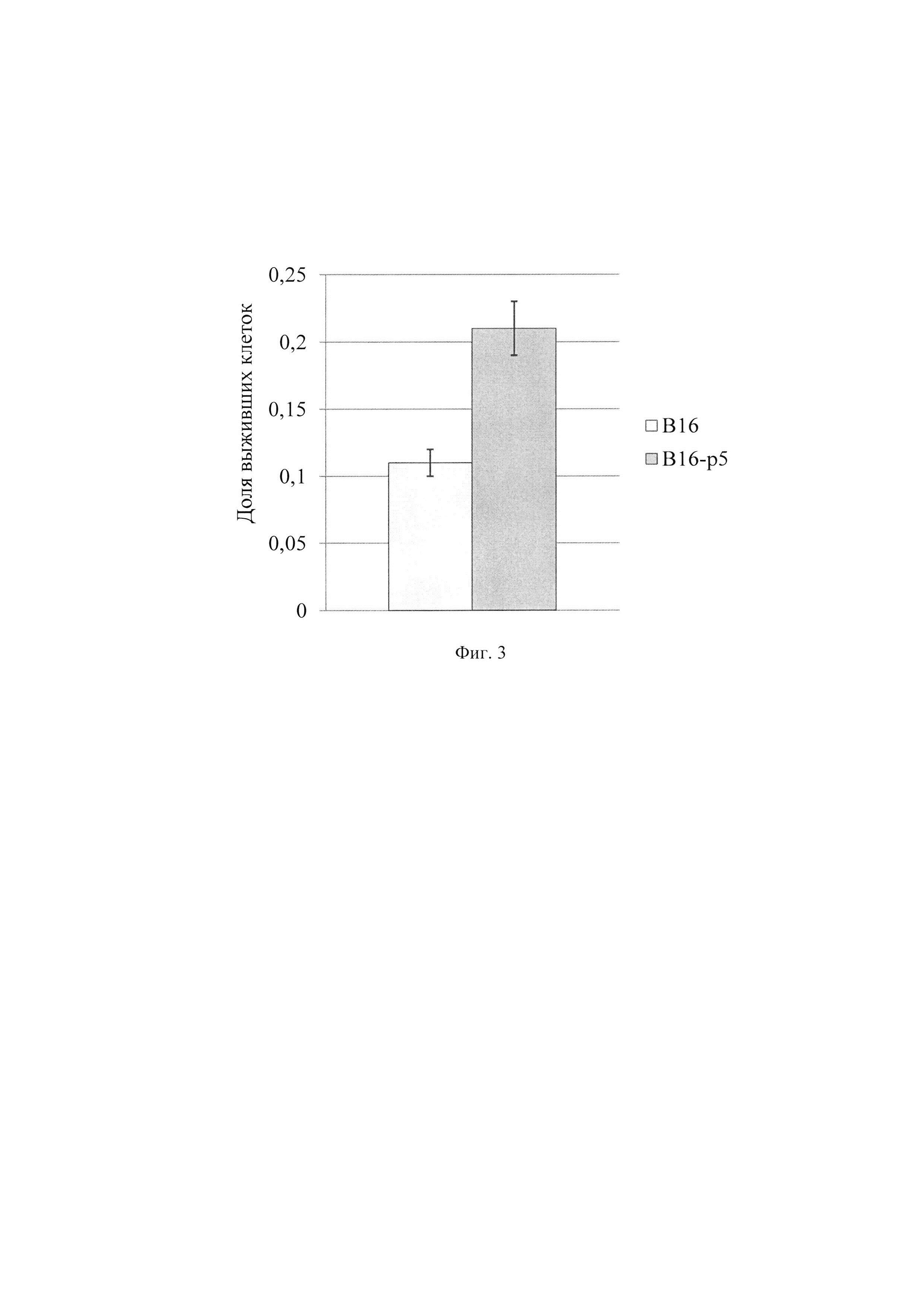
Фиг. 3 - Выживаемость клеток родительской линии и резистентных клонов при воздействии тестирующего облучения в дозе 4 Гр: белый столбик - родительские клетки, серый - резистентная к протонам сублиния.
Способ осуществляют следующим образом.
Культуру клеток мышиной меланомы В16 подвергают облучению электронами в разовой дозе (РОД) 6 Гр (1 раз в неделю) до суммарной дозы (СОД) 60 Гр или протонами в дозе 5 Гр (1 раз в неделю) суммарной дозы 70 Гр. В день облучения клетки снимают с пластика смесью растворов версена (0,02%) и трипсина (0,25%) в соотношении 1:1, ресуспендируют в среде RPMI-1640, содержащей 10% сыворотки, до получения одиночных клеток. Для облучения клеточную суспензию разливают в микроцентрифужные пробирки типа Эппендорф объемом 1,5 мл (Genfollower, Китай) по 1,3 мл. После облучения клетки подсчитывают в камере Горяева (Минимед, Россия) и высевают в количестве 200 тысяч на чашку Петри диаметром 35 мм (Corning, США). Пересев клеток и замена среды осуществляют при достижении плотности монослоя 90%. Между облучениями клетки культивируют в монослое в чашках Петри диаметром 35 мм (Corning, США) в среде RPMI-1640 (ПанЭко, Россия) с добавлением 10% эмбриональной телячьей сыворотки (Biosera, Франция) и гентамицина в количестве 0,01 мг/мл среды в СО2-инкубаторе (МСО-5АС, Sanyo, Япония) при температуре +37°C и 5% содержании CO2.
Выявленный эффект приобретенной опухолевыми клетками радиорезистентности к протонам может иметь ключевое значение в лучевой терапии с применением этого излучения. Это можно показать моделированием ответа клеток на большое количество фракций на основании кривых, представленных на Фиг. 1. При этом дозовая зависимость состоит из отдельных участков длиной в величину разовой дозы сеанса лучевой терапии. Моделирование для разовых доз 1, 2 и 4 Гр до суммарной дозы 20 Гр (20, 10 и 5 фракций соответственно) (Фиг. 2). Наибольшее отличие наблюдается при фракции в 1 Гр и составляет 5,5 Гр. С увеличением дозы за фракцию (переход к гипофракционированию) разница в эффективности воздействия уменьшается. Таким образом, даже незначительное (но статистически значимое) отклонение дозовой зависимости (при однократном облучении) ранее облученных клеток от кривой для исходных клеток может привести к значительному снижению эффективности облучения при фракционированном воздействии, принятом в лучевой терапии.
Предлагаемый способ подтверждается конкретными примерами использования.
Пример 1. После последнего фракционированного облучения клетки культивировали в течение двух недель. Затем проводили исследование радиочувствительности клеток получивших суммарную дозу электронов 60 Гр к действию протонного излучения методом клоногенной активности. Дозы тестирующего облучения протонами составили 4, 6, 8 Гр. До и после облучения клетки находились на льду. Сравнение проводили с родительской линией, клетки которой облучали теми же излучениями без предварительного воздействия. По результатам исследования был построен график зависимости выживаемости клеток В16 после облучения протонами (Фиг. 1) из которого видно, что кривая выживаемости после облучения протонами располагается ниже кривой выживаемости, где клетки были подвергнуты фракционированному облучению электронами. Применение парного критерия Стьюдента позволило судить о наличии статистически значимого различия в отклике на облучения двух сублиний В16 (Р<0.05).
Пример 2. После окончания фракционированного облучения протонами в суммарное дозе 70 Гр клетки культивировали в течение двух недель по стандартной методике. Затем проводили исследование радиочувствительности клеток к действию протонного излучения методом клоногенной активности. Доза тестирующего воздействия составила 4 Гр. Согласно представленным результатам (Фиг. 3) и данным применения критерия Стьюдента, клетки подверженные длительному фракционированному облучению протонами приобрели резистентность к последующему воздействию протонами.
Таким образом, предложенный способ позволяет эффективно получать резистентную клеточную культуру клеток, преимущество которой заключается в ее устойчивости к воздействию протонного излучения.
Полученная культура клеток может быть использована для проведения сравнительных радиобиологических исследований, направленных на выяснение и уточнение механизмов клеточной радиорезистентности, скрининг противоопухолевых препаратов в аспекте их применения в схемах химиолучевой терапии и на разработку эффективных схем лечения пациентов с рецидивами и метастазами, возникшими после ранее проведенного (неэффективного) курса лучевой терапии.
Способ формирования культуры опухолевых клеток, резистентной к протонам, включающий облучение в дозе 6 Гр⋅экв, с учетом величины относительной биологической эффективности, отличающийся тем, что культуру клеток подвергают облучению электронами 1 раз в неделю до суммарной дозы 60 Гр или протонами 1 раз в неделю до суммарной дозы 70 Гр (84 Гр⋅экв).