Результат интеллектуальной деятельности: МикроРНК-124 В КАЧЕСТВЕ БИОМАРКЕРА
Вид РИД
Изобретение
Настоящее изобретение относится к области биомаркеров, в частности, связанных с вирусными инфекциями.
В частности, изобретение относится к новому биомаркеру, пригодному к применению в качестве диагностического маркера для вирусных инфекций. Вирусные инфекции, в частности рассматриваемые, представляют собой вирусные инфекции, требующие сплайсинга РНК и, в частности, ретровирусные инфекции, такие как ВИЧ и СПИД-ассоциированные состояния. Изобретение также относится к сопутствующему маркеру для лечения указанных инфекций, и, в частности, ВИЧ и СПИД-ассоциированных состояний.
У высших эукариот матричные РНК не транскрибируются напрямую в их функциональную форму, а транскрибируются в виде пре-матричных РНК, которые должны претерпеть различный процессинг с целью стать приемлемыми к прочтению трансляционным аппаратом клетки. Сплайсинг представляет собой процесс, позволяющий элиминировать нежелательные последовательности (интроны) и соединить значимые последовательности (экзоны). Высоко скоординированные операции сплайсинга происходят в большом комплексе, называемом сплайсосомой. Образование данного функционального мегакомплекса представляет собой организованную систему из белков и РНК, которая требует идентификации экзон-интронных стыков. Экзоны регулярно подвергаются альтернативному сплайсингу, что означает, что они или включаются или исключаются из конечного транскрипта зрелой мРНК. В результате недавних крупных исследований по секвенированию оказалось, что более чем 90% генов подвергаются альтернативному сплайсингу. Продуцирование альтернативно сплайсированных мРНК регулируется системой действующих в трансположении белков, которые связываются с действующими в цис-положении сайтами на пре-мРНК. Такие белки включают активаторы сплайсинга, которые обеспечивают использование конкретного сайта сплайсинга, и репрессоров сплайсинга, которые уменьшают использование конкретного сайта, связывание на сайтах для энхансеров сплайсинга (энхансеры сплайсинга интронов, ISE, и энхансеры сплайсинга экзонов, ESE) и на сайтах ослабителей сплайсинга (ослабители сплайсинга интронов, ISS, и ослабители сплайсинга экзонов, ISS) соответственно.
Вирусы, в частности из семейства ретровирусов, являются основной причиной заболеваний в мире. Три подсемейства могут быть выделены внутри семейства ретровирусов: онковирусы, лентивирусы и спумавирусы.
Онковирусы названы так, поскольку они могут быть ассоциированы с раком и злокачественными инфекциями. Здесь могут быть упомянуты, например, вирусы возбудителя лейкоза (такие как вирус птичьей лейкемии (ALV), вирус мышиной лейкемии (MULV), также называемый вирусом Молони, вирус кошачьей лейкемии (FELV), вирусы лейкемии человека, такие как HTLV1 и HTLV2, вирус лейкемии обезьян или STLV, вирус коровьего лейкоза или BLV, онковирусы приматов типа D, онковирусы типа В, которые индуцируют опухоли молочных желез, или онковирусы, вызывающие быстрый рак (такой как вирус саркомы Рауса или RSV).
Спумавирусы проявляют относительно низкую специфичность к данному типу клеток и к данным видам, и они иногда ассоциированы с иммуносупрессивными явлениями; например, в случае вируса пенистости обезьян (или SFV).
Лентивирусы, такие как ВИЧ, названы таким образом из-за способности вызывать медленно прогрессирующие патологические состояния, которые очень часто включают иммуносупрессивные явления, включая СПИД.
Вирусы и, в частности, ретровирусы, такие как ВИЧ, известны тем, что используют сплайсинг РНК и регуляцию сплайсинга для распространения и распределения внутри клеток и тканей инфицированного индивидуума.
В последнее время факт того, что ВИЧ является ретровирусом, которому необходим сплайсинг РНК для экспрессии ключевых вирусных белков, был использован для разработки нового подхода, основанного на ингибировании сплайсинга для противодействия вирусным инфекциям и, в частности, СПИДу (WO 2010/143169). Более того, геном ВИЧ-1 экспрессирует первичный транскрипт 9 т.п.н., который не только служит в качестве геномной РНК для потомства вируса, но который также генерирует 40 различных мРНК. ВИЧ-1 использует четыре 5' сайта альтернативного сплайсинга и восемь 3' сайтов альтернативного сплайсинга для образования сплайсированных участков мРНК. Данные сплайсированные мРНК могут быть разделены на два класса: многократно сплайсированные (2 т.п.н.) и однократно сплайсированные (4 т.п.н.) РНК. Регуляция альтернативного сплайсинга ВИЧ-1 происходит прежде всего за счет присутствия сайтов субоптимального сплайсинга, которые снижают распознавание клеточным аппаратом сплайсинга сигналов сплайсинга. В дальнейшем сплайсинг в вирусных сайтах сплайсинга регулируется за счет присутствия ESEs, ESSs и ISSs.
В данном контексте, разработаны производные хинолина, в частности, 8-хлор-N-[4-(трифторметокси)фенил]хинолин-2-амин, ингибирующий репликацию в мононуклеарных клетках периферической крови (МКПК) ВИЧ-1 и ВИЧ-2 T-клеточно-тропных лабораторных штаммов, а также клинических изолятов различных подтипов в диапазоне нМ концентраций (WO 2010/143169).
микроРНК (miРНК), наиболее крупная некодирующая группа, представляет собой класс из приблизительно 22 нуклеотидных некодирующих РНК, которые ингибируют экспрессию генов через связывание с нетранслируемым участком (UnTranslated Region, UTR) транскриптов мишеневых мРНК (Lai et al., Nature Genetics, vol. 30, no. 4, pp. 363-364, 2002; Bartel et al., Cell, vol. 136, no. 2, pp. 215-233, 2009). Гены микроРНК составляют приблизительно 1-2% известных геномов эукариот. Расчеты подтверждают, что каждая микроРНК может иметь мишенью более 200 транскриптов и что единственная мРНК может регулироваться при помощи множества микроРНК (LINDOW, DNA Cell Biol., vol. 26(5), p. 339-351, 2007). микроРНК образуются из эндогенных транскриптов в форме шпильки и действуют за счет спаривания оснований с мишеневыми мРНК, что приводит к расщеплению мРНК или репрессии трансляции, в зависимости от степени спаривания оснований. Две операции процессинга приводят к образованию зрелой микроРНК: во-первых, возникающие транскрипты микроРНК (первичная микроРНК) процессируются в 70 нуклеотидные предшественники (пре-микроРНК), которые экспортируются из ядра и расщепляются в цитоплазме с образованием коротких (приблизительно 22 нуклеотида в длину) зрелых микроРНК (LEE, EMBO J., vol. 21, р; 4663-4670, 2002). микроРНК могут быть локализованы межгенно или внутригенно. В случае межгенного расположения их экспрессия скоординирована с другими микроРНК в виде кластера (Altuvia et al., Nucleic Acids Research, vol. 33, no. 8, pp. 2697-2706, 2005, Ozsolak et al., Genes and Development, vol. 22, no. 22, pp. 3172-3183, 2008). В случае внутригенного расположения, а именно, внутри гена, кодирующего белок (фактически исключительно в интронах), они часто экспрессируются с той же мишени, что и хозяйский ген (Liu et al., Cell Research, vol. 18, no. 10, pp. 985-996, 2008, Kim et al., EMBO Journal, vol. 26, no. 3, pp. 775-783, 2007) и на скореллированных уровнях (Baskerville et al., RNA, vol. 11, no. 3, pp. 241-247, 2005).
При вирусных инфекциях микроРНК вовлечены в сложное взаимодействие между хозяином и патогеном и в настоящее время полагают, что они играют основную роль в вирусном патогенезе (NAIR, Trends in Microbiol., vol. 14, p. 169-175, 2006). Более того, вирусы являются облигатными внутриклеточными паразитами, использующими клеточный аппарат для своего выживания и репликации, поэтому эта зависимость делает их чувствительными к механизмам генной регуляции хозяина. Клеточные микроРНК участвуют в противовирусном механизме защиты, но также могут в ряде случаев быть положительными вирусными регуляторами. С другой стороны вирусы сами по себе также могут продуцировать микроРНК для регуляции клеточных процессов или вирусных генов. МикроРНК, вовлеченные в инфекцию, вызванную ВИЧ-1, могут быть определены как ВИЧ-1-кодируемые или кодируемые хозяином соответственно их источнику биогенеза; они также могут быть определены в качестве супрессоров или активаторов инфекции согласно их функции. Кроме того они могут быть подразделены согласно тому будут ли они взаимодействовать напрямую с транскриптами ВИЧ-1 или оказывать непрямое влияние на ВИЧ-1 за счет нацеливания на факторы хозяина, вовлеченные в жизненный цикл вируса, или нацеливания на как РНК-генома ВИЧ-1, так и на факторы хозяина, необходимые для инфекции ВИЧ-1. Ряд данных подтверждает, что инфекция ВИЧ-1 оказывает влияние на микроРНК путь в целом за счет нарушения биогенеза микроРНК, но также отдельно за счет модификации профилей экспрессии микроРНК (Houzet et al., Biochim Biophys Acta. 2011 Nov-Dec; 1809(11-12): 686-693)). Более того, хозяйские микроРНК описаны в отношении регуляции ВИЧ-1.
Одним из ключевых факторов для успешной разработки данного лекарственного средства или вакцины является возможность быстрой и эффективной оценки его эффективности. Более того, для данного лекарственного средства или вакцины важно быть введенным в их терапевтическом окне для того, чтобы избежать нежелательных эффектов вследствие слишком высоких доз, или избежать потери эффективности вследствие слишком низких доз. Также необходимо быть уверенным, что соответствующее лекарственное средство или вакцину вводят соответствующему пациенту, и что данный пациент действительно чувствителен к лекарственному средству или вакцине. Таким образом, простое сочетание данного пациента и данного лекарственного средства или вакцины не всегда достаточно для получения благоприятного терапевтического эффекта. Поэтому критично наличие соответствующих средств, таких как специфические биомаркеры для надежной оценки эффективности лекарственного средства или вакцины.
Таким образом, существует необходимость в новом и чувствительном инструменте для оценки вирусной инфекции и, в частности, ретровирусной инфекции и в особенности инфекции ВИЧ (вирус иммунодефицита человека), а также эффективности лечения подобных состояний.
Существует потребность в новом биомаркере для оценки эффективности лечения вирусной инфекции, и, в частности, ретровирусной инфекции, и в особенности инфекции ВИЧ.
Существует потребность в новом и чувствительном инструменте для оценки эффективности производных хинолина, которые являются ингибиторами вирусов, в частности, таких как ВИЧ, и в особенности ВИЧ-1 и ВИЧ-2.
Существует потребность в новом биомаркере для оценки чувствительности пациента к производным хинолина для предупреждения или лечения вирусной инфекции, и, в частности, ретровирусной инфекции и в особенности ВИЧ-инфекции.
Существует также потребность в новом биомаркере для оценки терапевтической эффективности производных хинолина для предупреждения или лечения вирусной инфекции, и, в частности, ретровирусной инфекции, и в особенности ВИЧ-инфекции.
Существует потребность в новом биомаркере для скрининга лекарственных средств-кандидатов или вакцины, эффективных в отношении предупреждения и/или лечения вирусной инфекции, и в особенности ВИЧ-инфекции.
Целью настоящего изобретения является удовлетворение этих потребностей.
Согласно одной из целей, изобретение относится к применению по меньшей мере одной микроРНК, причем указанная по меньшей мере одна микроРНК представляет собой miR-124, в качестве биомаркера вирусной инфекции или эффективности терапевтического лечения указанной вирусной инфекции.
Неожиданно авторы изобретения наблюдали, как подробно описано в примерах ниже, что в МКПК, инфицированных штаммом ВИЧ, в частности, штаммом ADA-M R5, уровень экспрессии miR-124 снижен относительно неинфицированных МКПК.
Кроме того, авторы изобретения неожиданно наблюдали, что лечение производными хинолина, такими как производные хинолина формулы (I) или (II), и в частности 8-хлор-N-[4-(трифторметоксси)фенил]хинолин-2-амином, мононуклеарных клеток периферической крови (МКПК), инфицированных штаммами ВИЧ, в частности, ВИЧ ADA-M R5, приводит к удалению вирусов и существенному повышению (13-кратно относительно контроля) экспрессии miR-124. Производные хинолина могут быть выбраны среди соединений, описанных в WO 2010/143169 и в дальнейшем описанных ниже. Соответственно, терапевтическое лечение указанной вирусной инфекции может представлять собой лечение производными хинолина.
Соответственно, miR-124 выявлена в качестве инструмента, иными словами, в качестве биомаркера для мониторинга вирусной инфекции, в частности, ретровирусной инфекции, такой как ВИЧ-инфекция, в частности, у индивидуумов, страдающих от такой инфекции, а также для мониторинга индивидуумов, инфицированных ВИЧ, и для мониторинга таких индивидуумов, получающих лечение противовирусным лекарственным средством, в частности, производными хинолина формулы (I) или (II), как описано ниже, и, в частности, 8-хлор-N-[4-(трифторметокси)фенил]хинолин-2-амином.
Таким образом, за счет мониторинга уровня экспрессии miR-124, можно осуществить и выполнить контроль качества при клинических исследованиях на людях или отслеживать исполнительность больного в отношении приема лекарственного средства или вакцины за счет обеспечения средств для подтверждения того, что пациент получает соответствующее лечение лекарственным средством или вакциной, т.е. в отношении дозы и времени. Биомаркер miR-124 также может быть применен для оптимизации режима дозирования. Таким образом, miR-124 биомаркер может быть применен по отношению к, например, контролю лечения пациента, клиническим исследованиям и исследованиям, основанным на клетках.
Согласно другой своей цели, изобретение относится к применению по меньшей мере одной микроРНК, причем указанная по меньшей мере одна микроРНК представляет собой miR-124, в качестве биомаркера вирусной инфекции, предпочтительно ретро вируса и более предпочтительно, вируса иммунодефицита человека (ВИЧ).
Согласно другой его цели, изобретение относится к применению по меньшей мере одной микроРНК, причем указанная по меньшей мере одна микроРНК представляет собой miR-124, в качестве биомаркера для скрининга лекарственного средства-кандидата или вакцины, предположительно обладающего эффективностью в отношении предупреждения и/или лечения вирусной инфекции, в частности, ретровирусной инфекции и в особенности ВИЧ-инфекции.
Согласно другой его цели, изобретение относится к применению по меньшей мере одной микроРНК, причем указанная по меньшей мере одна микроРНК представляет собой miRNA-124, в качестве биомаркера для оценки биологического эффекта, в частности, фармакологического потенциала соединения-кандидата, для изменения физиологической активности клетки или белка.
В этом отношении, в данном документе показано, что уровень экспрессии miR-124 варьирует при введении различных соединений, относительно которых известно, что они обладают фармакологической активностью. Таким образом, авторы изобретения показали, что miR-124 включает соответствующий биомаркер потенциальной фармакологической активности соединения-кандидата.
В частности, лекарственное средство-кандидат или вакцина-кандидат, предположительно эффективные в отношении предупреждения и/или лечения вирусной инфекции, могут представлять собой производное хинолина.
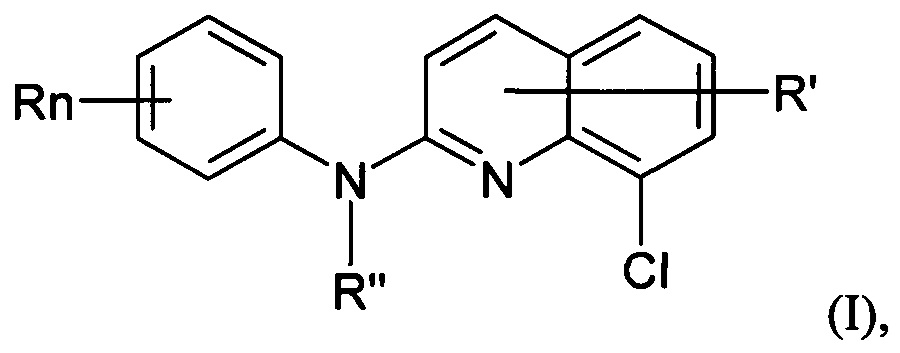
В частности, лекарственное средство-кандидат или вакцина-кандидат, предположительно эффективные в отношении предупреждения и/или лечения вирусной инфекции, могут представлять собой производное хинолина формулы (I):
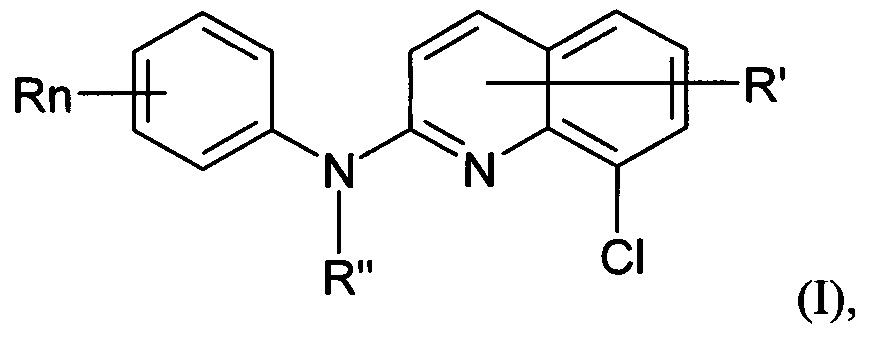
где:
- n представляет собой 1 или 2, и R независимо представляет собой атом водорода, атом галогена или группу, выбранную из (C1-C3)-алкильной группы; -NR1R2 группы, в которой R1 и R2 независимо представляют собой атом водорода или (C1-C3)-алкильную группу; (C1-C3)-фторалкокси группу; -NO2 группу; фенокси группу; и (C1-C4)-алкокси группу,
- R' представляет собой атом водорода, атом галогена или группу, выбранную из (C1-C4)-алкильной группы и (C1-C4)-алкокси группы,
- R'' представляет собой атом водорода или (C1-C4)-алкильную группу,
или одну из его фармацевтически приемлемых солей.
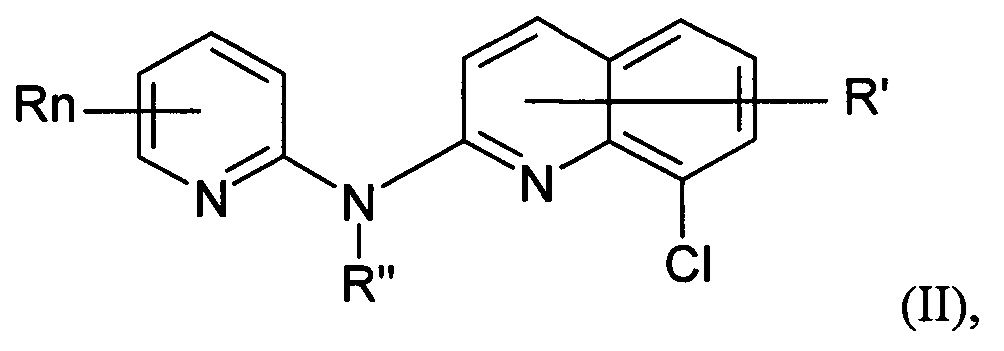
Лекарственное средство-кандидат или вакцина-кандидат, предположительно эффективные в отношении предупреждения и/или лечения вирусной инфекции, также могут представлять собой производное хинолина формулы (II):
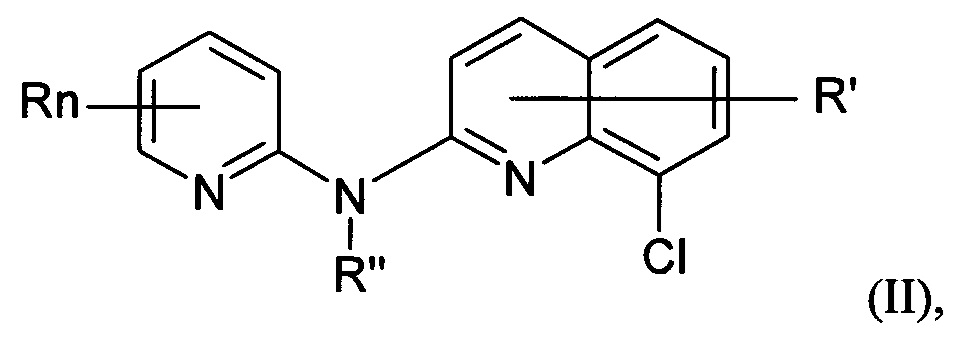
где:
- n представляет собой 1 или 2, и R независимо представляет собой атом водорода, атом галогена или группу, выбранную из (C1-C3)-алкильной группы; -CN группы; гидроксильной группы; -COOR1 группы; (C1-C3)-фторалкильной группы; -NO2 группы; -NR1R2 группы с R1 и R2, представляющими собой атом водорода или (C1-C3)-алкильную группу; и (C1-C4)-алкокси группы,
- R' представляет собой атом водорода, атом галогена или группу, выбранную из (C1-C4)-алкильной группы и (С1-С4)-алкокси группы,
- R'' представляет собой атом водорода или (С1-С4)-алкильную группу,
или одну из его фармацевтически приемлемых солей.
В рамках изобретения, термин «предупреждение» предназначен для обозначения снижения вероятности возникновения данного события, а именно, в контексте изобретения, вирусной инфекции.
Согласно другой его цели, изобретение относится к применению по меньшей мере одной микроРНК, причем указанная по меньшей мере одна микроРНК представляет собой miR-124, в качестве биомаркера активности производного хинолина, или одной из его фармацевтически приемлемых солей, при вирусной инфекции, в частности, ретровирусной инфекции и в особенности ВИЧ-инфекции.
Согласно другой его цели, изобретение относится к применению по меньшей мере одной микроРНК, причем указанная по меньшей мере одна микроРНК представляет собой miR-124, в качестве биомаркера активности производного хинолина формулы (I):
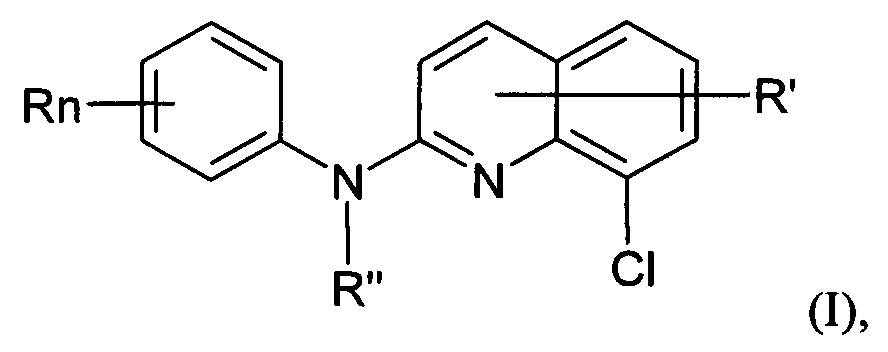
где:
- n представляет собой 1 или 2, и R независимо представляет собой атом водорода, атом галогена или группу, выбранную из (C1-C3)-алкильной группы; -NR1R2-группы, в которой R1 и R2 независимо представляют собой атом водорода или (C1-C3)-алкильную группу; (C1-C3)-фторалкокси группы; -NO2 группы; фенокси группы; и (C1-C4)-алкокси группы,
- R' представляет собой атом водорода, атом галогена или группу, выбранную из (C1-C4)-алкильной группы и (С1-С4)-алкокси группы,
- R'' представляет собой атом водорода или (C1-C4)-алкильную группу,
или одной из его фармацевтически приемлемых солей,
при вирусной инфекции и, в частности, при ретровирусной инфекции и в особенности ВИЧ-инфекции.
Согласно другой его цели изобретение относится к применению по меньшей мере одной микроРНК, причем указанная по меньшей мере одна микроРНК представляет собой miR-124, в качестве биомаркера активности производного хинолина формулы (II):
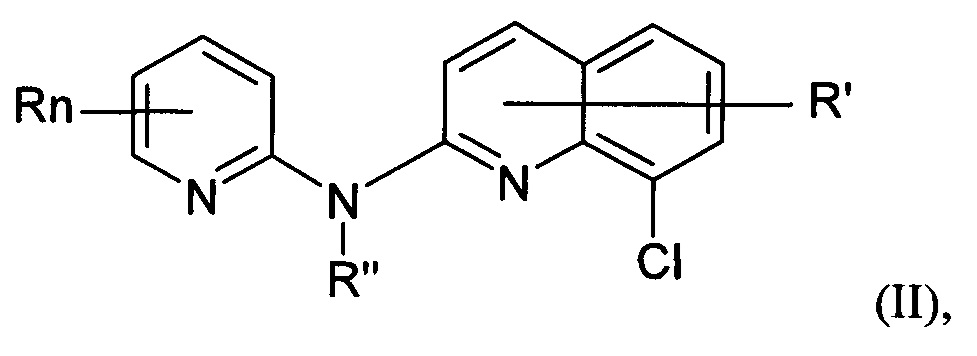
где
- n представляет собой 1 или 2, и R независимо представляет собой атом водорода, атом галогена или группу, выбранную из (C1-C3)-алкильной группы; -CN группы; гидроксильной группы; -COOR1 группы; (C1-C3)фторалкильной группы; -NO2 группы; -NR1R2 группы с R1 и R2, представляющими собой атом водорода или (C1-C3)-алкильную группы; и (C1-С4)-алкокси группы,
- R' представляет собой атом водорода или группу, выбранную из (С1-С4)-алкильной группы и (C1-C4)-алкокси группы,
- R'' представляет собой атом водорода или (C1-C4)-алкильную группу,
или одной из его фармацевтически приемлемых солей,
при вирусной инфекции, в частности, ретровирусной инфекции, и в особенности ВИЧ-инфекции.
Согласно конкретному варианту реализации, производное хинолина согласно изобретению может представлять собой 8-хлор-N-[4-(трифторметокси)фенил]хинолин-2-амин или 8-хлор-N-[4-(трифторметил)пиридин-2-ил]хинолин-2-амин.
Таким образом, согласно другой цели, изобретение относится к применению по меньшей мере одной микроРНК, причем указанная по меньшей мере одна микроРНК представляет собой miR-124, в качестве биомаркера активности производного хинолина, выбранного из:
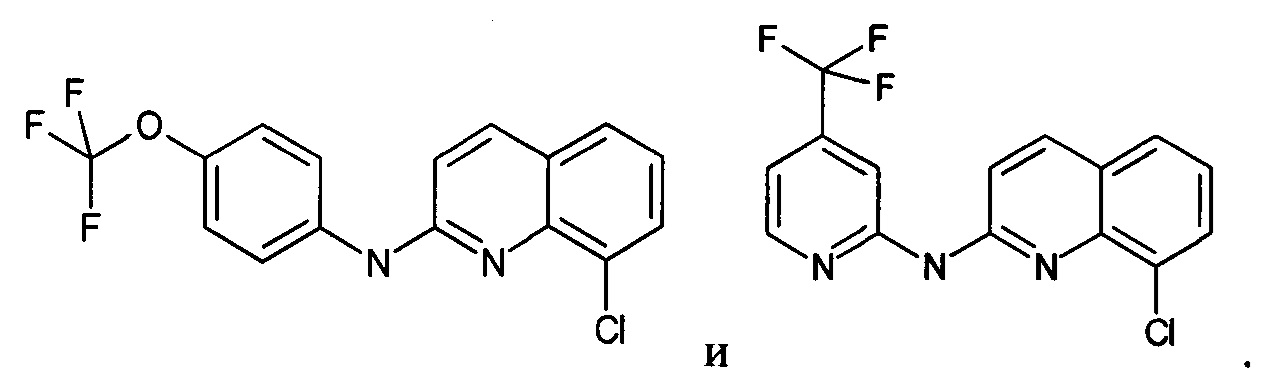
В рамках изобретения выражения «вирусная инфекция» и «инфекция вирусом» относятся к любой вирусной инфекции, и, в частности, к любой ретровирусной инфекции, которая может быть в клетке, ткани, органе или индивидууме, способному к экспрессии биомаркера согласно изобретению. Предпочтительно, ретровирусная инфекция может представлять собой лентивирусную инфекцию, и, в частности, ВИЧ-инфекцию. Индивидуум в рамках изобретения может представлять собой млекопитающее, и предпочтительно, человека, способного к экспрессии биомаркера согласно изобретению. В рамках изобретения термины «индивидуум» и «пациент» применяют взаимозаменяемо.
В рамках изобретения термин «вирус» относится к любому вирусу, в частности, к ретровирусу и предпочтительно лентивирусу, такому как ВИЧ вирус, более предпочтительно, ВИЧ-1 или ВИЧ-2.
Согласно другой цели, изобретение относится к способу оценки вирусной инфекции и, в частности, ретровирусной инфекции, и в особенности ВИЧ-инфекции, у пациента, предположительно инфицированного вирусом, при этом способ оценки включает этапы:
а - измерение присутствия или уровня экспрессии по меньшей мере одной микроРНК, причем указанная по меньшей мере одна микроРНК представляет собой miR-124, в биологическом образце, предварительно полученном от указанного пациента; и
b - сравнение указанного присутствия или уровня экспрессии с контрольным референсным значением,
при этом модулированное присутствие или уровень экспрессии указанной микроРНК относительно указанного контрольного референсного значения является показателем инфекции.
Согласно другой цели, изобретение относится к способу оценки активности производного хинолина формулы (I) для предупреждения и/или лечения вирусной инфекции, в частности, ретровирусной инфекции, и в особенности ВИЧ-инфекции, у пациента, получающего лечение указанным производным хинолина, содержащему по меньшей мере этапы:
а - измерение присутствия или уровня экспрессии по меньшей мере одной микроРНК, причем указанная по меньшей мере одна микроРНК представляет собой miR-124, в первом биологическом образце, предварительно полученном от пациента до введения указанного производного хинолина, и во втором биологическом образце, полученном предварительно от указанного пациента после введения указанного производного хинолина; и
b - определение того, являются ли указанное присутствие или уровень экспрессии модулированным во втором биологическом образце, полученном после лечения, по сравнению со вторым биологическим образцом, полученным до лечения;
при этом модулированное присутствие или уровень экспрессии указанной микроРНК является показателем активности указанного производного хинолина.
«Биологический образец», как использовано в данном документе, обычно относится к образцу, полученному от биологического субъекта, включая образец биологической ткани или жидкости, полученный или собранный in vivo или in situ. Такие образцы могут представлять собой, но не ограничиваясь, органы, ткани, фракции и клетки, выделенные от млекопитающего. Примеры биологических образцов, включают, но не ограничены ими, клеточный лизат, клеточную культуру, клеточную линию, ткань, ткань ротовой полости, желудочно-кишечную ткань, орган, органеллу, биологическую жидкость, образец крови, образец сыворотки, образец мочи, образец кожи, и т.п. Предпочтительные биологические образцы включают, но не ограничены, образцы крови, плазмы, сыворотки, МКПК, тканевые биоптаты, слизистую ротовой полости, слюны, интерстициальную жидкость, или образец мочи и т.п.
В одном варианте реализации биологический образец, приемлемый для изобретения, может быть выбран из группы, состоящей из образца биологической ткани, образца цельной крови, мазков, образца плазмы, образца сыворотки, образца слюны, образца вагинальной жидкости, образца спермы, образца фарингеальной жидкости, образца бронхиальной жидкости, образца фекальной жидкости, образца цереброспинальной жидкости, образца слезной жидкости и образца супернатанта культуры ткани.
Изобретение дополнительно относится к выделенному биологическому образцу, содержащему биомаркер, причем указанный биологический образец выбран из группы, состоящей из образца ткани, образца крови, мазка, плазмы, сыворотки, слюны, вагинальной жидкости, спермы, фарингеальной жидкости, бронхиальной жидкости, фекальной жидкости, цереброспинальной жидкости, слезной жидкости и супернатанта культуры ткани; при этом указанный биомаркер представляет собой микроРНК биомаркер, и предпочтительно miR-124.
Согласно другим целям, изобретение относится к способу оценки биологического эффекта соединения-кандидата и, в частности, к скринингу лекарственного средства-кандидата или вакцины-кандидата, предположительно эффективных при предупреждении и/или лечении вирусной инфекции, и, в частности, ретровирусной инфекции и в особенности ВИЧ-инфекции, включающему по меньшей мере этапы:
а - обработка по меньшей мере одной изолированной клетки, способной экспрессировать по меньшей мере одну микроРНК, причем указанная по меньшей мере одна микроРНК представляет собой miR-124, указанным кандидатом, при этом указанная клетка находится в условиях, приемлемых для экспрессии указанной по меньшей мере одной микроРНК,
b - измерение присутствия или уровня экспрессии указанной по меньшей мере одной микроРНК,
с - сравнение указанного измеренного присутствия или уровня экспрессии с измерением или уровнем экспрессии указанной по меньшей мере одной микроРНК в необработанной изолированной клетке,
причем модулированное присутствие или уровень экспрессии указанной микроРНК является показателем биологического эффекта соединения-кандидата и, в частности, эффективности указанного лекарственного средства-кандидата или вакцины-кандидата при вирусной инфекции.
В рамках изобретения термины «модуляция» и «модулированное присутствие или уровень экспрессии» предназначены для обозначения того, является ли «присутствие или уровень экспрессии» биомаркера согласно изобретению индуцированным или повышенным или альтернативно су премированным или пониженным.
Таким образом, из результатов экспериментов, приведенных в данном документе, следует, что miR-124, и, в частности, уровень экспрессии miR-124, включает соответствующий биомаркер, что является показателем физиологических изменений белка и клетки, включая метаболическое изменение клетки, изменение которого означает благоприятный фармакологический эффект.
Затем, как указано ранее, изобретение также относится к применению по меньшей мере одной микроРНК, причем указанная по меньшей мере одна микроРНК представляет собой miRNA-124, для оценки биологического эффекта, в частности, фармакологического эффекта или соединения-кандидата.
Данное изобретение также относится к применению по меньшей мере одной микроРНК, причем указанная по меньшей мере одна микроРНК представляет собой miRNA-124, для оценки способности соединения-кандидата изменять физиологическую активность белка или клетки.
Специалист в области техники может легко определить изменение физиологической активности белка или клетки за счет идентификации любого обнаруживаемого изменения при измерении физиологического параметра клетки, включая измерение метаболического параметра клетки, который охватывает электрофизиологические изменения, изменения проницаемости клеточной мембраны, изменения ферментативной активности, изменения экспрессии белка, изменения экспрессии микроРНК, изменения генной экспрессии, внутриклеточные значения pH и т.д.
Термины «определение», «измерение», «оценивание», «оценка» и «исследование», как используется в данном документе, обычно относятся к любой форме измерения и включают определение того, присутствует элемент или нет. Данные термины включают как количественные, так и/или качественные определения. Оценка может быть относительной или абсолютной. Фраза «оценка присутствия» может включать определение количества присутствия чего-либо, а также определение присутствия или отсутствия чего-либо.
Согласно одному предпочтительному варианту реализации, при оценке вирусной инфекции, наблюдение пониженного или супрессированного присутствия, или пониженного уровня экспрессии, указанной микроРНК относительно контрольного референсного значения, может быть показателем вирусной инфекции.
Согласно одному предпочтительному варианту реализации, при оценке активности производного хинолина формулы (I) для лечения вирусной инфекции или при скрининге лекарственного средства-кандидата или вакцины-кандидата, предположительно эффективных при предупреждении и/или лечении вирусной инфекции, наблюдение индуцированного или повышенного присутствия, или повышенного уровня экспрессии, указанной микроРНК относительно контрольного референсного значения, может быть показателем активности производного хинолина формулы (I) или эффективности указанного лекарственного средства-кандидата или вакцины-кандидата.
Согласно предпочтительному варианту реализации применение и способы согласно изобретению осуществляют in vitro или ex vivo.
Согласно другим целям, изобретение относится к выделенному нуклеиновокислотному зонду, способному к специфичной гибридизации с miR-124, в качестве диагностического агента для измерения присутствия или уровня экспрессии miR-124 для диагностики вирусной инфекции, в частности, ретровирусной инфекции и в особенности ВИЧ-инфекции, или для оценки активности лекарственного средства-кандидата или вакцины-кандидата, предположительно эффективных для предупреждения и/или лечения вирусной инфекции, в частности, ретровирусной инфекции, в особенности ВИЧ-инфекции.
Термин «зонд», как употреблено в данном документе, обычно относится к агенту захвата, который направлен на специфическую последовательность мишеневой биомаркерной микроРНК. Соответственно, каждый зонд из набора зондов обладает соответствующим мишеневым микроРНК биомаркером. Дуплекс зонд/мишень микроРНК представляет собой структуру, образованную за счет гибридизации зонда с ее мишеневым микроРНК биомаркером.
Выделенный нуклеиновокислотный зонд согласно изобретению предпочтительно может представлять собой нуклеиновокислотный зонд, состоящий из нуклеотидной последовательности, выбранной из группы, состоящей из последовательностей от SEQ ID NO: 6 до SEQ ID NO: 87.
Согласно одному из преимуществ, изобретение предлагает пригодный и надежный биомаркер для контроля пациентов, инфицированных вирусом, предпочтительно ретровирусом и более предпочтительно ВИЧ-вирусом.
Согласно одному из его преимуществ изобретение предлагает полезный и надежный биомаркер для контроля пациентов, инфицированных вирусом, предпочтительно ретровирусом, и, более предпочтительно, ВИЧ-вирусом, и получающих лечение производным хинолина формулы (I).
Согласно другим преимуществам, изобретение предлагает чувствительный и надежный биомаркер, который можно легко использовать у постели пациента.
Применения и способы
Согласно одному варианту реализации, применение и способы согласно изобретению, в частности, позволяют определить вирусную инфекцию у пациента и, в частности, контролировать такую инфекцию.
Согласно одному варианту реализации, присутствие или уровень экспрессии miR-124 измеряют в выделенном биологическом образце, и затем сравнивают с контрольным референсным значением.
Модуляция присутствия или уровня экспрессии miR-124 относительно контрольного референсного значения может быть показателем вирусной инфекции. В частности, пониженное и супрессированное присутствие или пониженный уровень экспрессии, указанной микроРНК относительно контрольного референсного значения может быть показателем вирусной инфекции.
В одном варианте реализации применение согласно изобретению может содержать получение измеренного уровня экспрессии указанной miR-124 в выделенном биологическом образце и сравнение указанного измеренного уровня экспрессии с контрольным референсным значением. Наблюдение модуляции указанного измеренного уровня относительно указанного контрольного референсного значения может быть показателем вирусной инфекции или эффективности терапевтического лечения указанной вирусной инфекции.
В случае, когда miR-124 из образца «понижена» или «подавлена» в биологическом образце, полученном от пациента, по сравнению с контрольным референсным значением, это снижение может представлять собой, например, приблизительно 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 90%, 100%, 200%, 300%, 500%, 1,000%, 5,000% или более сравнительного контрольного референсного значения (т.е., без лечения производным хинолина).
В частности, измеренный уровень экспрессии miR-124 может быть по меньшей мере двукратно, предпочтительно по меньшей мере четырехкратно, предпочтительно по меньшей мере шестикратно, предпочтительно по меньшей мере восьмикратно и более предпочтительно по меньшей мере десятикратно пониженным относительно указанного контрольного референсного значения.
Согласно одному варианту реализации, применения и способы, использующие miR-124 в качестве биомаркера для вирусной инфекции, и в частности, ретровирусной инфекции и, в особенности, ВИЧ-инфекции, могут быть скомбинированы с определением других биомаркеров, специфичных для указанной инфекции, таких как определение присутствия или уровня экспрессии пептидов, белков или нуклеотидных последовательностей, специфичных для данного вируса. Другие биомаркеры, специфичные для вирусной инфекции, и, в частности, ретровирусной инфекции, и в особенности ВИЧ-инфекции, могут представлять собой, например, белки или нуклеотидные последовательности, кодирующие Tat, gp120 или gp41, или уровень Т4-лимфоцитов.
Биомаркер miR-124 может быть использован для мониторинга или контроля пациента, страдающего от вирусной инфекции, и, в частности, ретровирусной инфекции, и в особенности ВИЧ-инфекции или СПИДа (синдром приобретенного иммунодефицита).
Согласно одному варианту реализации, повышение присутствия или уровня экспрессии miR-124 в биологическом образце, полученном от пациента, страдающего от вирусной инфекции и принимающего лечение от данной инфекции, относительно биологического образца, полученного от того же пациента до инициации указанного лечения, может быть показателем эффективности указанного лечения.
Согласно одному варианту реализации, применение и способы согласно изобретению могут служить для оценки чувствительности пациента к лечению указанными производными хинолина формулы (I).
Согласно другому варианту реализации, применение и способы согласно изобретению могут служить для оценки эффективности лечения указанным производным хинолина формулы (I).
Согласно другому варианту реализации, применение и способы согласно изобретению могут служить для оценки терапевтической эффективности производных хинолина формулы (I) в качестве терапевтического агента для предупреждения и/или лечения вирусной инфекции.
Согласно одному варианту реализации, применение и способы согласно изобретению могут служить для оценки исполнительности больного в отношении лечения производного хинолина формулы (I).
Биомаркер miR-124 может быть использован для мониторинга или контроля активности производных хинолина формулы (I) в течение периода лечения пациента от вирусной инфекции и, в частности от ретровирусной инфекции, и в особенности от ВИЧ-инфекции или СПИДа (синдром приобретенного иммунодефицита).
Способ оценки или мониторинга активности производного хинолина формулы (I) у пациента, получающего лечение производным хинолина, может включать измерение уровня экспрессии miR-124 в выделенном образце, предпочтительно взятых МКПК (мононуклеарные клетки периферической крови), сравнение измеренного уровня экспрессии с уровнем экспрессии miR-124 в выделенном образце, полученном от пациента перед лечением. На основании уровня miR-124 может быть отслежена активность производного хинолина в течение времени.
Согласно одному варианту реализации применение или способ согласно изобретению могут быть использованы для оптимизации режима дозирования для пациента. Пациенты могут по-разному реагировать на вводимое производное хинолина формулы (I), в зависимости от таких факторов как возраст, здоровье, наследственность, наличие других осложнений, прогресс заболевания и совместное введение других лекарственных средств. Это может быть полезно для применения биомаркера miR-124 для оценки и оптимизации режима дозирования, такого как количество дозы и/или режим введения, производного хинолина пациенту. В этом отношении, биомаркер на основе miR-124 также может быть применен для контроля и коррекции эффективности лечения отдельного пациента в течение времени. Биомаркер может быть использован для сбора информации, необходимой для корректировки лечения пациента, повышения или понижения дозы агента по необходимости. Например, пациент, принимающий производное хинолина, может быть изучен при помощи биомаркера на основе miR-124, чтобы увидеть будет ли дозировка эффективной или необходим план более агрессивного лечения. Количество вводимого лекарственного средства, время введения, частота введения, длительность введения затем могут быть скорректированы в зависимости от измерения биомаркера miR-124.
Биомаркер miR-124 также может быть использован для контроля исполнительности больного в период режимов индивидуального лечения или в течение клинических исследований. Это отслеживают в установленных интервалах для уверенности в том, что пациенты, включенные в исследование, принимают лекарственные средства согласно инструкции. Более того, пациент, принимающий производное хинолина, может быть протестирован при помощи биомаркера miR-124 для определения, соблюдает ли пациент режим дозирования согласно плану лечения. Повышенный уровень экспрессии биомаркера по сравнению с таковым необработанного контрольного образца свидетельствует о соблюдении протокола.
Биомаркер согласно изобретению может быть использован для оценки и наблюдения эффективности производных хинолина формулы (I). Соответственно, присутствие или уровень экспрессии miR-124 может быть измерен в выделенном биологическом образце, полученном от пациента, ранее получавшего лечение производным хинолина формулы (I). Затем, измеренное присутствие или уровень экспрессии miR-124 в выделенном биологическом образце можно сравнить с контрольным референсным значением.
В случае, когда наблюдают повышение измеренного уровня относительно контрольного референсного значения, то это измерение является показателем активности указанных производных хинолина формулы (I).
В другом варианте реализации, в случае, когда наблюдают повышение измеренного уровня относительно референсного контрольного значения, это измерение может являться показателем чувствительности пациента к лечению указанными производными хинолина формулы (I).
В другом варианте реализации в случае, когда наблюдают повышение измеренного уровня относительно контрольного референсного значения, то это измерение может быть показателем эффективности лечения указанными производными хинолина формулы (I).
В другом варианте реализации, в случае, когда наблюдают повышение измеренного уровня экспрессии относительно контрольного референсного значения, то это измерение может быть показателем терапевтической эффективности указанных производных хинолина формулы (I) в качестве терапевтического агента для предупреждения и/или лечения вирусной инфекции.
В случае, когда miR-124 из образца «повышена» или «активирована» после лечения производным хинолина, по сравнению с необработанным контрольным референсным значением, данное повышение может составлять, например, приблизительно 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 90%, 100%, 200%, 300%, 500%, 1,000%, 5,000% или более при сравнении с контрольным референсным значением (т.е. без лечения производным хинолина).
В частности, измеренный уровень экспрессии miR-124 может быть по меньшей мере двукратным, предпочтительно по меньшей мере четырехкратным, предпочтительно по меньшей мере шестикратным, предпочтительно по меньшей мере восьмикратным и более предпочтительно по меньшей мере десятикратным повышением относительно указанного контрольного референсного значения.
Согласно другому варианту реализации изобретения, в случае мониторинга вирусной инфекции или оценки эффективности лечения вирусной инфекции, в частности, при помощи производного хинолина формулы (I), пациент может быть протестирован при помощи способа или применения согласно изобретению в интервале времени, выбранном из группы, состоящей из почасового, дважды в день, дважды в неделю, еженедельно, дважды в месяц, ежемесячно, дважды в год и через год. Затем собранные образцы могут быть протестированы немедленно или могут быть сохранены для более позднего исследования.
Согласно другому варианту реализации, применение и способы согласно изобретению, в частности, позволяют проводить скрининг, идентификацию или оценку потенциально активных агентов в качестве лекарственного средства-кандидата.
В частности, применение и способы согласно изобретению являются особенно предпочтительными для скрининга, идентификации или оценки потенциально активных агентов, таких как лекарственное средство-кандидат или вакцина, предположительно эффективные в отношении вирусной инфекции.
Согласно другому варианту реализации изобретения, биомаркер miR-124 может быть использован для скрининга лекарственного средства-кандидата или вакцины-кандидата, предположительно эффективных для предупреждения и/или лечения вирусной инфекции. В таком варианте реализации присутствие или уровень экспрессии miR-124 может быть измерен в выделенном биологическом образце или изолированной клетке, ранее контактировавшей с лекарственным средством или вакциной, подлежащей скринингу. Затем, полученное измерение может быть сравнено с контрольным референсным значением.
В случае, когда наблюдают повышение измеренного уровня в выделенном биологическом образце или изолированной клетке, ранее контактировавшей с соединением-кандидатом, лекарственным средством-кандидатом или вакциной-кандидатом, подлежащим скринингу, относительно контрольного референсного значения, это измерение может быть показателем того, что указанный кандидат имеет биологический эффект, и в частности, может быть эффективен при изменении физиологической активности клетки.
В частности, лекарственное средство-кандидат или вакцина-кандидат могут быть охарактеризованы в качестве эффективных при предупреждении и/или лечении вирусной инфекции, и, в частности ретровирусной инфекции и в особенности ВИЧ-инфекции.
В случае, когда miR-124 в образце «повышена» или «активирована» после лечения лекарственным средством-кандидатом или вакциной-кандидатом по сравнению с необработанным контрольным референсным значением, данное повышение может составлять, например, приблизительно 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 90%, 100%, 200%, 300%, 500%, 1,000%, 5,000% или более при сравнении с контрольным референсным значением (т.е. без лечения производным хинолина).
В частности, измеренный уровень экспрессии miR-124 может быть по меньшей мере двукратным, предпочтительно по меньшей мере четырехкратным, предпочтительно по меньшей мере шестикратным, предпочтительно по меньшей мере восьмикратным и более предпочтительно по меньшей мере десятикратным повышением относительно указанного контрольного референсного значения.
Применение и способы согласно изобретению могут содержать измерение уровня экспрессии miR-124 в выделенном биологическом образце. Любой подходящий для этого образец можно использовать для оценки биомаркера miR-124.
В частности, биологический образец, приемлемый для изобретения, может представлять собой биологическую жидкость, такую как кровь, плазма или сыворотка, слюна, интерстициальная жидкость или образец мочи; клеточный образец, такой как клеточная культура, клеточная линия или образец МКПК, тканевой биоптат, такой как ткань ротовой полости, ткань желудочно-кишечного тракта, образец слизистой рта, или множество образцов из клинического исследования. Образец может быть неочищенным образцом или может быть очищен до различной степени перед хранением, обработкой или измерением.
Этап сбора биологических образцов для применения и способов согласно изобретению проводят до осуществления изобретения, и он не является этапом применения или способа согласно изобретению.
Образцы для оценки miRNA могут быть взяты в течение любых желательных интервалов. Например, образцы могут быть взяты ежечасно, дважды в день, ежедневно, еженедельно, ежемесячно, через месяц, ежегодно или т.п. Образец может быть протестирован немедленно или может быть сохранен для дальнейшего исследования.
Образцы могут быть очищены перед исследованием. В некоторых вариантах реализации, miR-124 может быть выделена из оставшегося содержимого клеток перед исследованием. Более того, молекулы miR-124 могут быть отделены от остальной мРНК в образце, при желании. Например, miR-124 может быть отделена от мРНК на основании различий в размере перед исследованием.
Контрольное референсное значение, подлежащее применению для сравнения измеренного уровня экспрессии miR-124 в тестируемом биологическом образце, получают из контрольного образца.
Контрольные образцы могут быть получены из различных источников. В некоторых вариантах реализации контрольные образцы берут от пациента перед лечением или перед началом заболевания (такой как архивный образец крови). В других вариантах реализации, контрольные образцы отбирают у группы нормальных, небольных членов популяции. В другом варианте реализации, анализ клеток может быть проведен на контрольной клеточной культуре, например, которая не была обработана тестируемым соединением или была обработана референсным соединением, таким как 8-хлор-N-[4-(трифторметокси)фенил]хинолин-2-амин.
Согласно одному варианту реализации, для определения или мониторинга вирусной инфекции у пациента, контрольное референсное значение может быть получено из выделенного биологического образца, полученного от индивидуума или группы индивидуумов, которые, как известно, не страдают от такого состояния.
Согласно другому варианту реализации, для определения или мониторинга эффективности лечения вирусной инфекции у пациента, контрольное референсное значение может быть получено из выделенного биологического образца, полученного от индивидуума или группы индивидуумов, которые, как известно, не страдают от такого состояния и не получают лечения, эффективность которого определяют или отслеживают. Альтернативно, контрольное референсное значение может быть получено из выделенного биологического образца, полученного от пациента, страдающего вирусной инфекцией и получающего лечение, эффективность которого определяют или отслеживают, при этом выделенный биологический образец получают от пациента до введения лечения.
Специалистам в области техники доступны различные методы измерения присутствия или уровня экспрессии биомаркера miR-124.
Например, для оценки присутствия и/или уровня экспрессии miR-124 в образце можно использовать анализы или нуклеотидные чипы.
Последовательность miR-124 может быть применена для получения соответствующего нуклеотида, действующего в качестве комплементарного зонда или праймера, применяемых при различных анализах нуклеиновых кислот для определения экспрессии или присутствия биомаркера miR-124 в образце, такой как, но не ограничиваясь ими, Нозерн-блот и методы на основе ПЦР (например, ПЦР в реальном времени с обратной транскрипцией или РВ-ПЦР). Методы, такие как РВ-ПЦР, могут быть использованы для точной количественной оценки количества miRNA в образце.
Смысловые и антисмысловые зонды или праймеры согласно изобретению могут быть получены при помощи любого способа, известного специалистам в области техники, в частности способов, описанных в Sambrook et al. (Molecular Cloning: A Laboratory Manual, 3rd ED., 2001, Cold Spring Harbour, N.Y.).
Способы, относящиеся к детекции и количественному определению РНК или ДНК, хорошо известны в области техники. Специалисты в области техники могут, например, обратиться к Wang et al. (1989, Proc Natl Acad Sci USA, Vol. 86: 917-921), de Wong et al. (2005, Bio Techniques, Vol. 39 (1): 75-85), de Nolan et al. (2006, Nat Protoc, Vol. 1(3): 1559-1582) et de Klinck et al. (2008, Cancer Research, Vol. 68: 657-663), или также к общему обзору, опубликованному Bustin (2000, Journal of Molecular Endocrinology, Vol. 25: 169-193).
В одном варианте реализации способ детекции и количественной оценки нуклеиновых кислот может представлять собой способ, основанный на флуоресцентном красителе, где концентрацию нуклеиновой кислоты оценивают посредством измерения интенсивности флуоресценции лигандов, таких как красители, которые связываются с указанными нуклеиновыми кислотами. Флуоресцентные красители хорошо известны в области техники.
Альтернативно, указанная нуклеиновая кислота может быть количественно оценена при помощи спектрофотометрии.
В другом варианте реализации способ детекции и количественной оценки нуклеиновых кислот может представлять собой способ на основе гибридизации. Указанные способы на основе гибридизации могут включать методики ПЦР или количественную ПЦР (РВ-ПЦР или к-ПЦР) или методики, основанные на обратной транскриптазе/полимеразе. Предпочтительно указанный способ может включать или может быть дополнительно скомбинирован с этапом секвенирования.
Такие способы могут содержать (i) этап экстракции клеточных мРНК, (ii) этап обратной транскрипции мРНК в ДНК при помощи обратной транскриптазы, и (iii) этап амплификации ДНК с ДНК, полученной на предыдущем этапе. Как правило, начиная с такого же образца, амплифицируют следующие нуклеиновые кислоты: (а) ДНК, полученную после этапа обратной транскрипции мишеневой мРНК, и (b) ДНК или множество ДНК, полученных после обратной транскрипции мРНК, которые непрерывно и постоянно экспрессируются клетками («конститутивные гены»), такие как РНК, кодируемые генами MRPL19, PUM1 и GADPH.
Амплифицированная ДНК может быть количественно оценена после разделения электрофорезом и измерения полос ДНК. Результаты, относящиеся к мишеневой мРНК, выражают в качестве относительных единиц по сравнению с мРНК, кодируемыми «конститутивными генами». В некоторых вариантах реализации этап разделения амплифицированных ДНК проводят после электрофореза в агарозном геле и затем окрашивают полосы ДНК бромистым этидием до количественной оценки ДНК, содержащейся в этих мигрирующих полосах, при помощи денситометрии. В других вариантах реализации можно использовать микроканальное устройство, в котором амплифицированную ДНК отделяют посредством капиллярного электрофореза, до количественного определения испускаемого сигнала при помощи луча лазера. Такое устройство может представлять собой устройство LabChip®, например, из серии «GX», продаваемое компанией Caliper LifeSciences (Хопкинтон, Миннесота, США).
Количественные результаты, полученные при помощи РВ-ПЦР, могут быть иногда более информативны, чем качественные данные и могут упростить стандартизацию исследования и управление качеством. Таким образом, в некоторых вариантах реализации исследования, основанные на РВ-ПЦР, могут быть пригодны для измерения уровней микроРНК в течение периода испытаний, основанных на клетках. Способ РВ-ПЦР также может быть полезен при мониторинге терапии пациента. Коммерчески доступны способы на основе РВ-ПЦР (например, TaqmanR Array™).
Любая приемлемая платформа для исследования может быть применена для определения экспрессии или присутствия микроРНК в образце. Например, исследование может быть в виде экспресс-пробы, мембраны, чипа, диска, испытательной полоски, фильтра, микросферы, слайда, многолуночного планшета или оптического волокна. Система анализа может иметь твердую подложку, на которой прикреплен олигонуклеотид, соответствующий микроРНК. Твердая подложка может содержать, например, пластик, силикон, металл, резину, стекло, мембрану, частицу, преципитат, гель, полимер, слой, сферу, полисахарид, капилляр, пленку, планшет или слайд. Компоненты анализа могут быть получены и упакованы вместе в качестве набора для детекции микроРНК.
В некоторых вариантах реализации олигонуклеотидный чип для тестирования активности производного хинолина или лекарственного средства-кандидата в биологическом образце может быть получен или закуплен. Чип обычно включает твердую подложку и по меньшей мере один олигонуклеотид, контактирующий с подложкой, где олигонуклеотид соответствует по меньшей мере части биомаркера miR-124. В некоторых вариантах реализации часть биомаркера miR-124 содержит по меньшей мере 5, 10, 15, 20 или более оснований.
Согласно одному варианту реализации, присутствие или экспрессия miR-124 может быть оценена в сочетании с другими микроРНК, также применяемыми в качестве биомаркеров. В таком варианте реализации можно использовать анализ для оценки экспрессии или присутствия множества микроРНК в образце, включая miRNA-124. Как правило, способ содержит следующие этапы: а) контактирование образца с областью, содержащей набор зондов, при условиях, достаточных для того, чтобы произошло специфичное связывание; и b) исследование области для детекции присутствия любой детектируемой метки, таким образом, оценивая количество соответствующих мишеневых микроРНК в образце. Применение экспрессионного биочипа делает возможным получение профиля экспрессии микроРНК для данного образца.
Способы получения анализов или чипов для исследования микроРНК хорошо известны в области техники и не нуждаются в дальнейшем описании.
Нуклеотидные чипы могут быть использованы для детекции присутствия или дифференциальной экспрессии микроРНК в биологических образцах. Полинуклеотидные чипы (такие как ДНК или РНК анализы), как правило, включают участки обычно различных по последовательности полинуклеотидов ("агенты захвата"), выстроенных в предварительно определенной конфигурации на подложке. Чипы являются «адресными», поскольку участки (иногда указываемые как «компоненты чипа») обладают различными предварительно определенными локализациями («адресами») на подложке чипа. Участок (т.е. «компонент» или «пятно» чипа) в конкретной предварительно определенной локализации (т.е. «адресе») на чипе будут детектировать конкретные микроРНК мишени. Полинуклеотидные чипы обычно изготавливают на плоских подложках или посредством нанесения заранее полученных полинуклеотидов на подложку сайт-специфичным образом или посредством сайт-специфичного синтеза полинуклеотидов in situ на подложке. Чипы для детекции экспрессии микроРНК могут быть получены при нанесении (например, посредством способов, основанных на контакте или распылении или фотолитографии) или единиц предшественников (таких как нуклеотиды или аминокислотные мономеры) или предварительно синтезированные агенты захвата. После нанесения полинуклеотидных агентов захвата на подложку, подложку, как правило, обрабатывают (например, промывают или блокируют) и хранят перед применением.
Чип для детекции экспрессии микроРНК имеет по меньшей мере две, три, четыре или пять различных целевых зонд. Однако в конкретных вариантах реализации заявленный чип может включать набор зондов, имеющий по меньшей мере 10, по меньшей мере 20, по меньшей мере 50, по меньшей мере 100, по меньшей мере 200, по меньшей мере 500 или по меньшей мере 1000 или более зондов, которые могут детектировать соответствующее число микроРНК. В некоторых вариантах реализации, заявленные чипы могут включать зонды для детекции по меньшей мере части или всех идентифицированных микроРНК организма, или могут включать ортологичные зонды из множества организмов.
Нуклеотидный чип может контактировать с образцом или меченым образцом, содержащим аналиты микроРНК при условиях, которые обеспечивают специфическое связывание микроРНК в образце с одним или более агентами захвата, присутствующими на чипе для проявления наблюдаемого характера связывания. Данный характер связывания может быть обнаружен при анализе чипа. Например, мишеневые микроРНК в образце могут быть мечены с помощью подходящей метки (такой как флуоресцентное соединение) и затем метку можно аккуратно выявить (например, посредством детекции вида флуоресценции) на чипе после контакта чипа с образцом. Наблюдаемый характер связывания может свидетельствовать о присутствии и/или концентрации одного или более компонентов микроРНК образца.
Мечение микроРНК может быть проведено при помощи способов, хорошо известных в области техники, таких как ДНК-лигаза, терминальная трансфераза или мечение цепи РНК и т.д. В некоторых вариантах реализации микроРНК могут быть мечены флуоресцентной меткой. Примеры флуоресцентных красителей включают, но не ограничены, ксантановые красители, флуоресцеиновые красители, родаминовые красители, флуоресцеин изотиоцианат (FITC), 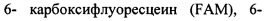
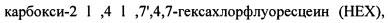
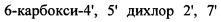
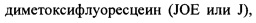 N,N,N',N' тетраметил 6 карбоксиродамин (TAMRA или Т), 6 карбокси X родамин (ROX или R), 5 карбоксиродамин 6G (R6G5 или G5), 6 карбоксиродамин 6G (R6G6 или G6), и родамин 110; цианиновые красители, например, Су3, Су5 и Су7 красители; Alexa красители, например, Alexa-fluor-555; кумарин, диэтиламинокумарин, умбелиферон; бензимидовые красители, например, Hoechst 33258; фенантридиновые красители, например, Texas Red; этидиевые красители; акридиновые красители; карбазольные красители; феноксазиновые красители; порфириновые красители; полиметиновые красители, BODIPY красители, хинолиновые красители, пирен, флуоресцеин хлортриазинил, Rl 10, Eosin, JOE, R6G, тетраметилродамин, лиссамин, ROX, нафтофлуоресцеин, и т.п.
N,N,N',N' тетраметил 6 карбоксиродамин (TAMRA или Т), 6 карбокси X родамин (ROX или R), 5 карбоксиродамин 6G (R6G5 или G5), 6 карбоксиродамин 6G (R6G6 или G6), и родамин 110; цианиновые красители, например, Су3, Су5 и Су7 красители; Alexa красители, например, Alexa-fluor-555; кумарин, диэтиламинокумарин, умбелиферон; бензимидовые красители, например, Hoechst 33258; фенантридиновые красители, например, Texas Red; этидиевые красители; акридиновые красители; карбазольные красители; феноксазиновые красители; порфириновые красители; полиметиновые красители, BODIPY красители, хинолиновые красители, пирен, флуоресцеин хлортриазинил, Rl 10, Eosin, JOE, R6G, тетраметилродамин, лиссамин, ROX, нафтофлуоресцеин, и т.п.
В некоторых вариантах реализации олигонуклеотидный чип для оценки иммуномодулирующей активности может быть получен или закуплен, например, у Affymetrix. Чип может включать твердую подложку и множество олигонуклеотидов, контактирующих с подложкой. Олигонуклеотиды могут присутствовать в специфичной адресной локализации на твердой подложке; каждая соответствует по меньшей мере части последовательностей микроРНК, которые могут быть различно экспрессированы при лечении производным хинолина или лекарственным средством-кандидатом в клетке или пациенте. Последовательности микроРНК содержат по меньшей мере одну последовательность miR-124.
В случае применения чипа для оценки микроРНК, типовой способ может включать этапы 1) получения чипа, контактирующего с поверхностно-связанными целевыми зондами; 2) гибридизации популяции микроРНК с поверхностно-связанными зондами при условиях, достаточных для обеспечения специфичного связывания; (3) постгибридизационные промывки для удаления нуклеиновых кислот, не связавшихся при гибридизации; и (4) детекцию гибридизованных микроРНК. Реагенты, применяемые на каждом из этих этапов, и условия для их применения могут сильно варьировать в зависимости от конкретного применения.
Гибридизация может быть проведена при условиях, жесткость которых при желании может варьировать. Обычные условия достаточны для получения комплексов зонд/мишень на поверхности чипа между комплементарно связанными членами, т.е. между поверхностно-связанными целевыми зондами и комплементарными микроРНК в образце. В конкретных вариантах реализации могут быть применены жесткие условия гибридизации. Гибридизацию обычно проводят при жестких условиях гибридизации. Для гибридизации образца с нуклеотидным чипом применяют стандартные техники гибридизации, хорошо известные в области техники, (например, при условиях достаточных для обеспечения специфичного связывания мишенных микроРНК в образце с зондами на чипе). Выбор соответствующих условий, включая температуру, концентрацию солей, концентрацию полинуклеотида, время гибридизации, жесткость условий промывки, и т.п. будет зависеть от схемы эксперимента, включая источник образца, идентичность агентов захвата, степень ожидаемой комплементарности и т.п. и может быть определен в качестве сущности рутинного эксперимента для специалистов в области техники. В целом, «жесткая гибридизация» и «жесткие условия гибридизационной промывки» в контексте гибридизации нуклеиновой кислоты, как правило, зависят от последовательности и различаются при разных условиях эксперимента. Гибридизация может быть выполнена в течение периода приблизительно 12-24 ч. Жесткость условий промывки может влиять на степень, с которой последовательности мРНК специфично гибридизуются с комплементарными агентами захвата. Специалисты в области техники быстро определят, что альтернативные, но сравнимые условия гибридизации и промывки могут быть применены для обеспечения условий сходной жесткости.
В качестве иллюстрации в одном варианте реализации эксперименты по установлению профиля экспрессии микроРНК могут быть проведены при помощи Affymetrix Genechip miRNA Array 2.0 и согласно протоколам, описанным в инструкции по применению.
В одном конкретном варианте реализации указанная гибридизация может быть выполнена при помощи GeneChip® Hybridization, Wash, and Stain Kit (Affymetrix Ref. #900720). В частности, указанную гибридизацию проводят согласно протоколам производителя.
После процедуры гибридизации микроРНК, полинуклеотиды, связавшиеся с поверхностью чипа, обычно промывают для удаления несвязавшихся нуклеиновых кислот. Промывка может быть выполнена согласно обычному протоколу промывки, где условия промывки обычно являются жесткими, как описано выше. Например, этап промывки может быть выполнен при помощи промывочных буферов, поставляемых компанией Affymetrix (Ref. #900721 and #900722). Гибридизацию мишеневых микроРНК с зондами затем детектируют при помощи стандартных техник считывания чипа. Считывание полученного гибридизованного чипа может быть проведено, например, посредством облучения чипа и считывания локализации и интенсивности полученной флуоресценции в каждом компоненте чипа для детектирования комплексов связывания микроРНК/зонд.
miRNA-124
МикроРНК (miPHK) представляют собой небольшие одноцепочечные некодирующие РНК, которые могут действовать в цитоплазме клетки, вызывая снижение экспрессии их узнаваемых мишеневых матричных РНК или трансляции белкового продукта мРНК. Зрелые микроРНК обычно имеют приблизительно 19-23 нуклеотида в длину. Данная способность микроРНК ингибировать продуцирование их мишеневых белков приводит к регуляции многих типов клеточной активности, таких как предопределение судьбы клеток, апоптоз, дифференциация и онкогенез.
miR-124 изначально была клонирована в мыши. Предшественник miR-124 человека (или miRN-124 или miRNA-124 или микроРНК 124) был клонирован из эмбриональных стволовых клеток. 9 гаплотипов предшественников miR-124 идентифицированы в настоящее время (Guo et al., PLoS ONE, 2009, 4(11):e7944), из которых 3 присутствуют у человека, hsa-miR-124-1, hsa-miR-124-2 и hsa-miR-124-3. (последовательности от SEQ ID NO: 1 до SEQ ID NO: 3).
Предшественник микроРНК miR-124 представляет собой небольшую некодирующую молекулу РНК. Зрелая ~21 нуклеотидная микроРНК процессируется из шпилечной последовательности предшественника за счет дайсер фермента. Зрелые последовательности представляют собой последовательность SEQ ID NO: 4, UAAGGCACGCGGUGAAUGCC для miR-124-3', и последовательность SEQ ID NO: 5, CGUGUUCACAGCGGACCUUGAU для miR-124-5'.
miRNA-124 предпочтительно экспрессируется в мозгу и может способствовать нейрогенезу за счет подавления экспрессии SCP1. Экспрессия miR124 в нервных клетках мыши индуцирует переключение с неспецифического на нейрон-специфичный альтернативный сплайсинг за счет прямого нацеливания мРНК РТВР1. miR-124 повышает численность нейрон-специфичных РТВР2 и Gabbr1 мРНК за счет предотвращения пропуска РТВР1-зависимого экзона, который приводит к промежуточному распаду данных мРНК.
В точке митотического выхода внутри нервной системы позвоночных, когда клетки теряют мультипотентность и начинают образовывать стабильные связи, которые будут существовать всю жизнь, происходит переключение в АТФ-зависимых механизмах ремоделирования хроматина. Данный переход может быть опосредован репрессией BAF53A за счет miR9* (микроРНК, процессированной из противоположного плеча предшественника miR9 стебель-петля) и miR-124.
Экспериментальный аутоиммунный энцефаломиелит (ЕАЕ) является моделью рассеянного склероза на грызунах, характеризующийся воспалением центральной нервной системы (ЦНС), ассоциированным с активацией резидентных макрофагов в ЦНС или микроглии и инфильтрацией периферических иммунных клеток в ЦНС. Обнаружено, что miR-124 высоко экспрессируется в микроглии и нейронах. Экспрессия miR-124 понижена в активированной микроглии в течение эпизода ЕАЕ и в активированной микроглии в культуре. Трансфекция производных miR-124 дезактивирует макрофагов, полученных из костного мозга, и внутривенное введение miR-124 ингибирует развитие поражений и снижает воспаление ЦНС в 3 моделях ЕАЕ на мышах. Обнаружено, что miR-124 обеспечивает неактивность микроглии за счет деактивации макрофагов через путь CEBPA-PU.1.
Также продемонстрировано, что экспрессия miR-124 в фибробластах человека индуцирует их преобразование в нейроны. Дальнейшее добавление нейрогенных транскрипционных факторов ASCL1 и MYT1L повышает скорость преобразования и созревания преобразованных нейронов, несмотря на то, что экспрессия данных транскрипционных факторов без вышеуказанной микроРНК неэффективна.
Выделенный нуклеиновокислотный зонд, подходящий для измерения присутствия или уровня экспрессии miR-124, представляет собой нуклеиновокислотный зонд, способный к специфичной гибридизации с miR-124, такой как предшественник или зрелая miR-124.
Такой нуклеиновокислотный зонд может содержать от 18 до 30 нуклеотидов, в частности 20-27, предпочтительно 20-25, предпочтительно 20, 22, или 25, и более предпочтительно приблизительно 25 нуклеотидов. Как показано ранее, такие нуклеиновокислотные зонды могут быть получены согласно любым известным способам в области техники.
Способы и составы хорошо известны в области техники для подбора оптимальной температуры гибридизации для данного зонда и данной мишени.
Таким образом, специалист в области техники может легко вычислить оптимальную температуру гибридизации на основании набора зондов, для данной мишеневой последовательности и конкретных условий гибридизации.
Предпочтительно, оптимальная температура гибридизации указанных зондов составляет 40°C-60°C, и в частности 45°C-55°C, и предпочтительно составляет приблизительно 48°C.
В качестве примеров буферов, которые можно использовать для гибридизации нуклеиновокислотных зондов согласно изобретению с биомаркером по изобретению, можно указать один буфер в качестве гибридизационного буфера, содержащего 100 мМ MES, 1М [Na+], 20 мМ ЭДТА, 0,01% Tween-20, в качестве нежесткого промывочного буфера, содержащего 6Х SSPE, 0,01% Tween-20, и в качестве жесткого промывочного буфера буфер, содержащий 100 мМ MES, 0,1М [Na+], 0,01% Tween-20.
Нуклеиновокислотный зонд, подходящий для измерения присутствия или уровня экспрессии miR-124, может, например, представлять собой нуклеиновокислотный зонд, представляющий собой нуклеотидную последовательность, выбранную из группы, состоящей из последовательностей от SEQ ID NO: 6 до SEQ ID NO: 87.
Нуклеиновокислотный зонд, приемлемый для измерения присутствия или уровня экспрессии предшественника miR-124-1, может, например, представлять собой нуклеиновокислотный зонд, представляющий собой нуклеотидную последовательность, выбранную из группы, состоящей из последовательностей от SEQ ID NO: 6 до SEQ ID NO: 34, SEQ ID NO 86 и SEQ ID NO 87.
Нуклеиновокислотный зонд, приемлемый для измерения присутствия или уровня экспрессии предшественника miR-124-2, может, например, представлять собой нуклеиновокислотный зонд, представляющий собой нуклеотидную последовательность, выбранную из группы, состоящей из последовательностей от SEQ ID NO: 35 до SEQ ID NO: 65, SEQ ID NO 86 и SEQ ID NO 87.
Нуклеиновокислотный зонд, приемлемый для измерения присутствия или уровня экспрессии предшественника miR-124-3, может, например, представлять собой нуклеиновокислотный зонд, представляющий собой нуклеотидную последовательность, выбранную из группы, состоящей из последовательностей от SEQ ID NO: 66 до SEQ ID NO: 85, SEQ ID NO 86 и SEQ ID NO 87.
Нуклеиновокислотный зонд, приемлемый для измерения присутствия или уровня экспрессии зрелой miR-124, может, например, представлять собой нуклеиновокислотный зонд, представляющий собой нуклеотидную последовательность, выбранную из группы, состоящей из последовательностей SEQ ID NO 86 и SEQ ID NO 87.
Производные хинолина
Производные хинолина, которые можно использовать согласно изобретению, могут представлять собой производные хинолина, эффективные при лечении вирусной инфекции, такие как описано в WO 2010/143169.
В частности, производные хинолина, которые можно использовать согласно изобретению, представляют собой производные хинолина, которые могут быть представлены следующей общей формулой (I):
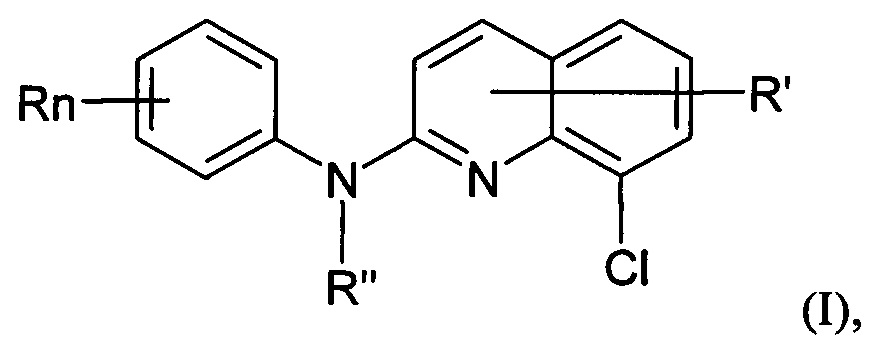
где
- n представляет собой 1 или 2, и R независимо представляет собой атом водорода, атом галогена или группу, выбранную из (C1-C3)-алкильной группы; -NR1R2 группы, в которой R1 и R2 независимо представляют собой атом водорода или (C1-C3)-алкильную группу; (C1-C3)-фторалкокси группы; -NO2 группы; фенокси группы; и (С1-С4) алкокси группы,
- R' представляет собой атом водорода, атом галогена или группу, выбранную из (C1-C4)-алкильной группы и (С1-С4)-алкокси группы,
- R'' представляет собой атом водорода или (С1-С4)-алкильную группу,
или одну из его фармацевтически приемлемых солей.
Согласно одному варианту реализации, R' и R'' предпочтительно представляют собой атом водорода.
Согласно другому варианту реализации, производное хинолина, подходящее для изобретения, может представлять собой соединение формулы (I), в которой R независимо представляет собой атом галогена или группу, выбранную из (C1-C3)-алкильной группы; -NR1R2 группы, в которой R1 и R2 независимо представляют собой атом водорода или (C1-C3)-алкильную группу; (C1-C3)-фторалкильной группы; и (C1-C4)-алкокси группы.
Согласно другому варианту реализации, R независимо представляет собой атом фтора или хлора или группу, выбранную из метальной или этильной группы, -NH2 группы, метокси или этокси группы, и (С1-С3) фторалкокси группы.
Согласно другому варианту реализации, n предпочтительно представляет собой 1.
Согласно предпочтительному варианту реализации, производное хинолина, подходящее для изобретения, может иметь формулу (I), где n представляет собой 1, R представляет собой (С1-С3) фторалкоксигруппу, и каждый из R' и R'' представляет собой атом водорода.
Согласно предпочтительному варианту реализации, R представляет собой метокси, этокси или пропокси группу, замещенную по меньшей мере одним атомом фтора. Предпочтительно, R представляет собой моно, би или трифторметокси группу.
Альтернативно, производные хинолина, подходящие для изобретения, представляют собой производные хинолина, которые могут быть представлены производным хинолина формулы (II):
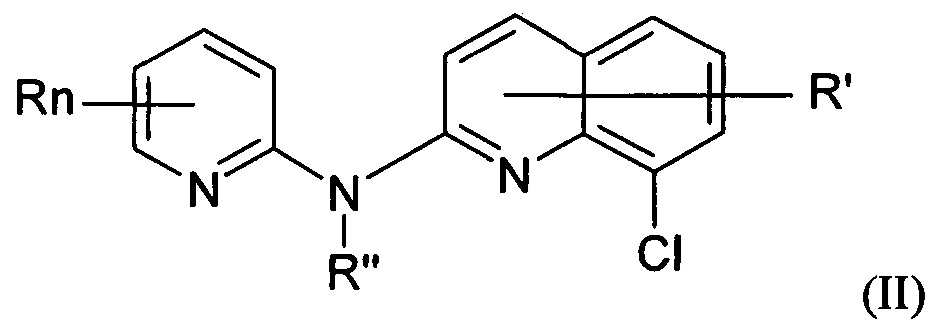
где:
- n представляет собой 1 или 2, и R независимо представляет собой атом водорода, атом галогена или группу, выбранную из (C1-C3)-алкильной группы; -CN группы; гидроксильной группы; -COOR1 группы; (C1-C3)фторалкильной группы; -NO2 группы; -NR1R2 группы с R1 и R2, представляющими собой атом водорода или (C1-C3)алкильную группу; и (C1-C4)-алкокси группы,
- R' представляет собой атом водорода, атом галогена или группу, выбранную из (C1-C4)-алкильной группы и (C1-C4)-алкокси группы,
- R'' представляет собой атом водорода или (C1-C4)-алкильную группу,
или одной из его фармацевтически приемлемых солей.
Согласно одному варианту реализации, производное хинолина, подходящее для изобретения, может иметь формулу (II), в которой R' и R'' предпочтительно представляют собой атом водорода.
Согласно другому варианту реализации, производное хинолина, подходящее для изобретения, может иметь формулу (II), в которой R независимо представляет собой атом водорода, атом галогена или группу, выбранную из (C1-C3)-алкильной группы, (C1-C3)фторалкильной группы, гидроксильной группы, -CN группы, -СООН группы и (C1-C3)-алкокси группы.
Согласно другому варианту реализации, производное хинолина, подходящее для изобретения, может иметь формулу (II), в которой R независимо представляет собой атом водорода, атом галогена, -CN группу, (C1-C3)-алкильную группу, (С1-С3) фторалкильную группу, и гидроксильную группу. Согласно другому варианту реализации, производное хинолина, подходящее для изобретения, может иметь формулу (II), в которой R независимо представляет собой (C1-C3)-фторалкильную группу.
Согласно другому варианту реализации, n предпочтительно представляет собой 1.
Согласно предпочтительному варианту реализации, производное хинолина, подходящее для изобретения, может иметь формулу (II), в которой n представляет собой 1, R представляет собой (C1-C3)фторалкильную группу, и каждый из R' и R'' представляет собой атом водорода.
Таким образом, согласно указанному варианту реализации, производное хинолина может быть представлено следующей формулой:
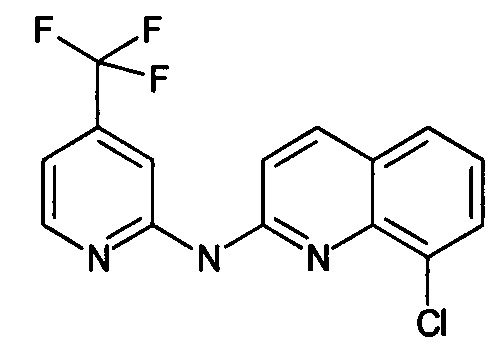
Согласно одному варианту реализации, производное хинолина, подходящее для изобретения, или его соль, могут быть выбраны из группы, состоящей из:
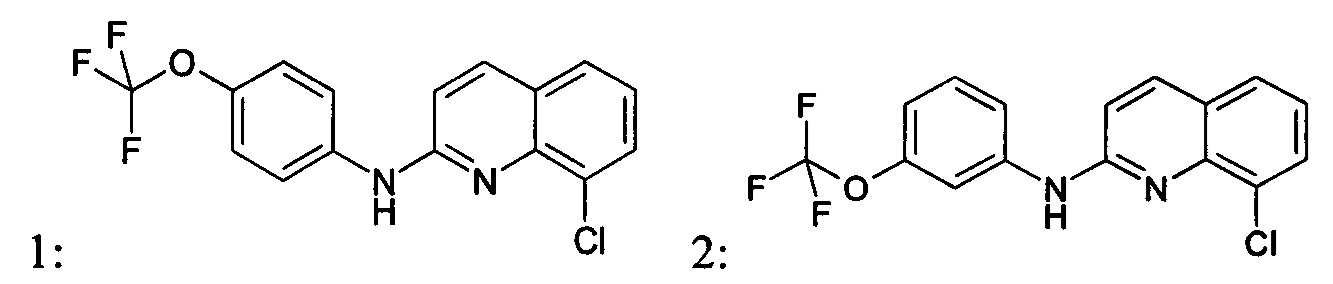
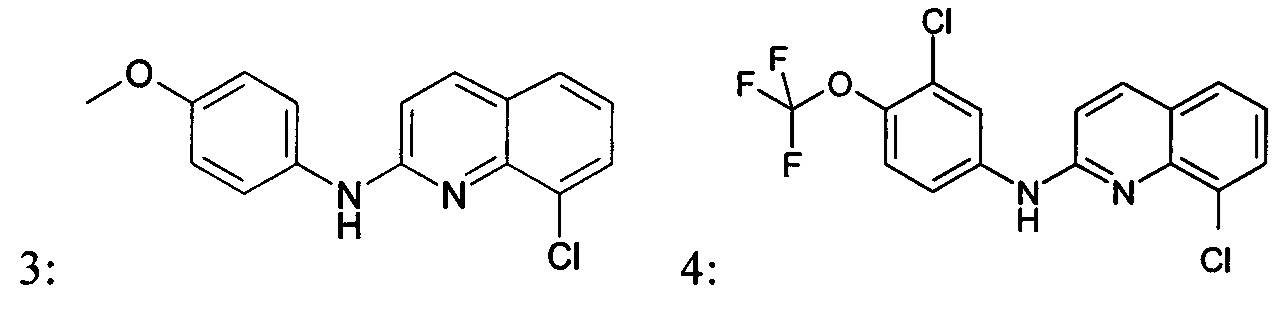
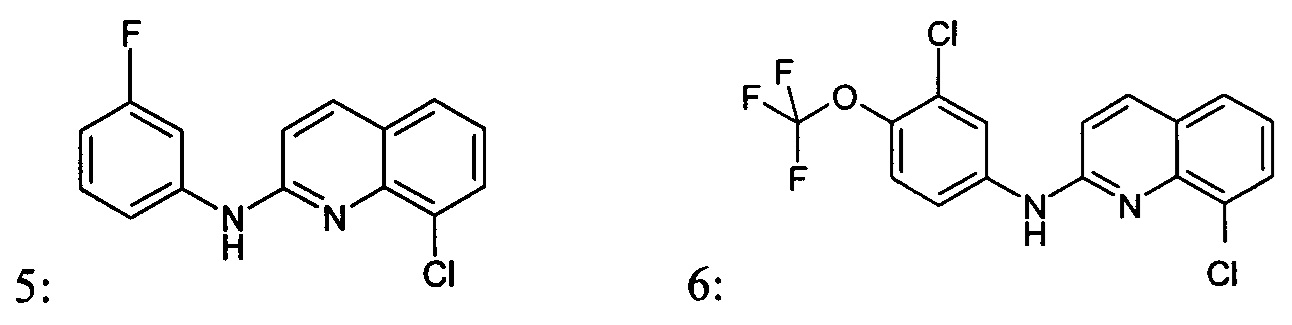
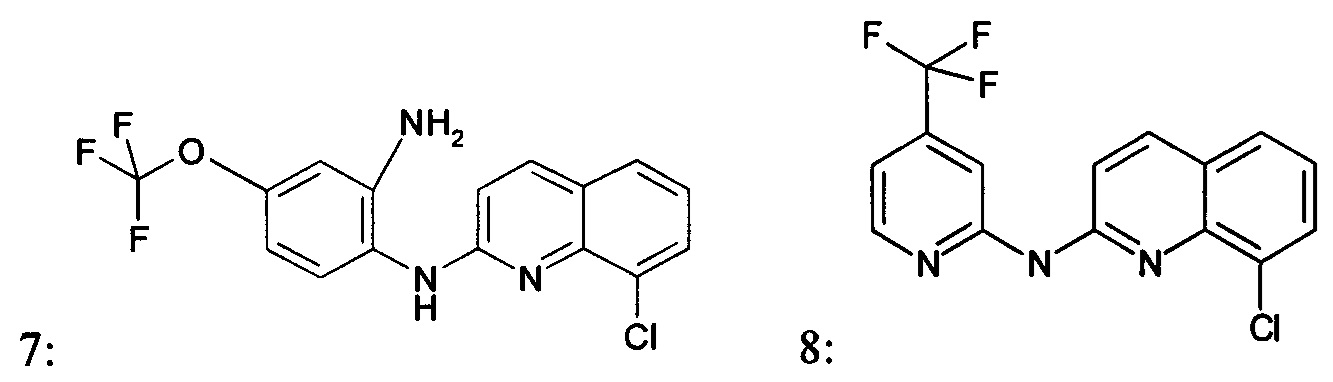
Фармацевтически приемлемая соль производного хинолина согласно изобретению, и более конкретно, соединения, имеющего общую формулу (I) или (II) согласно изобретению может представлять собой соль соединения, имеющего общую формулу (I) или (II), и щелочного металла, щелочно-земельного металла или аммония, полученную при помощи органических аммониевых оснований, или соли соединения, имеющего общую формулу (I) или (II) и органической или неорганической кислоты.
Более конкретно, соли, подходящие для изобретения, могут представлять собой соли натрия, калия, кальция, магния, четвертичного аммония, такие как тетраметиламмоний или тетраэтиламмоний, и соли присоединения аммония и фармацевтически приемлемые органические амины, такие как метиламин, диметиламин, триметиламин, этиламин, триэтиламин, этаноламин и трис(2-гидроксиэтил)амин.
Соли производного хинолина согласно изобретению, и более конкретно, соединения, имеющего общую формулу (I) или (II) и неорганической кислоты, подходящей для изобретения, могут быть получены при помощи соляной кислоты, бромоводородной кислоты, серной кислоты, азотной кислоты или фосфорной кислоты.
Соли производного хинолина согласно изобретению, и в частности соединения, имеющего общую формулу (I) или (II) и органической кислоты, подходящей для изобретения, могут быть получены при помощи карбоновых кислот и сульфоновых кислот, таких как муравьиная кислота, уксусная кислота, щавелевая кислота, лимонная кислота, молочная кислота, яблочная кислота, янтарная кислота, малоновая кислота, бензойная кислота, малеиновая кислота, фумаровая кислота, винная кислота, метансульфоновая кислота, бензолсульфоновая кислота или п-толуолсульфоновая кислота.
Согласно предпочтительному варианту реализации, производное хинолина, подходящее для изобретения, представляет собой 8-хлор-N-[4-(трифторметокси)фенил]хинолин-2-амин, который может быть представлен следующей формулой:
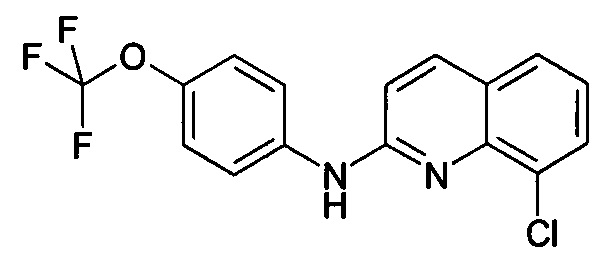
Производные хинолина, подходящие для изобретения, могут быть получены, как описано в WO 2010/143169.
Лечение может представлять собой оральное или парентеральное введение производного хинолина. Приемлемые способы введения и режим описаны в WO 2010/143169.
Можно использовать любой путь введения. Например, производное хинолина может быть введено орально, парентерально, внутривенно, трансдермально, внутримышечно, ректально, сублингвально, через слизистую, назально или другими способами. Кроме того, производное хинолина может быть введено в виде фармацевтической композиции и/или единичной дозированной формы.
Подходящие дозированные формы включают, но не ограничиваются, капсулы, таблетки (включая быстрорастворяющиеся и таблетки с замедленным высвобождением), порошок, сиропы, оральные суспензии и растворы для парентерального введения.
Примеры, предложенные в данном документе, приведены исключительно в качестве примеров и специалисты в области техники поймут, или будут способны определить при помощи не более чем рутинного эксперимента, ряд эквивалентов специфичных соединений, материалов, и способов. Все такие эквиваленты рассматриваются в качестве входящих в объем изобретения, и они охватываются прилагаемой формулой изобретения.
ПРИМЕРЫ
Пример 1
Модуляция экспрессии микроРНК при помощи 8-хлор-N-[4-(трифторметокс)фенил]хинолин-2-амина
Материалы и методы
В контексте ингибирования ВИЧ-1 производным хинолина 8-хлор-N-[4-(трифторметокси)фенил]хинолин-2-амином, изучалось, может ли лечение модулировать экспрессию хозяйской микроРНК.
Для этой цели, мононуклеарные клетки периферической крови (МКПК) от пяти здоровых доноров были выделены посредством центрифугирования в градиенте FICOLL. Затем клетки культивировали при 37°C, 5% СО2 до оптической плотности 1×106 клеток/мл в среде RPMI Glutamax (Life Technologies Ref 61870-010), дополненной 10% фетальной телячьей сывороткой (FCS) (Thermo Fischer Ref SV30160.03) 1000 ед/мл IL2 (Peprotech Ref 200-02) и 5 мкг/мл ФГА (Roche ref 1249738). Спустя три дня, клетки объединяли и ресуспендировали до оптической плотности 1×106 клеток/мл в среде RPMI Glutamax, дополненной 10% фетальной телячьей сывороткой (FCS) 1000 ед/мл IL-2 и распределяли в 12-луночных планшетах (Falcon Ref 353043) с 1,2 мл/лунку (4 лунки на тип условий).
ВИЧ инфекция может быть получена при помощи 1 нг Ada-M R5 ВИЧ штамма/лунку. Клетки обрабатывали в течение 6 дней по 1,2 мл/лунка 60 мкМ раствора 8-хлор-N-[4-(трифторметокси)фенил]хинолин-2-амина или 0,12% ДМСО (Sigma Ref D4818 в качестве отрицательного контроля).
Затем клетки объединяли по условиям, центрифугировали и осадки ресуспендировали в 700 мкл литического буфера Qiazol (Qiagen Ref 217004) из набора miRNeasy kit extraction от Qiagen (Qiagen Ref 217004). РНК экстрагировали согласно инструкциям производителя. Качество и количество экстрагированных РНК контролировали при помощи Agilent Bioanalyzer 2100 и спектрофотометра Nanodrop ND-1000. Среднее значение индекса целостности РНК составило 8,84 (от 7,2 до 9,7). Общее количество РНК 90 нг/образец метили при помощи FlashTag™ Biotin HSR RNA Labeling Kit (901911) и гибридизовали в течение ночи с Affymetrix Genechip miRNA Array 2.0. (901753) Чипы промывали и окрашивали при помощи стандартного протокола Affymetrix и сканировали при помощи Affymetrix Scanner. Контроли качества проводили при помощи Expression Console metrics от Affymetrix (версия 1.2).
Данные нормализовали при помощи способа нормализации Expression Console "RMA + DABG", и микроРНК рассматривали экспрессируемой, если соответствующее DABG Р-значение было меньше или эквивалентно 0,05. микроРНК рассматривали экспрессируемой в одних условиях, если микроРНК экспрессировалась в по меньшей мере 75% МКПК доноров данного состояния. Парный Т-тест Стьюдента применяли на экспрессированных микроРНК, которые рассматривали различно экспрессируемыми между двумя состояниями, если кратность изменения была выше или эквивалентной 1,5, и T-Test Р-значение было меньше или эквивалентно 0,05.
Результаты
Сравнение экспрессии микроРНК между инфицированными и неинфицированными клетками указало на множественную модификацию (активацию или подавление), возникающую в результате ВИЧ-1 инфекции. В частности, наблюдалось, что miRNA-124 была подавлена в ВИЧ-инфицированных МКПК.
Для контраста, сравнение между 8-хлор-N-[4-(трифторметокси)фенил]хинолин-2-амин обработанными и необработанными ВИЧ-инфицированными МКПК показало только одну микроРНК, miR-124, экспрессия которой была явно повышена (приблизительно 13 кратно) при лечении.
Соответственно, miR-124 подтверждена в качестве значимого биомаркера для мониторинга эффективности производных хинолина по изобретению в качестве противовирусных лекарственных средств у пациентов со СПИДом, и в частности 8-хлор-N-[4-(трифторметокси)фенил]хинолин-2-амина.
Пример 2
Оценка эффективности производных хинолина в отношении экспрессии miR-124 3р.
В дополнение к примеру 1, который предлагалась оценка экспрессии микроРНК в контексте ВИЧ-инфекции, в примере 2 оценивали вариацию экспрессии miR-124 в отсутствии ВИЧ-1. Способ скрининга тестировали для оценки набора производных хинолина и известных антиретровирусных лекарственных средств, таких как маравирок, эфавиренз, дарунавир и азидотимидин (AZT).
Материалы и методы
Экстракция МКПК при помощи градиента FICOLL™
Для данной цели мононуклеарные клетки периферической крови (МКПК) от четырех здоровых доноров выделяли при помощи центрифугирования в градиенте FICOLL™ согласно стандартным протоколам.
Вкратце, 60-70 мл лейкоцитной пленки заливали во флакон 175 см2, и объем доводили до 300 мл при помощи PBS с целью получения разведения приблизительно 5-кратной лейкоцитной пленки. 38 мл разведенной лейкоцитной пленки затем добавляли к пробирке Falcon™ из 50 мл, содержащим 12 мл FICOLL™ (Histopack-1077) при температуре окружающей среды. Препарат центрифугировали в течение 30 минут при 1600 об/мин (=515 ref) при температуре окружающей среды. Кольцо лимфоцитов восстанавливали из пробирки Falcon™ при помощи пипетки без градуировки (Pastette®) и затем промывали PBS при помощи центрифугирования в течение 10 минут при 1200 об/мин (=290 rcf) и при температуре окружающей среды до прозрачности супернатанта.
Затем клетки ресуспендировали при 37°C до оптической плотности 1,5×106 клеток/мл в среде RPMI Glutamax (Life Technologies Ref 61870-010), дополненной 10% фетальной телячьей сывороткой (FCS) (Thermo Fischer Ref SV30160.03) и без активации. Клетки инкубировали в течение 48 часов при 37°C при 5% СО2.
Обработка клеток исследуемыми молекулами
Для скрининга применяли шестилуночные планшеты. В каждую лунку, содержащую 3,106 клеток/4 мл среды RPMI, дополненной 10% фетальной телячьей сывороткой и 40 ед/мл IL-2 (Peprotech Ref 200-02), добавляли исследуемые молекулы. 100% ДМСО (0,8 мкл) добавляли к лунке и тестировали в качестве отрицательного контроля.
Устанавливали каждые тестовые условия, как описано в данном документе далее, и в лунке доводили до соответствующего конечного объема:
1) производные хинолина: (8-хлор-N-[4-(трифторметокси)фенил]хинолин-2-амин и 8-хлор-N-[4-(трифторметил)пиридин-2-ил]хинолин-2-амин - соответственно, соединения 1 и 8) в 100% ДМСО - (5 мкМ и конечный объем 0,4 мкл):
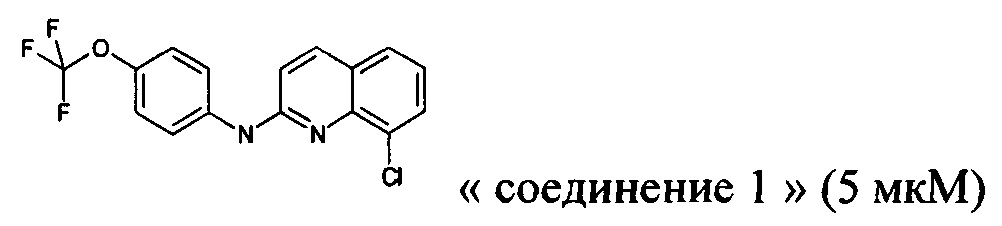

2) Другие антиретровирусные лекарственные средства: маравирок, эфавиренз, дарунавир, AZT (10 мкМ для всех - конечный объем 0,8 мкл).
Лунки инкубировали в течение трех дней при 37°C при 5% CO2. Среду меняли (день 3) согласно стандартным протоколам. Вкратце, плашки центрифугировали при 1200 об/мин в течение 5 минут, и 3 мл супернатанта удаляли. 3 мл RPMI, дополненной 10% фетальной телячьей сыворотки и 40 мл IL-2 затем добавляли с 0,6 мкл (для 10 мкМ конечной концентрации) или 0,3 мкл (для 5 мкМ конечной концентрации) стокового раствора скринированной молекулы при концентрации 50 мм в 100% ДМСО или 0,6 мкл 100% ДМСО в качестве отрицательного контроля.
Экстракция микроРНК (день 6)
Клетки восстанавливали внутри 15 мл пробирок Falcon™, центрифугировали при 1200 об/мин в течение 5 минут, и затем промывали в 10 мл PBS и в дальнейшем центрифугировали при 1200 об/мин в течение 5 минут. Затем клетки ресуспендировали в 1 мл PBS и подсчитывали.
6×106 клеток восстанавливали и центрифугировали при 1200 об/мин в течение 5 минут. Клеточный осадок лизировали в 300 мкл лизирующего буфера ML из набора для экстракции микроРНК Macherey Nagel Nucleospin® miRNA extraction kit (Macherey Nagel Ref 740971), и в дальнейшем хранили при -20°C.
5 мкл 2×108 копий/мкл положительного контроля (Ce_miR-39 от QIAGEN© - референс 219610, последовательность 5' UCACCGGGUGUAAAUCAGCUUG 3') добавляли к каждому образцу. Экстракцию микроРНК проводят при помощи протокола от набора для экстракции микроРНК Macherey Nagel Nucleospin® при помощи элюирующего объема для РНК 50 мкл и для микроРНК 30 мкл, и в дальнейшем хранили при -20°C.
Обратная транскрипция микроРНК (день 6)
Этап обратной транскрипции выполняли для 12 мкл микроРНК при помощи набора для обратной транскрипции miScript RT II от QIAGEN© при помощи буфера miScript HiSpec, и в дальнейшем хранили при -20°C.
Количественная ПЦР микроРНК (день 6)
Этап количественной ПЦР проводили при помощи набора QIAGEN© miScript SYBR® Green PCR kit и miScript Primer Assays согласно инструкции производителя.
Композиция реакционного буфера miScript для 384-луночных планшет:


(*) кДНК, полученная при помощи miScript II RT kit
Реакцию повторяли в трипликатах в 384-луночном планшете согласно инструкции производителя на системе для РВ-ПЦР LightCycler® 380 (Roche). Условия амплификации также устанавливали согласно протоколу производителя:

Относительная и абсолютная количественная оценка РВ-ПЦР представляют собой способы, известные в области техники и могут быть в дальнейшем детализированы ниже.
1) Относительная количественная оценка
Исходя из разведения до 1/10 в H2O для miR-124 РВ-ПЦР (Hs_miR-124a) или 1/100 для референсного гена/конститутивного гена РВ-ПЦР (Hs_miR-26a and Hs_miR-191, при помощи miScript Primer Assays (Hs_miR-124a, Hs_miR-26a and Hs_miR-191).
Анализ проводили при помощи модели относительной количественной оценки без коррекции эффективности (2-ΔΔCp) при помощи среднего значения точек пересечения (Ср) из трипликатов miR-124 и среднего трипликатов miR-26a и miR-191.
2) Абсолютная количественная оценка
Из разведения до 1/10 в Н2О для miR-124 РВ-ПЦР и miScript Primer Assays (Hs_miR-124a et Ce_ miR-39). Калибровочные кривые строили согласно стандартным протоколам. Анализ проводили посредством нормализации среднего трипликатов miR-124 со средним трипликатов miR-39 и дальнейшей нормализацией в отношении числа клеток.
Результаты
Результаты показывают хорошее соответствие между относительной и абсолютной количественной оценкой для всех молекул. Контрольные образцы ДМСО имеют изменение, кратное 1, что означает отсутствие вариации в экспрессии miR-124а. Все протестированные производные хинолина показывают модуляцию miR-124, соответствующую десятикратному повышению экспрессии miR-124.
Для сравнения другие антиретровирусные лекарственные средства не индуцируют существенную модуляцию экспрессии miR-124.
Таким образом, данный пример показывает, что miR-124 является приемлемым биомаркером для скрининга лекарственного средства-кандидата или вакцины-кандидата, предположительно эффективных при предупреждении и/или лечении вирусной инфекции. Он также особенно пригоден для оценки активности производного хинолина согласно изобретению.