Результат интеллектуальной деятельности: ИСПОЛЬЗОВАНИЕ ИНГИБИТОРОВ INOS ДЛЯ ПОВЫШЕНИЯ УРОЖАЯ ВИРУСОВ В КУЛЬТУРЕ
Вид РИД
Изобретение
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение, в общем, относится к способам для получения вирусов и рекомбинантных вирионов в культуре. В частности, изобретение относится к использованию ингибиторов iNOS, таких как ауринтрикарбоновая кислота, дексаметазон и вальпроевая кислота для увеличения урожая различных вирусов в культуре, включая рекомбинантные герпесвирусы, которые, в свою очередь, можно использовать в качестве вирусов-помощников для выработки вирионов рекомбинантного аденоассоциированного вируса.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Герпесвирусы широко распространены в природе и встречаются у большинства видов животных. Охарактеризовано, по меньшей мере, сто герпесвирусов, в том числе несколько от людей, такие как вирус простого герпеса-1 (HSV-1) и вирус простого герпеса-2 (HSV-2), вирус ветряной оспы (VZV), вирус Эпштейна-Барр (EBV), цитомегаловирус (CMV) и другие герпесвирусы человека, такие как HHV6 и HHV7. Эти вирусы несут ответственность за различные заболевания человека, такие как кожные инфекции, генитальный герпес, вирусный энцефалит и т.п.
Заражение HSV-1 активирует защитные силы организма и врожденный иммунный ответ за счет индуцирования внутриклеточных путей передачи сигнала, которые приводят к экспрессии белков с провоспалительными и противомикробными свойствами, включая цитокины и интерфероны (ИФ) (Sainz and Halford, J. Virol (2002) 76: 11541-11550; Haller et al., Virology (2006) 344: 119-130; Paludan et al., Nat. Rev. Immunol. (2011) 11: 143-154). Сигнальный путь интерферонов представляет собой один из наиболее важных механизмов клеточной защиты для элиминации вирусов (Brandner & Mueller, Hoppe-Seyler's Zeitschriftfur physiologische Chemie (1973) 354: 1176; De Vries et al., Gene Ther. (2008) 15:545-552).
Исследователи сообщают о противовирусной активности оксида азота (NO) против некоторых вирусов, таких как вирус осповакцины, вирус везикулярного стоматита, и вирус японского энцефалита, наряду с другими (Bi et al., J. Virol. (1995) 69:6466-6472; Harris et al., J. Virol. (1995) 69:910-915; Lin et al., Virol. (1997) 71:5227-5235; Pertile et al., Avian Dis. (1996) 40:342-348. NO представляет собой свободно радикальную газообразную молекулу и является медиатором иммунной системы организма (Croen K.D., J. Clin. Invest. (1993) 91:2446-2452; Karupiah et al., Science (1993) 261:1445-1448; Rolph et al., Virol. (1996) 217:470-477; Amaro et al., J. Med Virol. (1997) 51:326-331; Lane et al., J. Virol. (1997) 71:2202-2210. Известно, что HSV-1 способен, как вызывать противовирусные ответы организма, так и уклоняться от них (Mossman et al., J. Virol. (2001) 75:750-758). Заражение HSV способно вызывать экспрессию индуцибельной синтазы оксида азота (iNOS), гена, кодирующего индуцибельную изоформу NOS, которая производит большие количества NO.
Герпесвирусы и их рекомбинантные белки используют в производстве ряда вакцин. Помимо аденовирусов, было показано, что герпесвирусы полностью обеспечивают функции вируса-помощника для выработки вирионов рекомбинантного аденоассоциированного вируса (Buller, R.M.L., J. Virol. (1981) 40:241 -247; Mishra et al., Virology (1990) 179:632-639). Был установлен минимальный набор генов HSV-1, необходимый для репликации AAV и упаковки, включающий ранние гены UL5, UL8, UL52 и UL29 (Weindler et al., J. Virol. (1991) 65:2476-2483). Эти гены кодируют компоненты корового комплекса репликации HSV-1 - геликазу, праймазу и вспомогательные белки праймазы (UL5, UL8 и UL52) и белок, связывающий одноцепочечную ДНК (UL29).
Векторы на основе рекомбинантных AAV (rAAV) успешно применяют для получения высокого уровня длительной трансдукции in vivo. Несмотря на вышеперечисленные преимущества, производство больших количеств вирионов rAAV с высоким титром для клинического применения в генотерапии продолжает оставаться сложным из-за ограничений в масштабируемости протокола котрансфекции. Процесс требует эффективной клеточной доставки трех компонентов: (1) вектора, содержащего интересующий ген, фланкированный инвертированными концевыми повторами AAV (ITR); (2) вектора, содержащего гены rep и cap AAV; и (3) генов, обеспечивающих использование вируса-помощника, такого как аденовирус или вирус простого герпеса или использование безвирусных хелперных плазмид (см., Muzyczka, N., Curr. Top. Microbiol. Immunol. (1992) 158:97-129). Таким образом, в производственных протоколах rAAV на основе rHSV, урожай rAAV ограничен максимальным титром векторов-помощников rHSV.
Вектор с HSV-1, дефицитный по репликации, который называется d27.1-rc, экспрессирует гены rep и cap AAV (Conway et al., Gene Ther. (1999) 6:986-993) и сконструирован из исходного вируса d27-1 (Рис at al., J. Virol. 1989 vol. 63 (8) pp. 3399-407), который не вырабатывает ICP27, белок, необходимый для репликации HSV-1.
Хотя этот вектор является дефицитным по репликации, он все же экспрессирует ранние гены HSV-1, необходимые для репликации и упаковки rAAV (Conway et al., Gene Ther. (1999) 6:986-993).
Как правило, одним вектором, несущим матрицу rAAV и другим вектором, экспрессирующим регионы rep и cap AAV, совместно инфицируют клетки 293 для выработки вирионов rAAV. Оба вектора на основе HSV-1, являются дефицитными по репликации и, таким образом, могут размножаться только в линии клеток, дополненной ICP27, V27 (Рис at al., J. Virol. 1989 vol. 63 (8) pp. 3399-407). По протоколу выработки AAV на основе HSV, клетки 293 необходимо инфицировать HSV-1 с высокой множественностью заражения (MOI), равной 12. Это является ограничением, поскольку урожаи векторов-производных d27-1 в клетках V27 составляют, как правило, приблизительно 1×107 бляшкообразующих единиц (БОЕ)/мл.
Были исследованы несколько способов и реагентов для того чтобы дополнительно повысить титры HSV-1 (see, e.g., Wechucket al., Biotechnol. Prog. (2000) 16:493-496; Ozuer et al., Biotechnol. Prog. (2002) 18:476-482; Erlandsson et al., J. Endocrinol, (2002) 175:165-176; Otsuki et al., Mol. Ther. (2008) 16:1546-1555).
Как дексаметазон, так и вальпроевая кислота ингибируют защитные механизмы организма, представленные несколькими интерферон (ИФН)-чувствительными противовирусными генами, повышают уровень транскрипции вирусных генов, и, таким образом, улучшают распространение вируса и урожай HSV-1 (Erlandsson et al., J. Endocrinol. (2002) 175:165-176; Otsuki et al., Mol. Ther. (2008) 16:1546-1555).
Несмотря на вышеизложенные знания, необходимы дополнительные способы для ингибирования иммунной системы с целью улучшения продукции вируса в культуре. Как упоминалось выше, исследователи сообщают о противовирусной активности оксида азота (NO) против некоторых вирусов, таких как вирус осповакцины, вирус везикулярного стоматита и вирус японского энцефалита, наряду с другими (Bi et al, J. Virol. (1995) 69:6466-6472; Harris et al., J. Virol. (1995) 69:910-915; Lin et al, J. Virol. (1997) 71:5227-5235; Pertile et al. Avian Dis. (1996) 40:342-348. NO представляет собой свободнорадикальную газообразную молекулу и является медиатором иммунной системы (Croen K.D., J. Clin. Invest. (1993) 91:2446-2452; Karupiah et al., Science (1993) 261:1445-1448; Rolph et al., Virol. (1996) 217:470-477; Amaro et al., J. Med. Virol. (1997) 51:326-331; Lane et al., J. Virol. (1997) 71:2202-2210). Как описано выше, инфекция HSV может вызывать экспрессию iNOS, гена, кодирующего индуцибельную изоформу NOS, которая производит большие количества NO.
Присутствие ингибитора iNOS, N-метил-L-аргинина (L-NMA), отменяет ингибирование репликации вирусов для всех этих трех вирусов (Karupiah et al. Science (1993) 261: 1445-1448). Для обзора ингибиторов iNOS, см. Southan et al,Biochem. Pharmacol. (1996) 51:383-394. Было показано, что другое соединение, ауринтрикарбоновая кислота (АТК), защищает макрофаги от гибели клеток, вызванной бактериальным липополисахаридом посредством подавления экспрессии iNOS, и, таким образом, снижения выработки NO (Chen et al., British Journal of Pharmacology (2002) vol. 137 (7) pp. 1011-20). АТК представляет собой гетерогенную смесь полимеров, которым приписывают все большее количество видов биологической активности, таких как взаимодействие с рядом ферментов, включая ДНК-полимеразы, РНК-полимеразы, обратную транскриптазу (РНК-зависимую ДНК-полимеразу), аминоацил-тРНК-синтетазу, рибонуклеотидредуктазу, нуклеазу рибонуклеаз, ингибирование синтеза белка, предотвращение апоптоза и блокирование фрагментации ДНК в олигодендроцитах, вызванное окислительным стрессом (Tscherne and Pestka, Antimicrob. Agents Chemother.(1975) 8:479-487; Mikelens et al., Biochemical Pharmacology (1976) 25:821-827; Vollgraf et al., J. Neurochem.(l999) 73:2501-2509).
Также описано, что ауринтрикарбоновая кислота (АТК) предотвращает активацию транскрипции, опосредованную ИФН (Tsi et al., Mol. Pharmacol. (2002) 101:90-101; Chen et al., British J. Pharmacol. (2002) 137:1011-1020). АТК известна как активатор пути Raf/MEK/MAPK, рецептора IGF-1 и сигнального пути протеинкиназы C (Beery et al., Endocrinology (2001) 142:3098-3107; Chen et al., J. Biol. Chem. (2001) 276:46722-46728). Противовирусное, противомикробное и антипролиферативное действие цитокинов, таких как интерфероны, может быть связано с их способностью вызывать экспрессию iNOS, гена, кодирующего изоформу синтазы оксида азота (NOS), которая производит большие количества радикального газа, NO, из гуанидинового азота L-аргинина (Nathan, C, FASAB J. (1992) 6:3051; Werner-Felmayer et al., J. Exp. Med. (1990) 172:1599). Показано, что обработка макрофагами с ИФН-γ серьезно ограничивает репликацию вируса оспы мышей (EV), вируса осповакцины (VV) и HSV-1.
С одной стороны, АТК также известна как противовирусное средство против некоторых вирусов, включая ВИЧ, вирус герпеса HHV-7, SARS-CoV и других (Cushman et al., J. Med. Chem. (1991) 34:329-3371991; Zhang et al., Antiviral Res. (1999) 43:23-35; Yap et al., ComputationalBiol andChem. (2005) 29:212-219; De Clercq, Advents, Advances, and Adventures Med. Res. Rev. (2011) 31:118-160). АТК, однако, не блокирует репликацию аденовируса типа 5 (Ad5) в клетках HEK-293 (He, Biochem. Biophys. Res. Comm. (2004) 320:1199-1203). Кроме того, сообщают, что АТК неожиданно повысила титр контрольного аденовирусного вектора в клетках 293, хотя в то же самое время оказала противовирусное воздействие на вирус осповакцины (Myskiw et al., J. Virol. (2007) 81:3027-3032).
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение, таким образом, преодолевает недостатки известного уровня техники путем решения проблем, которые ограничивают продукцию вируса, таких как низкая продукция rHSV, что затрудняет усилия по производству достаточных количеств rHSV для различных целей, включая производство вакцины, а также для продукции вирионов rAAV в количествах необходимых для эффективных процедур генотерапии. С использованием способов, описываемых в настоящем документе, можно получать более высокие титры вирусов, такие как, по меньшей мере, на порядок больше, чем при традиционных способах.
В частности, авторы изобретения в настоящем документе открыли, что ауринтрикарбоновая кислота (АТК) ингибирует iNOS и повышает продукцию HSV. Как показано в примерах в настоящем документе, микромолярные концентрации АТК в присутствии эмбриональной телячьей сыворотки (ЭТС) повысили как урожай вектора HSV-1/d27-1 в клетках V27, так и вируса дикого типа (wt) HSV-1 в клетках Vero, V27 и 293. Другие ингибиторы iNOS, включая дексаметазон и вальпроевую кислоту, также повысили титры HSV-1 в культуре. Было показано, что экспрессия iNOS, вызванная HSV, снизилась в образцах HSV+АТК при анализе с микропанелью SABiosciences. Аналогично, анализ при помощи панели генома человека Affymetrix подтвердил, что повышенная экспрессия всех трех генов синтазы оксида азота (nNOS, iNOS и eNOS), вызванная HSV, была снижена в образцах HSV+АТК. Affymetrix Gene Array также выявил, что экспрессия генов, которые участвуют в сигнальном пути IgE и ИФН, связанном с воспалением, и в системных иммунных ответах, была снижена за счет HSV-1 и подавлена после добавления АТК. С другой стороны, экспрессия генов, преимущественно вовлеченных в фазу клеточного цикла G1/S и передачу сигнала при развитии, опосредованном WNT, была значительно снижена за счет HSV и повышена после добавления АТК.
Эти результаты являются значимыми из-за спроса на более высокие титры HSV-1 для продукции вирионов rAAV, а также для профилактических, терапевтических и диагностических целей.
Таким образом, в одном из вариантов осуществления изобретение относится к способу получения вируса, включающему культивирование вируса в культуре клеток, которая содержит ауринтрикарбоновую кислоту. В определенных вариантах осуществления вирус представляет собой вирус герпеса, такой как HSV-1.
В дополнительных вариантах осуществления вирус герпеса представляет собой HSV-1 дикого типа или рекомбинантный вектор HSV-1, такой как вектор HSV-1 d27.1.
В дополнительных вариантах осуществления вирус культивируют в клетках 293, HeLa или Vero, таких как клетки V27.
В дополнительных вариантах осуществления изобретение относится к способу культивирования вектора HSV-1 d27.1, включающему:
(a) заражение клеток V27 вектором HSV-1 d27.1; и
(b) культивирование зараженных клеток V27 в культуре клеток, содержащей ауринтрикарбоновую кислоту, вальпроевую кислоту или дексаметазон.
В определенных вариантах осуществления культура клеток дополнительно содержит сыворотку, такую как эмбриональная телячья сыворотка.
В дополнительных вариантах осуществления изобретение относится к культуре клеток, содержащей ауринтрикарбоновую кислоту и клетки 293, HeLa или Vero, такие как клетки V27.
Эти и другие варианты осуществления рассматриваемого изобретения будут очевидны специалистам в данной области в свете описания в настоящем документе.
КРАТКОЕ ОПИСАНИЕ РИСУНКОВ
Фигура 1 представляет собой Вестерн-блоттинг, показывающий, что ауринтрикарбоновая кислота (АТК) ингибирует экспрессию iNOS в лизатах V27, зараженных d27-1.
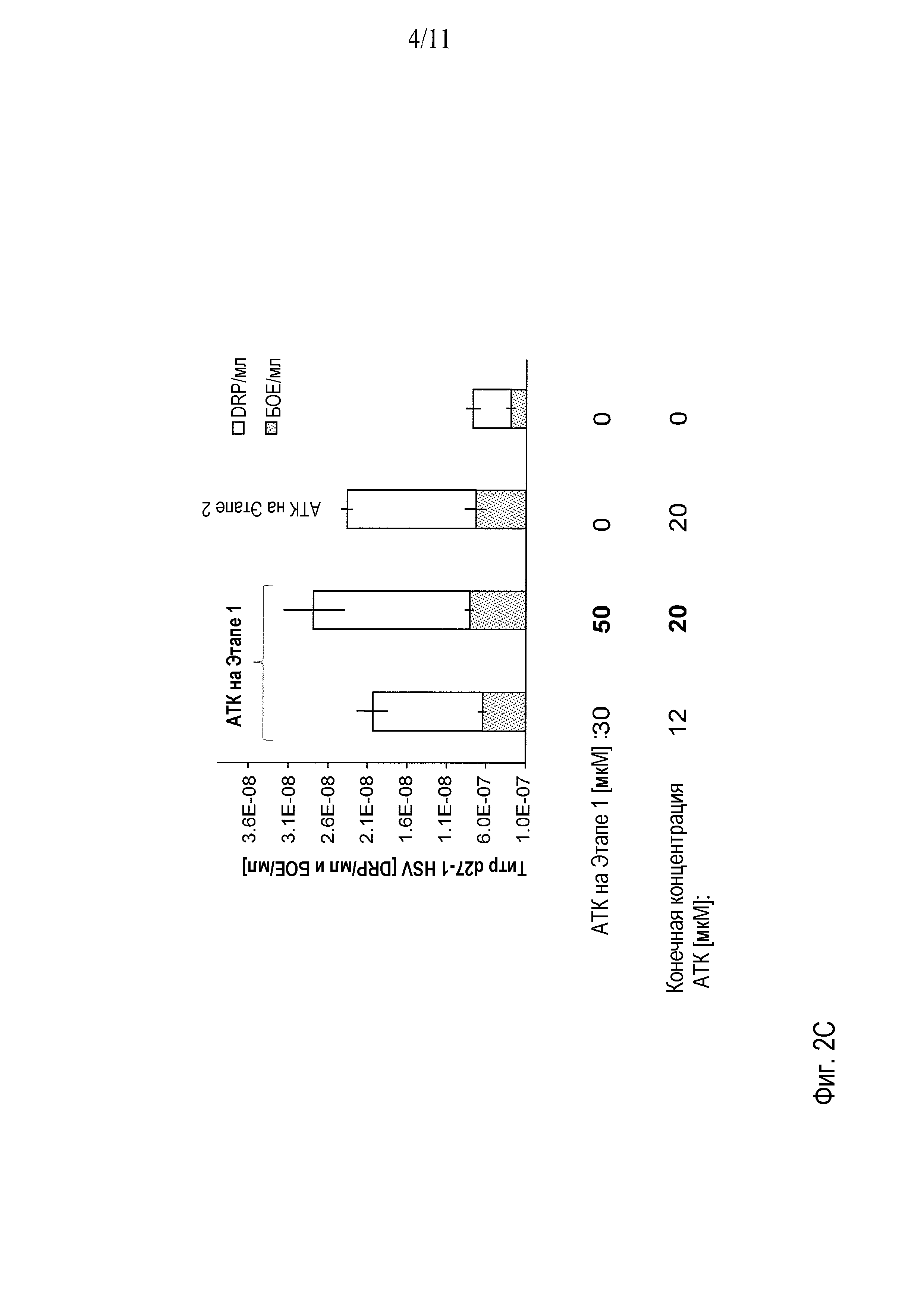
Фигуры 2A-2C показывают принципы протокола АТК-HSV (фигура 2A) и оптимизацию титров d27-1 HSV-1 в супернатантах V27 для того чтобы определить, какие концентрации и условия добавления АТК оказывают воздействие на урожаи HSV. Фигура 2B показывает вирусные титры, выраженные в виде частиц, устойчивых к ДНКазе (DRP/мл) при различных концентрациях АТК в 6-луночных планшетах (фигура 2B) и колбах T150 (фигура 2C).
На фигуре 3 представлена важность присутствия сыворотки в протоколе АТК-HSV. Дополнительная оптимизация и важность присутствия ЭТС в протоколе АТК-HSV были продемонстрированы на титрах d27-l HSV-1, выраженных в виде drp/мл и БОЕ/мл.
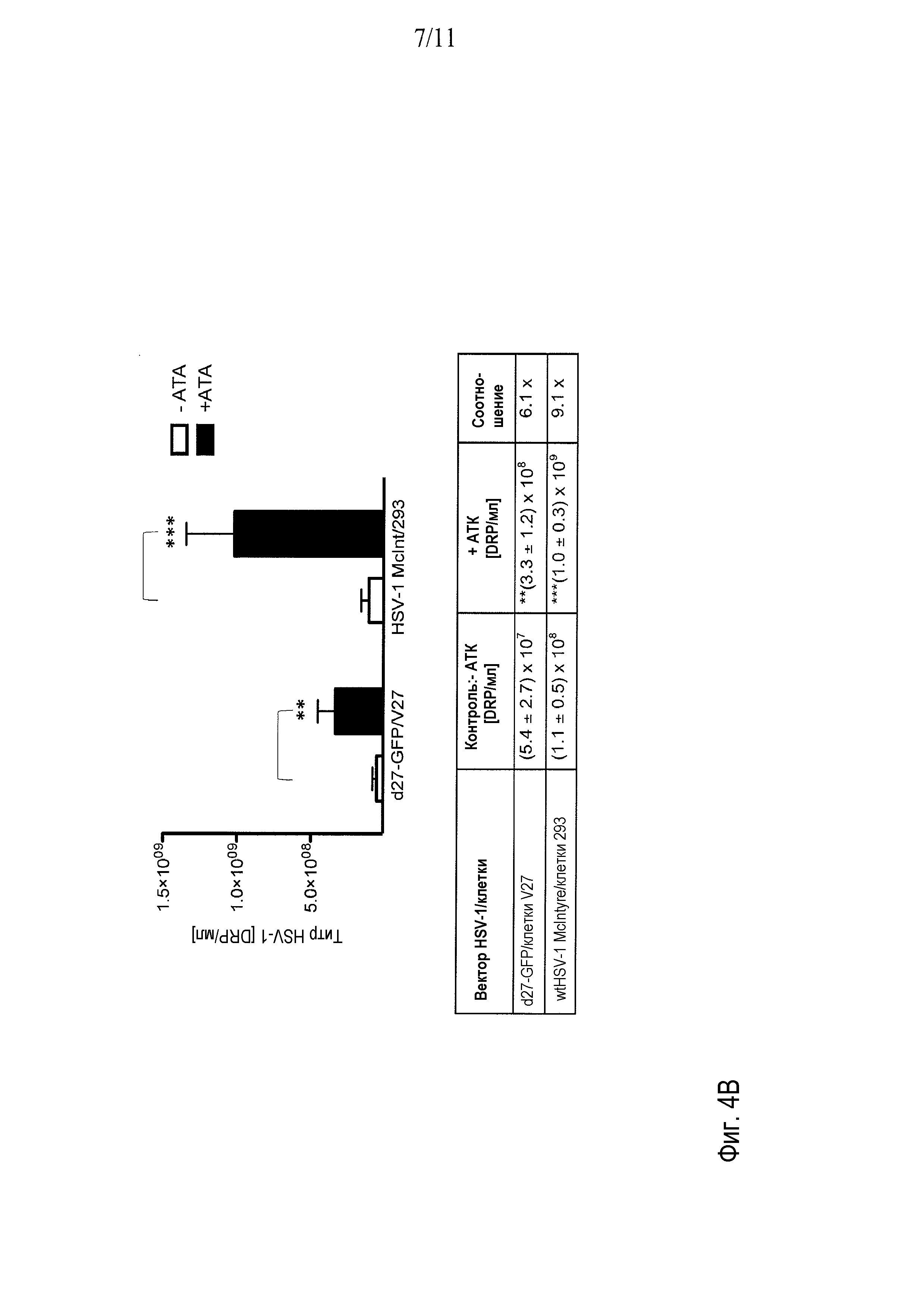
Фигуры 4A-4B демонстрируют влияние АТК на штаммы KOS и McIntyre HSV дикого типа в культуре. АТК повышает урожай обоих типов вируса в клетках Vero, однако АТК, по-видимому, ингибирует рост HSV-1 KOS в клетках 293. С другой стороны, штамм McIntyre wtHSV-1 достигает наибольших титров после индукции АТК в клетках 293. Кроме того, АТК, по-видимому, ингибирует оба типа вирусов HSV-1 в клетках HeLa.
Фигуры 5A-5B демонстрируют влияние АТК в стоках HSV на продукцию вирионов rAAV. Титры rAAV были слегка увеличены, когда добавляли сток HSV, приготовленный с 20 мкМ АТК, добавленной во время заражения. Также было показано, что АТК повышает титр rAAV, когда 10 мкМ АТК вводили непосредственно в среду с клетками 293 в течение 2 часов этапа совместного заражения с HSV.
На фигуре 6 представлено влияние дексаметазона (Dex) на вирусный титр d27-1/GFP HSV-1. Конечные титры d27-1/GFP HSV-1 были, в основном, слегка повышены после предварительных обработок или обработок dex по сравнению с необработанным контролем.
На фигуре 7 представлено влияние предварительной обработки вальпроевой кислотой (ВК) на вирусный титр d27-1/GFP HSV-1. ВК в концентрации 5 мМ слегка повысила титр d27-1/GFP HSV-1, однако концентрации ниже и выше 5 мМ, по-видимому, оказывают ингибирующее действие на титр d27-1/GFP HSV-1 по сравнению с необработанным контролем.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В практическом осуществлении настоящего изобретения используют, если не указано иначе, общепринятые способы химии, биохимии, технологии рекомбинантной ДНК и иммунологии в пределах данной области техники. Такие способы полностью описаны в литературе. См., например, Fundamental Virology, 2nd Edition, vol. I & II (B.N. Fields and D.M. Knipe, eds.); Handbook of Experimental Immunology, Vols. I-IV (D.M. Weir and C.C. Blackwell eds., Blackwell Scientific Publications); Т.Е. Creighton, Proteins: Structures and Molecular Properties (W.H. Freeman and Company, 1993); A.L. Lehninger, Biochemistry (Worth Publishers, Inc., current addition); Sambrook, et al., Molecular Cloning: A Laboratory Manual (2nd Edition, 1989); Methods In Enzymology (S. Colowick and N. Kaplan eds., Academic Press, Inc.).
Все публикации, патенты и патентные заявки, процитированные в настоящем документе, выше или ниже, включены, таким образом, в качестве ссылки полностью.
1. ОПРЕДЕЛЕНИЯ
В описании настоящего изобретение будут использованы следующие термины, и они определены, как указано ниже.
Следует отметить, что, при использовании в данном описании и прилагаемой формуле изобретения, формы единственного числа включают отсылки к формам множественного числа, если текст ясно не указывает на иное. Таким образом, например, ссылка на "вирус герпеса" включает смесь из двух или более таких вирусов, и т.п.
Термины "рекомбинантный HSV" "rHSV" и "вектор rHSV" относятся к изолированным, генетически модифицированым формам вируса простого герпеса (HSV), содержащим гетерологичные гены, вставленные в вирусный геном. Под термином "rHSV/rc" или "вирус rHSV/rc" или "вирус rHSV с хелперной функцией" подразумевают rHSV, в котором rep и/или cap гены AAV вставлены в геном rHSV. Термины "экспресссирующий вирус rHSV" и "rHSV/AAV" обозначают rHSV, в котором последовательности инвертированного концевого повтора (ITR) из AAV вставлены в геном rHSV.
Термины "полипептид" и "белок" относятся к полимеру из аминокислотных остатков и не ограничены минимальной длиной продукта. Таким образом, пептиды, олигопептиды, димеры, мультимеры и т.п. включены в определение. Определение включает как полноразмерные белки, так и их фрагменты. Термины также включают постэкспрессионные модификации полипептида, например, гликозилирование, ацетилирование, фосфорилирование и т.п. Кроме того, для целей настоящего изобретения, "полипептид" относится к белку, который содержит модификации, такие как делеции, вставки и замены (как правило, консервативные по своей природе), в нативной последовательности, при условии, что белок сохраняет желаемую активность. Эти модификации могут быть намеренными, например, посредством сайт-специфического мутагенеза, или могут быть случайными, такими как мутации организмов, которые вырабатывают белки, или ошибки из-за амплификации посредством ПЦР. В зависимости от используемой экспрессирующей системы, в полипептиде может присутствовать или отсутствовать N-концевой метионин. Кроме того, полипептид может содержать или не содержать нативную сигнальную последовательность, если она присутствует изначально. Если сигнальная последовательность в норме отсутствует, белок можно получать с гетерологичной последовательностью.
"Нативный" полипептид относится к полипептиду с той же самой аминокислотной последовательностью, что и соответствующая молекула, полученная из природного источника. Такие нативные последовательности можно выделять из природных источников или можно получать рекомбинантными или синтетическими способами. Термин "нативная" последовательность конкретно включает природные укороченные или секретируемые формы конкретной молекулы (например, последовательность внеклеточного домена), природные вариантные формы (например, формы с альтернативным сплайсингом) и природные аллельные варианты полипептида.
Под "вариантом" подразумевают активный полипептид, определенный в настоящем документе, имеющий, по меньшей мере, приблизительно 80% идентичности аминокислотных последовательностей с соответствующей полноразмерной нативной последовательностью, полипептид без сигнального пептида, внеклеточный домен полипептида, с наличием или отсутствием сигнального пептида, или любой другой фрагмент последовательности полноразмерного полипептида, как описано в настоящем документе. Такие полипептидные варианты включают, например, полипептиды, где один или несколько аминокислотных остатков добавлены или удалены с N- и/или C-конца полноразмерной нативной аминокислотной последовательности. Как правило, такой вариант будет иметь, по меньшей мере, приблизительно 80% идентичности аминокислотных последовательностей, альтернативно, по меньшей мере, приблизительно 81% идентичности аминокислотных последовательностей, альтернативно, по меньшей мере, приблизительно 82% идентичности аминокислотных последовательностей, альтернативно, по меньшей мере, приблизительно 83% идентичности аминокислотных последовательностей, альтернативно, по меньшей мере, приблизительно 84% идентичности аминокислотных последовательностей, альтернативно, по меньшей мере, приблизительно 85% идентичности аминокислотных последовательностей, альтернативно, по меньшей мере, приблизительно 86% идентичности аминокислотных последовательностей, альтернативно, по меньшей мере, приблизительно 87% идентичности аминокислотных последовательностей, альтернативно, по меньшей мере, приблизительно 88% идентичности аминокислотных последовательностей, альтернативно, по меньшей мере, приблизительно 89% идентичности аминокислотных последовательностей, альтернативно, по меньшей мере, приблизительно 90% идентичности аминокислотных последовательностей, альтернативно, по меньшей мере, приблизительно 91% идентичности аминокислотных последовательностей, альтернативно, по меньшей мере, приблизительно 92% идентичности аминокислотных последовательностей, альтернативно, по меньшей мере, приблизительно 93% идентичности аминокислотных последовательностей, альтернативно, по меньшей мере, приблизительно 94% идентичности аминокислотных последовательностей, альтернативно, по меньшей мере, приблизительно 95% идентичности аминокислотных последовательностей, альтернативно, по меньшей мере, приблизительно 96% идентичности аминокислотных последовательностей, альтернативно, по меньшей мере, приблизительно 97% идентичности аминокислотных последовательностей, альтернативно, по меньшей мере, приблизительно 98% идентичности аминокислотных последовательностей и альтернативно, по меньшей мере, приблизительно 99% идентичности аминокислотных последовательностей с соответствующей полноразмерной нативной последовательностью. Как правило, вариантные полипептиды имеют, по меньшей мере, приблизительно 10 аминокислот в длину, такие как, по меньшей мере, приблизительно 20 аминокислот в длину, например, по меньшей мере, приблизительно 30 аминокислот в длину, альтернативно, по меньшей мере, приблизительно 40 аминокислоты в длину, альтернативно, по меньшей мере, приблизительно 50 аминокислот в длину, альтернативно, по меньшей мере, приблизительно 60 аминокислот в длину, альтернативно, по меньшей мере, приблизительно 70 аминокислот в длину, альтернативно, по меньшей мере, приблизительно 80 аминокислот в длину, альтернативно, по меньшей мере, приблизительно 90 аминокислот в длину, альтернативно, по меньшей мере, приблизительно 100 аминокислот в длину, альтернативно, по меньшей мере, приблизительно 150 аминокислот в длину, альтернативно, по меньшей мере, приблизительно 200 аминокислот в длину, альтернативно, по меньшей мере, приблизительно 300 аминокислот в длину или больше.
Особенно предпочтительные варианты содержат замены, которые являются консервативными по своей природе, т.е., те замены, которые происходят внутри семейства аминокислот, являющихся родственными по своим боковым цепям. Конкретно, аминокислоты, как правило, делят на четыре семейства: (1) кислые - аспарагиновая кислота и глутаминовая кислота; (2) основные - лизин, аргинин, гистидин; (3) неполярные - аланин, валин, лейцин, изолейцин, пролин, фенилаланин, метионин, триптофан; и (4) незаряженные полярные - глицин, аспарагин, глутамин, цистеин, серин, треонин, тирозин. Фенилаланин, триптофан и тирозин иногда классифицируют как ароматические аминокислоты. Например, вполне предсказуемо, что отдельная замена лейцина на изолейцин или валин, аспарагиновой кислоты на глутаминовую кислоту, треонина на серин, или аналогичная консервативная замена аминокислоты структурно родственной аминокислотой, не будет иметь важного воздействия на биологическую активность. Например, интересующий полипептид может содержать вплоть до приблизительно 5-10 консервативных или не-консервативных аминокислотных замен, или даже вплоть до приблизительно 15-25 или 50 консервативных или не-консервативных аминокислотных замен, или любое количество в пределах от 5 до 50, при условии, что желаемая функция молекулы остается интактной.
"Гомология" относится к проценту идентичности между двумя полинуклеотидами или двумя полипептидными молекулами. Две ДНК или две полипептидных последовательности являются "по существу гомологичными" друг другу, если последовательности демонстрируют, по меньшей мере, приблизительно 50%, предпочтительно, по меньшей мере, приблизительно 75%, более предпочтительно, по меньшей мере, приблизительно 80%-85%, предпочтительно, по меньшей мере, приблизительно 90%, и наиболее предпочтительно, по меньшей мере, приблизительно 95%-98% идетнтичности последовательности по всей определенной длине молекул. Применяемый в настоящем документе, термин «по существу гомологичный» также относится к последовательности, демонстрирующей полную идентичность с конкретной последовательностью ДНК или полипептида.
В общем случае, "идентичность" относится к точному нуклеотид-к-нуклеотиду или аминокислота-к-аминокислоте соответствию двух полинуклеотидных или полипептидных последовательностей, соответственно. Процент идентичности можно определять путем прямого сравнения информации о последовательностях между двумя молекулами посредством сопоставления последовательностей, подсчета точного числа совпадений между двумя совмещенными последовательностями, деления числа на длину более короткой последовательности и умножения результата на 100. Для помощи в анализе можно использовать легкодоступные компьютерные программы, такие как ALIGN, Dayhoff, M.O. in Atlas of Protein Sequence and Structure M.O. Dayhoff ed., 5 Suppl. 3:353-358, National Biomedical Research Foundation, Washington, DC, которая адаптирует алгоритм локальной гомологии из Smith and Waterman Advances in Appl. Math. 2:482-489, 1981 для анализа пептидов. Программы для определения идентичности нуклеотидных последовательностей доступны в Wisconsin Sequence Analysis Package, Version 8 (доступна у Genetics Computer Group, Madison, WI), например, программы BESTFIT, FASTA и GAP, которые также опираются на алгоритм Смита и Уотермана. Эти программы легко использовать с параметрами по умолчанию, рекомендованными производителем, и описанными в вышеуказанном Wisconsin Sequence Analysis Package. Например, процент идентичности конкретной нуклеотидной последовательности с референсной последовательностью можно определять с использованием алгоритма гомологии Смита и Уотермана с таблицей оценки по умолчанию и штрафом за пропуск шести нуклеотидных положений.
Другим способом оценки процента идентичности в контексте настоящего изобретения является использование пакета программ MPSRCH, с охраняемым авторским правом университета Эдинбурга, разработанных John F. Collins и Shane S. Sturrok, и распространяемых IntelliGenetics, Inc. (Mountain View, CA). Из этого набора пакетов можно использовать алгоритм Смита-Уотермана, где параметры по умолчанию используют для таблицы оценки (например, штраф за создание пропуска из 12 нуклеотидов, штраф за продление пропуска из одного, и пропуска из шести). Из сгенерированных данных величина "Match" отражает "идентичность последовательности". Другие подходящие программы для расчета процента идентичности или сходства между последовательностями, как правило, известны в данной области, например, другой программой выравнивания является BLAST, используемый с параметрами по умолчанию. Например, BLASTN и BLASTP можно использовать со следующими параметрами по умолчанию: генетический код = стандартный; фильтр = отсутствует; цепь =обе; порог = 60; ожидаемое = 10; матрица = BLOSUM62; описания = 50 последовательностей; сортировать по = наивысшей оценке; базы данных = не резервировано, GenBank + EMBL + DDBJ + PDB + GenBank CDS translations + Swiss белок + Spupdate + PIR. Подробности об этих программах хорошо известны в данной области.
Альтернативно, гомологию можно определять путем гибридизации полинуклеотидов в условиях, при которых образуются стабильные дуплексы между гомологичными областями, с последующим расщеплением нуклеазой/нуклеазами, специфичными по отношению к одноцепочечной ДНК, и определением размеров расщепленных фрагментов. Последовательности ДНК, которые, по существу, гомологичны можно выявлять в экспериментах с гибридизацией по Саузерну, например, при жестких условиях, установленных для этой конкретной системы. Определение подходящих условий гибридизации известно специалистам в данной области. См., например, Sambrook et al., выше; DNA Cloning, выше; Nucleic Acid Hybridization, выше.
Под термином "вырожденный вариант" понимают полинуклеотид, содержащий замены в последовательности его нуклеиновой кислоты, кодирующей полипептид с той же самой аминокислотной последовательностью, что и полипептид, кодирующийся полинуклеотидом, из которого получен вырожденный вариант.
"Кодирующая последовательность" или последовательность, которая "кодирует" выбранный полипептид, представляет собой молекулу нуклеиновой кислоты, которая транскрибируется (в случае ДНК) и транслируется (в случае мРНК) в полипептид in vivo, если она помещена под контроль соответствующих регуляторных последовательностей. Границы кодирующей последовательности определяют по старт-кодону на 5'- (амино) конце и стоп-кодону трансляции на 3'- (карбокси) конце. Последовательность терминации транскрипции может быть расположена в 3'-положении по отношению к кодирующей последовательности.
Под "вектором" подразумевают любой генетический элемент, такой как плазмида, фаг, транспозон, космида, хромосома, вирус, вирион и т.д., который способен к репликации, когда он связан с надлежащими контрольными элементами и который может переносить последовательности генов в клетки. Таким образом, термин включает носители для клонирования и экспрессии, а также вирусные векторы.
Под "рекомбинантным вектором" подразумевают вектор, который содержит гетерологичную последовательность нуклеиновой кислоты, способной к экспрессии in vivo.
Под "рекомбинантным вирусом" подразумевают вирус, который был генетически изменен, например, путем добавления или вставки конструкции гетерологичной нуклеиновой кислоты в частицу.
Термин "трансген" относится к полинуклеотиду, который вводят в клетку и который способен транскрибироваться в РНК и необязательно, транслироваться и/или экспрессироваться при подходящих условиях. В одном из аспектов, он придает желаемое свойство клетке, в которую он был введен, или в ином случае приводит к желаемому терапевтическому или диагностическому исходу.
Термины "геномные частицы (gp)" и "эквиваленты генома" при использовании по отношению к вирусному титру относятся к числу вирионов, содержащих ДНК генома рекомбинантного AAV, безотносительно к инфекционности или функциональности. Число геномных частиц в конкретном препарате вектора можно измерять известными в данной области способами, такими, как описанные, например, у Clark et al., Hum. Gene Ther. (1999) 10:1031-1039; и Veldwijk et al., Mol. Ther. (2002) 6:272-278.
Термины "единица инфекции (iu)" "инфекционная частица" или "единица репликации" при использовании по отношению к вирусному титру относятся к числу инфекционных частиц рекомбинантного вектора AAV, измеренному с помощью анализа инфицированных фокусов, также известного анализ фокусов репликации, как описано, например, у McLaughlin et al., J. Virol. (1988) 62:1963-1973.
Термин "единица трансдукции (tu)" при использовании по отношению к вирусному титру относится к числу инфекционных частиц рекомбинантного вектора cAAV, которые приводят к выработке функционального продукта трансгена, измеренному с помощью функциональных анализов, таких, как описанные, например, у Xiao et al., Exp. Neurobiol. (1997) 144:1 13-124; или in Fisher et al., J. Virol. (1996) 70:520-532 (анализ LFU).
Термин "трансфекция" используют по отношению к захвату чужеродной ДНК клеткой, и клетка является "трансфецированной", когда экзогенная ДНК введена внутрь клеточной мембраны. Ряд способов трансфекции, как правило, известен в данной области. См., например, Graham et al. (1973) Virology, 52:456, Sambrook et al. (1989) Molecular Cloning, a laboratory manual, Cold Spring Harbor Laboratories, New York, Davis et al. (1986) Basic Methods in Molecular Biology, Elsevier, and Chu et al. (1981) Gene13:197. Такие способы можно использовать для введения одной или нескольких экзогенных молекул ДНК в подходящие клетки-хозяева.
Термин "гетерологичный" по отношению к последовательностям нуклеиновой кислоты, таким как кодирующие последовательности и контрольные последовательности, обозначает последовательности, которые в норме не соединены вместе и/или которые в норме не связаны с конкретной клеткой. Таким образом, "гетерологичная" область конструкции нуклеиновой кислоты или вектора представляет собой сегмент нуклеиновой кислоты находящийся в составе или присоединенный к другой молекуле нуклеиновой кислоты, для которой не обнаружена ассоциация с другой молекулой в природе. Например, гетерологичная область конструкции нуклеиновой кислоты могла бы содержать кодирующую последовательность, фланкированную последовательностями, которые не находятся в ассоциации с кодирующей последовательностью в природе. Другим примером гетерологичной кодирующей последовательности является конструкция, где кодирующая последовательность сама по себе не обнаруживается в природе (например, синтетические последовательности с кодонами, отличными от нативного гена). Аналогично, клетка, трансформированная конструкцией, которая в норме не присутствует в клетке, могла бы считаться гетерологичной для целей по настоящему изобретению. Аллельная вариация или природные мутационные события не приводят к гетерологичной ДНК, используемой в настоящем документе.
Последовательность "нуклеиновой кислоты" относится к последовательности ДНК или РНК. Термин включает последовательности, которые содержат любые из известных аналогов оснований ДНК и РНК, в качестве неограничивающих примеров, такие как 4-ацетилцитозин, 8-гидрокси-N6-метиладенозин, азиридинилцитозин, псевдоизоцитозин, 5-(карбоксигидроксил-метил) урацил, 5-фторурацил, 5-бромоурацил, 5-карбоксиметиламинометил-2-тиоурацил, 5-карбоксиметил-аминометилурацил, дигидроурацил, инозин, N6-изопентениладенин, 1-метиладенин, 1-метилпсевдоурацил, 1-метилгуанин, 1-метилинозин, 2,2-диметил-гуанин, 2-метиладенин, 2-метилгуанин, 3-метилцитозин, 5-метилцитозин, N6-метиладенин, 7-метилгуанин, 5-метиламинометилурацил, 5-метокси-амино-метил-2-тиоурацил, бета-D-маннозилквеозин, 5'-метоксикарбонилметилурацил, 5-метоксиурацил, 2-метилтио-N6-изопентениладенин, метиловый эфир урацил-5-оксиуксусной кислоты, урацил-5-оксиуксусная кислота, оксибутоксозин, псевдоурацил, квеозин, 2-тиоцитозин, 5-метил-2-тиоурацил, 2-тиоурацил, 4-тиоурацил, 5-метилурацил, метиловый эфир урацил-5-оксиуксусной кислоты, урацил-5-оксиуксусная кислота, псевдоурацил, квеозин, 2-тиоцитозин и 2,6-диаминопурин.
Термин "контрольные последовательности" ДНК относится в обобщенном смысле к промоторным последовательностям, сигналам полиаденилирования, последовательностям терминации транскрипции, вышележащим регуляторным доменам, участкам начала репликации, внутренним участкам связывания рибосом ("IRES"), энхансерам и т.п., которые в совокупности обеспечивают репликацию, транскрипцию и трансляцию кодирующей последовательности в реципиентной клетке. Не все из этих контрольных последовательностей всегда должны присутствовать, при условии, что выбранная кодирующая последовательность способна реплицироваться, транскрибироваться и транслироваться в подходящей клетке-хозяине.
Термин "промотор" используют в настоящем документе в его обычном значении по отношению к нуклеотидной области, содержащей регуляторную последовательность ДНК, где регуляторная последовательность получена из гена, и способна связываться с РНК-полимеразой и инициировать транскрипцию нижележащей (3'-направление) кодирующей последовательности. Транскрипционные промоторы могут включать "индуцибельные промоторы" (где экспрессия полинуклеотидной последовательности, функционально связанная с промотором, индуцируется аналитом, кофактором, регуляторным белком и т.д.), "репрессируемые промоторы" (где экспрессия полинуклеотидной последовательности, функционально связанная с промотором, индуцируется аналитом, кофактором, регуляторным белком и т.д.) и "конститутивные промоторы".
"Функционально связанный" относится к перестройке элементов, где описанные таким образом компоненты сконфигурированы так, чтобы выполнять свою обычную функцию. Таким образом, контрольные последовательности, функционально связанные с кодирующей последовательностью, способны к воздействию на экспрессию кодирующей последовательности. Контрольные последовательности не обязательно должны быть смежными с кодирующей последовательностью, при условии, что они функционируют, чтобы направлять ее экспрессию. Таким образом, например, между промоторной последовательностью и кодирующей последовательностью могут присутствовать промежуточные нетранслируемые, но транскрибируемые последовательности, и промоторная последовательность все еще будет рассматриваться как "функционально связанная" с кодирующей последовательностью.
Под "изолированным" по отношению к белку или нуклеотидной последовательности подразумевается, что указанная молекула присутствует в условиях отсутствия по существу биологических макромолекул того же типа. Таким образом, например, "изолированная молекула нуклеиновой кислоты, которая кодирует конкретный полипептид" относится к молекуле нуклеиновой кислоты, которая по существу свободна от других молекул нуклеиновой кислоты, которые не кодируют указанный полипептид; однако молекула может содержать некоторые дополнительные основания или группы, которые не оказывают вредного воздействия на основные характеристики композиции.
С целью описания относительных положений нуклеотидных последовательностей в конкретной молекуле нуклеиновой кислоты на всем протяжении настоящей заявки, в случаях, когда конкретная нуклеотидная последовательность описана, как расположенная "выше" или "ниже" "3-штрих (3')" или "5-штрих (5')" относительно другой последовательности, следует понимать, что это положение последовательностей в "смысловой" или "кодирующей" цепи молекулы ДНК, которое обозначено, как общепринято в данной области.
Термин "приблизительно", в частности, по отношению к данному количеству, означает, что количество включает отклонения на плюс или минус пять процентов.
2. СПОСОБЫ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Перед подробным описанием настоящего изобретения, следует понимать, что это изобретение не ограничено конкретными составами или параметрами процессов, поскольку таковые, конечно, могут варьировать. Также следует понимать, что терминология, используемая в настоящем документе, предназначена только для описания конкретных вариантов осуществления изобретения и является неограничивающей.
Хотя в практическом осуществлении настоящего изобретения можно использовать ряд способов и материалов, аналогичных или эквивалентных тем, которые описаны в настоящем документе, предпочтительными материалами и способами являются описанные в настоящем документе.
Центральным местом в настоящем изобретении является открытие того, что ауринтрикарбоновая кислота (АТК) в микромолярных концентрациях увеличивает урожай вектора HSV-1. Этот факт является важным, как для широкомасштабного производства HSV, так и для выработки векторов rHSV и rAAV. Кроме того, неожиданно, что продемонстрировано в примерах, присутствие АТК в стоках rHSV-1 не оказывает негативного воздействия на урожай rAAV. Этот результат является неожиданным, поскольку известно, что АТК в миллимолярных количествах и в более высоких концентрациях является противовирусным средством (Cushman et al., J. Med. Chem. (1991) 34:329-337; Zhang et al., Antiviral Res. (1999) 43:23-35; Yap et al., Computational Biol. and Chem. (2005) 29:212-219; De Clercq, Advents, Advances, and Adventures Med. Res. Rev. (2011) 31:118-160).
Как упоминалось выше, исследователи сообщают о противовирусной активности оксида азота (NO) против некоторых вирусов, таких как вирус осповакцины, вирус везикулярного стоматита и вирус японского энцефалита, наряду с другими (Bi et al., J. Virol. (1995) 69:6466-6472; Harris et al., J. Virol. (1995) 69:910-915; Lin et al., 1997; Pertile et al., Avian Dis. (1996) 40:342-348). NO представляет собой свободнорадикальную газообразную молекулу и является медиатором иммунной системы (Croen K.D., J. Clin. Invest. (1993) 91:2446-2452; Karupiah et al., Science (1993) 261:145-1448; Rolph et al., Virol. (1996) 217:470-477; Amaro et al., J. Med. Virol. (1997) 51:326-331; Lane et al., J. Virol. (1997) 71:2202-2210). Заражение HSV способно вызывать экспрессию iNOS, гена, кодирующего индуцибельную изоформу NOS, которая производит большие количества NO.
Как показано в настоящем документе, АТК подавляет вызванное HSV увеличение экспрессии iNOS и, таким образом, повышает титры HSV. Дополнительные ингибиторы iNOS, в том числе дексаметазон и вальпроевая кислота, также имеют такой же эффект. В одном из вариантов осуществления, использование таких ингибиторов iNOS повышает титры рекомбинантного вируса герпеса в культуре, позволяя производить значительно больше вируса, чем производится в отсутствие конкретного ингибитора. Вирусы, произведенные по способу, можно использовать для различных целей, в том числе для профилактических, терапевтических и диагностических целей, а также для производства в достаточном количестве рекомбинантных конструкций для применения для получения рекомбинантных вирионов для доставки генов и генотерапии.
Ауринтрикарбоновая кислота (АТК), 5-((3-карбокси-4-гидроксифенил)(3-карбокси-4-оксо-2,5-циклогексадиен-1-илиден)метил)-2-гидроксибензойная кислота, представляет собой гетерогенную смесь несульфатированных отрицательно заряженных ароматических полимеров, которые образуются при обработке салициловой кислоты формальдегидом, серной кислотой и нитритом натрия (см. Cushman, et al., (1991) J. Med. Chem.34:329-337; Cushman, et al., J. Med. Chem. 34:337-342). Ауринтрикарбоновая кислота имеет формулу:
Было описано, что гетерогенная смесь АТК ингибирует взаимодействия белок-нуклеиновая кислота (Gonzalezet al., Biochim. Biophys. Acta, (1979) 562:534-545); взаимодействует со стероидными рецепторами на уровне захвата и связывания с ядром (Mellon, W. S., Biochem. Pharmacol. (1984) 33:1047-1057; Moudgilet al., J. Стероид Biochem. (1985) 23:125-132); нигибирует ДНК-полимеразу (Nakaneet al., Eur. J. Biochem. (1988) 177:91-96); и действует как ингибитор РНК-азы (Skidmoreet al., Biochem. J.(1989) 263:73-80).
Для добавления к вирусу в культуре можно использовать АТК в кислой форме или в виде соли, такой как тринатриевая соль ауринтрикарбоновой кислоты, кальциевая соль, аммонийная соль и т.д.
Дополнительные вещества, которые найдут применение в настоящих способах, включают дексаметазон (Dex) и вальпроевую кислоту (ВК). Было показано, что Dex ингибирует экспрессию iNOS в мезангиальных клетках крысы на транскрипционном и посттранскрипционном уровнях (Kunz et al., Biochem. J. (1994) 304:337-340; Kunz et al., Proc. Natl. Acad. Sci. USA (1996) 93:255-259). Также было показано, что Dex способствует oriL репликации ДНК HSV-1 в клетках PC12. Было показано, что вальпроат натрия, натриевая соль ВК, стимулирует репликацию HSV-1, цитомегаловируса человека, HIF-1, вируса герпеса-8 человека, вируса кори и полиовируса типа 1 (Motamedifar et al., Iran. J. Med. Sci. (2006) 31:28-32; Kuntz-Simon et al., J. Gen. Virol (1995) 76:1409-1415; Moog et al., J. Gen. Virol (1996) 77:1993-1999; Ylisastigui et al., AIDS (2004) 18:1101-1108; Shaw et al., AIDS (2000) 14:899-902; Kabiri et al. Iran J. Med. Sci. (2001) 26:55-61). Кроме того, было показано, что вальпроевая кислота ингибирует iNOS (Guo et al. Surgery (2007) 142:156-162). Как и в случае с АТК, в настоящих способах можно использовать ВК, или ее соли, такие как соли натрия, кальция, аммония и т.п.
Хотя в качестве примера в настоящем документе приведено использование АТК, Dex, и ВК для выработки векторов rHSV-1 в более высоких титрах, эти ингибиторы iNOS можно использовать для повышения титра множества вирусов в культуре, таких как, но не ограничиваясь ими, вирусы семейств Adenoviridae, Picornaviridae (например, полиовирусы и т.д.); Caliciviridae; Togaviridae (например, вирус краснухи, вирус лихорадки денге и т.д.); Flaviviridae; Coronaviridae; Reoviridae; Birnaviridae; Rhabodoviridae (например, вирус бешенства и т.д.); Poxviridae; Filoviridae; Paramyxoviridae (например, вирус эпидемического паротита, вирус кори, респираторно-синцитиальный вирус, и т.д.); Orthomyxoviridae (например, вирус гриппа типов A, B и C и т.д.); Bunyaviridae; Arenaviridae; различные вирусы гепатита, такие как HAV, HBV и HCV; вирусы папилломы и ротавирусы; ретровирусы; и т.д. См., например, Virology, 3rd Edition (W.K. Joklik ed. 1988); Fundamental Virology, 2nd Edition (B.N. Fields и D.M. Knipe, eds. 1991), для описания этих и других вирусов. Эти вирусы, или полученные из них иммуногены, можно использовать для производства вакцин и диагностики. Кроме того, некоторые из этих вирусов, и в частности, герпесвирусы, можно использовать для выработки рекомбинантных векторов для производства рекомбинантных вирионов для применения в способах доставки генов, описанных ниже.
Таким образом, АТК, Dex и ВК можно использовать для повышения урожая любого из герпесвирусов, которые являются членами семейства herpesviridae. Наряду с другими, оно включает вирус конского герпеса, вирус бычьего герпеса (BHV) и вирус простого герпеса (HSV) человека типов 1 и 2, такие как BHV-1, BHV-2, HSV-1 и HSV-2, вирус ветряной оспы (VZV), вирус Эпштейна-Барр (EBV), цитомегаловирус (CMV), HHV6 и HHV7. Герпесвирусы можно получать из любого из множества штаммов. Например, если при помощи изобретения получают вирус HSV, вирус можно получать, например, из HSV-1 или HSV-2, и можно из любого из различных штаммов HSV, таких как HSV-1 штамм KOS, HSV-1 штамм McIntyre, HSV-1 штамм Patton, HSV-2 штамм 333, HSV-2 штамм G и т.п. Кроме того, получаемые вирусы могут быть вирусами дикого типа или их производными, включая рекомбинантные вирусы, и межтиповыми рекомбинантами, содержащими ДНК из HSV-1 и HSV-2. Производные предпочтительно имеют, по меньшей мере, 70% гомологию последовательности с геномами HSV-1 или HSV-2 или с их частями, более предпочтительно, по меньшей мере, 80%, даже более предпочтительно, по меньшей мере, 90 или 95%. Производное может иметь последовательность генома HSV-1 или HSV-2, модифицированную нуклеотидными заменами, например, от 1, 2 или 3 до 10, 25, 50 или 100 замен. Геном HSV-1 или HSV-2 может быть модифицирован альтернативно или дополнительно за счет одной или нескольких вставок и/или делеций и/или за счет удлинения с одного или с обоих концов.
Другие производные включают штаммы, которые уже имеют мутации в генах, в частности, мутации в генах, которые приводят к ослаблению вируса. Примеры таких вирусов включают штамм 1716 (MacLean et al., J. Gen. Virol. (1991) 72:632-639), штаммы R3616 и R4009 (Chou и Roizman, Proc. Natl. Acad. Sci USA (1992) 89: 3266-3270) и R930 (Chou et al., J. Virol. (1994) 68:8304-8311), которые все имеют мутации в ICP34.5, штамм d120, который имеет делецию в ICP4 (DeLuca et al.,J. Virol. (1985) 56:558-570), штамм d27-1 (Rice and Knipe, J. Virol. (1990) 64: 1704-1715), который имеет делецию в ICP27) или штамм d92, который имеет делецию в ICP27 и ICP4 (Samaniego et al., J. Virol. (1995) 69:5705-5715). Терминологию, которую используют при описании различных генов HSV можно найти, например, у Coffin и Latchman (1996), In: Genetic Manipulation of Nervous System (DS Latchman Ed.) pp 99-114: Academic Press, London.
Очевидно, что в изобретении можно использовать любой rHSV, подходящий по назначению. В определенных вариантах осуществления rHSV, который используют по изобретению, является дефицитным по репликации. Для выработки вирионов rAAV предпочтительна инфекция клеток-продуцентов при помощи rHSV, который неспособен к репликации, поскольку в отличие от способов, включающих использование аденовируса, rHSV не становится значительным загрязнителем продукта rAAV. Это может служить увеличению конечного урожая вирионов rAAV за счет удаления этапов очистки, связанных с удалением аденовируса. В конкретном варианте осуществления изобретения rHSV конструируют из мутанта HSV-1, в котором неспособность к репликации вызвана делецией в гене ICP27. Для конструкции rHSV также можно использовать любых других подходящих мутантов HSV, демонстрирующих фенотип, дефицитный по репликации.
Одним особенно предпочтительным рекомбинантным мутантным штаммом HSV-1 для выработки rAAV с использованием рассматриваемых способов является штамм d27-1 HSV-1. Этот штамм можно получать, как описано, например, у Conway et al., Gene Ther. (1999) 6:973 985 и в патенте США № 7091029, полностью включенным в настоящий документ в качестве ссылки. Как описано выше, этот мутантный вектор не вырабатывает ICP27 и преимущественно используется для продукции вирионов rAAV, поскольку известно, что сплайсинг мРНК в клетке-хозяине ингибируется ICP27. ICP27 может также воздействовать на соответствующий сплайсинг мРНК rep и cap AAV-2. Этот вектор является дефицитным по репликации и демонстрирует сниженную цитотоксичность по сравнению с HSV-1 дикого типа (wt). Вирус d27-1 демонстрирует несколько других характеристик, которые являются благоприятными для применения в качестве вируса-помощника для продукции вирионов rAAV. Во-первых, он экспрессирует ранние гены, о которых известно, что они необходимы для продукции rAAV (Weindler et al., J. Virol. (1991) 65:2476-2483). Кроме того, d27.1 имеет повышенную экспрессию ICP8, белка, связывающегося с одноцепочечной ДНК, который является продуктом UL29, одного из генов HSV-1, необходимых для репликации и упаковки AAV (Weindler et al., J. Virol. (1991) 65:2476-2483).
Геном AAV представляет собой линейную одноцепочечную молекулу ДНК, содержащую приблизительно 4681 нуклеотидов. Геном AAV, как правило, содержит внутренний геном без повторов, фланкированный с каждого конца инвертированными концевыми повторами (ITR). ITR составляет приблизительно 145 пар оснований (п.н.) в длину. ITR имеют множество функций, включая обеспечение точек начала репликации ДНК и сигнала упаковки для вирусного генома. Внутренняя часть генома без повторов содержит две больших открытых рамки считывания, известных как гены репликации (rep) и капсида (cap) AAV. Гены rep и cap кодируют вирусные белки, которые позволяют вирусу реплицироваться и упаковываться в вирион. В частности, с области rep AAV экспрессируется семейство, по меньшей мере, из четырех вирусных белков, Rep 78, Rep 68, Rep 52 и Rep 40, названные соответственно их явной молекулярной массе. Область cap AAV кодирует по меньшей мере три белка, VPI, VP2, и VP3.
Под "кодирующей областью rep AAV" подразумевают принятую в данной области область генома AAV, которая кодирует белки репликации Rep 78, Rep 68, Rep 52 и Rep 40. Показано, что эти продукты экспрессии Rep обладают множеством функций, включая, распознавание, связывание и одноцепочечный разрыв в точке начала репликации ДНК AAV, ДНК-хеликазную активность и модуляцию транскрипции с AAV (или других гетерологичных) промоторов. Продукты экспрессии Rep все вместе необходимы для репликации генома AAV. Для описания кодирующей области rep AAV, см., например, Muzyczka, N. (1992) Current Topics in Microbiol, and Immunol.158:97-129: и Kotin, R.M. (1994) Human Genotherapy 5:793-S0. Подходящие гомологи кодирующей области rep AAV включают ген rep вируса герпеса 6 (HHV-6) человека, который также известен тем, что опосредует репликацию ДНК AAV-2 (Thomson et al. (1994) Virology 204:304-311).
Под "кодирующей областью cap AAV" подразумевают принятую в данной области область генома AAV, которая кодирует белки капсида VP1, VP2, и VP3, или их функциональные гомологи. Эти продукты экспрессии Cap обеспечивают функции упаковки, которые совместно необходимы для упаковки вирусного генома. Для описания кодирующей области cap AAV, см., например, Muzyczka, N. и Kotin, R.M. (выше).
Как правило, для получения вирионов rAAV будут использоваться два вектора rHSV. Один представляет собой вектор rHSV с хелперной функцией, в котором гены rep и/или cap AAV введены в геном rHSV. Другой представляет собой экспрессирующий вектор rHSV, в котором последовательности ITR из AAV были введены в геном rHSV и фланкируют интересующий ген.
Таким образом, в одном из вариантов осуществления можно использовать ингибитор iNOS для повышения урожая первого вектора rHSV, который содержит гены rep и/или cap AAV. Варианты осуществления первого вектора rHSV по способу в качестве неограничивающих примеров включают генетические конструкции на основе гена cap, обнаруженного в различных серотипах AAV, включая AAV-1, AAV-2, AAV-3, AAV-4, AAV-5 и AAV-6, AAV-7 и AAV-8, козий и бычий AAV (см., например, публикацию США. No. 20080292595, полностью включенную в настоящий документ в качестве ссылки), и их варианты. Также в пределе объема изобретения находятся гены rep и cap из новых серотипов AAV, и гены rep и cap, модифицированные путем рекомбинации или мутации существующих серотипов. Гены rep и cap вектора AAV с хелперной функцией можно получать из любых известных серотипов AAV, как описано выше. Например, вектор rHSV с хелперной функцией может иметь ген rep, полученный из AAV-2 и ген cap, полученный из AAV-6; специалист в данной области будет понимать, что возможны и другие сочетания генов rep и cap, определяющей чертой является способность поддерживать производство вирионов rAAV.
В определенных вариантах осуществления гены rep и cap AAV в векторе rHSV с хелперной функцией могут находиться под управлением их нативных промоторов. Промоторы p5 и p19 AAV-2 контролируют экспрессию Rep 78 и 68 и Rep 52 и 40, соответственно. Промотор p40 контролирует экспрессию VP1, VP2 и VP3. Кроме того, для управления экспрессией генов AAV можно использовать гетерологичные промоторы. Примеры других промоторов, которые можно использовать в описанных способах в качестве неограничивающих примеров включают ранний промотор SV40, промотор CMV, промотор тимидинкиназы HSV-1 (HSV-1 tk), индуцибельный промотор металлотионина, промотор вируса опухоли молочной железы мыши и промотор β-актина курицы.
Генетическая конструкция может быть вставлена в любой сайт или сайты генома HSV, подходящие для интеграции генов rep и cap. В определенных вариантах осуществления вектор конструируют путем гомологичной рекомбинации генов rep и cap AAV в локус тимидинкиназы (tk) вируса rHSV-1, как описано в Conway et al., Gene Ther. (1999) 6:986-993 и патенте США № 7091029, полностью включенных в настоящий документ в качестве ссылки.
Как описано в настоящем документе, вектор rHSV с хелперной функцией кодирует последовательности "AAV с хелперной функцией" (т.е., rep и cap), которые функционируют в транс-положении для продуктивной репликации AAV и упаковки в капсид. Предпочтительно, вектор rHSV с хелперной функцией поддерживает эффективное производство вирионов rAAV без создания каких-либо выявляемых вирионов AAV дикого типа (т.е., вирионов AAV, содержащих функциональные гены rep и cap). Примером такого вектора является rHSV-1 d27.1rc. Вектор и способы его получения описаны в настоящем документе в примерах, а также в Conway et al., Gene Ther. (1999) 6:986-993; и патенте США № 7091029, полностью включенных в настоящий документ в качестве ссылки.
Второй вектор rHSV обозначается экспрессирующий вектор rHSV и содержит ITR из AAV с одним или несколькими интересующими генами под управлением одного или нескольких промоторов. В некоторых вариантах осуществления интересующий ген вставлен между парой ITR. Гетерологичный ген, как правило, функционально связан с гетерологичным промотором (конститутивным, клеточно-специфичным, или индуцибельным), способным управлять экспрессией гена в клетках-мишенях пациента при подходящих условиях. Можно также включать сигналы терминации, такие как сайты полиаденилирования.
Нуклеотидные последовательности областей ITR AAV известны. См., например, Kotin, R.M. (1994) Human Genotherapy 5:793-801; Berns, K.I. "Parvoviridae and their Replication" in Fundamental Virology, 2nd Edition, (B.N. Fields and D.M. Knipe, eds.) для последовательности AAV-2. ITR AAV, используемые в векторах по изобретению необязательно должны иметь нуклеотидную последовательность дикого типа, и ее можно изменять, например, путем вставки, делеции или замены нуклеотидов. Кроме того, ITR AAV могут быть получены из любого из нескольких серотипов AAV, включая в качестве неограничивающих примеров, AAV-1, AAV-2, AAV-3, AAV-4, AAV-5, AAV-6, AAV-7 и AAV-8, козий и бычий AAV (см., например, публикацию США. No. 20080292595, полностью включенную в настоящий документ в качестве ссылки), и их варианты. Кроме того, 5'- и 3'-ITR, которые фланкируют выбранную нуклеотидную последовательность в экспрессирующем векторе необязательно должны быть идентичны или получены из одного серотипа или изолята AAV, при условии, что они функционируют подобающим образом, т.е., позволяют вырезать и извлекать интересующие последовательности из генома клетки-хозяина или вектора, и вводить молекулу ДНК в геном реципиентной клетки, когда продукты генов rep AAV присутствуют в клетке.
ITR AAV можно вырезать из вирусного генома или из вектора AAV, содержащего их, и сливать с 5' и 3' концами выбранной конструкции нуклеиновой кислоты с использованием стандартных способов лигирования, таких как описанные в Sambrook et al., выше. Например, лигирование можно проводить в 20 мМ Tris-Cl с pH 7,5, 10 мМ MgCl2, 10 мМ DTT, 33 мкг/мл БСА, 10 мМ-50 мМ NaCl, и либо с 40 мкМ АТФ, 0,01-0,02 (Weiss) единиц T4 ДНК-лигазы при 0°C (для лигирования с "липкими концами") или с 1 мМ АТФ, 0,3-0,6 (Weiss) единиц T4 ДНК-лигазы при 14°C (для лигирования с "тупыми концами"). Межмолекулярное лигирование с "липкими концами", как правило, проводят при общей концентрации ДНК 30-100 мкг/мл (5-100 нМ общая концентрация концов). Векторы AAV, которые содержат ITR, были описаны, например, в патенте США no. 5139941. В частности, некоторые векторы AAV, описанные в том патенте, доступны в Американской коллекции типовых культур ("ATCC") под номерами доступа 53222, 53223, 53224, 53225 и 53226.
Выбранная полинуклеотидная последовательность функционально связана с контрольными элементами, которые направляют ее транскрипцию или экспрессию у рассматриваемых клеток. Такие контрольные элементы могут включать контрольные последовательности, в норме связанные с выбранным геном. Альтернативно, можно использовать гетерологичные контрольные последовательности. Подходящие гетерологичные контрольные последовательности, как правило, включают те, которые получены из последовательностей, кодирующих гены вирусов или млекопитающих. Примеры в качестве неограничивающих примеров включают, промотор нейронспецифичной енолазы, промотор GFAP, ранний промотор SV40, промотор LTR вируса опухоли молочной железы мыши; основной поздний промотор аденовируса (Ad MLP); промотор вируса простого герпеса (HSV), промотор цитомегаловируса (CMV), такой как область предраннего промотора CMV (CMVIE), промотор вируса саркомы рауса (RSV), синтетические промоторы, гибридные промоторы и т.п. Кроме того, последовательности, полученные из не вирусных генов, таких как ген металлотионеина мыши, также найдут применение в настоящем документе. Такие промоторные последовательности коммерчески доступны, например, у StrATKgene (San Diego, CA), Invivogen (San Diego, CA) и других.
Интересующий ген может быть геном, имеющим, по-видимому, терапевтическую ценность. Примеры терапевтических генов в качестве неограничивающих примеров включают α-1 антитрипсин, Фактор VIII, Фактор IX, GAA, эритропоэтин и PEDF. Если необходимо провести отбор или выявить успешную трансэкспрессию гена, ген, представляющий интерес, может быть репортерным геном. Известно множество примеров генов, которые используются в качестве репортерных или для отбора и которые можно использовать в изобретении. Эти гены в качестве неограничивающих примеров включают гены, кодирующие β-галактозидазу, неомицин, фосфоротрансферазу, хлорамфеникол ацетилтрансферазу, тимидинкиназу, люциферазу, бета-глюкуронидазу, аминогликозид, фосфотрансферазу, гигромицин B, ксантин-гуанин фосфорибозил, люциферазу, DHFR/метотрексат, и зеленый флуоресцентный белок (GFP).
Экспрессионный вирус rHSV-1 можно получать во многом таким же образом, как описано выше, а именно, путем гомологичной рекомбинации в ген tk HSV-1, как описано, например, в Conway et al., Gene Ther. (1999) 6:986-993 и патенте США № 7091029, полностью включенным в настоящий документ в качестве ссылки.
После получения векторы rHSV или любой другой вирус, представляющий интерес, выращивают в культуре в подходящей линии клеток. Для герпесвирусов, такие линии клеток в качестве неограничивающих примеров включают, клетки Vero, клетки 293, клетки HeLa, и т.п., доступные в Американской коллекции типовых культур, Rockville, Md. Если используют вектор HSV-1 d27.1, то этот вирус, как правило, культивируют в ICP27-дополненной линии клеток V27 (Рис et al., J. Virol. (1990) 64: 1704-1715). Можно использовать любую подходящую среду для вирусов, рассматриваемую в данном документе, с сывороткой или без, такой как эмбриональная телячья сыворотка, такую как, без ограничений, среда RPMI 1640, модифицированная Дульбекко среда Игла (DMEM), среда F12 или смесь последних (среда DF). Если присутствует сыворотка, культура может содержать, например, от 2% до 20% сыворотки, больше, как правило, от 5% до 15% сыворотки, от 7% до 12% сыворотки, или любое число в пределах этих диапазонов, такое как 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14%, 15%, и т.п. Кроме того, если используют сыворотку, она может присутствовать в исходной культуре, и/или в последующей свежей среде, которую добавляют к культурам.
Количество ингибитора iNOS, который добавляют в способе по изобретению, может варьировать и представляет собой конкретную величину, зависящую от используемого конкретного ингибитора, используемой среды и культивируемого вируса. Например, если герпесвирусы культивируют в клетках Vero, концентрация АТК в начальной культуре, если АТК присутствует, будет, как правило, составлять от 5 мкМ до 500 мкМ, предпочтительно от 10 мкМ до 250 мкМ, такая как от 20 мкМ до 100 мкМ, т.е., от 30 мкМ до 75 мкМ, такая как 30..35..40..45..50..55..60..65..70..75, и т.д. или любое целое число в пределах этих установленных диапазонов. Аналогично, концентрация дексаметазона, если он присутствует, в начальной культуре будет, как правило, составлять от 1 мкМ до 500 мкМ, предпочтительно от 5 мкМ до 250 мкМ, такая как от 1 мкМ до 100 мкМ, т.е., от 5 мкМ до 75 мкМ, такая как 1..5..15..10.. 20..25..30..35..40..45..50..55..60..65..70..75, и т.д. или любое целое число в пределах этих установленных диапазонов. Если используют вальпроевую кислоту, исходная концентрация будет составлять от 1 мМ до 500 мМ, предпочтительно от 5 мМ до 250 мМ, такая как от 1 мМ до 100 мМ, т.е., от 5 мМ до 75 мМ, такая как 1..5..15..10..20..25..30..35..40..45..50..55..60..65..70..75, и т.д. или любое целое число в пределах этих установленных диапазонов.
В определенных вариантах осуществления зараженные вирусом клетки исходно культивируют в среде, описанной выше, от 0,5 часов до 24 часов, от 0,75 часов до 12 часов, от 1 часа до 5 часов, от 1 часа до 2 часов, или любое число часов или их долей в пределах этих диапазонов. Ингибитор iNOS и/или сыворотка могут присутствовать или отсутствовать в исходной культуре. Затем добавляют свежую среду и культуры инкубируют от 24 до 120 часов, от 48 до 96 часов, от 50 до 80 часов, от 60 до 75 часов, от 70 до 74 часов, или любое число часов или их долей в пределах этих диапазонов. Ингибитор iNOS и/или сыворотка могут присутствовать или отсутствовать в последующей культуре, при условии, что ингибитор iNOS присутствует или в одной из них или в обеих из исходной культуры и последующей культуры.
В некоторых вариантах осуществления ингибитор iNOS присутствует в исходной культуре в более высокой концентрации, чем в последующей культуре. Таким образом, например, если ингибитор iNOS представляет собой АТК, он может присутствовать в количестве от 30 до 75 мкМ в исходной культуре, а затем от 5 до 25 мкМ в последующей культуре. Альтернативно, ингибитор может присутствовать только в исходной или последующей культуре.
Как показано в примерах ниже, один особенно предпочтительный способ с использованием АТК включает наличие 50 мкМ АТК в исходной культуре, с уменьшением количества АТК в последующей культуре до 20 мкМ. Кроме того, в случае АТК, предпочтительно включение сыворотки одновременно с наличием АТК. Таким образом, если АТК добавляют к исходной культуре, полезно добавлять эмбриональную телячью сыворотку (ЭТС) в среду. Сходно, если АТК добавляют к последующей культуре, для получения более высоких урожаев вируса необходимо добавление ЭТС.
Вирусы затем культивируют для получения желаемого титра вируса. Например, в случае векторов HSV-1 d27-1, описываемых в настоящем документе, АТК повышает урожаи d27-l в супернатантах клеток V27 в 3-5 раз, и титры могут составлять, по меньшей мере, 1×108 БОЕ/мл или 4×108 DRP/мл. Аналогично, АТК также повышает урожаи вирусов дикого типа (wt) HSV-1 штаммов McIntyre и KOS на 1 лог, и титры 293 или Vero могут вырасти вплоть до 1×109 DRP/мл. Вирусы затем собирают для дальнейшего использования.
Для целей изобретения, подходящие клетки-хозяева для получения вирионов rAAV включают микроорганизмы, дрожжевые клетки, клетки насекомых, и клетки млекопитающих, которые используются или могут быть использованы в качестве реципиентов гетерологичной молекулы ДНК и которые способны к росту, например, в суспензионной культуре, колбах, планшетах, биореакторе или т.п. Термин включает потомство исходной клетки, которая была трансфецирована. Таким образом, "клетка-хозяин", применяемая в настоящем документе, как правило, относится к клетке, которая была трансдуцирована экзогенной последовательностью ДНК. Если рекомбинантные герпесвирусы для применения в производстве вирионов rAAV получают в одном типе клеток, собранные векторы затем трансфецируют в другую подходящую клетку-хозяина. Клетки 293, происходящие из стабильной клеточной линии человека, (легко доступны, например, в Американской коллекции типовых культур под номером доступа ATCC CRL1573) являются предпочтительными клетками-хозяевами для получения вирионов rAAV. В частности, клеточная линия человека 293 представляет собой линию клеток эмбриональной почки человека, которая была трансформирована фрагментами ДНК аденовируса типа 5 (Graham et al. (1977) J. Gen. Virol. 36:59), и экспрессирует аденовирусные гены E1a и E1b (Aiello et al. (1979) Virology 94:460). Линия клеток 293 легко трансфецируется, и обеспечивает особенно подходящую платформу для получения вирионов rAAV.
Хелперные функции AAV вводят в клетку-хозяина путем трансдукции клетки-хозяина конструкцией rHSV с хелперной функцией или до или одновременно с использованием экспрессирующего вектора rHSV. Таким образом, хелперные конструкции rHSV используют для обеспечения, по меньшей мере, транзиторной экспрессии генов rep и/или cap AAV для восполнения утраченных функций AAV, которые необходимы для продуктивной инфекции AAV. В хелперных конструкциях AAV отсутствуют ITR AAV, и они не могут самостоятельно ни реплицироваться, ни упаковываться.
После репликации рекомбинантного AAV вирионы rAAV можно очищать от клетки-хозяина при помощи множества общепринятых способов очистки, таких как хроматография на колонках, градиенты CsCl и т.п. Например, можно использовать многоэтапную очистку на колонках, такую как очистка на анионообменной колонке, аффинной колонке и/или катионообменной колонке. См., например, Международную Публикацию WO 02/12455.
Полученные вирионы rAAV, которые содержат нуклеотидную последовательность, представляющую интерес, можно затем использовать для доставки генов при помощи способов, хорошо известных в данной области и описанных, например, в патентах США №№ 5173414 и 5139941; международных публикациях WO 92/01070 (опубликована 23 января 1992 года) и WO 93/03769 (опубликована 4 марта 1993 года); Lebkowski et al., Molec. Cell. Biol. (1988) 8:3988-3996; Vincent et al., Vaccines 90 (1990) (Cold Spring Harbor Laboratory Press); Carter, B.J. Current Opinion in Biotechnology (1992) 3:533-539; Muzyczka, N. Current Topics in Microbiol. and Immunol. (1992) 158:97-129; Kotin, R.M. Human Gene Therapy (1994) 5:793-801; Shelling and Smith, Gene Therapy (1994) 1:165-169; and Zhou et al., J. Exp. Med. (1994) 179:1867-1875.
2. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Ниже приведены примеры конкретных вариантов осуществления для проведения настоящего изобретения. Примеры предлагаются исключительно с иллюстративными целями, и никоим образом не предназначены для ограничения объема настоящего изобретения.
Были предприняты усилия, чтобы обеспечить точность в отношении используемых чисел (например, количества, температуры, и т.д.), но, конечно, следует сделать поправку на некоторые экспериментальные ошибки и отклонения.
Материалы и Способы
Клетки
Vero-производные клетки V27 (Рис et al., J. Virol. (1989) 63:3399-3407) и клетки 293, производные клеток эмбриональной почки человека (HEK) (Graham et al., J. Gen. Virol. (1977) 36:59-74) получали от Applied Genetic Technologies Corporation (AGTC, Alachua, FL), Vero и клетки HeLa приобретали в Американской коллекции типовых культур (ATCC, Manassas, VA). Все клетки поддерживали в модифицированной Дульбекко среде Игла (DMEM; HyClone, South Logan, UT), содержащей 10% эмбриональную телячью сыворотку (ЭТС; HyClone) и либо генетицин (50 мг/мл; Invitrogen) для клеток V27 или 1% пенициллин/стрептомицин (Cellgro Mediatech, Manassas, VA) для других клеток.
Выработка HSV-1
Штамм KOS HSV-1 дикого типа и ICP27-дефицитные производные штамма KOS HSV-1 дикого типа: векторы d27-1 (Rice and Knipe, J. Virol. (1990) 64: 1 04-1715), rHSV-rep2/cap2 и rHSV-EGFP (Kang et al. Gene Ther. (2009) 16:229-239) и их продуцент ICP27-дополненную линию клеток V27 получали от AGTC (Alachua, FL). Штамм Maclntyre HSV-1 дикого типа, приобретенный у Advanced Biotechnologies Inc. (ABI, Columbia MD) и штамм KOS HSV-1 дикого типа (wtHSV-1 KOS) выращивали в линиях клеток Vero, 293 или HeLa. Собирали инфекционные векторные частицы через 72 часа после заражения путем извлечения супернатанта культуры. Титры стоков HSV-1 в частицах, устойчивых к ДНКазам/мл (DRP/мл) определяли посредством анализа Taqman. Вирусные геномы в неочищенной среде для культивирования количественно определяли путем обработки в присутствии ДНКазы I (50 Ед/мл конечная концентрация; Promega) при 37°C в течение 60 мин, с последующим расщеплением протеиназой K (Invitrogen) (1 Ед/мл) при 50°C в течение 60 мин, а затем денатурации при 95°C в течение 30 мин.
Линеаризованную плазмиду pZero 195 UL36 (полученную от AGTC, Inc., Alachua, FL) использовали для получения стандартных кривых. Следующий набор праймеров-зондов был специфическим для последовательности UL36 векторного генома (HSV-UL36 F: 5'- GTTGGTTATGGGGGAGTGTGG (SEQ ID NO: 1); HSV-UL36 R: 5'-TCCTTGTCTGGGGTGTCTTCG (SEQ ID NO:2); HSV-UL36 Зонд: 5'-6FAM- CGACGAAGACTCCGACGCCACCTC-TAMRA (SEQ ID NO:3). Амплификацию ПЦР-продукта проводили со следующими параметрами цикла: 1 цикл при 50°C в течение 2 мин, 1 цикл при 95°C в течение 10 мин; 40 циклов с 95°C в течение 15 сек, и 60°C в течение 60 сек.
Эксперименты с АТК
Исходный раствор АТК (Sigma-A1895 Ауринтрикарбоновая кислота, практическая чистота >85% (титрация), порошок) получали как концентрацию 500 мкМ в водном растворе 100 мМ бикарбоната натрия. Исходный раствор АТК затем разводили в DMEM+/-10% эмбриональной телячьей сыворотки (ЭТС, Hyclone, Waltham, MA) в диапазоне концентраций 12-60 мкМ АТК (8,5-21 мкг АТК /мл). Проводили заражение HSV-1 с множественностью заражения 0,15 (MOI=0,15) (как правило, 6×105 клеток в 6-луночном планшете) в 40% (2/5 объема) от общего конечного объема среды в течение 1-2 часов и добавляли оставшуюся среду (60% или 3/5 от общего конечного объема) во время этапа разведения. Клетки затем инкубировали в течение 72 часов и собирали супернатант для проведения анализа бляшкообразующих единиц на миллилитр (БОЕ/мл) и анализа титра DRP/мл.
Эксперименты с дексаметазоном (Dex)
Дексаметазон (Sigma-D4902) растворяли до 2 мг/мл в абсолютном спирте. Потом разбавляли DMEM для получения концентрации 1M и хранили при 20°C.
Клетки V27 высевали в 6-луночные планщеты за сутки до заражения с концентрацией 6×105 клеток/лунку. Добавляли дексаметазон до получения концентрации 1 мкМ в среду для посева. Хорошо смешивали и добавляли в лунки.
Отбирали среду и добавляли инфекционный сток HSV-1 d27-1 с MOI 0,15 (= плотность посева клеток × 0,15/титр БОЕ стока HSV) на 1 мл DMEM (без добавок). Добавляли 1 мл инфекционного инокулята на лунку. Инкубировали в течение 1-2 часов при 37°C, в инкубаторе 5% CO2, после чего добавляли 1,5 мл DMEM-10% с ЭТС. Культуры возвращали в инкубатор на 70-74 часа.
Свободную среду собирали, вортексировали, центрифугировали при 1,100 × g в течение 10 минут при 4°C. Супернатант переносили в новую дозированную пробирку, вортексировали, делали аликвоты и замораживали стоки при -80°C.
Эксперименты с вальпроевой кислотой (ВК)
Вальпроевую кислоту (Sigma-P4543) растворяли до концентрации 1M в воде. Клетки V27 высевали в 6-луночные планщеты за сутки до заражения с концентрацией 6×105 клеток/лунку. 1M вальпроевую кислоту добавляли в 1 мл DMEM-10% с ЭТС для получения концентрации 5 мкМ. Хорошо вортексировали и добавляли в лунки. Планшеты инкубировали в течение шести часов, отбирали среду и добавляли инфекционный сток HSV-1 d27-1 с MOI 0,15 (= плотность посева клеток × 0,15/титр БОЕ стока HSV) на 1 мл DMEM (без добавок).
Добавляли 1 мл инфекционного инокулята на лунку и инкубировали в течение 1-2 часов при 37°C, в инкубаторе 5% CO2, после чего добавляли 1,5 мл DMEM-10% с ЭТС. Культуры возвращали в инкубатор на 70-74 часа. Свободную среду собирали, вортексировали, центрифугировали при 1,100 × g в течение 10 минут при 4°C. Супернатант переносили в новую дозированную пробирку, вортексировали, делали аликвоты и замораживали стоки при -80°C.
Производство rAAV
Клетки 293 (2,5×106) одновременно заражали совместно векторами rHSV-rep2/cap2 и rHSV-EGFP, как описано Kang et al., Gene Ther (2009) 16:229-239. Через 2-4 часа после заражения инфицированную среду заменяли DMEM +10% ЭТС, в объеме эквивалентном двойному объему культуры до заражения. В момент сбора клеток клеточный осадок замораживали при -80°C. Титры DRP количественно определяли путем полимеразной цепной реакции в реальном времени (qPCR) в термоциклере с 96-луночным блоком (Applied Biosystems; 7500 Real Time PCR system). Неочищенные образцы подвергали трем циклам замораживания-оттаивания, затем инкубировали в присутствии Бензоназы (250U/мл), 2 мМ MgCl2, Tween 80 (Calbiochem) с конечной концентрацией 1% и инкубировали при 37°C в течение 60 мин, с последующим расщеплением 0,25% Трипсином (Gibco) при 50°C в течение 60 мин. Наконец, обрабатывали ДНКазой I (50 Ед/мл; Promega) при 37°C в течение 30 мин, а затем денатурировали при 95°C в течение 20 мин. Линеаризованную плазмиду pDC67/+SV40 использовали для получения стандартных кривых. Следующий набор праймеров-зондов был специфическим для поли(A)-последовательности вируса обезьян 40 (SV40): rAAV-F: 5'-AGCAATKGCATCACAAATTTCACAA-3' (SEQ ID NO:4); rAAV-R: 5'-GCAGACATGATKAGATKCATTGATGAGTT-3' (SEQ ID NO:5); rAAV-зонд: 5'-6-FAM-AGCATTTTTTTCACTGCATTCTAGTTGTGGTTTGTC-TAMRA-3' (SEQ ID NO:6). Амплификацию ПЦР-продукта проводили со следующими параметрами цикла: 1 цикл при 50°C в течение 2 мин, 1 цикл при 95°C в течение 10 мин; 40 циклов с 95°C в течение 15 сек, и 60°C в течение 60 сек.
Анализ генома человека (Human Genome Array)
Конфлюэнтные клетки 293 (2,4×106 клеток в колбе объемом 75 см2) культивировали в DMEM+10% ЭТС в течение приблизительно 20 часов и затем заражали одной бляшкообразующей единицей на клетку (БОЕ/клетку) штамма Maclntyre HSV-1 в течение 90 минут. Через 90 минут после заражения добавляли АТК в концентрации 20 мкМ (конечной). Зараженные клетки собирали через 24 час после заражения. Выделяли из суспензии тотальную РНК в подходящем количестве и качестве с использованием набора RNeasy Plus Mini Kit (QIAGEN, Valencia, CA) по инструкциям производителя. Полногеномное определение профиля экспрессии проводили на Affymetrix Human U133 Plus 2.0 Array от Asuragen, Inc. В качестве исходного материала использовали 3 мкг тотальной РНК.
В общем, качество РНК, оцененное на биоанализаторе, имело значения RI >9. Гибридизационный анализ и коэффициенты масштабирования находились в диапазоне прохождения контроля качества. После сканирования, необработанные файлы экспрессии CEL обрабатывали при помощи Affymetrix Expression Console vs.1.1.2 (affymetrix.com). Каждый файл CEL был обработан Robust Multichip Analysis (RMA), и обобщенная таблица была экспортирована в виде текстового файла. Все последующие геномные и статистические анализы были сделаны при помощи JMP Genomics (версия 5) (jmp.com/software/genomics). Сначала, использовали этап фильтрации для отсева низкой экспрессии, конкретно, значений ниже 6 в режиме log2, по меньшей мере, в 2 из 8 образцов. Из всех 54,675 зондов Affy U133 Plus2, 41,569 (76%) зондов остались после отсева. Также наблюдали два положительных контроля, головной мозг человека и объединенную универсальную референсную РНК человека, соответственно, которые хорошо гибридизовались. Из дальнейшего анализа эти два образца были исключены.
Метод главных компонент выявил две различных популяции, а именно, образцы, обработанные и необработанные HSV. Выделение первой главной компоненты (91,7%), таким образом, объясняется влиянием HSV по сравнению с контрольным растворителем. Данные были нормализованы по среднему по каждой пробе для получения среднего сигнала, равного 0. Проводили дисперсионный анализ (ANOVA) для выявления значительно отличающихся транскриптов между HSV по сравнению с контрольным растворителем, АТК по сравнению с контрольным растворителем, HSV+AVA по сравнению с контрольным растворителем, и HSV+АТК по сравнению с HSV отдельно. Поправки на множественные сравнения не вводили, и гены считали значимыми при значении p меньше 0,01.
Использовали самоорганизующуюся карту для исследования паттернов экспрессии в контрольным растворителе, HSV1, и HSV1+АТК. Желательно было найти специфические транскрипты, которые или активируются или подавляются при обработке АТК. Был обнаружен отдельный кластер генов, которые продемонстрировали некоторую стимуляцию в присутствии HSV, а коррекция по АТК вернула эти гены обратно на исходный уровень контрольного растворителя. Аналогично, был также обнаружен кластер генов, которые подавлялись HSV по сравнению с контрольным растворителем, а затем активировались при обработке АТК. Эти кластеры были названы Кластеры A и B, соответственно (см., таблицы 1 и 2). Анализ был завершен запросом о биологических функциях этих кластеров с использованием программного обеспечения GeneGO (genego.com).
RT2Profiler™ PCR Array (SABiosciences-QIAGEN)
6×105 клеток 293 (от AGTC) заражали штаммом McIntyre wtHSV-1 с MOI 1 в присутствии DMEM и 10% ЭТС с наличием или отсутствием 50 мкМ АТК в течение 1-2 часов и разводили до 40% при помощи DMEM и 10% ЭТС (конечная концентрация АТК 20 мкм). Собирали по три образца тотальной РНК через 24 часа с использованием набора Qiagen RNeasy mini, обрабатывали ДНКазой на колонке и элюировали. Тройные образцы элюата РНК комбинировали и проводили измерения O.D. элюата на спектрофотометре при 260 и 280 нм для определения концентрации. Образец РНК конвертировали в матричную кДНК с использованием набора для первой цепи SABiosciences RT2. Затем использовали кДНК в ПЦР-анализе пути передачи сигнала JAK/STAT человека (PAHS-039A).
Пример 1
Ингибирование уровней iNOS, индуцированных HSV, на клетках V27 с использованием АТК
Клетки V27 в модифицированной Дульбекко среде Игла (DMEM) (Hyclone, Waltham, MA) заражали вектором HSV-1 d27.1 при MOI 1 и обрабатывали 30 мкМ АТК (Sigma, St. Louis, MO), с наличием или отсутствием 10% эмбриональной телячьей сыворотки (ЭТС). Также проводили контрольные эксперименты без АТК. Лизаты клеток V27 получали через 24 часа после заражения (h.p.i.), проводили Вестерн-блоттинги лизатов и детектировали белок iNOS с использованием очищенного кроличьего антитела анти-iNOS/NOS тип II ПАТ (BD Biosciences, Кат. № 610332). Результаты показаны на фигуре 1.
Как показано, заражение HSV вызвало экспрессию iNOS в тех культурах, которые не содержали АТК (линии 4 и 5). Экспрессия iNOS была ингибирована в присутствии 30 мкМ АТК (линии 2 и 3). Наличие или отсутствие 10% ЭТС не повлияло на экспрессию iNOS.
Пример 2
Оптимизация протокола АТК-HSV
Для того чтобы проверить, может ли АТК повысить урожай вектора rHSV-1 d27-l (d27-1) в клетках V27, добавляли АТК в среду во время заражения (Этап 1) или этапов разведения (Этап 2) (фигура 2A). Заражение d27-l проводили при MOI=0,15 в 2/5 от конечного объема среды и оставшиеся 3/5 среды добавляли во время этапа разведения.
Обработка АТК замедляла формирование бляшек HSV-1 или клеточный лизис в монослоях клеток V27. Цитопатическое действие (CPE) во время сбора клеток, через 72 часа после заражения (hpi), находилось в пределах 20-60% по сравнению с 100% CPE в отсутствие АТК.
Обработка АТК на этапе заражения HSV-1 (АТК на Этапе 1) показала повышенные титры d27-1 в супернатантах клеток V27, собранных через 72 часа после заражения (фигура 4B). Оптимальная концентрация АТК при добавлении на этапе заражения (АТК I) составила 50 мкМ, и затем была разведена до конечной концентрации 20 мкМ АТК во время этапа разведения при добавлении оставшихся 3/5 объема среды. В этом случае, АТК повышала титры d27-1 в супернатанте во время сбора (72 часа после заражения) приблизительно в 10 раз: от 4,0±0,3×107 DRP/мл или 1,4±0,2×107 PFU/мл до 3,7±0,2×108 DRP/мл или 1,2±0,3×108 БОЕ/мл (фигура 4B).
Для того чтобы определить, какие концентрации и условия для добавления АТК оказывают влияние на урожаи HSV, проводили следующие эксперименты. Добавляли АТК в различных концентрациях к культурам V27, зараженным векторами HSV-1 d27-1, или в шестилуночных планшетах (фигура 2B) или в колбах T150 (фигура 2C) в два этапа, как описано далее. На Этапе 1 протокола, клетки V27 инфицировали вектором rHSV с 0,15 MOI в 2/5 от конечного объема DMEM с 10% ЭТС и концентрациями АТК 0-60 мкМ. Клетки культивировали в течение 1-2 часа при 37°C для завершения Этапа 1. На Этапе 2 уменьшали концентрацию АТК в пределах диапазона 12-24 мкМ путем добавления 3/5 от конечного объема среды. Клетки культивировали в течение 70-74 часов при 37°C и собирали супернатант. Вирусные титры выражали в виде частиц, устойчивых к ДНКазам (DRP/мл) или Бляшкообразующих единиц (БОЕ/мл) на мл и определяли, как описано выше.
Результаты показаны на фигурах 2B и 2C, а оптимальные концентрации АТК выделены жирным. Как можно видеть, и в шестилуночных планшетах (фигура 2B) и в колбах T150 (фигура 2C) культуры с АТК, добавленной или на Этапе 1 или на Этапе 2, имели значительно более высокие титры HSV, чем без АТК. Кроме того, наиболее высокие титры наблюдали при концентрациях АТК 50 мкМ на Этапе 1, сниженных до 20 мкМ на Этапе 2 (фигура 2B), хотя все концентрации АТК производили более высокие вирусные титры, чем культуры, в которых не было АТК.
Проводили дополнительные эксперименты для определения оптимальных условий и влияния присутствия или отсутствия ЭТС на титр HSV. Наличие сыворотки, конкретно, 10% эмбриональной телячьей сыворотки (ЭТС), в АТК-содержащей среде было наиболее важным параметром для титра урожая HSV-1, индуцированного АТК-. Добавление АТК в бессывороточную среду во время этапа разведения (АТК на Этапе 2) привело к снижению вирусного титра, при этом титр "DRP" стал ниже контрольного уровня и титр БОЕ/мл не детектировался (фигура 3). Еще более значительное влияние в бессывороточной среде наблюдали, когда АТК добавляли во время этапа заражения, начиная с концентрации 3 мкМ, и оба титра, DRP/мл и БОЕ/мл, оказались ниже предела детекции.
В этом эксперименте, клетки V27 высевали в шестилуночные планшеты за сутки до заражения с 6×105 клеток/лунку. Заражающий 2x раствор HSV получали следующим образом: сток HSV-1 d27.1 добавляли к DMEM (без ЭТС) в 2x титре, чтобы клетки V27 были заражены с конечным MOI 0,15. Получали несколько комбинаций 2x раствора АТК, содержащего или 100 мкМ или 40 мкМ АТК в DMEM и без ЭТС или с 20% ЭТС. Заражающий 2x раствор HSV смешивали в равных объемах или с DMEM -/+ 20%ЭТС или с желаемым 2x раствором АТК -/+ 20% ЭТС, вортексировали, и добавляли 1 мл заражающего инокулята на лунку на Этапе 1. Если лунки содержали АТК на Этапе 1, концентрация была 50 мкМ, и все лунки инкубировали в течение 1-2 часов. На Этапе 2 добавляли дополнительные 1,5 мл комбинаций DMEM -/+ 40 мкМ АТК и -/+20% ЭТС. Если лунки содержали АТК или на Этапе 1 или Этапе 2, конечная концентрация АТК была 20 мкМ. Планшеты возвращали в инкубатор на 70-74 часа, после чего собирали свободную среду, вортексировали, и центрифугировали при 1,100 × g в течение 10 минут при 4°C. Супернатанты переносили в новую дозированную пробирку, вортексировали, делали аликвоты и замораживали стоки при -80°C.
Пример 3
Важность присутствия сыворотки в протоколе АТК-HSV
Проводили дополнительные эксперименты для определения оптимальных условий и влияния присутствия или отсутствия ЭТС на титр HSV. Наличие сыворотки, конкретно, 10% эмбриональной телячьей сыворотки (ЭТС), в АТК-содержащей среде было наиболее важным параметром для титра урожая HSV-1, индуцированного АТК. Добавление АТК в бессывороточную среду во время этапа разведения (АТК на Этапе 2) привело к снижению вирусного титра, при этом титр "DRP" стал ниже контрольного уровня и титр БОЕ/мл не детектировался (фигура 3). Еще более значительное влияние в бессывороточной среде наблюдали, когда АТК добавляли во время этапа заражения, начиная с концентрации 3 мкМ, и оба титра, DRP/мл и БОЕ/мл, оказались ниже предела детекции.
В этом эксперименте, клетки V27 высевали в шестилуночные планшеты за сутки до заражения с 6×105 клеток/лунку. Заражающий 2x раствор HSV получали следующим образом: сток HSV-1 d27.1 добавляли к DMEM (без ЭТС) в 2x титре, чтобы клетки V27 были заражены с конечным MOI 0,15. Получали несколько комбинаций 2x раствора АТК, содержащего или 100 мкМ или 40 мкМ АТК в DMEM и без ЭТС или с 20% ЭТС.
Заражающий 2x раствор HSV смешивали в равных объемах или с DMEM -/+ 20%ЭТС или с желаемым 2x раствором АТК -/+ 20% ЭТС, вортексировали, и добавляли 1 мл заражающего инокулята на лунку на Этапе 1. Если лунки содержали АТК на Этапе 1, концентрация была 50 мкМ, и все лунки инкубировали в течение 1-2 часов. На Этапе 2 добавляли дополнительные 1,5 мл комбинаций DMEM -/+ 40 мкМ АТК и -/+20% ЭТС. Если лунки содержали АТК или на Этапе 1 или Этапе 2, конечная концентрация АТК была 20 мкМ. Планшеты возвращали в инкубатор на 70-74 часа, после чего собирали свободную среду, вортексировали, и центрифугировали при 1,100 × g в течение 10 минут при 4°C. Супернатанты переносили в новую дозированную пробирку, вортексировали, делали аликвоты и замораживали стоки при -80°C.
Пример 4
Влияние АТК на титры HSV дикого типа в культуре
Фигура 4A показывает титры штаммов KOS и McIntyre wtHSV-1 в супернатантах линий клеток, разрешающих размножение wtHSV-1: клетки 293, HeLa и Vero. Штаммы KOS и McIntyre wtHSV-1 выращивали в клетках 293, HeLa и Vero с использованием протокола АТК-HSV, в котором 50 мкМ АТК добавляли на Этапе 1, конечную концентрацию после Этапа 2 разбавляли до 20 мкМ АТК. Супернатанты, содержащие вирус, собирали через три дня, как описано выше. АТК повышала урожай обоих типов вируса в клетках Vero. Штамм McIntyre wtHSV-1 достигал наиболее высоких титров после индукции АТК в клетках 293, однако АТК, по-видимому, ингибировала рост KOS HSV-1 в клетках 293. Наконец, АТК также, по-видимому, ингибировала оба типа вирусов HSV-1 в клетках HeLa. Двухсторонний дисперсионный анализ (ANOVA); тест Бонферрони; - АТК vs. + АТК: ***: p 0,001, ns: p>0,05; n=4 независимых экспериментов.
Для статистических расчетов проводили большое исследование партии из десяти независимых экспериментов (n=10) в 6-луночных планшетах с наличием или отсутствием АТК, добавленной во время этапа заражения (Этап 1) по сравнению с дефицитным по репликации d27-GFP и также штаммом McIntyre wtHSV-1 для того чтобы исследовать может ли АТК также повысить титр штамма wtHSV-1 (фигура 4B). АТК добавляли в концентрации 50 мМ к кофлюэнтным монослоям клеток, V27 для d27-1 или 293 для McIntyre wtHSV-1, во время этапа заражения (Этап 1), и заражали клетки векторами при MOI=0,15, в то время как АТК разбавляли через один час до конечной концентрации 20 мМ. После добавления АТК, титр d27-1 достоверно повысился в 6,1 раз от 5,4×107 DRP/мл или 1,1×108 DRP/мл (**P<0,01) и титр McIntyre wtHSV-1 достоверно повысился в 9,1 раз от 3,3×108 DRP/мл или 1,0×109 DRP/мл (***P<0,001) при анализе 2-сторонней ANOVA и тесте Бонферрони (фигура 4B).
Пример 5
Влияние АТК в стоках HSV на выработку или вирионы rAAV
Для того чтобы определить влияет ли присутствие АТК во время выработки HSV на урожай вирионов rAAV, вырабатываемях при помощи векторов HSV, проводили следующий эксперимент, показывающий, что на титры rAAV воздействует остаток АТК, присутствующий в стоках rHSV-1, полученных в клетках 293 (фигура 5A). Вектор rAAV-GFP производили путем совместного заражения векторами rHSV-rep2/cap2 и rHSV-EGFP клеток 293 в 60 мм планшетах с использованием АТК-содержащих стоков rHSV-1, приготовленных при различных концентрациях АТК (конечные концентрации 12 мкМ или 20 мкМ) (см. Материалы и способы). Титр rAAV в DRP/мл был слегка повышен в 1,3 раза при использовании стока rHSV-rep2/cap2, который получали с 20 мкМ АТК, добавленной во время заражения (АТК на Этапе 1), по сравнению с контролем "Без АТК" (*p<0,05), где концентрация АТК во время выработки rAAV была приблизительно 3 мкМ. Не выявили никакого достоверного повышения титра rAAV при использовании стока rHSV-rep2/cap2, который получали с 12 мкМ АТК (фигура 5A). Односторонний дисперсионный анализ (ANOVA); тест Тьюки:*p<0,05; 20 мкМ АТК по сравнению с без АТК; n=4 независимых экспериментов.
В другом эксперименте, было показано, что АТК повышает титр rAAV, когда 10 мкМ АТК добавляют непосредственно в среду с клетками 293 в течение 2 часов этапа совместного заражения rHSV-rep2/cap2 и rHSV-EGFP. Этого влияния не наблюдали, когда концентрации АТК были выше 20 мкМ (фигура 5B).
Пример 6
Механизм действия АТК
Для того чтобы прояснить механизм действия АТК путем анализа генома человека, и с учетом факта, что Vero и V27 являются линиями клеток, полученными от обезьяны, размножение wtHSV-1 тестировали в нескольких клеточных линиях человека (фигуры 4A-4B). Размножение двух штаммов дикого типа HSV-1 (wtHSV-1), KOS и McIntyre, сравнивали в трех линиях клеток: эмбриональной почки человека 293 (клетки 293), клетки рака шейки матки человека HeLa и клетки эпителия почки африканской зеленой мартышки Vero. Эксперименты проводили в среде, содержащей 10% ЭТС, с последующей схемой протокола АТК I, где 50 мкМ АТК добавляли во время этапа заражения и далее разводили до конечной концентрации АТК 20 мкМ (см. Материалы и способы). В полученных от человека клетках 293 только титр вируса wtHSV-1 McIntyre значимо повысился из-за АТК, от 1,4×108 DRP/мл до 1,2×109 DRP/мл (***p<0,001). В клетках Vero АТК значимо повысила титры только штамма KOS wtHSV-1 от 1,7×108 DRP/мл до 9,1×108 DRP/мл (***p<0,001; оба статистических теста: двухсторонний ANOVA, тест Бонферрони; n=4). Неожиданно, в клетках HeLa, АТК, кажется, подавляет размножение обоих штаммов KOS и McIntyre HSV-1.
Для выявления генетических профилей клеточного ответа на заражение wtHSV-1 McIntyre, проводили транскрипционное профилирование при помощи Affymetrix Human U133 Plus 2.0 Array на клетках 293, которые были или с имитацией обработки, или обработаны АТК (АТК), заражены wtHSV-1 McIntyre (HSV) или обработаны АТК и заражены wtHSV-1 McIntyre(HSV&АТК) в течение 24 часов. Изменения в экспрессии генов, вызванные заражением или обработкой АТК, выявляли путем сравнения уровня экспрессии гена для каждого зонда с уровнем экспрессии соответствующего образца унинфицированных клеток. Заражение HSV-1 само по себе оказывало серьезное воздействие на профиль экспрессии генов в клетках 293 по сравнению с генетическим профилем необработанных клеток.
Сначала, использовали этап фильтрации для отсева низкой экспрессии, и из всех 54,675 зондов Affy U133 Plus2, 41,569 (76%) зондов остались после отсева.
Метод главных компонент выявил две различных популяции, а именно, образцы, обработанные и необработанные HSV. Проводили дисперсионный анализ (ANOVA) для выявления значительно отличающихся транскриптов между HSV по сравнению с контрольным растворителем, АТК по сравнению с контрольным растворителем, HSV+AVA по сравнению с контрольным растворителем, и HSV+АТК по сравнению с HSV отдельно. Гены считали значимыми при значении p меньше 0,01. Использовали самоорганизующуюся карту для исследования паттернов экспрессии в контрольным растворителе, HSV1, и HSV1+АТК. Был обнаружен отдельный кластер генов, Кластер A и B (Таблицы 1 и 2), который показал изменения в транскрипционных профилях, вызванные HSV-1, и их коррекцию АТК, которая вернула эти гены обратно к исходному уровню контрольного растворителя.
Биологические функции этих кластеров анализировали в GeneGo. Кластер A (таблица 2) представлял собой 58 зондов, которые показали усиление экспрессии в HSV-1 и подавление после добавления АТК. Эти гены были преимущественно вовлечены в передачу воспалительного сигнала IgE и ИФН, и в общий иммунный ответ. Кластер B (таблица 1) представлял собой 152 зонда, которые показали снижение экспрессии из-за HSV-1 и их последующую активацию АТК за счет возвращения их обратно к исходному уровню контрольного растворителя. Гены в этом кластере были преимущественно вовлечены в клеточный цикл G1/S, передачу сигнала в PTEN, и развитие, опосредованное WNT. Например, АТК в присутствии HSV-1 повышает экспрессию генов CDC25A, CDKNIA, CDKNIC, CCNK, CNNM2 из каскада прохождения клеточного цикла и генов из каскада Ras/Raf/MEK, в том числе FOXC1, FOXD3, FOXO3 (См. таблицу 1).
Таблицы 3A и 3B показывают снижение экспрессии nNOS, iNOS и eNOS в образцах HSV-АТК при анализе Affymetrix Gen Array и снижение экспрессии iNOS в образцах HSV+АТК при анализе микропанели Qiagene SAB Jak-Stat RT-PCR.
Пример 7
Влияние дексаметазона на урожаи HSV
Для того чтобы определить, повышает ли также ингибитор iNOS дексаметазон урожаи rHSV в культуре, проводили следующий эксперимент (фигура 6). Он показывает влияние дексаметазона (Dex) на вирусный титр d27-1/GFP HSV-1. Конечные титры d27-1/GFP HSV-1 были, в основном, слегка повышены после предварительной обработки dex или обработки по сравнению с необработанным контролем.
Клетки V27 высевали в шестилуночные планшеты за сутки до заражения при 6×105 клеток/лунку, на следующие сутки добавляли различные концентрации дексаметазона (dex) в лунки или до заражения HSV-1 (предварительная обработка) или во время заражения (обработка) в 2/5 объема среды DMEM-10% ЭТС. Через 1-2 часа инкубации при 37°C, добавляли 3/5 объема DMEM-10% ЭТС. Культуры возвращали в инкубатор, и собирали супернатант через 70-74 часа. Данные показаны в виде среднего значения титров + S.D. в БОЕ/мл (n=2).
Пример 8
Влияние вальпроевой кислоты на урожаи HSV
Для того чтобы определить, повышает ли также ингибитор iNOS вальпроевая кислота урожаи rHSV в культуре, проводили следующий эксперимент. На фигуре 7 представлено влияние предварительной обработки вальпроевой кислотой (ВК) на вирусный титр d27-1/GFP HSV-1. ВК в концентрации 5 мМ слегка повысила титр d27-1/GFP HSV-1, однако концентрации ниже и выше 5 мМ, по-видимому, оказывают ингибирующее действие на титр d27-1/GFP HSV-1 по сравнению с необработанным контролем.
Клетки V27 высевали в шестилуночные планшеты за сутки до заражения при 6×105 клеток/лунку, на следующие сутки добавляли различные концентрации ВК в лунки. Планшеты инкубировали в течение 6 часов, отбирали среду, добавляли 2/5 объема среды, содержащей заражающий сток HSV-1 d27-1, и инкубировали в течение 1-2 часов при 37°C, после чего добавляли 3/5 объема среды DMEM 10% ЭТС. Культуры возвращали в инкубатор, и собирали супернатант через 70-74 часа.
Как показано в вышеуказанных примерах, АТК в микромолярных концентрациях повышает урожай вектора HSV-1. Этот факт важен как для широкомасштабной продукции HSV, так и для выработки векторов rHSV и rAAV. Кроме того, неожиданно, присутствие АТК в стоках rHSV-1 не оказывает негативного влияния на урожай rAAV. Этот результат является неожиданным, поскольку известно, что АТК в миллимолярных количествах и более высоких концентрациях является противовирусным средством (Cushman et al., J. Med. Chem. (1991) 34:329-337; Zhang et al., Antiviral Res. (1999) 43:23-35; Yap et al., Computational ВЫ. and Chem. (2005) 29:212-219; De Clercq, Advents, Advances, and Adventures Med. Res. Rev. (2011) 31:118-160).
В бессывороточной среде, но не в присутствии сыворотки (10% ЭТС), авторы изобретения также наблюдали возможное противовирусное влияние АТК в микромолярных концентрациях.
Также как показано в настоящем документе, обработка АТК замедляет формирование бляшек HSV-1 и лизис клеток в монослоях клеток V27 и цитопатическое действие (CPE), что свидетельствует о противоапоптозных свойствах. Механизм действия АТК, связанный с повышением урожая HSV-1, по-видимому, включает изменение факторов, необходимых для выработки HSV-1 и уменьшения клеточного внутреннего противовирусного иммунного ответа, который отвечает за удаление вируса. Из вышеописанного анализа генома человека, было обнаружено, что заражение HSV-1 само по себе оказывает сильное влияние на профиль экспрессии генов в клетках 293, и что влияние АТК в основном наблюдается в клетках V27, обработанных и HSV-1, и АТК. Гены, участвующие в клеточном цикле G1/S, передаче сигнала через PTEN, и развитии, опосредованном WNT, были значительно подавлены HSV-1 и активированы после добавления АТК.
Гены, преимущественно вовлеченные в передачу воспалительного сигнала IgE и ИФН, и общий иммунный ответ, имели сниженную экспрессию из-за HSV-1 и были супрессированы после добавления АТК. В присутствии HSV-1, АТК повышает экспрессию генов CDC25A, CDKNIA, CDKNIC, CCNK, CNNM2 из каскада прохождения клеточного цикла и генов из каскада Ras/Raf/MEK, в том числе FOXC1, FOXD3, FOXO3.
Тот факт, что АТК может повышать урожай HSV-1 является важным, потому что необходимы более высокие урожаи векторов HSV-1 для широкомасштабного производства для генотерапии и других применений.
Таким образом, описаны способы для увеличения урожая вирусов с использованием ингибиторов iNOS. Хотя предпочтительные варианты осуществления рассматриваемого изобретения были описаны в некоторых деталях, следует понимать, что можно производить очевидные вариации в пределах сущности и объема изобретения, определенных в настоящем документе.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|