Результат интеллектуальной деятельности: СПОСОБ ПЕРФУЗИИ ПРИ ТОТАЛЬНЫХ РЕКОНСТРУКЦИЯХ НА ДУГЕ АОРТЫ
Вид РИД
Изобретение
Способ относится к медицине, в частности к сердечно-сосудистой хирургии, и может быть использован в качестве варианта перфузиологического обеспечения оперативного лечения различной патологии дуги аорты.
Хирургия дуги аорты, в той или иной степени, предусматривает ишемию головного мозга и висцеральных органов. Длительная гипоксия в результате отсутствия кровообращения, в условиях нормотермии, приводит к выраженным нарушениям целостности тканей и выполняемых ими функций.
Первым решением данной проблемы стало внедрение в практику «тотального циркуляторного ареста в условиях глубочайшей гипотермии».
Данный вариант подразумевает охлаждение пациента во время ИК до 18-16 градусов Цельсия, позволяющее выполнять полную остановку ИК длительностью до 60 минут на весь основной этап реконструкции дуги (J.S. Cosseli, S.A. Lemaire, "Aortic Arch Surgery: Principles, Strategies and Outcomes", 2008, pgs 135-154).
Недостатками данного варианта перфузии, вследствие нефизиологичности циркуляторного ареста и наличия побочных нежелательных эффектов гипотермии, являются:
1. Ограничение по времени выполнения основного этапа операции.
2. Синдром полиорганной недостаточности.
3. Выраженные нарушения гемостаза.
4. Глубокие и частые неврологические расстройства в послеоперационном периоде.
В 80-90-х гг. прошлого века, для уменьшения постоперационного неврологического дефицита, стала использоваться ретроградная перфузия головного мозга (ГМ) (J.S. Cosseli, S.A. Lemaire, "Aortic Arch Surgery: Principles, Strategies and Outcomes", 2008, pgs 167-176). Плюсом методики является сохранение перфузии ГМ на основном этапе оперативного лечения. Однако этот способ защиты ГМ, вследствие клапанного строения брахиоцефальных вен, венозного шунтирования и возникновения синдрома «обкрадывания» ГМ, также не является физиологичным, и, несмотря на снижение выраженности неврологических расстройств в постоперационном периоде, не позволяет снизить их частоту. Также в данном варианте перфузии нет решения проблемы циркуляторного ареста висцеральных органов и последующих нарушений их функций.
На данный момент «золотым стандартом» хирургии дуги аорты и защиты ГМ, является «циркуляторный арест в условиях глубокой гипотермии и антеградной моно- или бигемисферальной церебральной перфузии». (Frank W. Sellke, Scott J. Swanson «SABISTON & SPENCER SURGERY OF THE CHEST», NINTH EDITION, 2016, pgs 1159-1181).
Несмотря на сохранение кровоснабжения ГМ на протяжении всего основного хирургического этапа, перфузия все так же проводится при глубокой гипотермии до 24- 26°С в условиях циркуляторного ареста висцеральных органов. Объем подаваемый при антеградной перфузии ГМ является эмпирическим для всех пациентов и составляет 10 мл/кг/мин, что, в условиях отсутствия интраоперационного подтверждения адекватности проводимой церебральной перфузии, может приводить к гипо- или гиперперфузии ГМ и нежелательным неврологическим расстройствам. Так же последние встречаются как следствие реперфузионного повреждения и дисметаболических нарушений, возникающих в результате циркуляторного ареста висцеральных органов.
Этот вариант является наиболее близким к предлагаемому способу перфузии при тотальных реконструкциях на дуге аорты.
Проблема, на решение которой направлен способ перфузии, является создание достоверной визуализации адекватности антеградной перфузии головного мозга и возможности точной ее регуляции при параллельной перфузии висцеральных органов.
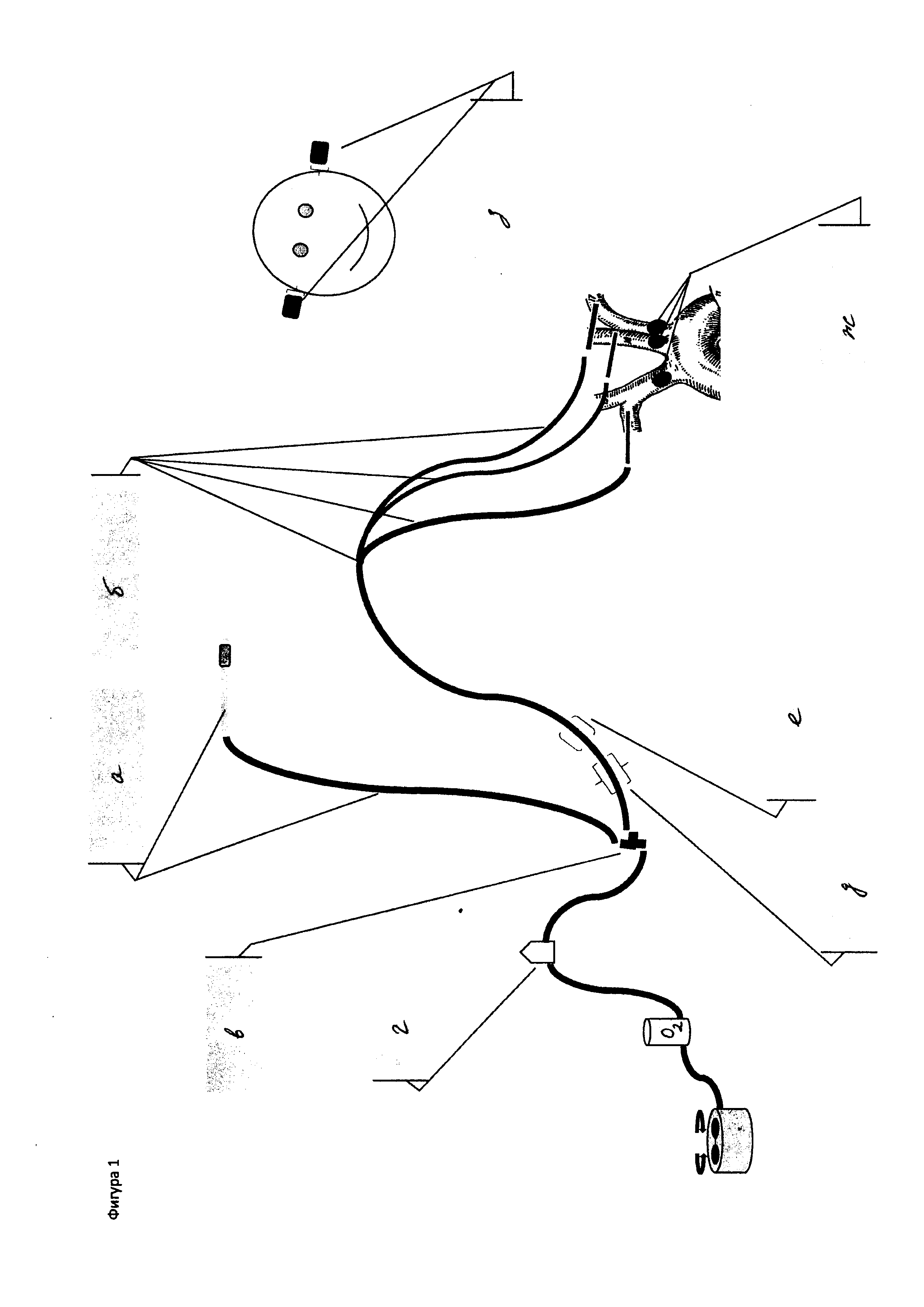
Поставленная проблема решается предлагаемым способом перфузии при тотальных реконструкциях на дуге аорты заключающимся (Фигура 1): в дублировании артериальной магистрали диаметром 3/8'' с маркировками «тело» и «голова» (пункты а и б) посредством соответствующего У-образного переходника после артериального фильтра - ловушки (пункты в и г), с последующей установкой на «головную» магистраль дистанционного окклюдера и датчика пикфлуометра (пункты д, е) и выполнением ультразвуковой допплерографии (УЗДГ) брахиоцефального ствола (БЦС), левой общей сонной артерии (лОСА) и левой аксиллярной артерии (лАА) на доперфузионном этапе, согласно температурным, гемодинамическим параметрам пациента (пункт ж) с транскраниальной допплерографией среднемозговых артерий (ТКДГ СМА, пункт з), и, после инициации искусственного кровообращения (ИК), повторением ТКДГ СМА, полученные цифры с коррекцией на аналогичные показатели на доперфузионном этапе, являются контрольными скоростями, для последующей регуляция церебральной перфузии на всех этапах ИК; в установке после рассечения дуги аорты ниже лАА во время кратковременного ареста аортальной канюли для проведения параллельной перфузии тела при реконструкциях дуги диаметром 24 Fr, представляющей собой поливинилхлоридную трубку, с закругленным выходным окончанием и надувным баллоном-манжетой, объемом до 60 мл с одной стороны, и прямолинейным коннектором 3/8 дюйма для соединения с артериальной магистралью экстракорпорального контура с другой стороны, участок трубки расположенный под баллоном-манжетой снабжен втулкой из нержавеющей стали, с подведенной в толще стенки трубки к баллону инфляторной линии с двухходовым краником, подсоединением этой канюли к магистрали «тело» и осуществлением параллельной перфузии по обеим магистралям «голова»-«тело», с предварительной поочередной канюляцией лОСА и лАА и подсоединением канюль к отводкам магистрали «голова» диаметрами 1/4'', с последующим, контролируемым пикфлуометром, выставлением дистанционным окклюдером скорости по «головной» магистрали, равной сумме скоростей потоков по БЦС + лОСА + лАА и выполнением ТКДГ СМА с последующей коррекцией окклюдером потока по «головной» магистрали при различии полученных и контрольных скоростей по результатами ТКДГ на всех этапах РЖ.
Предлагаемый способ перфузии иллюстрируется нижеследующим примером.
Пример
Пациент П., 52 года, оперирован в кардиохирургическом отделении №2 Клиники аортальной и сердечно-сосудистой хирургии по данной перфузиологической методике.
Диагноз при поступлении:
Основной: Расслоение аорты 2 типа по De-Bakey, подострая стадия.
Сопутствующий: Гипертоническая болезнь III стадии, 3 степени повышения АД, риск 4. Атеросклероз аорты, брахиоцефальных артерий.
Антропометрия пациента: m = 67 кг, рост = 171 см, St - 1,78 м2. Расчетная скорость перфузии 4.40 л/мин. Прайм в резервуар: гелофузин 500.0, маннитол 200.0, гидрокарбонат натрия 200.0, раствор Рингера 500.0
Контроль ТКДГ: при АД 90 мм рт. ст. скорость по средней мозговой артерии справа - 49 см/сек, слева 41 см/сек. В правой подключичной области выделена правая аксиллярная артерия, пришит дакроновый сосудистый протез диаметром 8 мм. Полная продольная срединная стернотомия. Измерения потоков по БЦС ОСА и АА слева равны 255, 125 и 155 мл/минуту соответственно. Канюляция аксиллярного протеза высокопоточной канюлей 24 Fr. Канюляция правого предсердия. Начало ИК по схеме «правое предсердие - правая подмышечная артерия» с последующим охлажденим больного до 26°С. Контроль ТКДГ при АД 80 мм рт. ст.: пСМА - 30, лСМА - 24 см/сек. По достижении необходимой температуры пережата восходящая аорта проксимальнее устья БЦС. Выполнены продольная аортотомия и антеградная селективная фармакохолодовая кардиоплегия раствором «Кустодиол». После пережатия БЦС и левой общей сонной артерии, начало циркуляторного ареста с моногемисферальной антеградной перфузией головного мозга со скоростью 10 мл/кг/мину, по данным, СПГ - 800 мл/мин, FiO2 21%, иАД - 50 мм Hg. Далее выполнена канюляция левой общей сонной артерии, начата бигемисферальная антеградная перфузия головного мозга, через отводку от основной магистрали ИК. Контроль ТКДГ при сАД 45 мм Hg: пСМА - 25, лСМА - 13 см/сек. На данном этапе регуляция подаваемого объема через основную магистраль осуществлялась изменением скорости основного насоса. Далее в нисходящую аорту установлена канюля для проведения параллельной перфузии тела, 24Fr. После раздувания баллона манжеты выход на полную расчетную производительность перфузии. Контроль ТКДГ при сАД 70 мм Hg: пСМА - 50 см/сек, лСМА - 40 см/сек. Данные цифры, при температуре 26°С, и полной расчетной скорости, значительно превышали контрольные цифры 30 см/сек и 24 см/сек соответственно, датчик потока артериальной лини «голова» показывал поток крови 2.3 л/мин. Путем работы венозного окллюдера уменьшен просвет данной артериальной линии до показателей ТКДГ 36 см/с и 27 см/с, при цифрах потока на артериальной линии около 700-800 мл/мин. После наложения дистального анастомоза дуги аорты и протеза, согревание пациента. Далее - наложение проксимального анастомоза корня аорты и протеза, снятие зажим с протеза, деаэрация, пуск кровотока по коронарному руслу. В заключение последовательно были наложены анастомозы между протезом и левой общей сонной артерией и протезом и БЦА. После этого перфузия осуществлялась по полностью открытой основной артериальной линии «голова», линия «тело» была пережата. Далее стандартный протокол окончания перфузии и схода с искусственного кровообращения.
Длительность перфузии составила 148 минуты, длительность циркуляторного ареста - 12 минут. Лактат крови по окончании операции не превышал 2.5 ммоль/л, уровень Tr - 171*103/л (при длительном ЦА около 30 и более минут, лактат выше 10-13 ммоль/л, уровень Tr ниже 90*103/л).
Пациент был экстубирован на следующее утро, переведен из РАО в палату в 1-е сутки после операции, выписан из стационара на 8-е сутки в удовлетворительном состоянии
Предлагаемый способ перфузии, путем параллельно проводимой индивидуально контролируемой и регулируемой церебральной и висцеральной перфузии в условиях легкой гипотермии, позволяет улучшить эффективность оперативного лечения патологии дуги аорты, избежать синдрома полиорганной недостаточности и нарушений гемостаза, снизить процент и выраженность неврологических расстройств в постоперационном периоде, уменьшить необходимость в значительном использовании гемостатической и трансфузионной терапии. Предлагаемый способ позволяет проводить перфузию одним мастер-насосом.
Результат, который может быть получен использованием предлагаемого способа перфузии, заключается в улучшении качества всех этапов лечения данной патологии. При рутинном использовании способ приводит к увеличению количества реконструктивных операций на дуге аорты и уменьшению длительности пребывания пациентов в стационаре.
Способ перфузии при тотальной реконструкции дуги аорты представляет собой: дублирование артериальной магистрали диаметром 3/8'' с маркировками «тело» и «голова» посредством соответствующего У-образного переходника после артериального фильтра-ловушки, последующую установку на «головную» магистраль дистанционного окклюдера и датчика пикфлуометра и выполнение, с учетом температурных, гемодинамических параметров пациента на доперфузионном этапе, ультразвуковой допплерографии (УЗДГ) брахиоцефального ствола (БЦС), левой общей сонной артерии (лОСА) и левой аксиллярной артерии (лАА) с транскраниальной допплерографией среднемозговых артерий (ТКДГ СМА); после инициации искусственного кровообращения (ИК) повторение ТКДГ СМА, сравнение, с учетом аналогичных температурных и гемодинамических параметров, полученных результатов с ТКДГ СМА на доперфузионном этапе и взятие полученных цифр за контрольные показатели ТКДГ для последующей регуляции церебральной перфузии на всех этапах ИК; после рассечения дуги аорты ниже лАА, во время кратковременного ареста установка аортальной канюли для проведения параллельной перфузии тела при реконструкциях дуги, 24 Fr, представляющей собой поливинилхлоридную трубку с закругленным выходным окончанием и надувным баллоном-манжетой, объемом до 60 мл с одной стороны, и прямолинейным коннектором 3/8 дюйма для соединения с артериальной магистралью экстракорпорального контура с другой стороны, участок трубки, расположенный под баллоном-манжетой, снабжен втулкой из нержавеющей стали, с подведенной в толще стенки трубки к баллону инфляторной линии с двухходовым краником, данную канюлю подсоединяют к магистрали «тело» и осуществляют параллельную перфузию по обеим магистралям - «голова» и «тело», с предварительной поочередной канюляцией лОСА и лАА и подсоединением канюль к отводкам магистрали «голова» диаметрами 1/4'', с контролируемым пикфлуометром выставлением, изменяя диаметр просвета с помощью дистанционного окклюдера, скорости по «головной» магистрали, равной сумме скоростей потоков по БЦС + лОСА + лАА, полученной измерением УЗДГ данных сосудов на доперфузионном этапе, и выполнением ТКДГ СМА с дальнейшей коррекцией окклюдером, увеличивая или уменьшая просвет «головной» магистрали, потока БЦС + лОСА + лАА при различии полученных и контрольных скоростей по результатам ТКДГ СМА на всех этапах ИК при аналогичных температурных и гемодинамических показателях пациента на начальных этапах ИК.