Результат интеллектуальной деятельности: ЦИАНОПОРФИРАЗИНОВОЕ СВОБОДНОЕ ОСНОВАНИЕ И ЕГО ПРИМЕНЕНИЕ
Вид РИД
Изобретение
Предлагаемая группа изобретений относится к области биомедицины, к мультимодальным противораковым препаратам для персонализированной медицины, касается в частности цианопорфиразинового свободного основания и его применения в качестве мультимодального агента фотодинамической терапии злокачественных новообразований, а именно в качестве фотосенсибилизатора и одновременно в качестве оптического сенсора внутриклеточной вязкости.
Флуоресцентные тетрапиррольные макроциклы, к которым относится заявляемое соединение, занимают центральное место в современной биоорганической химии, поскольку эти красители обладают свойством вначале избирательно накапливаться в ткани опухоли, а затем под действием света с подходящей длиной волны продуцировать активные формы кислорода, в частности, синглетный кислород, которые вызывают гибель клеток. Эта концепция лежит в основе фотодинамической терапии (ФДТ) онкологических заболеваний.
К настоящему времени описан обширный ряд тетрапиррольных фотосенсибилизаторов (ФС) для фотодинамической терапии (ФДТ) на основе хлоринов, порфиринов, фталоцианинов и некоторых других тетрапирролов. В последнее время показано, что порфиразины также перспективны в качестве агентов ФДТ, так как хорошо накапливаются в клетках и обладают высокой фотоцитотоксичностью [Е.R. Trivedi, A.S. Harney, М.В. Olive, I. Podgorski, K. Moin, В.F. Sloane, A. G.M. Barrett, Т.J. Meade, and В.M. Hoffman. Chiral porphyrazine near-IR optical imaging agent exhibiting preferential tumor accumulation // PNAS. - 2010. - V. 107. - №4. - Р 1284-1288].
Известно, что в процессе фотоиндуцированной гибели клетки [M. Kuimova, S. Butchway, A. Parker, H. Anderson, P. Ogiby Nature Chemistry, 1, 2009, 69-73] наблюдается значительное увеличение внутриклеточной вязкости. Вязкость является важным параметром, определяющим скорость диффузии и, следовательно, скорость бимолекулярных реакций, протекающих в живой клетке. Изменение локальной вязкости в биологических системах может привести к серьезным дисфункциям в поведении живых клеток и даже их смерти. Таким образом, разработка препаратов, обладающих свойствами высокочувствительных неинвазивных сенсоров внутриклеточной вязкости, является актуальной проблемой. Для агента ФДТ наличие таких свойств означает важную дополнительную модальность, открывающую новый персонализированный терапевтический подход к лечению онкологических заболеваний. Такой подход позволяет осуществлять мониторинг функционального состояния клеток опухоли по изменению внутриклеточной вязкости в реальном времени в процессе фотодинамического воздействия [Izquierdo М.А.,  A., Lermontova S.A., Grigoryev I.S., Shilyagina N.Y., Balalaeva I.V., Klapshina L.G., Kuimova M.K. J. Mater. Chem. (B). 2015, 3. 1089-1102].
A., Lermontova S.A., Grigoryev I.S., Shilyagina N.Y., Balalaeva I.V., Klapshina L.G., Kuimova M.K. J. Mater. Chem. (B). 2015, 3. 1089-1102].
Известно, что для некоторых флуоресцентных красителей наблюдается различная степень свободы внутримолекулярного движения фрагментов светоизлучающей молекулы в зависимости от вязкости окружающей среды [М.A. Haidekker, Е.A. Theodorakis. J. of Biol. Eng. - 2010 - V. 4. - P. 1-14.; T.  , G. Hoffmann // J. Phys Chem. - 1971. - V. 75. - Р. 63-76].
, G. Hoffmann // J. Phys Chem. - 1971. - V. 75. - Р. 63-76].
Высоковязкие среды затрудняют внутримолекулярное движение (вращение или скручивание вокруг отдельных химических связей) и связанную с этим диссипацию энергии возбужденного состояния. Это приводит к сильному возрастанию интенсивности флуоресценции. Поскольку зависимость параметров флуоресценции (квантового выхода и времени жизни) от вязкости среды может быть описана простыми математическими уравнениями (1, 2) такие соединения могут быть использованы в качестве зондов локальной вязкости.
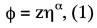
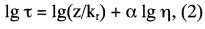
где φ - квантовый выход, η - вязкость, z и α - константы, kr - константа скорости излучательного перехода.
Такие красители обозначаются в научной литературе термином «флуоресцентные молекулярные роторы» [Т.  , G. Hoffmann. J. Phys Chem. 1971. V. 75. Р. 63-76]. Установлено, что значение α, определяющее тангенс угла наклона прямых зависимости квантового выхода от локальной вязкости в логарифмическом выражении для красителей типа молекулярных роторов меняется в интервале 0.3-0.6 [Kuimova, М.K., Chimia, 2012, vol. 66, p. 159.].
, G. Hoffmann. J. Phys Chem. 1971. V. 75. Р. 63-76]. Установлено, что значение α, определяющее тангенс угла наклона прямых зависимости квантового выхода от локальной вязкости в логарифмическом выражении для красителей типа молекулярных роторов меняется в интервале 0.3-0.6 [Kuimova, М.K., Chimia, 2012, vol. 66, p. 159.].
Наиболее близким по технической сущности и достигаемому результату к предлагаемому изобретению является порфиразин, а именно тетра(4-фторфенил)тетрацианопорфиразин, защищенный патентом RU 2621710 С1, кл. C07D 487/22, C07D F5/00, опубл. 07.06.2017 г., принятый за ближайший аналог (прототип).
Тетра(4-фторфенил)тетрацианопорфиразин по прототипу является не только сенсибилизатором фотодинамического воздействия на раковые клетки, но и высокочувствительным оптическим сенсором внутриклеточной вязкости, позволяющим проводить ее количественную оценку в различные моменты процесса фотодинамической терапии. Возможность осуществления контроля функционального состояния опухолевой ткани в режиме реального времени открывает новые возможности для персонализированной противораковой медицины.
Однако, прототип не лишен недостатков. В частности, для него существует проблема повышения фотоцитотоксичности и понижения темновой цитотоксичности. Этим недостатком обусловлено низкое значение потенциального терапевтического индекса данного препарата для ФДТ, который показывает широту безопасного использования лекарственного средства и представляет собой отношение токсичной дозы в темновых условиях к эффективной лечебной дозе при облучении.
В задачу группы изобретений положено создание цианопорфиразинового свободного основания с разнообразными арильными заместителями в периферийном обрамлении макроцикла для его применения в качестве мультимодального агента фотодинамической терапии злокачественных новообразований, а именно в качестве фотосенсибилизатора и одновременно в качестве оптического сенсора внутриклеточной вязкости.
Техническим результатом от использования группы изобретений является суммарное повышение фотодинамической активности макроциклов при сохранении высокой вязкостной чувствительности параметров их флуоресценции, необходимой для использования их в качестве потенциального неинвазивного оптического сенсора внутриклеточной вязкости.
Поставленная задача была достигнута тем, что инструментом химического дизайна структуры молекулярных роторов на основе цианопорфиразинового свободного основания и тонкой настройки его фотофизических и цитотоксических свойств явилось варьирование ароматических групп, обрамляющих макроцикл.
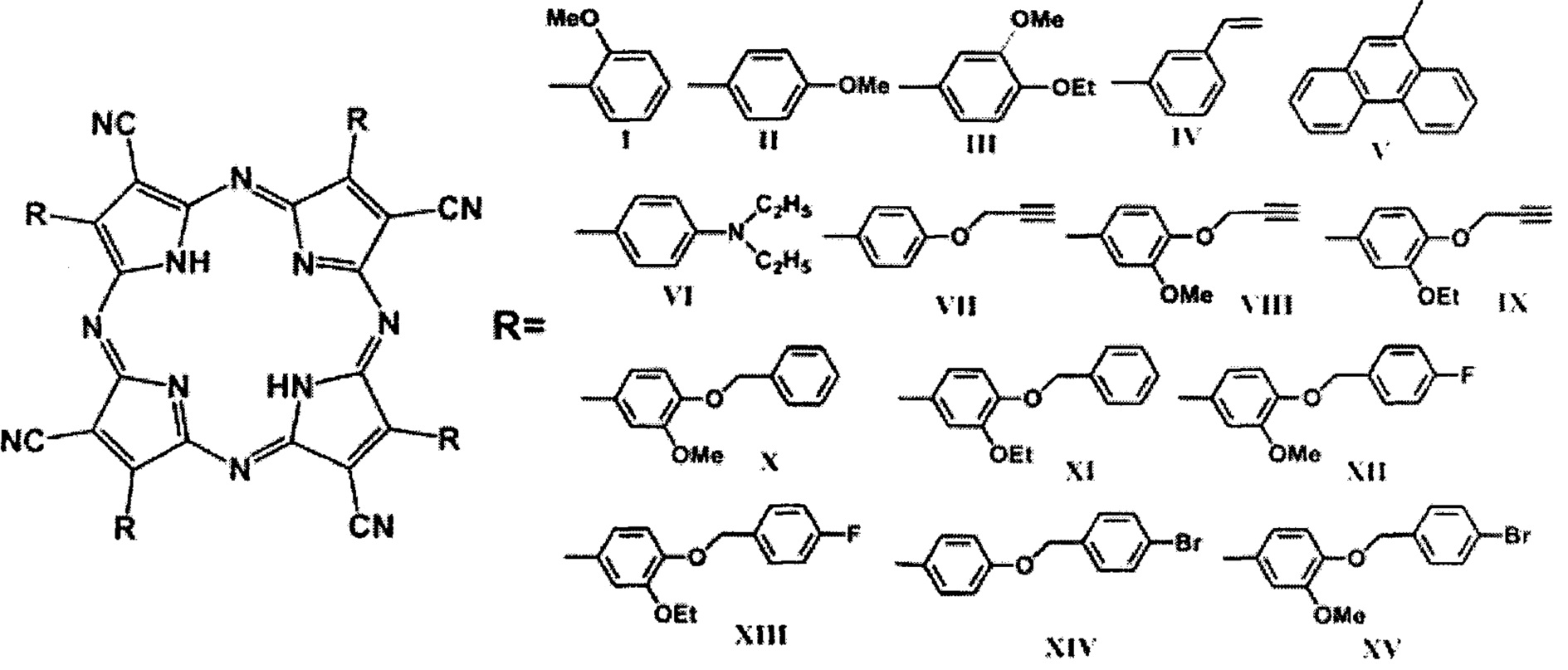
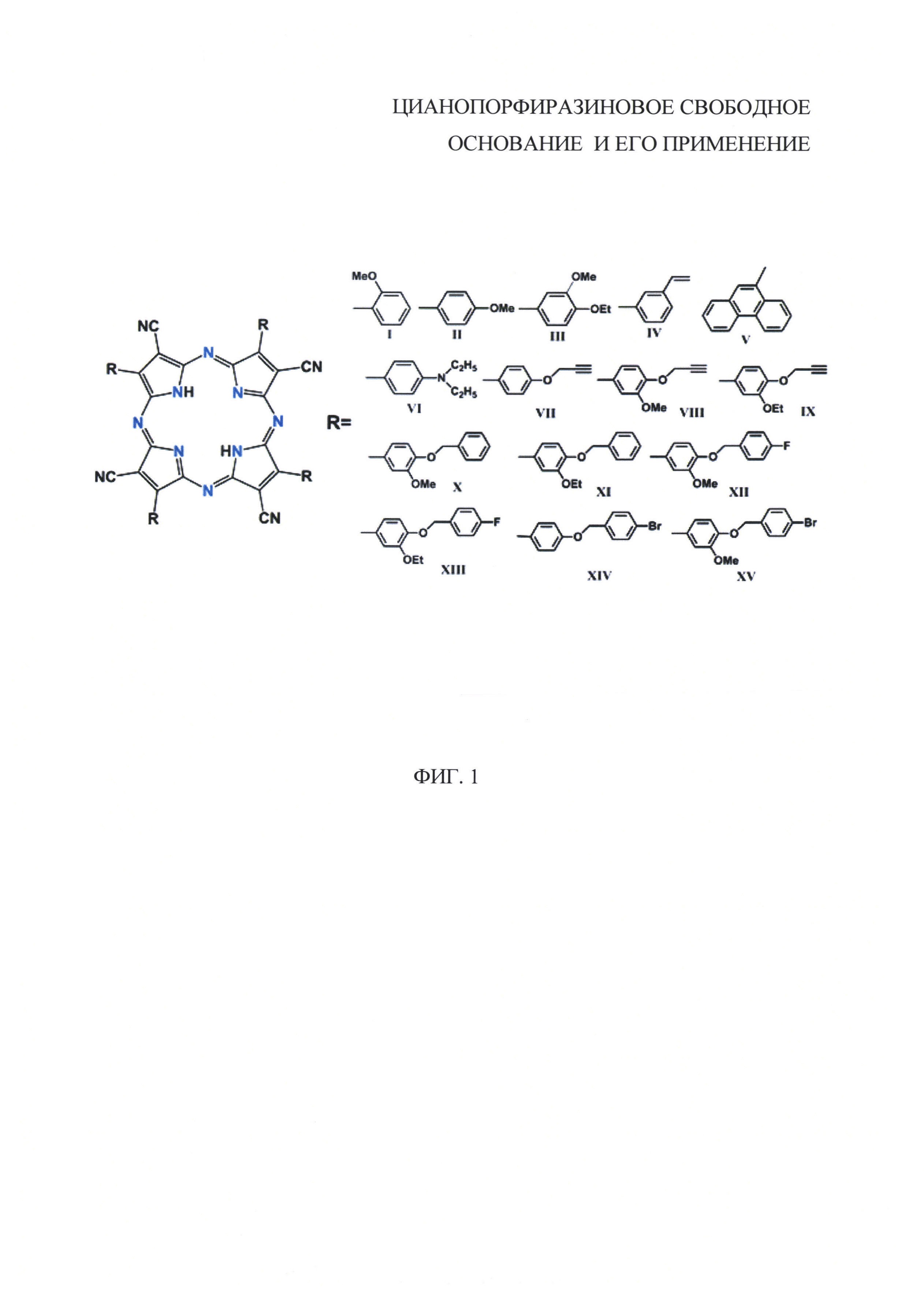
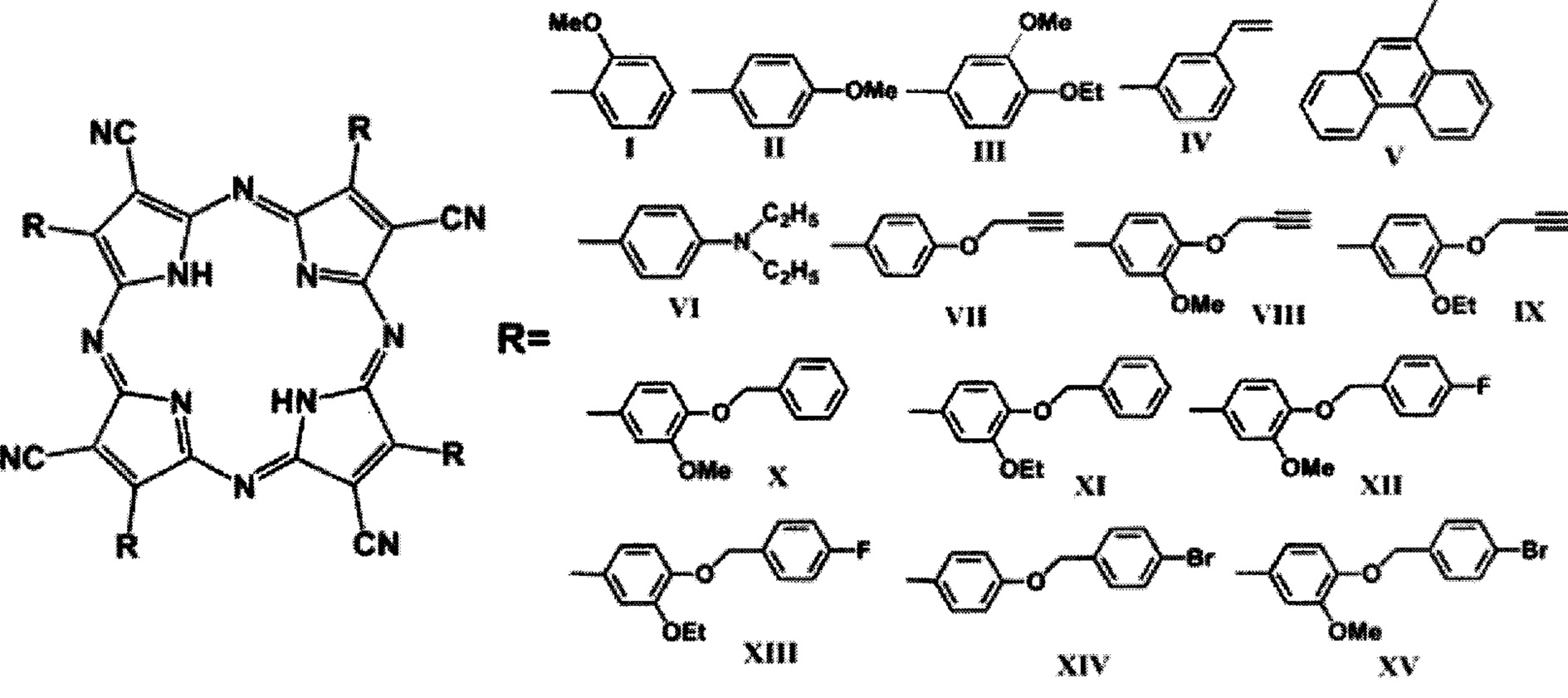
На фиг. 1 представлена общая формула полученного цианопорфиразинового свободного основания I-XV, где: R - заместитель,
R=2-MeOPh (I, 2-метоксифенил),
R=4-MeOPh (II, 4-метоксифенил),
R=4-EtO-3-MeOPh (III, 3-метокси-4-этоксифенил),
R=3-C2H3Ph (IV, 3-винилфенил),
R=Phen (V, 9-фенантренил),
R=Et2NPh (VI, 4-диэтиламинофенил),
R=4-C3H3OPh (VII, 4-(2-пропинилокси)фенил),
R=4-C3H3O-3-MeOPh (VIII, 3-метокси-4-(2-пропинилокси)фенил),
R=4-C3H3O-3-EtOPh (IX, 4-(2-пропинилокси)-3-этоксифенил),
R=4-BnO-3-MeOPh (X, 3-метокси-4-бензилоксифенил),
R=4-BnO-EtOPh (XI, 4-бензилокси-3-этоксифенил),
R=4-FBnO-3-MeOPh (XII, 3-метокси-4-(4-фторбензилокси)фенил),
R=4-FBnO-3-EtOPh (XIII, 4-(4-фторбензилокси))-3-этоксифенил),
R=4-BrBnOPh (XIV, 4-(4-бромбензилокси)фенил),
R- 4-BrBnO-3-MeOPh (XV, 4-(4-бромбензилокси)-3-метоксифенил).
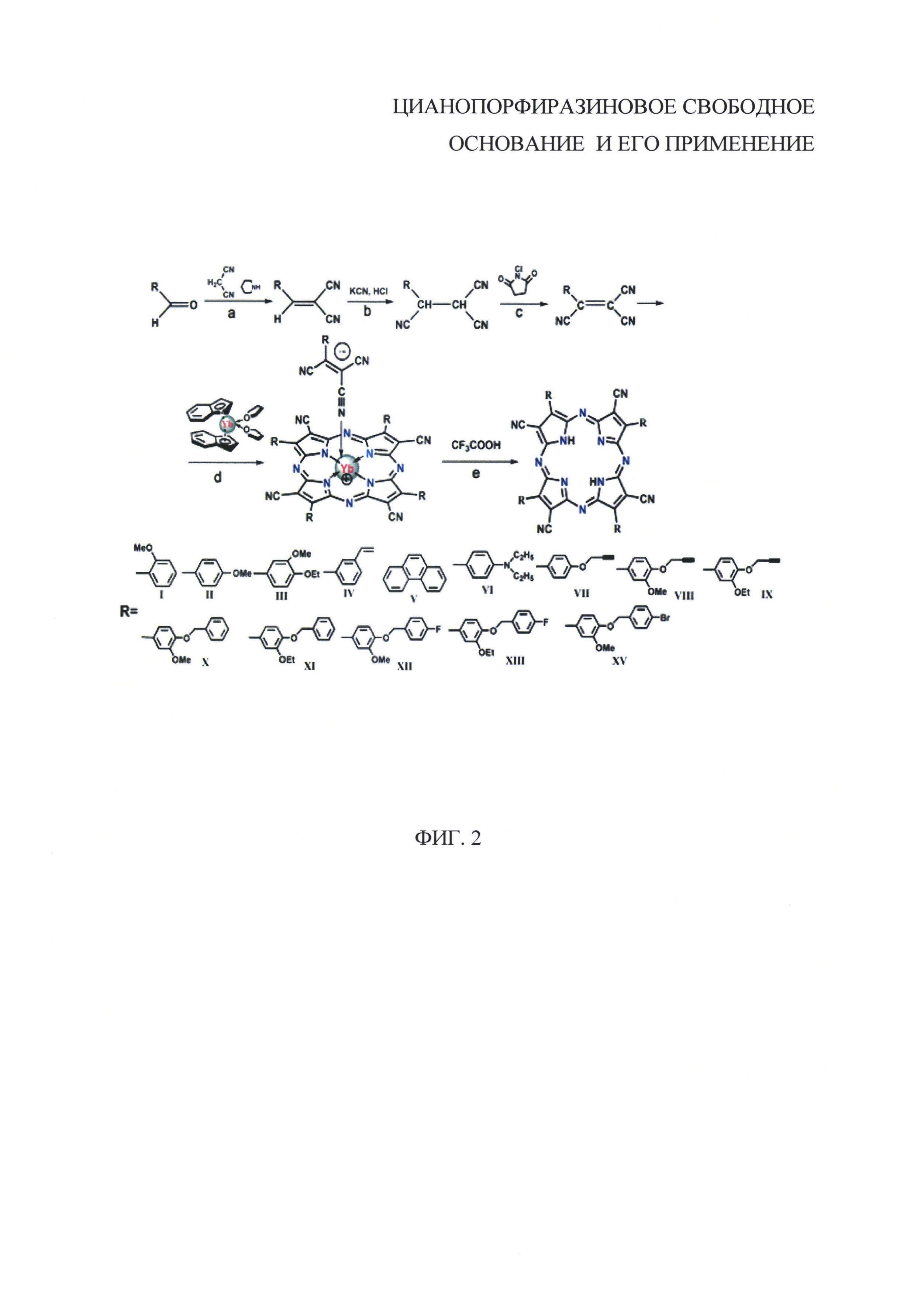
На фиг. 2 представлена схема синтеза цианопорфиразинового свободного основания I-XV в виде свободных оснований.
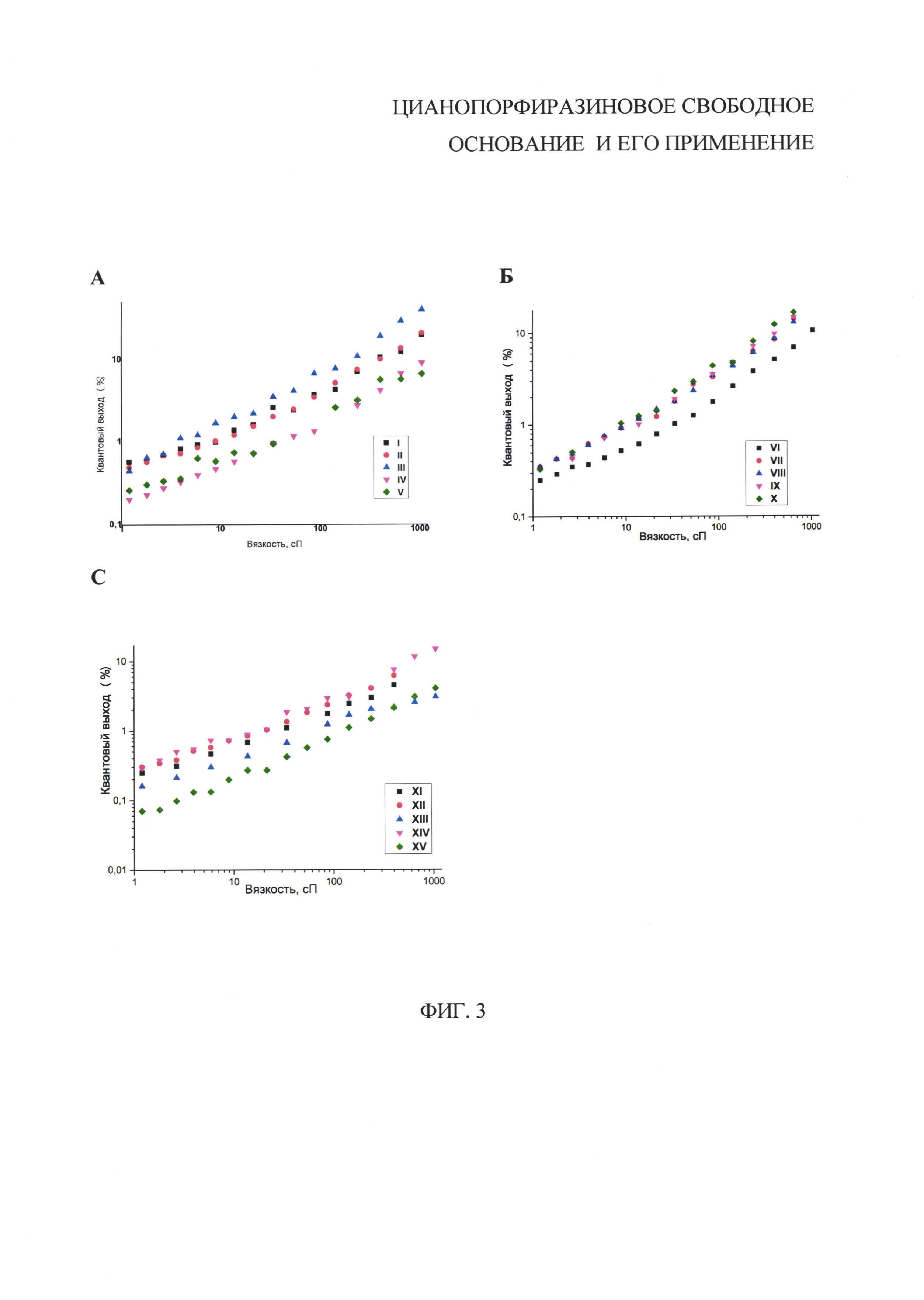
На фиг. 3 представлены графики зависимости квантового выхода флюоресценции цианопорфиразинового свободного основания I-XV от вязкости растворителя (спиртово-глицериновые смеси), где:
А:  - для порфиразина I;
- для порфиразина I;  - для порфиразина II;
- для порфиразина II;  - для порфиразина III;
- для порфиразина III;  - для порфиразина IV;
- для порфиразина IV;  - для порфиразина V;
- для порфиразина V;
Б:  - для порфиразина VI;
- для порфиразина VI;  - для порфиразина VII;
- для порфиразина VII;  - для порфиразина VIII;
- для порфиразина VIII;  - для порфиразина IX;
- для порфиразина IX;  - для порфиразина X;
- для порфиразина X;
В:  - для порфиразина XI;
- для порфиразина XI;  - для порфиразина XII;
- для порфиразина XII;  - для порфиразина XIII;
- для порфиразина XIII;  - для порфиразина XIV;
- для порфиразина XIV;  - для порфиразина XV.
- для порфиразина XV.
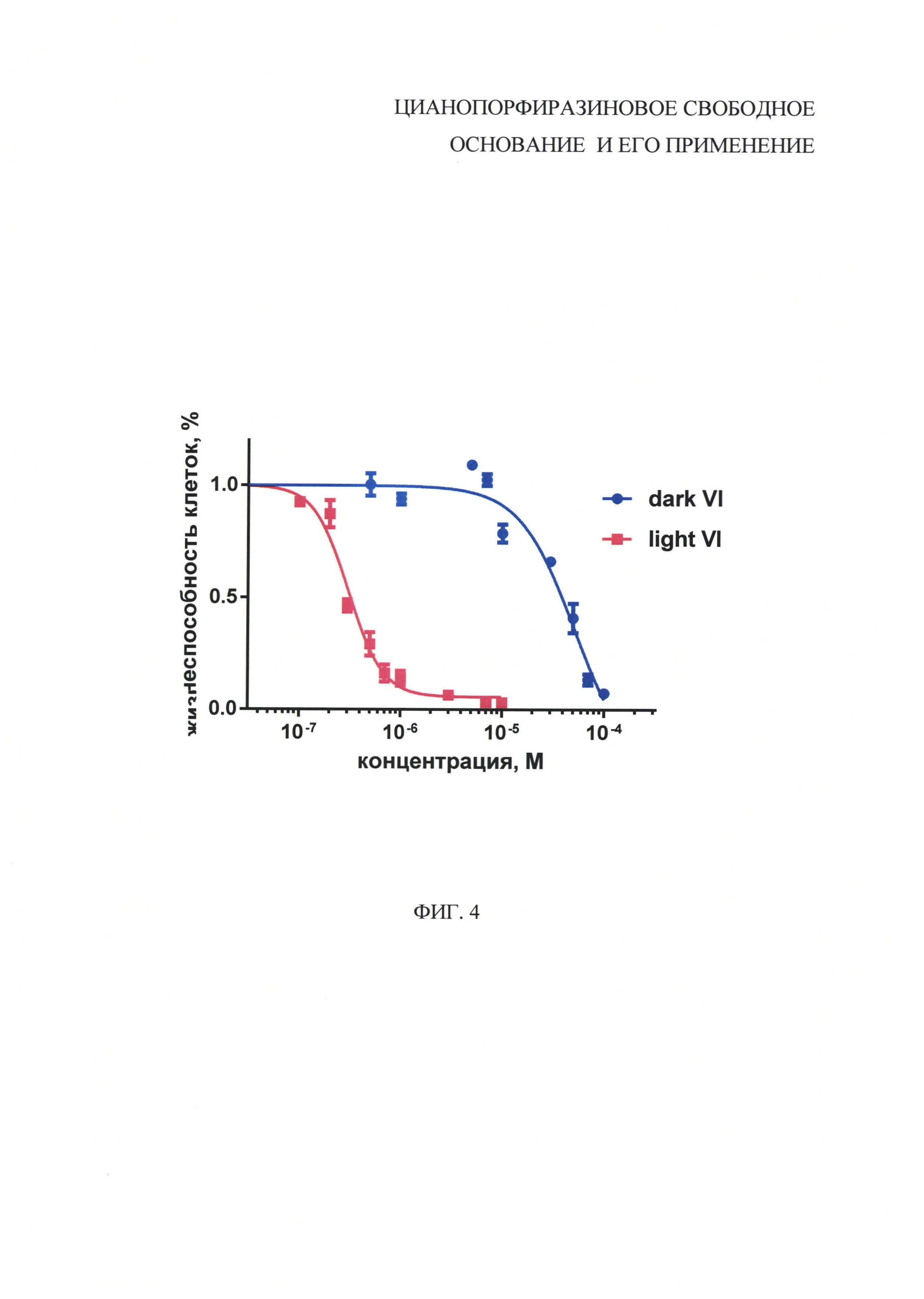
На фиг. 4 представлен график зависимости жизнеспособности клеток А431 от концентрации в среде цианопорфиразинового свободного основания pzVI.
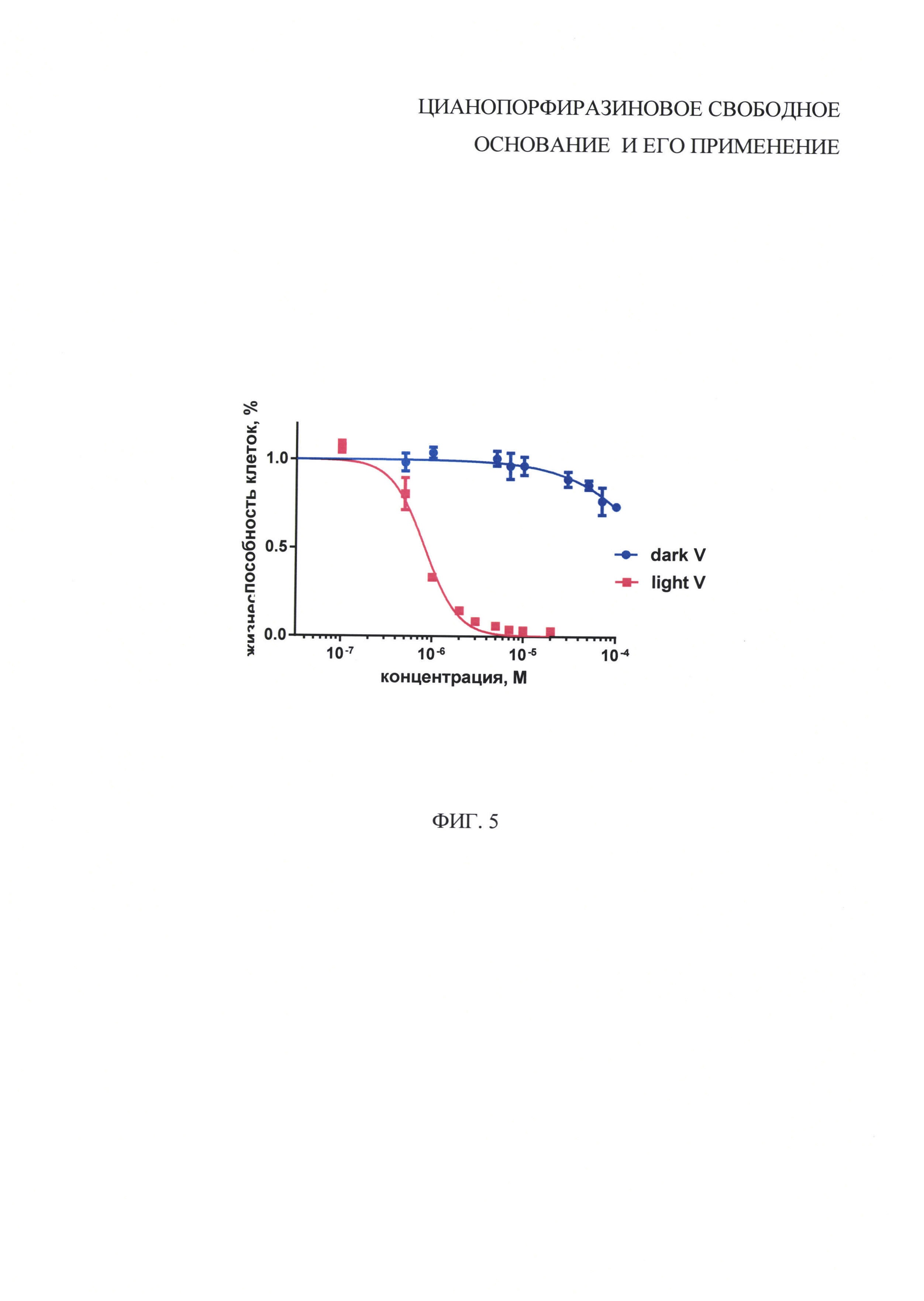
На фиг. 5 представлен график зависимости жизнеспособности клеток А431 от концентрации в среде цианопорфиразинового свободного основания pzV.
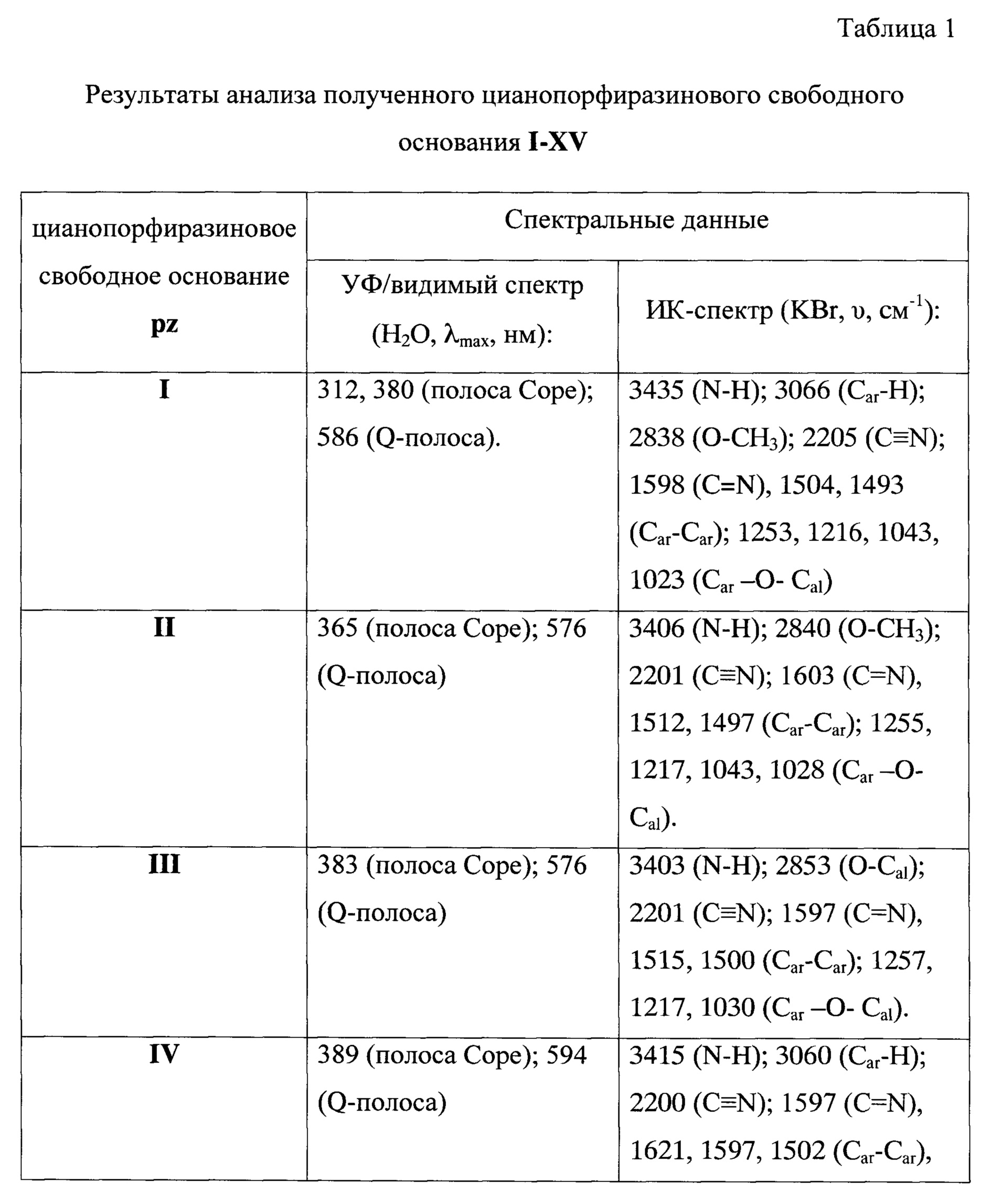
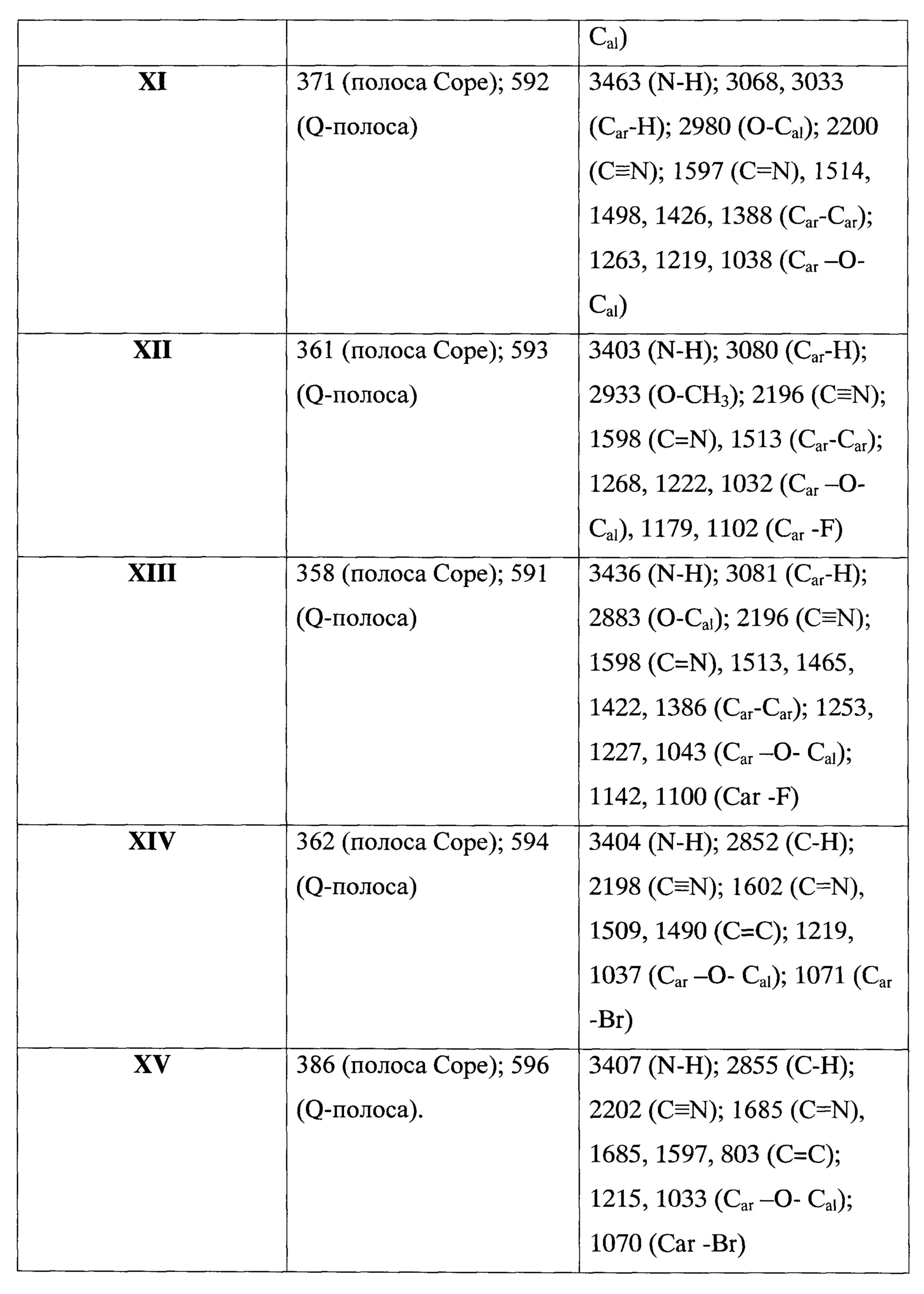
В таблице 1 представлены результаты анализа полученного цианопорфиразинового свободного основания I-XV.
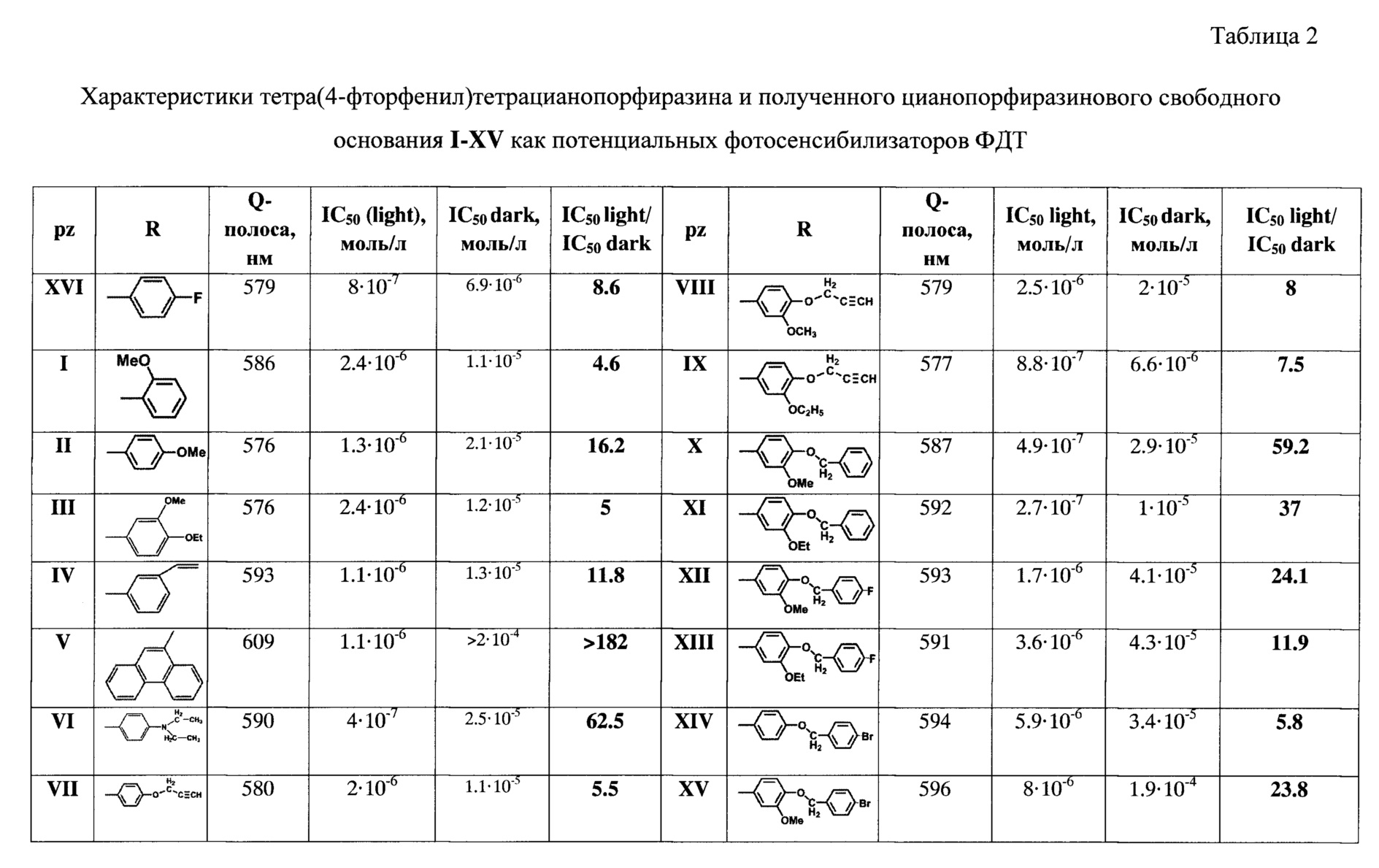
В таблице 2 представлены характеристики тетра(4-фторфенил)тетрацианопорфиразина и полученного цианопорфиразинового свободного основания I-XV в виде свободных оснований как потенциальных фотосенсибилизаторов ФДТ.
В таблице 3 представлены значения коэффициента α в уравнении Фёрстера-Хоффмана, характеризующего чувствительность квантового выхода красной флуоресценции, тетра(4-фторфенил)тетрацианопорфиразина и полученного цианопорфиразинового свободного основания I-XV от вязкости среды.
Полученное цианопорфиразиновое свободное основание имеет общую формулу:
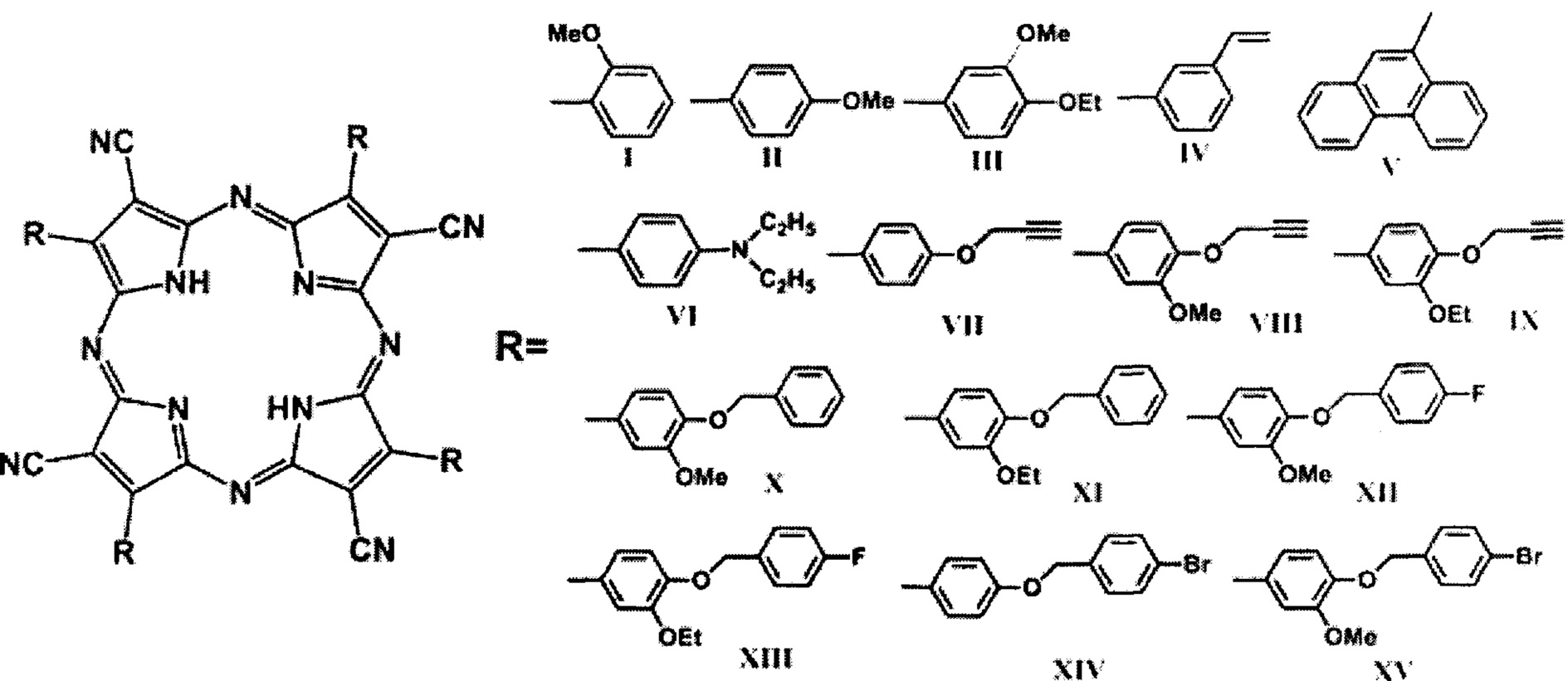
где R - заместитель,
R=2-MeOPh (2-метоксифенил), или 4-MeOPh (4-метоксифенил), или 4-EtO-3-MeOPh (3-метокси-4-этоксифенил), или 3-C2H23Ph (3-винилфенил), или Phen (9-фенантренил), или Et2NPh (4-диэтиламинофенил), или 4-C3H3OPh (4-(2-пропинилокси)фенил), или 4-C3H3O-3-MeOPh(3-метокси-4-(2-пропинилокси)фенил), или 4-C3H3O-3-EtOPh (4-(2-пропинилокси)-3-этоксифенил), или 4-BnO-3-MeOPh (3-метокси-4-бензилоксифенил), или 4-BnO-EtOPh (4-бензилокси-3-этоксифенил), или 4-FBnO-3-MeOPh (3-метокси-4-(4-фторбензилокси)фенил), или 4-FBnO-3-EtOPh (4-(4-фторбензилокси-)3-этоксифенил), или 4-BrBnOPh (4-(4-бромбензилокси)фенил), или 4-BrBnО-3-MeOPh (4-(4-бромбензилокси)-3-метоксифенил).
При R=2-MeOPh (2-метоксифенил)цианопорфиразиновое свободное основание представляет собой тетра(2-метоксифенил)тетрацианопорфиразин.
При R=4-MeOPh (4-метоксифенил) цианопорфиразиновое свободное основание представляет собой тетра(4-метоксифенил)тетрацианопорфиразин.
При R=4-EtO-3-MeOPh (3-метокси-4-этоксифенил) цианопорфиразиновое свободное основание представляет собой тетра(3-метокси-4-этоксифенил)тетрацианопорфиразин.
При R=3-C2H3Ph (3-винилфенил)цианопорфиразиновое свободное основание представляет собой тетра(3-винилфенил)тетрацианопорфиразин.
При R=Phen (9-фенантренил) цианопорфиразиновое свободное основание представляет собой тетра(9-фенантренил)тетрацианопорфиразин.
При R=Et2NPh (4-диэтиламинофенил) цианопорфиразиновое свободное основание представляет собой тетра(4-диэтиламинофенил)тетрацианопорфиразин.
При R=4-C3H3OPh (4-(2-пропинилокси)фенил) цианопорфиразиновое свободное основание представляет собой тетра(4-(2-пропинилокси)фенил) тетрацианопорфиразин.
При R=4-C3H3O-3-MeOPh (3-метокси-4-(2-пропинилокси)фенил) цианопорфиразиновое свободное основание представляет собой тетра(3-метокси-4-(2-пропинилокси)фенил)тетрацианопорфиразин.
При R=4-C3H3O-3-EtOPh (4-(2-пропинилокси)-3-этоксифенил) цианопорфиразиновое свободное основание представляет собой тетра(4-(2-пропинилокси)-3-этоксифенил)тетрацианопорфиразин.
При R=4-BnO-3-MeOPh (3-метокси-4-бензилоксифенил)
цианопорфиразиновое свободное основание представляет собой тетра(3-метокси-4-бензилоксифенил)тетрацианопорфиразин.
При R=4-BnO-EtOPh (4-бензилокси-3-этоксифенил)цианопорфиразиновое свободное основание представляет собой тетра(4-бензилокси-3-этоксифенил)тетрацианопорфиразин.
При R=4-FBnO-3-MeOPh (3-метокси-4-(4-фторбензилокси)фенил) цианопорфиразиновое свободное основание представляет собой тетра(3-метокси-(4-(4-фторбензилокси)фенил)тетрацианопорфиразин.
При R=4-FBnO-3-EtOPh (4-(4-фторбензилокси)-3-этоксифенил) цианопорфиразиновое свободное основание представляет собой тетра(4-(4-фторбензилокси)-3-этоксифенил)тетрацианопорфиразин.
При R=4-BrBnOPh (4-(4-бромбензилокси)фенил) цианопорфиразиновое свободное основание представляет собой тетра(4-(4-бромбензилокси)фенил)-тетрацианопорфиразин.
При R=4-BrBnO-3-MeOPh (4-(4-бромбензилокси)-3-метоксифенил) цианопорфиразиновое свободное основание представляет собой тетра(4-(4-бромбензилокси)-3-метоксифенил)тетрацианопорфиразин.
Синтез предлагаемого цианопорфиразинового свободного основания осуществляют следующим образом.
В качестве структурных единиц для темплатной сборки цианопорфиразинового свободного основания используют различные арилтрицианоэтилены, которые, в свою очередь, синтезируют в три стадии из ароматических альдегидов с разнообразными арильными группами (фиг. 2 стадия а-с). К арилбензальдегиду, растворенного этиловом спирте (100 мл), добавляют малонодинитрил в мольном соотношении 1:1 и 2 капли пиперидина (фиг. 2 стадия а). Реакционную смесь перемешивают в течение 24 часов при комнатной температуре. Выпавший осадок отфильтровывают, промывают водой (4×80 мл) и высушивают при комнатной температуре и пониженном давлении. Полученный 2-(арил)-1,1-дицианэтилен растворяют в этиловом спирте (150 мл), добавляют KCN в двукратном мольном избытке, предварительно растворенного в 80 мл воды (фиг. 2 стадия b). Реакционную смесь перемешивают, охлаждая колбу ледяной баней. В реакционную смесь добавляют 240 мл воды и перемешивают в течение 45 мин. при комнатной температуре. Далее добавляют 6 мл 37% HCl. После этого реакционную смесь охлаждают. Выпавший осадок отфильтровывают, тщательно промывают водой и высушивают при комнатной температуре и пониженном давлении. К полученному 2-(арил)-1,1,2-трицианэтану, растворенному в диэтиловом эфире (100 мл) добавляют N-хлорсукцинимид в мольном соотношении 1:1,5 (фиг. 2 стадия с). Через час добавляют воду (150 мл), отделяют органический слой и промывают водой (3×150 мл). Растворитель удаляют при пониженном давлении. Продукт возгоняют при пониженном давлении.
Тетра(арил)тетрацианопорфиразинат иттербия (фиг. 2 стадия d). В вакууме растворяют арилтрицианоэтилен (ArTCE) в предварительно дегазированном THF. Далее небольшими порциями добавляют полученный раствор к бис-инденильному π-комплексу иттербия (II) [(С9Н7)2Yb(ТГФ)2)] в THF (ArTCE:(С9Н7)2Yb(ТГФ)2) в мольном соотношении 1:5). Через 1 сутки раствор фильтровают в вакууме. Для удаления из смеси не вступившего в реакцию соединения и его комплекса полученный раствор промывают предварительно дегазированным толуолом до исчезновения окраски. Выделенный продукт кипятят в толуоле на воздухе в течение 24 ч. Нерастворившийся осадок отделяют и сушат при пониженном давлении.
Тетра(арил)тетрацианопорфиразинат иттербия растворяют в 2 мл трифторуксусной кислоте и перемешивают при комнатной температуре в течение 30 мин. для удаления металла (фиг. 2 стадия е). Далее добавляют воду ~ 30 мл, наблюдают выпадение темно-синего осадка, центрифугируют, тщательно промывают водой до нейтральной среды. Очистку продукта проводят с помощью колоночной хроматографии (силикагель 60, 40-60 μm, элюент THF).
ИК спектры полученных соединений в виде суспензий в вазелиновом масле регистрируют на ИК Фурье-спектрометре ФСМ 1201. Спектры поглощения в УФ и видимой области снимают на спектрометре Perkin Elmer Lambda 25. Спектры ЯМР 1H записывают на приборе Bruker Avance II+[400 (1Н), 100 (13С), 375 МГц (19F)] при 25°С. Исследования флуоресценции в стационарном режиме проводят на спектрометре Perkin Elmer LS 55 в диапазоне длин волн 300-800 нм. Масс-спектры (MALDI TOF) снимают на масс-спектрометре Bruker Microflex LT.
Пример 1.
Фотоиндуцированная и темновая цитотоксичности цианопорфиразинового свободного основания I-XV в системе in vitro.
Полученное цианопорфиразиновое свободное основание I-XV демонстрирует отчетливо выраженную фотоцитотоксичность в отношении опухолевых клеток А431 на длине волны облучения 635 нм.
Концентрации раствора цианопорфиразинового свободного основания I-XV варьировались от 0,1 до 100 мкМ. Время инкубации до светового воздействия составляло 4 часа. Исследование световой активности проводилось с использованием светодиодного излучателя для получения равномерного светового потока в стандартных 96-луночных планшетах. Доза облучения составляла 20 Дж/см2 при плотности мощности 20 мВт/см2 [Н.Ю. Шилягина, В.И. Плеханов, И.В. Шкунов, П.А. Шилягин, Л.В. Дубасова, А.А. Брилкина, Е.А. Соколова, И.В. Турчин, И.В. Балалаева. Современные технологии медицине. 2014, Т. 6, №2, С. 15-24].
Жизнеспособность клеточной культуры оценивали через 24 часа после облучения с помощью микротитрационного теста для анализа метаболической активности (МТТ-тест), позволяющего определить ингибирующую концентрацию IC50, т.е. концентрацию соединения, вызывающую снижение роста культуры клеток на 50% (или их гибель). Величины IC50 приведены в таблице 2.
Как показывают данные исследования фотоиндуцированной и темновой цитоксичности (таблица 2) все полученные порфиразиновые свободные основания являются потенциальными сенсибилизаторами ФДТ, поскольку их фотоцитоксичность существенно превышает их цитоксичность в отсутствие облучения светом. При этом, как видно из данных таблицы 2, весь ряд полученных порфиразинов показал улучшение свойств новых соединений как потенциальных фотосенсибилизаторов процесса ФДТ по сравнению с выбранным прототипом (тетра(4-фторфенил)тетрацианопорфиразином, pzXVI), по крайней мере, по одному критерию из указанных выше.
Так цианопорфиразиновое свободное основание pzI, pzII, pzIII, pzVII и pzVIII показывает значительно более высокое значение IC50 dark, т.е. допустимую концентрацию красителя в клетках, не приводящую к их гибели в темновых условиях (критерий 2).
Цианопорфиразиновое свободное основание pzII и pzXIV также превосходит прототип по этому критерию, в то же время, первый демонстрирует увеличение потенциального терапевтического индекса (критерий 3), а второй - заметный сдвиг максимума поглощения в электронном спектре в длинноволновую область (критерий 4). Цианопорфиразиновое свободное основание pzIV, pzV, pzXII, pzXIII и pzXV превосходят прототип по 2-му, 3-му и 4-му критериям.
Наилучший результат получен для цианопорфиразинового свободного основания pzVI, pzX и pzXI, которые заметно опережают прототип по всем 4-м критериям (примеры 3 и 4).
Таким образом, продемонстрирована эффективность варьирования ароматических групп в обрамлении цианопорфиразинового свободного основания для улучшения свойств порфиразиновых красителей как потенциальных фотосенсибилизаторов процесса ФДТ по сравнению с прототипом.
Пример 2.
Цианопорфиразиновое свободное основание I-XV как флуоресцентный молекулярный ротор: зависимости квантового выхода красной флуоресценции цианопорфиразинового свободного основания I-XV от вязкости среды в этанольно-глицериновых смесях.
Цианопорфиразиновое свободное основание растворяли в 3 мл смеси этанол/глицерин (концентрация порфиразина 1*10-5 моль/л). Состав смесей с известной вязкостью [Abdullah S. Alkindi, Yahya М. Al-Wahaibi, and Ann H. Muggeridge. Journal of Chemical & Engineering Data, Vol. 53, No. 12, 2008] варьировался от 40 до 100% глицерина. Интенсивность красной флуоресценции измеряли с помощью спектрофлуориметра (Perkin Elmer LS 55) при температуре 23°С.
Квантовый выход определяли относительно перхлората крезила фиолетового.
По полученным данным в логарифмических координатах для полученного цианопорфиразинового свободного основания I-XV строили зависимость квантового выхода от вязкости среды. Данные измерений представлены на фиг. 3 и в таблице 3.
Характер зависимости квантового выхода от вязкости среды для всех полученного цианопорфиразинового свободного основания I-XV полностью соответствует уравнению (1) Фёрстера-Хоффмана, а значения α в этом уравнении находятся в интервале 0.46-0.64, что позволяет отнести полученный краситель к ряду флуоресцентных молекулярных роторов, т.е. потенциальных сенсоров локальной вязкости.
Таким образом, предлагаемые в данной заявке фотосенсибилизаторы ФДТ на основе полученного цианопорфиразинового свободного основания I-XV сохраняют высокую вязкостную чувствительность красной флуоресценции, характерную для прототипа (pzXVI).
Пример 3.
Оценка фотодинамической активности in vitro цианопорфиразинового свободного основания pzVI, содержащего диэтиламино-группу в арилъном заместителе.
Измерения ингибирующих концентраций, характеризующих выживаемость клеток в условиях облучения (IC50(light)) и в темноте (IC50(dark)) для цианопорфиразинового свободного основания pzVI показали значительное усиление его фотодинамической активности по сравнению с прототипом pzXVI. Новое соединение показало величину IC50(light) в 2 раза меньше, чем для pzXVI, что свидетельствует о возрастании способности нового фотосенсибилизатора вызывать фотоиндуцированную гибель раковых клеток. В то же время собственная клеточная токсичность, не связанная с фотодинамическим процессом (IC50(dark)) почти в 25 раз ниже, чем для pzXVI (фиг. 4). Таким образом, гибель клеток, наблюдаемая при облучении раковых клеток, содержащих pzVI, обусловлена главным образом его фотоиндуцированной активностью, а не присущей препарату и нежелательной в данном случае собственной (темновой) токсичностью. В результате наблюдается сильное (более чем в 7 раз) возрастание терапевтического индекса, IC50(dark)/IC50(light). Это позволяет рассчитывать в перспективе на гораздо более высокую эффективность ФДТ при использовании pzVI в качестве фотосенсибилизатора.
Пример 4.
Оценка фотодинамической активности in vitro цианопорфиразинового свободного основания pzV, содержащего фенантрилъные заместители в обрамлении макроцикла.
Оценка эффективности фотодинамического воздействия полученного цианопорфиразинового свободного основания pzV на раковые клетки показала очень низкую темновую цитотоксичность (более 2⋅10-4 моль/л), показывающую, что в области концентраций, использующихся для ФДТ, данный препарат является практически нетоксичным для клеток в темноте (фиг. 5). С этим связан наблюдаемый высокий терапевтический индекс порфиразина pzV (>182).
Кроме того, для цианопорфиразинового свободного основания pzV наблюдается максимальный сдвиг максимума полосы поглощения в длинноволновую область спектра (609 нм), характеризующуюся большей прозрачностью биоткани.
Таким образом, представленные примеры показывают эффективность подхода к химическому дизайну потенциальных сенсибилизаторов ФДТ на основе цианопорфиразинового свободного основания I-XV и получению потенциальных препаратов с улучшенными свойствами.
Полученные цианопорфиразиновые свободные основания демонстрировали заметное повышение эффективности в качестве потенциальных фотосенсибилизаторов ФДТ по сравнению с тетра(4-фторфенил)тетрацианопорфиразином (pzXVI) и высокую чувствительность параметров флуоресценции к локальной вязкости область.
Критерием успешности достижения поставленной цели явилось улучшение, по крайней мере, одной из ниже перечисленных характеристик полученного цианопорфиразинового свободного основания I-XV по сравнению с прототипом:
- существенное понижение выживаемости клеточных культур, инкубированных в присутствии цианопорфиразинового свободного основания, при облучении светом (уменьшение ингибирующей концентрации цианопорфиразинового свободного основания (IC50(light));
- рост выживаемости клеточных культур, инкубированных в присутствии цианопорфиразинового свободного основания в темновых условиях, (увеличение ингибирующей концентрации порфиразина IC50(dark);
- возрастание отношения IC50(dark)/IC50(light), характеризующего потенциальный терапевтический индекс препарата для ФДТ, который показывает широту безопасного использования лекарственного средства и представляет собой отношение токсичной дозы в темновых условиях к эффективной лечебной дозе при облучении;
- заметный сдвиг максимума поглощения в длинноволновую область.