Результат интеллектуальной деятельности: ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ АМИДА N-(6-ФЕНИЛГЕКСАНОИЛ)ГЛИЦИЛ-L-ТРИПТОФАНА С ПЛЕНОЧНЫМ ПОКРЫТИЕМ И СПОСОБЫ ЕЕ ПОЛУЧЕНИЯ
Вид РИД
Изобретение
Область техники, к которой относится изобретение
Изобретение относится к медицине, в частности к фармации, и касается фармацевтической композиции, содержащей в качестве действующего вещества - амид N-(6-фенилгексаноил)глицил-L-триптофана (ГБ-115) [Патент РФ 2227144], обладающий анксиолитической активностью. Технический результат изобретения заключается в повышении эффективности применения лекарственного средства ГБ-115 - создание композиции с использованием покрытия, повышающего биодоступность амида N-(6-фенилгексаноил)глицил-L-триптофана (ГБ-115).
Уровень техники
В ФГБНУ «НИИ фармакологии имени В.В. Закусова» разработан безопасный препарат на основе анксиогенного тетрапептида холецистокинина (ХЦК), идея которого состоит в достижении анксиолитического действия без прямого влияния на ГАМКд-рецепторы. Синтезированное на основе холецистокинина-4 соединение амид N-(6-фенилгексаноил)глицил-триптофана реализует анксиолитическое действие, направленное на животных с «freezing» реакцией в условиях эмоционального стресса, при взаимодействии с центральными ХЦК1-рецепторами [Гудашева Т.А., Кирьянова Е.П., Колик Л.Г., Константинопольский М.А., Середенин СБ. // Биоорган, химия. 2007. Т. 33. №4. С. 413-420; Колик Л.Г. Гудашева Т.А., Середенин С.Б. // Бюлл. экспер. биол. и мед. 2012. Т. 153, №6. С. 28-32; Kolik L.G, Gudasheva Т.А, Seredenin S.B. // Bull Exp Biol Med. 2003. V. 135, №5. P. 440-444; Kolik L.G., Gudasheva T.A., Seredenin S.B. // Eur. Neuropsychopharmacol. 2011. V. 21 Suppl. 2. S 146-147.].
Согласно доклиническим исследованиям безопасности, амид N-(6-фенилгексаноил)глицил-триптофана не влияет на показатели дыхания, деятельности сердца, кровообращение и артериальное давление, относится к практически нетоксичным соединениям (LD50>6 г/кг для крыс при введении per os) [Сорокина А.В., Алексеева СВ., Немова Е.П., Коваленко Л.П., Смольникова Н.М., Шипаева Е.В., Шредер О.В., Мирошкина И.А., Дюкова С.А., Даугель-Дауге H.О., Кулакова А.В., Колик Л.Г., Дурнев А.Д., Середенин С.Б. // Экспериментальная и клиническая фармакология. 2010. Т. 73. №6. С. 29-32.], в экспериментальных исследованиях доказано отсутствие развития толерантности к анксиолитическому эффекту и синдрома отмены при длительном введении дипептидного анксиолитика ГБ-115, что выгодно его отличает от препаратов бенздиазепинового ряда [Колик Л.Г., Гарибова Т.Л., Литвинова С.А., Кузнецова А.Л., Капица И.Г., Кадников И.А., Константинопольский М.А., Гудашева Т.А., Воронина Т.А., Середенин С.Б. // Вестник Российской академии медицинских наук. 2011. №7. С. 37-42]. Боле того, установлена способность амида N-(6-фенилгексаноил)глицил-триптофана устранять анксиогенез, вызванный отменой бензодиазепиновых транквилизаторов [Колик Л.Г., Кадников И.А., Жуков В.Н., Гудашева Т.А., Середенин С.Б. Экспериментальная и клиническая фармакология. 2011. Т. 74. №10. С. 7-11].
В отличие от других пептидных препаратов, используемых в клинической практике для фармакотерапии тревожных расстройств (селанк, семакс), амида N-(6-фенилгексаноил)глицил-триптофан по химической структуре принадлежит к коротким дипептидам и проявляет анксиолитические свойства при пероральном способе введения, что подтверждается результатами фармакодинамических исследований [Колик Л.Г., Константинопольский М.А., Рыбина И.В., Поварнина П.Ю., Гудашева Т.А., Середенин С.Б. // Бюллетень экспериментальной биологии и медицины. 2013. Т. 155. №2. С. 163-166].
Несмотря на расширяющийся поиск альтернативного пути введения и методов лекарственной доставки, оральный путь введения остается наиболее популярным. По подсчетам около 70% всех лекарственных форм (ЛФ) предназначены для перорального применения, так как данный способ введения является наиболее приемлемым и удобным для пациентов. Кроме того, это широко изученный и отработанный метод заводского производства, используемый для получения твердых лекарственных форм (ТЛФ). ТЛФ дешевы в производстве, у них оптимально соотношение цена - качество.
Среди ТЛФ наиболее часто используемыми являются таблетки и капсулы, которые могут различаться по размерам и содержимому. Твердые желатиновые капсулы (ТЖК) могут заполняться порошками, гранулами, пеллетами и другим содержимым, приемлемым для данной ЛФ.
Все большее распространение приобретают ТЛФ, покрытые оболочкой. Среди них различают ТЛФ, покрытые защитной, кишечнорастворимой или оболочкой пролонгированного действия, причем использование защитных оболочек является наиболее распространенным [Теоретические и экспериментальные основы процесса нанесения покрытий на твердые лекарственные формы: дис. на соиск. учен. степ, д-ра фармацевт, наук: специальность 15.00.01 «Технология лекарств и орг.фармацевт, дела» / Флисюк Елена Владимировна; [С.-Петерб. гос. хим. - фармацевт. акад. Росздрава]. - Санкт-Петербург: 2006. - 418 с: 25 ил.].
Оболочки, предназначенные для создания защитных покрытий можно, в свою очередь, рассматривать как:
- оболочки, растворимые в воде и желудочном соке.
Эти оболочки улучшают внешний вид таблеток, корригируют их вкус и запах, защищают от механических повреждений, от воздействия углекислоты и кислорода воздуха, но такие оболочки не предохраняют таблетки от воздействия влаги воздуха. Водорастворимые оболочки наносятся на таблетки в виде водно-этанольньгх или водных растворов.
- оболочки, не растворимые в воде, но растворимые в желудочном соке.
Эти оболочки наносятся с целью предохранения лекарственного вещества (ЛВ) от воздействия влаги, и в то же время не препятствуют быстрому разрушению их в желудке (в течение 10-30 минут). Такие оболочки образуют полимеры, имеющие в молекуле заместители основного характера, главным образом, аминогруппы, например, диэтиламиноэтилцеллюлоза, бензиламиноцеллюлоза и другие.
Кишечнорастворимые покрытия наносят для создания лекарственных препаратов, растворимых только в щелочной среде кишечника. Кишечнорастворимые покрытия обладают выраженным влагозащитным эффектом. Они способствуют локализации ЛВ в кишечнике, пролонгируя в определенной степени их действие.
Варьируя различные полимеры и толщину пленки, можно добиться абсорбции ЛВ в определенном отделе кишечного тракта. Эти покрытия исключают побочное влияние некоторых ЛВ на слизистую оболочку желудка и устраняют диспептические явления, предотвращают разложение ЛВ.
Кишечнорастворимые покрытия образуют шеллак, ацетил фталилцеллюлоза, фталат гидроксипропилметилцеллюлозы, поливинилацетатфталат, полиметакрилаты и другие вспомогательные вещества (ВВ).
Существует несколько видов покрытий: дражированные, суспензионные, прессованные и пленочные. В настоящее время наиболее перспективными и современными из всех существующих видов покрытий являются пленочные, так как применение этих оболочек обеспечивает необходимый профиль растворения и уровень биодоступности ЛВ.
Пленочные покрытия формируются на таблетках путем нанесения раствора пленкообразующего вещества с последующим удалением растворителя. При этом на поверхности таблеток образуется тонкая оболочка.
С экологической точки зрения наиболее перспективным является нанесение пленочных покрытий с применением водных растворов полимеров, так как это дает возможность существенно снизить стоимость, токсичность, огне- и взрывоопасность производства.
Задачей данного изобретения является разработка фармацевтических композиций с использованием покрытия, а также разработка на основе этой композиции ТЛФ, обеспечивающих высвобождение и однородность дозирования амида N-(6-фенилгексаноил)глицил-L-триптофана в ЛФ и соответствующих требованиям Государственной фармакопеи РФ XII издания и СССР XI издания.
Раскрытие изобретения
Фармацевтические композиции, выполненные в ТЛФ, содержат внутреннее ядро из растворимых или нерастворимых в воде ВВ в виде таблеток, микротаблеток или пеллет, в качестве действующего вещества - амид N-(6-фенилгексаноил)глицил-L-триптофана в терапевтически эффективном количестве, а в качестве покрытия - водорастворимые производные целлюлозы, поливинилового спирта.
В состав покрытия в качестве пленкообразующего вещества входит, по меньшей мере, одно вещество, выбранное из группы, включающее производные целлюлозы (гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза), выпускаемые в промышленности под наименованиями: AquaPolish (BIOGRUND GmbH, Германия), Pharmacoat® (Harke, Германия), VIVACOAT® (JRS Pharma, Германия), VIVAPHARM® HPMC (JRS Pharma, Германия), метилцеллюлозы, поливинилового спирта, выпускаемые промышленностью под наименованиями: Kollicoat IR (BASF, Германия).
Фармацевтические композиции в качестве ВВ, обеспечивающего достаточную массу таблетки-ядра (наполнитель), содержит, по меньшей мере, одно вещество, выбранное из группы: целлюлоза и ее производные (микрокристаллическая целлюлоза, выпускаемая под наименованиями: Avicel (FMC, США), Tabulose (Blanver, Бразилия), Microcel (Blanver, Бразилия), Vivacel, Vivapur (JRS Pharma, Германия), Emcocel (JRS Pharma, Германия), Celocal (FMC, США), Prosolv (Penwest, США), MicroceLac (MEGGLE, Германия)); полиолы (лактоза и ее производные, выпускаемые под наименованиями: Tablettose (MEGGLE, Германия), FlowLac (MEGGLE, Германия), DuraLac (MEGGLE, Германия), Cellactose (MEGGLE, Германия), MicroceLac (MEGGLE, Германия), StarLac (Roquette, Франция), Pharmatose (DMV, Голландия), Ludipress (BASF, Германия); сахароза, выпускаемая под наименованиями CompriSugar (Sudzucker, Германия), Di-pac (American sugar, США); мальтоза, выпускаемая под наименованиями Advantose 100 (SPI Pharma, Франция); фруктоза, выпускаемая под наименованиями Advantose FS 95 (SPI Pharma, Франция); сорбит, выпускаемый под наименованиями Parteck SI (Merck Millipore, Германия); маннит, выпускаемый под наименованием Parteck М (Merck Millipore, Германия); ксилитол, выпускаемый под наименованиями XyliTab (MEGGLE, Германия)); соли неорганических соединений (кальция карбонат, выпускаемый под наименованиями Formaxx (Merck Millipore, Германия); кальция фосфат, кальция дигидрофосфат, кальция гидрофосфат дигидрат, кальция сульфат дигидрат). Данные группы ВВ так же используют для приготовления пеллет непосредственно на производстве.
В качестве ВВ, предотвращающего налипание и обеспечивающего выталкивание из матрицы (антифрикционное), внутреннее ядро содержит, по меньшей мере, одно вещество, выбранное из группы: стеариновая кислота и/или ее соли, коллоидный кремний (аэросил).
Внутреннее ядро пеллет представляет собой растворимые в воде гранулы, выпускаемые промышленностью: гранулы сахарозы, выпускаемые под наименованиями Sugar Spheres Sanaq® (Pharmatrans-Sanaq AG, Швейцария), SURINERTS® SUGAR SPHERES (IPS, Италия), SURINPATHICS® (IPS, Италия), SUGLETS® Sugar Spheres (Colorcon, Великобритания), Pharm-a-spheres™ sugar spheres (Harms G. Werner GmbH, Германия), SPRAYSPHERES™ - SS (UMANG PHARMATECH PVT. LTD., Индия); или, представляет собой не растворимые в воде гранулы, выпускаемые промышленностью: гранулы микрокристаллической целлюлозы (МКЦ), выпускаемые под наименованиями Cellets (Harke, Германия), Cellets (Pharmatrans-Sanaq AG, Швейцария), Cellulose pellets (Blanver, Бразилия), SPRAYSPHERES™. MS (UMANG PHARMATECH PVT. LTD., Индия).
Предложены варианты изготовления таблеток-ядер. Одним из вариантов способа изготовления является прямое прессование. Все ингредиенты просеиваются, в смесителе смешиваются наполнители. Таблеточная масса поступает на стадию опудривания и далее прессуется в матрице подходящего размера. Готовые таблетки обеспыливают. Последней стадией является нанесение покрытия.
Предложены также варианты изготовления ТЛФ с пленочным покрытием на основе предлагаемой композиции. Один из вариантов способа заключается в изготовлении ТЛФ методом нанесения пленочного покрытия на таблетки-ядра, микротаблетки-ядра или готовые пеллеты. Готовят водную суспензию пленочного покрытия путем добавления порошка покрытия к воде, образующей воронку при постоянном перемешивании. После образования гомогенной суспензии покрытия при постоянном перемешивании к суспензии добавляют амид N-(6-фенилгексаноил)глицил-L-триптофана, не растворимый в воде, и продолжают перемешивание. Полученную суспензию наносят на таблетки-ядра, микротаблетки-ядра или пеллеты. Полученными пеллетами или микротаблетками наполняют твердые желатиновые капсулы (ТЖК), или пеллеты спрессовывают в таблетки.
Второй вариант способа изготовления ТЛФ заключается в том, что на первой стадии технологического процесса амид N-(6-фенилгексаноил)глицил-L-триптофана просеивается и смешивается с порошком пленочного покрытия до однородности. Затем готовят водную суспензию покрытия с амидом N-(6-фенилгексаноил)глицил-L-триптофана и наносят пленочное покрытие на таблетки-ядра, микротаблетки-ядра или пеллеты. Покрытые пеллеты или микротаблетки помещают в ТЖК, или пеллеты спрессовывают в таблетки.
Еще один вариант способа изготовления ТЛФ заключается в том, что пеллеты с амидом N-(6-фенилгексаноил)глицил-L-триптофана получают в процессе пеллетизации известными методами. Пеллеты с амидом N-(6-фенилгексаноил)глицил-L-триптофана и пленочным покрытием помещают в ТЖК или спрессовывают в таблетки.
Еще один вариант способа изготовления ТЛФ заключается в том, что таблетки-ядра, микротаблетки-ядра или пеллеты покрывают пленочным покрытием, в которое включен не растворимый в воде амид N-(6-фенилгексаноил)глицил-L-триптофана, и затем дополнительно наносят еще одно покрытие. Пеллетами или микротаблетками наполняют ТЖК, или пеллеты спрессовывают в таблетки.
Осуществление изобретения
Фармацевтические композиции выполнены в ТЛФ, в виде таблеток или ТЖК, содержащих 0,0005-0,0200 г амида N-(6-фенилгексаноил)глицил-L-триптофана. Масса полученной таблетки составляет от приблизительно 0,0500 г до приблизительно 0,2000 г.
Наилучшими показателями обладает композиция в виде таблетки-ядра или ТЖК, содержащая микротаблетки или пеллеты с пленочным покрытием, включающим ЛВ - амид N-(6-фенилгексаноил)глицил-L-триптофана, а в качестве ВВ - микрокристаллическую целлюлозу, лактозу, и дополнительно, в качестве пленочного покрытия, гидроксипропилметилцеллюлозу или поливиниловый спирт с допустимым, но необязательным добавлением пластификаторов, пигментов, корригентов запаха, вкуса и цвета, при следующем соотношении компонентов в масс. % в таблетке:
|
Средняя масса таблетки может составлять 0,0500, 0,1000, 0,1500 и 0,2000 г.
ТЛФ отвечает всем требованиям Государственной Фармакопеи РФ XII издания и СССР XI издания.
Следующие примеры иллюстрируют варианты получения фармацевтической композиции без ограничения объема притязаний по изобретению.
Пример 1. Все ингредиенты просеиваются. Приготовление ядер таблеток: смешиваются не растворимый в воде наполнитель (микрокристаллическая целлюлоза) и антифрикционное вещество (магния стеарат) до получения однородной смеси. Полученную порошковую смесь просеивают для достижения однородности смешивания и подвергают прямому прессованию и таблетированию. Вес ядер составляет 0,09 г. В качестве пленочного покрытия используется водная суспензия гидроксипропилметилцеллюлозы, в которую после образования однородной суспензии вводится амид N-(6-фенилгексаноил)глицил-L-триптофана в сухом виде. Суспензию пленочного покрытия с амидом N-(6-фенилгексаноил)глицил-L-триптофана наносят на таблетки-ядра при температуре 40±2°С в приборе INNOJET AirCoater 025. Прирост массы таблеток-ядер составляет не более 5%. Высушенные таблетки обеспыливают, фасуют и маркируют.
Соотношение компонентов в масс % в таблетке:
|
Пример 2. Все ингредиенты просеиваются.
Соотношение компонентов в масс % в таблетке:
|
Приготовление ядер таблеток: по способу, описанному в примере 1. Вес ядер составляет 0,09 г. В качестве пленочного покрытия выступает 5% водная суспензия поливинилового спирта, в которую после образования однородной суспензии вводится амид N-(6-фенилгексаноил)глицил-L-триптофана в сухом виде. Суспензию пленочного покрытия с амидом N-(6-фенилгексаноил)глицил-L-триптофана наносят на таблетки-ядра при температуре 40±2°С в приборе INNOJET AirCoater 025. Прирост массы таблеток-ядер составляет не более 5%. Высушенные таблетки обеспыливают, фасуют и маркируют.
Пример 3. Все ингредиенты просеиваются. Соотношение компонентов в масс % в таблетке:
|
Приготовление таблеток-ядер: по способу, описанному в примере 2. Вес ядра составляет 0,09 г. Пленочное покрытие гидроксипропилметилцеллюлозы (порошок) смешивается с порошком амида N-(6-фенилгексаноил)глицил-L-триптофана до получения однородной смеси. В качестве пленочного покрытия выступает 3% водная суспензия. Суспензию пленочного покрытия наносят на таблетки-ядра при температуре 40±2°С в приборе INNOJET AirCoater 025. Прирост массы ядер не превышает 6,0%. Высушенные таблетки обеспыливают, фасуют и маркируют.
Пример 4. Соотношения всех ингредиентов взяты из примера 2. Приготовление таблеток-ядер: по способу, описанному в примере 2. Вес ядра составляет 0,09 г. Пленочное покрытие поливинилового спирта (порошок) смешивается с порошком амида N-(6-фенилгексаноил)глицил-L-триптофана до получения однородной смеси. Далее готовят водную суспензию пленочного покрытия. Суспензию пленочного покрытия наносят на таблетки-ядра при температуре 40±2°С в приборе INNOJET AirCoater 025. Прирост массы ядер не превышает 5%. Высушенные таблетки обеспыливают, фасуют и маркируют.
Пример 5. Соотношения всех ингредиентов взяты из примера 2. Приготовление таблеток-ядер: по способу, описанному в примере 2. В качестве наполнителя взята гидроксипропилцеллюлоза, а в качестве скользящего - коллоидный кремний. Вес ядра составляет 0,09 г. Пленочное покрытие поливинилового спирта (порошок) смешивается с порошком амида N-(6-фенилгексаноил)глицил-L-триптофана до получения однородной смеси. Далее готовят водную суспензию пленочного покрытия с амидом N-(6-фенилгексаноил)глицил-L-триптофана. Суспензию пленочного покрытия наносят на таблетки-ядра при температуре 40±2°С в приборе INNOJET AirCoater 025. Прирост массы ядер не превышает 5%. Высушенные таблетки обеспыливают, фасуют и маркируют.
Пример 6. Все ингредиенты просеиваются.
Соотношение компонентов в масс % в таблетке:
|
Приготовление ядер таблеток: смешиваются наполнитель (маннит) и антифрикционное вещество (магния стеарат) до получения однородной смеси. Полученную порошковую смесь просеивают для достижения однородности смешивания и подвергают прямому прессованию и таблетированию. Вес ядер составляет 0,09 г. В качестве пленочного покрытия используется 5% водная суспензия поливинилового спирта, в которую после образования однородной суспензии вводится амид N-(6-фенилгексаноил)глицил-L-триптофана в сухом виде. Суспензию пленочного покрытия с амидом N-(6-фенилгексаноил)глицил-L-триптофана наносят на таблетки-ядра при температуре 40±2°С в приборе INNOJET AirCoater 025. Прирост массы таблеток-ядер составляет не более 8%. Высушенные таблетки обеспыливают, фасуют и маркируют.
Пример 7. Соотношения всех ингредиентов взяты из примера 3. Приготовление таблеток-ядер: по способу, описанному в примере 3. В качестве наполнителя взята сахароза, а в качестве скользящего - магния стеарат. Вес ядра составляет 0,09 г. Пленочное покрытие поливинилового спирта (порошок) смешивается с порошком амида N-(6-фенилгексаноил)глицил-L-триптофана до получения однородной смеси. Далее готовят водную суспензию пленочного покрытия с амидом N-(6-фенилгексаноил)глицил-L-триптофана. Суспензию пленочного покрытия наносят на таблетки-ядра при температуре 40±2°С в приборе INNOJET AirCoater 025. Прирост массы ядер не превышает 6%. Высушенные таблетки обеспыливают, фасуют и маркируют.
Пример 8. Соотношения всех ингредиентов взяты из примера 2. Приготовление таблеток-ядер: по способу, описанному в примере 2. В качестве наполнителя взята лактоза, а в качестве скользящего - коллоидный кремний. Вес ядра составляет 0,09 г. Пленочное покрытие поливинилового спирта (порошок) смешивается с порошком амида N-(6-фенилгексаноил)глицил-L-триптофана до получения однородной смеси. Далее готовят водную суспензию пленочного покрытия с амидом N-(6-фенилгексаноил)глицил-L-триптофана. Суспензию пленочного покрытия наносят на таблетки-ядра при температуре 40±2°С в приборе INNOJET AirCoater 025. Прирост массы ядер не превышает 5%. Высушенные таблетки обеспыливают, фасуют и маркируют.
Пример 9. Все ингредиенты просеиваются. Приготовление таблеток-ядер: смешиваются два вида наполнителя (лактоза и микрокристаллическая целлюлоза), оболочка - суспензия смеси ГБ-115 и гидроксипропилметицеллюлозы. Смесь наполнителей подвергают таблетированию. Суспензию пленочного покрытия с лекарственным веществом наносят на таблетки-ядра при температуре 40±2°С в приборе INNOJET AirCoater 025. Прирост массы ядра не превышает 12%. Высушенные таблетки обеспыливают, фасуют и маркируют.
|
Пример 10. Результаты теста «Растворение» вариантов фармацевтической композиции на основе амид N-(6-фенилгексаноил)глицил-L-триптофана, изготовленной согласно примерам 1-9.

Согласно Биофармацевтической классификационной системе (Biopharmaceutical Classification System, 1995 г. ), подразделяющей все лекарственные вещества в зависимости от их растворимости и проницаемости в кишечнике, ГБ-115 относится ко II классу веществ, характеризующихся низкой растворимостью и высокой степенью проницаемости. Лекарственные вещества II класса являются классическими объектами для теста "Растворение", поскольку именно для них наибольшее значение имеют такие факторы, как размер частиц субстанции, ее кристаллическое состояние, вид и свойства лекарственной формы [Великая Е.В. и др. Хим.-фарм. журнал. 2004 №5. С. 38-41.]. Корреляция испытаний invivo I invitro с наибольшей вероятностью может быть обнаружена для веществ II класса [Конюшкова А.Н. и др. Обзор требований к исследованиям биоэквивалентности дженериковых лекарственных средств. Требования FDA. Ремедиум. 2011. №5. С. 54-56]. Для всех предлагаемых вариантов выполнения фармацевтической композиции ГБ-115, раскрытых в примерах, был осуществлен тест «Растворение» (согласно ОФС 42-0003-04.), что позволяет экстраполировать значения высвобождения in vitro на эксперименты in vivo и обосновывает достаточность приводимых в описании изобретения сведений для подтверждения фармакокинетических и фармакодинамических свойств заявляемой композиции (Раменская, Г.В. In vivo in vitro корреляция (ivivc): современный инструмент для оценки поведения лекарственных форм в условиях in vivo / invitro Г.В. Раменская, Шохин И.Е., Давыдова К.С., Савченко А.Ю. // Медицинский альманах. - №1. - 2011. - С. 222-226).
Близкие внутриинтервальные показатели высвобождения ГБ-115 из фармацевтических композиций позволяют сделать вывод о возможности установления для данного лекарственного средства корреляции in vivo-in vitro и о близости значений фармакокинетических/фармакодинамических показателей для композиций по всем приведенным примерам (Таблица 1).
Пример 11. Фармакологический эксперимент на крысах после перорального введения субстанции и фармацевтической композиции амида N-(6-фенилгексаноил)глицил-L-триптофана.
Эксперименты были выполнены на беспородных белых крысах-самцах, массой 220-260 г. Животные содержались в стандартных условиях вивария, включая пищевой и водный режимы, 1 неделю до начала эксперимента. В течение 3-4 дней до тестирования с каждым животным проводили процедуру «хэндлинга» для снижения уровня стресса, вызванного экспериментатором. Крыс помещали в стандартные клетки, по 8-10 особей в каждую, не позднее, чем за 3 часа до начала основной части эксперимента, который выполняли в период с 17.00 до 20.00 час в отдельной затемненной комнате при рассеянном свете.
Оценку анксиолитической активности субстанции и фармацевтических композиций амида N-(6-фенилгексаноил)глицил-L-триптофана, их влияние на выраженность тревоги у контрольных и опытных крыс выполняли, используя тест «приподнятый крестообразный лабиринт» (ПКЛ) в базовой модификации. Данный тест рассматривается как наиболее специфический для выявления анксиолитической активности биологически активных соединений. Процедура тестирования в ПКЛ выполнялась в течение 5 минут.Регистрировали стандартные показатели активности животных в ПКЛ, наиболее адекватно характеризующие анксиолитическую активность - число заходов в открытые рукава лабиринта и время пребывания в них [Т.А. Гудашева, М.А. Константинопольский, Р.У. Островская, С.Б. Середенин. Бюлл. экспер. биол. и мед. №5, 2001 г., с. 547-550; S. Pellow, P. Chopin, S.E. File, М. Briley. J. Neyrosci. Methods, 1985, v 14(3): 149-167; S.E. File. Behav. Brain Res. 1993, v 58 (1-2), 199-202].
Водные растворы исследуемой субстанции амида N-(6-фенилгексаноил)глицил-L-триптофана и ее фармацевтической композиции готовили ex tempore с добавлением твин 80 в объеме от 6 до 10 капель в зависимости от массы навески амида N-(6-фенилгексаноил)глицил-L-триптофана с последующим растиранием в стеклянном бюксе. Введение твин 80 в растворитель обусловлено низкой растворимостью в воде субстанции амида N-(6-фенилгексаноил)глицил-L-тршггофана. Напротив, фармацевтическая композиция амида N-(6-фенилгексаноил)глицил-L-триптофана обладала хорошей растворимостью в воде (твин 80 в этом случае добавляли для создания равных по составу растворителей для фармацевтической композиции и субстанции). При приготовлении раствора фармацевтической композиции амида N-(6-фенилгексаноил)глицил-L-триптофана и соответствующего ей раствора плацебо учитывали соотношение субстанции амида N-(6-фенилгексаноил)глицил-L-триптофана к массе ее фармацевтической композиции, равное 1/80. Полученные растворы вводили животным перорально (внутрижелудочно) в объеме 1 мл/ 1 кг массы тела. В качестве контроля вводили равные объемы растворителя для субстанции (дистиллированная вода + твин 80) или водный раствор плацебо + твин 80 при изучении фармацевтической композиции.
Полученные результаты обрабатывали статистически, используя непараметрический критерий "Mann-Whitney - U-test" и описательную статистику для оценки средних значений и различий внутри групп (стандартная ошибка среднего отмечена на диаграммах вертикальными линиями, уровни статистической значимости обозначены как * - Р<0,05; ** - Р<0,01; *** - Р<0,001. Каждый столбец диаграммы отражает усредненные данные по 10-20 животным).
Полученные результаты представлены на фиг. 1-4.
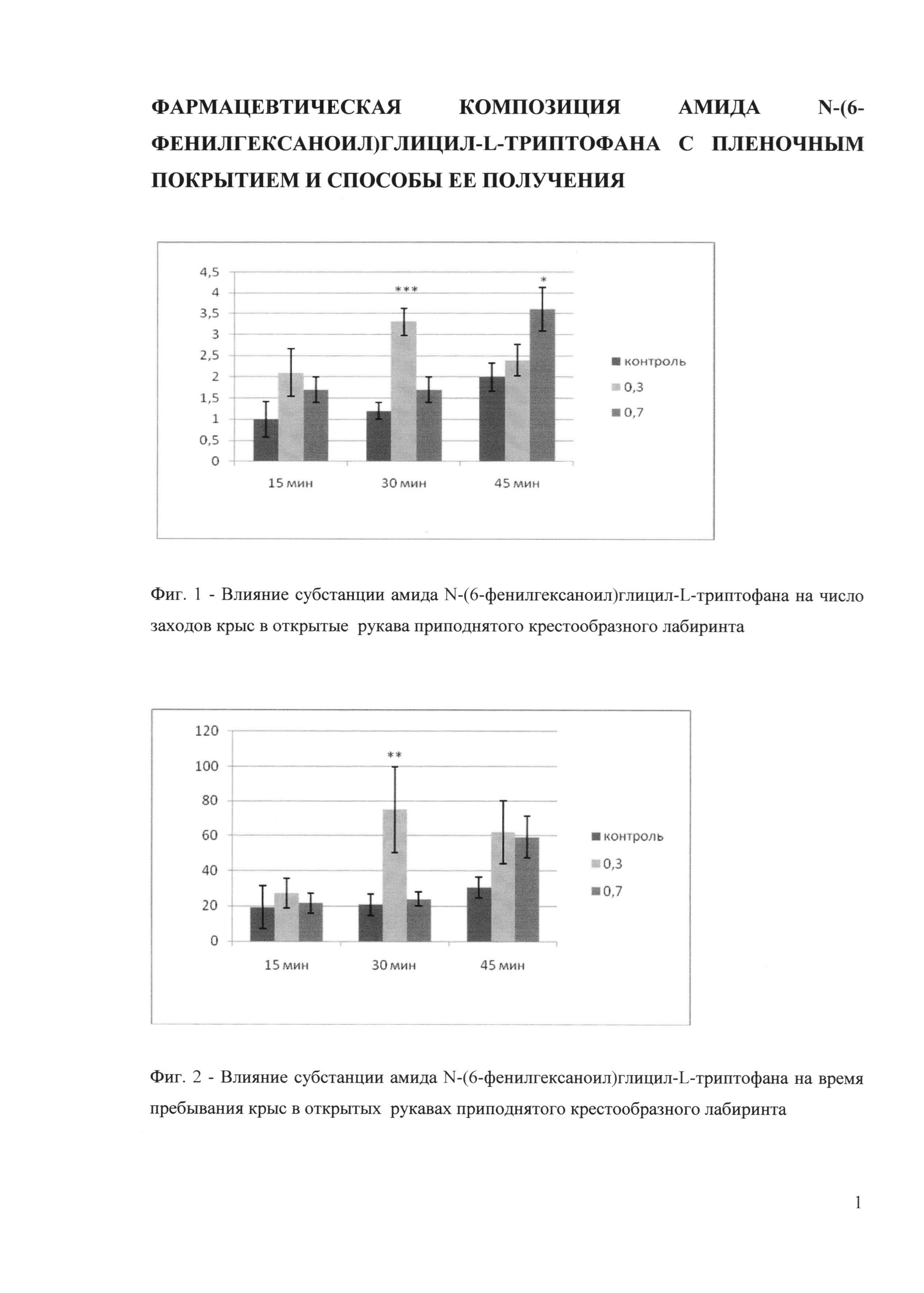
Субстанция амида N-(6-фенилгексаноил)глицил-L-триптофана при введении в дозе 0,3 мг/кг через 30 минут в тесте «приподнятого крестообразного лабиринта» увеличивала число заходов в открытые рукава в 2,8 раза (Р<0,001) и в дозе 0,7 мг/кг через 45 минут - в 1,8 раза (Р<0,05); при этом время пребывания в открытых рукавах через 30 минут после введения данной субстанции в дозе 0,3 мг/кг возрастало в 3,6 раза, Р<0,01 (фиг. 1-2).
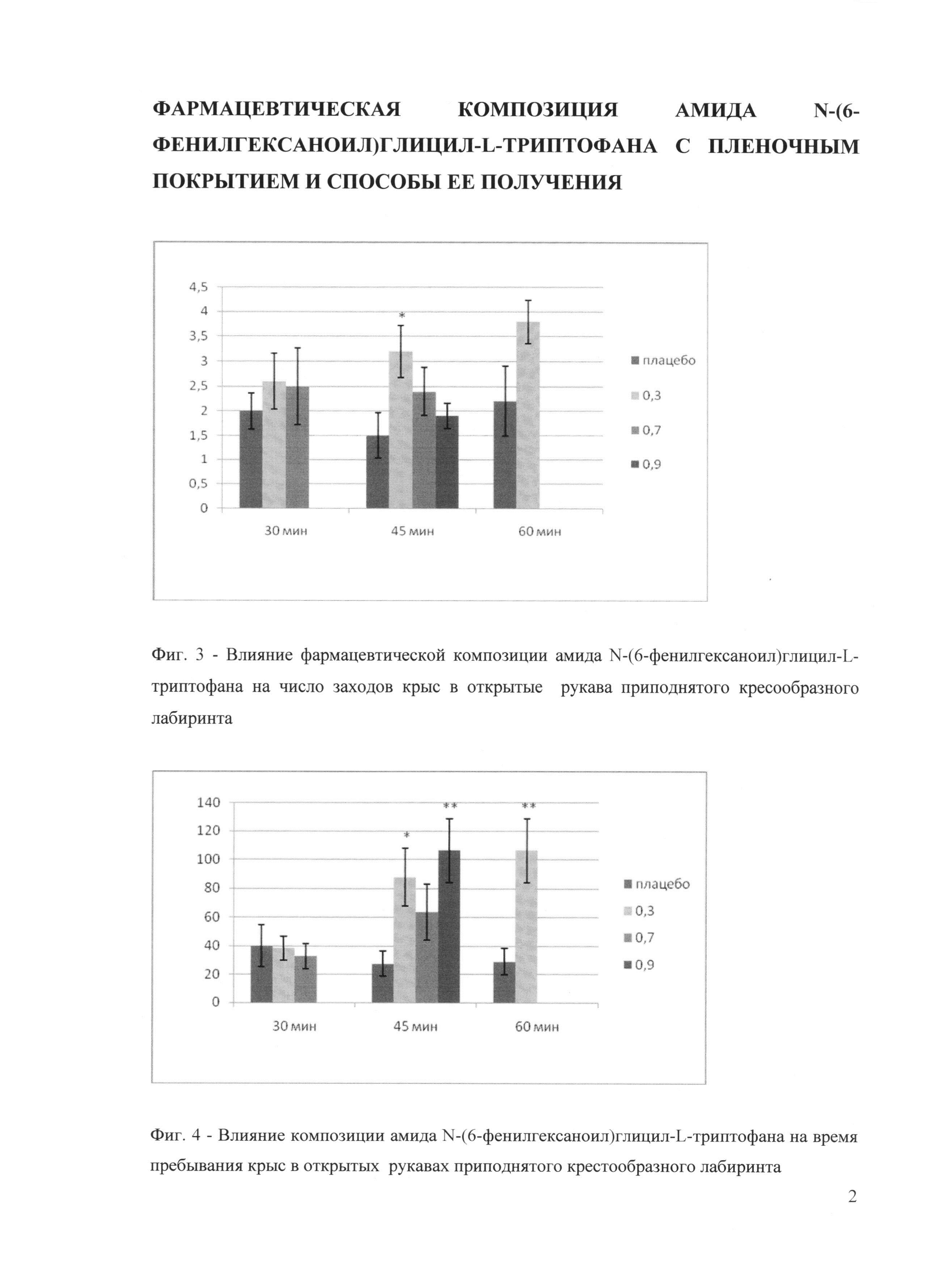
Фармакологическое изучение фармацевтической композиции амида N-(6-фенилгексаноил)глицил-L-триптофана показало наличие выраженной анксиолитической активности у данной композиции - число заходов в открытые рукава возрастало в 2,1 раза через 45 минут после введения в дозе 0,3 мг/кг, Р<0,05 (фиг. 3). Более выражено увеличивалось время пребывания в открытых рукавах - через 45 минут после введения дозы 0,3 мг/кг - в 3,2 раза, после введения дозы 0,9 мг/кг - в 3,9 раза, Р<0,01. Эффект фармацевтической композиции амида N-(6-фенилгексаноил)глицил-L-триптофана в дозе 0,3 мг/кг был продолжительным - через 60 минут после введения в дозе 0,3 мг/кг время пребывания в открытых рукавах превышало соответствующий показатель для контрольной группы (плацебо) в 3,7 раза, Р<0,01 (фиг. 4).
Полученные результаты позволяют заключить, что изученная фармацевтическая композиция амида N-(6-фенилгексаноил)глицил-L-триптофана демонстрирует выраженную анксиолитическую активность по специфическим показателям - числу заходов в открытые рукава «приподнятого крестообразного лабиринта» и времени пребывания в них. Фармацевтическая композиция амида N-(6-фенилгексаноил)глицил-L-триптофана показала специфическую эффективность по анксиолитическому действию в дозе 0,3 мг/кг в интервале времени 45-60 минут после перорального введения животным. Фармацевтическая композиция амида N-(6-фенилгексаноил)глицил-L-триптофана хорошо растворима в воде, без признаков образования взвеси, осадка, хлопьев или помутнения раствора. Субстанция амида N-(6-фенилгексаноил)глицил-L-триптофана была близка по выраженности анксиолитического эффекта к показателям для фармацевтической композиции и демонстрировала эффективность также в дозе 0,3 мг/кг через 30 минут после введения.
Пример 12. Изучение экспериментальной фармакокинетики и биодоступности субстанции ГБ-115 и его фармацевтической композиций для перорального применения
Экспериментальные животные. Фармакокинетику ГБ-115 изучали после перорального введения субстанции и фармацевтической композиции в виде водной суспензии белым беспородным крысам самцам (массой 180П220 г), полученных из питомника «Столбовая». Животных содержали в стандартных условиях вивария при 12 часовом световом режиме и свободном доступе к корму и воде. Исследования проводили на здоровых, бодрствующих животных. До проведения исследования животные находились в течение 12 ч на водной диете.
Масс-спектрометрический анализ соединения ГБ-115 в плазме крови крыс. Анализ биологических проб ГБ-115 проводили с использованием метода высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектором для точной идентификации структуры пептида. Разделение проводили с помощью хроматографа Agilent 1200 Series LC-MSD TRAP (Agilent Technologies, Palo Alto, США) с автоматическим вводом проб, детектора Agilent 6300 series ion-trap (США) и компьютера с соответствующим пакетом для обсчета хроматограмм. Мобильная фаза состояла из 1 л водного раствора с добавлением 50 мл 0.1 М раствора аммония ацетата и 5 мл муравьиной кислоты (А) и 100% ацетонитрила (В). ВЭЖХ анализ проводился в режиме градиентного элюирования: 0 мин - 5% (В), 5 мин - 60% (В), 7 мин - 80% (В), 12 мин - 80% (В), 15 мин - 10% (В). Скорость потока подвижной фазы составляла 0,25 мл/мин. Температура колонки составила 30°С. Объем вкола: 1 мкл.
Масс-спектры были получены с использованием ионизации электрораспылением (ИЭР) и регистрацией как положительных, так и отрицательных ионов. В результате позитивной ионизации образуется ряд положительных ионов с m/z 473, 457, 435, 418, которые предположительно соответствуют катионированным молекулярным ионам [М+K]+, [M+Na]+, [МН]+ и [MH-NH3]+ соответственно. Наличие большого количества пиков затрудняет количественное определение анализируемого вещества. Поэтому была выбрана негативная ионизация, посредством которой образуется один отрицательный ион с m/z=434, который в дальнейшем подвергается фрагментации с образованием ионов с массовыми числами - 286 и 304, что предположительно соответствует следующим фрагментам: ацетат глицил-L-триптофана и гидроксилированный ацетат глицил-L-триптофана, соответственно.
В качестве распыляющего газа использовали азот со скоростью - 9 л/мин.
Методика количественного определения соединения ГБ-115 в плазме крови крыс с применением метода высокоэффективной хроматографии с УФ-детектором. Разделение проводили на жидкостном хроматографе, состоящем из изократической помпы SYSTEM COLD 127 (США), ультрафиолетового детектора и компьютера с соответствующим пакетом программ для обсчета хроматограмм "Амперсенд" (Россия).
Хроматографическое разделение проводили на аналитической колонке - Luna 5μ С 18(2), 250×4,6 мм, детектирование проводили при длине волны 282 нм, что позволило избежать влияния коэкстрактивных веществ, которые мешали бы определению ГБ-115. При использовании диапазона длин волн 200-230 нм наблюдается совпадение максимумов поглощения ГБ-115 и примесей, что и обусловило выбор максимума поглощения в УФ-свете при длине волны 282 нм.
Подвижная фаза - ацетонитрил:вода (400:450), трифторуксусная кислота. Скорость потока подвижной фазы - 1,0 мл/мин. рН раствора составлял 3,2.
Хроматографический анализ проводили при комнатной температуре (22-24°С). Перед хроматографированием подвижную фазу дегазировали на ультразвуковой бане. Пробу вводили при помощи микрошприца в петлю хроматографа объемом 100 мкл.
Обработка биологических проб, экстракция ГБ-115 из биологических образцов
Подготовка плазмы крови крыс к хроматографическому анализу.
Экстракцию ГБ-115 из биологических образцов проводили следующим образом: к 1 мл плазмы крови, содержащей ГБ-115, добавляли двукратный объем ацетонитрила для осаждения белков. Водно-ацетонитрильный раствор центрифугировали при Т -2°С со скоростью 4000 об/мин в течение 10 мин. Далее отбирали очищенную от белков плазму, добавляли 5 мл эфира, встряхивали в течение 15 мин, отделяли эфирный слой и высушивали в токе азота досуха, остаток растворяли в элюенте и вводили в систему ВЭЖХ-УФ.
Фармакокинетические параметры, используемые для интерпретации экспериментальных данных
Основные фармакокинетические параметры рассчитаны модельно-независимым методом (программа «М-IND») [Агафонов А.А., Пиотровский В.К. Метод статистических моментов и внемодельные характеристики распределения и элиминации лекарственных средств. // Хим-фарм. журн. - 1984, №. 7, - С. 845-849]
AUC0→∞ (нг/мл×мин) - площадь под кривой «концентрация лекарственного вещества - время», рассчитывается от момента введения до бесконечности;
AUC0→Т (нг/мл×мин) - площадь под фармакокинетической кривой, рассчитывается от момента введения до момента последней регистрации концентрации исследуемого соединения;
С (нг/мл) - концентрация препарата в плазме крови после перорального введения;
Тмакс (мин) - время достижения максимальной концентрации препарата в плазме крови после перорального введения;
Смаке (нг/мл) - максимальная концентрация лекарственного вещества в плазме крови после перорального введения;
Смаке/AUC (мин-1) - параметр, характеризующий скорость всасывания препарата в системный кровоток;
MRT (мин) - среднее время пребывания лекарственного вещества в организме;
Кэл (мин-1) - константа скорости элиминации, параметр, характеризующий скорость выведения препарата из организма;
Т1/2 (мин) - период, за который выводится половина введенной и всосавшейся дозы лекарственного вещества;
Vzpo, (л) - гипотетический объем распределения;
F (%) - относительная биодоступность: (AUC0→T(A)/AUC0→T(B)×100%).
Статистическая обработка полученных результатов Полученные экспериментальные данные были обработаны с помощью программы «Excel v. 11.0». Достоверность различий для сравниваемых концентраций исследуемых соединений оценивали с помощью критерия Стьюдента [Сергиенко В.И., Бондарева И.Б. Математическая статистика в клинических исследованиях - М.; ГЕОТАР-МЕД, 2001, - с. 256].
Представленные фармакокинетические кривые были построены по усредненным значениям 5-8 полученных данных на каждую временную точку, поэтому при расчетах фармакокинетических параметров отсутствует статистическая обработка результатов. На всех графиках представлены средние значения Xcp±SD (SD - стандартное отклонение).
На фиг. 5 представлены фармакокинетические кривые ГБ-115 в плазме крови крыс после однократного перорального введения ГБ-115 в виде водного раствора субстанции, а также его фармацевтической композици в дозе 100 мг/кг.
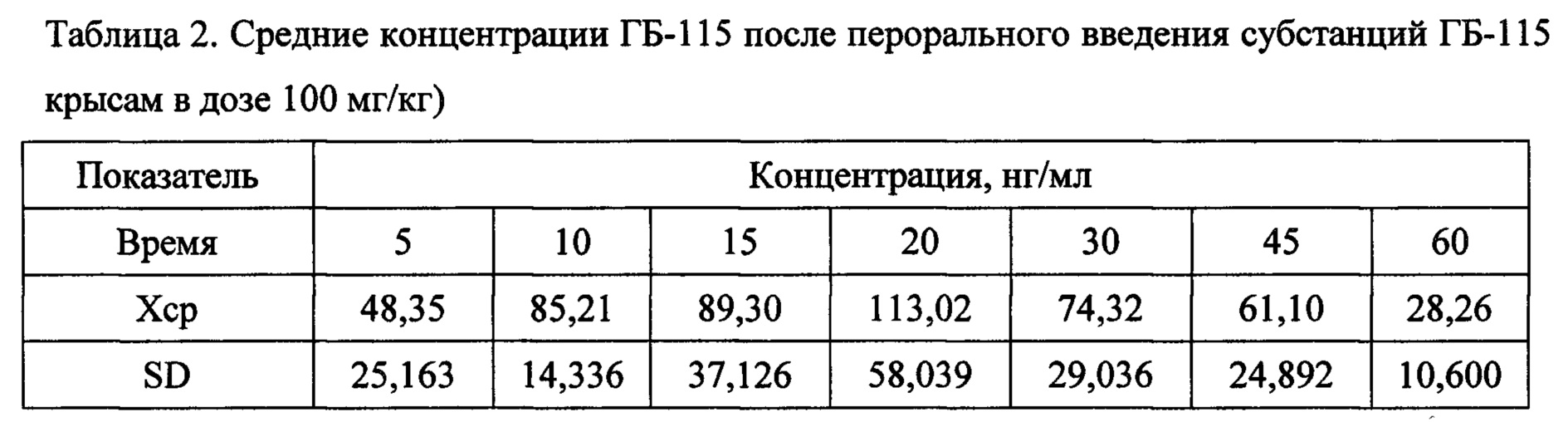
Как видно из фиг. 5 ГБ-115 быстро всасывается в ЖКТ, поступает в системный кровоток и определяется в плазме крови крыс уже через 5 мин после введения как субстанции, так и фармацевтической композиции. В таблице 2 представлены средние концентрации ГБ-115 после перорального введения субстанций ГБ-115 крысам в дозе 100 мг/кг. Время регистрации ГБ-115 в плазме крови крыс 60 мин. Максимум его концентрации наблюдаются через 20 мин после введения субстанции.
На фиг. 5 представлены фармакокинетические кривые ГБ-115 полученные после перорального однократного введения в дозе 100 мг/кг субстанции (1) и фармацевтической композиции (2).
Фармацевтическая композиция отличается начальным резким подъемом концентрации фармакологически активного соединения: уже через 5 мин после введения она составляет более 106,67 нг/мл и достигает максимума через 15 мин - 121,5 нг/мл. В последующие интервалы времени концентрация ГБ-115 постепенно снижается на протяжении 1,5 ч и в конечный период времени (через 90 мин) регистрируется в достаточно высоком количестве - 53,68 нг/мл.
На основании полученных экспериментальных данных рассчитаны основные фармакокинетические параметры ГБ-115, которые представлены в сводной табл.3. Для сравнения длительности пребывания активного вещества в неизменном виде в организме испытуемых животных после введения каждого из рассматриваемых объектов необходимо сравнить следующие параметры: Kel, T1/2, MRT. ГБ-115 быстрее выводится из организма после введения субстанции: значение константы скорости элиминации - 0,0323 мин-1, период полувыведения - 21,49 мин и время удержания лекарственного вещества в плазме крови крыс - 39,87 мин. Фармацевтическая композиция отличается от субстанции более медленным выведением неизмененного вещества, что является хорошим показателем для фармацевтических композиций, содержащих пептидные соединения, Kel 0,0109 мин-1. Получены следующие фармакокинетические характеристики для фармацевтической композиции: невысокое значение клиренса Clpo 1,585 мл/мин, длительный период полувыведения - 63,86 мин и значительная величина показателя среднего времени удержания ГБ-115 в плазме крови крыс - MRT - 95,75 мин, значение клиренса невысокое Clpo 1,585 мл/мин.

Для фармацевтической композиции характерно высокое значение гипотетического объема распределения - 146,00 мл, что выше объема распределения субстанции - 124,40 мл.
По сравнению с субстанцией при введении животным фармацевтической композиции наблюдается большее значение площади под фармакокинетической кривой ГБ-115 (табл. 3) - показатель относительной биодоступности составляет 133,83%, что указывает на преимущество композиции перед субстанцией.
Описание чертежей
Фиг. 1. Влияние субстанции амида N-(6-фенилгексаноил)глицил-L-триптофана на число заходов крыс в открытые рукава приподнятого крестообразного лабиринта. По оси абсцисс представлены группы животных и соответствующие дозы вводимых веществ: 1 - контроль (Н2О + твин 80); 2 - 0,3 мг/кг; 3 - 0,7 мг/кг для субстанции амида N-(6-фенилгексаноил)глицил-L-триптофана. По оси ординат - число заходов в открытые рукава лабиринта; вертикальные линии на столбцах показывают стандартную ошибку среднего. Статистическая значимость (Р): * - Р<0,05; *** - Р<0,001. Число животных в каждой группе 9-11.
Фиг.2. Влияние субстанции амида N-(6-фенилгексаноил)глицил-L-триптофана, вводимой per os за 30 минут до тестирования, на время пребывания крыс в открытых рукавах приподнятого крестообразного лабиринта. По оси абсцисс представлены группы животных и соответствующие дозы вводимых веществ: 1 - контроль (Н2О + твин 80); 2 - 0,3 мг/кг; 3 - 0,7 мг/кг для субстанции амида N-(6-фенилгексаноил)глицил-L-триптофана. По оси ординат - время пребывания крыс в открытых рукавах лабиринта в секундах; вертикальные линии на столбцах показывают стандартную ошибку среднего. Статистическая значимость: ** - Р<0,01. Число животных в каждой группе 9-11.
Фиг. 3. Влияние фармацевтической композиции амида N-(6-фенилгексаноил)глицил-L-триптофана на число заходов, совершенных крысами, в открытые рукава приподнятого крестообразного лабиринта. По оси абсцисс представлены группы животных и соответствующие им дозы веществ, вводимые на каждом из временных интервалов (15-45 мин): 1 - контроль (плацебо + твин 80); 2 - 0,3 мг/кг; 3 - 0,7 мг/кг; 4 - 0,9 мг/кг для фармацевтической композиции амида N-(6-фенилгексаноил)глицил-L-триптофана; по оси ординат - число заходов в открытые рукава; вертикальные линии на столбцах показывают стандартную ошибку среднего. Статистическая значимость: * - Р<0,05. Число животных в каждой группе 10-12.
Фиг. 4. Влияние фармацевтической композиции амида N-(6-фенилгексаноил)глицил-L-триптофана на время пребывания крыс в открытых рукавах приподнятого крестообразного лабиринта. По оси абсцисс представлены группы животных и соответствующие им дозы веществ, вводимые на каждом из временных интервалов (15-45 мин): 1. - контроль (плацебо + твин 80); 2. - 0,3 мг/кг; 3. - 0,7 мг/кг; 4. - 0,9 мг/кг для фармацевтической композиции амида N-(6-фенилгексаноил)глицил-L-триптофана; по оси ординат - время пребывания крыс в открытых рукавах лабиринта в секундах; вертикальные линии на столбцах показывают стандартную ошибку среднего. Статистическая значимость: * - Р<0,05; ** - Р<0,01. Число животных в каждой группе 10-12.