Результат интеллектуальной деятельности: ФОТОСТАБИЛЬНАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ТЕРАПИИ ОЧАГОВ БАКТЕРИАЛЬНОГО ПОРАЖЕНИЯ
Вид РИД
Изобретение
Настоящее изобретение относится к микробиологии и медицине, а именно к фармацевтической композиции, используемой для терапии очагов бактериального поражения.
Проблема борьбы с инфекционными заболеваниями, связанная с возрастающей резистентностью штаммов патогенных бактерий, вызывающих хронические заболевания различной локализации, к антибиотикам широкого спектра действия, стала одной из основных проблем современной медицины. В последнее время установлено, что имеющие сложную структуру организованные сообщества патогенных бактерий (так называемые бактериальные биопленки) практически не поддаются терапии с помощью антибиотиков и являются причиной не только хронических инфекционных заболеваний (таких как гнойные раны, трофические язвы), но и возникающих тяжелых осложнений в кардиохирургии, урологии и других областях медицины, при которых в организм пациента вводятся медицинские изделия (катетеры, стенты, искусственные клапаны и суставы). Кроме того, установлено, что одной из причин образования почечных камней и камней желчного пузыря, а также до 80% инфекционных рецидивов мочекаменной болезни являются именно бактериальные пленки (Романова Ю.М. и др. Микробные сообщества на мочевых камнях // Молекулярная генетика, микробиология и вирусология. 2015. №2. С. 20-25).
Сложная инфраструктура и иерархия бактерий в бактериальной пленке, формирование ею специальных средств жизнеобеспечения и защиты в виде пленочного матрикса приводят к тому, что для лечения таких бактериальных поражений дозы антибиотиков надо было бы увеличивать в сотни раз, что выходит за пределы реальных возможностей организма.
Обнаружено, что для инактивации бактерий и биопленок может быть использована фотодинамическая терапия, причем у бактерий не формируется резистентность к этому способу лечения. Наиболее целесообразно для повышения эффективности фотодинамической инактивации бактерий и биопленок использовать катионные фотосенсибилизаторы, которые позволяют эффективно воздействовать как на грамположительные, так и на грамотрицательные бактерии (RU 2282647 C1, RU 2397172 С1). Возбуждение этих фотосенсибилизаторов осуществляется в спектральном диапазоне 670-770 нм.
Известна группа изобретений относящихся к фармацевтической химии, а именно к катионному пурпуринимиду и его применению в качестве фотосенсибилизатора (ФС) для фотодинамической инактивации бактериальных биопленок. Группа изобретений раскрывает катионный пурпуринимид, представляющий собой метиловый эфир 133-N-(N-метилникотинил)пурпуринимида, и его применение в виде кремофорной дисперсии для фотодинамической инактивации бактериальных биопленок (RU 2565450 С1).
Самым близким является способ фотодинамической терапии локальных очагов инфекции, включающий сенсибилизацию очагов катионным фотосенсибилизатором и их облучение светом на длине волны поглощения фотосенсибилизатора, используют фотосенсибилизатор с поглощением в спектральном диапазоне 810-850 нм, в качестве фотоактивной субстанции фотосенсибилизатора используют метиловый эфир 133-N-(N-метилникотинил)бактериопурпуринимида. При этом для введения субстанции фотосенсибилизатора используется композиция на основе метилового эфира 133-N-(N-метилникотинил) бактериопурпуринимида и гидрогенизированного касторового масла (Кремофора). Данная композиция используется для приготовления жидкой лекарственной формы метилового эфира 133-N-(N-метилникотинил)бактериопурпуринимида в виде эмульсии (RU 2610566 С1).
К недостаткам такой композиции следует отнести низкий уровень фотостабильности получаемой жидкой лекарственной формы метилового эфира 133-N-(N-метилникотинил) бактериопурпуринимида, что приводит к недостаткам, обусловленным коротким сроком хранения вышеуказанной жидкой лекарственной формы, и, как следствие, к существенным ограничениям при проведении терапии. К таким ограничениям относится необходимость приготовления жидкой лекарственной формы метилового эфира 133-N-(N-метилникотинил) бактериопурпуринимида в виде эмульсии на основе вышеуказанной композиции непосредственно перед проведением терапии. Другим ограничением при использовании вышеуказанной композиции является низкий уровень эффективности терапии очагов бактериального поражения жидкой лекарственной формы метилового эфира 133-N-(N-метилникотинил) бактериопурпуринимида в виде эмульсии на основе вышеуказанной композиции, обусловленный низким уровнем биодоступности молекул 133-N-(N-метилникотинил) бактериопурпуринимида для вследствие гетерогенности используемой эмульсии.
Задачей данного изобретения является создание фармацевтической композиции для терапии локальных очагов инфекции, обладающей высоким уровнем фотостабильности, а также высоким уровнем эффективности терапии очагов бактериального поражения.
Решение поставленной задачи обеспечивается тем, что фармацевтическая композиция для терапии локальных очагов инфекции, содержит (% мас.):
|
Как вариант осуществления изобретения, заявленная фармацевтическая композиция используется для приготовления лекарственных форм для парентерального введения. Заявленную фармацевтическую композицию получают путем:
- смешения Твина - 80 и воды с получением водного раствора Твина-80,
- одновременного растворения гидроксипропил-бета-циклодекстрина и метилового эфира 133-N-(N-метилникотинил) бактериопурпуринимида при равномерном перемешивании и нагревании до температуры 60°С с получением водного раствора Твина-80, гидроксипропил-бета-цикл о декстрина и метилового эфира 133-N-(N-метилникотинил) бактериопурпуринимида,
- фильтрации водного раствора Твина-80, гидроксипропил-бета-циклодекстрина и метилового эфира 133-N-(N-метилникотинил)бактериопурпуринимида с получением водного раствора заявленной фармацевтической композиции,
- высушивания водного раствора заявленной фармацевтической композиции с получением заявленной фармацевтической композиции.
Заявителем экспериментально установлен высокий уровень фотостабильности и эффективности предложенной фармацевтической композиции при терапии локальных очагов инфекции.
Вышеуказанная композиция обладает высоким уровнем фотостабильности за счет стабилизации метилового эфира 133-N-(N-метилникотинил)бактериопурпуринимида молекулами гидроксипропил-бета-циклодекстрина посредством образования водородных и Ван-дер-Ваальсовых связей, а также за счет гидрофобных взаимодействий. При этом композиция обладает высоким уровнем эффективности терапии локальных очагов инфекции за счет высокого уровня биодоступности молекул метилового эфира 133-N-(N-метилникотинил)бактериопурпуринимида за счет эффекта, заключающегося в стабилизации метилового эфира 133-N-(N-метилникотинил)бактериопурпуринимида молекулами гидроксипропил-бета-циклодекстрина при повышении растворимости заявленной фармацевтической композиции в воде за счет Твина-80 (Полисорбата-80).
Примеры осуществления вышеизложенного изобретения
Пример 1
Оценка эффективности заявленной фармацевтической композиции при терапии очагов бактериального поражения.
Целью исследования является оценка эффективности заявленной фармацевтической композиции при терапии очагов бактериального поражения.
Заявленная фармацевтическая композиция (Группа 1) представляет собой аморфный порошок от розового цвета, растворимый в воде, практически не растворимый в хлороформе, ацетоне, гексане. Водные растворы композиции прозрачные, не содержат механических включений. В составе композиции содержится Метиловый эфир 133-N-(N-метилникотинил)бактериопурпуринимида, гидроксипропил-бета-циклодекстрин (ГПЦД) и Твин-80 (Полисорбат-80).
Состав композиции (% мас.):
|
В качестве положительного контроля (Группа 2) использовали композицию, содержащую метиловый эфир 133-N-(N-метилникотинил)бактериопурпуринимида, а также гидрогенизированное касторовое масло (Кремофор) в качестве стабилизатора.
Состав композиции (% мас.):
|
Для моделирования раневой инфекции, вызванной клиническими изолятами Р. aeruginosa, и S. aureus были использованы мыши Balb/c, приобретенные в питомниках «Столбовая» и «Андреевское», которые поддерживались в виварии ФГБУ «ФНИЦЭМ им. Н.Ф. Гамалеи» Минздрава РФ в соответствии с Требованиями по содержанию животных МЗ РФ №775. Воду и пищу животные получали ad libitum. В опытах были использованы самцы, весом 18-20 г. Количество животных, используемых в исследовании, по 18 голов в 1 и 2 группе и в 3 группе 6 голов, что является достаточным для полной регистрации изучаемых эффектов.
Бактериальную культуру выращивали в жидкой среде LB (LB - бульон), при 37°С в течение 18 часов, затем разводили в 100 раз средой LB и культивировали с аэрацией в течение 3-х часов. После окончания периода культивирования культуру центрифугировали (6000 об/мин, 5 мин.), бактериальный осадок ресуспендировали в физиологическом растворе до оптической плотности 0,9 при 600 нм и использовали для заражения животных. Для определения количества КОЕ отбирали аликвоту полученной суспензии (100 мкл), готовили серию десятикратных разведений и по 500 мкл разведенной культуры наносили на чашки Петри с агаром LB. Чашки Петри культивировали при 37°С, через 18 часов производили подсчет колоний. Титр бактерий в суспензии выражали числом КОЕ/мл.
Для создания экспериментальной раневой инфекции мышам после депиляции участка задней конечности и анестезии были нанесены хирургические раны путем отрезания ножницами участка кожи размером 0,5 см2 на полную глубину. Салфетку из стерильного бинта клали на поверхность раны и закрывали липкой стерильной повязкой OPSITE. Бактериальные суспензии P. aeruginosa или S. aureus в объеме 100 мкл вносили шприцем через повязку и бинт на поверхность раны, в дозах от 1×108 до 1×104 КОЕ/мышь.
На 1 сутки после инфицирования раны животным в Группах 1 и 2 однократно внутривенно вводили соответствующие композиции в различных дозах в пересчете на метиловый эфир 133-N-(N-метилникотинил)бактериопурпуринимида. Дизайн экспериментов представлен в таблицах 1 и 2. Также в качестве отрицательного контроля (Группа 3) животным вводили растворитель. ФДТ проводили под обезболиванием. За 4-5 минут до облучения животное было анестезировано. Во время процедуры мышь фиксировали и накрывали защитным экраном из черной фотобумаги. Для облучения животных был использован светодиодный источник СФД-820 с длиной волны спектрального максимума 822 нм и полушириной 35 нм. Формы спектров излучения заявленной фармацевтической композиции и положительного контроля были близки к форме контура спектра абсорбции метилового эфира 133-N-(N-метилникотинил)бактериопурпуринимида. Источник формировал на облучаемой поверхности равномерное пятно света квадратной формы размером 1×1 см2. Мощность и плотность мощности контролировалась с помощью измерителя мощности «Coherentlabmax" ("Coherent", USA). Плотность дозы облучения регулировалась изменением длительности экспозиции и вычислялось по формуле:
D=P×T,
где D [Дж/см2] - плотность дозы,
Р [Вт/см2] - плотность мощности,
Т - время экспозиции, сек.
После облучения регистрировалось общее состояние животных, наличие отека и струпа в зоне облучения. Рану после облучения закрывали стерильной повязкой Тегадерм, которую меняли ежедневно. Эффективность заявленной фармацевтической композиции (Группа 1) при терапии очагов бактериального поражения оценивалась по статистически достоверному сокращению сроков полной эпителизации раны. Также определяли минимальную эффективную дозу фармацевтической композиции (Группа 1) при плотности световой энергии (дозе света) 15 Дж/см.
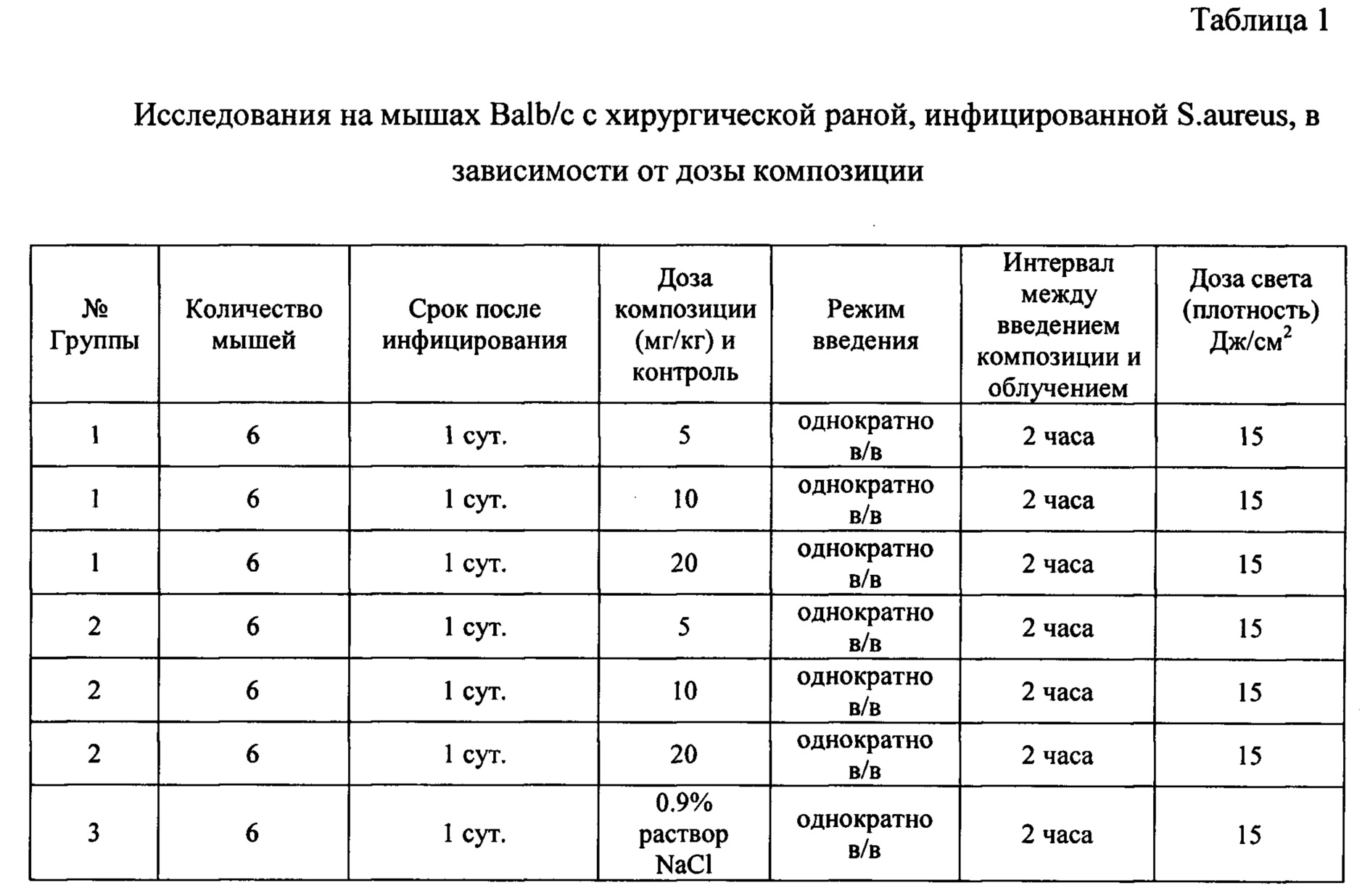
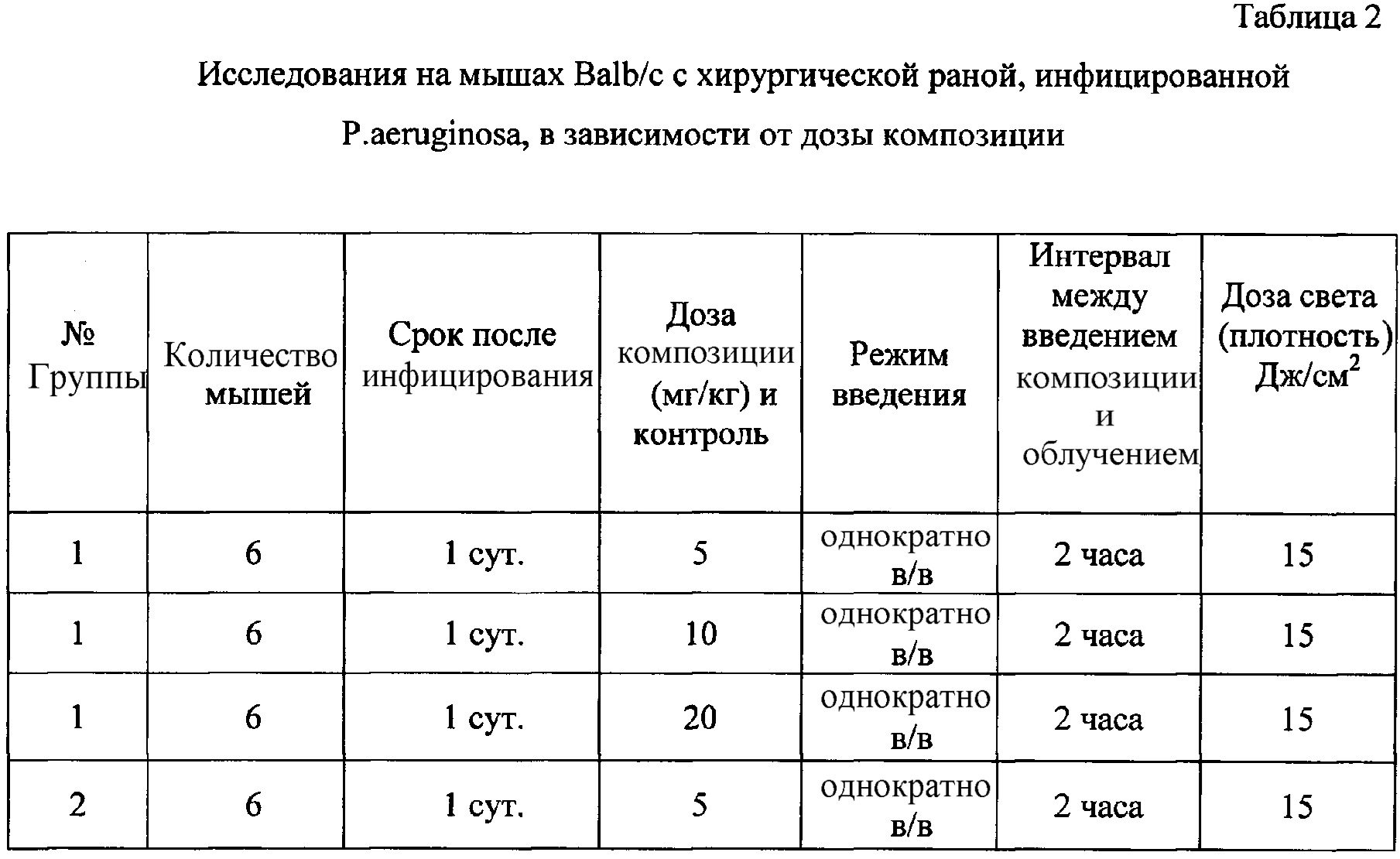
На основании полученных данных были рассчитаны следующие критерии: средний срок полной эпителизации раны для всех групп от дня инфицирования, стандартная ошибка средней, доверительный интервал. При сравнении групп использовали метод Стьюдента-Фишера, по которому различия между группами можно считать достоверными при p≤0,05.
Все данные, полученные в ходе настоящего исследования, были занесены в специальные регистрационные карты.
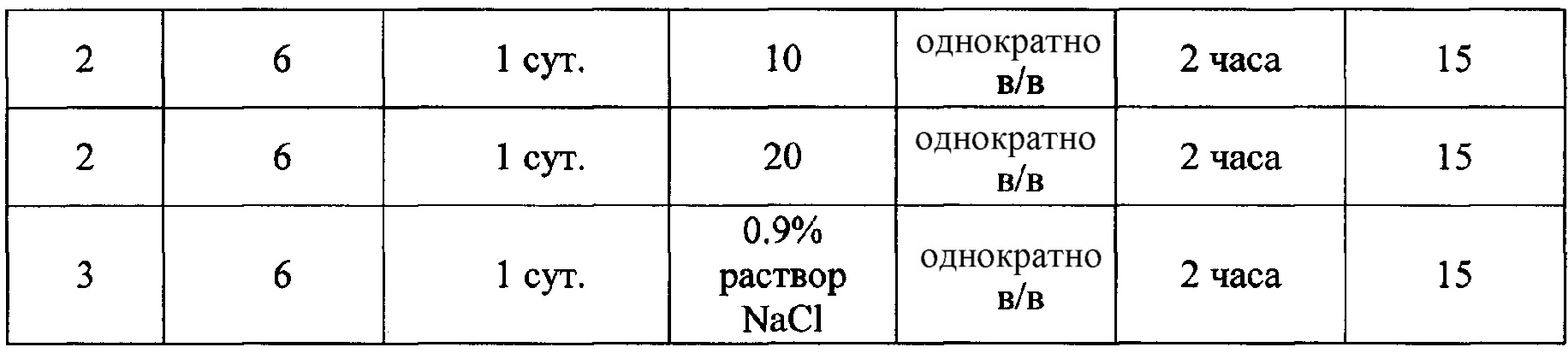
Результаты исследования приведены в таблицах 3 и 4.
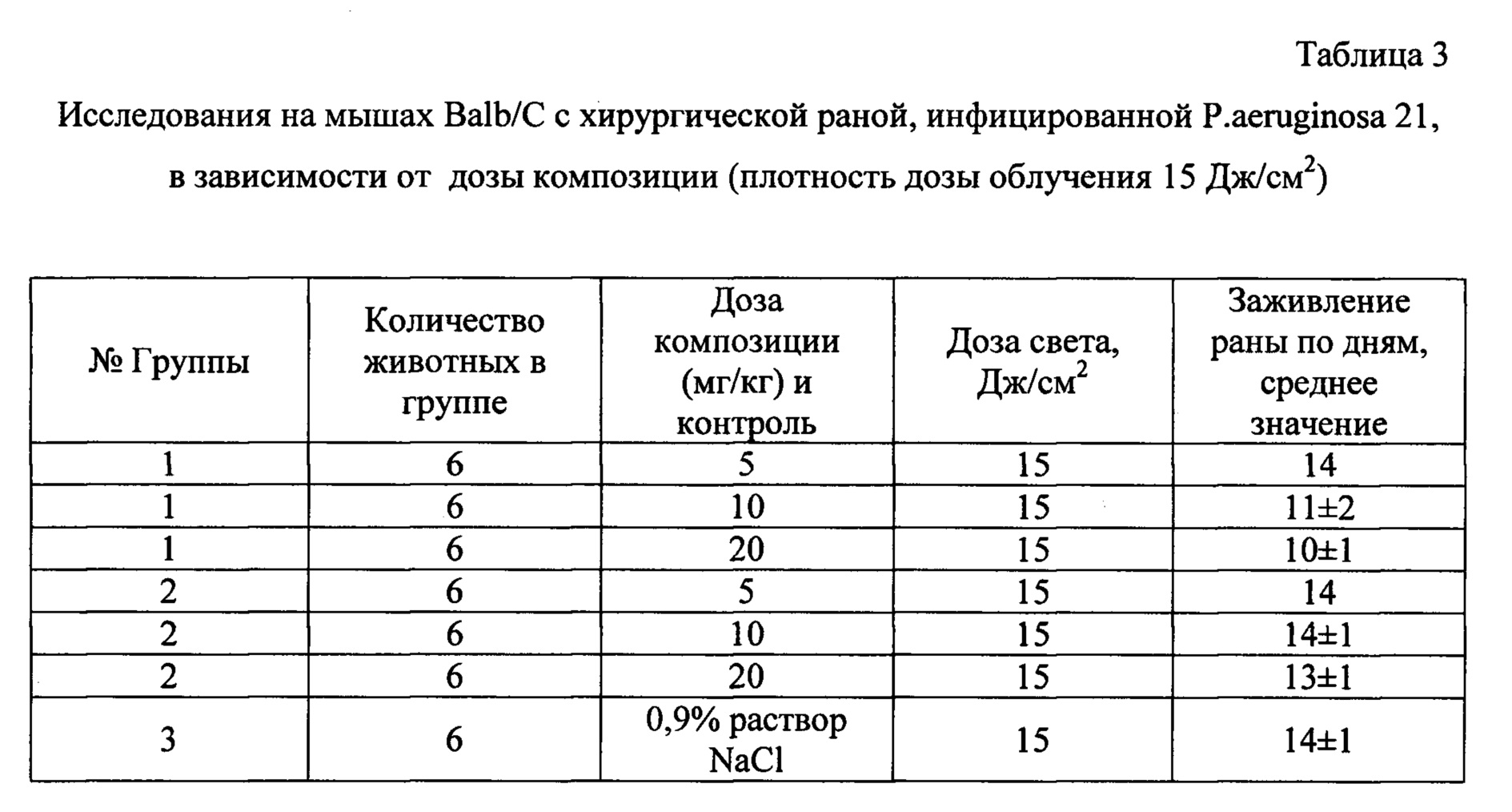

В группах мышей, подвергнутых ФДТ, общее состояние удовлетворительное. В зоне облучения отеков не обнаружено, с первого дня лечения раневой экссудат не выделяется. Состояние контрольных мышей (Группы 2 и 3) также удовлетворительное, но в зоне раны обнаружен отек и гной.
В результате проведенных исследований была выявлена минимальная эффективная доза фармацевтической композиции, составляющая:
|
|
Проведенные in vivo на модели инфицированных ран у белых мышей исследования, целью которых было оценка эффективности заявленной фармацевтической композиции при терапии очагов бактериального поражения, показали следующее:
- заявленная фармацевтическая композиция при однократном внутривенном введении эффективна при раневых инфекциях, вызванных как S. aureus, так и P. aeruginosa, что выражается в достоверном сокращении времени заживления ран у животных, подвергнутых терапии, по сравнению с положительным и отрицательным контролем; заявленная фармацевтическая композиция эффективна при терапии очагов бактериального поражения;
- оптимальная доза заявленной фармацевтической композиции для S. aureus составила 10 мг/кг, а для P. aeruginosa - 20 мг/кг.
Пример 2
Исследование фотостабильности фармацевтической композиции (Образец 1) для терапии очагов бактериального поражения следующего состава (% мас.):
|
Навеску 35,8 мг, содержащую 0,5 мг активного вещества, растворили в 1 мл 0,9% хлорида натрия. Композиция легко растворяется в хлориде натрия с образованием раствора розового цвета. Концентрация активного вещества - 0,5 мг/мл.
В качестве положительного контроля (Образец 2) в 1 мл 0,9% хлорида натрия растворили 40,5 мг композиции, содержащей 0,5 мг активного вещества (Метиловый эфир 133-N-(N-метилникотинил)бактериопурпуринимида), а также 40 мг гидрогенизированного касторового масла (Кремофор) в качестве стабилизатора. Концентрация активного вещества - 0,5 мг/мл.
Оценку фотостабильности проводили методом флуоресцентной спектроскопии. Спектры флуоресценции регистрировали на лазерной установке для флуоресцентной диагностики и контроля за фото динамической терапией «ЛЭСА-06». Спектры регистрировали в 0,9% растворе хлорида натрия и 3% растворе ЧСА. Концентрация по активному веществу при измерении спектров флуоресценции составляла 0,1 мг/мл. Флуоресценцию измеряли ex tempore, через 1, 2 и 4 часа. Интенсивность флуоресценции представлена в таблице 5.
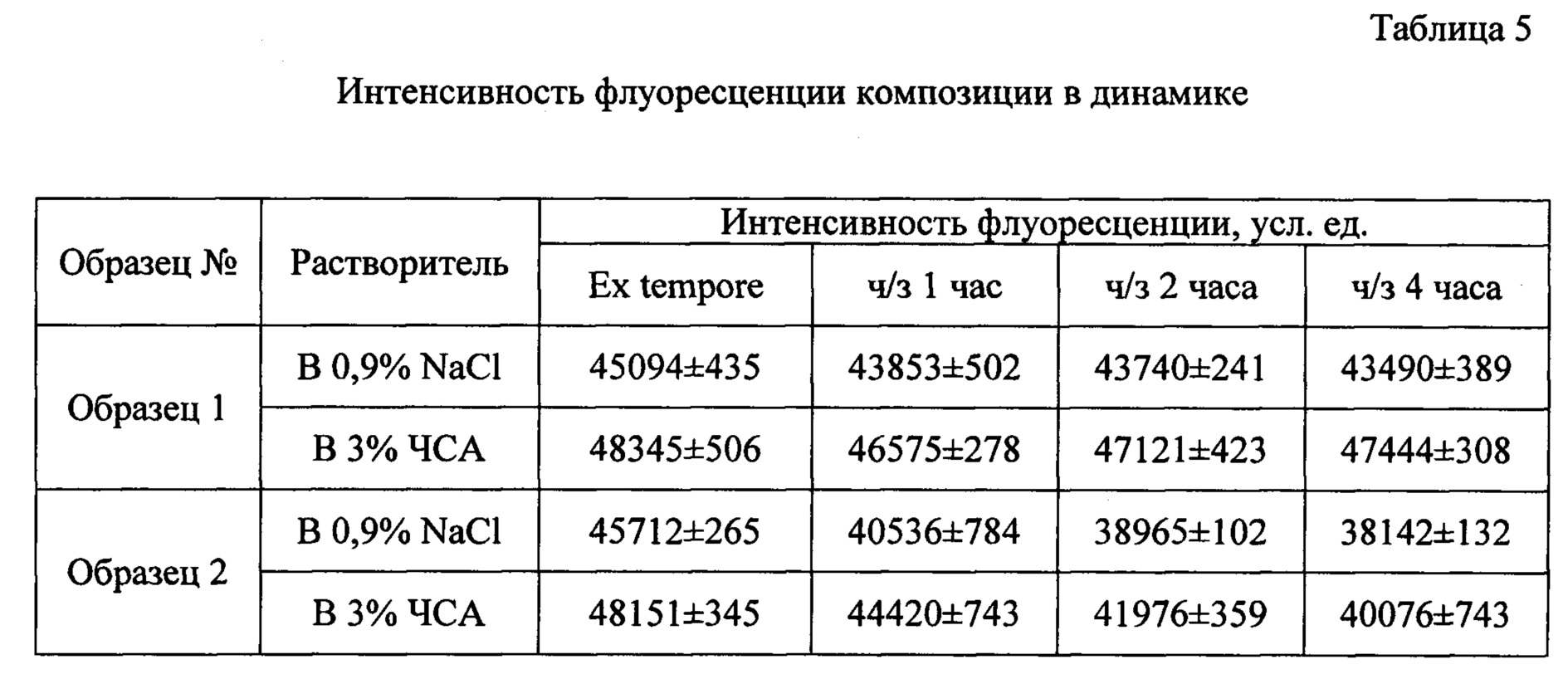
Из полученных в результате исследования данных можно сделать вывод о повышенном уровне фотостабильности заявленной фармацевтической композиции по сравнению с контролем в виде композиции, содержащей Кремофор.
Пример 3
Оценка эффективности инактивации биопленок путем использования заявленной фармацевтической композиции.
Целью исследования является оценка эффективности заявленной фармацевтической композиции при инактивации биопленок.
Заявленная фармацевтическая композиция (ФК) представляет собой аморфный порошок розового цвета, растворимый в воде, практически не растворимый в хлороформе, ацетоне, гексане. Водные растворы продукта прозрачные, не содержат механических включений. В составе продукта содержится Метиловый эфир 133-N-(N-метилникотинил)бактериопурпуринимида, гидроксипропил-бета-циклодекстрин (ГПЦЦ) и Твин-80 (Полисорбат-80).
Состав композиции (% мас.):
|
Бактерии и их культивирование.
Использовали эталонные штаммы бактерий Staphylococcus aureus и Pseudomonas aeruginosa (из международных и региональных коллекций) и изоляты из образцов клинического материала из коллекции ФНИЦЭМ им. Н.Ф. Гамалеи. Культуры бактерий пересевали каждый месяц, делая не более 5 пассажей с агара на агар, после чего использовали исходную культуру со среды хранения.
Тест-штаммы бактерий хранили при температуре -74°С в среде LB с глицерином 1:1.
Питательные среды:
|
Для приготовления питательного агара LB добавляли 1% агара.
Фосфатно-солевой буфер 0,01 М (ЭКО сервис, Россия) (в таблетках)
|
Проверка способности бактерий к образованию биопленок
Для изучения способности микроорганизмов формировать биопленки ночную культуру бактерий, выращенную в бульоне LB, в разведении 1:100 в LB вносили по 100 мкл в 4 лунки 96-ти луночного плоскодонного полистиролового планшета. После 24 ч инкубации в термостате при 37°С во влажной камере интенсивность роста культуры оценивали в фотометре при длине волны 540 нм, затем планктонные клетки удаляли, в лунки вносили по 100 мкл 0,1% раствора кристалл-виолета для окраски сформировавшихся биопленок в течение 1 часа. После окраски биопленки трижды промывали дистиллированной водой и в лунки вносили по 100 мкл 96% этанола для экстракции связавшегося с биопленками красителя. По истечении 1 часа интенсивность экстрагированного спиртом красителя измеряли на фотометре при длине волны 540 нм. Вычисляли среднее арифметическое значение из 4 лунок. Контролем служили лунки, заполненные LB-бульоном. Превышение оптической плотности кристалл-виолета над контролем свидетельствовало об образовании бактериями биопленок.
Выращивание ночной культуры тест-микроорганизмов
В стерильный LB-бульон засевали культуру бактерий с чашки Петри и выращивали в термостате при 37°С с интенсивной аэрацией 18 ч.
Выращивание биопленок бактерий на стеклянных пластинках
Для определения фотоинактивации бактерий в биопленках использовали плоские стеклянные пластинки и механическое разрушение биопленок Вортексом. Стеклянные пластинки 8×12 мм толщиной 1 мм стерилизовали в 70% этаноле и подсушивали в чашке Петри 90 мм диаметром в стерильных условиях (в ламинарном боксе). Ночную культуру бактерий разводили 1:100 бульоном LB и 22 мл разведенной культуры переносили в чашку со стерильными пластинками. Чашку инкубировали при 37°С в течение 20 ч при покачивании 10 раз в минуту, угол наклона 4°.
Пластинки переносили в лунки двух 24-луночных планшетов (один для освещения, другой для неосвещенного контроля). Лунки заполняли 400 мкл ФСБ и через 1 мин жидкость отбирали аспиратором. Следующие процедуры проводили при затемнении.
Фотосенсибилизация
В каждую лунку вносили по 400 мкл раствора заявленной фармацевтической композиции определенной концентрации из двукратных разведений, в контроле - 400 мкл ФСБ. Планшеты инкубировали в течение 1 ч в темноте при 37°С. Затем жидкость отбирали аспиратором и в лунки добавляли по 400 мкл ФСБ.
Облучение
Для облучения использовали светодиодный источник СФД-820 с длиной волны спектрального максимума 821 нм и полушириной 35 нм. Форма спектра излучения была близкой к форме контура спектра поглощения фармацевтической композиции. Источник формировал на облучаемой поверхности равномерное пятно света круглой формы размером 8×8 см. Мощность и плотность мощности контролировалась с помощью измерителя мощности «Coherent labmax" ("Coherent ",USA).
Разрушение биопленок
Пластинки и жидкость из лунок переносили в пробирки «Eppendorf», биопленку с обеих сторон стекла снимали одноразовыми гинекологическими зондами, щеточки зондов отрезали и оставляли в пробирках. Пробирки обрабатывали на Вортексе 10 мин на максимальном режиме.
Высев и учет результата
Из каждой пробирки отбирали по 30 мкл для приготовления пяти десятикратных разведений в микротитровальном планшете, в лунки которого был налит ФСБ по 270 мкл. На чашку Петри диаметром 90 мм, разделенную на 6 секторов высевали по 20 мкл из каждой лунки, начиная с 5 разведения и заканчивая неразведенной пробой. Таким образом производили высев с каждой пластинки на 3 чашки. Чашки инкубировали в темноте при 37°С в течение 20 ч, затем производили подсчет колоний, в разведениях, где это возможно, и вычисляли титр КОЕ/мл по формуле:
N=C*50*10x/3,
где N - число КОЕ в 1 мл,
С - сумма колоний на 3 чашках в одном разведении,
x - номер разведения.
Результаты
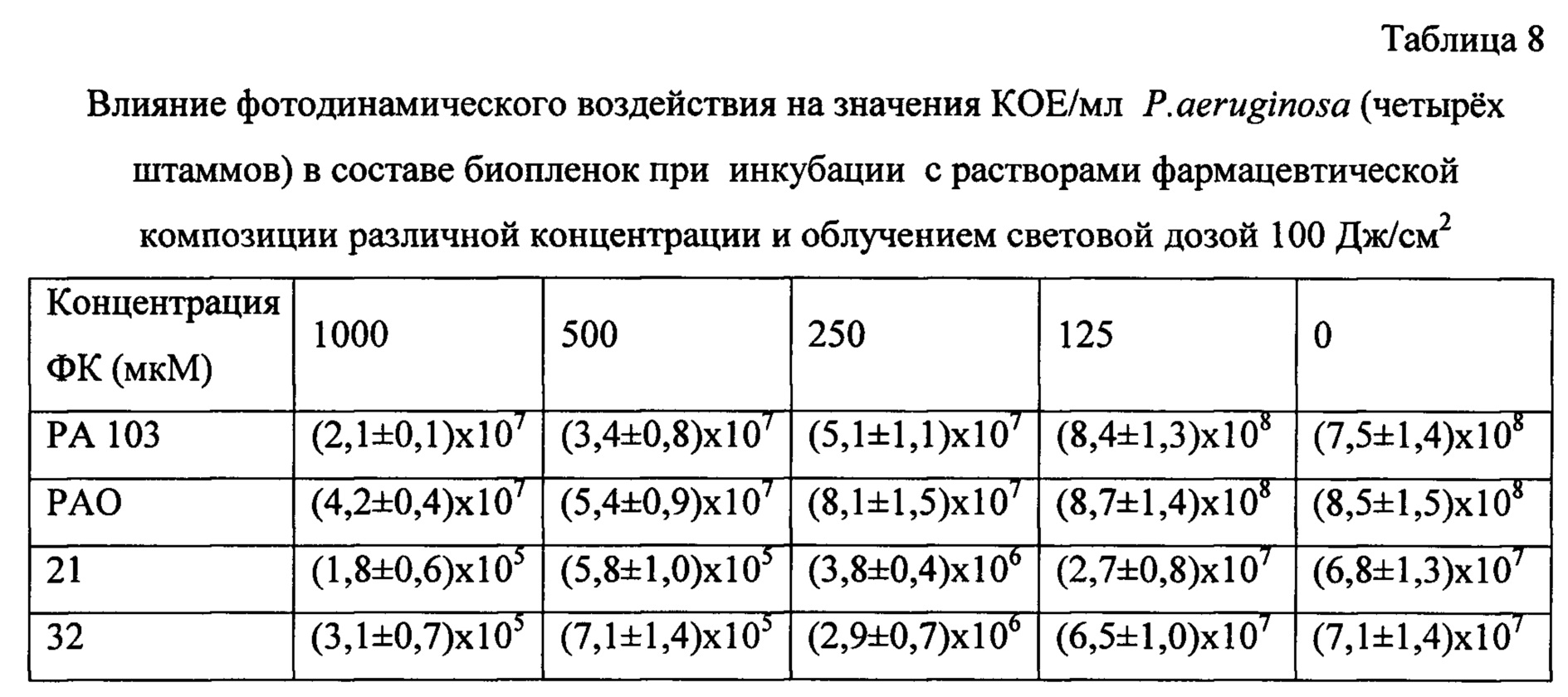
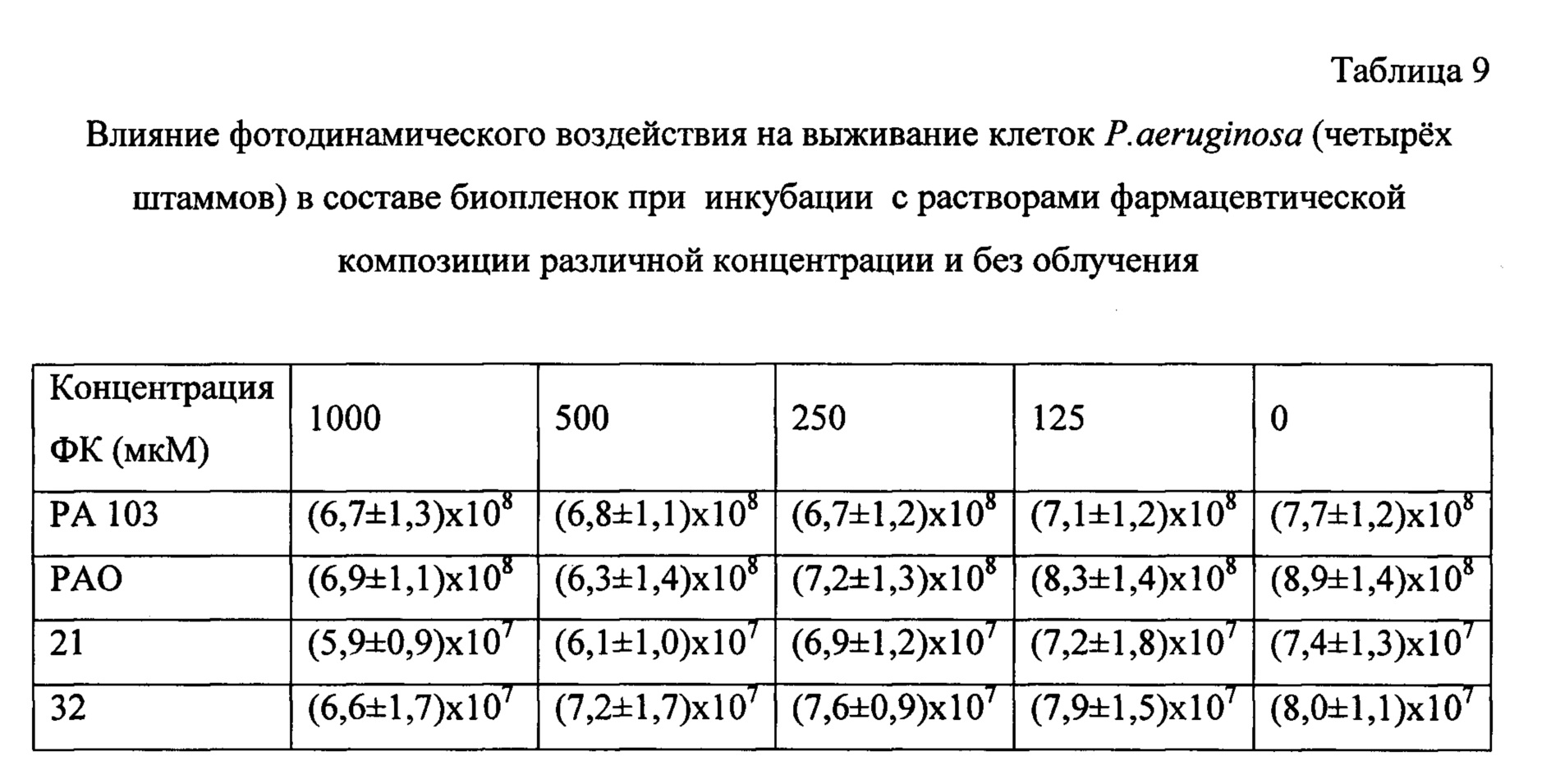
Опыты по фотоинактивации бактерий в биопленках были проведены на 4 штаммах грамположительных S. aureus и 4 грамотрицательных P. aeruginosa. Результаты приведены в таблицах 6 и 7 для S. aureus (с облучением и без) и в таблицах 8 и 9 для P. aeruginosa (с облучением и без него).
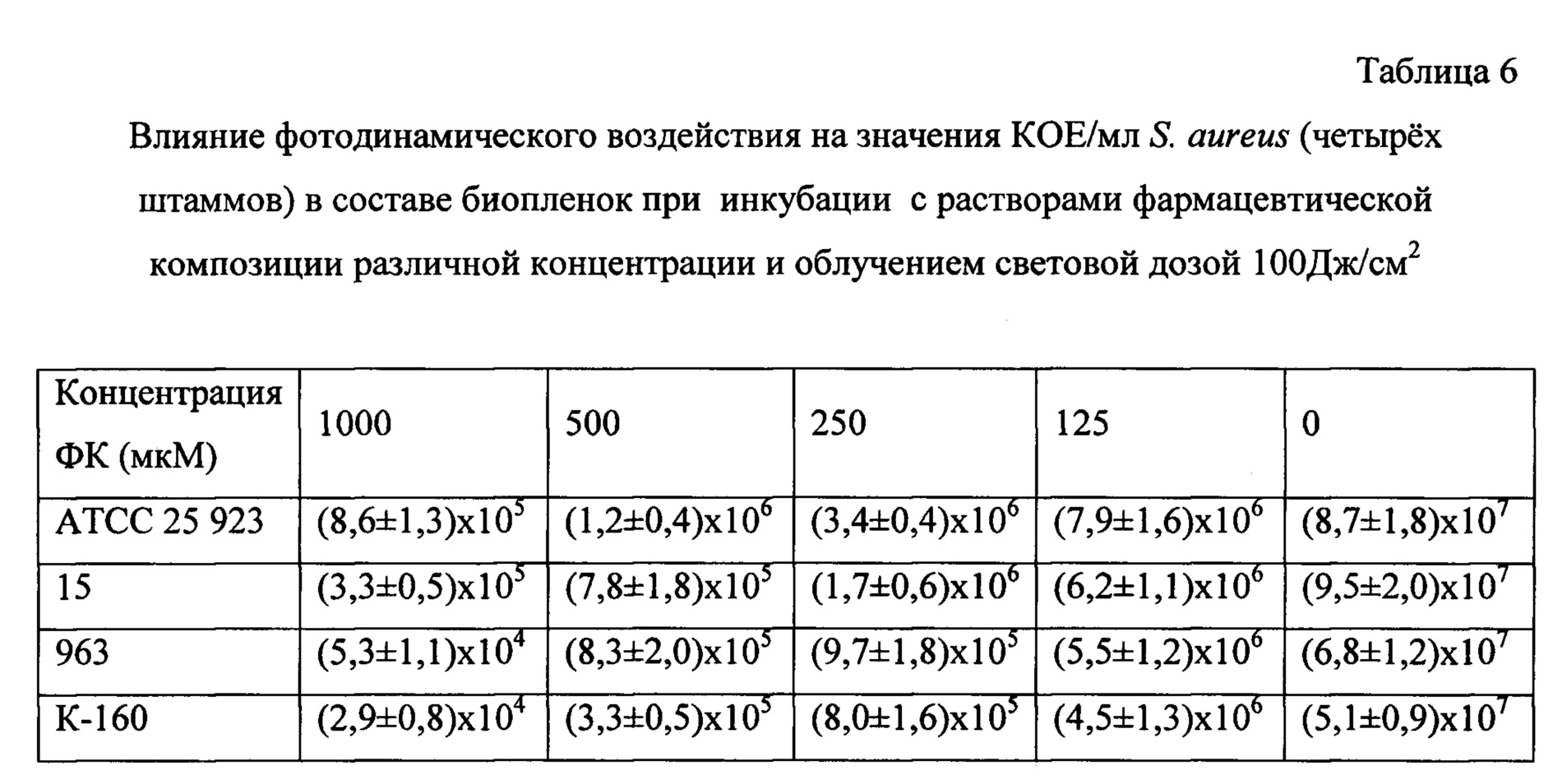
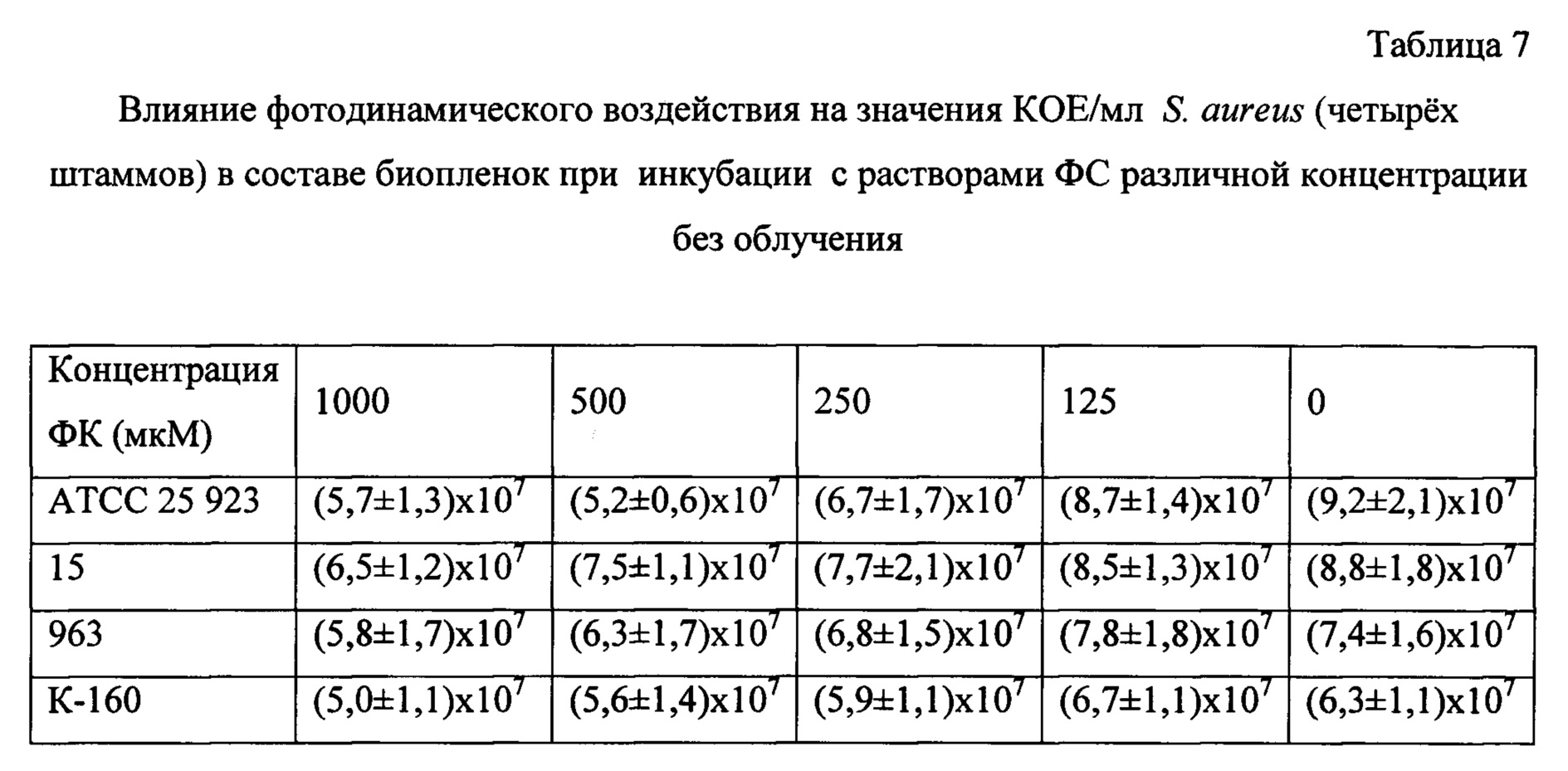
Из таблиц 6 и 7 следует, что штаммы S. aureus в составе биопленок чувствительны к фотодинамическому воздействию и при фотосенсибилизации раствором фармацевтической композиции в концентрации 1000 мкМ облучение приводит к снижению титра бактерий (КОЕ/мл) более, чем на 99%, по сравнению с контролем без ГЛФ. Инкубация бактериальных биопленок с растворами ГЛФ в темноте не вызывает снижения титра КОЕ/мл. Штаммы 963 и К-160 более чувствительны к фотоинактивации при действии изучаемой фармацевтической композиции.
Как следует из данных таблиц 8 и 9, штаммы P. aeruginosa значительно различаются по чувствительности к фотоинактивации при действии изучаемой фармацевтической композиции: стандартные штаммы РАО и РА 103 в составе биопленок не чувствительны к испытанным концентрациям ГЛФ и дозам света, при фотодинамическом воздействии их значения КОЕ/мл снижаются менее чем на 99%. Эти штаммы являются мукоидными и отличаются повышенной продукцией слизи, что, по-видимому, и является причиной их устойчивости. Однако, клинические изоляты, множественно резистентные к антибиотикам и немукоидные, в составе биопленок чувствительны к фотоинактивации при концентрации ГЛФ 1000 мкМ и дозе света 100 Дж/см2.
На основании проведенных экспериментов сделан вывод: фотодинамическое воздействие с исследуемой фармацевтической композицией обладает бактерицидным действием на все испытанные штаммы грамположительных бактерий S. aureus в виде биопленок; стандартные мукоидные штаммы грамотрицательных бактерий P. aeruginosa в виде биопленок устойчивы к испытанным концентрациям фармацевтической композиции и дозам света, однако, клинические изоляты, множественно резистентные к антибиотикам и немукоидные, чувствительны в виде биопленок к фотоинактивации при концентрации ГЛФ 1000 мкМ и дозе света 100 Дж/см2 при этом значение КОЕ/мл снижается более, чем на 99%.
Из приведенных выше данных можно сделать вывод о высокой эффективности инактивации биопленок путем использования заявленной фармацевтической композиции.
Пример 4
Получение фармацевтической композиции для терапии локальных очагов инфекции.
В мерной колбе объемом 100 мл растворили 0, 94 г Твина-80 в 100 мл воды очищенной с получением водного раствора Твина - 80. Затем в полученный раствор одновременно добавили 25 г гидроксипропил-бета-циклодекстрина и 0,376 г метилового эфира 133-N-(N-метилникотинил)бактериопурпуринимида при равномерном перемешивании и нагревании до температуры 60°С до полного растворения компонентов. Затем полученный водный раствор подвергли стерилизующей фильтрации и высушиванию досуха методом лиофильной сушки с получением фармацевтической композиции следующего состава (% мас.):
|
Таким образом, полученная фармацевтическая композиция обладает высоким уровнем фотостабильности и эффективности для терапии локальных очагов бактериального поражения.

