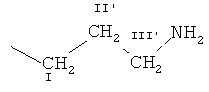Результат интеллектуальной деятельности: ОФТАЛЬМОЛОГИЧЕСКИЙ ПРЕПАРАТ В ВИДЕ ГЛАЗНЫХ КАПЕЛЬ, СОДЕРЖАЩИЙ РАЗВЕТВЛЕННЫЕ ПОЛИГЕКСАМЕТИЛЕНГУАНИДИНЫ
Вид РИД
Изобретение
Область техники, к которой относится изобретение
Изобретение относится к офтальмологическим препаратам, более конкретно - к глазным каплям, которые можно применять для лечения синдрома сухого глаза, а также бактериальных конъюнктивитов и/или блефаритов. Уровень техники
Синдром сухого глаза является распространенным патологическим состоянием, имеющим различную этиологию. Например, он может быть связан с возрастными изменениями, ношением контактных линз, заболеваниями тканей глаза и др. Основными проявлениями являются недостаточная толщина и прерывистость слезной пленки на роговице, раздражение слизистых оболочек и ощущение дискомфорта в глазу.
Кроме того, слезная пленка является местным иммунным барьером. Поэтому нарушение ее целостности или уменьшение толщины может стать причиной возникновения и развития инфекционных заболеваний глаза.
Препараты, предназначенные для восполнения слезной жидкости при синдроме сухого глаза, по ряду физико-химических свойств должны быть близки к естественной слезной жидкости здорового человека. Так, плотность должна составлять 1,001-1,009 г/мл, pH находиться в интервале 6,0-7,8, сила адгезии слезной пленки к роговице равна 30-40 дин/см2, а поверхностное натяжение должно быть равно 46 дин/см2.
В патенте EP 0198490 (опубл. 22.10.1986) раскрыты составы увлажняющих капель на основе гидроксиэтилцеллюлозы и полоксамера, содержащие мочевину в качестве консерванта.
В патенте EP 0780121 (опубл. 25.06.1997) раскрыты составы глазных капель, содержащих полиакриловую кислоту и поливинилпирролидон, и соли бензалкония в качестве консерванта.
В патенте EP 0342297 (опубл. 23.11.1989) раскрыт водный раствор, имеющий низкое поверхностное натяжение, образующий непрерывный смачиваемый водой абсорбированный слой на гидрофобной поверхности, включающий частично гидролизованный поливинилацетат в комбинации с поливиниловым спиртом. В состав такого раствора входят также декстран, коллидон, цитратно-фосфатный буферный раствор, ЭДТА, хлориды натрия, кальция и хлорбутанол в качестве консерванта.
Общим недостатком указанных решений является наличие у консерванта аллергизирующего эффекта и повреждающего действия на мягкие контактные линзы ввиду высокой реакционной способности их молекул (Материалы статьи Системы ухода за контактными линзами. / Н.Б.Демина, М.Н.Чиркова, А.В.Астахова, Л.А.Травина // Химико-фармацевтический журнал, 2001, т.35, №2).
Известно применение сульфацетамида в качестве активного компонента глазных капель, предназначенных для лечения заболеваний бактериальной этиологии (конъюнктивита, блефарита, хламидийных и гонококковых инфекций) у новорожденных, детей и взрослых. Применяемые препараты эффективны при содержании 10-30%, например «Сульфацил-натрия, 20% раствор», что часто обусловливает сильное раздражение слизистой оболочки глаза, приводящее к невозможности дальнейшего применения.
В качестве ближайшего аналога авторы рассматривают изобретение, раскрытое в патенте RU 2241444 (опубл. 10.12.2004), обеспечивающее капли для лечения синдрома сухого глаза, содержащие любрикант, консервант, фосфатный буфер, хлорид натрия, воду очищенную, отличающиеся тем, что содержат в качестве консерванта полигексаметиленгуанидина фосфат, коллидон VA 64 в качестве любриканта при следующем соотношении компонентов (в масс.%):
|
Недостатком аналога является слабое бактерицидное действие.
Поэтому существует потребность в новых гидратирующих, бактериостатических и/или бактерицидных средствах для лечения синдрома сухого глаза и борьбы с его последствиями, особенно - с развитием бактериальных инфекций. Раскрытие изобретения
Целью изобретения является расширение арсенала лекарственных средств путем создания эффективного комбинированного препарата для лечения синдрома сухого глаза и сопутствующей бактериальной инфекции.
Техническим результатом является препарат, обладающий бактерицидным действием, сопоставимым с действием 20% раствора сульфацетамида («Сульфацил-натрия»), при этом не оказывающий раздражающего действия при длительном применении.
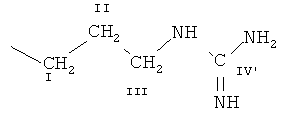
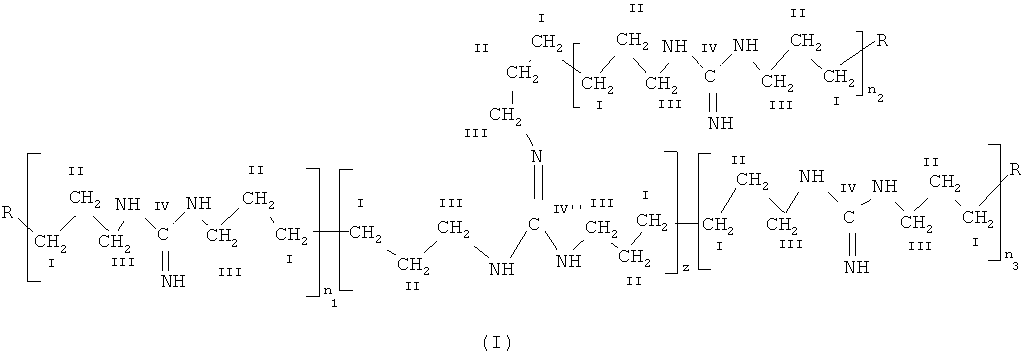
В результате исследований авторы изобретения установили, что недостатки известного уровня техники могут быть преодолены созданием офтальмологического препарата в виде капель, содержащего комбинацию активных компонентов, пролонгирующий компонент, вспомогательные вещества и воду, в котором комбинация активных компонентов состоит из разветвленного полигексаметиленгуанидина формулы (I)
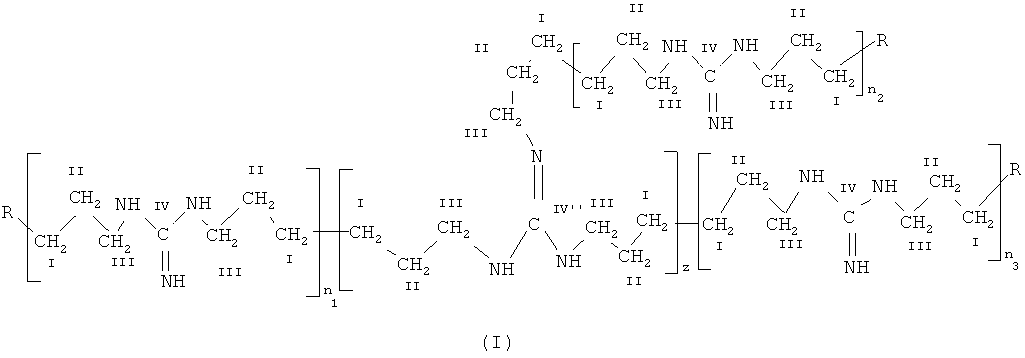
где R представляет 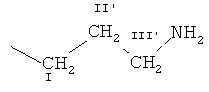 или
или 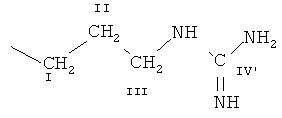 ,
,
n1, n2 и n3 равны 1-3, a z равно 0,15-1,10 с молекулярно-массовым распределением Mw/Mn от 5,4 до 9,3 при среднемассовой молекулярной массе Mw в интервале от приблизительно 3800 до 6300 и среднечисловой молекулярной массе Мn в интервале от приблизительно 600 до 1100, присутствующего в форме гидрохлорида, и сульфацетамида;
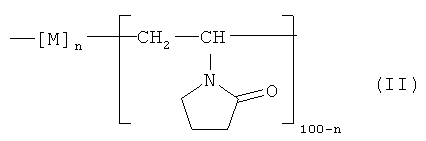
пролонгирующий компонент выбран из группы, состоящей из поливинилового спирта, водорастворимой метилцеллюлозы или гидроксипропилметилцеллюлозы, сополимера винилпирролидона/винилацетата и сополимера на основе N-винилпирролидона общей формулы (II)
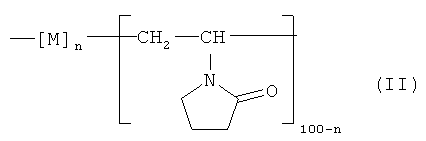 ,
,
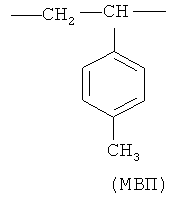
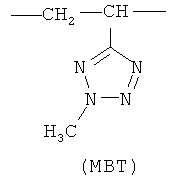
где мономерное звено М. представляет фрагмент 2-метил-5-винилтетразола (МВТ) или 2-метил-5-винилпиридина (МВП)
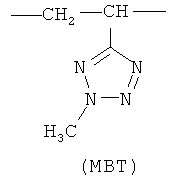
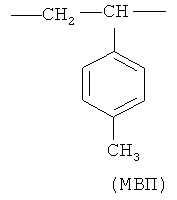 ,
,
и содержание мономерных звеньев n составляет 25-50 мольн.%, средневязкостная молекулярная масса Мµ сополимера зависит от природы М: если М представляет МВТ, то Мµ=30-50 кДа; если М представляет МВП, то Мµ=15-40 кДа
со следующим содержанием компонентов (в масс.%):
|
вспомогательные вещества выбраны из группы, состоящей из физиологически переносимых щелочных или кислотных агентов, присутствующих в количествах, требуемых для поддержания рН препарата в интервале от 6,0 до 7,8,, и солевого тонического агента, выбранного из физиологически переносимых солей натрия или калия и их смесей, присутствующего в количестве, обеспечивающем тоничность препарата, сопоставимую с тоничностью естественной слезной жидкости здорового человека.
Физиологически переносимые щелочные или кислотные агенты могут быть соответствующим образом выбраны из щелочей, таких как гидроксид натрия или гидроксид калия, кислот, таких как хлористоводородная кислота, фосфорная кислота, лимонная кислота, янтарная кислота и солей, подвергающихся гидролизу в водных растворах, таких как гидрофосфат натрия, дигидрофосфат натрия, цитрат натрия. Выбор подходящего щелочного или кислотного агента и определение его необходимого количества могут быть без затруднений выполнены специалистом в данной области, не выходя за рамки общих знаний, при необходимости - путем рутинного эксперимента.
Солевой тонический агент может быть выбран из хлорида натрия или хлорида калия, а его количество может быть теоретически оценено специалистом в данной области на основе общих знаний и экспериментально уточнено в рамках рутинного эксперимента, например определением осмоляльности полученного офтальмологического препарата.
Гидрохлорид полигексаметиленгуанидина (ПГМГ-ГХ) формулы (I) относится к 4 классу токсичности, т.е. не является опасным для человеческого организма, при этом он обладает выраженным микробиоцидным эффектом в отношении основных возбудителей инфекционных заболеваний глаз: Escherichia coli,, Staphylococcus, Streptococcus, Candida, Proteus.
Эффективность ПГМГ-ГХ относительно перечисленных штаммов, определенная методом серийных разведений с питательной средой и оцениваемая минимальной ингибирующей концентрацией, составляет от 1,0 до 300 мкг/мл, таким образом, минимальная бактериостатическая концентрация ПГМГ-ГХ составляет 0,01%. Для достижения бактерицидного эффекта может быть использована концентрация до 0,5%. Сульфацетамид также является малотоксичным соединением, о чем свидетельствует его применение в педиатрии, в частности - у младенцев грудного возраста.
Прозрачность является естественным требованием для оптических сред. Поэтому, выбор пролонгирующего компонента должен быть сделан с учетом требования прозрачности при соответствующей тоничности препарата. Моделью может служить изотоничный раствор хлорида натрия, содержащий максимальную концентрацию ПГМГ-ГХ. Полимеры, физико-химически совместимые с солевым раствором Г-ПГМГ и позволяющие получать составы, близкие по вязкости к слезной жидкости (1,2-1,4), пригодны к применению в соответствии с изобретением. Такими являются поливиниловый спирт, сополимер винилпирролидона/винилацетата в мольных соотношениях 6:4 (концентрация 3-3,5%) и водорастворимая метилцеллюлоза с молекулярной массой порядка 20 кДа (концентрация 0,05-0,1%), а также сополимера на основе N-винилпирролидона общей формулы (II), приведенной выше.
Другими важными требованиями к растворам, предназначенным для инстилляции в конъюнктивальную полость, являются стерильность, изотоничность, значение pH, близкое к естественному, и продолжительность действия.
Стерильность необходима для обеспечения длительного хранения препарата перед реализацией, а также гарантирует отсутствие патогенных микроорганизмов в препарате после вскрытия его упаковки во время применения. Изотоничность и близкий к естественному показатель рН создают комфортную среду для клеток конъюнктивы, что исключает их повреждение и неприятные ощущения (чувства рези или жжения в глазу). Продолжительность действия позволяет уменьшить число инстилляции, что снижает лекарственную нагрузку и делает возможным долговременное применение препарата без выраженных побочных эффектов.
Специалисту в данной области очевидны теоретические и экспериментальные способы оценки концентраций компонентов в препаратах подобного типа. Наиболее известными являются теоретический расчет с учетом изотонических эквивалентов и криометрия при переохлаждении смесью соль/лед.
Дополнительным преимуществом препарата в соответствии с изобретением является его пригодность к применению в течение 3 лет, что подтверждено сравнением физико-химических и микробиологических показателей свежефасованного препарата и препарата после хранения. Показатель pH, поверхностное натяжение, удельное электрическое сопротивление и показатель преломления для препаратов после хранения статистически достоверно (p<0,05) не отличались от исходных значений.
Время удерживания препарата на роговице можно косвенно оценить по степени выраженности бактериостатического или бактерицидного действия. Оценкой времени удерживания является время, после которого наблюдается рост колонии микроорганизма при бактериостатической концентрации препарата (0,01-0,05%) или время, до которого отсутствует рост колонии микроорганизма при бактерицидной концентрации (0,1-0,5%) в посеве пробы слезной жидкости на соответствующую питательную среду. Проведенные исследования показали, что наибольшее время удерживания препарата (8-9 часов) достигается с применением метилцеллюлозы или гидроксипропилметилцеллюлозы в качестве пролонгирующего агента. Препарат, содержащий поливиниловый спирт или сополимер винилпирролидона/винилацетата, удерживаются в течение 6-7 часов.
Достижение технического результата изобретения будет доказано результатами, полученными в предпочтительных примерах его осуществления.
Осуществление изобретения
Приготовление препаратов в соответствии с изобретением и оценки их фармакологических характеристик проиллюстрированы следующими примерами.
Пример 1. Капли для лечения синдрома сухого глаза с бактериостатическим действием
В асептических условиях в стеклянный аппарат с мешалкой, термометром и обогреваемой рубашкой помещают 45 мл горячей апирогенной воды и последовательно растворяют в ней 0,05 г гидрохлорида полигексаметиленгуанидина формулы (I), 2,00 г сульфацетамида, 0,10 г дигидрофосфата натрия, 0,25 г гидрофосфата натрия и 0,50 г хлорида натрия.
Во втором аналогичном аппарате в 50 мл воды растворяют 3,0 г пролонгирующего агента (метилцеллюлоза). Растворы смешивают в предварительно взвешенной асептической емкости, в которую добавляют воду до 100,00 г.
Стерилизацию раствора проводят при 120°C в течение 8-12 минут. После стерилизации готовый препарат порциями по 2 мл фасуют в стерильные капельницы из полиэтилена высокого давления, снабжают навинчиваемыми крышками и помещают в коробки с указанием информации, необходимой для идентификации и применения.
Пример 2. Капли для лечения синдрома сухого глаза с бактерицидным действием
Приготовление капель осуществляют аналогично примеру 1, применяя для этого 0,20 г гидрохлорида
полигексаметиленгуанидина формулы (I), 5,00 г сульфацетамида, 0,15 г дигидрофосфата натрия, 0,85 г гидрофосфата натрия, 0,3 г хлорида натрия и 2,0 г гидроксипропилметилцеллюлозы в качестве пролонгирующего агента.
Пример 3. Капли для лечения синдрома сухого глаза с выраженным бактерицидным действием
В асептических условиях в стеклянный аппарат с мешалкой, термометром и обогреваемой рубашкой помещают 45 мл апирогенной воды и последовательно растворяют в ней 0,50 г гидрохлорида полигексаметиленгуанидина формулы (I), 5,00 г сульфацетамида и 0,70 г хлорида натрия, перемешивают до полного растворения и добавляют хлористоводородную кислоту до pH 6,5 (приблизительно 0,4 г в пересчете на хлористый водород).
Во втором аналогичном аппарате в 50 мл апирогенной 0,60 г пролонгирующего агента (поливиниловый спирт). Растворы смешивают в предварительно взвешенной асептической емкости для работы под давлением или при разрежении, после чего добавляют воду до массы раствора 100,00 г.
После получения прозрачного раствора проводят стерилизацию полученного раствора фильтрованием через мембранный фильтр с отсекающей способностью 0,2 мкм, принимая его во вторую асептическую емкость, в которой создают и поддерживают необходимое разрежение.
После стерилизации готовый препарат порциями по 2 мл фасуют в стерильные капельницы из полиэтилена высокого давления, снабжают навинчиваемыми крышками и помещают в коробки с указанием информации, необходимой для идентификации и применения.
Пример 4. Определение спектра бактерицидной эффективности препаратов in vitro и минимальной бактериостатической (подавляющей рост) концентрации (МПК)
Спектр бактерицидной эффективности препаратов в опыте in vitro характеризуют суспензионным методом в соответствии с руководством Р 4.2.2643-10 «Методы лабораторных исследований и испытаний дезинфекционных средств для оценки их эффективности и безопасности». Исследуют 0,05% раствор гидрохлорида полигексаметиленгуанидина формулы (I) (Г-ПГМГ), 20% раствор сульфацетамида («Сульфацил-натрия», ОАО «Синтез», г.Курган) и препарат, приготовленный в соответствии с примером 2 изобретения.
Минимальную бактериостатическую (МПК) и минимальную бактерицидную (МБК) концентрации определяют микрометодом серийных двукратных разведений в среде Мюллера-Хинтона (Oxoid) в соответствии с нормативным документом «Методические указания по определению чувствительности микроорганизмов к антибактериальным препаратам» (МУК 4.2 1890-04).
Препараты с концентрацией активного компонента 1000 мкг/мл, приготовленные на апирогенной дистиллированной воде, разводят 128 мкг/мл питательной среды. Исследования выполняют в 96-луночных планшетах для иммунологических исследований. Готовят серии двукратных разведений исследуемого препарата в среде II Мюллера-Хинтона (Oxoid) в объеме 50 мкл. Для микроорганизмов, плохо растущих на обычных питательных средах, в указанную выше среду добавляют 5% дефибринированной бараньей крови.
Инокулят бактериальных культур из изолированных колоний готовят в виде суспензии по стандарту мутности МакФарланда (0,5) в физиологическом растворе. Суспензию разводят в среде II Мюллера-Хинтона до концентрации 108 КОЕ/мл. Приготовленную суспензию вносят в лунки планшетов (50 мкл/лунка) и готовят разведения в диапазоне концентраций от 128 до 0,0003 мкг/мл. Инокулированные планшеты инкубируют в течение 18 часов при 37°C. Наименьшая концентрация исследуемого препарата, при которой отсутствует видимый рост микроорганизмов, является оценкой МПК.
Для определения МПК Candida albicans из изолированной колонии готовят суспензию в питательной среде Сабуро по стандарту мутности МакФарланда (0,5), что соответствует 106 КОЕ/мл для грибных культур. Серию двукратных разведений препаратов готовят в среде Сабуро в объеме 100 мл. После посева дрожжевых культур планшеты инкубируют 48 часов при 30°C. Серию двукратных разведений препаратов готовят в среде Сабуро в объеме 100 мл. Результаты представлены в таблице 1.
|
Пример 5. Определение минимальной бактерицидной (МБК) концентрации
Исследуют 0,2% раствор гидрохлорида полигексаметиленгуанидина формулы (I) (Г-ПГМГ), 20% раствор сульфацетамида («Сульфацил-натрия», ОАО «Синтез», г.Курган) и препарат, приготовленный в соответствии с примером 1 изобретения.
Определение бактерицидной эффективности в отношении микроорганизмов проводят в суспензии, содержащей 109 КОЕ/мл. В культуру микроорганизмов (Escherichia coli, Candida albicans, Pseudomonas aeruginosa, Streptococcus oralis) в количестве 0,5 мл вносят 4,5 мл препаратов, перемешивают и выдерживают в течение требуемого времени индукции (tHIW,). Из смеси отбирают 0,5 мл и переносят в нейтрализующий раствор, содержащий 1% лаурилсульфата с 10% обезжиренным молоком, после чего перемешивают и оставляют на 5 минут.
По истечении указанного времени 0,5 мл нейтрализованной культуры переносят в 4,5 мл стерильной воды. После перемешивания по 0,1 мл суспензию переносили в 5 мл жидкой питательной среды и на поверхность агаризованной среды (агаризованная жидкая среда Сабуро для Candida albicans и среда БТН для остальных штаммов). Подсчет колоний осуществляют через 24 часа инкубации для Candida albicans и через 48 часа инкубации для остальных. Результаты приведены в таблице 2.
|
Полученные данные показывают, что препарат в соответствии с изобретением эффективен в отношении большинства исследованных штаммов в той же степени, что и «Сульфацил-натрия», что подтверждает достижение технического результата изобретения.
Пример 6. Лечение синдрома сухого глаза у собак Эффективность лечения синдрома сухого глаза у собак оценивают по стабильности слезной пленки (пробы по Норну (M.S. Norn, 1969) и продуцированию слезной жидкости. В соответствии с протоколом исследования в нижний конъюнктивальный мешок инстиллируют 1 каплю 0,2% флюоресцеина-натрия, после чего определяют время от последнего моргания до появления в подкрашенной слезной пленке разрыва в виде черного пятна или щели на поверхности роговицы. Время разрушения слезной пленки является важным показателем ее стабильности. Результаты оценивают следующим образом:
более 10 секунд норма;
5-10 секунд меньше нормы;
менее 5 секунд резкое снижение стабильности слезной пленки.
Результаты представлены в таблице 3.
|
Таким образом, через 2 недели после лечения был устранен гнойный конъюнктивит, у животных исчезли болезненный спазм век и светобоязнь. Выделение слезы практически нормализовано.