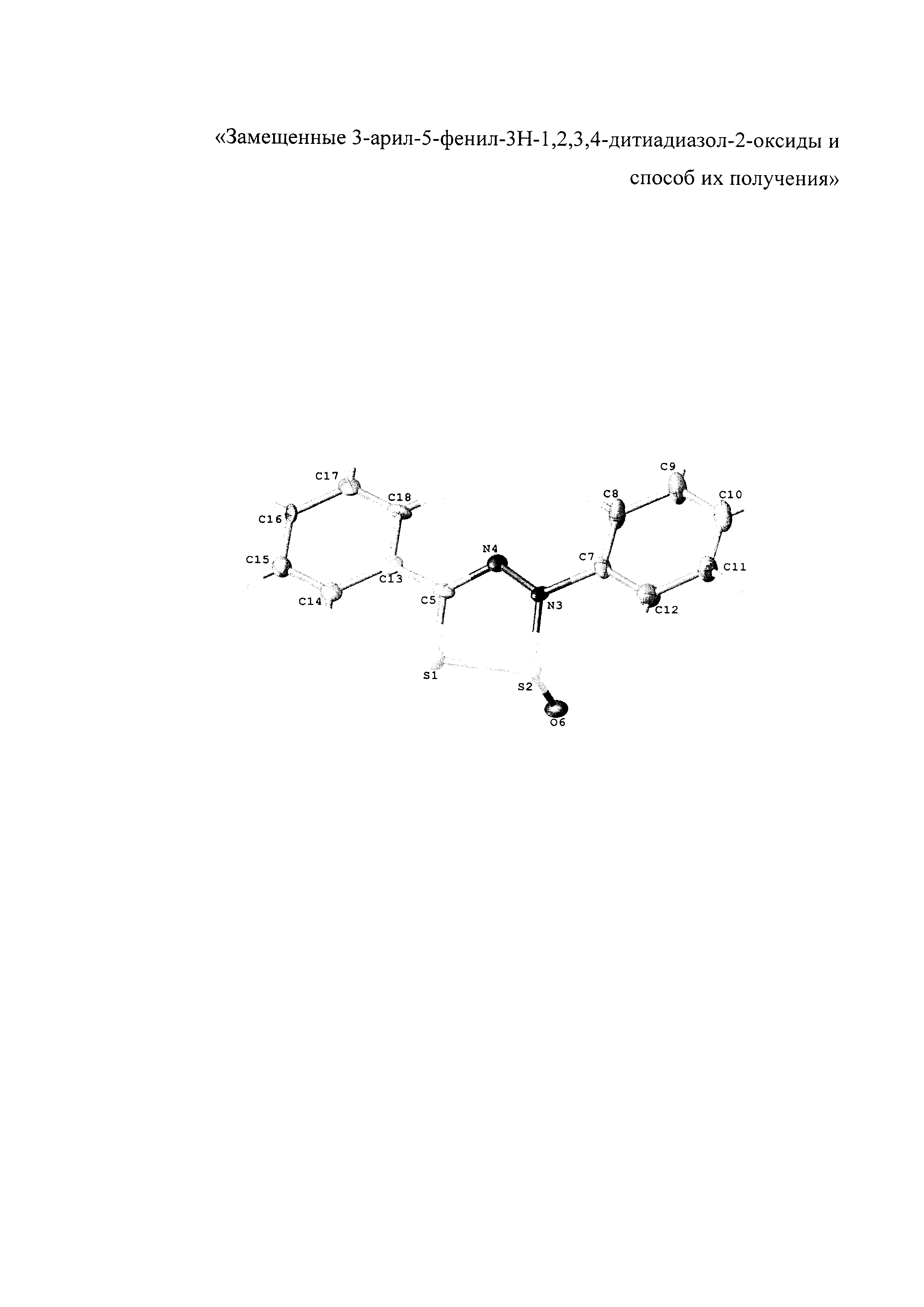Результат интеллектуальной деятельности: Замещенные 3-арил-5-фенил-3Н-1,2,3,4-дитиадиазол-2-оксиды и способ их получения
Вид РИД
Изобретение
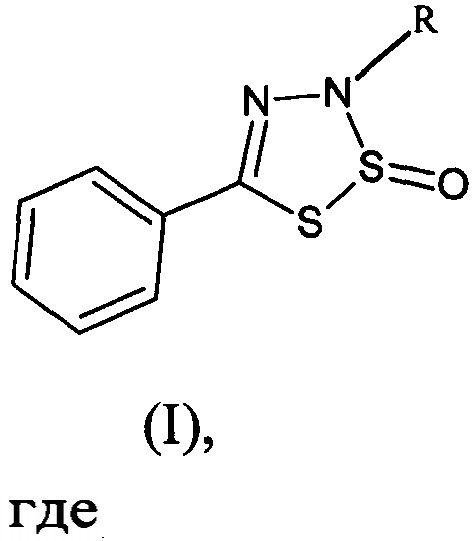
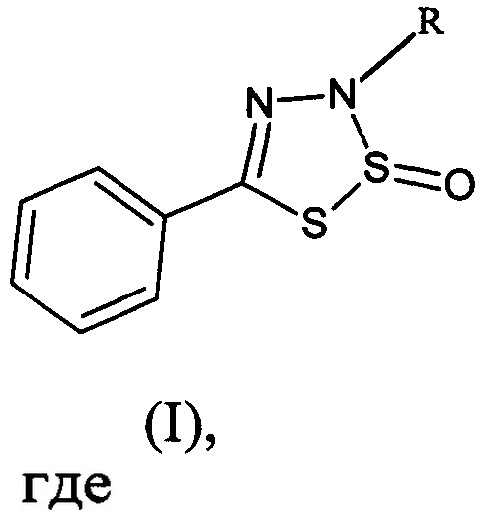
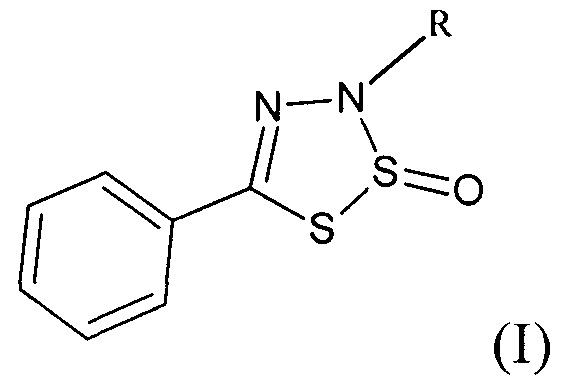
Группа изобретений относится к области органической и медицинской химии, а именно к новым индивидуальным соединениям класса гетероциклических систем - замещенным 3-арил-5-фенил-3Н-1,2,3,4-дитиадиазол-2-оксидам общей формулы I, и способу их получения, которые могут быть использованы для синтеза новых гетероциклических соединений и в медицине в качестве потенциального антимикробного средства

где
R=Ph (Ia - 3,5-дифенил-3Н-1,2,3,4-дитиадиазол-2-оксид);
R=2-СН3С6Н4 (Iб - 3-(2-метилфенил)-5-фенил-3Н-1,2,3,4-дитиадиазол-2-оксид);
R=Bn (Iв - 3-бензил-5-фенил-3Н-1,2,3,4-дитиадиазол-2-оксид);
R=4-FC6H4 (Iг - 3-(4-фторфенил)-5-фенил-3Н-1,2,3,4-дитиадиазол-2-оксид);
R=4-NO2C6H4 (Iд - 3-(4-нитрофенил)-5-фенил-3Н-1,2,3,4-дитиадиазол-2-оксид);
R=3,5-ди FC6H4 (Ie - 3-(3,5-дифторфенил)-5-фенил-3Н-1,2,3,4-дитиадиазол-2-оксид).
Описаны 5-фенилгидразино-1,2,3,4-дитиадиазол-2-оксида III, которые были получены взаимодействием тионилхлорида (II) и N-фенилтиокарбазида (III).
Реакция, описанная Guha и Roy-Choudhury, является основной для получения 5-фенилгидразино-1,2,3,4-дитиадиазол-2-оксида (IV) [Guha and Roy-Choudhury // J. Indian Chem. Soc., 5, 163 (1928); Chem. Abstr., 23, 1398 (1929)]

В литературе описан 3-фенил-5-фенилазо-1,2,3,4-дитиадиазол-2-оксид (VI), который получали взаимодействием тионилхлорида (II) и соединения (V) [Freund and Wischewiansky // Ber., 26, 2494 (1893)]

Задачей группы изобретений является создание новых неописанных в литературе соединений - замещенных 3-арил-5-фенил-3Н-1,2,3,4-дитиадиазол-2-оксидов (I), что позволит расширить ассортимент потенциальных антимикробных средств.
Техническим результатом, на решение которого направлена группа изобретений, является получение нового класса соединений - замещенных 3-арил-5-фенил-3Н-1,2,3,4-дитиадиазол-2-оксидов общей формулы I, которые могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем и в медицине, например, в качестве антимикробных средств; разработка простого способа их получения.
Поставленная задача осуществляется путем взаимодействия замещенного N'-арилтиобензгидразида (VII) с тионилхлоридом (II) по схеме:

где
R=Ph (Ia - 3,5-дифенил-3Н-1,2,3,4-дитиадиазол-2-оксид);
R=2-СН3С6Н4 (Iб - 3-(2-метилфенил)-5-фенил-3Н-1,2,3,4-дитиадиазол-2-оксид);
R=Bn (Iв - 3-бензил-5-фенил-3Н-1,2,3,4-дитиадиазол-2-оксид);
R=4-FC6H4 (Iг - 3-(4-фторфенил)-5-фенил-3Н-1,2,3,4-дитиадиазол-2-оксид);
R=4-NO2C6H4 (Iд - 3-(4-нитрофенил)-5-фенил-3Н-1,2,3,4-дитиадиазол-2-оксид);
R=3,5-ди FC6H4 (Iе - 3-(3,5-дифторфенил)-5-фенил-3Н-1,2,3,4-дитиадиазол-2-оксид).
Способ получения замещенных 3-арил-5-фенил-3Н-1,2,3,4-дитиадиазол-2-оксидов изучен и проведен в лабораторных условиях на стандартном товарном сырье.
Данные элементного анализа приведены в табл. 1, выходы продуктов реакций, температуры плавления и величины Rf приведены в табл. 2, спектральные характеристики полученных соединений сведены в табл. 3 и 4, антимикробная активность в табл. 5.
Величины длин связей, валентных и торсионных углов молекулы Iа приведены в таблицах 6, 7, 8 и 9.
Группа изобретений проиллюстрирована снимком (чертежом) и примерами практического осуществления.
На чертеже представлен общий вид молекулы 3,5-дифенил-3Н-1,2,3,4-дитиадиазол-2-оксид (Iа).
Пример 1. 3,5-дифенил-3Н-1,2,3,4-дитиадиазол-2-оксид (Iа)
В грушевидную круглодонную колбу емкостью 50 мл, снабженную магнитной мешалкой, обратным холодильником, загружают 5 мл (69 мМоль) тионилхлорида, постепенно прибавляют 3 г (13 мМоль) N'-фенил-бензтиогидразида, перекристаллизованного из четыреххлористого углерода. Происходит бурное выделение газа, раствор окрашивается в темно-зеленокоричневый цвет. Избыток тионилхлорида отгоняют в вакууме при 45°С. Остаток, светло-желтое вещество, перекристаллизовывают из циклогексана. Выход 2,58 г (86%), Т.пл. 97-98°С, желтоватые игольчатые пушистые кристаллы устойчивые на воздухе.
Продукт хроматографически однороден - Rf=0.49 (дихлорметан-тетрахлорметан 1:1).
Состав синтезированного соединения подтвержден элементным анализом. Брутто-Формула: C13H10N2OS2. Найдено %: С - 56.96, Н - 3.70, N - 10.17. Вычислено %: С - 56.91, Н - 3.67, N - 10.21.
Строение синтезированного вещества было доказано физико-химическими методами идентификации органических соединений: ЯМР 1Н и 13С-спектроскопией.
В спектре ЯМР 1Н полученного соединения в ДМСО-d6 присутствуют сигналы протонов бензольных колец (δ 7.31 (t, J 7.4 Гц, 1H); 7.50-7.57 (m, 5Н); 7,67 (d, J 7,8 Гц, 2Н); 7.88 (m, 2Н)). В спектре отсутствуют сигналы NH групп исходного тиогидразина.
Спектр ЯМР 13С этого соединения характеризуется сигналами ядер углерода бензольных колец (δ 126.54-131.44 м.д.), присутствует слабопольный сигнал атома углерода гетероцикла (144,93 м.д.).
Масс-спектрометрия высокого разрешения (HRMS) выполнена с ионизацией электроспреем (ESI). Вычислено для C13H10N2NaOS2 [M+Na]+ 297,3513, найдено 297,3516.
Структура соединения Iа однозначно установлена на основании данных рентгеноструктурного анализа. Монокристалл соединения Iа был изучен на дифрактометре Xcalibur, Eos. Обработка данных была проведена с помощью программы ShelXS прямым методом и уточнена ShelXL с использованием метода наименьших квадратов.
Пример 2. 3-(2-метилфенил)-5-фенил-3Н-1,2,3,4-дитиадиазол-2-оксид (Iб)
В грушевидную круглодонную колбу емкостью 50 мл, снабженную магнитной мешалкой, обратным холодильником, загружали 5 мл тионилхлорида, постепенно прибавляли 3 г N'-2-метилфенил-бензтиогидразида, перекристаллизованного из четыреххлористого углерода. Происходит бурное выделение газа, раствор окрашивается в темно-зеленокоричневый цвет. Избыток тионилхлорида отгоняли в вакууме при 45°С. Остаток, светло-желтое вещество, перекристаллизовывали из циклогексана. Выход 2,67 г (89%), Т.пл. 88-89°С, желтоватые игольчатые пушистые кристаллы устойчивые на воздухе.
Пример 3. 3-бензил-5-фенил-3Н-1,2,3,4-дитиадиазол-2-оксид (Iв)
В грушевидную круглодонную колбу емкостью 50 мл, снабженную магнитной мешалкой, обратным холодильником, загружали 5 мл тионилхлорида, постепенно прибавляли 3 г N'-бензилбензтиогидразида, перекристаллизованного из четыреххлористого углерода. Происходит бурное выделение газа, раствор окрашивается в темно-зеленокоричневый цвет. Избыток тионилхлорида отгоняли в вакууме при 45°С. Остаток, светло-желтое вещество, перекристаллизовывали из циклогексана. Выход 2,31 г (77%), Т.пл. 87-88°С, желтоватые игольчатые пушистые кристаллы устойчивые на воздухе.
Пример 4. 3-(4-фторфенил)-5-фенил-3Н-1,2,3,4-дитиадиазол-2-оксид (Iг)
В грушевидную круглодонную колбу емкостью 50 мл, снабженную магнитной мешалкой, обратным холодильником, загружали 5 мл тионилхлорида, постепенно прибавляли 3 г N'-4-фторфенилбензтиогидразида, перекристаллизованного из четыреххлористого углерода. Происходит бурное выделение газа, раствор окрашивается в темно-зеленокоричневый цвет. Избыток тионилхлорида отгоняли в вакууме при 45°С. Остаток, светло-желтое вещество, перекристаллизовывали из циклогексана. Выход 2,49 г (83%), Т.пл. 124-125°С, желтоватые игольчатые пушистые кристаллы устойчивые на воздухе.
Пример 5. 3-(4-нитрофенил)-5-фенил-3Н-1,2,3,4-дитиадиазол-2-оксид (Iд)
В грушевидную круглодонную колбу емкостью 50 мл, снабженную магнитной мешалкой, обратным холодильником, загружали 5 мл тионилхлорида, постепенно прибавляли 3 г N'-4-нитрофенилбензтиогидразида, перекристаллизованного из четыреххлористого углерода. Происходит бурное выделение газа, раствор окрашивается в темно-зеленокоричневый цвет. Избыток тионилхлорида отгоняли в вакууме при 45°С. Остаток, светло-желтое вещество, перекристаллизовывали из циклогексана. Выход 2,25 г (75%), Т.пл. 163-164°С, желтоватые игольчатые пушистые кристаллы устойчивые на воздухе.
Пример 6. 3-(3,5-дифторфенил)-5-фенил-3Н-1,2,3,4-дитиадиазол-2-оксид (Iе)
В грушевидную круглодонную колбу емкостью 50 мл, снабженную магнитной мешалкой, обратным холодильником, загружали 5 мл тионилхлорида, постепенно прибавляли 3 г N'-3,5-дифторфенилбензтиогидразида, перекристаллизованного из четыреххлористого углерода. Происходит бурное выделение газа, раствор окрашивается в темно-зеленокоричневый цвет. Избыток тионилхлорида отгоняли в вакууме при 45°С. Остаток, светло-желтое вещество, перекристаллизовывали из циклогексана. Выход 2,52 г (84%), Т.пл. 147-148°С, желтоватые игольчатые пушистые кристаллы устойчивые на воздухе.
Пример 8. На примере соединения Iа проверена антимикробная активность.
Определение минимально ингибирующих концентраций (МИК) проводили методом серийных разведений в мясопептонном бульоне в отношении тест-культур микроорганизмов Staphylococcus aureus (штамм 209-Р), Escherichia coli (штамм 1257), Candida albicans (штамм АТСС 885-635), рекомендованных Государственной Фармакопеей [Государственная Фармакопея Российской Федерации XIII издание, Том 2. Метод предельных разведений с последующим высевом на жидкие или полужидкие питательные среды. - Москва, 2015. - С. 650-651]. Исследуемые соединения ограниченно растворяются в воде, поэтому в качестве растворителя использовали 20% раствор ДМСО, не подавляющий роста ни одной из использованных тест-культур в условиях эксперимента. Минимальная ингибирующая концентрация соединения Iа на Е. coli и C. albicans составляет 125 и 62,5 мкг/мл соответственно, а на St. aureus составляет 4 мкг/мл, что находится на уровне широко используемых на практике антибиотиков (эдицин - 10-20 мкг/мл, ванкомицин и тейкопланин - 0,3-12,5 мкг/мл).
Получены новые соединения - замещенные 3-арил-5-фенил-3Н-1,2,3,4-дитиадиазол-2-оксиды общей формулы I, которые могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем и в медицине, например в качестве антимикробных средств. Разработан простой одностадийный способ их синтеза с высоким выходом. Способ занимает мало времени, не требует дорогого оборудования, основан на использовании доступного дешевого сырья.