Результат интеллектуальной деятельности: ПЕСТИЦИДНЫЕ КОМПОЗИЦИИ И СВЯЗАННЫЕ С НИМИ СПОСОБЫ
Вид РИД
Изобретение
ЗАЯВЛЕНИЕ О ПРИОРИТЕТЕ
По настоящей заявке испрашивается преимущество с даты подачи предварительной заявки США № 61/894364, поданной 22 октября 2013 г., под названием "PESTICIDAL COMPOSITIONS AND RELATED METHODS".
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к области соединений, в качестве пестицидов против вредителей отрядов нематоды, членистоногие и/или моллюски, к способам получения таких соединений и к промежуточным продуктам, применяющимся в таких способах. Эти соединения можно использовать, например, в качестве как нематоцидов, акарицидов, пестицидов, инсектицидов, майтицидов и/или моллюскоцидов.
УРОВЕНЬ ТЕХНИКИ
Борьба с популяциями вредителей важна для обеспечения здоровья человека, современного сельского хозяйства, хранения пищевых продуктов и гигиены. Имеется более десяти тысяч видов вредителей, которые приводят к потерям в сельском хозяйстве, и ежегодные потери в сельском хозяйстве во всем мире составляют триллионы долларов США. Соответственно существует постоянная потребность в новых пестицидах и способах получения и применения таких пестицидов.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Определения
Примеры, приведенные в определениях, не являются исчерпывающими и их не следует рассматривать в качестве ограничивающих настоящее изобретение. Следует понимать, что заместитель должен соответствовать правилам образования химических связей и ограничениям по стерической совместимости для конкретной молекулы, к которой он присоединен.
"Алкил" означает и включает ациклический насыщенный, разветвленный или неразветвленный углеводород. Неограничивающие примеры могут включать метил, этил, пропил, изопропил, 1-бутил, 2-бутил, изобутил, трет-бутил, пентил, 2-метилбутил, 1,1-диметилпропил, гексил, гептил, октил, нонил или децил.
"Циклоалкил" означает и включает моноциклический или полициклический насыщенный углеводород. Неограничивающие примеры могут включать циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил, циклодецил, норборнил, бицикло[2.2.2]октил или декагидронафтил.
"Алкенил" означает и включает ациклический разветвленный или неразветвленный углеводород, содержащий по меньшей мере одну двойную связь углерод-углерод. Неограничивающие примеры могут включать этенил, пропенил, бутенил, пентенил, гексенил, гептенил, октенил, ноненил или деценил.
"Циклоалкенил" означает и включает моноциклический или полициклический углеводород, содержащий по меньшей мере одну двойную связь углерод-углерод. Неограничивающие примеры могут включать циклопентенил, циклогексенил, циклогептенил, циклооктенил или циклодеценил.
"Алкинил" означает и включает циклический разветвленный или неразветвленный углеводород, содержащий по меньшей мере одну тройную связь углерод-углерод. Неограничивающие примеры могут включать этинил, пропаргил, бутинил, пентинил, гексинил, гептинил, октинил, нонинил или децинил.
"Циклоалкинил" означает и включает моноциклический или полициклический углеводород, содержащий по меньшей мере одну тройную связь углерод-углерод. Неограничивающие примеры могут включать циклогептинил, циклооктинил или циклодецинил.
"Арил" означает и включает ароматическое соединение, содержащее или не содержащее заместители. Неограничивающие примеры могут включать фенил или нафтил.
"Алкоксигруппа" означает и включает алкильную группу, содержащую по меньшей мере одну ординарную связь углерод-кислород. Неограничивающие примеры могут включать метоксигруппу, этоксигруппу, пропоксигруппу, бутоксигруппу, циклопропоксигруппу, циклобутоксигруппу или циклопентоксигруппу.
"Алкенилоксигруппа" означает и включает алкенил, содержащий по меньшей мере одну ординарную связь углерод-кислород. Неограничивающие примеры могут включать аллилоксигруппу, бутенилоксигруппу, пентенилоксигруппу, гексенилоксигруппу, гептенилоксигруппу, октенилоксигруппу, ноненилоксигруппу или деценилоксигруппу.
"Алкинилоксигруппа" означает и включает алкинил, содержащий по меньшей мере одну ординарную связь углерод-кислород. Неограничивающие примеры могут включать пентинилоксигруппу, гексинилоксигруппу, гептинилоксигруппу, октинилоксигруппу, нонинилоксигруппу или децинилоксигруппу.
"Циклоалкоксигруппа" означает и включает циклоалкил, содержащий по меньшей мере одну ординарную связь углерод-кислород. Неограничивающие примеры могут включать циклопропилоксигруппу, циклобутилоксигруппу, циклопентилоксигруппу, циклогексилоксигруппу, циклогептилоксигруппу, циклооктилоксигруппу, циклодецилоксигруппу, норборнилоксигруппу или бицикло[2.2.2]октилоксигруппу.
"Циклогалогеналкил" означает и включает моноциклический или полициклический насыщенный заместитель, состоящий из атомов углерода, галогена и водорода. Неограничивающие примеры могут включать 1-хлорциклопропил, 1-хлорциклобутил или 1-дихлорциклопентил.
"Циклоалкенилоксигруппа" означает и включает циклоалкенил, дополнительно содержащий ординарную связь углерод-кислород. Неограничивающие примеры могут включать циклобутенилоксигруппу, циклопентенилоксигруппу, циклогексенилоксигруппу, циклогептенилоксигруппу, циклооктенилоксигруппу, циклодеценилоксигруппу, норборненилоксигруппу или бицикло[2.2.2] октенилоксигруппу.
"Алкилтиогруппа" означает и включает алкильную группу, содержащую по меньшей мере одну ординарную связь углерод-сера.
"Галогеналкилтиогруппа" означает и включает алкильную группу, содержащую по меньшей мере одну ординарную связь углерод-сера и атом галогена.
"Галоген" означает и включает фтор, хлор, бром или йод.
"Галогеналкил" означает и включает алкильную группу, замещенную по меньшей мере одним атомом галогена.
"Галогеналкоксигруппа" означает и включает алкоксигруппу, замещенную по меньшей мере одним атомом галогена.
"Гетероатом" означает и включает атом серы (S), кислорода (O) или азота (N).
"Гетероалкил" означает и включает алкил, содержащий по меньшей мере один атом серы (S), кислорода (O) или азота (N).
"Гетероциклил" означает циклический заместитель, который может быть полностью насыщенным, частично ненасыщенным или полностью ненасыщенным, где циклическая структура содержит по меньшей мере один атом углерода и по меньшей мере один гетероатом, где указанный гетероатом представляет собой азот, серу или кислород. В случае серы этот атом может находиться в других состояниях окисления, как в таких соединениях, как сульфоксид и сульфон. Примеры ароматических гетероциклилов включают, но не ограничиваются только ими, бензофуранил, бензоизотиазолил, бензоизоксазолил, бензоксазолил, бензотиенил, бензотиазолил, циннолинил, фуранил, имидазолил, индазолил, индолил, изоиндолил, изохинолинил, изотиазолил, изоксазолил, оксадиазолил, оксазолинил, оксазолил, фталазинил, пиразинил, пиразолинил, пиразолил, пиридазинил, пиридил, пиримидинил, пирролил, хиназолинил, хинолинил, хиноксалинил, тетразолил, тиазолинил, тиазолил, тиенил, триазинил и триазолил. Примеры полностью насыщенных гетероциклилов включают, но не ограничиваются только ими, пиперазинил, пиперидинил, морфолинил, пирролидинил, оксетанил, тетрагидрофуранил, тетрагидротиенил и тетрагидропиранил. примеры частично ненасыщенных гетероциклилов включают, но не ограничиваются только ими, 1,2,3,4-тетрагидрохинолинил, 4,5-дигидрооксазолил, 4,5-дигидро-1H-пиразолил, 4,5-дигидроизоксазолил и 2,3-дигидро-[1,3,4]-оксадиазолил. Дополнительные примеры включают следующие
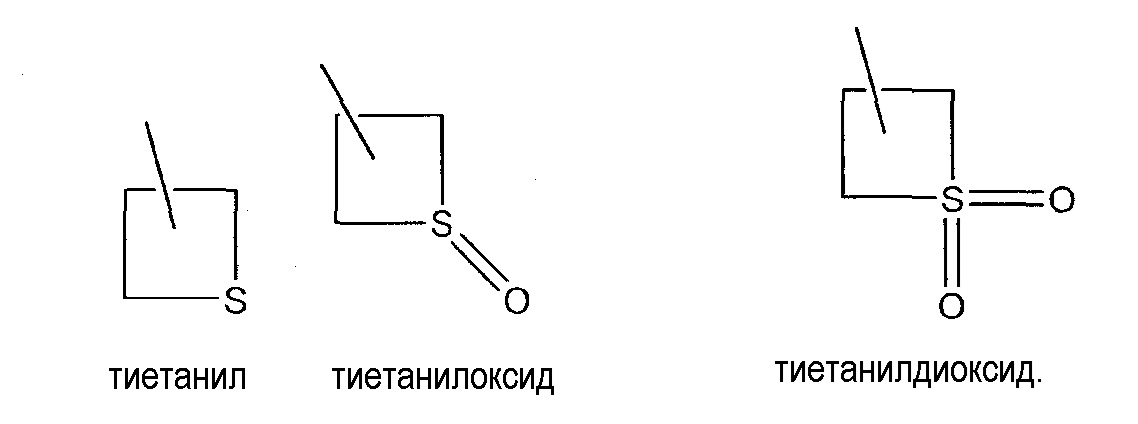
"Пестицидно эффективное количество" означает и включает количество активного вещества, которое приводит к неблагоприятному воздействию по меньшей мере на одно насекомое, где неблагоприятное воздействие может включать отклонение от естественного развития, уничтожение, регулирование количества и т.п.
"Борьба" или его грамматические варианты означает и включает регулирование количества живых насекомых или регулирование количества живых яиц насекомых.
"Синергетический эффект" или его грамматические варианты означает и включает кооперативное воздействие, наблюдающееся для комбинации двух или большего количества активных агентов, в которые суммарная активность двух или большего количества активных агентов превышает сумму активностей каждого активного агента, использующегося по отдельности.
Пестицидные соединения
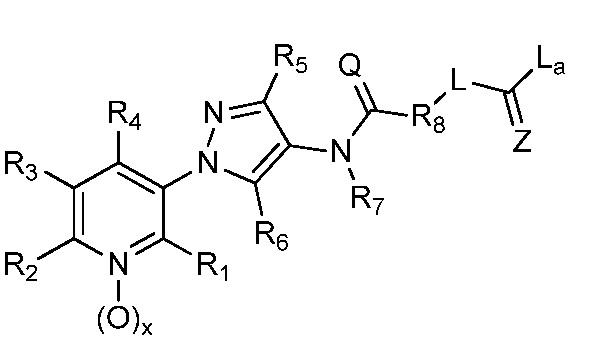
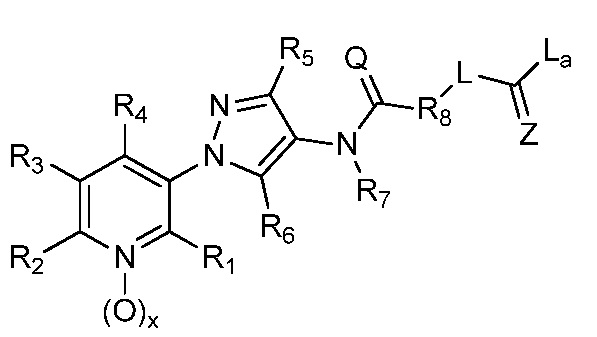
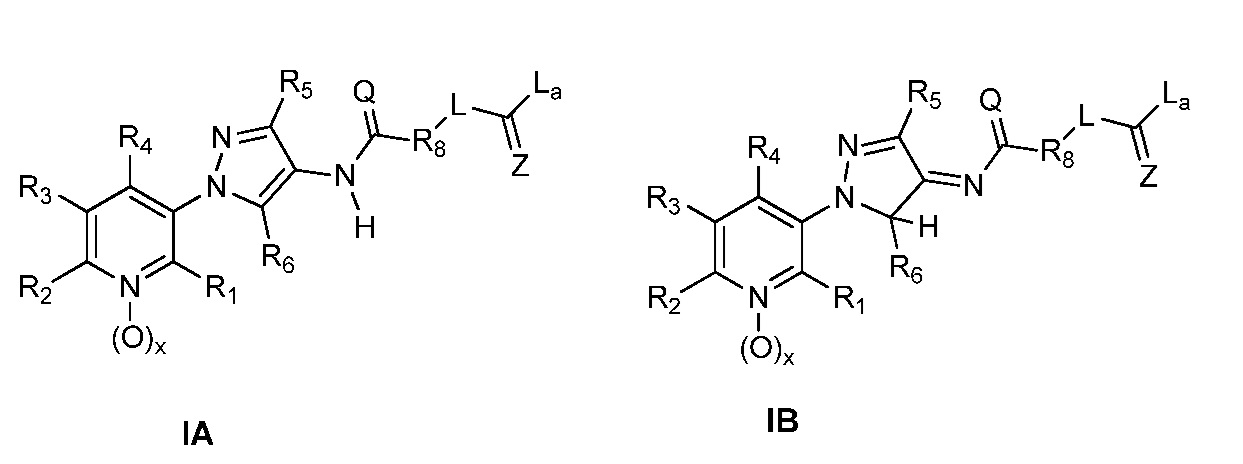
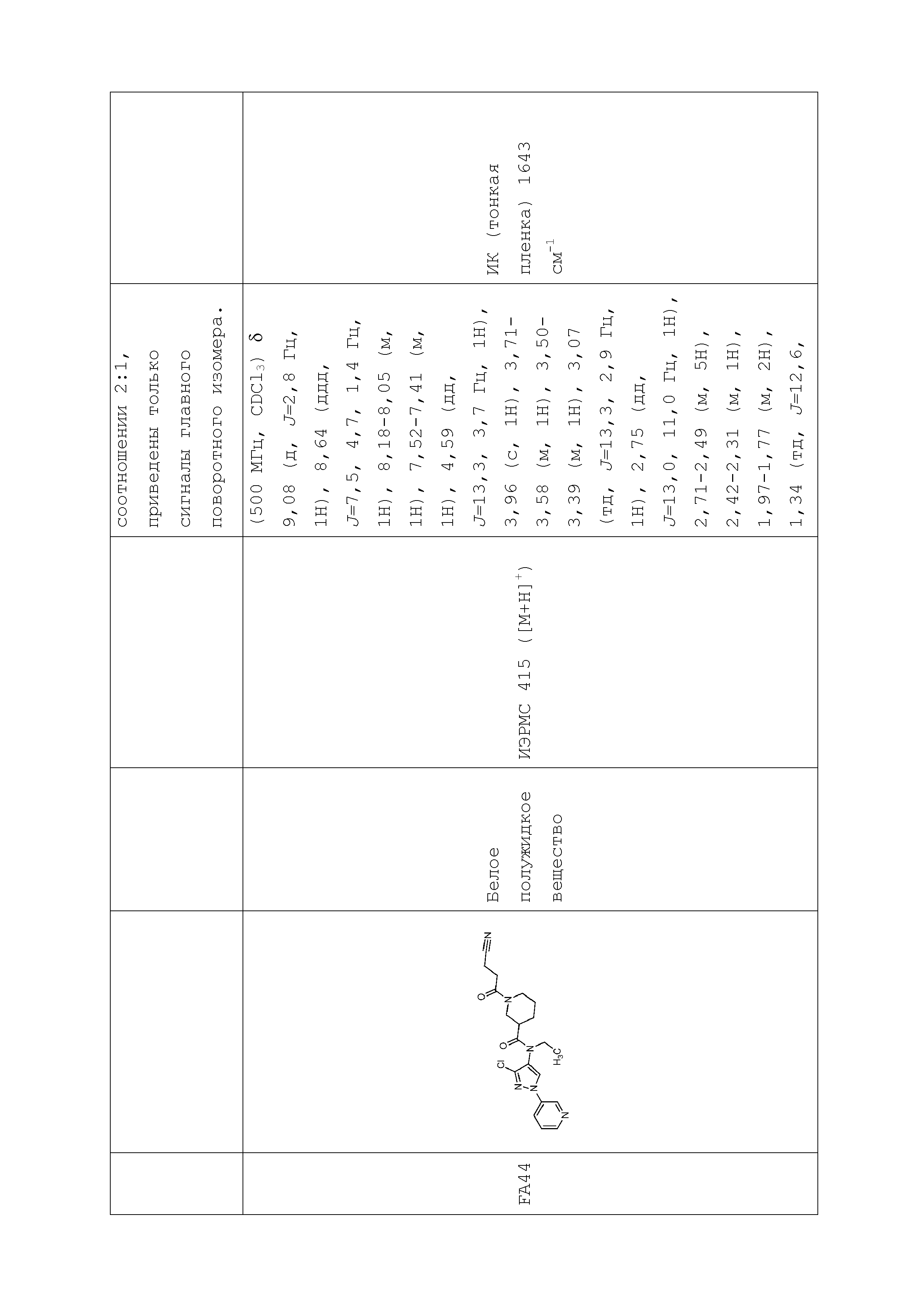
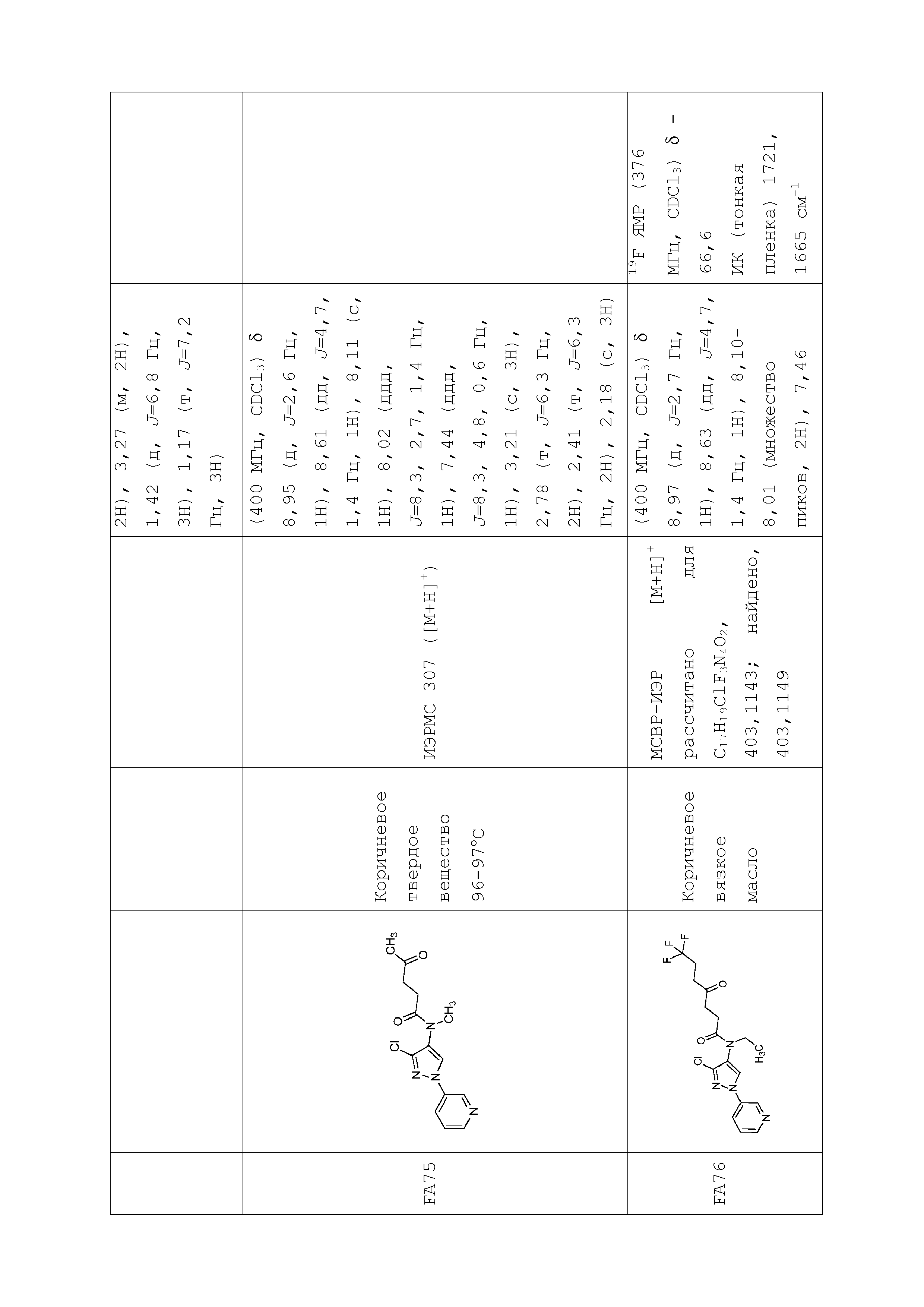
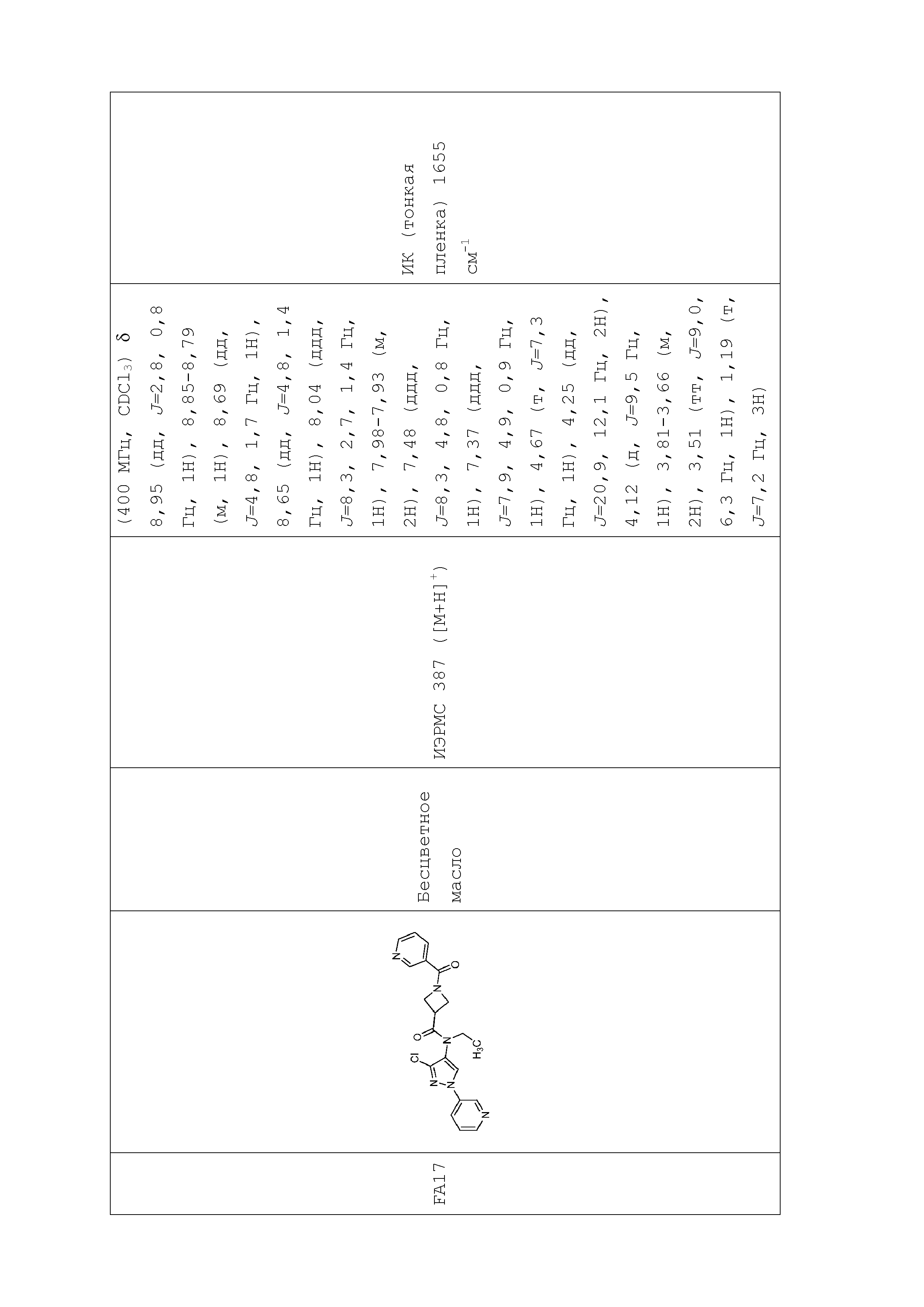
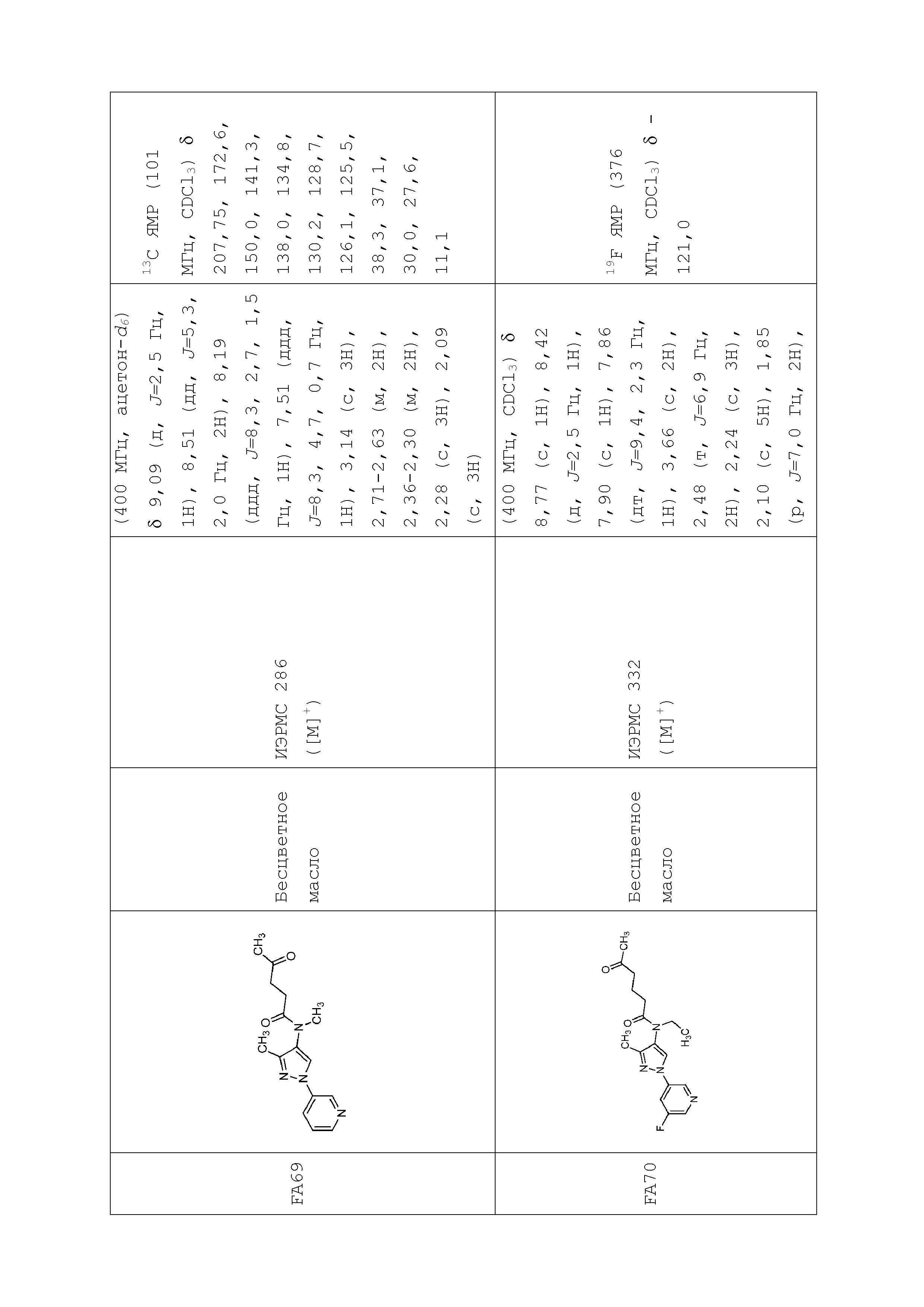
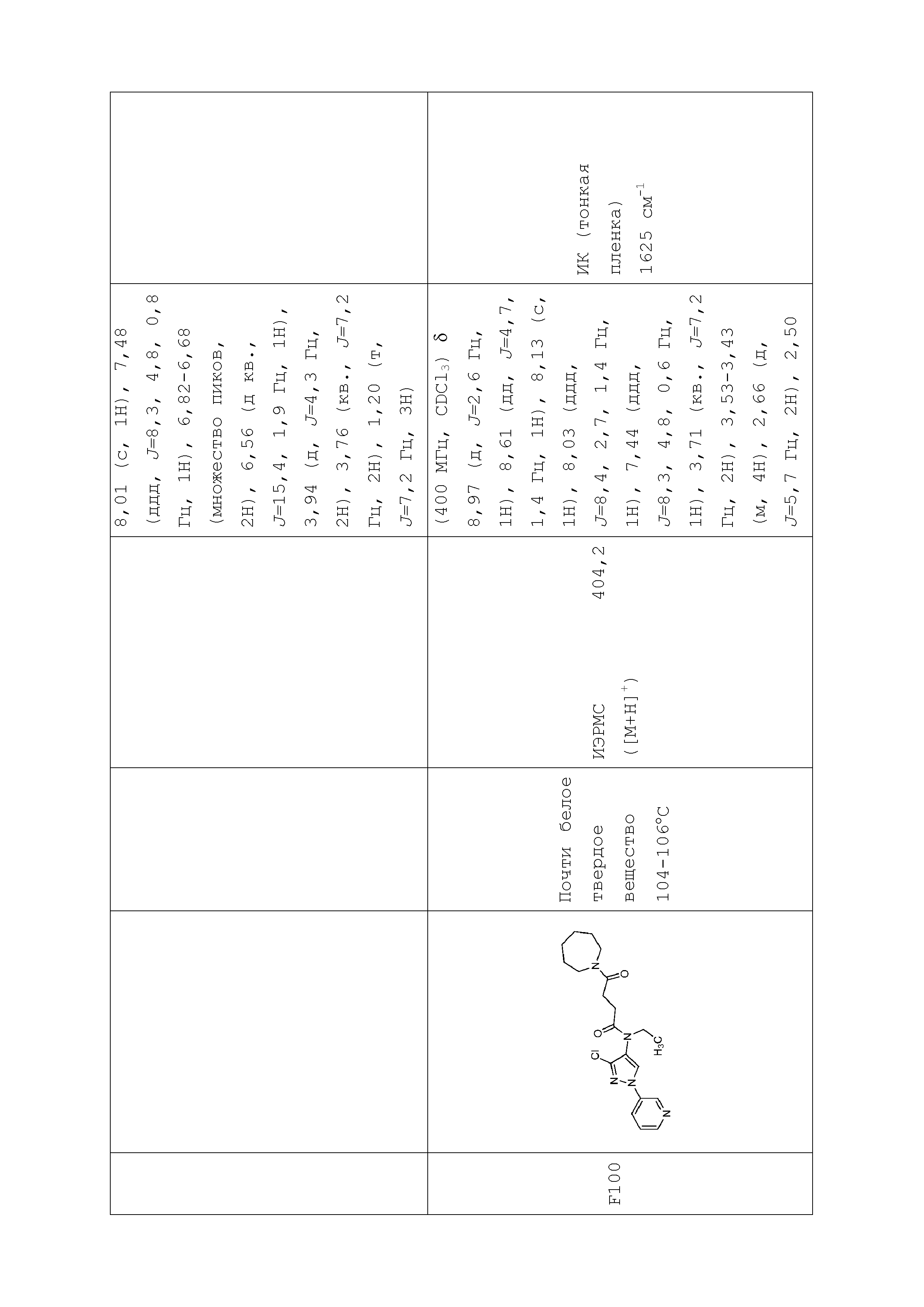
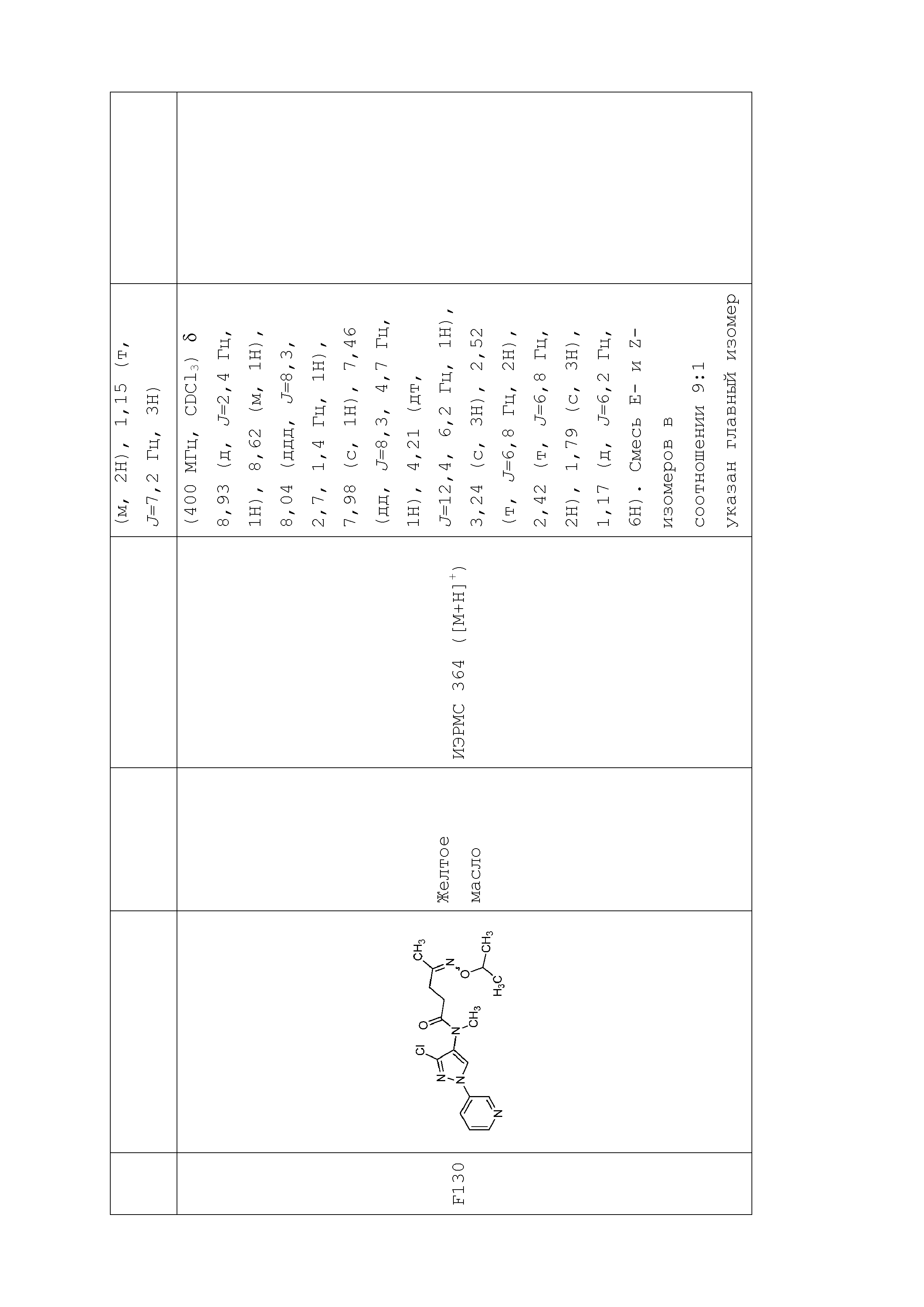
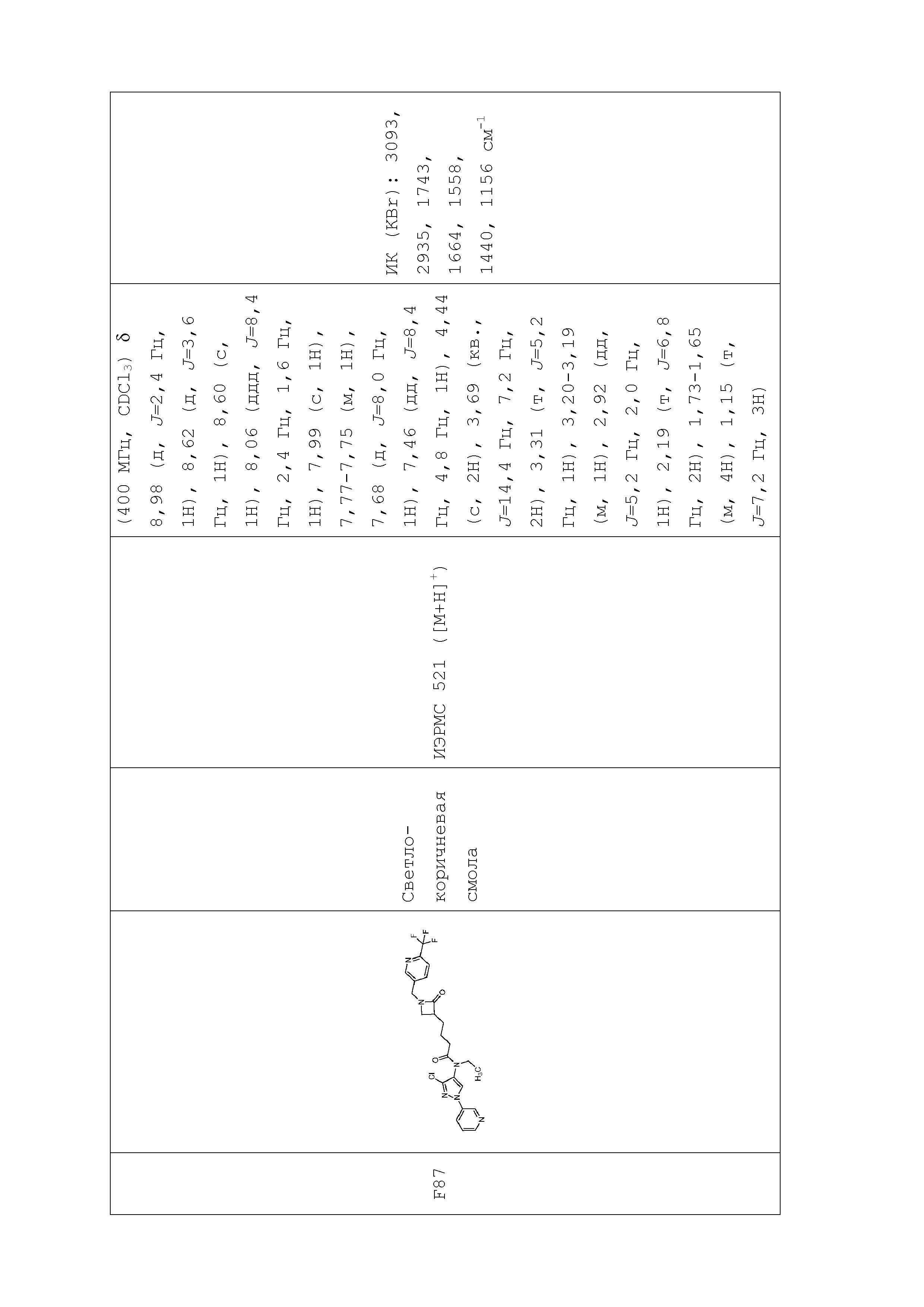
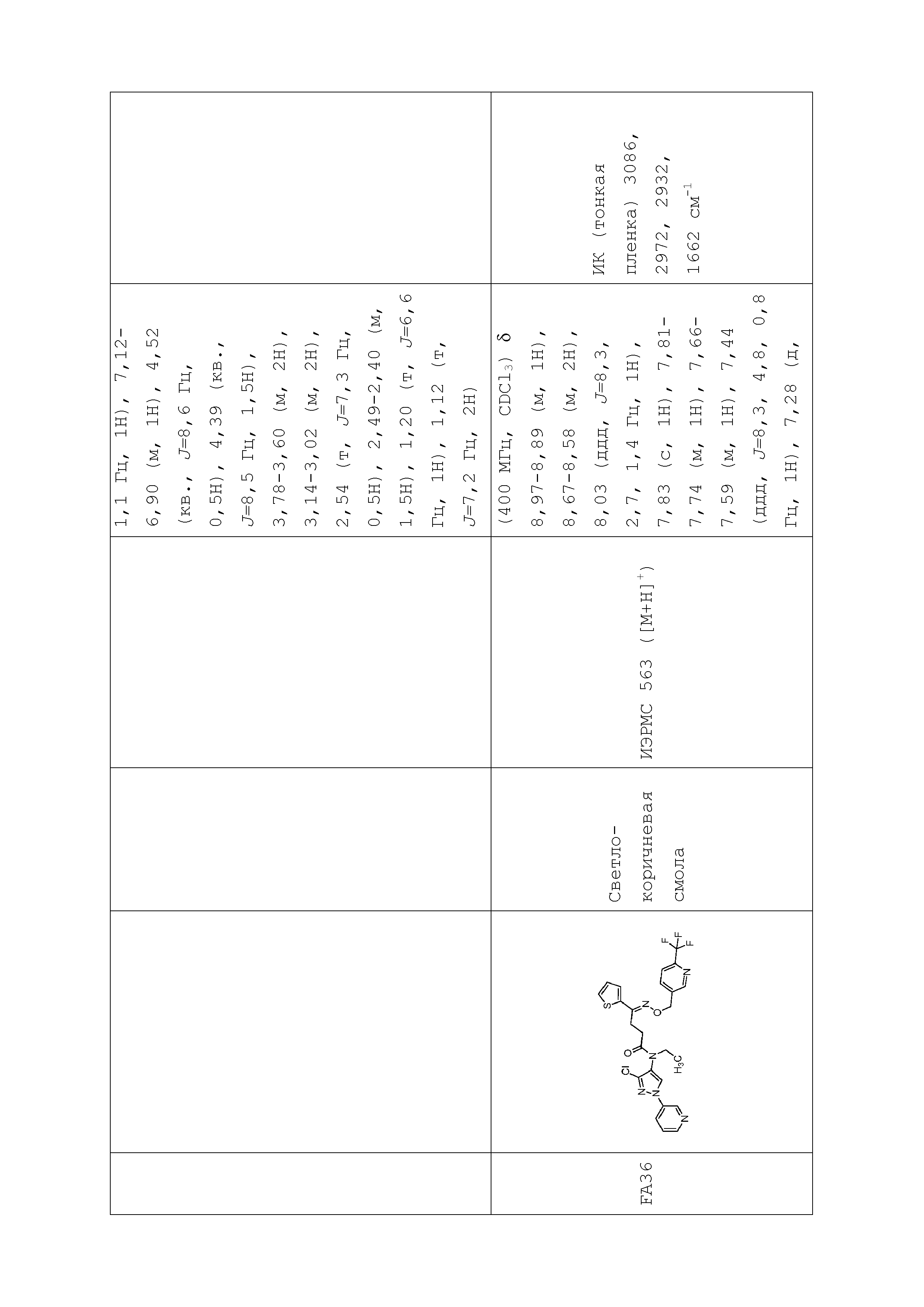
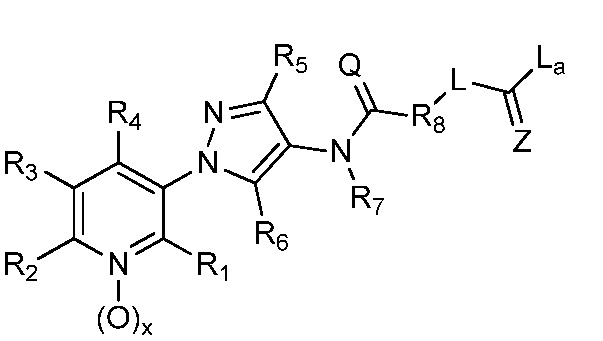
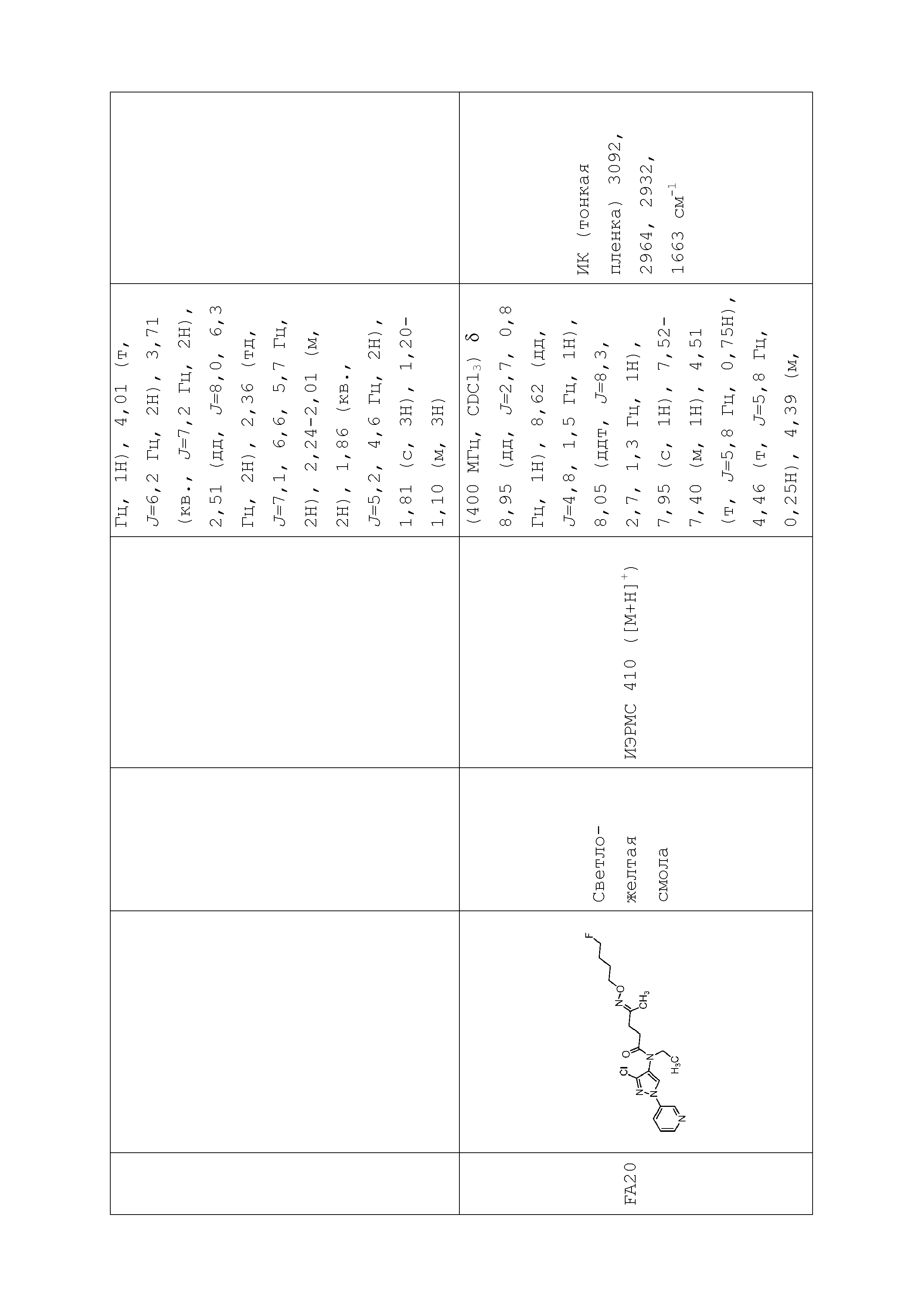
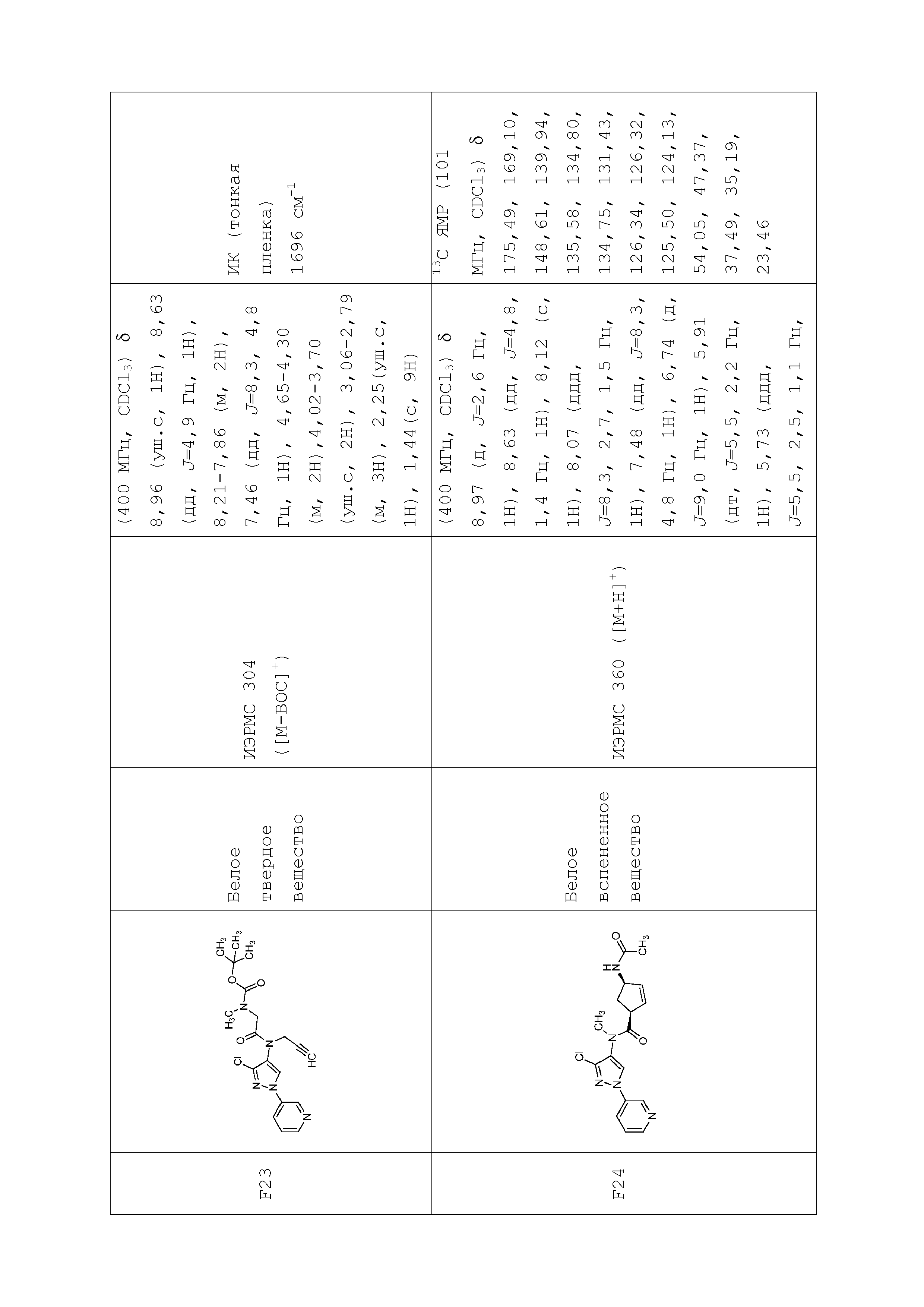
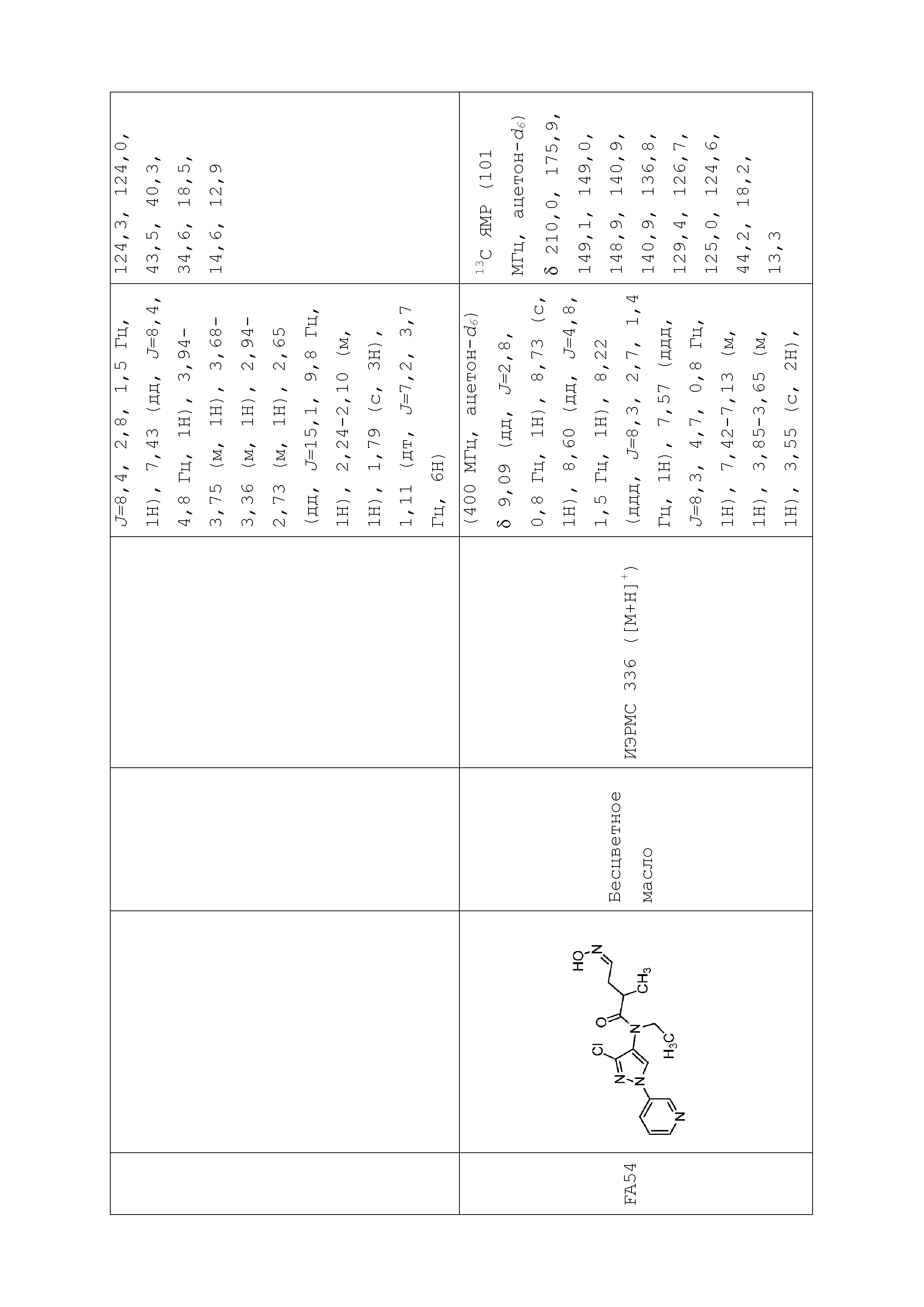
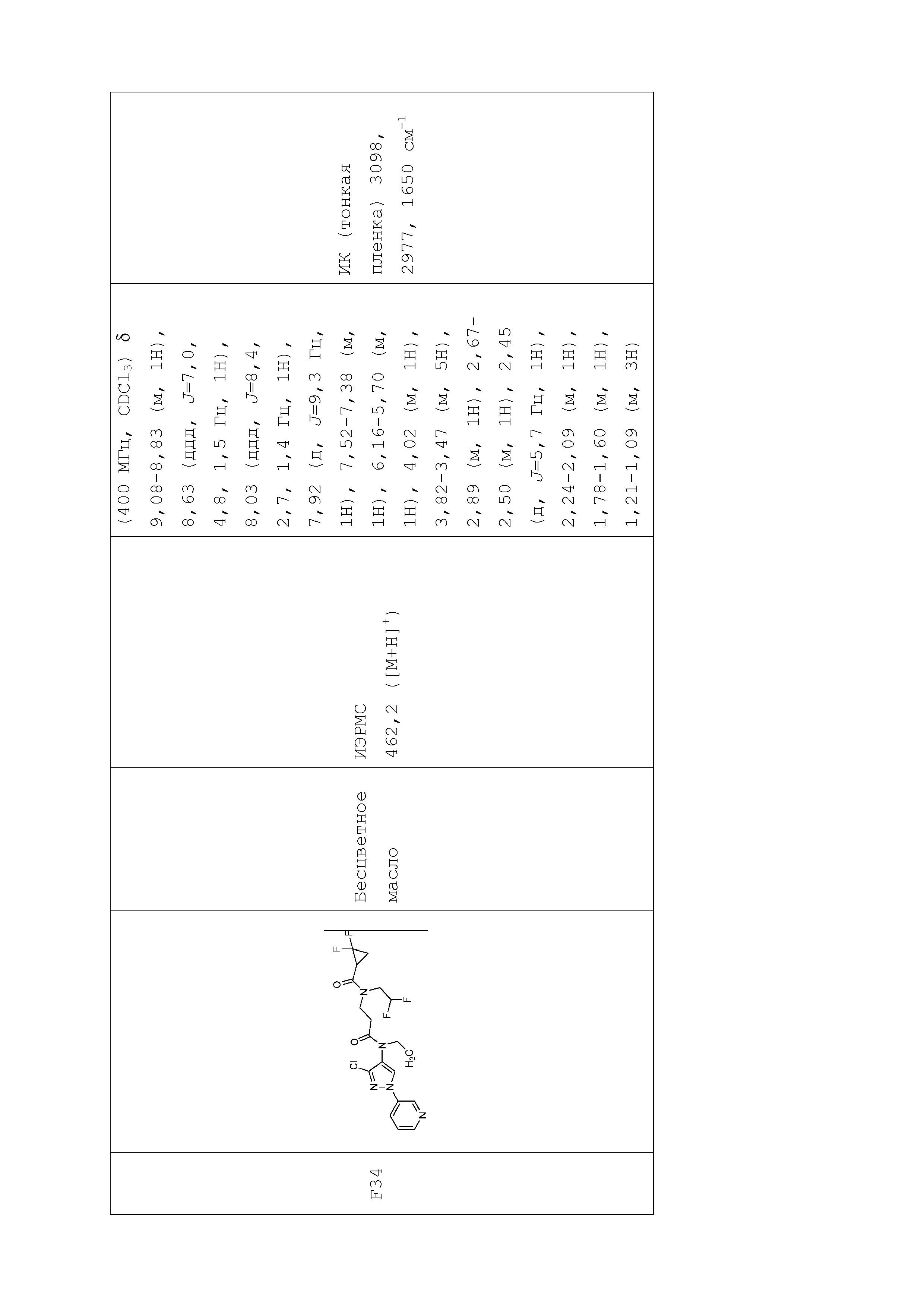
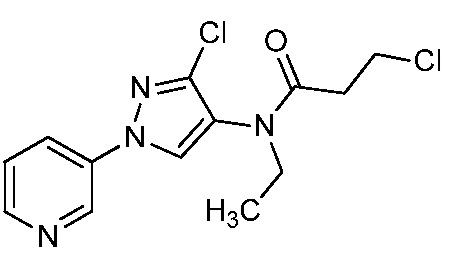
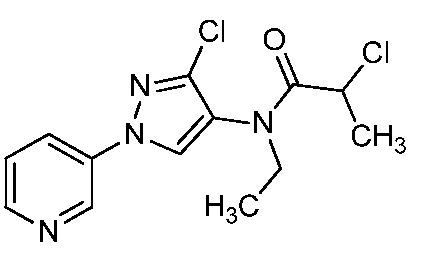
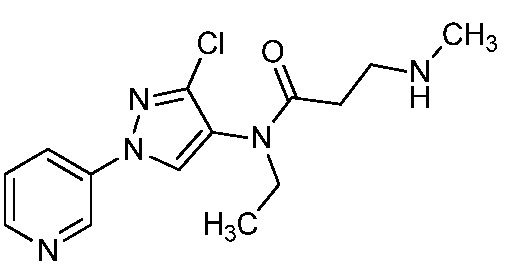
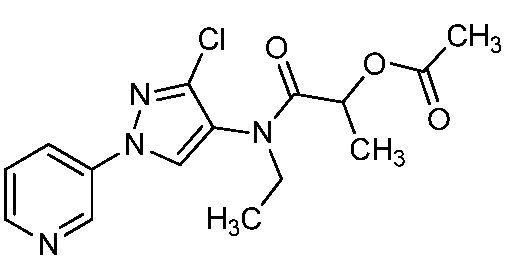
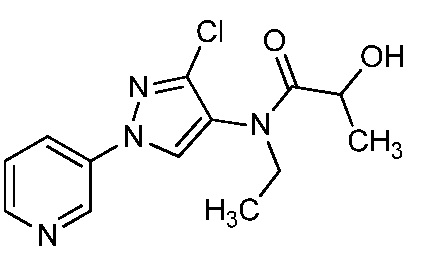
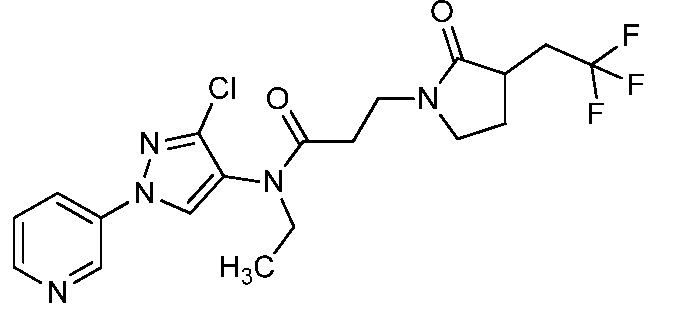
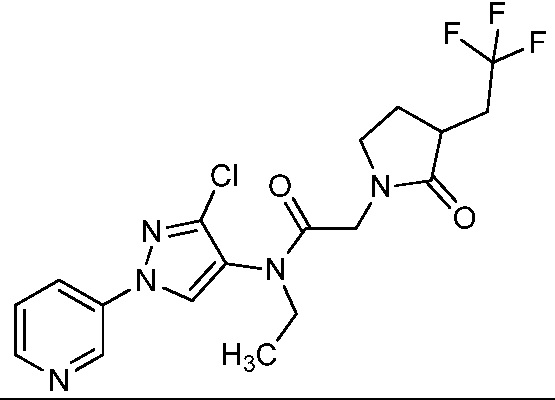
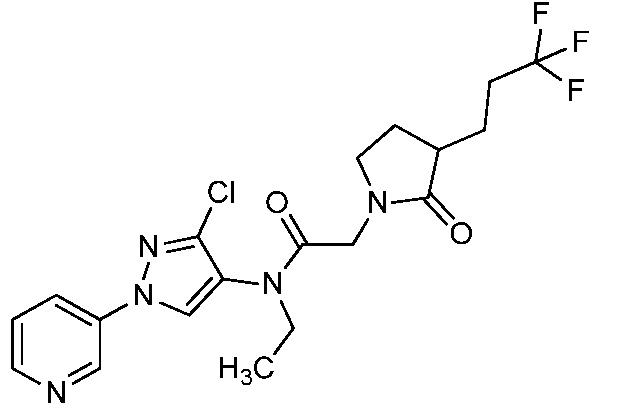
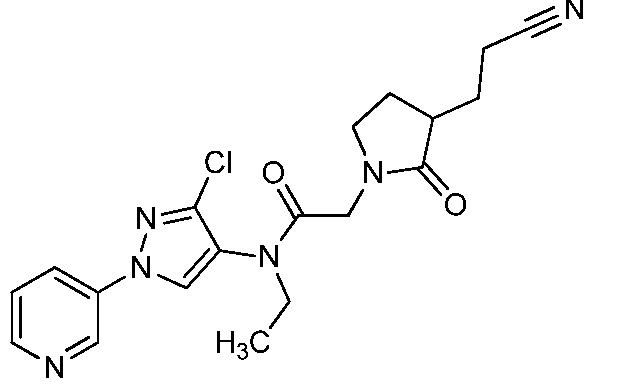
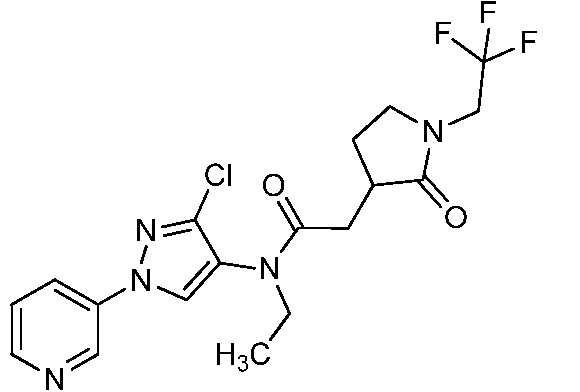
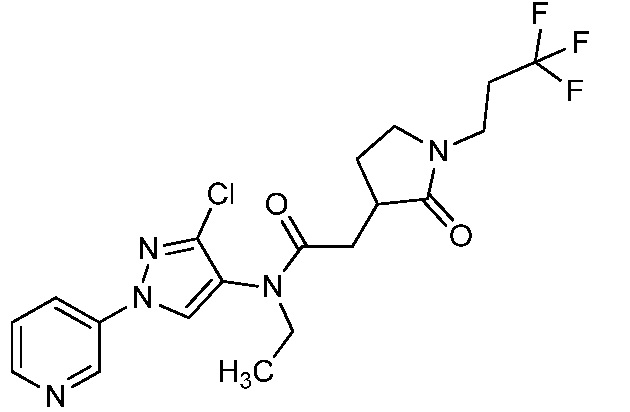
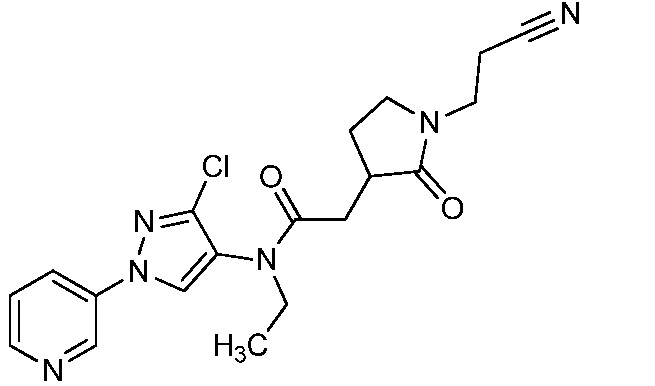
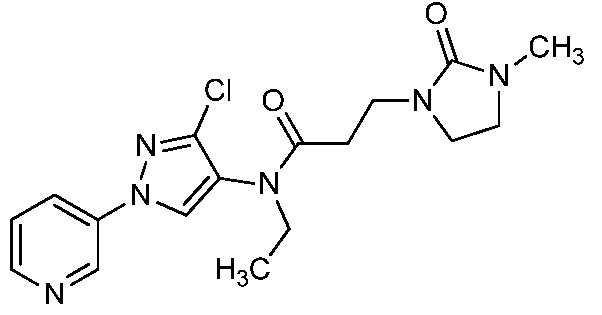
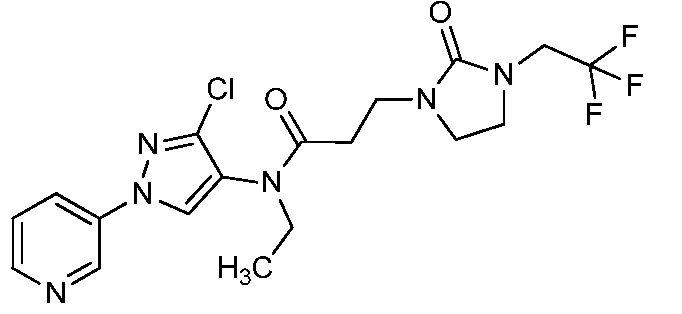
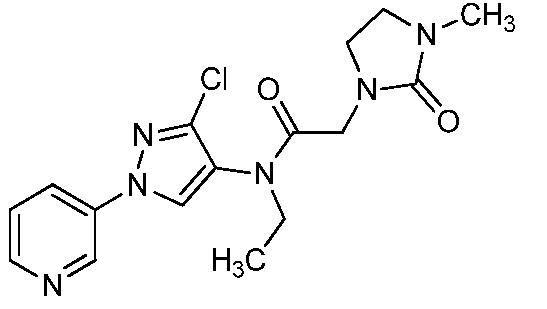
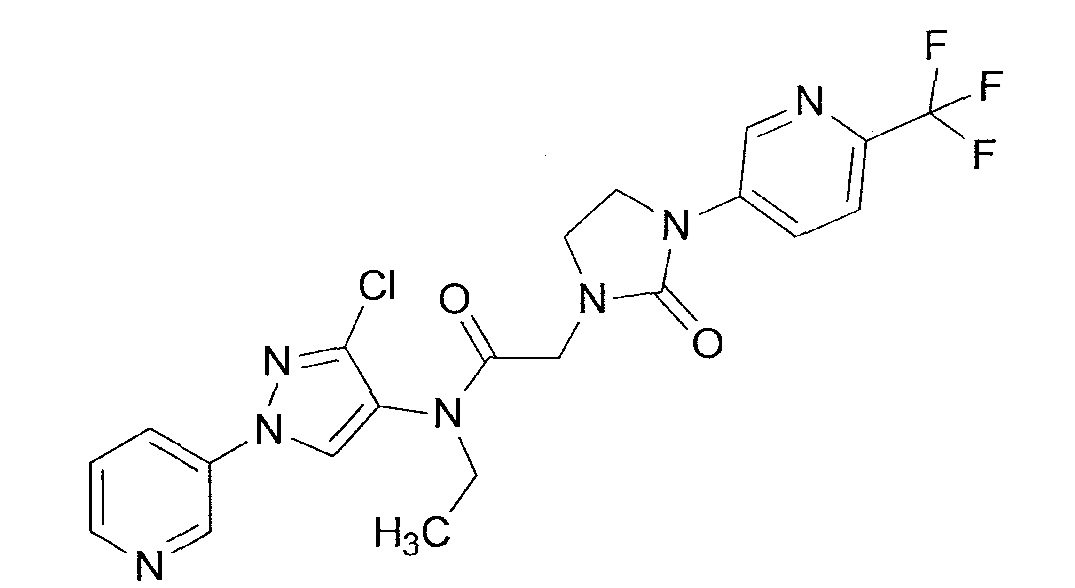
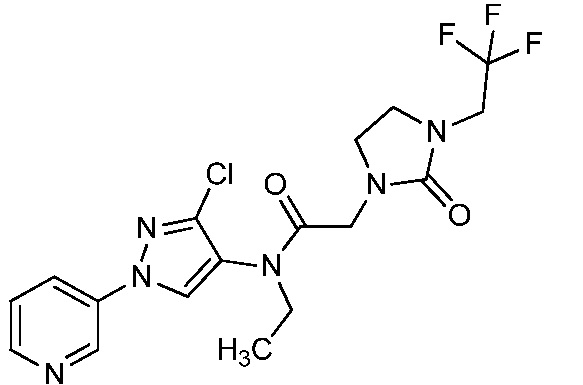
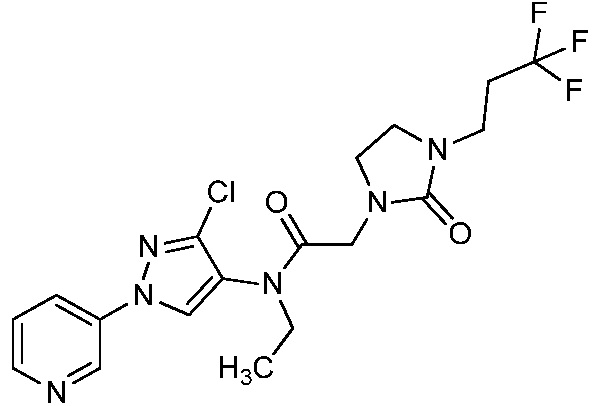
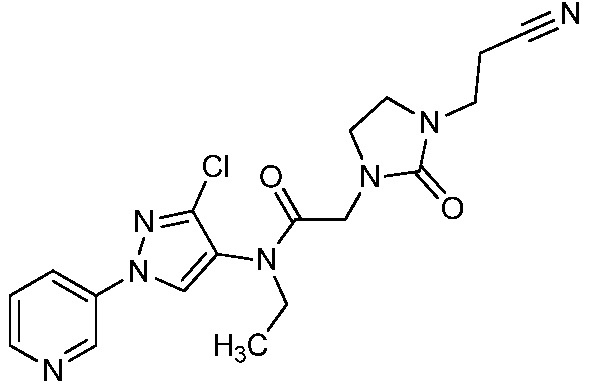
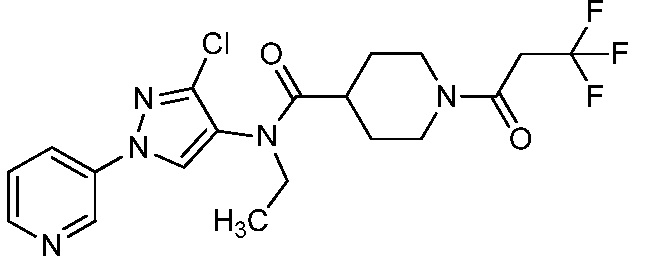
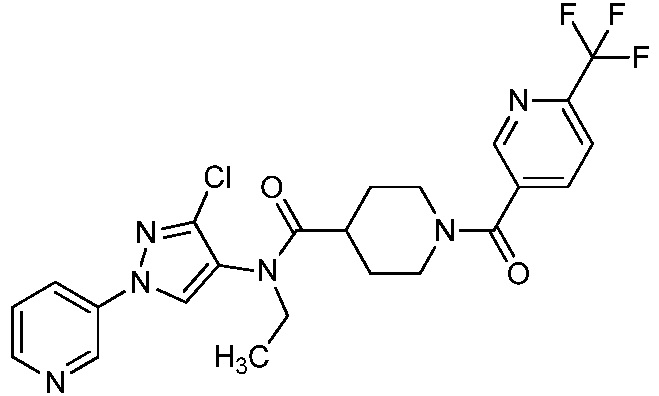
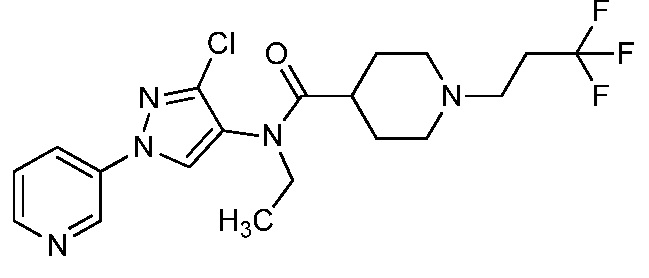
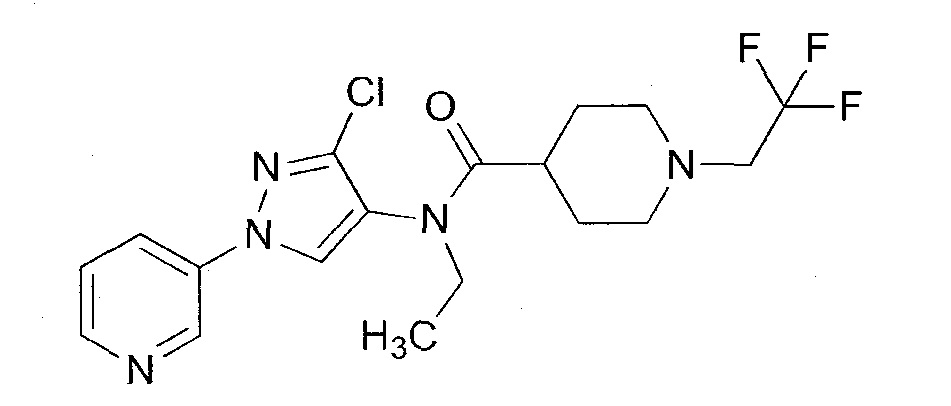
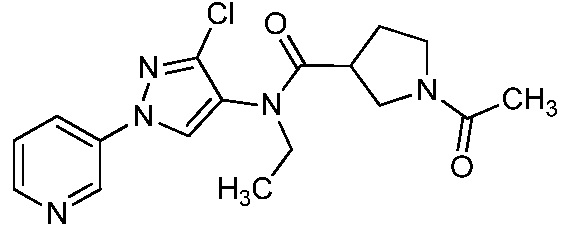
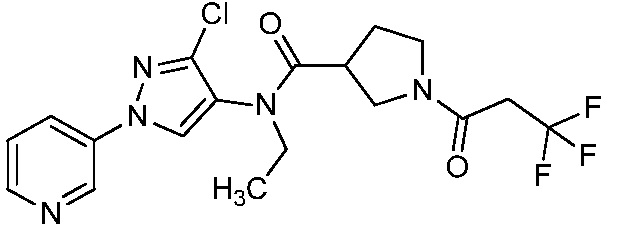
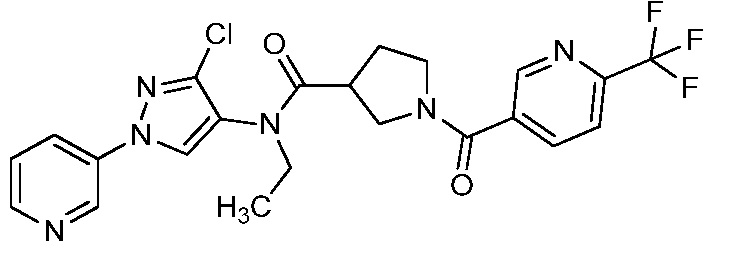
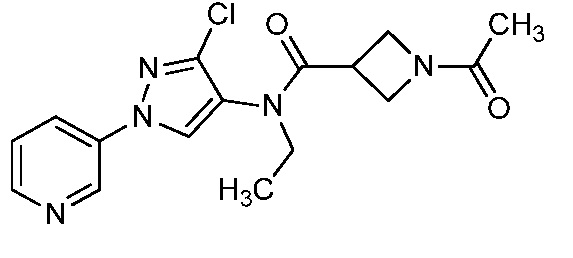
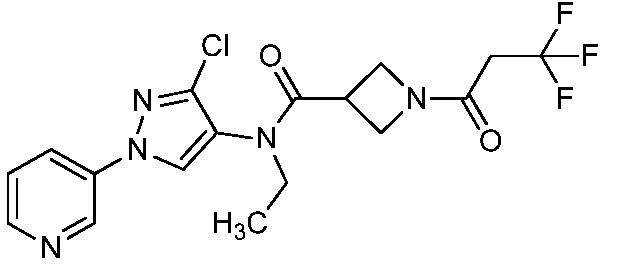
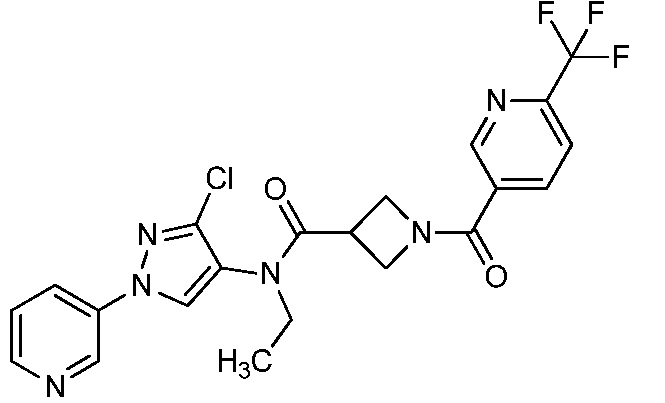
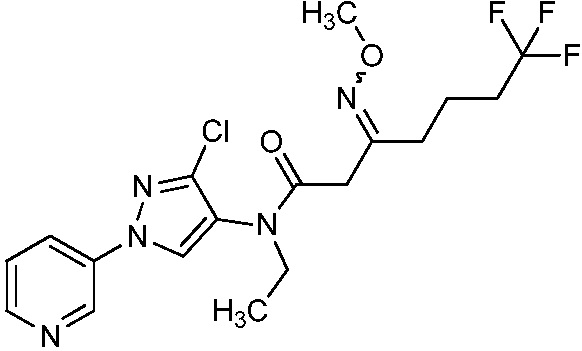
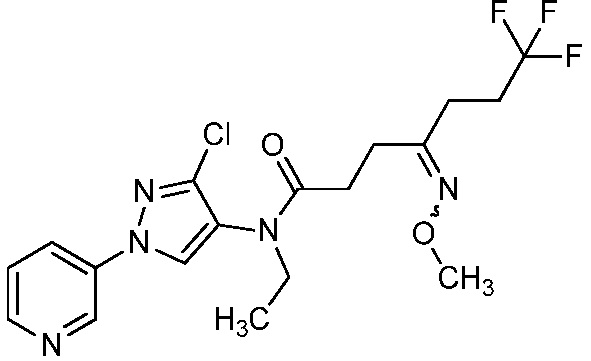
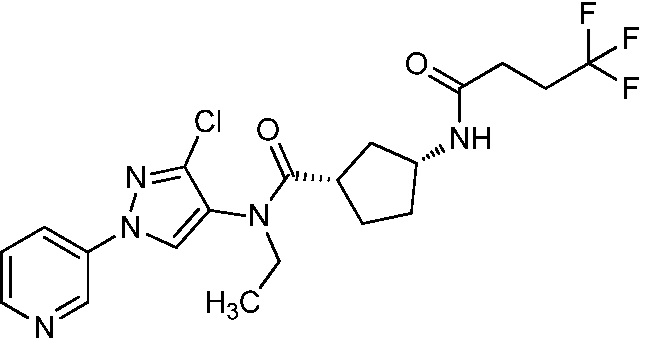
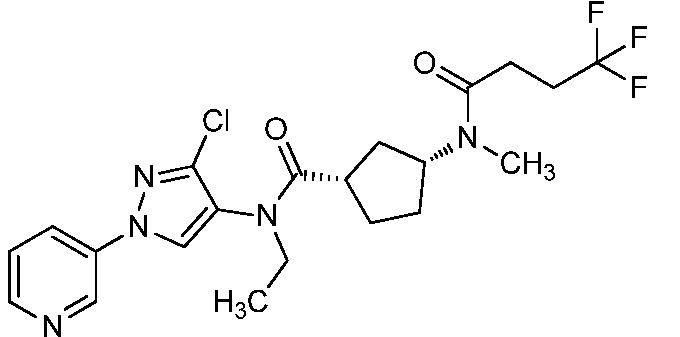
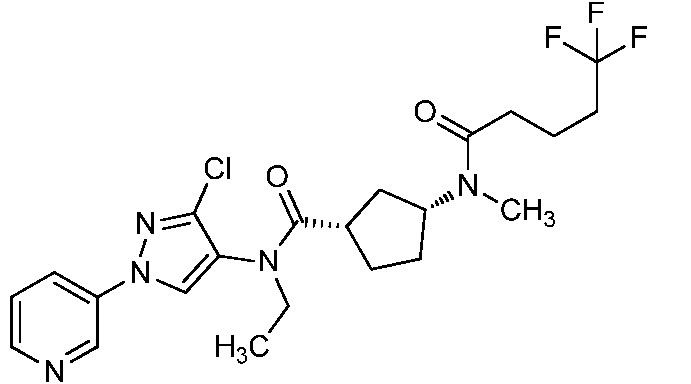
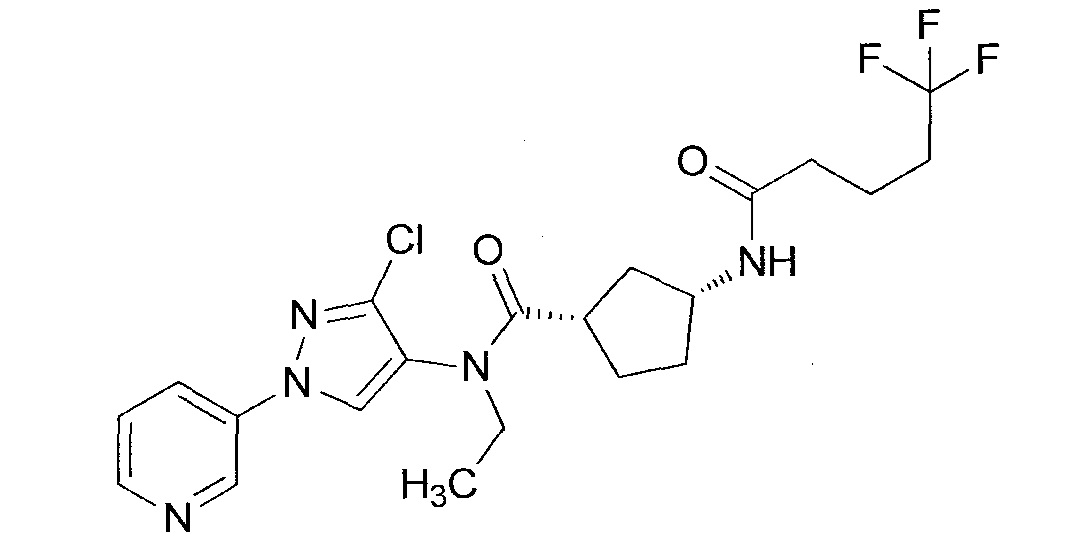
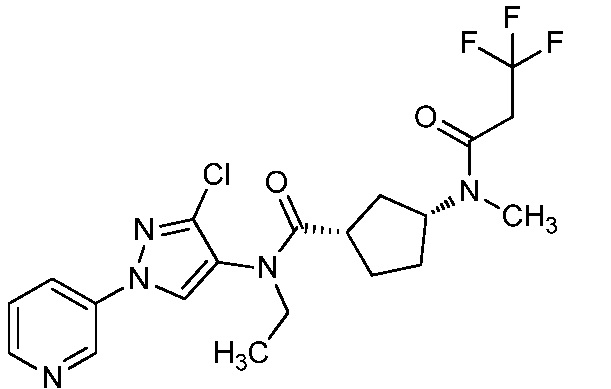
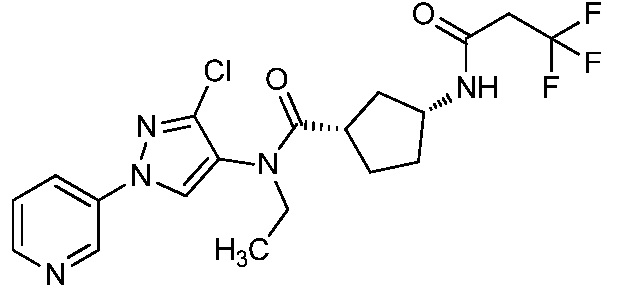
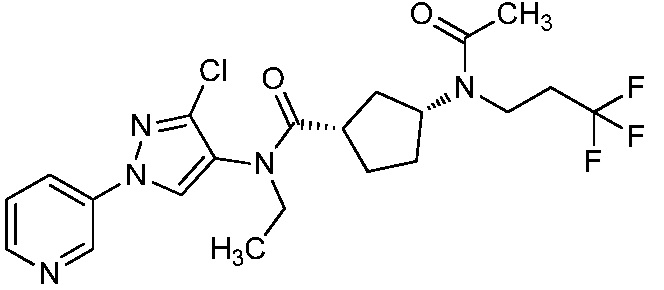
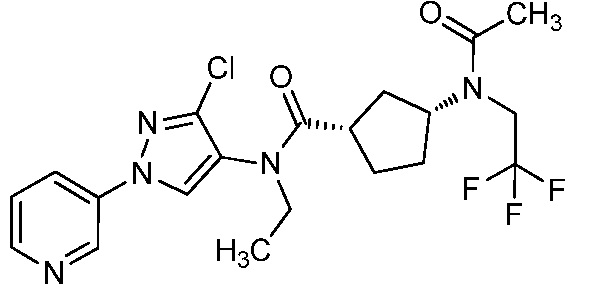
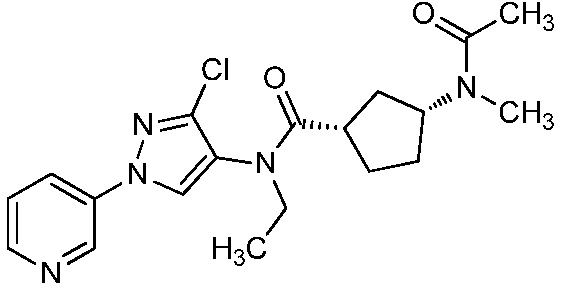
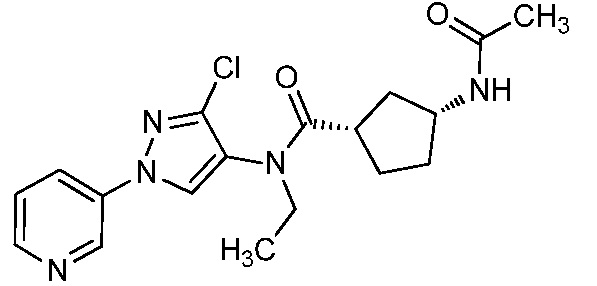
В одном предпочтительном варианте осуществления пестицидная композиция содержит по меньшей мере одно соединение, выбранное из соединений формулы I, или любую его сельскохозяйственно приемлемую соль:
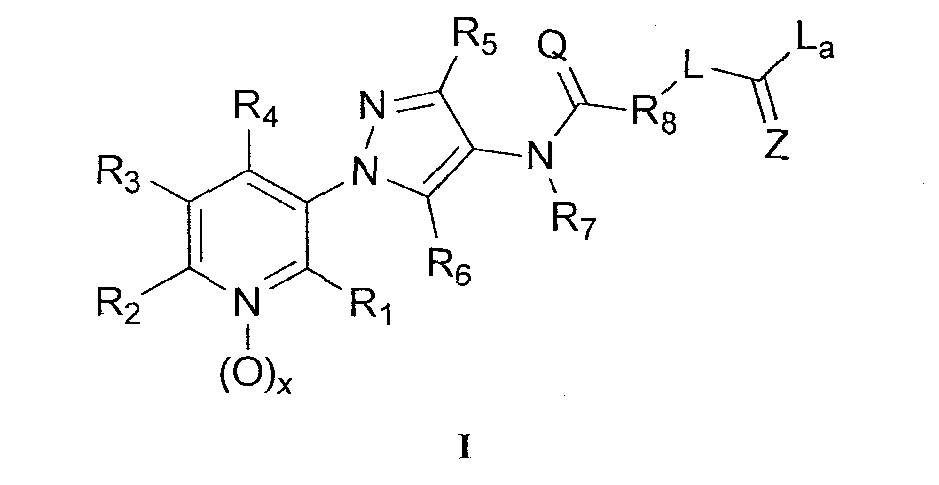
в которой:
R1, R2 и R4 независимо выбраны из группы, включающей водород, F, Cl, Br, I, замещенный или незамещенный C1-C6-алкил, или замещенный или незамещенный C1-C6-галогеналкил, где каждый указанный R1, R2 и R4, если является замещенным, содержит один или несколько заместителей, выбранных из группы, включающей F, Cl, Br, I, CN, NO2, C1-C6-алкил, C2-C6-алкенил, C1-C6-галогеналкил, C3-C10-циклоалкил или C3-C10-галогенциклоалкил (каждый из которых, который может быть замещенным, может быть необязательно замещен с помощью R10);
R3 выбран из группы, включающей водород, F, Cl, Br, I, CN, NO2, замещенный или незамещенный C1-C6-алкил, замещенный или незамещенный C2-C6-алкенил, замещенную или незамещенную C1-C6-алкоксигруппу, замещенный или незамещенный C3-C10-циклоалкил, замещенный или незамещенный C1-C6-галогеналкил, замещенный или незамещенный C6-C20-арил, замещенный или незамещенный C1-C20-гетероциклил, OR10, C(=X1)R10, C(=X1)OR10, C(=X1)N(R10)2, N(R10)2, N(R10)C(=X1)R10, SR10, S(O)nOR10 или R10S(O)nR10, где каждый указанный R3, если является замещенным, содержит один или несколько заместителей, выбранных из группы, включающей F, Cl, Br, I, CN, NO2, C1-C6-алкил, C2-C6-алкенил, C1-C6-галогеналкил, C2-C6-галогеналкенил, C1-C6-галогеналкилоксигруппу, C2-C6-галогеналкенилоксигруппу, C3-C10-циклоалкил, C3-C10-циклоалкенил, C3-C10-галогенциклоалкил, C3-C10-галогенциклоалкенил, OR10, S(O)nOR10, C6-C20-арил или C1-C20-гетероциклил (каждый из которых, который может быть замещенным, может быть необязательно замещен с помощью R10);
R5 выбран из группы, включающей H, F, Cl, Br, I, CN, NO2, замещенный или незамещенный C1-C6-алкил, замещенный или незамещенный C2-C6-алкенил, замещенную или незамещенную C1-C6-алкоксигруппу, C3-C10-циклоалкил, замещенный или незамещенный C6-C20-арил, замещенный или незамещенный C1-C20-гетероциклил, OR10, C(=X1)R10, C(=X1)OR10, C(=X1)N(R10)2, N(R10)2, N(R10)C(=X1)R10, S(O)nR10, S(O)nOR10 или R10S(O)nR10, где каждый указанный R5, если является замещенным, содержит один или несколько заместителей, выбранных из группы, включающей F, Cl, Br, I, CN, NO2, C1-C6-алкил, C2-C6-алкенил, C1-C6-галогеналкил, C2-C6-галогеналкенил, C1-C6-галогеналкилоксигруппу, C2-C6-галогеналкенилоксигруппу, C3-C10-циклоалкил, C3-C10-циклоалкенил, C3-C10-галогенциклоалкил, C3-C10-галогенциклоалкенил, OR10, S(O)nOR10, C6-C20-арил или C1-C20-гетероциклил (каждый из которых, который может быть замещенным, может быть необязательно замещен с помощью R10);
R6 выбран из группы, включающей H, F, Cl, Br, I, замещенный или незамещенный C1-C6-алкил, или C1-C6-галогеналкил, где каждый указанный R6, если является замещенным, содержит один или несколько заместителей, выбранных из группы, включающей F, Cl, Br, I, CN, NO2, C1-C6-алкил, C2-C6-алкенил, C1-C6-галогеналкил, C2-C6-галогеналкенил, C1-C6-галогеналкилоксигруппу, C2-C6-галогеналкенилоксигруппу, C3-C10-циклоалкил, C3-C10-циклоалкенил, C3-C10-галогенциклоалкил или C3-C10-галогенциклоалкенил;
R7 выбран из группы, включающей водород, замещенный или незамещенный C1-C6-алкил, замещенный или незамещенный C2-C6-алкенил, замещенный или незамещенный C2-C6-алкинил, замещенную или незамещенную C1-C6-алкоксигруппу, замещенный или незамещенный C3-C10-циклоалкил, C1-C6-алкил C2-C6-алкинил (где алкил и алкинил может независимо быть замещенным или незамещенным), замещенный или незамещенный C6-C20-арил, замещенный или незамещенный C1-C20-гетероциклил, C1-C6-алкил C6-C20-арил (где алкил и арил может независимо быть замещенным или незамещенным), C1-C6-алкил-(C3-C10-циклогалогеналкил), где алкил и циклогалогеналкил может независимо быть замещенным или незамещенным, или C1-C6-алкил-(C3-C10-циклоалкил), где алкил и циклоалкил может независимо быть замещенным или незамещенным, где каждый указанный R7, если является замещенным, содержит один или несколько заместителей, выбранных из группы, включающей F, Cl, Br, I, CN, NO2, C1-C6-алкил, C2-C6-алкенил, C2-C6-алкинил, C1-C6-галогеналкил, C2-C6-галогеналкенил, C1-C6-галогеналкилоксигруппу, C2-C6-галогеналкенилоксигруппу, C3-C10-циклоалкил, C3-C10-циклоалкенил, C3-C10-галогенциклоалкил, C3-C10-галогенциклоалкенил, OR10, S(O)nOR10, C6-C20-арил или C1-C20-гетероциклил, R10-арил (каждый из которых, который может быть замещенным, может быть необязательно замещен с помощью R10);
R8 выбран из группы, включающей замещенный или незамещенный C1-C6-алкил, замещенный или незамещенный C2-C6-алкенил, замещенную или незамещенную C1-C6-алкоксигруппу, замещенный или незамещенный C3-C10-циклоалкил, замещенный или незамещенный C3-C10-галогенциклоалкил, замещенный или незамещенный C3-C10-циклоалкенил, замещенный или незамещенный C6-C20-арил, или замещенный или незамещенный C1-C20-гетероциклил,
где каждый указанный R8, если является замещенным, содержит один или несколько заместителей, выбранных из группы, включающей F, Cl, Br, I, CN, NO2, замещенный или незамещенный C1-C6-алкил, замещенный или незамещенный C2-C6-алкенил, замещенный или незамещенный C1-C6-галогеналкил, замещенный или незамещенный C2-C6-галогеналкенил, замещенную или незамещенную C1-C6-галогеналкилоксигруппу, замещенную или незамещенную C2-C6-галогеналкенилоксигруппу, замещенный или незамещенный C3-C10-циклоалкил, замещенный или незамещенный C3-C10-циклоалкенил, замещенный или незамещенный C3-C10-галогенциклоалкил, замещенный или незамещенный C3-C10-галогенциклоалкенил, оксогруппу, OR10, S(O)nR10, замещенный или незамещенный C6-C20-арил, или замещенный или незамещенный C1-C20-гетероциклил (каждый из которых, если является замещенным, замещен с помощью R10);
L выбран из группы, включающей связь, R9, O, S, N(R9), N(R9)C(=X1), C(R9)2 или C(R9)(R11);
La выбран из группы, включающей R9, OR9, N(R9)2, N(R9)(R11), N(R9)(OR11), N(R9)C(=X1)R9, N(R9)C(=X1)(R11), C(R9)3, C(R9)(R11)(R12) или SR9;
необязательно L и La объединены в циклическую структуру, которая образует 3- - 8-членные гетероциклы или карбоциклы, включающие L и La, где циклическая структура не содержит или содержит по меньшей мере один из гетероатомов O, S или N, и циклическая структура является незамещенной или замещенной, где, если циклическая структура является замещенной, то циклическая структура содержит один или несколько заместителей, выбранных из группы, включающей F, Cl, Br, I, CN, NO2, замещенный или незамещенный C1-C6-алкил, замещенный или незамещенный C2-C6-алкенил, замещенный или незамещенный C2-C6-алкинил, замещенный или незамещенный C1-C6-галогеналкил, замещенный или незамещенный C2-C6-галогеналкенил, замещенную или незамещенную C1-C6-галогеналкилоксигруппу, замещенную или незамещенную C2-C6-галогеналкенилоксигруппу, замещенный или незамещенный C3-C10-циклоалкил, замещенный или незамещенный C3-C10-циклоалкенил, замещенный или незамещенный C3-C10-галогенциклоалкил, замещенный или незамещенный C3-C10-галогенциклоалкенил, N(R9)S(O)nR11, оксогруппу, OR9, S(O)nOR9, R9S(O)n R11, S(O)nR9, замещенный или незамещенный C6-C20-арил, или замещенный или незамещенный C1-C20-гетероциклил (каждый из которых, если является замещенным, замещен с помощью R10);
R9, R11, R12 и R13 независимо выбраны из группы, включающей водород, CN, NO2, замещенный или незамещенный C1-C6-алкил, замещенный или незамещенный C2-C6-алкенил, замещенную или незамещенную C1-C6-алкоксигруппу, замещенный или незамещенный C3-C10-циклоалкил, замещенный или незамещенный C3-C10-галогенциклоалкил, замещенный или незамещенный C3-C10-циклоалкенил, замещенный или незамещенный C6-C20-арил, или замещенный или незамещенный C1-C20-гетероциклил;
где каждый из указанных R9, R11 и R12, если является замещенным, содержит один или большее количество заместителей, выбранных из группы, включающей F, Cl, Br, I, CN, NO2, замещенный или незамещенный C1-C6-алкил, замещенный или незамещенный C2-C6-алкенил, замещенный или незамещенный C1-C6-галогеналкил, замещенный или незамещенный C2-C6-галогеналкенил, замещенную или незамещенную C1-C6-галогеналкилоксигруппу, замещенную или незамещенную C2-C6-галогеналкенилоксигруппу, замещенный или незамещенный C3-C10-циклоалкил, замещенный или незамещенный C3-C10-циклоалкенил, замещенный или незамещенный C3-C10-галогенциклоалкил, замещенный или незамещенный C3-C10-галогенциклоалкенил, оксогруппу, OR10, C(=X1)R10, S(O)nR10, замещенный или незамещенный C6-C20-арил, или замещенный или незамещенный C1-C20-гетероциклил (каждый из которых, если является замещенным, замещен с помощью R10);
R10 означает H, F, Cl, Br, I, CN, NO2, замещенный или незамещенный C1-C6-алкил, замещенный или незамещенный C2-C6-алкенил, замещенную или незамещенную C1-C6-алкоксигруппу, замещенную или незамещенную C2-C6-алкенилоксигруппу, замещенный или незамещенный C3-C10-циклоалкил, замещенный или незамещенный C3-C10-циклоалкенил, замещенный или незамещенный C6-C20-арил, замещенный или незамещенный C1-C20-гетероциклил, замещенный или незамещенный S(O)nC1-C6-алкил, или замещенный или незамещенный N(C1-C6-алкил)2,
где каждый указанный R10, если является замещенным, содержит один или несколько заместителей, выбранных из группы, включающей F, Cl, Br, I, CN, NO2, C1-C6-алкил, C2-C6-алкенил, C1-C6-галогеналкил, C2-C6-галогеналкенил, C1-C6-галогеналкилоксигруппу, C2-C6-галогеналкенилоксигруппу, C3-C10-циклоалкил, C3-C10-циклоалкенил, C3-C10-галогенциклоалкил, C3-C10-галогенциклоалкенил, OC1-C6-алкил, OC1-C6-галогеналкил, S(O)nC1-C6-алкил, S(O)nOC1-C6-алкил, C6-C20-арил или C1-C20-гетероциклил;
Q означает (каждый независимо) O или S;
Z означает (каждый независимо) O, S, CH2, NR13 или NOR13;
X1 означает (каждый независимо) O или S;
n равно 0, 1 или 2; и
x равно 0 или 1.
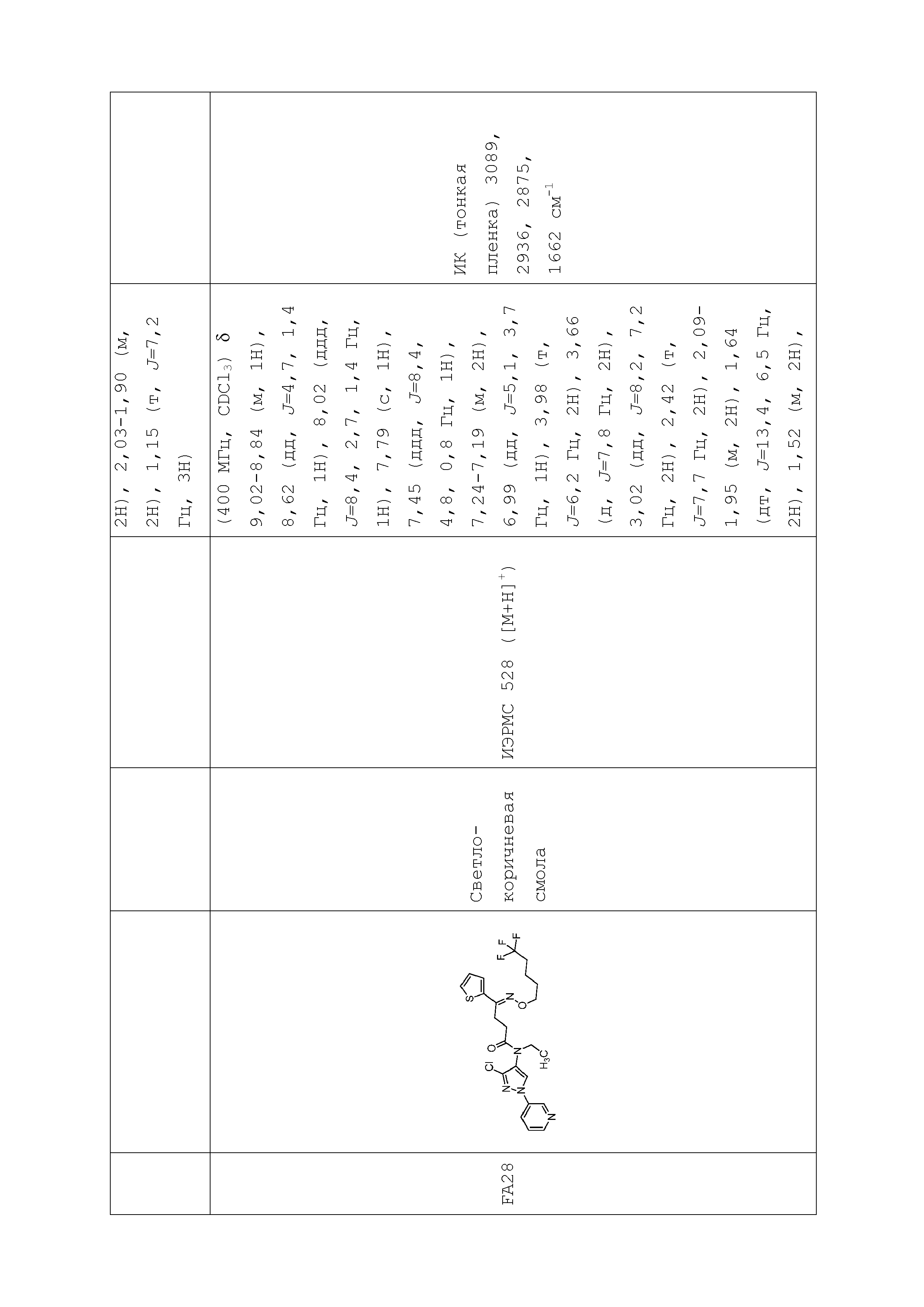
Соединение формулы I, в которой R7 означает H, может находится в различных изомерных формах. Неограничивающие примеры таких изомерных форм могут включать, но не ограничиваются только ими, соединения IA или IB, приведенные ниже.
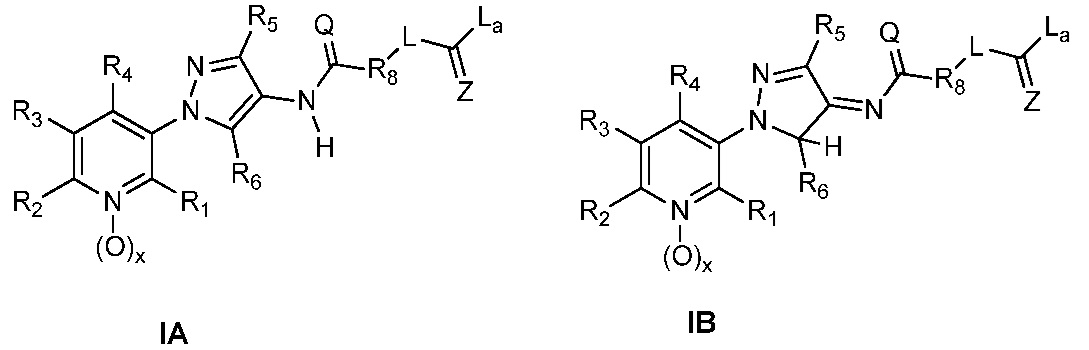
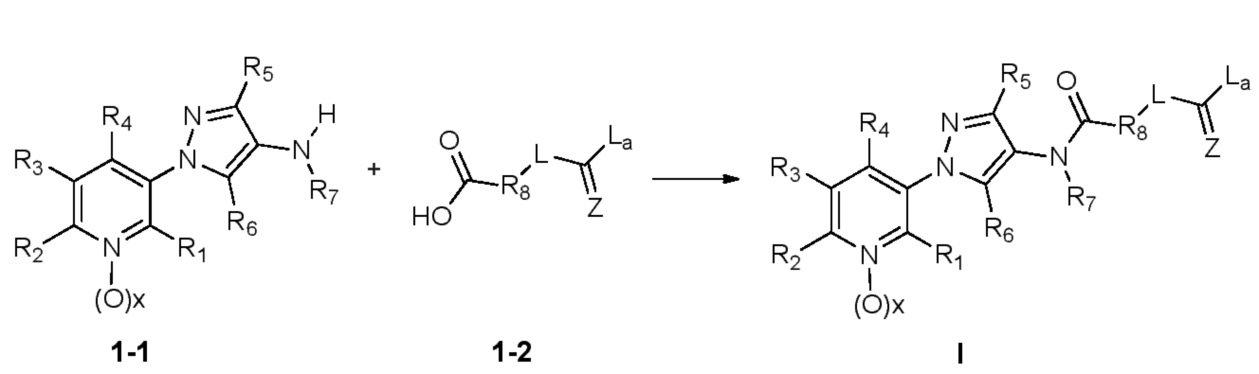
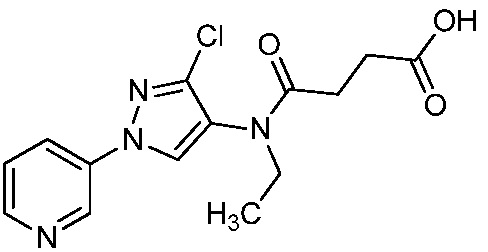
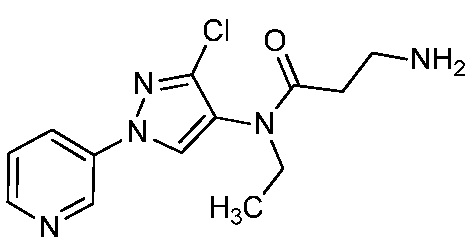
В одном варианте осуществления соединения формулы I можно получить с использованием карбоновых кислот, как показано на схеме 1.
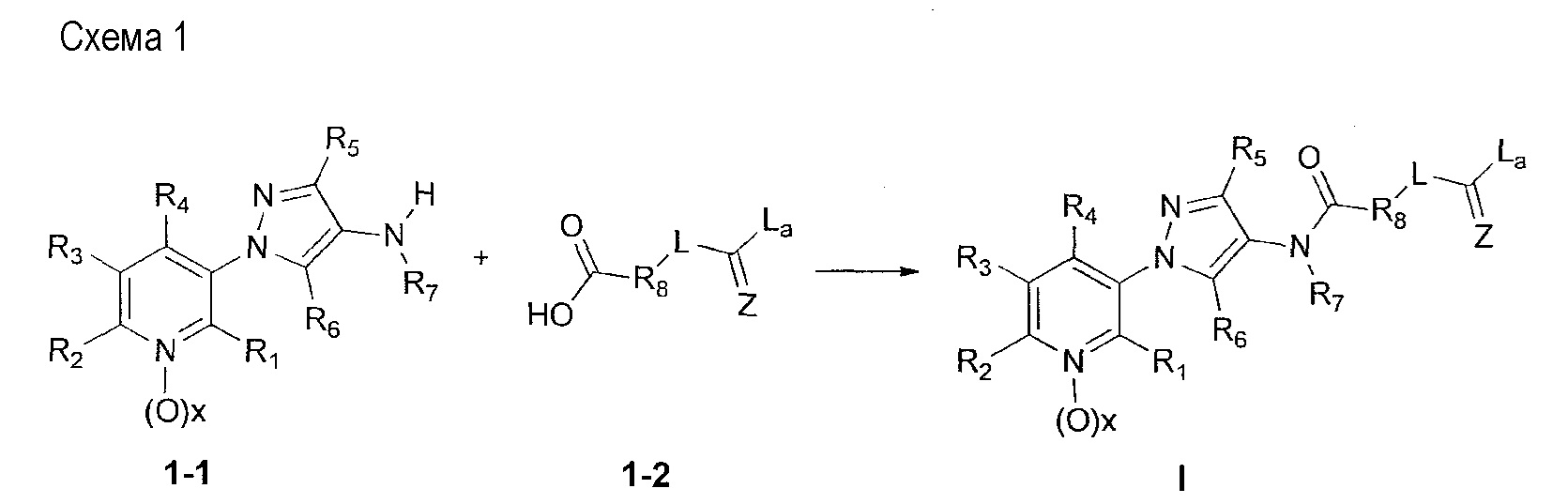
Как показано на схеме 1, соединения формулы I, в которой R1, R2, R3, R4, R5, R6, R7, L, La и x являются такими, как определено выше, можно получить по реакции соответствующего 1-(пиридин-3-ил)-1H-пиразол-4-амина формулы 1-1 (получют в соответствии с публикацией патента U.S. № 2012/0110702) и карбоновой кислоты 1-2. 1-(Пиридин-3-ил)-1H-пиразол-4-амин (1-1) можно ввести в реакцию сочетания с карбоновой кислотой (1-2) с использованием реагента сочетания, такого как 1-этил-3-(3-диметиламинопропил)карбодиимид (ЭДК) или дициклогексилкарбодиимид (ДЦК), в присутствии основания, такого как 4-диметиламинопиридин (ДМАП) или диизопропилэтиламин (ДИПЭА), в полярном апротонном растворителе, таком как N,N-диметилформамид (ДМФ), дихлорметан (CH2Cl2) или 1,2-дихлорэтан (ДХЭ), при температуре, равной от примерно -10°C до примерно 40°C, с получением соединения формулы I.
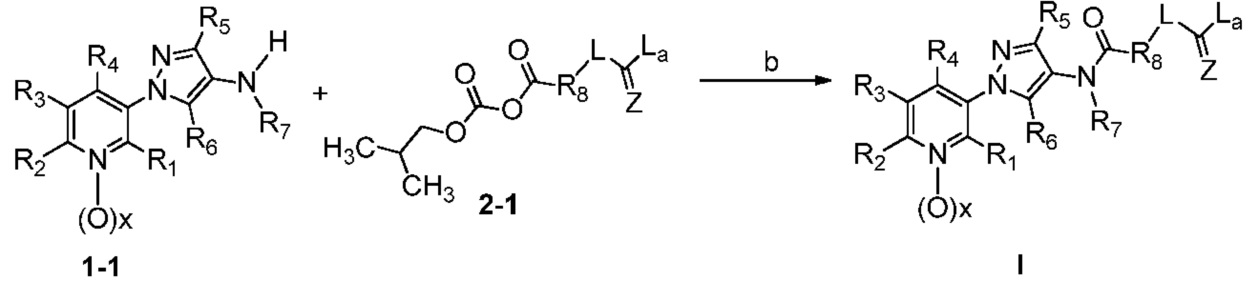
В другом варианте осуществления соединения формулы I можно получить с использованием ангидрида кислоты, как показано на схеме 2.
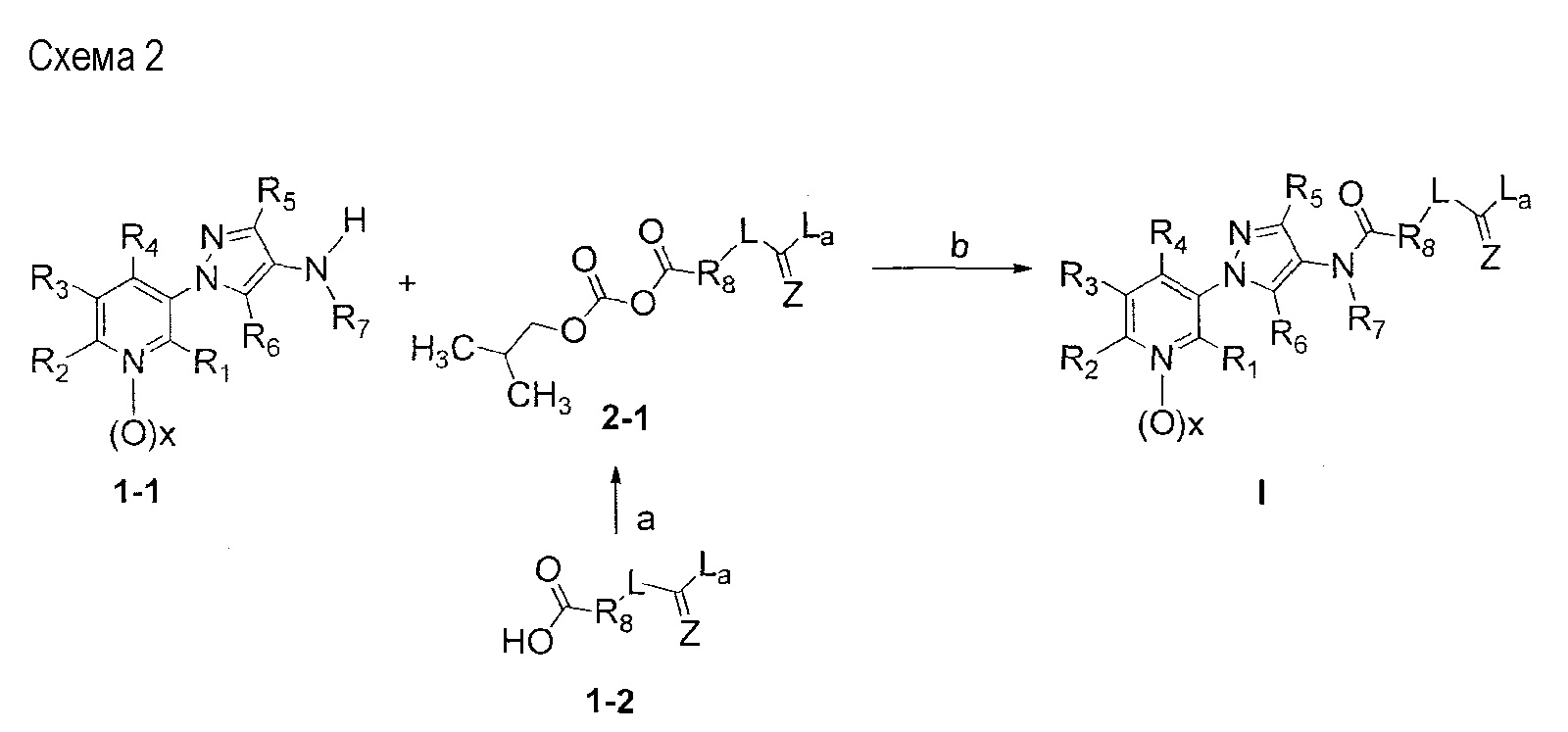
Как показано на схеме 2, соединения формулы I можно получить по реакции соответствующего 1-(пиридин-3-ил)-1H-пиразол-4-амина (1-1) и ангидрида кислоты (2-1). На стадии a схемы 2 ангидрид кислоты (2-1) можно получить из предшественника карбоновой кислоты (1-2) с использованием реагента, такого как изобутилхлорформиат, и основания, такого как ДИПЭА, в полярном апротонном растворителе, таком как CH2Cl2, при температуре, равной от примерно -78°C до примерно 30°C. На стадии b схемы 2, 1-(пиридин-3-ил)-1H-пиразол-4-амин формулы 1-1 можно ввести в реакцию сочетания с ангидридом кислоты (2-1) в полярном апротонном растворителе, таком как CH2Cl2, при температуре, равной от примерно -78°C до примерно 30°C, и получить соединения формулы I.
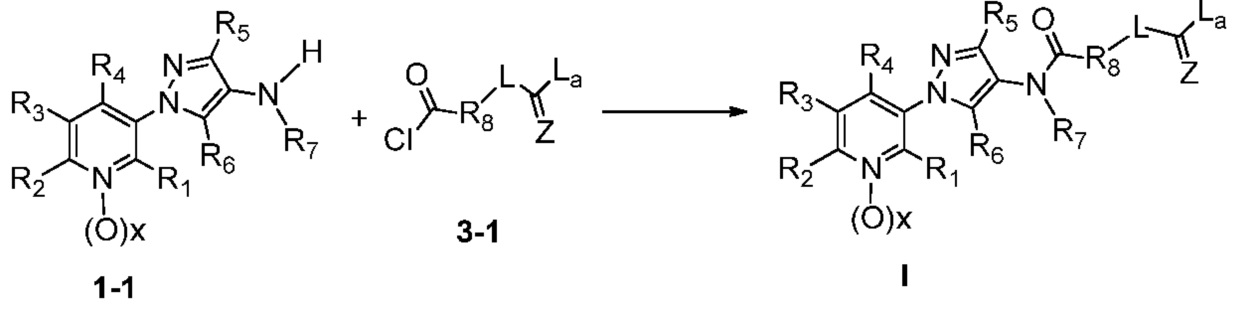
В еще одном варианте осуществления соединения формулы I можно получить с использованием хлорангидрида кислоты, как показано на схеме 3.
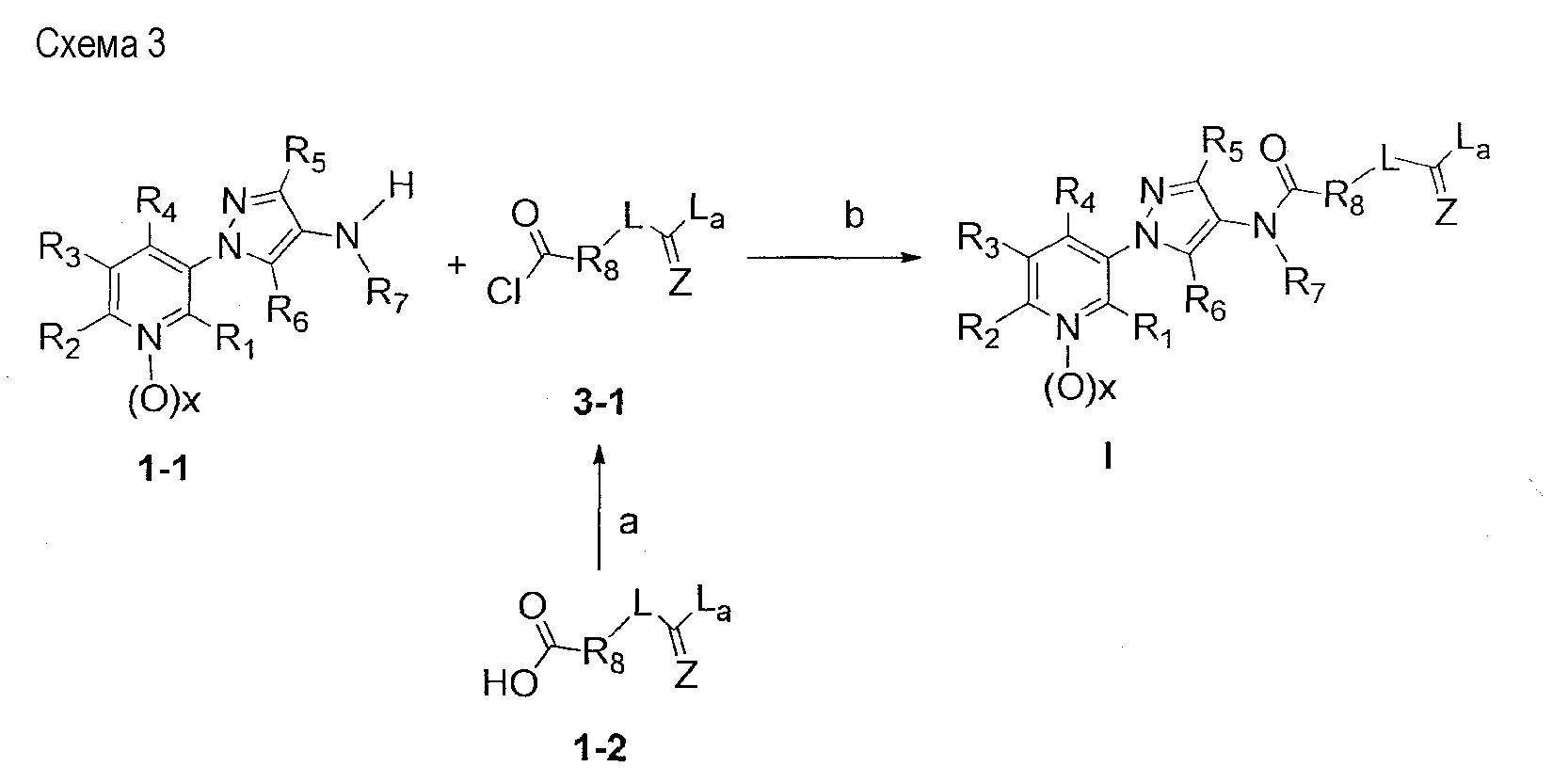
На стадии a схемы 3 карбоновые кислоты формулы 1-2 можно обработать реагентом, таким как оксалилхлорид или тионилхлорид, в присутствии инициатора, такого как диметилформамид, в апротонном растворителе, таком как CH2Cl2, при температуре, равной от примерно -20°C до примерно 60°C, и получить хлорангидрид кислоты формулы (3-1). На стадии b схемы 3 хлорангидрид кислоты (3-1) можно затем ввести в реакцию сочетания с 1-(пиридин-3-ил)-1H-пиразол-4-амин формулы 1-1 в присутствии основания, такого как диизопропилэтиламин, и апротонного растворителя, такого как дихлорэтан, при температуре, равной от примерно -20°C до примерно 60°C, и получить соединения формулы I.
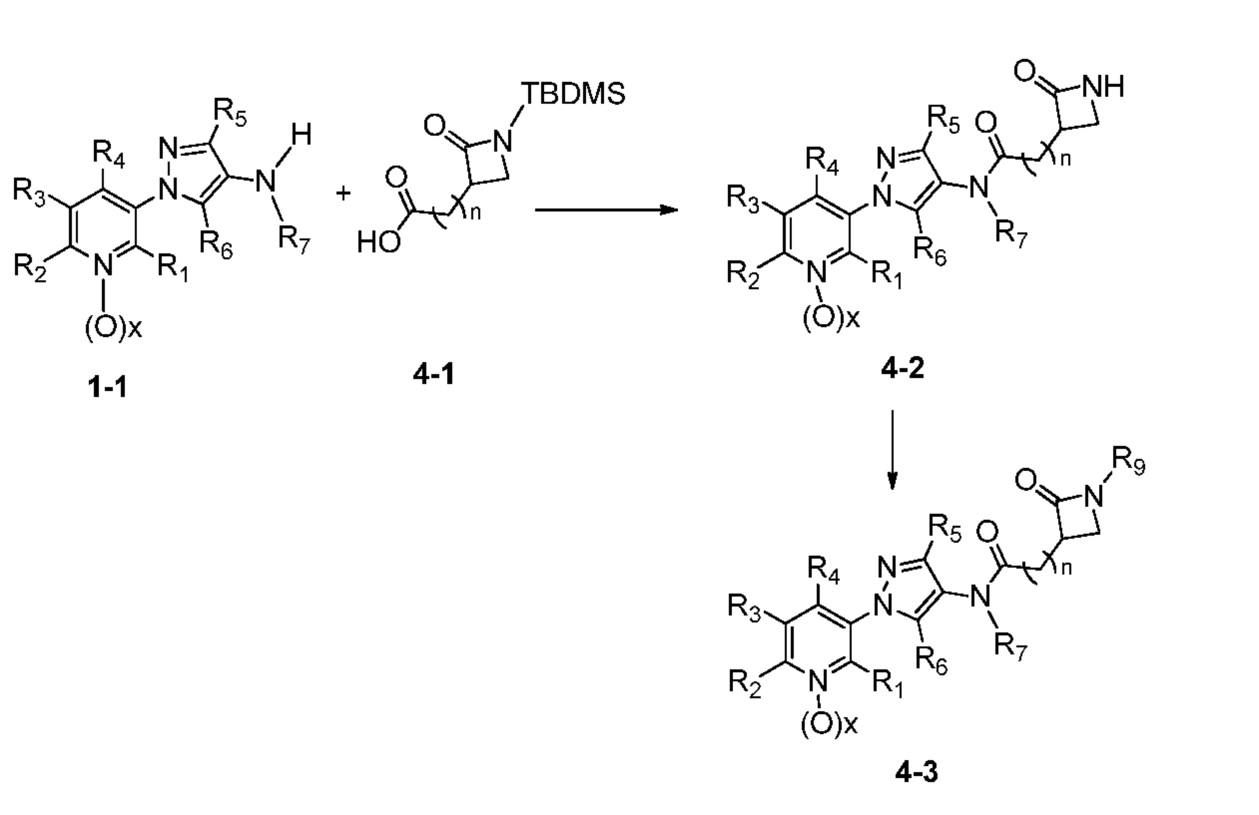
В одном варианте осуществления соединения формулы 4-3 можно получить, как показано на схеме 4.
Схема 4
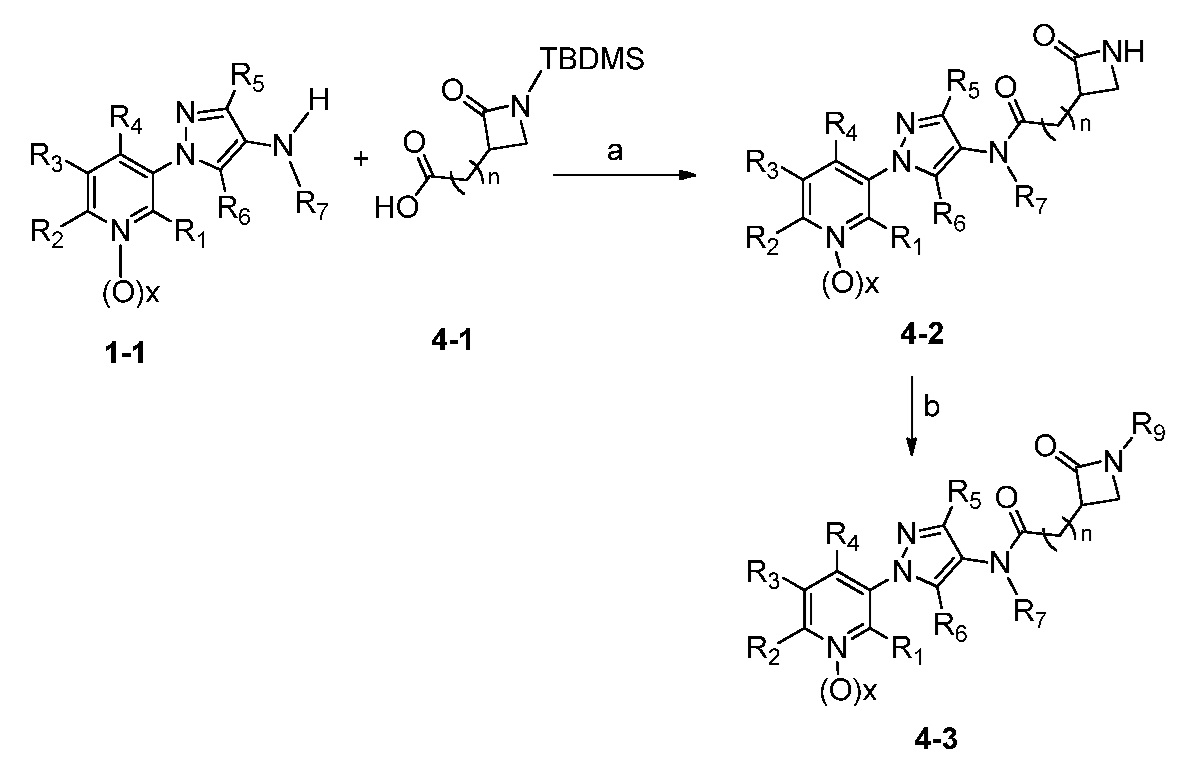
Как показано на схеме 4, соединения формулы 4-3 можно получить по реакции соответствующего 1-(пиридин-3-ил)-1H-пиразол-4-амин (1-1) (получают в соответствии с публикацией U.S. № 2012/0110702) и известной карбоновой кислоты (4-1) (Bioorganic & Medicinal Chemistry Letters, 2008, 18, 4163). На стадии a схемы 4, 1-(пиридин-3-ил)-1H-пиразол-4-амин (1-1) можно ввести в реакцию сочетания с карбоновой кислотой (4-1) в присутствии реагента сочетания, такого как ангидрид н-пропилфосфоновой кислоты (T3P®), и основания, такого как триэтиламин, в полярном апротонном растворителе, таком как этилацетат (EtOAc), при температуре, равной от примерно -10°C до примерно 80°C, и получить соединения формулы 4-2. На стадии b схемы 4 амидную группу N-H в соединениях 4-2 можно дополнительно ввести в реакцию с основанием, таким как гидрид натрия (NaH), в присутствии подходящего электрофила, такого как метилйодид, в полярном апротонном растворителе, таком как ДМФ, при температуре, равной от примерно -30°C до примерно 30°C, и получить продукты 4-3.
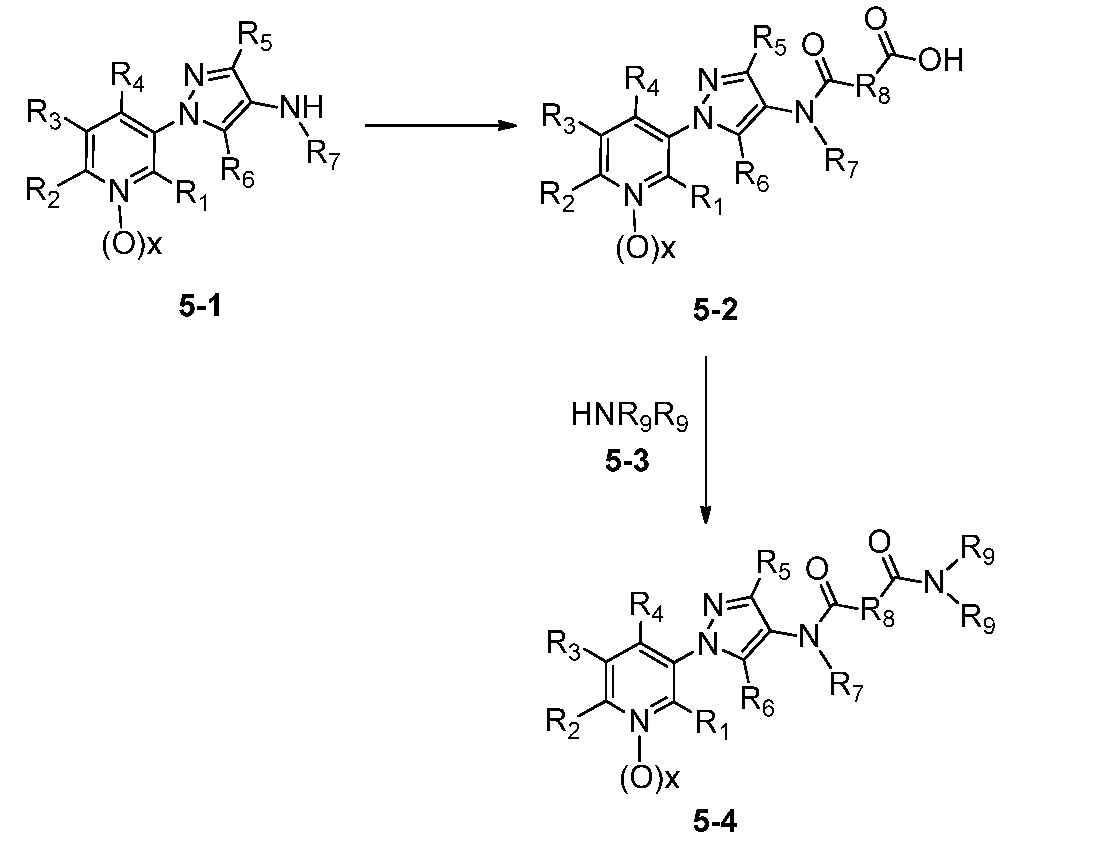
В одном варианте осуществления соединения формулы 5-4 можно получить, как показано на схеме 5.
Схема 5
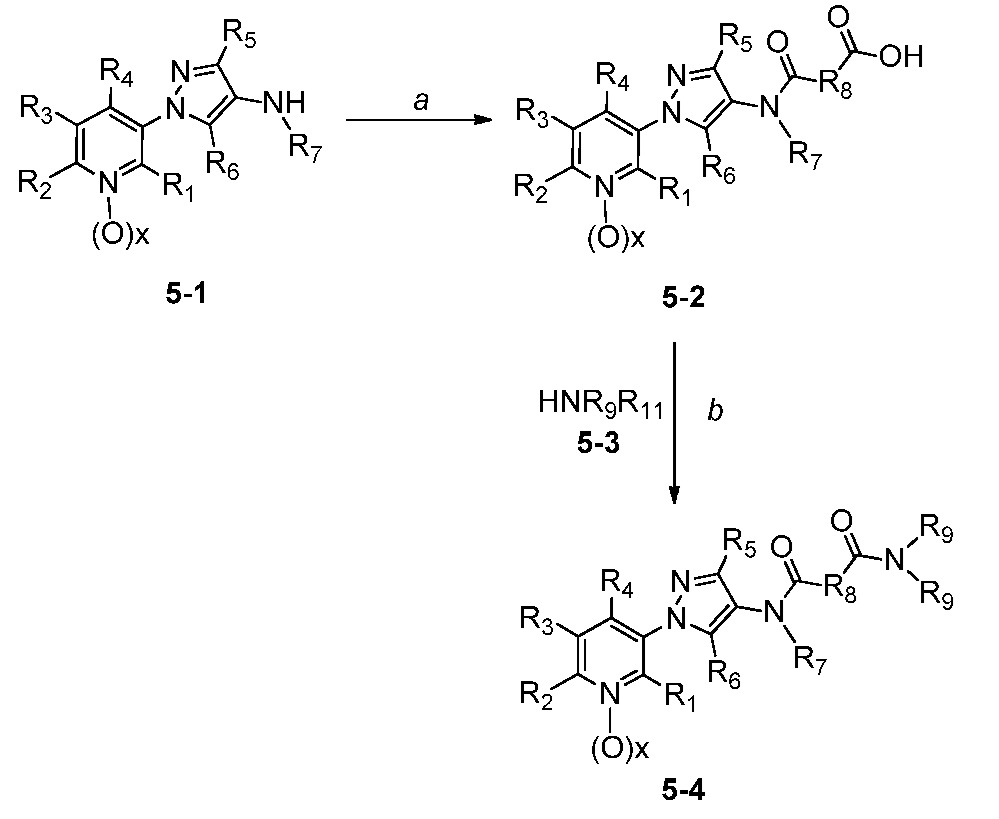
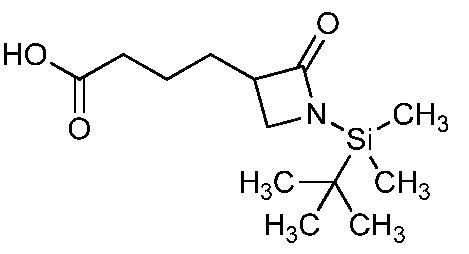
На стадии a схемы 5, 1-(пиридин-3-ил)-1H-пиразол-4-амин формулы 5-1 можно обработать подходящим электрофилом, таким как янтарный ангидрид, в присутствии амина, такого как триэтиламин, и катализатора, такого как ДМАП, в полярном апротонном растворителе, таком как ДХЭ, при температуре, равной от примерно 0°C до примерно 80°C, и получить соединения формулы 5-2. На стадии b схемы 5 соединения формулы 5-2 можно обработать подходящим амином формулы 5-3 (который может быть в форме соли) в присутствии реагента сочетания, такого как N,N'-дициклогексилкарбодиимид (ДЦК) или 1-(3-диметиламинопропил)-3-этилкарбодиимидгидрохлорид (EDCI), и основания, такого как ДМАП, в полярном апротонном растворителе, таком как диэтиловый эфир или CH2Cl2, при температуре, равной примерно 0°C до примерно 25°C, и получить продукты 5-4.
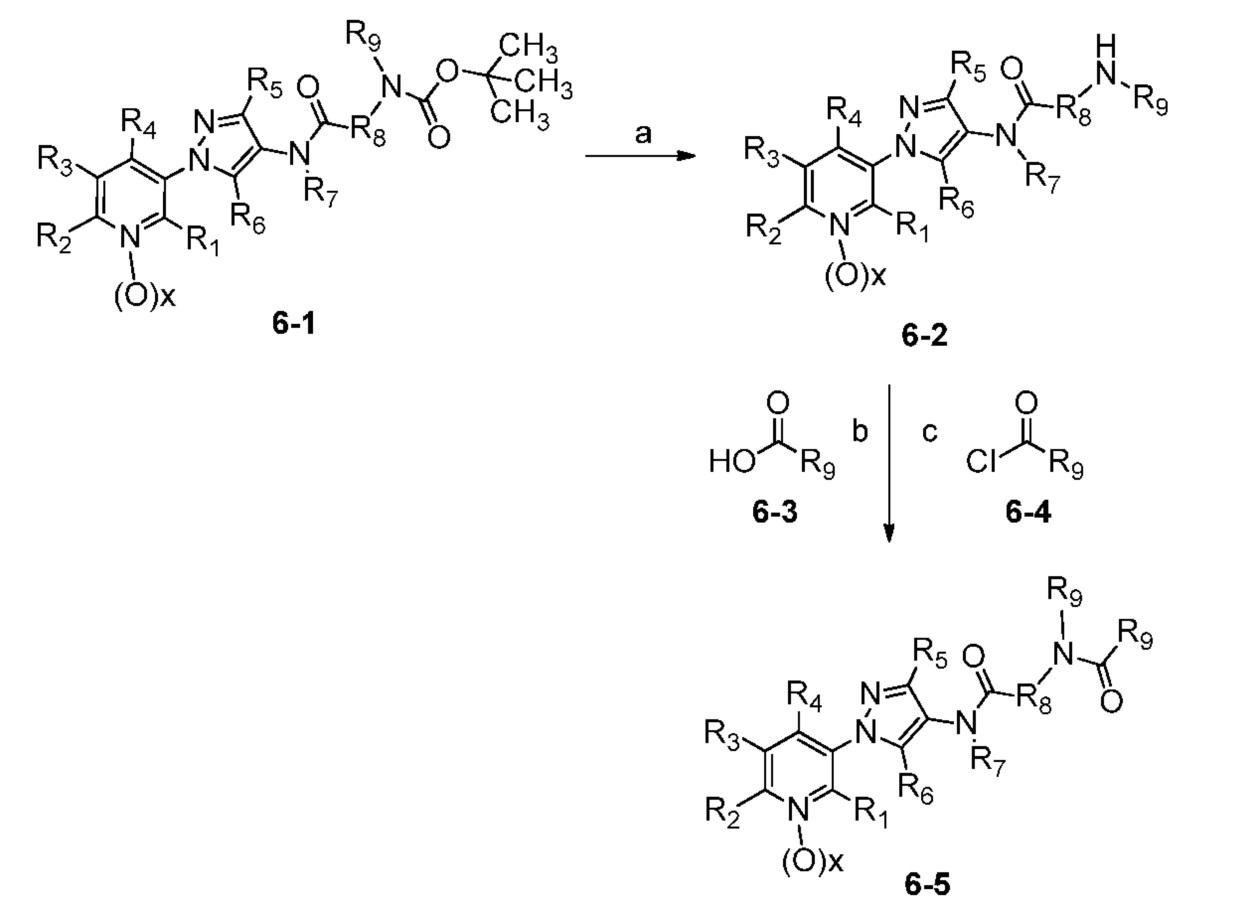
В одном варианте осуществления соединения формулы 6-5 можно получить, как показано на схеме 6.
Схема 6
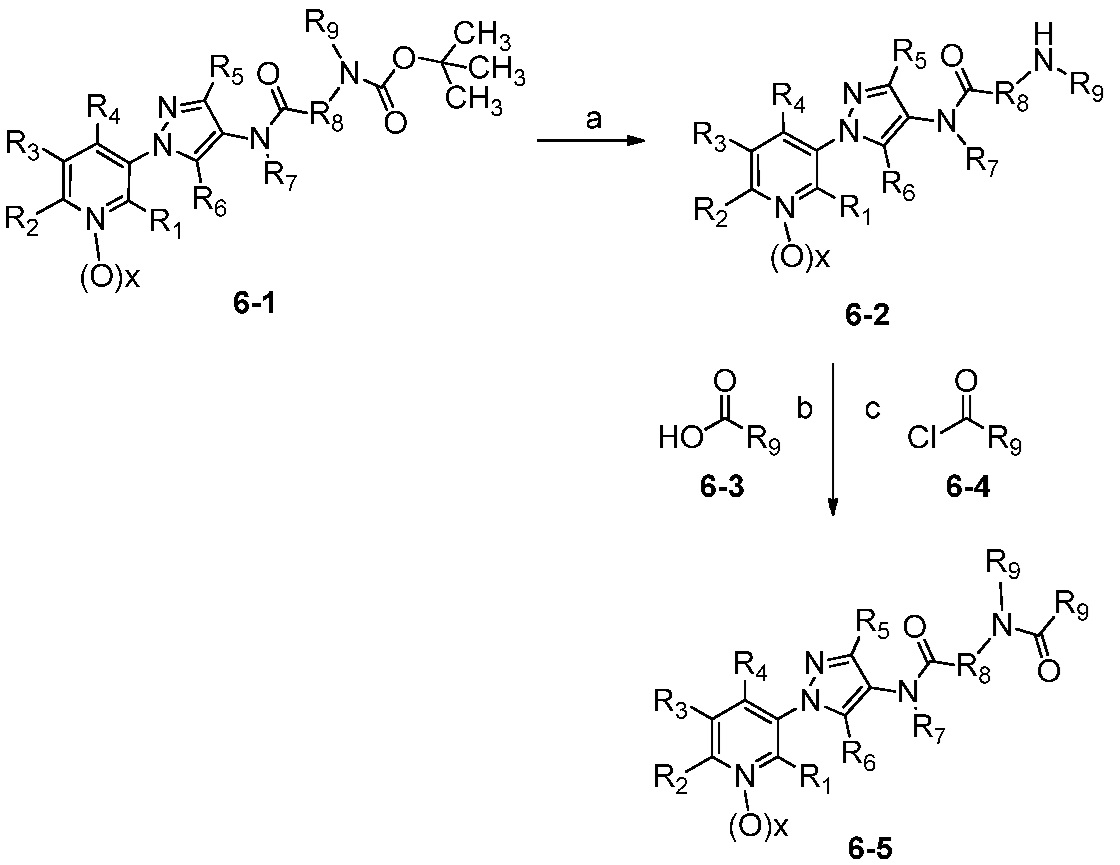
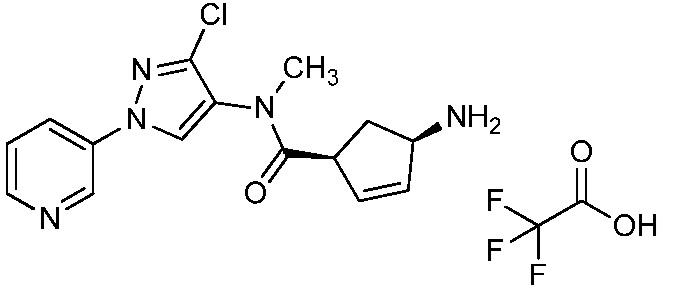
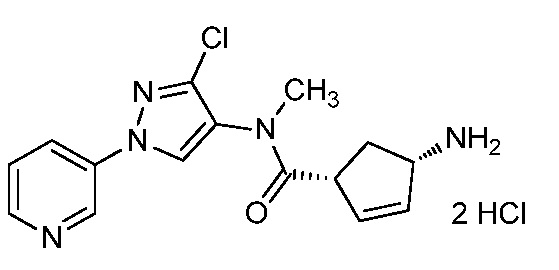
На стадии a схемы 6 содержащий защитную группу N-Boc бис-гетероциклический амид формулы 6-1 можно обработать кислотой, такой как трифторуксусная кислота (ТФК), в полярном апротонном растворителе, таком как CH2Cl2, при температуре, равной от примерно 0°C до примерно 30°C, и получить бис-гетероциклический амин формулы 6-2. На стадии b бис-гетероциклический амин (6-2) можно обработать кислотой формулы 6-3 в присутствии реагента сочетания, такого как ДЦК или EDCI, и основания, такого как ДМАП, в растворителе, таком как диэтиловый эфир или CH2Cl2, при температуре, равной от примерно 0°C до примерно 25°C, и получить продукты 6-5. Альтернативно, как показано на стадии c, бис-гетероциклический амин (6-2) можно обработать ацилхлоридом формулы 6-4 в присутствии основания, такого как ДМАП и/или пиридин, в полярном апротонном растворителе, таком как CH2Cl2, при температуре, равной от примерно 0°C до примерно 30°C, и получить продукты 6-5.
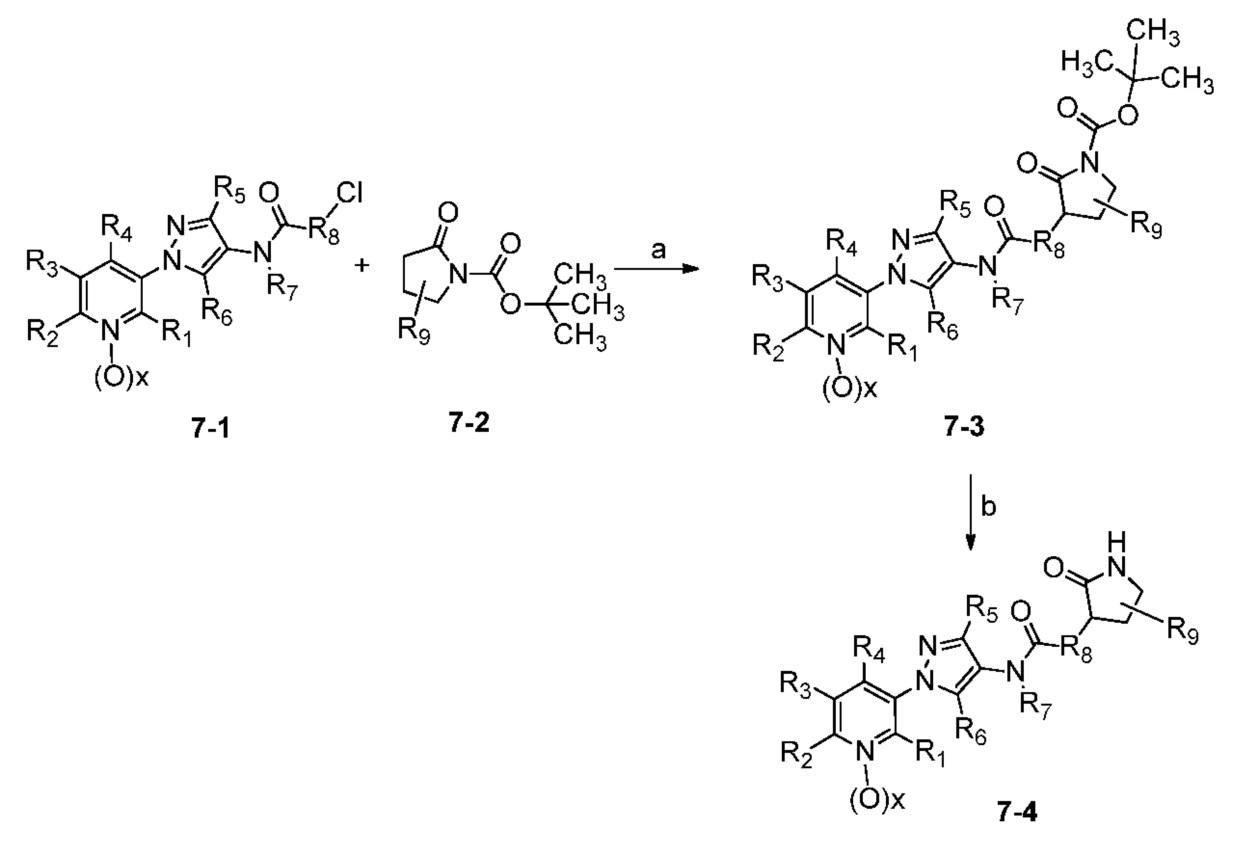
В одном варианте осуществления соединения формулы 7-4 и 7-7 можно получить, как показано на схеме 7.
Схема 7
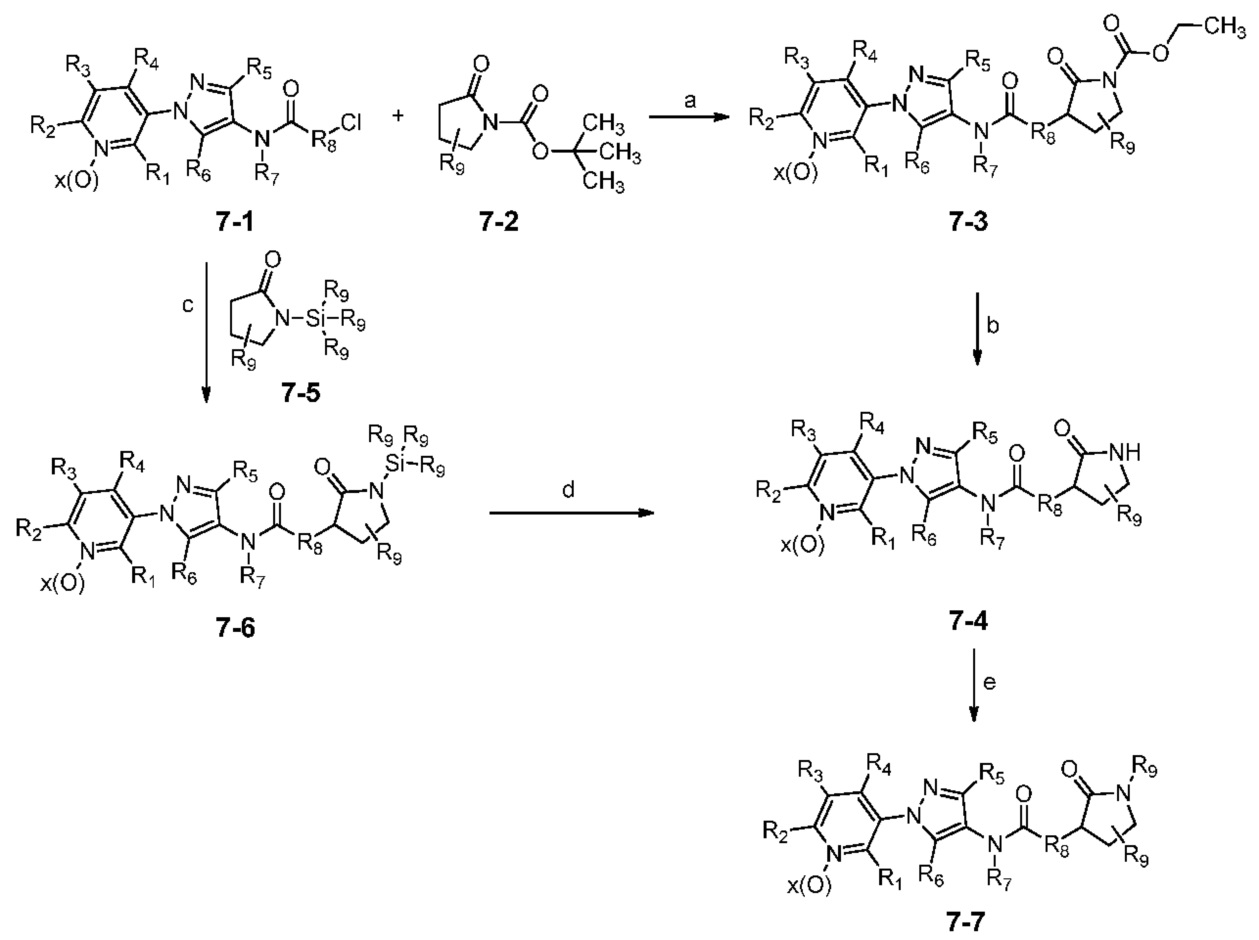
На стадии a схемы 7 соединения формулы 7-1 можно обработать содержащими защитную группу N-Boc соединениями формулы 7-2, которые можно предварительно обработать основанием, таким как бис(триметилсилил)амид лития (LiHMDS), в полярном апротонном растворителе, таком как тетрагидрофуран (ТГФ), при температуре, равной от примерно -78°C до примерно -60°C, и получить содержащий защитную группу N-Boc бис-гетероциклический амид формулы 7-3. На стадии b содержащий защитную группу N-Boc бис-гетероциклический амид формулы 7-3 затем можно обработать кислотой, такой как ТФК, в полярном апротонном растворителе, таком как CH2Cl2, при температуре, равной от примерно 0°C до примерно 30°C, и получить соединения 7-4.
Альтернативно, как показано на стадии c схемы 7, соединения формулы 7-1 можно обработать содержащими N-силильную защитную группу соединениями формулы 7-5, которые можно предварительно обработать основанием, таким как н-бутиллитий, в полярном апротонном растворителе, таком как ТГФ, при температуре, равной от примерно -78°C до примерно -60°C, и получить содержащий N-силильную защитную группу бис-гетероциклический амид формулы 7-6. На стадии d соединения формулы 7-6 можно обработать источником фторида, таким как тетрабутиламмонийфторид, в полярном апротонном растворителе, таком как ТГФ, при температуре, равной от примерно 0°C до примерно 30°C, и получить соединения 7-4. На стадии e соединения формулы 7-4 можно обработать основанием, таким как гидрид натрия, и алкилирующим реагентом, таким как 2,2,2-трифторэтилтрифторметансульфонат, в полярном апротонном растворителе, таком как ТГФ, при температуре, равной от примерно -30°C до примерно 40°C, и получить соединения 7-7.
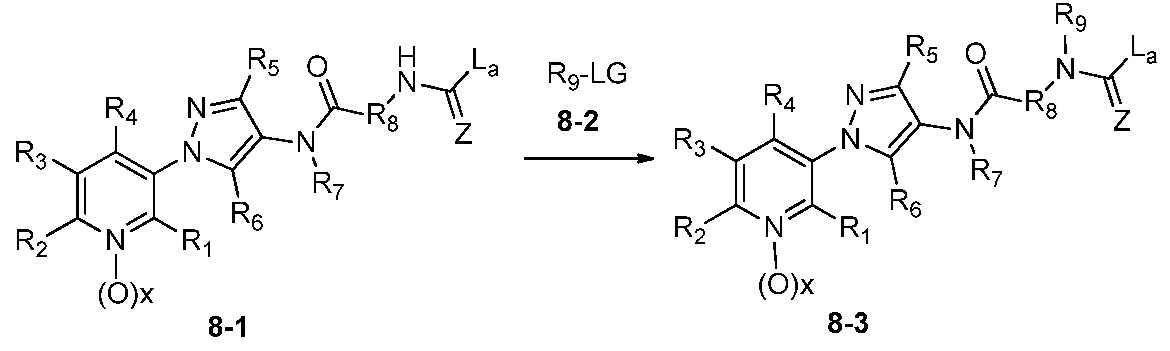
В одном варианте осуществления соединения формулы 8-3 можно получить, как показано на схеме 8.
Схема 8
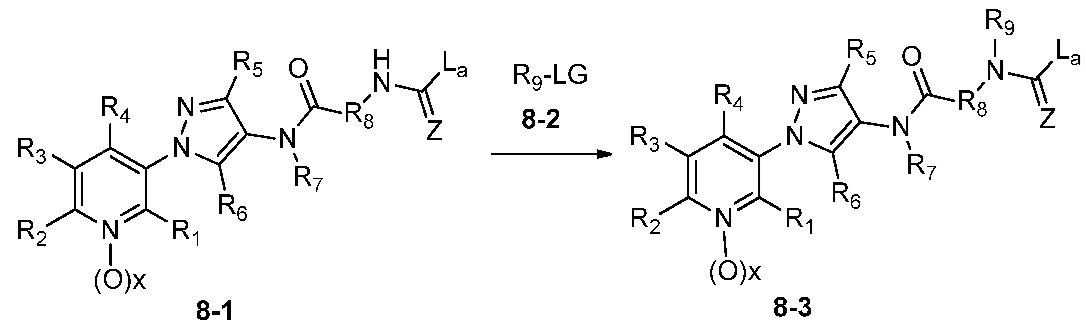
Как показано на схеме 8, соединения формулы 8-1 можно обработать подходящим основанием, таким как NaH, и последовательно обработать подходящим электрофилом R9-LG (8-2), таким как метилйодид, в котором LG означает отщепляющуюся группу, в апротонном растворителе, таком как ДМФ, при температуре, равной от примерно 0°C до примерно 30°C, и получить соединения формулы 8-3.
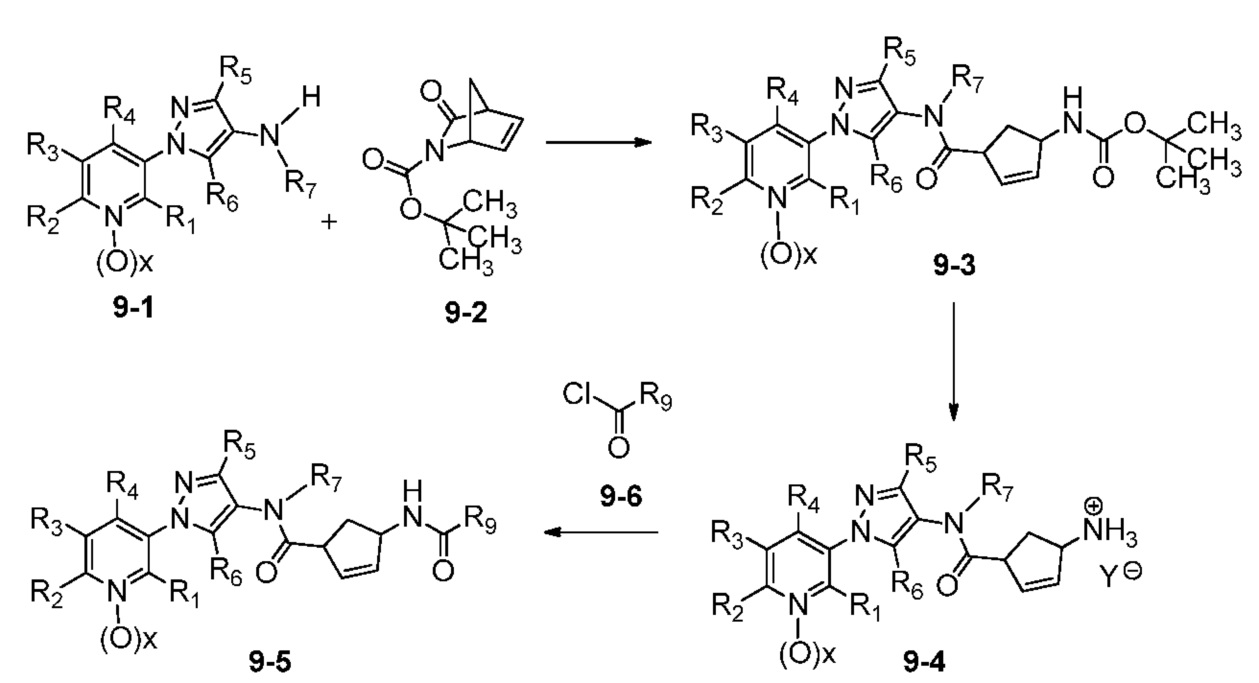
В одном варианте осуществления соединения формулы 9-5 можно получить, как показано на схеме 9.
Схема 9
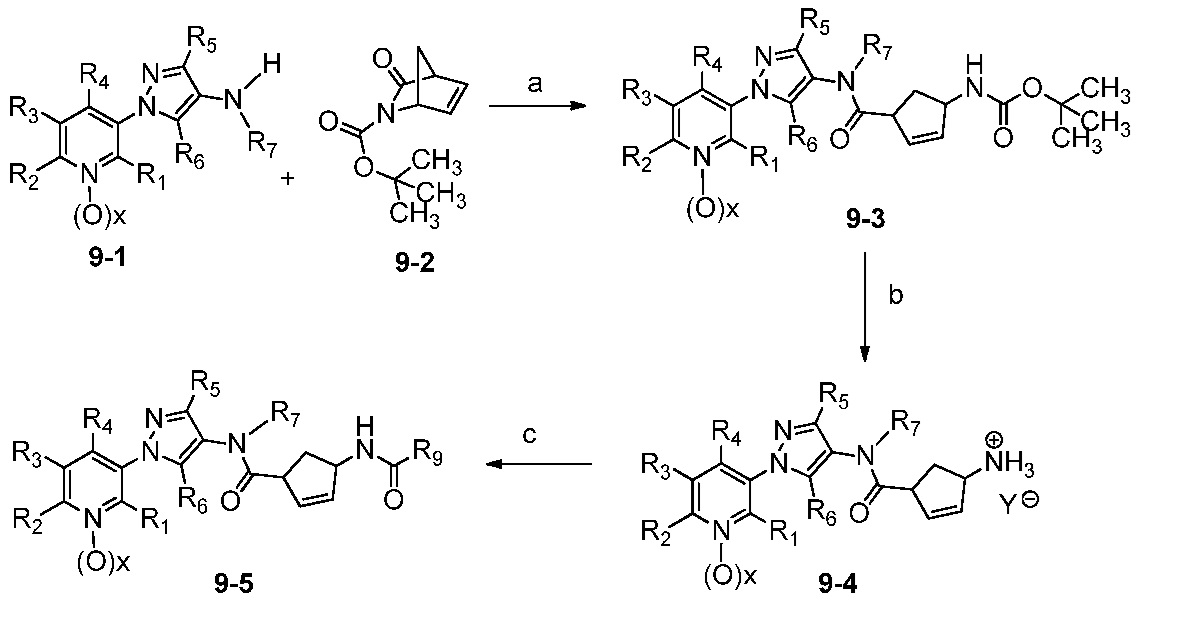
На стадии a схемы 9, 1-(пиридин-3-ил)-1H-пиразол-4-амин формулы 9-1 можно депротонировать основанием, таким как LiHMDS, и ацилировать содержащим защитную группу N-Boc имидом формулы 9-2 в полярном апротонном растворителе, таком как ТГФ, при температуре, равной от примерно -78°C до примерно 0°C, и получить содержащий защитную группу N-Boc бис-гетероциклический амид формулы 9-3.
На стадии b схемы 9 из содержащего защитную группу N-Boc бис-гетероциклического амид (9-3) можно удалить защитную группу с помощью кислоты, такой как ТФК, в полярном апротонном растворителе, таком как CH2Cl2, при температуре, равной от примерно 0°C до примерно 30°C, и получить бис-гетероциклическую соль аммония формулы 9-4, в которой Y означает противоанион, такой как трифторацетат.
На стадии c схемы 9 бис-гетероциклическую соль аммония (9-4) можно ацилировать хлорангидридом кислоты, таким как ацетилхлорид, в присутствии основания, такого как триэтиламин, в полярном апротонном растворителе, таком как CH2Cl2, при температуре, равной от примерно 0°C до примерно 60°C, и получить продукты 9-5.
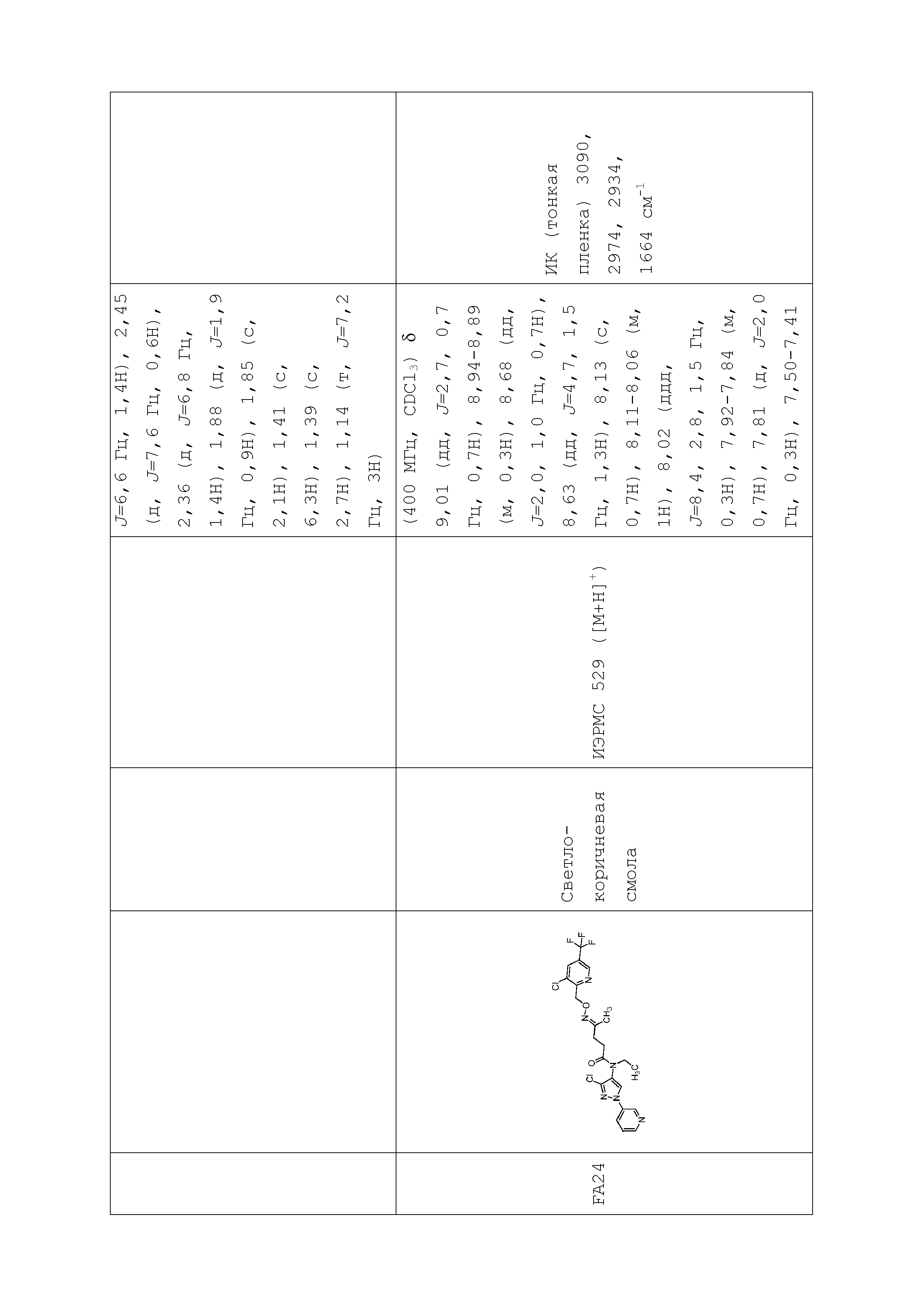
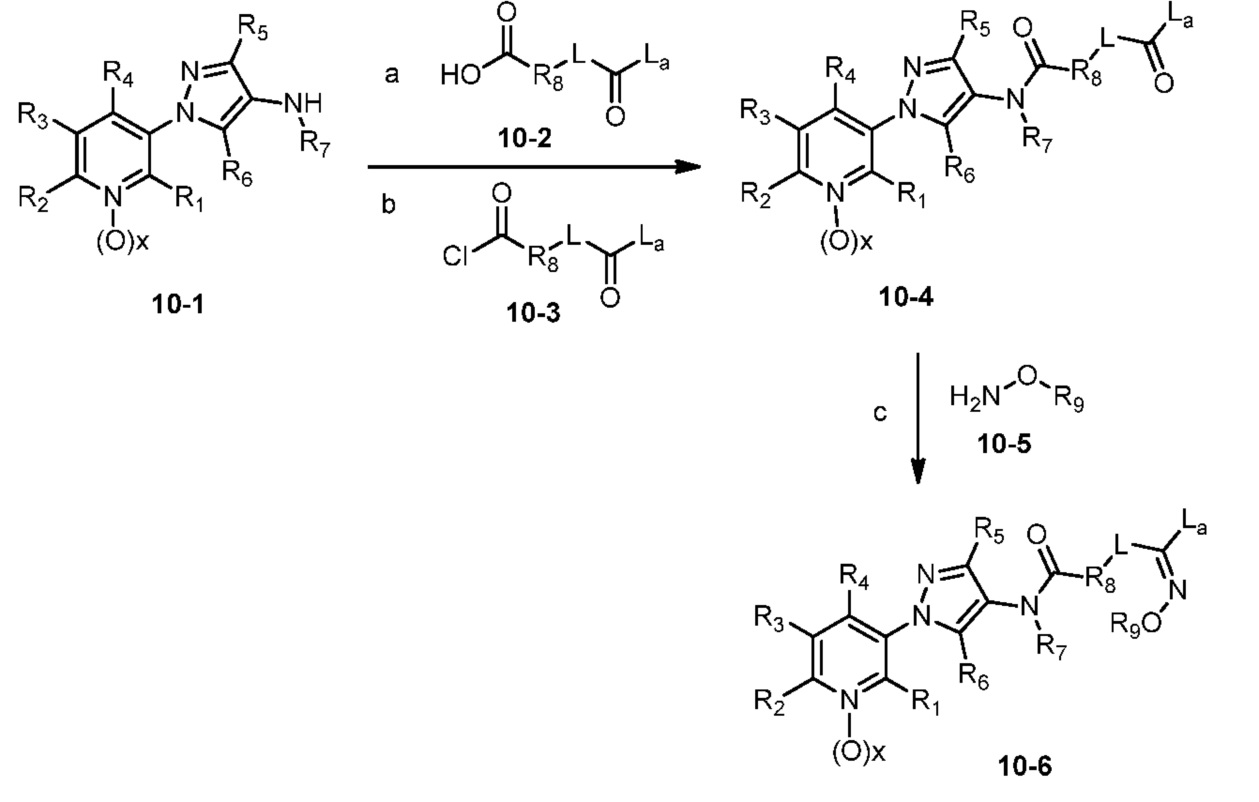
В одном варианте осуществления оксим формулы 10-6 можно получить, как показано на схеме 10.
Схема 10
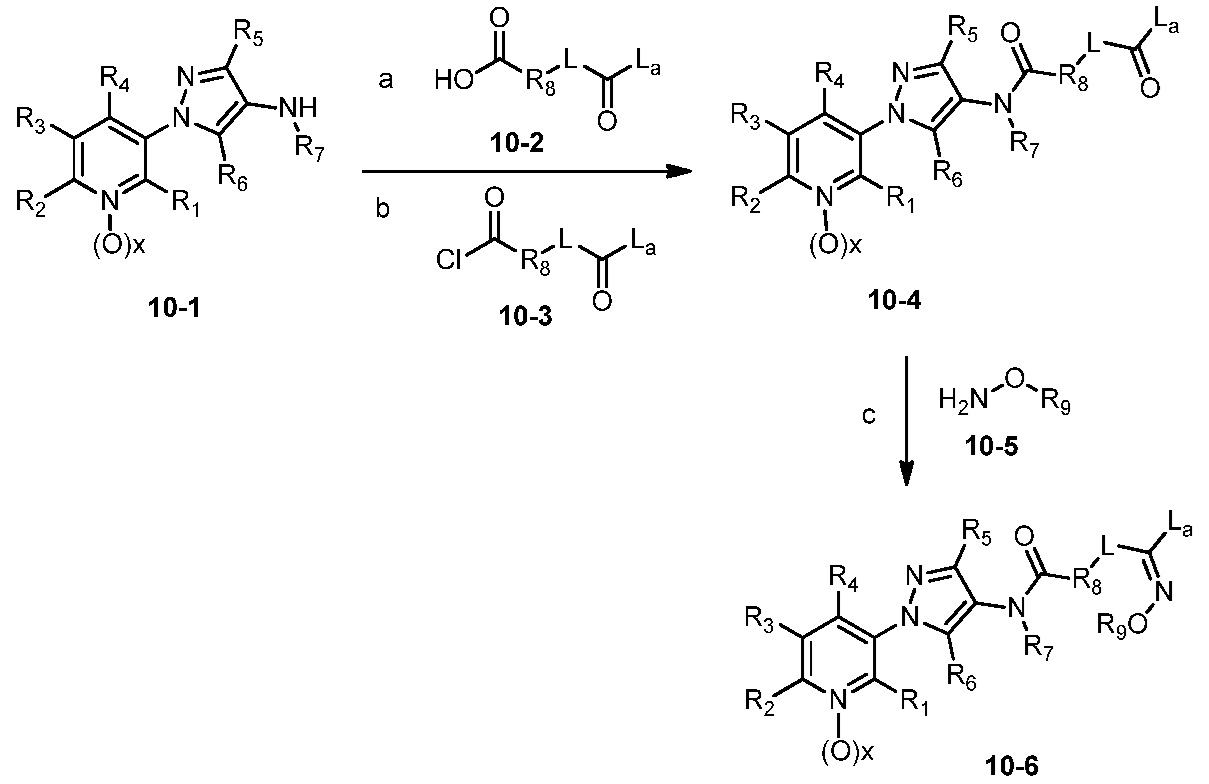
На стадии a схемы 10, 1-(пиридин-3-ил)-1H-пиразол-4-амин формулы 10-1 можно обработать кислотой формулы 10-2 в присутствии реагента сочетания, такого как ЭДК, и основания, такого как ДМАП, в полярном апротонном растворителе, таком как CH2Cl2, при температуре, равной от примерно -20°C до примерно 70°C, и получить бис-гетероциклический кетон формулы 10-4. Альтернативно, как показано на стадии b, бис-гетероциклический кетон (10-4) можно получить по реакции 1-(пиридин-3-ил)-1H-пиразол-4-амина формулы 10-1 с ацилхлоридом формулы 10-3 в присутствии основания, такого как ДМАП, в полярном апротонном растворителе, таком как CH2Cl2. На стадии c бис-гетероциклический кетон (10-4) можно ввести в реакцию с гидроксиламином формулы 10-5 или его гидрохлоридом, таким как O-метилгидроксиламингидрохлорид или изопропилгидроксиламингидрохлорид, в присутствии основания, такого как ДИПЭА, триэтиламин или пиридин, в протонном растворителе, таком как этанол (EtOH), при температуре, равной от примерно 25°C до примерно 100°C, и получить оксим бис-гетероциклического амида формулы 10-6.
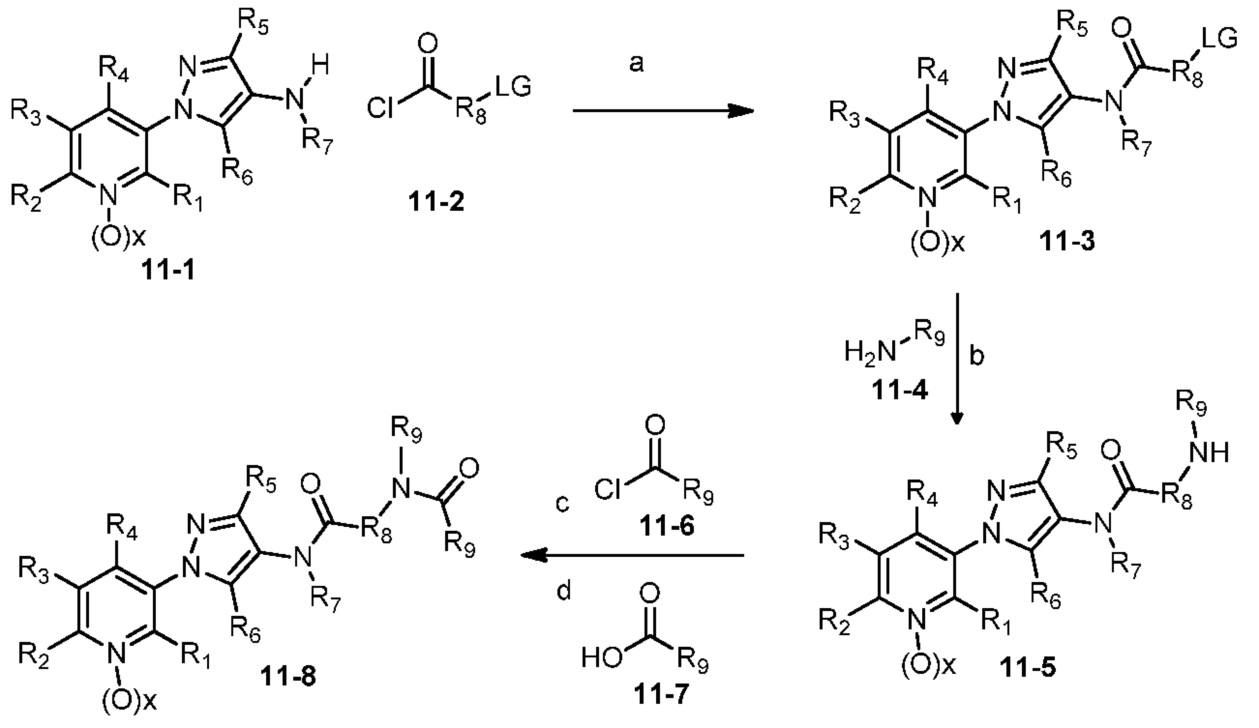
В одном варианте осуществления соединения формулы 11-8 можно получить, как показано на схеме 11.
Схема 11
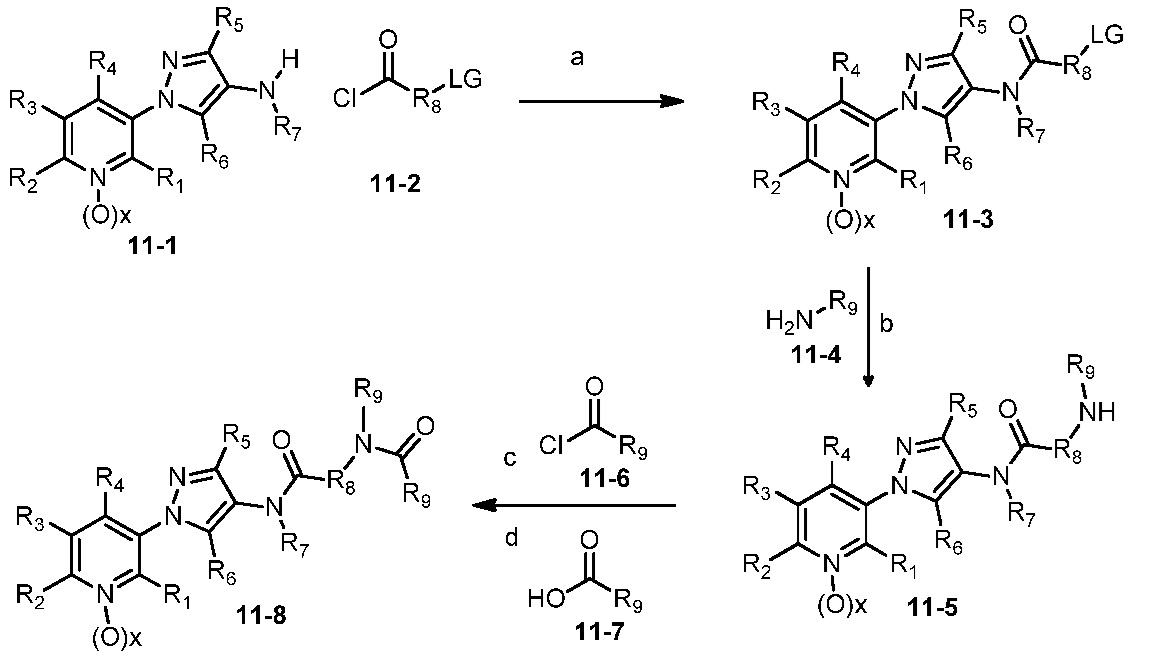
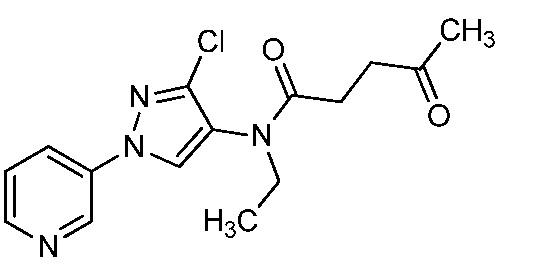
На стадии a схемы 11, 1-(пиридин-3-ил)-1H-пиразол-4-амин формулы 11-1 можно ввести в реакцию с хлорангидридом кислоты формулы 11-2, в которой LG означает отщепляющуюся группу, такую как Cl, в присутствии поглотителя протонов, такого как пропиленоксид, ДМАП или пиридин, и апротонного растворителя, такого как ДХЭ, при температуре, равной от примерно -20°C до примерно 200°C, и получить соединения формулы 11-3. На стадии b соединения формулы 11-3 можно обработать алкиламином формулы 11-4, таким как метиламин, в протонном растворителе, таком как этанол, при температуре, равной от примерно 25°C до примерно 150°C, и получить бис-гетероциклический амин формулы 11-5. На стадии c бис-гетероциклический амин формулы 11-5 можно обработать ацилхлоридом формулы 11-6, таким как ацетилхлорид или этилхлорформиат, в присутствии основания, такого как ДМАП, ДИПЭА, триэтиламин или пиридин, в апротонном растворителе, таком как ТГФ или CH2Cl2, при температуре, равной от примерно 0°C до примерно 30°C, и получить бис-гетероциклический амид формулы 11-8. Альтернативно, как показано на стадии d, бис-гетероциклический амин формулы 11-5 можно обработать карбоновой кислотой формулы 11-7 в присутствии реагента сочетания, такого как EDCI, и основания, такого как ДМАП, в полярном апротонном растворителе, таком как CH2Cl2, при температуре, равной от примерно -20°C до примерно 70°C, и получить соединения формулы 11-8.
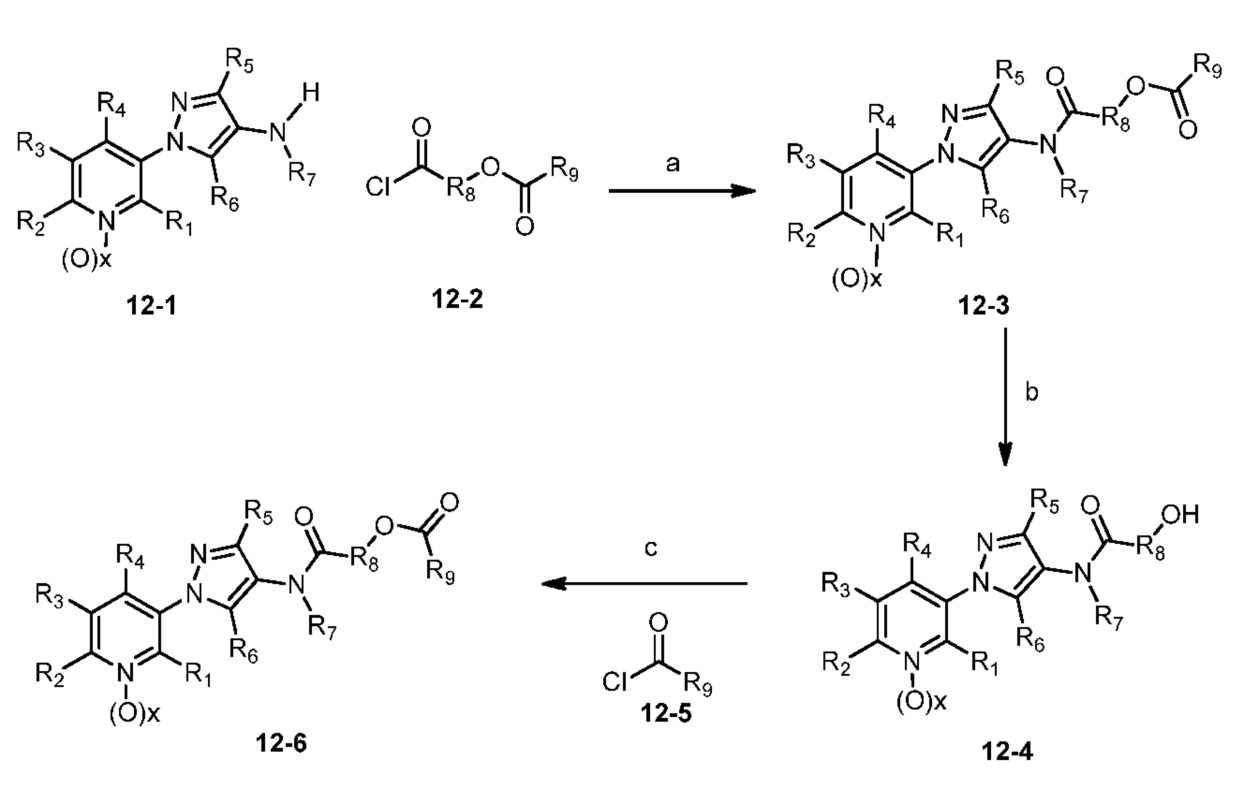
В одном варианте осуществления соединения формулы 12-6 можно получить, как показано на схеме 12.
Схема 12
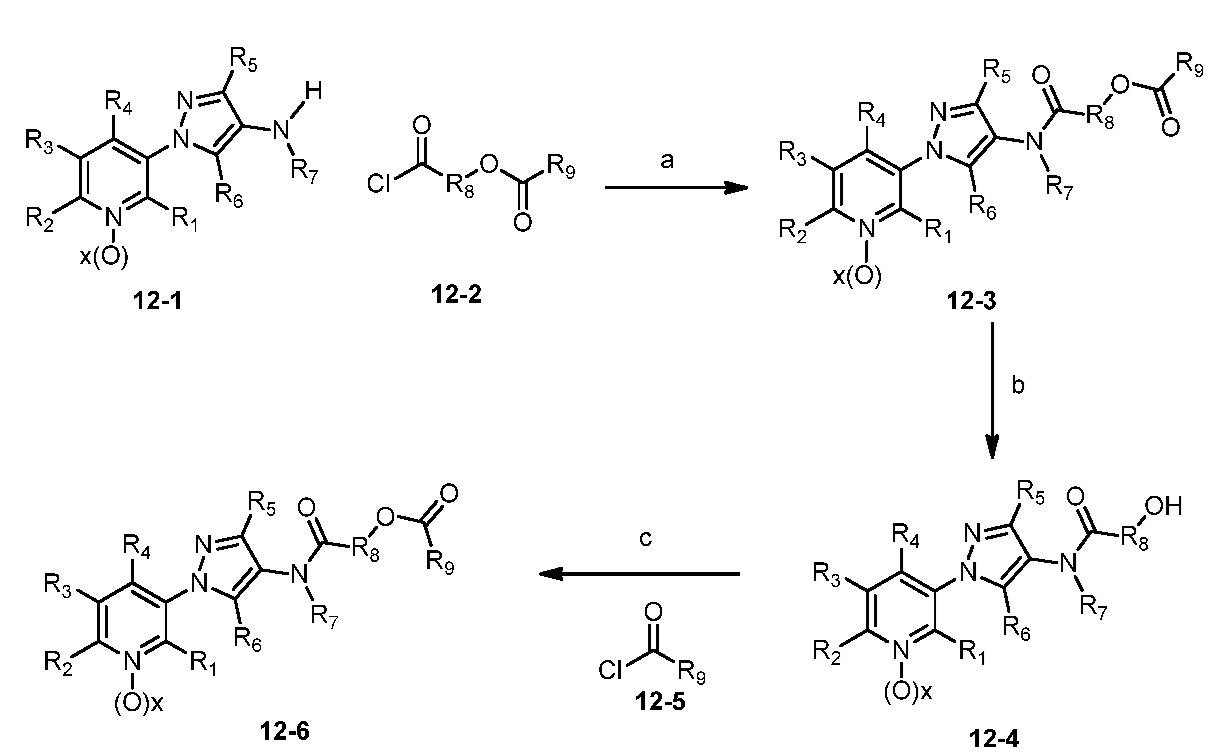
На стадии a схемы 12, 1-(пиридин-3-ил)-1H-пиразол-4-амин формулы 12-1 можно ввести в реакцию с хлорангидридом кислоты формулы 12-2 в присутствии основания, такого как ДМАП, ДИПЭА, триэтиламин или пиридин, в апротонном растворителе, таком как ТГФ или CH2Cl2, при температуре, равной от примерно 0°C до примерно 30°C, и получить бис-гетероциклические соединения формулы 12-3. Как показано на стадии b, обработкой бис-гетероциклического соединения формулы 12-3 основанием, таким как 2M водный раствор гидроксида лития, в полярном растворителе, таком как метанол (MeOH), можно получить бис-гетероциклические соединения формулы 12-4. На стадии c реакция бис-гетероциклического соединения формулы 12-4 с хлорангидридом кислоты формулы 12-5 в присутствии основания, такого как ДМАП, ДИПЭА, триэтиламин или пиридин, в апротонном растворителе, таком как ТГФ или CH2Cl2, при температуре, равной от примерно 0°C до примерно 30°C, может дать соединения формулы 12-6.
В одном варианте осуществления соединения формулы 13-4 можно получить, как показано на схеме 13.
Схема 13
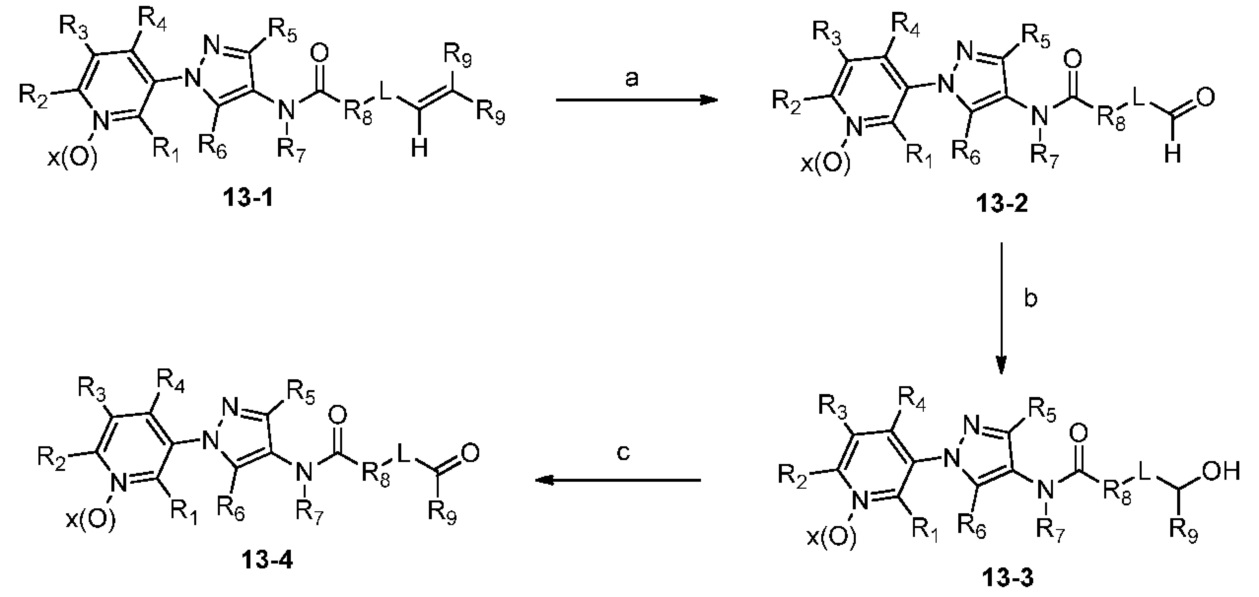
На стадии a схемы 13 соединения формулы 13-1 можно обработать окислителем, таким как озон, в полярном растворителе, таком как CH2Cl2 и метанол, при температуре, равной от примерно -78°C до примерно -40°C, и получить соединения формулы 13-2. На стадии b соединения формулы 13-2 можно обработать нуклеофилом, таким как метилмагнийбромид, в полярном апротонном растворителе, таком как ТГФ, при температуре, равной от примерно -78°C до примерно -40°C, и получить соединения формулы 13-3. На стадии c соединения формулы 13-3 можно обработать окислителем, таким как перйодинан Десса-Мартина, в полярном апротонном растворителе, таком как CH2Cl2, при температуре, равной от примерно -30°C до примерно 30°C, и получить соединения формулы 13-4.
ПЕСТИЦИДНО ПРИЕМЛЕМЫЕ КИСЛОТНО-АДДИТИВНЫЕ СОЛИ, ПРОИЗВОДНЫЕ СОЛЕЙ, СОЛЬВАТЫ, СЛОЖНОЭФИРНЫЕ ПРОИЗВОДНЫЕ, ПОЛИМОРФНЫЕ ФОРМЫ, ИЗОТОПЫ, РАДИОНУКЛИДЫ И СТЕРЕОИЗОМЕРЫ
В некоторых вариантах осуществления соединение формулы I можно получить в виде кислотно-аддитивных солей с пестицидно приемлемыми кислотами. В качестве неограничивающих примеров можно отметить, что амины могут образовать соли с хлористоводородной, бромистоводородной, серной, фосфорной, уксусной, бензойной, лимонной, малоновой, салициловой, яблочной, фумаровой, щавелевой, янтарной, винной, молочной, глюконовой, аскорбиновой, малеиновой, аспарагиновой, бензолсульфоновой, метансульфоновой, этансульфоновой, гидроксиметансульфоновой, гидроксиэтансульфоновой и трифторуксусной кислотами. Кроме того, в качестве неограничивающего примера можно отметить, что кислоты могут образовать соли, включая соли щелочных или щелочноземельных металлов и соли с аммиаком и аминами. Примеры предпочтительных катионов включают катионы натрия, калия и магния.
В некоторых вариантах осуществления соединение формулы I можно получить в виде солей. В качестве неограничивающего примера можно отметить, что соль можно получить путем взаимодействия свободного основания с достаточным количеством необходимой кислоты с получением соли. Свободное основание можно регенерировать путем обработки соли разбавленным водным раствором подходящего основания, таким как разбавленный водный раствор гидроксида натрия (NaOH), карбоната калия, аммиака и бикарбоната натрия. Например, во многих случаях пестицид, такой как 2,4-D, лучше растворяется в воде при превращении его в диметиламиновую соль.
В других вариантах осуществления соединение формулы I можно получить в виде стабильных комплексов с растворителем, так что комплекс не изменяется после удаления незакомплексованного растворителя. Эти комплексы часто называют "сольватами". Однако особенно предпочтительно получать стабильные гидраты с водой в качестве растворителя.
В некоторых вариантах осуществления соединение формулы I можно получить в виде сложноэфирных производных. Затем эти сложноэфирные производные можно использовать таким же образом, как используется настоящее изобретение, раскрытое в этом документе.
В некоторых вариантах осуществления соединение формулы I можно получить в виде различных полиморфных кристаллических форм. Полиморфизм важен для разработки сельскохозяйственных химикатов, поскольку разные полиморфные кристаллические формы или структуры одной молекулы могут обладать сильно различающимися между собой физическими характеристиками и биологической активностью.
В других вариантах осуществления соединение формулы I можно получить с различными изотопами. Особенно важны молекулы, содержащие 2H (также известный, как дейтерий) вместо 1H.
В некоторых вариантах осуществления соединение формулы I можно получить с различными радионуклидами. Особенно важны молекулы, содержащие 13C или 14C.
В некоторых вариантах осуществления соединение формулы I может существовать в виде одного или нескольких стереоизомеров. Таким образом, некоторые молекулы можно получить в виде рацемических смесей. Специалисты в данной области техники должны понимать, что один стереоизомер может быть более активным, чем другие стереоизомеры. Отдельные стереоизомеры можно получить по известным методикам селективного синтеза с использованием разделенных исходных веществ или по обычным методикам разделения. Некоторые молекулы, раскрытые в настоящем документе, могут существовать в виде двух или большего количества стереоизомеров. Различные изомеры включают геометрические изомеры, диастереоизомеры и энантиомеры. Таким образом, молекулы, раскрытые в настоящем документе, включают геометрические изомеры, рацемические смеси, отдельные стереоизомеры и оптически активные смеси. Специалисты в данной области техники должны понимать, что один стереоизомер может быть более активным, чем другие. Структуры, раскрытые в настоящем изобретении, для простоты изображены в виде только одной геометрической формы, но предполагается, что они представляют все геометрические формы молекулы.
Пестицидные композиции
В одном предпочтительном варианте осуществления пестицидная композиция содержит по меньшей мере одно соединение, выбранное из числа соединений формулы I, или любую его сельскохозяйственно приемлемую соль.
В некоторых вариантах осуществления пестицидная композиция содержит по меньшей мере одно соединение, выбранное из числа соединений формулы I, или любую его сельскохозяйственно приемлемую соль и фитологически приемлемый инертный носитель (например, твердый носитель или жидкий носитель)).
В одном варианте осуществления пестицидная композиция может дополнительно содержать по меньшей мере одну добавку, выбранную из группы, включающей поверхностно-активное вещество, стабилизатор, вещество, вызывающее рвоту, разрыхляющий агент, противовспенивающий агент, смачивающий агент, диспергирующий агент, связующий агент, красители или наполнители.
В некоторых вариантах осуществления пестицидные композиции могут находиться в форме твердого вещества. Неограничивающие примеры твердых форм могут включать порошок, дуст или гранулированные составы.
В других вариантах осуществления пестицидные композиции могут находиться в форме жидкого состава. Примеры жидких форм могут включать, но не ограничиваются только ими, дисперсию, суспензию, эмульсию или раствор в подходящем жидком носителе.
В других вариантах осуществления пестицидные композиции могут находиться в форме жидкой дисперсии, в которой соединение формулы I может быть диспергировано в воде или в другом сельскохозяйственно приемлемом жидком носителе.
В других вариантах осуществления пестицидные композиции могут находиться в форме раствора в подходящем органическом растворителе. В одном варианте осуществления инсектицидные масла, которые широко применяются в агрохимии, можно использовать в качестве органического растворителя для пестицидных композиций.
Пестицидную композицию можно использовать вместе (например, в виде композиционной смеси или путем одновременного или последовательного нанесения) с одним или несколькими соединениями, обладающих акарицидной, альгицидной, авицидной, бактерицидной, фунгицидной, гербицидной, инсектицидной, моллюскоцидной, нематоцидной, родентицидной и/или вирулицидной способностью.
Кроме того, пестицидную композицию можно использовать вместе (например, в виде композиционной смеси или путем одновременного или последовательного нанесения) с одним или несколькими соединениями, которые представляют собой антифиданты, средства для отпугивания птиц, хемостерилизаторы, антидоты гербицидов, приманки для насекомых, средства для отпугивания насекомых, средства для отпугивания млекопитающих, средства, препятствующие спариванию, активаторы растений, регуляторы роста растений и/или синергетики.
Инсектициды
Неограничивающие примеры инсектицидов, которые можно использовать в комбинации с соединением формулы I, могут включать 1,2-дихлорпропан, абамектин, ацефат, ацетамиприд, ацетион, ацетопрол, акринатрин, акрилонитрил, аланикарб, альдикарб, альдоксикарб, альдрин, аллетрин, аллосамидин, аллилоксикарб, альфа-циперметрин, альфа-экдизон, α/ρ/ω-эндосульфан, амидитион, аминокарб, амитон, амитон оксалат, амитраз, анабазин, атидатион, азадирахтин, азаметифос, азинфос-этил, азинфос-метил, азотоат, гексафторсиликат бария, бартрин, бендиокарб, бенфуракарб, бенсултап, бета-цифлутрин, бета-циперметрин, бифентрин, биоаллетрин, биоэтанометрин, биоперметрин, бистрифлурон, бура, борную кислоту, бромфенвинфос, бромоциклен, бром-DDT, бромофос, бромофос-этил, буфенкарб, бупрофезин, бутакарб, бутатиофос, бутокарбоксим, бутонат, бутоксикарбоксим, кадусафос, арсенат кальция, полисульфид кальция, камфехлор, карбанолат, карбарил, карбофуран, дисульфид углерода, тетрахлорид углерода, карбофенотион, карбосульфан, картап, гидрохлорид картапа, хлорантранилипрол, хлорбициклен, хлордан, хлордекон, хлордимеформ, гидрохлорид хлордимеформа, хлорэтоксифос, хлорфенапир, хлорфенвинфос, хлорфлуазурон, хлормефос, хлороформ, хлорпикрин, хлорфоксим, хлорпразофос, хлорпирифос, хлорпирифос-метил, хлортиофос, хромафенозид, цинерин I, цинерин II, цинерины, цисметрин, клоэтокарб, клозантел, клотианидин, ацетоарсенит меди, арсенат меди, нафтенат меди, олеат меди, кумафос, кумитоат, кротамитон, кротоксифос, круфомат, криолит, цианофенфос, цианофос, циантоат, циантранилипрол, циклетрин, циклопротрин, цифлутрин, цигалотрин, циперметрин, цифенотрин, циромазин, цитиоат, DDT, декарбофуран, дельтаметрин, демефион, демефион-O, демефион-S, деметон, деметон-метил, деметон-O, деметон-O-метил, деметон-S, деметон-S-метил, деметон-S-метилсульфон, диафентиурон, диалифос, диатомовую землю, диазинон, дикаптон, дихлофентион, дихлорвос, дикрезил, дикротофос, дицикланил, диэльдрин, дифлубензурон, дилор, димефлутрин, димефокс, диметан, диметоат, диметрин, диметилвинфос, диметилан, динекс, динекс-диклексин, динопроп, диносам, динотефуран, диофенолан, диоксабензофос, диоксакарб, диоксатион, дисульфотон, дитикрофос, d-лимонен, DNOC, DNOC-аммоний, DNOC-калий, DNOC-натрий, дорамектин, экдилстерон, эмамектин, бензоат эмамектина, EMPC, эмпентрин, эндосульфан, эндотион, эндрин, EPN, эпофенонан, эприномектин, эсдепаллетрин, эсфенвалерат, этафос, этиофенкарб, этион, этипрол, этоат-метил, этопрофос, этилформиат, этил-DDD, этилендибромид, этилендихлорид, этиленоксид, этофенпрокс, этримфос, EXD, фампур, фенамифос, феназафлор, фенхлорфос, фенетакарб, фенфлутрин, фенитротион, фенобукарб, феноксакрим, феноксикарб, фенпиритрин, фенпропатрин, фенсульфотион, фентион, фентион-этил, фенвалерат, фипронил, флоникамид, флубендиамид (дополнительно его разделенные изомеры), флукофурон, флуциклоксурон, флуцитринат, флуфенерим, флуфеноксурон, флуфенпрокс, флувалинат, фонофос, форметанат, гидрохлорид форметаната, формотион, формпаранат, гидрохлорид формпараната, фосметилан, фоспират, фостиетан, фуфенозид, фуратиокарб, фуретрин, гамма-цигалотрин, гамма-HCH, галфенпрокс, галофенозид, HCH, HEOD, гептахлор, гептенофос, гетерофос, гексафлумурон, HHDN, гидраметилнон, цианид водорода, гидропрен, хиквинкарб, имидаклоприд, имипротрин, индоксакарб, йодметан, IPSP, изазофос, изобензан, изокарбофос, изодрин, изофенфос, изофенфос-метил, изопрокарб, изопротиолан, изотиоат, изоксатион, ивермектин, жасмолин I, жасмолин II, иодфенфос, ювенильный гормон I, ювенильный гормон II, ювенильный гормон III, келеван, кинопрен, лямбда-цигалотрин, арсенат свинца, лепимектин, лептофос, линдан, лиримфос, луфенурон, литидатион, малатион, малонобен, мазидокс, мекарбам, мекарфон, меназон, меперфлутрин, мефосфолан, хлорид ртути(I), месульфенфос, метафлумизон, метакрифос, метамидофос, метидатион, метиокарб, метокротофос, метомил, метопрен, метотрин, метоксихлор, метоксифенозид, метилбромид, метилизотиоцианат, метилхлороформ, метиленхлорид, метофлутрин, метолкарб, метоксадиазон, мевинфос, мексакарбат, милбемектин, милбемициноксим, мипафокс, мирекс, молосултап, монокротофос, мономегипо, моносултап, морфотион, моксидектин, нафталофос, налед, нафталин, никотин, нифлуридид, нитенпирам, нитиазин, нитрилакарб, новалурон, новифлумурон, ометоат, оксамил, оксидеметон-метил, оксидепрофос, оксидисульфотон, пара-дихлорбензол, паратион, паратион-метил, пенфлурон, пентахлорфенол, перметрин, фенкаптон, фенотрин, фентоат, форат, фозалон, фосфолан, фосмет, фоснихлор, фосфамидон, фосфин, фоксим, фоксим-метил, пириметафос, пиримикарб, пиримифос-этил, пиримифос-метил, арсенит калия, тиоцианат калия, pp'-DDT, праллетрин, прекоцен I, прекоцен II, прекоцен III, примидофос, профенофос, профлуралин, профлутрин, промацил, промекарб, пропафос, пропетамфос, пропоксур, протидатион, протиофос, протоат, протрифенбут, пиметрозин, пираклофос, пирафлупрол, пиразофос, пиресметрин, пиретрин I, пиретрин II, пиретрины, пиридабен, пиридалил, пиридафентион, пирифлухиназон, пиримидифен, пиримитат, пирипрол, пирипроксифен, кассия, хиналфос, хиналфос-метил, хинотион, рафоксанид, ресметрин, ротенон, риания, сабадиллу, шрадан, селамектин, силафлуофен, силикагель, арсенит натрия, фторид натрия, гексафторсиликат натрия, тиоцианат натрия, софамид, спинеторам, спиносад, спиромезифен, спиротетрамат, сулкофурон, сулкофурон-натрий, сульфлурамид, сульфотеп, сульфоксафлор, сульфурилфторид, сульпрофос, тау-флувалинат, тазимкарб, TDE, тебуфенозид, тебуфенпирад, тебупиримфос, тефлубензурон, тефлутрин, темефос, TEPP, тераллетрин, тербуфос, тетрахлорэтан, тетрахлорвинфос, тетраметрин, тетраметилфлутрин, Λeto-циперметрин, тиаклоприд, тиаметоксам, тикрофос, тиокарбоксим, тиоциклам, оксалат тиоциклама, тиодикарб, тиофанокс, тиометон, тиосултап, тиосултап-динатрий, тиосултап-мононатрий, турингенсин, толфенпирад, тралометрин, трансфлутрин, трансперметрин, триаратен, триазамат, триазофос, трихлорфон, трихлорметафос-3, трихлоронат, трифенофос, трифлумурон, триметакарб, трипрен, вамидотион, ванилипрол, XMC, ксилилкарб, дзета-циперметрин или золапрофос.
Акарициды
Неограничивающие примеры акарицидов, которые можно использовать в комбинации с соединением формулы I, могут включать ацехиноцил, амидофлумет, триоксид мышьяка, азобензол, азоциклотин, беномил, беноксафос, бензоксимат, бензилбензоат, бифеназат, бинапакрил, бромпропилат, хинометионат, хлорбензид, хлорфенетол, хлорфенсон, хлорфенсульфид, хлорбензилат, хлоромебуформ, хлорометиурон, хлорпропилат, клофентезин, циенопирафен, цифлуметофен, цигексатин, дихлофлуанид, дикофол, диенохлор, дифловидазин, динобутон, динокап, динокап-4, динокап-6, диноктон, динопентон, диносульфон, динотербон, дифенилсульфон, дисульфирам, дофенапин, этоксазол, феназахин, фенбутатиноксид, фенотиокарб, фенпироксимат, фензон, фентрифанил, флуакрипирим, флуазурон, флубензимин, флуенетил, флуметрин, фторбензид, гекситиазокс, месульфен, MNAF, никкомицины, проклонол, пропаргит, хинтиофос, спиродиклофен, сульфирам, серу, тетрадифон, тетранактин, тетрасул или тиохинокс.
Нематоциды
Неограничивающие примеры нематоцидов, которые можно использовать в комбинации с соединением формулы I, могут включать 1,3-дихлорпропен, бенклотиаз, дазомет, дазомет-натрий, DBCP, DCIP, диамидафос, флуенсульфон, фостиазат, фурфураль, имициафос, изамидофос, изазофос, метам, метам-аммоний, метам-калий, метам-натрий, фосфокарб или тионазин.
Фунгициды
Неограничивающие примеры фунгицидов, которые можно использовать в комбинации с соединением формулы I, могут включать (3-этоксипропил)меркурбромид, 2-метоксиэтилмеркурхлорид, 2-фенилфенол, 8-гидроксихинолинсульфат, 8-фенилмеркуроксихинолин, ацибензолар, ацибензолар-S-метил, аципетакс, аципетакс-медь, аципетакс-цинк, альдиморф, аллиловый спирт, аметоктрадин, амисулбром, ампропилфос, анилазин, ауреофунгин, азаконазол, азитирам, азоксистробин, полисульфид бария, беналаксил, беналаксил-M, беноданил, беномил, бенхинокс, бенталурон, бентиаваликарб, бентиаваликарб-изопропил, бензалконийхлорид, бензамакрил, бензамакрилизобутил, бензаморф, бензогидроксамовую кислоту, бетоксазин, бинапакрил, бифенил, битертанол, битионол, биксафен, бластицидин-S, бордосскую жидкость, боскалид, бромуконазол, бупиримат, бургундская жидкость, бутиобат, бутиламин, полисульфид кальция, каптафол, каптан, карбаморф, карбендазим, карбоксин, карпропамид, карвон, Смесь Cheshunt, хинометионат, хлобентиазон, хлораниформетан, хлоранил, хлорфеназол, хлординитронафталин, хлоронеб, хлорпикрин, хлороталонил, хлорхинокс, хлозолинат, климбазол, клотримазол, ацетат меди, основной карбонат меди, гидроксид меди, нафтенат меди, олеат меди, оксихлорид меди, силикат меди, сульфат меди, хромат меди-цинка, крезол, куфранеб, купробам, оксид меди(I), циазофамид, циклафурамид, циклогексимид, цифлуфенамид, цимоксанил, ципендазол, ципроконазол, ципродинил, дазомет, дазомет-натрий, DBCP, дебакарб, декафентин, дегидроуксусную кислоту, дихлофлуанид, дихлон, дихлорофен, дихлозолин, диклобутразол, диклоцимет, дикломезин, дикломезин-натрий, диклоран, диэтофенкарб, диэтилпирокарбонат, дифеноконазол, дифлуметорим, диметиримол, диметоморф, димоксистробин, диниконазол, диниконазол-M, динобутон, динокап, динокап-4, динокап-6, диноктон, динопентон, диносульфон, динотербон, дифениламин, дипиритион, дисульфирам, диталимфос, дитианон, DNOC, DNOC-аммоний, DNOC-калий, DNOC-натрий, додеморф, ацетат додеморфа, бензоат додеморфа, додицин, додицин-натрий, додин, дразоксолон, эдифенфос, эпоксиконазол, этаконазол, этем, этабоксам, этиримол, этоксихин, этилмеркур-2,3-дигидроксипропилмеркаптид, этилмеркурацетат, этилмеркурбромид, этилмеркурхлорид, этилмеркурфосфат, этридиазол, фамоксадон, фенамидон, фенаминосульф, фенапанил, фенаримол, фенбуконазол, фенфурам, фенгексамид, фенитропан, феноксанил, фенпиклонил, фенпропидин, фенпропиморф, фентин, хлорид фентина, гидроксид фентина, фербам, феримзон, флуазинам, флудиоксонил, флуметовер, флуморф, флуопиколид, флуопирам, фторимид, флуотримазол, флуоксастробин, флухинконазол, флусилазол, флусульфамид, флутанил, флутоланил, флутриафол, флуксапироксад, фолпет, формальдегид, фосетил, фосетилалюминий, фуберидазол, фуралаксил, фураметпир, фуркарбанил, фурконазол, фурконазол-цис, фурфураль, фурмециклокс, фурофанат, глиодин, гризеофульвин, гуазатин, галакринат, гексахлорбензол, гексахлорбутадиен, гексаконазол, гексилтиофос, гидраргафен, гимексазол, имазалил, имазалилнитрат, имазалилсульфат, имибенконазол, иминоктадин, иминоктадинтриацетат, иминоктадинтриальбезилат, йодметан, ипконазол, ипробенфос, ипродион, ипроваликарб, изопротиолан, изопиразам, изотианил, изоваледион, касугамицин, крезоксим-метил, манкоппер, манкозеб, мандипропамид, манеб, мебенил, мекарбинзид, мепанипирим, мепронил, мептилдинокап, хлорид ртути(II), оксид ртути(II), хлорид ртути(I), металаксил, металаксил-M, метам, метам-аммоний, метам-калий, метам-натрий, метазоксолон, метконазол, метасульфокарб, метфуроксам, метилбромид, метилизотиоцианат, метилмеркурбензоат, метилмеркурдициандиамид, метилмеркурпентахлорфеноксид, метирам, метоминостробин, метрафенон, метсульфовакс, мильнеб, миклобутанил, миклозолин, N-(этилмеркур)-п-толуолсульфонанилид, набам, натамицин, нитростирол, нитротал-изопропил, нуаримол, OCH, октилинон, офурац, орисастробин, оксадиксил, оксин-коппер, окспоконазол, фумарат окспоконазола, оксикарбоксин, перфуразоат, пенконазол, пенцикурон, пенфлуфен, пентахлорфенол, пентиопирад, фенилмеркурмочевина, фенилмеркурацетат, фенилмеркурхлорид, фенилмеркурпроизводное пирокатехина, фенилмеркурнитрат, фенилмеркурсалицилат, фосдифен, фталид, пикоксистробин, пипералин, поликарбамат, полиоксины, полиоксорим, полиоксорим-цинк, азид калия, полисульфид калия, тиоцианат калия, пробеназол, прохлораз, процимидон, пропамокарб, гидрохлорид пропамокарба, пропиконазол, пропинеб, проквиназид, протиокарб, гидрохлорид протиокарба, протиоконазол, пиракарболид, пираклостробин, пираклостробин, пираметостробин, пираоксистробин, пиразофос, пирибенкарб, пиридинитрил, пирифенокс, пириметанил, пириофенон, пирохилон, пироксихлор, пироксифур, хинацетол, сульфат хинацетола, хиназамид, хинконазол, хиноксифен, квинтоцен, рабензазол, салициланилид, седаксан, силтиофам, симеконазол, азид натрия, ортофенилфеноксид натрия, пентахлорфеноксид натрия, полисульфид натрия, спироксамин, стрептомицин, серу, сультропен, TCMTB, тебуконазол, тебуфлохин, теклофталам, текназен, текорам, тетраконазол, тиабендазол, тиадифтор, тициофен, тифлузамид, тиохлорфенфим, тиомерсал, тиофанат, тиофанат-метил, тиохинокс, тирам, тиадинил, тиоксимид, толклофос-метил, толилфлуанид, толилмеркурацетат, триадимефон, триадименол, триамифос, триаримол, триазбутил, триазоксид, трибутилоловооксид, трихламид, трициклазол, тридеморф, трифлоксистробин, трифлумизол, трифорин, тритиконазол, униконазол, униконазол-P, валидамицин, валифеналат, винклозолин, зариламид, нафтенат цинка, зинеб, зирам или зоксамид.
Гербициды
Неограничивающие примеры гербицидов, которые можно использовать в комбинации с соединением формулы I, могут включать 2,3,6-TBA, 2,3,6-TBA-диметиламмоний, 2,3,6-TBA-натрий, 2,4,5-T, 2,4,5-T-2-бутоксипропил, 2,4,5-T-2-этилгексил, 2,4,5-T-3-бутоксипропил, 2,4,5-TB, 2,4,5-T-бутометил, 2,4,5-T-бутотил, 2,4,5-T-бутил, 2,4,5-T-изобутил, 2,4,5-T-изоктил, 2,4,5-T-изопропил, 2,4,5-T-метил, 2,4,5-T-пентил, 2,4,5-T-натрий, 2,4,5-T-триэтиламмоний, 2,4,5-T-троламин, 2,4-D, 2,4-D-2-бутоксипропил, 2,4-D-2-этилгексил, 2,4-D-3-бутоксипропил, 2,4-D-аммоний, 2,4-DB, 2,4-DB-бутил, 2,4-DB-диметиламмоний, 2,4-DB-изоктил, 2,4-DB-калий, 2,4-DB-натрий, 2,4-D-бутотил, 2,4-D-бутил, 2,4-D-диэтиламмоний, 2,4-D-диметиламмоний, 2,4-D-диоламин, 2,4-D-додециламмоний, 2,4-DEB, 2,4-DEP, 2,4-D-этил, 2,4-D-гептиламмоний, 2,4-D-изобутил, 2,4-D-изоктил, 2,4-D-изопропил, 2,4-D-изопропиламмоний, 2,4-D-литий, 2,4-D-мептил, 2,4-D-метил, 2,4-D-октил, 2,4-D-пентил, 2,4-D-калий, 2,4-D-пропил, 2,4-D-натрий, 2,4-D-тефурил, 2,4-D-тетрадециламмоний, 2,4-D-триэтиламмоний, 2,4-D-трис(2-гидроксипропил)аммоний, 2,4-D-троламин, 3,4-DA, 3,4-DB, 3,4-DP, 4-CPA, 4-CPB, 4-CPP, ацетохлор, ацифлюорфен, ацифлюорфен-метил, ацифлюорфен-натрий, аклонифен, акролеин, алахлор, аллидохлор, аллоксидим, аллоксидим-натрий, аллиловый спирт, алорак, аметридион, аметрин, амбузин, амикарбазон, амидосульфурон, аминоциклопирахлор, аминоциклопирахлорметил, аминоциклопирахлор-калий, аминопиралид, аминопиралид-калий, аминопиралид-трис(2-гидроксипропил)аммоний, амипрофос-метил, амитрол, сульфамат аммония, анилофос, анисурон, асулам, асулам-калий, асулам-натрий, атратон, атразин, азафенидин, азимсульфурон, азипротрин, барбан, BCPC, бефлубутамид, беназолин, беназолиндиметиламмоний, беназолин-этил, беназолин-калий, бенкарбазон, бенфлуралин, бенфуресат, бенсульфурон, бенсульфурон-метил, бенсулид, бентазон, бентазон-натрий, бензадокс, бензадокс-аммоний, бензфендизон, бензипрам, бензобициклон, бензофенап, бензофтор, бензоилпроп, бензоилпроп-этил, бензтиазурон, бициклопирон, бифенокс, биланафос, биланафос-натрий, биспирибак, биспирибак-натрий, бура, бромацил, бромацил-литий, бромацилнатрий, бромбонил, бромобутид, бромфеноксим, бромоксинил, бромоксинилбутират, бромоксинилгептаноат, бромоксинилоктаноат, бромоксинилкалий, бромпиразон, бутахлор, бутафенацил, бутамифос, бутенахлор, бутидазол, бутиурон, бутралин, бутроксидим, бутурон, бутилат, какодиловую кислоту, кафенстрол, хлорат кальция, цианамид кальция, камбендихлор, карбасулам, карбетамид, карбоксазол, карфентразон, карфентразон-этил, CDEA, CEPC, хлометоксифен, хлорамбен, хлорамбен-аммоний, хлорамбен-диоламин, хлорамбен-метил, хлорамбен-метиламмоний, хлорамбен-натрий, хлоранокрил, хлоразифоп, хлоразифоп-пропаргил, хлоразин, хлорбромурон, хлорбуфам, хлорэтурон, хлорфенак, хлорфенак-натрий, хлорфенпроп, хлорфенпроп-метил, хлорфлуразол, хлорфлуренол, хлорфлуренол-метил, хлоридазон, хлоримурон, хлоримурон-этил, хлорнитрофен, хлоропон, хлортолурон, хлороксурон, хлороксинил, хлорпрокарб, хлорпрофам, хлорсульфурон, хлортал, хлортал-диметил, хлортал-монометил, хлортиамид, цинидон-этил, цинметилин, циносульфурон, цисанилид, клетодим, клиодинат, клодинафоп, клодинафоп-пропаргил, клофоп, клофоп-изобутил, кломазон, кломепроп, клопроп, клопроксидим, клопиралид, клопиралид-метил, клопиралид-оламин, клопиралид-калий, клопиралид-трис(2-гидроксипропил)аммоний, клорансулам, клорансулам-метил, CMA, сульфат меди, CPMF, CPPC, кредазин, крезол, кумилурон, цианамид, цианатрин, цианазин, циклоат, циклосульфамурон, циклоксидим, циклурон, цигалофоп, цигалофоп-бутил, циперкват, хлорид циперквата, ципразин, ципразол, ципромид, даимурон, далапон, далапон-кальций, далапон-магний, далапон-натрий, дазомет, дазомет-натрий, делахлор, десмедифам, десметрин, диаллат, дикамба, дикамба-диметиламмоний, дикамба-диоламин, дикамба-изопропиламмоний, дикамба-метил, дикамба-оламин, дикамба-калий, дикамба-натрий, дикамба-троламин, дихлобенил, дихлоральмочевина, дихлормат, дихлорпроп, дихлорпроп-2-этилгексил, дихлорпроп-бутотил, дихлорпроп-диметиламмоний, дихлорпроп-этиламмоний, дихлорпроп-изоктил, дихлорпроп-метил, дихлорпроп-P, дихлорпроп-P-диметиламмоний, дихлорпроп-калий, дихлорпроп-натрий, диклофоп, диклофоп-метил, диклосулам, диэтамкват, дихлорид диэтамквата, диэтатил, диэтатилэтил, дифенопентен, дифенопентен-этил, дифеноксурон, дифензокват, дифензокват метилсульфат, дифлуфеникан, дифлубензопир, дифлубензопир-натрий, димефурон, димепиперат, диметахлор, диметаметрин, диметенамид, диметенамид-P, димексано, димидазон, динитрамин, динофенат, динопроп, диносам, диносеб, ацетат диносеба, диносеб-аммоний, диносеб-диоламин, диносеб-натрий, диносеб-троламин, динотерб, ацетат динотерба, дифацинон-натрий, дифенамид, дипропетрин, дикват, дибромид диквата, дисул, дисул-натрий, дитиопир, диурон, DMPA, DNOC, DNOC-аммоний, DNOC-калий, DNOC-натрий, DSMA, EBEP, эглиназин, эглиназин-этил, эндотал, эндотал-диаммоний, эндотал-дикалий, эндотал-динатрий, эпроназ, EPTC, эрбон, эспрокарб, эталфлуралин, этаметсульфурон, этаметсульфурон-метил, этидимурон, этиолат, этофумезат, этоксифен, этоксифен-этил, этоксисульфурон, этинофен, этнипромид, этобензанид, EXD, фенасулам, фенопроп, фенопроп-3-бутоксипропил, фенопроп-бутометил, фенопроп-бутотил, фенопроп-бутил, фенопроп-изоктил, фенопроп-метил, фенопроп-калий, феноксапроп, феноксапроп-этил, феноксапроп-P, феноксапроп-P-этил, феноксасульфон, фентеракол, фентиапроп, фентиапроп-этил, фентразамид, фенурон, фенурон-TCA, сульфат железа(II), флампроп, флампроп-изопропил, флампроп-M, флампроп-метил, флампроп-M-изопропил, флампроп-M-метил, флазасульфурон, флорасулам, флуазифоп, флуазифоп-бутил, флуазифоп-метил, флуазифоп-P, флуазифоп-P-бутил, флуазолат, флукарбазон, флукарбазон-натрий, флуцетосульфурон, флухлоралин, флуфенацет, флуфеникан, флуфенпир, флуфенпир-этил, флуметсулам, флумезин, флумиклорак, флумиклорак-пентил, флумиоксазин, флумипропин, флуометурон, фтордифен, фторгликофен, фторгликофен-этил, фтормидин, фторнитрофен, флуотиурон, флупоксам, флупропацил, флупропанат, флупропанат-натрий, флупирсульфурон, флупирсульфурон-метилнатрий, флуридон, флурохлоридон, флуроксипир, флуроксипир-бутометил, флуроксипир-мептил, флуртамон, флутиацет, флутиацет-метил, фомесафен, фомесафен-натрий, форамсульфурон, фосамин, фосаминаммоний, фурилоксифен, глуфосинат, глуфосинат-аммоний, глуфосинат-P, глуфосинат-P-аммоний, глуфосинат-P-натрий, глифосат, глифосат-диаммоний, глифосат-диметиламмоний, глифосат-изопропиламмоний, глифосат-моноаммоний, глифосат-калий, глифосат-сесквинатрий, глифосат-тримезий, галосафен, галосульфурон, галосульфурон-метил, галоксидин, галоксифоп, галоксифоп-этотил, галоксифоп-метил, галоксифоп-P, галоксифоп-P-этотил, галоксифоп-P-метил, галоксифоп-натрий, гексахлорацетон, гексафлурат, гексазинон, имазаметабенз, имазаметабенз-метил, имазамокс, имазамокс-аммоний, имазапик, имазапик-аммоний, имазапир, имазапир-изопропиламмоний, имазахин, имазахинаммоний, имазахин-метил, имазахин-натрий, имазетапир, имазетапир-аммоний, имазосульфурон, инданофан, индазифлам, йодобонил, йодметан, йодосульфурон, йодосульфурон-метилнатрий, иоксинил, иоксинилоктаноат, иоксинил-литий, иоксинилнатрий, ипазин, ипфенкарбазон, ипримидам, изокарбамид, изоцил, изометиозин, изонорурон, изополинат, изопропалин, изопротурон, изоурон, изоксабен, изоксахлортол, изоксафлутол, изоксапирифоп, карбутилат, кетоспирадокс, лактофен, ленацил, линурон, MAA, MAMA, MCPA, MCPA-2-этилгексил, MCPA-бутотил, MCPA-бутил, MCPA-диметиламмоний, MCPA-диоламин, MCPA-этил, MCPA-изобутил, MCPA-изоктил, MCPA-изопропил, MCPA-метил, MCPA-оламин, MCPA-калий, MCPA-натрий, MCPA-тиоэтил, MCPA-троламин, MCPB, MCPB-этил, MCPB-метил, MCPB-натрий, мекопроп, мекопроп-2-этилгексил, мекопроп-диметиламмоний, мекопроп-диоламин, мекопроп-этадил, мекопроп-изоктил, мекопроп-метил, мекопроп-P, мекопроп-P-диметиламмоний, мекопроп-P-изобутил, мекопроп-калий, мекопроп-P-калий, мекопроп-натрий, мекопроп-троламин, мединотерб, меацетат динотерба, мефенацет, мефлуидид, мефлуидид-диоламин, мефлуидид -калий, мезопразин, мезосульфурон, мезосульфурон-метил, мезотрион, метам, метам-аммоний, метамифоп, метамитрон, метам-калий, метам-натрий, метазахлор, метазосульфурон, метфлуразон, метабензтиазурон, металпропалин, метазол, метиобенкарб, метиозолин, метиурон, метометон, метопротрин, метилбромид, метилизотиоцианат, метилдимрон, метобензурон, метолахлор, метосулам, метоксурон, метрибузин, метсульфурон, метсульфурон-метил, молинат, моналид, монисоурон, монохлоруксусную кислоту, монолинурон, монурон, монурон-TCA, морфамкват, дихлорид морфамквата, MSMA, напроанилид, напропамид, напталам, напталам-натрий, небурон, никосульфурон, нипираклофен, нитралин, нитрофен, нитрофторфен, норфлуразон, норурон, OCH, орбенкарб, орто-дихлорбензол, ортосульфамурон, оризалин, оксадиаргил, оксадиазон, оксапиразон, оксапиразон-димоламин, оксапиразон-натрий, оксасульфурон, оксазикломефон, оксифлуорфен, парафлурон, паракват, дихлорид параквата, диметилсульфат параквата, пебулат, пеларгоновую кислоту, пендиметалин, фенокссулам, пентахлорфенол, пентанохлор, пентоксазон, перфлуидон, пентоксамид, фенизофам, фенмедифам, фенмедифам-этил, фенобензурон, фенилмеркурацетат, пиклорам, пиклорам-2-этилгексил, пиклорам-изоктил, пиклорам-метил, пиклорам-оламин, пиклорам-калий, пиклорам-триэтиламмоний, пиклорам-трис(2-гидроксипропил)аммоний, пиколинафен, пиноксаден, пиперофос, арсенит калия, азид калия, цианат калия, претилахлор, примисульфурон, примисульфурон-метил, проциазин, продиамин, профлуазол, профлуралин, профоксидим, проглиназин, проглиназин-этил, прометон, прометрин, пропахлор, пропанил, пропахизафоп, пропазин, профам, пропизохлор, пропоксикарбазон, пропоксикарбазон-натрий, пропирисульфурон, пропизамид, просульфалин, просульфокарб, просульфурон, проксан, проксан-натрий, принахлор, пиданон, пираклонил, пирафлуфен, пирафлуфен-этил, пирасульфотол, пиразолинат, пиразосульфурон, пиразосульфурон-этил, пиразоксифен, пирибензоксим, пирибутикарб, пириклор, пиридафол, пиридат, пирифталид, пириминобак, пириминобак-метил, пиримисульфан, пиритиобак, пиритиобак-натрий, пироксасульфон, пироксулам, хинклорак, хинмерак, хинокламин, хинонамид, хизалофоп, хизалофоп-этил, хизалофоп-P, хизалофоп-P-этил, хизалофоп-P-тефурил, родетанил, римсульфурон, сафлуфенацил, себутилазин, секбуметон, сетоксидим, сидурон, симазин, симетон, симетрин, SMA, S-метолахлор, арсенит натрия, азид натрия, хлорат натрия, сулкотрион, сульфаллат, сульфентразон, сульфометурон, сульфометурон-метил, сульфосульфурон, серную кислоту, сулгликапин, свеп, TCA, TCA-аммоний, TCA-кальций, TCA-этадил, TCA-магний, TCA-натрий, тебутам, тебутиурон, тефурилтрион, темботрион, тепралоксидим, тербацил, тербукарб, тербухлор, тербуметон, тербутилазин, тербутрин, тетрафлурон, тенилхлор, тиазафлурон, тиазопир, тидиазимин, тидиазурон, тиенкарбазон, тиенкарбазон-метил, тифенсульфурон, тифенсульфурон-метил, тиобенкарб, тиокарбазил, тиоклорим, топрамезон, тралкоксидим, три-аллат, триасульфурон, триазифлам, трибенурон, трибенурон-метил, трикамба, триклопир, триклопир-бутотил, триклопир-этил, триклопир-триэтиламмоний, тридифан, триэтазин, трифлоксисульфурон, трифлоксисульфурон-натрий, трифлуралин, трифлусульфурон, трифлусульфурон-метил, трифоп, трифоп-метил, трифопсим, тригидрокситриазин, триметурон, трипропиндан, тритак, тритосульфурон, вернолат или ксилахлор.
Биопестициды
Соединение формулы I также можно использовать в комбинации (такой как композиционная смесь, или путем одновременного или последовательного нанесения) с одним или несколькими биопестицидами. Термин "биопестицид" используют для обозначения микробиологических средств для борьбы с вредителями, которые применяют по методикам, аналогичным использующимся для химических пестицидов. Обычно они являются бактериальными, но имеются примеры грибковых средств борьбы, включая Trichoderma spp. и Ampelomyces quisqualis (средство борьбы с настоящей мучнистой росой винограда). Bacillus subtilis используют для борьбы с патогенами растений. С помощью микробиологических средств также борются с сорняками и грызунами. Одним широко известным примером инсектицида является Bacillus thuringiensis, средство борьбы с бактериальным заболеванием чешуекрылых, жесткокрылых и двукрылых. Поскольку он мало влияет на другие организмы, его считают экологически более приемлемым, чем синтетические пестициды. Биологические инсектициды включают продукты, основанные на:
1. энтомопатогенных грибах (например, Metarhizium anisopliae);
2. энтомопатогенных нематодах (например, Steinernema feltiae); и
3. энтомопатогенных вирусах (например, грануловирус Cydia pomonella).
Другие примеры энтомопатогенных микроорганизмов включают, но не ограничиваются только ими, бакуловирусы, бактерии и другие прокариотные микроорганизмы, грибы, простейшие и микроспоридии. Биологически образованные инсектициды включают, но не ограничиваются только ими, ротенон, вератридин, а также микробные токсины; стойкие или резистентные к насекомым сорта растений; и микроорганизмы, модифицированные с помощью технологии рекомбинантной ДНК, так что они вырабатывают инсектициды или придают генетически модифицированному микроорганизму стойкость к насекомым. В одном варианте осуществления соединение формулы I можно использовать с одним или несколькими биопестицидами в качестве средств для обработки семян и улучшения почвы. В публикации The Manual of Biocontrol Agents приведен обзор имеющихся биологических инсектицидных (и основанных на биологических веществах систем борьбы) продуктов. Copping L.G. (ed.) (2004). The Manual of Biocontrol Agents (formerly the Biopesticide Manual) 3rd Edition. British Crop Production Council (BCPC), Farnham, Surrey UK.
Другие активные соединения
Соединение формулы I также можно использовать в комбинации (такой как композиционная смесь, или путем одновременного или последовательного нанесения) с одним или несколькими из следующих соединений:
1. 3-(4-хлор-2,6-диметилфенил)-4-гидрокси-8-окса-1-азаспиро[4,5]дец-3-ен-2-он;
2. 3-(4'-хлор-2,4-диметил[1,1'-бифенил]-3-ил)-4-гидрокси-8-окса-1-азаспиро[4,5]дец-3-ен-2-он;
3. 4-[[(6-хлор-3-пиридинил)метил]метиламино]-2(5H)-фуранон;
4. 4-[[(6-хлор-3-пиридинил)метил]циклопропиламино]-2(5H)-фуранон;
5. 3-хлор-N2-[(1S)-1-метил-2-(метилсульфонил)этил]-N1-[2-метил-4-[1,2,2,2-тетрафтор-1-(трифторметил)этил]фенил]-1,2-бензолдикарбоксамид;
6. 2-циано-N-этил-4-фтор-3-метоксибензолсульфонамид;
7. 2-циано-N-этил-3-метоксибензолсульфонамид;
8. 2-циано-3-дифторметокси-N-этил-4-фторбензолсульфонамид;
9. 2-циано-3-фторметокси-N-этилбензолсульфонамид;
10. 2-циано-6-фтор-3-метокси-N,N-диметилбензолсульфонамид;
11. 2-циано-N-этил-6-фтор-3-метокси-N-метилбензолсульфонамид;
12. 2-циано-3-дифторметокси-N,N-диметилбензолсульфонамид;
13. 3-(дифторметил)-N-[2-(3,3-диметилбутил)фенил]-1-метил-1H-пиразол-4-карбоксамид;
14. N-этил-2,2-диметилпропионамид-2-(2,6-дихлор-α,α,α-трифтор-п-толил)гидразон;
15. N-этил-2,2-дихлор-1-метилциклопропан-карбоксамид-2-(2,6-дихлор-α,α,α-трифтор-п-толил)гидразон никотина;
16. O-{(E-)-[2-(4-хлорфенил)-2-циано-1-(2-трифторметилфенил)-винил]}S-метилтиокарбонат;
17. (E)-Ν1-[(2-хлор-1,3-тиазол-5-илметил)]-Ν2-циано-Ν1-метилацетамид;
18. 1-(6-хлорпиридин-3-илметил)-7-метил-8-нитро-1,2,3,5,6,7-гексагидроимидазо[1,2-a]пиридин-5-ол;
19. 4-[4-хлорфенил-(2-бутилидин-гидразоно)метил)]фенилмезилат; и
20. N-этил-2,2-дихлор-1-метилциклопропанкарбоксамид-2-(2,6-дихлор-α,α,α-трифтор-п-толил)гидразон.
Соединение формулы I также можно использовать в комбинации (такой как композиционная смесь, или путем одновременного или последовательного внесения) с одним или несколькими соединениями из следующих групп: альгициды, антифиданты, авициды, бактерициды, средства для отпугивания птиц, хемостерилизаторы, антидоты гербицидов, приманки для насекомых, репелленты для насекомых, репелленты для млекопитающих, средства, препятствующие спариванию, моллюскоциды, активаторы растений, регуляторы роста растений, родентициды или вирициды.
Синергетические смеси и синергетики
Соединение формулы I можно использовать в комбинации по меньшей мере с одним другим инсектицидом с образованием синергетической смеси, где тип воздействия таких соединений по сравнению с типом воздействия соединения формулы I является таким же, сходным или иным. Примеры типов воздействий, включают, но не ограничиваются только ими: ингибитор ацетилхолинэстеразы; модулятор натриевого канала; ингибитор биосинтеза хитина; регулируемый посредством ГАМК (гамма-аминомасляная кислота) антагонист хлоридного канала; регулируемый посредством ГАМК и глутамата агонист хлоридного канала; агонист ацетилхолинового рецептора; ингибитор MET I; стимулируемый с помощью Mg ингибитор АТФазы (аденозинтрифосфатаза); никотиновый ацетилхолиновый рецептор; средство, разрушающее мембрану средней кишки; средство, нарушающее окислительное фосфорилирование, или рианодиновый рецептор (RyRs).
Кроме того, соединение формулы I можно использовать в комбинации по меньшей мере с одним из фунгицидов, акарицидов, гербицидов или нематоцидов с образованием синергетической смеси.
Кроме того, соединение формулы I можно использовать в комбинации с другими активными соединениями, такими как соединения, указанные в разделе "Другие активные соединения", альгициды, авициды, бактерициды, моллюскоциды, родентициды, вирициды, антидоты гербицидов, вспомогательные вещества и/или поверхностно-активные вещества с образованием синергетической смеси. Кроме того, следующие соединения известны, как синергетики, и их можно использовать в комбинации с соединением формулы I: пиперонилбутоксид, пипротал, пропилизом, сезамекс, сезамолин, сульфоксид и трибуфос.
Препараты
Пестицид редко пригоден для использования в чистом виде. Обычно необходимо добавлять другие вещества, так чтобы пестицид можно было использовать при необходимой концентрации и в подходящей форме, обеспечивающей легкое применение, обращение, транспортировку, хранение и максимальную активность пестицида. Таким образом, пестициды готовят, например, как приманки, концентрировали эмульсии, дусты, эмульгирующиеся концентраты, фумиганты, гели, гранулы, микрокапсулированные препараты, средства для обработки семян, концентраты суспензий, суспоэмульсии, таблетки, растворимые в воде жидкости, диспергирующиеся в воде гранулы или сухие сыпучие смеси, смачивающиеся порошки и сверхмалообъемные растворы. Дополнительная информация о типах препаратов приведена в публикации "Catalogue of Pesticide Formulation Types and International Coding System" Technical Monograph n°2, 5th Edition by CropLife International (2002).
Пестициды чаще всего используют в виде водных суспензий или эмульсий, полученных из концентрированных препаратов таких пестицидов. Такие растворимые в воде, суспендирующиеся или эмульгирующиеся в воде препараты представляют собой твердые вещества, обычно известные, как смачивающиеся порошки или диспергирующиеся в воде гранулы, или жидкости, обычно известные, как эмульгирующиеся концентраты или водные суспензии. Смачивающиеся порошки, которые можно спрессовать в диспергирующиеся в воде гранулы, представляют собой однородную смесь пестицида, носителя и поверхностно-активных веществ. Концентрация пестицида обычно равна от примерно 10% до примерно 90 мас.%. Носитель обычно выбирают из группы включающей аттапульгитовые глины, монтмориллонитовые глины, диатомовые земли или очищенные силикаты. Эффективные поверхностно-активные вещества, содержащие от примерно 0,5% до примерно 10% смачивающегося порошка, включают сульфированные лигнины, конденсированные нафталинсульфонаты, нафталинсульфонаты, алкилбензолсульфонаты, алкилсульфаты и неионогенные поверхностно-активные вещества, такие как аддукты этиленоксида с алкилфенолами.
Эмульгирующиеся концентраты пестицидов содержат пестицид в обычной концентрации, такой как равная от примерно 50 до примерно 500 г/л жидкости, растворенный в носителе, которым является смешивающийся с водой растворитель или смесь несмешивающегося с водой органического растворителя и эмульгаторов. Подходящие органические растворители включают ароматические соединения, в особенности ксилолы и фракции нефти, в особенности высококипящие нафталиновые и олефиновые фракции нефти, такие как тяжелая ароматическая нафта. Также можно использовать другие органические растворители, такие как терпеновые растворители, включая производные канифоли, алифатические кетоны, такие как циклогексанон, и сложные спирты, такие как 2-этоксиэтанол. Подходящие эмульгаторы для эмульгирующихся концентратов выбирают из числа обычных анионогенных и неионогенных поверхностно-активных веществ.
Водные суспензии включают суспензии нерастворимых в воде пестицидов, диспергированных в водном носителе при концентрации, находящейся в диапазоне от примерно 5% до примерно 50 мас.%. Суспензии получают путем тонкого размола пестицида и его энергичного смешивания с носителем, включающим воду и поверхностно-активные вещества. Для увеличения плотности и вязкости водного носителя также можно добавить такие ингредиенты, как неорганические соли и синтетические или натуральные камеди. Часто наиболее эффективно размалывать и смешивать пестицид одновременно путем приготовления водной смеси и ее гомогенизации в аппарате, таком как песочная мельница, шаровая мельница или гомогенизатор поршневого типа.
Пестициды также можно использовать в виде гранулированной композиций, которая является особенно подходящей для внесения в почву. Гранулированные композиции обычно содержат от примерно 0,5% до примерно 10 мас.% пестицида, диспергированного в носителе, который включает глину или аналогичное вещество. Такие композиции обычно получают путем растворения пестицида в подходящем растворителе и его нанесения на гранулированный носитель, который предварительно сформован в частицы подходящего размера, находящегося в диапазоне от примерно 0,5 до примерно 3 мм. Такие композиции также можно получить путем приготовления теста или пасты из носителя и соединения и измельчения и сушки с получением гранул необходимого размера.
Дусты, содержащие пестицид, получают путем тщательного смешивания пестицида в порошкообразном виде с подходящим пылеобразным сельскохозяйственным носителем, таким как каолиновая глина, размолотая вулканическая порода и т. п. Дусты предпочтительно могут содержать от примерно 1% до примерно 10% пестицида. Их можно использовать в качестве средства для протравливания семян или для некорневого внесения с помощью опыливателя.
Столь же целесообразно использовать пестицид в виде раствора в подходящем органическом растворителе, обычно нефтяном масле, таком как инсектицидные масла, которые широко используют в агрохимии.
Пестициды также можно использовать в виде аэрозольной композиции. В таких композициях пестицид растворен или диспергирован в носителе, которым является создающая давление смесь пропеллентов. Аэрозольная композиция упакована в контейнер, из которого смесь дозируется через распыляющий клапан.
Пестицидные приманки получают, когда пестицид смешивают с кормом или аттрактантом или с сразу с обоими. Когда вредители поедают приманку, они также потребляют пестицид. Приманки могут находиться в форме гранул, гелей, сыпучих порошков, жидкостей или твердых веществ. Их можно использовать в местах укрытия вредителей.
Фумиганты представляют собой пестициды, которые обладают относительно высоким давлением насыщенного пара, и поэтому могут находиться в виде газа в концентрациях, достаточных для уничтожения вредителей в почве или закрытых пространствах. Токсичность фумиганта пропорциональна его концентрации и длительности воздействия. Они характеризуются хорошей способностью к диффузии и действуют путем проникновения в дыхательную систему вредителя или впитывания через кутикулу вредителя. Фумиганты используют для борьбы с вредителями хранящихся продуктов с использованием листового материала, защищающего от выхода газа, в герметизированных помещениях или строениях или в специальных камерах.
Пестициды можно микрокапсулировать путем суспендирования частиц или капелек пестицида в полимерах разных типов. Путем изменения химического строения полимера или изменения характеристик обработки можно сформировать микрокапсулы разных размеров, растворимости, с разной толщиной стенок и степенью проникновения. Эти факторы определяют скорость, с которой высвобождается находящийся там активный ингредиент, что, в свою очередь, влияет на остаточное воздействие, скорость действия и запах продукта.
Концентраты масляных растворов получают путем растворения пестицида в растворителе, который удерживает пестицид в растворе. Масляные растворы пестицида обычно обеспечивают более быстрое разрушение и уничтожение вредителей, чем другие препараты, поскольку сами растворители обладают пестицидным воздействием и растворение воскообразного покрытия наружного покрова увеличивает скорость поступления пестицида. Другие преимущества масляных растворов включают лучшую стабильность при хранении, лучшее проникновение через трещины и лучшую адгезию к жирным поверхностям.
Другим вариантом осуществления является эмульсия типа масло-в-воде, где эмульсия содержит масляные шарики, на которых находится слоистое жидкокристаллическое покрытие и которые диспергированы в водной фазе, где каждый шарик содержит по меньшей мере одно соединение, которое сельскохозяйственно активно, и по отдельности покрыто моноламеллярным или олиголамеллярным слоем, включающим: (1) по меньшей мере одно неионогенное липофильное поверхностно-активное вещество, (2) по меньшей мере одно неионогенное гидрофильное поверхностно-активное вещество и (3) по меньшей мере одно ионогенное поверхностно-активное вещество, где шарики обладают средним диаметром, равным менее 800 нм. Дополнительная информация об этом варианте осуществления раскрыта в публикации патента U.S. 20070027034, опубликованной 1 февраля 2007 г., обладающей номером заявки на патент 11/495228. Для удобства использования этот вариант осуществления обозначен, как "OIWE".
Дополнительная информация приведена в публикации "Insect Pest Management" 2nd Edition by D. Dent, copyright CAB International (2000). Кроме того, более подробная информация приведена в публикации "Handbook of Pest Control - The Behavior, Life History, and Control of Household Pests" by Arnold Mallis, 9th Edition, copyright 2004 by GIE Media Inc.
Другие компоненты препаратов
Обычно, когда соединение формулы I или его любую сельскохозяйственно приемлемую соль используют в препарате, такой препарат также может содержать другие компоненты. Эти компоненты включают, но не ограничиваются только ими (этот перечень не является исчерпывающим и взаимоисключающим), смачиватели, распределяющие средства, клеющие средства, средства, обеспечивающие проницаемость, буферы, комплексообразующие соединения, агенты, уменьшающие снос, агенты, обеспечивающие совместимость, противовспениватели, очищающие агенты и эмульгаторы. Некоторые компоненты описаны ниже.
Смачивающий агент является веществом, которое при добавлении к жидкости усиливает растекание или проникающую способность жидкости путем уменьшения межфазного натяжения между жидкостью и поверхностью, по которой она растекается. Смачивающие агенты используются в агрохимических препаратах для двух основных целей: во время обработки и изготовления для повышения степени смачивания порошков в воде при приготовлении концентратов растворяющихся жидкостей или концентратов суспензий; и во время смешивания продукта с водой в баке для опрыскивания для уменьшения времени смачивания смачивающихся порошков и для улучшения проникновения воды в диспергирующиеся в воде гранулы. Примерами смачивающих агентов, использующихся в препаратах смачивающихся порошков, концентратов суспензий и диспергирующихся в воде гранул, являются: лаурилсульфат натрия; диоктилсульфосукцинат натрия; алкилфенолэтоксилаты; и этоксилаты алифатических спиртов.
Диспергирующий агент является веществом, которое адсорбируется на поверхности частиц и способствует сохранению частиц в диспергированном состоянии и предупреждает их повторную агрегацию. Диспергирующие агенты добавляют к агрохимическим препаратам для облегчения диспергирования и суспендирования при изготовлении и для обеспечения повторного диспергирования в воде в баке для опрыскивания. Они широко используются в смачивающихся порошках, концентратах суспензий и диспергирующихся в воде гранулах. Поверхностно-активные вещества, которые используют в качестве диспергирующих агентов, могут обладать способностью к прочной адсорбции на поверхности частицы и создавать зарядовый или стерический барьер для повторной агрегации частиц. Чаще всего использующиеся поверхностно-активные вещества являются анионогенными, неионогенными или смесями этих двух типов. Для препаратов смачивающихся порошков чаще всего использующимися диспергирующими агентами являются лигносульфонаты натрия. Для концентратов суспензий очень хорошая адсорбция и стабилизация обеспечиваются при использовании полиэлектролитов, таких как продукты конденсации нафталинсульфоната натрия с формальдегидом. Также используют тристирилфенолэтоксилатфосфаты. Неионогенные соединения, такие как продукты конденсации алкиларилэтиленоксида с блок-сополимерами ЭО-ПО (этиленоксид-пропиленоксид) иногда объединяют с анионогенными соединениями в качестве диспергирующих агентов для концентратов суспензий. В последние годы для использования в качестве диспергирующих агентов разработаны новые типы обладающих очень большой молекулярной массой полимерных поверхностно-активных веществ. Они обладают очень длинными гидрофобными основными цепями и большим количеством этиленоксид цепей, образующих "зубья" "гребенки" поверхностно-активного вещества. Эти обладающие очень большой молекулярной массой полимеры могут придать концентратам суспензий очень длительную стабильность, поскольку гидрофобные основные цепи обладают способностью закрепляться во многих положениях на поверхностях частиц. Примерами диспергирующих агентов, использующихся в агрохимических препаратах, являются: лигносульфонаты натрия; продукты конденсации нафталинсульфоната натрия с формальдегидом; тристирилфенолэтоксилатфосфаты; этоксилаты алифатических спиртов; алкилэтоксилаты; блок-сополимеры ЭО-ПО; и привитые сополимеры.
Эмульгирующий агент является веществом, которое стабилизирует суспензию капелек жидкой фазы в другой жидкой фазе. Без эмульгирующего агента две жидкости разделяются на две несмешивающиеся жидкие фазы. Чаще всего использующиеся смеси эмульгаторов содержат алкилфенол или алифатический спирт, содержащий 12 или большее количество этиленоксидных звеньев, и маслорастворимую кальциевую соль додецилбензолсульфоновой кислоты. В диапазоне значений показателя липофильно-гидрофильного баланса ("ЛГБ"), составляющем от 8 до 18, обычно образуются эмульсии, обладающие хорошей стабильностью. Стабильность эмульсии иногда можно улучшить путем добавления небольшого количества блок-сополимерного поверхностно-активного вещества ЭО-ПО.
Солюбилизирующий агент является поверхностно-активным веществом, которое образует в воде мицеллы при концентрациях, превышающих критическую концентрацию мицеллообразования. Затем мицеллы могут растворять или солюбилизировать нерастворимые в воде вещества внутри гидрофобной части мицеллы. Типами поверхностно-активных веществ, обычно использующихся для солюбилизации, являются неионогенные вещества, сорбитанмоноолеаты, сорбитанмоноолеатэтоксилаты и метилолеаты.
Поверхностно-активные вещества иногда используют по отдельности или вместе с другими добавками, такими как минеральные или растительные масла, в качестве вспомогательных веществ в баковых смесях для опрыскивания с целью улучшения биологического воздействия пестицида на мишень. Типы поверхностно-активных веществ, использующихся для усиления биологического воздействия, обычно зависят от природы и типа воздействия пестицида. Однако они часто являются неионогенными, такими как: алкилэтоксилаты; этоксилаты линейных алифатических спиртов; алифатические аминэтоксилаты.
Носитель или разбавитель в сельскохозяйственном препарате является веществом, добавляемым к пестициду для получения продукта необходимой концентрации. Носители обычно являются веществами, обладающими высокой абсорбционной емкостью, а разбавители обычно являются веществами, обладающими низкой абсорбционной емкостью. Носители и разбавители используют в таких препаратах, как дусты, смачивающиеся порошки, гранулы и диспергирующиеся в воде гранулы.
Органические растворители используют преимущественно в препаратах эмульгирующиеся концентраты, эмульсии масло-в-воде, суспоэмульсии и сверхмалообъемные препараты и в меньшей степени в гранулированных препаратах. Иногда используют смеси растворителей. Первыми главными группами растворителей являются алифатические парафиновые масла, такие как керосин или рафинированные парафины. Вторая главная группа (и самая распространенная) включает ароматические растворители, такие как ксилол и обладающие более высокой молекулярной массой фракции C9 и C10 ароматических растворителей. Хлорированные углеводороды применимы в качестве coрастворителей для предупреждения кристаллизации пестицидов, когда препарат эмульгируют в воде. Спирты иногда используют в качестве coрастворителей для увеличения растворяющей способности. Другие растворители могут включать растительные масла, масла из семян растений и сложные эфиры растительных масел и масел из семян растений.
Загустители или гелеобразующие агенты используют преимущественно в таких составах, как концентраты суспензий, эмульсии и суспоэмульсии для изменения реологических характеристик или характеристик текучести жидкости и для предупреждения разделения и осаждения диспергированных частиц или капелек. Загущающие, гелеобразующие и препятствующие осаждению агенты обычно подразделяются на две категории, а именно, нерастворимые в воде измельченные частицы и растворимые в воде полимеры. Составы концентратов суспензий можно получить с использованием глин и диоксидов кремния. Примеры материалов этих типов включают, но не ограничиваются только ими, монтмориллонит, бентонит, алюмосиликат магния и аттапульгит. Растворимые в воде полисахариды в течение многих лет используют в качестве загущающих-гелеобразующих агентов. Этими чаще всего использующимися типами полисахаридов являются натуральные экстракты семян и морских водорослей или синтетические производные целлюлозы. Примеры материалов этих типов включают, но не ограничиваются только ими, гуаровую камедь; камедь плодов рожкового дерева; каррагенан; альгинаты; метилцеллюлозу; натриевую соль карбоксиметилцеллюлозы (НКМЦ); гидроксиэтилцеллюлозу (ГЭЦ). Другие типы препятствующих осаждению агентов основаны на модифицированных крахмалах, полиакрилатах, поливиниловом спирте и полиэтиленоксиде. Другим хорошим препятствующим осаждению агентом является ксантановая камедь.
Микроорганизмы могут испортить готовые продукты. Поэтому для устранения или уменьшения их влияния используют консервирующие агенты. Примеры таких агентов включают, но не ограничиваются только ими: пропионовую кислоту и ее натриевую соль; сорбиновую кислоту и ее натриевую или калиевую соли; бензойную кислоту и ее натриевую соль; натриевую соль п-гидроксибензойной кислоты; метил-п-гидроксибензоат; и 1,2-бензизотиазолин-3-он (БИТ).
Наличие поверхностно-активных веществ часто приводит к вспениванию препаратов на водной основе во время операций приготовления и применения с помощью бака для опрыскивания. Для уменьшения склонности к вспениванию противовспениватели часто добавляют на стадии изготовления или до расфасовки в бутылки. Обычно имеются два типа противовспенивателей, а именно, силиконы и не являющиеся силиконами. Силиконы обычно представляют собой водные эмульсии диметилполисилоксана, несиликоновые противовспениватели представляют собой нерастворимые в воде масла, такие как октанол и нонанол, или диоксид кремния. В обоих случаях назначением противовспенивателя является смещение поверхностно-активного вещества с границы раздела воздух-вода.
"Зеленые" агенты (например, вспомогательные вещества, поверхностно-активные вещества, растворители) могут уменьшить общее влияние средств защиты растений на окружающую среду. "Зеленые" агенты являются биологически разлагающимися и обычно их получают из природных и/или стабильных источников, например, из растительных и животных источников. Конкретными примерами являются: растительные масла, масла из семян растений и их сложные эфиры, а также алкоксилированные алкилполиглюкозиды.
Дополнительная информация приведена в публикации "Chemistry and Technology of Agrochemical Formulations" edited by D.A. Knowles, copyright 1998 by Kluwer Academic Publishers. См. также "Insecticides in Agriculture and Environment - Retrospects and Prospects" by A.S. Perry, I. Yamamoto, I. Ishaaya и R. Perry, copyright 1998 by Springer-Verlag.
Пестицидная активность
Раскрытые пестицидные композиции можно использовать, например, в качестве нематоцидов, акарицидов, пестицидов, инсектицидов, майтицидов и/или моллюскоцидов.
В одном предпочтительном варианте осуществления способ борьбы с вредителями включает нанесение пестицидной композиции, включающей соединение формулы I или его любую сельскохозяйственно приемлемую соль, вблизи от популяции вредителей.
Соединение формулы I для обеспечения борьбы обычно используют в количествах, равных от примерно 0,01 г/га до примерно 5000 г/га. Количества, равные от примерно 0,1 г/га до примерно 500 г/га, обычно являются предпочтительными и количества, равные от примерно 1 г/га до примерно 50 г/га, обычно являются более предпочтительными.
Участком, на который наносят соединение формулы I, может быть любой участок, на котором обитают (или могут обитать или который пересекают) вредители, например, на котором произрастают: сельскохозяйственные культуры, деревья, фрукты, злаки, фуражные культуры, виноград, травяной покров и декоративные растения; на котором постоянно находятся одомашненные животные; внутренние или наружные поверхности зданий (таких как помещения, в которых хранят зерно), строительные материалы, использующиеся в зданиях (такие как пропитанная древесина) и почва вокруг зданий. Предпочтительными участками, для использования соединений формулы I являются участки, на которых произрастают яблони, кукуруза, подсолнечник, хлопчатник, соя, канола, пшеница, рис, сорго, ячмень, овес, картофель, апельсины, люцерна, латук, земляника, томаты, перцы, крестоцветные, груши, табак, миндаль, сахарная свекла, фасоль и другие ценные культуры или на которых собираются высевать их семена. При выращивании различных растений также предпочтительно использовать сульфат аммония вместе с соединениями формулы I.
Борьба с вредителями обычно означает уменьшение на участке популяции вредителя, активность вредителя или их обе. Это может быть, когда: популяции вредителя удаляют с участка; когда вредителей делают недееспособными на участке или вокруг участка; или вредителей полностью или частично уничтожают на участке или вокруг участка. Разумеется, может происходить сочетание этих результатов. Обычно популяции вредителя, активность или и то и другое желательно уменьшить более, чем на 50%, предпочтительно более, чем на 90%. Обычно участок не находится в или на человеке; следовательно, местоположением обычно не является участок, занятый людьми.
Соединение формулы I можно использовать в смесях, наносить одновременно или последовательно, по отдельности или с другими соединениями для увеличения мощности растения (например, для выращивания лучшей корневой системы, лучшего перенесения трудных условий произрастания). Такими другими соединениями являются, например, соединения, которые модулируют этиленовые рецепторы растения, наиболее примечательным является 1-метилциклопропен (также обозначаемый, как 1-МЦП). Кроме того, такие молекулы можно использовать в периоды времени, когда активность вредителя является низкой, такие как предшествующие тому, когда растущее растение начинает образовывать ценные сельскохозяйственные продукты. Такие периоды времени включают ранний сезон посадки, когда количество вредителей обычно является небольшим.
Соединение формулы I можно использовать для борьбы с вредителями на лиственных и плодовых частях растений. Молекулы или приходят в непосредственное взаимодействие с вредителем, или вредитель потребляет пестицид при поедании листьев, плодовой массы или при высасывании сока, который содержит пестицид. Соединения формулы I также можно вносить в почву и при использовании его таким образом в борьбе с вредителем могут участвовать корни и стебли, поедаемые вредителями. Корни могут поглощать молекулу, передавая ее в лиственные части растения для борьбы с указанными находящимися над почвой жующими и высасывающими сок вредителями.
Обычно в случае приманок их размещают на грунте, где, например, термиты могут соприкасаться с приманкой и/или привлекаться к приманке. Приманки также можно наносить на поверхность здания (горизонтальную, вертикальную или наклонную поверхность), на которой, например, муравьи, термиты, таракановые и мухи, могут соприкасаться с приманкой и/или привлекаться к приманке. Приманки могут включать соединения формулы I.
Соединение формулы I можно капсулировать внутри капсулы или помещать на поверхность капсулы. Размер капсулы может быть от нанометрового (диаметром примерно 100-900 нм) до микрометрового (диаметром примерно 10-900 мкм).
Вследствие специфической стойкости яиц некоторых вредителей по отношению к некоторым пестицидам, для борьбы с появившимися личинками может быть желательно повторное нанесение соединения формулы I.
Системное перемещение пестицидов в растениях можно использовать для борьбы с вредителями в одной части растения путем нанесения (например, путем опрыскивания участка) соединений формулы I на разные участки растения. Например, борьбу с насекомыми, поедающими листья, можно обеспечить с помощью капельного орошения или внесения в борозды путем обработки почвы, например, путем орошения почвы до или после высевания или путем обработки семян растения до высевания.
Обработку семян можно проводить для всех типов семян, включая те, из которых вырастают растения, генетически модифицированные для экспрессирования специальных признаков. Типичные примеры включают семена, экспрессирующие белки, токсичные для беспозвоночных вредителей, таких как Bacillus thuringiensis, или другие инсектицидные токсины, вырабатывающие стойкость к гербициду, такому как "Roundup Ready" для семян, или обладающие последовательностью посторонних генов, экспрессирующих инсектицидные токсины, обеспечивающие стойкость к гербициду, усиленное питание, засухоустойчивость или любые другие благоприятные признаки. Кроме того, такие средства для обработки семян соединением формулы I могут дополнительно усилить способность растения лучше переносить трудные условия произрастания. Это приводит к более здоровым, более сильным растениям, что может привести к большей урожайности в период уборки. Обычно к благоприятным результатам предположительно приводит примерно от 1 грамма соединения формулы I до примерно 500 г на 100000 семян, количества, равные от примерно 10 г до примерно 100 г на 100000 семян, предположительно приводят к лучшим результатам и количества, равные от примерно 25 г до примерно 75 г на 100000 семян, предположительно приводят к еще лучшим результатам.
Должно быть очевидно, что соединение формулы I можно использовать на, в или вокруг растений, генетически модифицированных для экспрессирования специальных признаков, таких как Bacillus thuringiensis или другие инсектицидные токсины, или выработки стойкости к гербициду, или обладающих последовательностью посторонних генов, экспрессирующих инсектицидные токсины, обеспечивающие стойкость к гербициду, усиленное питание или любые другие благоприятные признаки.
Соединение формулы I можно использовать для борьбы с эндопаразитами и эктопаразитами в ветеринарии или в области содержания животных, не являющихся людьми. Соединение формулы I используют, например, путем перорального введения в виде, например, таблеток, капсул, питья, гранул, путем нанесения на кожу посредством, например, погружения, опрыскивания, полива, нанесения на участки и опыливания и посредством парентерального введения, например, с помощью инъекции.
Соединение формулы I также можно эффективно использовать при содержании домашнего скота, например, крупного рогатого скота, овец, свиней, цыплят и гусей. Их также можно эффективно использовать для домашних животных, таких как, лошади, собаки и кошки. Особенно важно проводить борьбу с такими вредителями, как блохи и иксодовые клещи, которые беспокоят таких животных. Подходящие препараты вводят животным перорально с питьевой водой или кормом. Дозы и то, какие препараты являются подходящими, зависят от вида животного.
Соединение формулы I также можно использовать для борьбы с паразитическими червями, в особенности в кишечнике перечисленных выше животных.
Соединение формулы I также можно использовать в терапевтических методиках лечения людей. Такие методики включают, но не ограничиваются только ими, пероральное введение в виде, например, таблеток, капсул, питья, гранул и путем нанесения на кожу.
Во всем мире вредители мигрируют на новые (для такого вредителя) территории и затем превращаются в новые инвазивные виды на такой новой территории. Соединение формулы I также можно использовать для борьбы с такими новыми инвазивными видами на такой новой территории.
Соединение формулы I также можно использовать на участке, на котором произрастают растения, такие как сельскохозяйственные культуры (например, до высадки, после высадки, до уборки), и на котором имеется небольшое количество вредителей (или даже они отсутствуют), которые могут привести к крупномасштабному повреждению таких растений. Применение таких молекул на таком участке благоприятно для растений, произрастающих на участке. Такие благоприятные факторы могут включать, но не ограничиваются только ими, улучшение состояния растения, повышение урожайности растения (например, увеличение биомассы и/или увеличение содержания ценных компонентов), улучшение мощности растения (например, улучшение роста растения и/или образование более зеленых листьев), улучшение качества растения (например, увеличение содержания или улучшение состава некоторых компонентов) и улучшение стойкости растения к абиотическому и/или биотическому стрессу.
Прежде чем становится возможным использование или выпуск в продажу пестицида, различные государственные органы (местные, региональные, штатные, национальные и международные) проводят длительные процедуры исследования такого пестицида. Регламентирующие органы определяют многочисленные требования и они должны соблюдаться при получении данных и предоставлении продукта регистрирующим лицом или третьей стороной от имени регистрирующего лица, часто с использованием компьютера, присоединенного к интернету. Затем эти государственные органы рассматривают такие данные и, если сделано заключение о безопасности, предоставляют возможному потребителю или продавцу продукта постановление о регистрации. Затем такой потребитель или продавец может использовать или продавать такой пестицид в районе, в котором проведена и утверждена регистрация продукта.
Соединение формулы I можно исследовать для определения его эффективности для борьбы с вредителями. Кроме того, можно провести исследование типа воздействия для определения того, обладает ли указанная молекула типом воздействия, отличающимся от воздействия других пестицидов. Затем эти полученные данные можно направить третьим сторонам, например, с помощью интернета.
Раскрытую пестицидную композицию, содержащую соединение формулы I, можно использовать для борьбы с самыми различными вредителями.
В качестве неограничивающего примера в одном или большем количестве вариантов осуществления способ, предлагаемый в настоящем изобретении, можно использовать для борьбы с одним или большим количеством представителей Lyriomiza sativae, Caliothrips phaseoli, Paratrioza cockerel, Spodoptera exigua, Myzus persicae, Nilaparvata lugens и Bemisia tabaci.
В дополнительных вариантах осуществления способ, предлагаемый в настоящем изобретении, можно использовать для борьбы с одним или большим количеством представителей по меньшей мере одного из следующих: типа членистоногие, типа нематоды, подтипа хелицеровые, подтипа мириаподы, подтипа шестиногие, класса насекомые, класса паукообразные и класса многоножки. По меньшей мере в некоторых вариантах осуществления способ, предлагаемый в настоящем изобретении, можно использовать для борьбы с одним или большим количеством представителей по меньшей мере одного из следующих: класса насекомые и класса паукообразные.
В других вариантах осуществления способ, предлагаемый в настоящем изобретении, можно использовать для борьбы с представителями отряда жесткокрылые (жуки), включая, но не ограничиваясь только ими, Acanthoscelides spp. (зерновки), Acanthoscelides obtectus (зерновка фасолевая), Agrilus planipennis (златка ясеневая изумрудная узкотелая), Agriotes spp. (проволочники), Anoplophora glabripennis (усач азиатский), Anthonomus spp. (зерновки), Anthonomus grandis (долгоносик хлопковый), Aphidius spp., Apion spp. (зерновки), Apogonia spp. (червовидные личинки), Ataenius spretulus (черный корневой жук), Atomaria linearis (крошка свекловичная), Aulacophore spp., Bothynoderes punctiventris (долгоносик свекловичный), Bruchus spp. (зерновки), Bruchus pisorum (зерновка гороховая), Cacoesia spp., Callosobruchus maculatus (зерновка пятнистая), Carpophilus hemipteras (блестянка полужесткокрылая), Cassida vittata, Cerosterna spp., Cerotoma spp. (листоеды), Cerotoma trifurcata (листоед бобовый), Ceutorhynchus spp. (зерновки), Ceutorhynchus assimilis (скрытнохоботник семенной), Ceutorhynchus napi (скрытнохоботник репный), Chaetocnema spp. (листоеды), Colaspis spp. (жуки грунтовые), Conoderus scalaris, Conoderus stigmosus, Conotrachelus nenuphar (плодовый долгоносик), Cotinus nitidis (хрущ блестящий зеленый), Crioceris asparagi (трещалка спаржевая), Cryptolestes ferrugineus (мукоед ржаво-красный), Cryptolestes pusillus (мукоед малый), Cryptolestes turcicus (мукоед турецкий), Ctenicera spp. (проволочники), Curculio spp. (зерновки), Cyclocephala spp. (червовидные личинки), Cylindrocpturus adspersus (подсолнечниковый стеблевой долгоносик), Deporaus marginatus (долгоносик-листорез манговый), Dermestes lardarius (кожеед ветчинный), Dermestes maculates (кожеед пятнистый), Diabrotica spp. (листоеды), Epilachna varivestis (мексиканский жук), Faustinus cubae, Hylobius pales (жук-долгоносик), Hypera spp. (зерновки), Hypera postica (долгоносик люцерновый), Hyperdoes spp. (долгоносик Hyperodes), Hypothenemus hampei (огневка кофейная), Ips spp. (заболонники), Lasioderma serricorne (жук табачный), Leptinotarsa decemlineata (колорадский жук), Liogenys fuscus, Liogenys suturalis, Lissorhoptrus oryzophilus (долгоносик рисовый водяной), Lyctus spp. (древесные жуки/капюшонники), Maecolaspis jоливаti, Megascelis spp., Melanotus communis, Meligethes spp., Meligethes aeneus (цветоед рапсовый), Melolontha melolontha (хрущ западный майский), Oberea brevis, Oberea linearis, Oryctes rhinoceros (пальмовый жук-носорог), Oryzaephilus mercator (плоскотелка арахисовая), Oryzaephilus surinamensis (рисоед суринамский), Otiorhynchus spp. (зерновки), Oulema melanopus (пьявица красногрудая), Oulema oryzae, Pantomorus spp. (зерновки), Phyllophaga spp. (майский/июньский жук), Phyllophaga cuyabana (листоеды), Phynchites spp., Popillia japonica (хрущик японский), Prostephanus truncates (большой точильщик зерновой), Rhizopertha dominica (точильщик зерновой), Rhizotrogus spp. (европейский хрущ), Rhynchophorus spp. (зерновки), Scolytus spp. (жуки-короеды), Shenophorus spp. (долгоносик), Sitona lineatus (долгоносик полосатый), Sitophilus spp. (долгоносики амбарные), Sitophilus granaries (долгоносик амбарный обыкновенный), Sitophilus oryzae (долгоносик рисовый), Stegobium paniceum (точильщик хлебный), Tribolium spp. (мучные хрущаки), Tribolium castaneum (хрущак каштановый), Tribolium confusum (хрущак малый мучной), Trogoderma variabile (трогодерма изменчивая) и Zabrus tenebioides.
В других вариантах осуществления способ, предлагаемый в настоящем изобретении, также можно использовать для борьбы с представителями отряда кожистокрылые (уховертки).
В дополнительных вариантах осуществления способ, предлагаемый в настоящем изобретении, можно использовать для борьбы с представителями отряда кожистокрылые (таракановые) включая, но не ограничиваясь только ими, Blattella germanica (таракан рыжий), Blatta orientalis (таракан черный), Parcoblatta pennylvanica, Periplaneta americana (таракан американский), Periplaneta australoasiae (таракан австралийский), Periplaneta brunnea (коричневый таракан), Periplaneta fuliginosa (темно-коричневый таракан), Pyncoselus suninamensis (таракан суринамский) и Supella longipalpa (мебельный таракан).
В других вариантах осуществления способ, предлагаемый в настоящем изобретении, можно использовать для борьбы с представителями отряда двукрылые (мухи настоящие) включая, но не ограничиваясь только ими, Aedes spp. (комары), Agromyza frontella (минер люцерновый), Agromyza spp. (минирующие мушки), Anastrepha spp. (плодовые мушки), Anastrepha suspensa (карибская плодовая муха), Anopheles spp. (комары), Batrocera spp. (плодовые мушки), Bactrocera cucurbitae (муха дынная), Bactrocera dorsalis (муха восточная фруктовая), Ceratitis spp. (плодовые мушки), Ceratitis capitata (Муха плодовая средиземноморская), Chrysops spp. (оленьи слепни), Cochliomyia spp. (личинки мясной мухи), Contarinia spp. (галлицы), Culex spp. (комары), Dasineura spp. (галлицы), Dasineura brassicae (галлица капустная), Delia spp., Delia platura (личинка мухи ростковой), Drosophila spp. (дрозофилы), Fannia spp. (комнатные мухи), Fannia canicularis (муха комнатная малая), Fannia scalaris (муха лестничная), Gasterophilus intestinalis (желудочные оводы), Gracillia perseae, Haematobia irritans (жигалка коровья малая), Hylemyia spp. (личинки корневые), Hypoderma lineatum (личинка бычьего полосатого овода), Liriomyza spp. (листовые минирующие мушки), Liriomyza brassica (минер крестоцветный), Melophagus ovinus (рунец овечий), Musca spp. (настоящие мухи), Musca autumnalis (муха обыкновенная полевая), Musca domestica (муха комнатная), Oestrus ovis (овод овечий), Oscinella frit (мушка шведская), Pegomyia betae (муха свекловичная), Phorbia spp., Psila rosae (муха морковная), Rhagoletis cerasi (муха вишневая), Rhagoletis pomonella (личинка пестрокрылки яблонной), Sitodiplosis mosellana (оранжевая злаковая галлица), Stomoxys calcitrans (жигалка обыкновенная), Tabanus spp. (слепни) и Tipula spp. (долгоножки).
В других вариантах осуществления способ, предлагаемый в настоящем изобретении, можно использовать для борьбы с представителями отряда полужесткокрылые (клопы настоящие полужесткокрылые) включая, но не ограничиваясь только ими, Acrosternum hilare (клоп-щитник), Blissus leucopterus (земляной клоп), Calocoris norvegicus (клоп картофельный), Cimex hemipterus (клоп постельный тропический), Cimex lectularius (клоп постельный), Dagbertus fasciatus, Dichelops furcatus, Dysdercus suturellus (красноклоп хлопковый), Edessa meditabunda, Eurygaster maura (черепашка маврская), Euschistus heros, Euschistus servus (щитник коричневый), Helopeltis antonii, Helopeltis theivora (слепняк чайный индийский), Lagynotomus spp. (щитники), Leptocorisa oratorius, Leptocorisa varicornis, Lygus spp. (слепняки), Lygus hesperus (клоп травяной западный), Maconellicoccus hirsutus, Neurocolpus longirostris, Nezara viridula (южный зеленый овощной клоп), Phytocoris spp. (слепняки), Phytocoris californicus, Phytocoris relativus, Piezodorus guildingi, Poecilocapsus lineatus (четырехполосый слепняк), Psallus vaccinicola, Pseudacysta perseae, Scaptocoris castanea и Triatoma spp. (кровососущие конусоносные триатомы/поцелуйные клопы).
В дополнительных вариантах осуществления способ, предлагаемый в настоящем изобретении, можно использовать для борьбы с представителями отряда равнокрылые (тли, равнокрылые, белокрылки, цикадки) включая, но не ограничиваясь только ими, Acrythosiphon pisum (тля гороховая), Adelges spp. (хермесы), Aleurodes proletella (белокрылка капустная), Aleurodicus disperses, Aleurothrixus floccosus (шерстистая белокрылка), Aluacaspis spp., Amrasca bigutella bigutella, Aphrophora spp. (цикадки), Aonidiella aurantii (щитовка красная померанцевая), Aphis spp. (тли), Aphis gossypii (тля хлопковая), Aphis pomi (тля яблонная), Aulacorthum solani (тля картофельная обыкновенная), Bemisia spp. (белокрылки), Bemisia argentifolii, Bemisia tabaci (табачная белокрылка), Brachycolus noxius (тля ячменная), Brachycorynella asparagi (тля спаржевая), Brevennia rehi, Brevicoryne brassicae (тля капустная), Ceroplastes spp. (равнокрылые), Ceroplastes rubens (ложнощитовка рубиновая), Chionaspis spp.(равнокрылые), Chrysomphalus spp. (равнокрылые), Coccus spp. (равнокрылые), Dysaphis plantaginea (тля розовая), Empoasca spp. (цикадки), Eriosoma lanigerum (тля кровяная яблонная), Icerya purchasi (червец австралийский желобчатый), Idioscopus nitidulus (манговая цикадка), Laodelphax striatellus (малый коричневый дельфацид), Lepidosaphes spp., Macrosiphum spp., Macrosiphum euphorbiae (тля картофельная), Macrosiphum granarium (тля злаковая), Macrosiphum rosae (тля розанная зеленая), Macrosteles quadrilineatus (астровая цикадка), Mahanarva frimbiolata, Metopolophium dirhodum (тля розанно-злаковая), Mictis longicornis, Myzus spp., Myzus persicae (тля персиковая зеленая), Nephotettix spp. (цикадки), Nephotettix cinctipes (цикадка зеленая), Nilaparvata lugens (коричневый дельфацид), Parlatoria pergandii (щитовка цитрусовая фиолетовая), Parlatoria ziziphi (щитовка черная), Peregrinus maidis (цикадка кукурузная), Philaenus spp. (пенницы), Phylloxera vitifoliae (филлоксера виноградная), Physokermes piceae (ложнощитовка еловая малая), Planococcus spp. (войлочники), Pseudococcus spp. (войлочники), Pseudococcus brevipes (мучнистый червец ананасовый), Quadraspidiotus perniciosus (щитовка калифорнийская), Rhapalosiphum spp. (тли), Rhapalosiphum maida (тля кукурузная), Rhapalosiphum padi (тля черемухо-злаковая), Saissetia spp. (равнокрылые), Saissetia oleae (червец черный), Schizaphis graminum (тля злаковая обыкновенная), Sitobion avenae (тля злаковая), Sogatella furcifera (дельфацид белоспинный), Therioaphis spp. (тли), Toumeyella spp. (равнокрылые), Toxoptera spp. (тли), Trialeurodes spp. (белокрылки), Trialeurodes vaporariorum (белокрылка тепличная), Trialeurodes abutiloneus (белокрылка окаймленнокрылая), Unaspis spp. (равнокрылые), Unaspis yanonensis (щитовка восточная цитрусовая) и Zulia entreriana. По меньшей мере в некоторых вариантах осуществления способ, предлагаемый в настоящем изобретении, можно использовать для борьбы с Myzus persicae.
В других вариантах осуществления способ, предлагаемый в настоящем изобретении, можно использовать для борьбы с представителями отряда перепончатокрылые (муравьи, осы и пчелы), включая, но не ограничиваясь только ими, Acromyrrmex spp., Athalia rosae, Atta spp. (муравьи-листорезы), Camponotus spp. (муравьи-древоточцы), Diprion spp. (пилильщики), Formica spp. (ants), Iridomyrmex humilis (муравей аргентинский), Monomorium ssp., Monomorium minumum (муравей малый), Monomorium pharaonis (муравей домовый), Neodiprion spp. (пилильщики), Pogonomyrmex spp. (муравей-жнец), Polistes spp. (бумажные осы), Solenopsis spp. (муравьи огненные), Tapoinoma sessile (муравей домашний пахучий), Tetranomorium spp. (муравьи дерновые), Vespula spp. (настоящие осы) и Xylocopa spp. (пчелы-плотники).
В некоторых вариантах осуществления способ, предлагаемый в настоящем изобретении, можно использовать для борьбы с представителями отряда термиты (термиты), включая, но не ограничиваясь только ими, Coptotermes spp., Coptotermes curvignathus, Coptotermes frenchii, Coptotermes formosanus (китайский подземный термит), Cornitermes spp. (термиты-солдаты с рострумом), Cryptotermes spp. (термиты, поедающие сухое дерево), Heterotermes spp. (пустынные ринотермиты), Heterotermes aureus, Kalotermes spp. (термиты, поедающие сухое дерево), Incistitermes spp. (термиты, поедающие сухое дерево), Macrotermes spp. (термиты, разводящие грибковые сады), Marginitermes spp. (термиты, поедающие сухое дерево), Microcerotermes spp. (термиты-жнецы), Microtermes obesi, Procornitermes spp., Reticulitermes spp. (ринотермитиды), Reticulitermes banyulensis, Reticulitermes grassei, Reticulitermes flavipes (термит желтоногий), Reticulitermes hageni, Reticulitermes hesperus (западный ринотермит), Reticulitermes santonensis, Reticulitermes speratus, Reticulitermes tibialis, Reticulitermes virginicus, Schedorhinotermes spp. и Zootermopsis spp. (термиты, поедающие трухлявое дерево).
В дополнительных вариантах осуществления способ, предлагаемый в настоящем изобретении, можно использовать для борьбы с представителями отряда чешуекрылые (моли и бабочки)), включая, но не ограничиваясь только ими, Achoea janata, Adoxophyes spp., Adoxophyes orana, Agrotis spp. (совки), Agrotis ipsilon (совка-ипсилон), Alabama argillacea (гусеница хлопковая), Amorbia cuneana, Amyelosis transitella (гусеница, вредящая цитрусовым), Anacamptodes defectaria, Anarsia lineatella (моль фруктовая полосатая), Anomis sabulifera (джутовая пяденица), Anticarsia gemmatalis (гусеница, вредящая соевым культурам), Archips argyrospila (листовертка плодовых деревьев), Archips rosana (листовертка европейская), Argyrotaenia spp. (листовертки), Argyrotaenia citrana (листовертка апельсиновая), Autographa gamma, Bonagota cranaodes, Borbo cinnara (огневка рисовая), Bucculatrix thurberiella (сверлильщик хлопковый), Caloptilia spp. (минирующие мушки), Capua reticulana, Carposina niponensis (персиковая плодожорка), Chilo spp., Chlumetia transversa (листовертка манговая), Choristoneura rosaceana (скошеннополосая листовертка), Chrysodeixis spp., Cnaphalocerus medinalis (листовертка травяная), Colias spp., Conpomorpha cramerella, Cossus cossus (древоточец), Crambus spp. (луговые мотыльки), Cydiafunebrana (плодожорка сливовая), Cydia molesta (плодожорка восточная персиковая), Cydia nignicana (листовертка гороховая), Cydia pomonella (плодожорка яблонная), Darna diducta, Diaphania spp. (стеблевые точильщики), Diatraea spp. (стеблевые точильщики), Diatraea saccharalis (огневка сахарного тростника), Diatraea graniosella (огневка кукурузная юго-западная), Earias spp. (совки хлопковые), Earias insulata (Совка хлопковая египетская), Earias vitella (северная совка шершавая), Ecdytopopha aurantianum, Elasmopalpus lignosellus (мотылек малый кукурузный), Epiphysias postruttana (светло-коричневая моль яблонная), Ephestia spp. (огневки мельничные), Ephestia cautella (огневка сухофруктовая), Ephestia elutella (моль табачная), Ephestia kuehniella (огневка амбарная), Epimeces spp., Epinotia aporema, Erionota thrax (листовертка банановая), Eupoecilia ambiguella (листовертка виноградная), Euxoa auxiliaris (гусеница озимой совки), Feltia spp. (совки), Gortyna spp. (сверлильщики), Grapholita molesta (плодожорка восточная персиковая), Hedylepta indicata (соевый мотылек), Helicoverpa spp. (ночницы), Helicoverpa armigera (совка хлопковая), Helicoverpa zea (совка хлопковая/кукурузная), Heliothis spp. (ночницы), Heliothis virescens (табачная листовертка), Hellula undalis (огневка капустная), Indarbela spp. (сверлильщики корневые), Keiferia lycopersicella (нематода томатная), Leucinodes orbonalis (баклажанный сверлильщик), Leucoptera malifoliella, Lithocollectis spp., Lobesia botrana (листовертка гроздевая), Loxagrotis spp. (ночницы), Loxagrotis albicosta (совка западная бобовая), Lymantria dispar (шелкопряд непарный), Lyonetia clerkella (моль яблонная минирующая), Mahasena corbetti (мешочницы масляной пальмы), Malacosoma spp. (коконопряды), Mamestra brassicae (совка капустная), Maruca testulalis (огневка акациевая), Metisa plana (мешочница), Mythimna unipuncta (гладкий походный червь), Neoleucinodes elegantalis (маленький томатный точильщик), Nymphula depunctalis (рисовая куколка), Operophthera brumata (пяденица зимняя), Ostrinia nubilalis (мотылек кукурузный), Oxydia vesulia, Pandemis cerasana (листовертка кривоусая смородинная), Pandemis heparana (коричневая яблочная листовертка), Papilio demodocus, Pectinophora gossypiella (розовый коробочный червь), Peridroma spp. (совки), Peridroma saucia (совка грязнобурая земляная), Perileucoptera coffeella (белая кофейная минирующая мушка), Phthorimaea operculella (картофельная моль), Phyllocnisitis citrella, Phyllonorycter spp. (минирующие мушки), Pieris rapae (белянка репная), Plathypena scabra, Plodia interpunctella (моль индийская мучная), Plutella xylostella (моль капустная), Polychrosis viteana (листовертка виноградная), Prays endocarpa, Prays oleae (моль маслинная), Pseudaletia spp. (ночницы), Pseudaletia unipunctata (походный червь), Pseudoplusia includens (пяденица соевая), Rachiplusia nu, Scirpophaga incertulas, Sesamia spp. (сверлильщики), Sesamia inferens (розовая совка рисовая стеблевая), Sesamia nonagrioides, Setora nitens, Sitotroga cerealella (моль зерновая амбарная), Sparganothis pilleriana, Spodoptera spp. (походные черви), Spodoptera exigua (совка малая), Spodoptera fugiperda (совка травяная), Spodoptera oridania (южные походные черви), Synanthedon spp. (сверлильщики корневые), Thecla basilides, Thermisia gemmatalis, Tineola bisselliella (моль комнатная), Trichoplusia ni (совка ни), Tuta absсoluta, Yponomeuta spp., Zeuzera coffeae (сверлильщик красных веток), and Zeuzera pyrina (древесница въедливая). По меньшей мере в некоторых вариантах осуществления способ, предлагаемый в настоящем изобретении, можно использовать для борьбы с Spodoptera exigua.
Способ, предлагаемый в настоящем изобретении, также можно использовать для борьбы с представителями отряда пухоеды (пухоеды), включая, но не ограничиваясь только ими, Bovicola ovis (власоед овечий), Menacanthus stramineus (пухоед двухщетинковый куриный) и Menopon gallinea (пухоед куриный).
В дополнительных вариантах осуществления способ, предлагаемый в настоящем изобретении, можно использовать для борьбы с представителями отряда прямокрылые (кузнечики, саранча и сверчки), включая, но не ограничиваясь только ими, Anabrus simplex (Кузнечик-мормон), Gryllotalpidae (медведки обыкновенные), Locusta migratoria, Melanoplus spp. (кузнечики), Microcentrum retinerve (кузнечик углокрылый), Pterophylla spp. (кузнечики), chistocerca gregaria, Scudderia furcata (кузнечик вилохвостый) и Valanga nigricorni.
В других вариантах осуществления способ, предлагаемый в настоящем изобретении, можно использовать для борьбы с представителями отряда пухоеды и вши (вши), включая, но не ограничиваясь только ими, Haematopinus spp. (вши крупного рогатого скота и свиней), Linognathus ovillus (вошь овечья), Pediculus humanus capitis (головная вошь), Pediculus humanus humanus (нательные вши), and Pthirus pubis (вошь лобковая).
В предпочтительных вариантах осуществления способ, предлагаемый в настоящем изобретении, можно использовать для борьбы с представителями отряда блохи (блохи), включая, но не ограничиваясь только ими, Ctenocephalides canis (блоха собачья), Ctenocephalides felis (блоха кошачья), and Pulex irritans (блоха человеческая).
В дополнительных вариантах осуществления способ, предлагаемый в настоящем изобретении, можно использовать для борьбы с представителями отряда бахромчатокрылые (трипсы), включая, но не ограничиваясь только ими, Frankliniella fusca (трипс табачный), Frankliniella occidentalis (трипс цветочный западный), Frankliniella shultzei, Frankliniella williamsi (трипс хлебный), Heliothrips haemorrhaidalis (трипс тепличный), Riphiphorothrips cruentatus, Scirtothrips spp., Scirtothrips citri (трипс цитрусовый), Scirtothrips dorsalis (трипс желтый чайный), Taeniothrips rhopalantennalis, and Thrips spp.
Способ, предлагаемый в настоящем изобретении, также можно использовать для борьбы с представителями отряда щетинохвостки (щетинохвостки), включая, но не ограничиваясь только ими, Lepisma spp. (чешуйницы) и Thermobia spp. (чешуйницы домашние).
В других вариантах осуществления способ, предлагаемый в настоящем изобретении, можно использовать для борьбы с представителями отряда клещи (клещи и зудни), включая, но не ограничиваясь только ими, Acarapsis woodi (трахеальный клещ медоносных пчел), Acarus spp. (тироглифоидные клещи), Acarus siro (зерновой клещ), Aceria mangiferae (клещ манговых почек), Aculops spp., Aculops lycopersici (ржавчинный клещ томатов), Aculops pelekasi, Aculus pelekassi, Aculus schlechtendali (ржавчинный яблонный клещ), Amblyomma americanum (иксодовый клещ Amblyomma), Boophilus spp. (зудни), Brevipalpus obovatus (красный плоский клещ), Brevipalpus phoenicis (красно-черный плоский клещ), Demodex spp. (зудни чесоточные), Dermacentor spp. (твердые клещи), Dermacentor variabilis (собачий иксодовый клещ), Dermatophagoides pteronyssinus (клещ домашней пыли), Eotetranycus spp., Eotetranychus carpini (желтый грабовый паутинный клещ), Epitimerus spp., Eriophyes spp., Ixodes spp. (зудни), Metatetranycus spp., Notoedres cati, Oligonychus spp., Oligonychus coffee, Oligonychus ilicus (клещик паутинный южный), Panonychus spp., Panonychus citri (клещик красный цитрусовый), Panonychus ulmi (Клещ красный плодовый), Phyllocoptruta oleivora (цитрусовый ржавчинный клещ), Polyphagotarsonemun latus (оранжерейный прозрачный клещ), Rhipicephalus sanguineus (коричневый собачий клещ), Rhizoglyphus spp. (клещики корневые), Sarcoptes scabiei (клещ чесоточный), Tegolophus perseaflorae, Tetranychus spp., Tetranychus urticae (клещик паутинный двупятнистый) и Varroa destructor (клещ медоносных пчел).
В дополнительных вариантах осуществления способ, предлагаемый в настоящем изобретении, можно использовать для борьбы с представителями отряда нематоды (нематоды), включая, но не ограничиваясь только ими, Aphelenchoides spp. (листовые нематоды), Belonolaimus spp. (жалящие нематоды), Criconemella spp. (кольцевые нематоды), Dirofilaria immitis (сердечные черви), Ditylenchusspp. (стеблевые и клубеньковые нематоды), Heterodera spp. (гетеродериды), Heterodera zeae (цистообразующая нематода), Hirschmanniella spp. (корневые нематоды), Hoplolaimus spp. (ланцетовидные нематоды), Meloidogyne spp. (галловые нематоды), Meloidogyne incognita (яванская галловая нематода), Onchocerca volvulus (онхоцерка), Pratylenchus spp. (ранящие нематоды), Radopholus spp. (сверлящие нематоды) и Rotylenchus reniformis (почковидная нематода).
По меньшей мере в некоторых вариантах осуществления способ, предлагаемый в настоящем изобретении, можно использовать для борьбы по меньшей мере с одним насекомым одного или большего количества следующих отрядов: чешуекрылые, жесткокрылые, полужесткокрылые, бахромчатокрылые, термиты, прямокрылые, двукрылые, перепончатокрылые и блохи, и по меньшей мере с одним клещом отряда клещи.
Исследование инсектицидов
Пример A: Биологическое исследование для тли персиковой зеленой (Myzus persicae) (ТПЗ) (MYZUPE).
Тля персиковая зеленая (Myzus persicae) является наиболее существенной тлей-вредителем персиковых деревьев, вызывающим уменьшение роста, увядание листьев и гибель различных тканей. Она также является опасной, поскольку действует в качестве вектора переноса вирусов растений, таких как вирус Y картофеля и вирус скручивания листьев картофеля, действующий на представителей паслена/картофеля семейства пасленовые, и различные вирусы мозаики, действующие на многие другие продовольственные сельскохозяйственные культуры. ТПЗ, наряду с другими растениями, поражает такие растения, как брокколи, лопух, капуста, морковь, цветная капуста, дайкон, баклажан, зеленая фасоль, латук, макадамия, папайя, перцы, батат, томаты, кресс водяной и цукини. ТПЗ также поражает многие декоративные культуры, такие как гвоздика, хризантема, цветущая белокочанная капуста, пуансеттия и розы. ТПЗ приобрела устойчивость по отношению ко многим пестицидам.
В качестве исследуемого субстрата использовали рассаду капусты, выращенную в горшках размером 7,6 см, в стадии 2-3 небольших (3-5 см) настоящих листьев. Рассаду заражали с помощью 20-50 ТПЗ (бескрылые взрослые особи и находящиеся на стадии куколок) за день до нанесения химиката. Для каждой обработки использовали 4 горшка с отдельными экземплярами рассады. Исследуемые соединения (2 мг) растворяли в 2 мл растворителя ацетон/метанол (1:1) и получали исходные растворы исследуемого соединения концентрации 1000 част./млн. Исходные растворы разбавляли 5×с помощью 0,025% Tween 20 в H2O и получали раствор исследуемого соединения концентрации 200 част./млн. Для опрыскивания обеих сторон листьев капусты до стекания жидкости использовали ручной опрыскиватель аспираторного типа. Контрольные растения (контроль растворителем) опрыскивали только разбавителем, представляющим собой растворитель 20 об.% ацетон/метанол (1:1). Обработанные растения до оценки помещали в камеру для хранения на 3 дня при температуре, равной примерно 25°C, и относительной влажности (ОВ) окружающей среды. Оценку проводили путем проводимого под микроскопом подсчета количества живых тлей для каждого растения. Степень уничтожения в процентах определяли по корректирующей формуле Эбботта (W.S. Abbott, "A Method of Computing the Effectiveness of an Insecticide" J. Econ. Entomol. 18 (1925), pp,265-267) следующим образом.
Скорректированная степень уничтожения, % = 100*(X - Y)/X
где
X = количество живых тлей на растениях, опрысканных только растворителем, и
Y = количество живых тлей на обработанных растениях.
Результаты приведены в таблице под названием "Таблица 2. Биологические данные для тли персиковой зеленой (ТПЗ) (MYZUPE) и гусеницы табачной белокрылки (БГ) (BEMITA)" (см. раздел, содержащий таблицы).
Пример B: Исследование инсектицидов для гусеницы табачной белокрылки (БГ) (Bemisia tabaci) (BEMITA) с помощью некорневого опрыскивания.
Сообщали, что табачная белокрылка (Bemisia tabaci) является существенным вредителем возделываемых сельскохозяйственных культур во всем мире. Она обладает чрезвычайно большим кругом хозяев, поражающих более 500 видов растений, относящихся к 63 семействам растений. Сорняки часто выступают в качестве альтернативных хозяев вредителей сельскохозяйственных культур. Повреждение при непосредственном кормлении вызывается прокалыванием и высасыванием сока из листьев растений. Это кормление приводит к ослаблению и раннему увяданию растения и уменьшает рост растения и урожайность. Непрямое повреждение приводит к накоплению клейкой жидкости, выделяемой белокрылками. Клейкая жидкость выступает в качестве субстрата для роста черных плесневых налетов на листьях и плодах, что ослабляет фотосинтез и снижает рыночную стоимость растений или урожайность. Повреждение также происходит, когда табачная белокрылка действует в качестве вектора вирусов растений. Табачная белокрылка считается самым распространенным и важным вектором белокрылки вирусов растений во всем мире.
В качестве исследуемого субстрата использовали растения хлопчатника (Gossypium hirsutum), выращенные в горшках размером 7,6 см, в стадии 1 небольшого (4-5 см) настоящего листа. Растения заражали с помощью 200-400 яиц белокрылки за 4-5 дней до нанесения химиката. Для каждой обработки использовали 4 горшка с отдельными экземплярами растения. Исследуемые соединения (2 мг) растворяли в 1 мл растворителя ацетона и получали исходные растворы исследуемого соединения концентрации 2000 част./млн. Исходные растворы разбавляли 10× с помощью 0,025% Tween 20 в H2O (разбавители) и получали раствор исследуемого соединения концентрации 200 част./млн. Для опрыскивания обеих сторон листьев хлопчатника до стекания жидкости использовали ручной опрыскиватель аспираторного типа. Контрольные растения (контроль растворителем) опрыскивали только разбавителем, содержащим 10 об.% растворителя ацетона. Обработанные растения до оценки помещали в камеру для хранения на 9 дней при температуре, равной примерно 25°C, и относительной влажности (ОВ) окружающей среды. Оценку проводили путем проводимого под микроскопом подсчета количества живых личинок стадии 3-4 для каждого растения. Степень уничтожения в процентах определяли по корректирующей формуле Эбботта (W.S. Abbott, "A Method of Computing the Effectiveness of an Insecticide" J. Econ. Entomol. 18 (1925), pp,265-267) следующим образом.
Скорректированная степень уничтожения, % = 100*(X - Y)/X
где
X = количество живых личинок на растениях, опрысканных только растворителем, и
Y = количество живых личинок на обработанных растениях.
В таблице 2 указаны пестицидные активности пестицидных соединений по отношению к тле персиковой зеленой (ТПЗ) (MYZUPE) и гусеницам табачной белокрылки (БГ, BEMITA). Эффективность уничтожения для пестицидных соединений по отношению к насекомым ТПЗ и БГ определяли после обработки. Эффективность уничтожения для раскрытых пестицидных соединений по отношению к насекомым ТПЗ и БГ оценивали, как указано в таблице 1.
|
|
Приведенные ниже примеры предназначены для более подробного описания вариантов осуществления настоящего изобретения. Эти примеры не следует рассматривать, как исчерпывающие или исключительные применительно к объему настоящего изобретения.
ПРИМЕРЫ
Эти примеры предназначены для иллюстрации и их не следует рассматривать, как ограничивающие настоящее изобретение только вариантами осуществления, раскрытыми в этих примерах.
Исходные вещества, реагенты и растворители, которые получали из коммерческих источников, использовали без дополнительной очистки. Безводные растворители марки SURE/SEAL™ приобретали у фирмы Aldrich и использовали в том виде, в котором они были поставлены. Температуры плавления измеряли с помощью капиллярного аппарата для измерения температур плавления Thomas Hoover Unimelt или автоматической системы для определения температур плавления OptiMelt, выпускающейся фирмой Stanford Research Systems, и не корректировали. Примеры, которые проводили при "комнатной температуре", выполняли в лабораториях с использованием кондиционеров с поддержанием температуры в диапазоне от примерно 20°C до примерно 24°C. Для молекул приведены их известные названия, полученные с помощью программ по составлению названий, входящих в программы ISIS Draw, ChemDraw или ACD Name Pro. Если такие программы не способны образовать название молекулы, то ее название образуют по обычным правилам образования названий. Данные спектров 1H ЯМР приведены в част./млн (δ) и спектры снимали при 300, 400 или 600 МГц. Данные спектров 13C ЯМР приведены в част./млн (δ) и спектры снимали при 75, 100 или 150 МГц. Данные спектров 19F ЯМР приведены в част./млн (δ) и спектры снимали при 376 МГц, если не указано иное.
Пример 1: Получение N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-(циклопропилметил)-2-(2-оксопирролидин-1-ил)ацетамида (соединение F98)
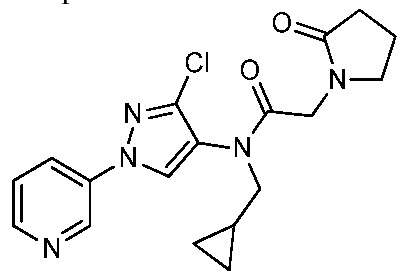
Во флакон объемом 3 мл добавляли 3-хлор-N-(циклопропилметил)-1-(пиридин-3-ил)-1H-пиразол-4-амин (0,124 г, 0,500 ммоля) (получали в соответствии с публикацией U.S. № 2012/0110702), ДМАП (0,183 г, 1,50 ммоля), 2-(2-оксопирролидин-1-ил)уксусную кислоту (0,143 г, 1,00 ммоля), EDCI (0,240 г, 1,25 ммоля), затем CH2Cl2 (1 мл). Реакционную смесь перемешивали при температуре, равной примерно 25°C в течение 18 ч, затем ее очищали с помощью хроматографии на силикагеле (0%-15% MeOH/CH2Cl2) и получали искомое соединение F98 в виде светло-желтого масла (0,131 г, 70%).
Указанные ниже молекулы получали по методикам, раскрытым в примере 1:
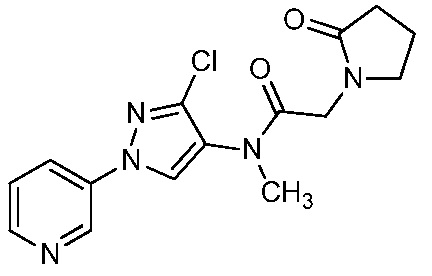
F6
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-метил-2-(2-оксопирролидин-1-ил)ацетамид (соединение F6) выделяли в виде почти белого твердого вещества (0,167 г, 100%).
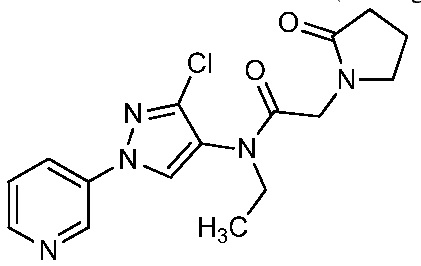
F124
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-2-(2-оксопирролидин-1-ил)ацетамид (соединение F124) выделяли в виде светло-желтого масла (0,169 г, 97%).
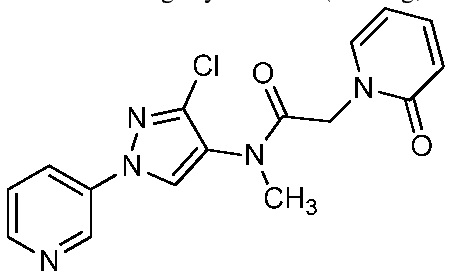
F3
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-метил-2-(2-оксопиридин-1(2H)-ил)ацетамид (соединение F3) выделяли в виде белого полужидкого вещества (0,056 г, 33%).
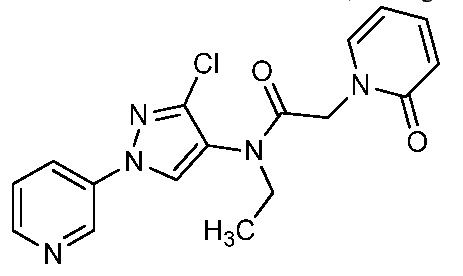
F122
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-2-(2-оксопиридин-1(2H)-ил)ацетамид (соединение F122) выделяли в виде белого полужидкого вещества (0,054 г, 30%).
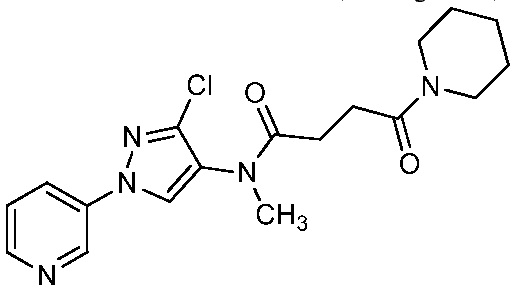
F33
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-метил-4-оксо-4-(пиперидин-1-ил)бутанамид (соединение F33) выделяли в виде белого твердого вещества (0,181 г, 95%).
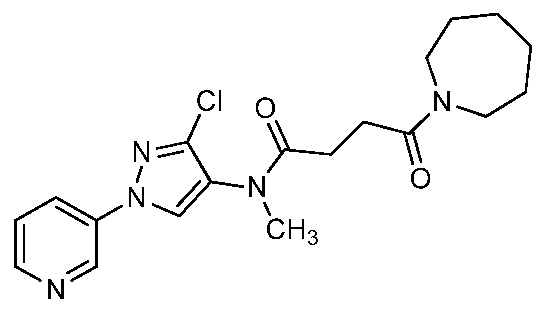
F27
4-(Азепан-1-ил)-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-метил-4-оксобутанамид (соединение F27) выделяли в виде белого твердого вещества (0,188 г, 96%).
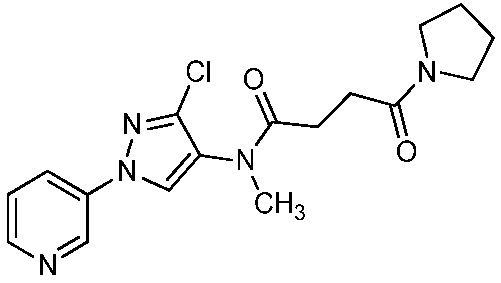
F37
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-метил-4-оксо-4-(пирролидин-1-ил)бутанамид (соединение F37) выделяли в виде белого твердого вещества (0,180 г, 99%).
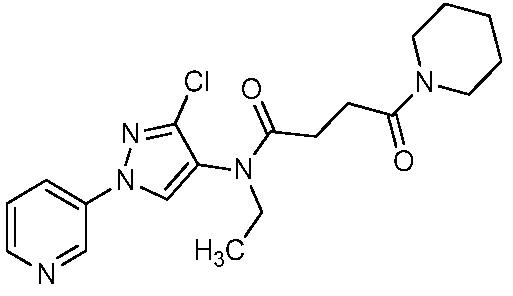
F21
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-оксо-4-(пиперидин-1-ил)бутанамид (соединение F21) выделяли в виде почти белого твердого вещества (0,192 г, 98%).
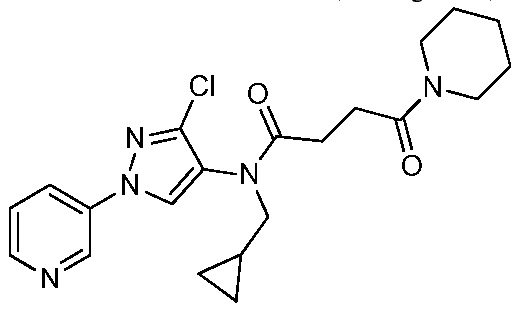
F82
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-(циклопропилметил)-4-оксо-4-(пиперидин-1-ил)бутанамид (соединение F82) выделяли в виде почти белого твердого вещества (0,140 г, 67%).
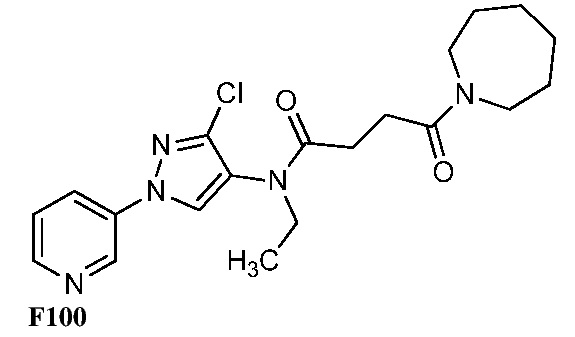
F100
4-(Азепан-1-ил)-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-оксобутанамид (соединение F100) выделяли в виде почти белого твердого вещества (0,181 г, 90%).
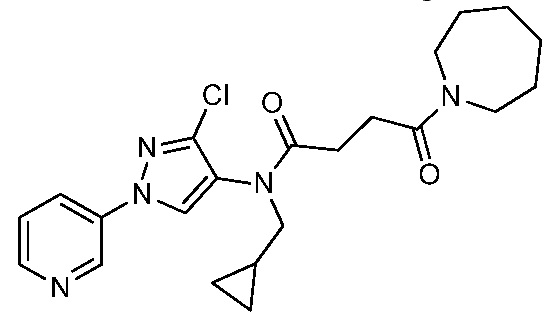
F18
4-(Азепан-1-ил)-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-(циклопропилметил)-4-оксобутанамид (соединение F18) выделяли в виде почти белого твердого вещества (0,167 г, 78%).
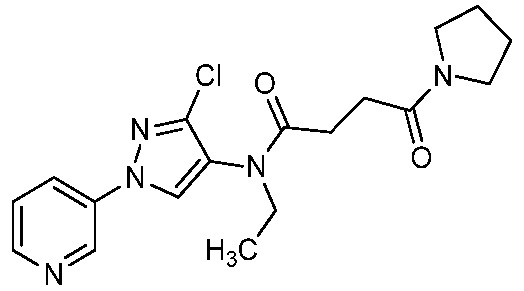
F106
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-оксо-4-(пирролидин-1-ил)бутанамид (соединение F106) выделяли в виде светло-желтого полужидкого вещества (0,125 г, 67%).
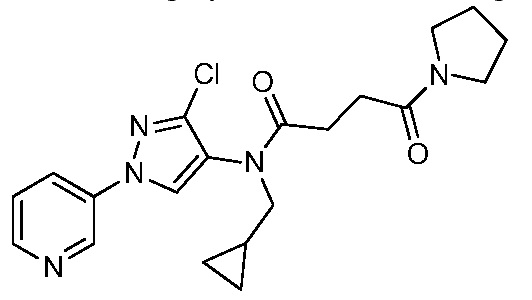
F95
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-(циклопропилметил)-4-оксо-4-(пирролидин-1-ил)бутанамид (соединение F95) выделяли в виде светло-желтого твердого вещества (0,130 г, 65%).
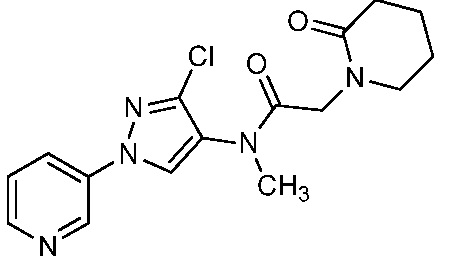
F77
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-метил-2-(2-оксопиперидин-1-ил)ацетамид (соединение F77) выделяли в виде почти белого твердого вещества (0,062 г, 36%).
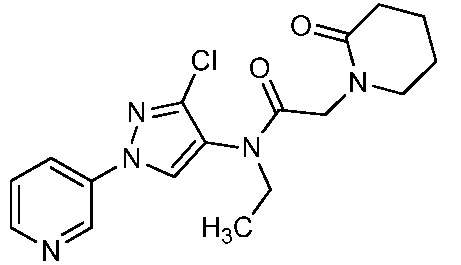
F47
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-2-(2-оксопиперидин-1-ил)ацетамид (соединение F47) выделяли в виде почти белого твердого вещества (0,045 г, 25%).
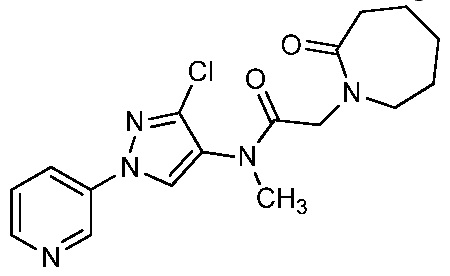
F22
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-метил-2-(2-оксоазепан-1-ил)ацетамид (соединение F22) выделяли в виде почти белого твердого вещества (0,162 г, 90%).
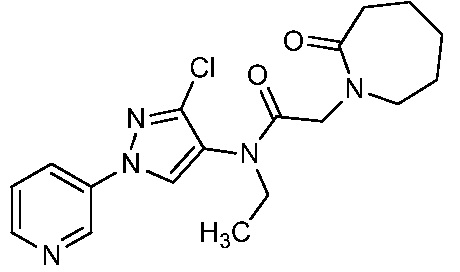
F123
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-2-(2-оксоазепан-1-ил)ацетамид (соединение F123) выделяли в виде светло-желтого полужидкого вещества (0,152 г, 81%).
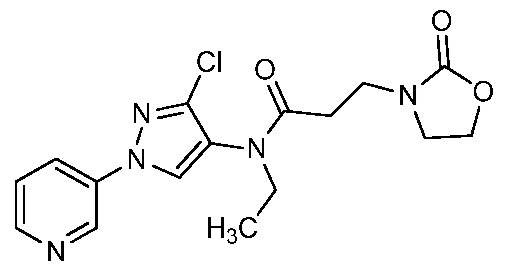
F69
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-3-(2-оксооксазилидин-3-ил)пропанамид (соединение 69) выделяли в виде бесцветного полужидкого вещества (0,178 г, 98%).
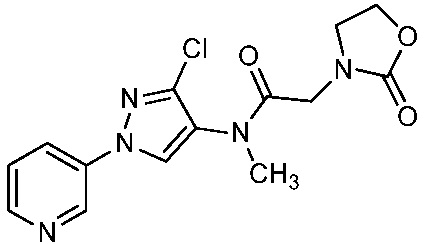
F111
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-метил-2-(2-оксооксазилидин-3-ил)ацетамид (соединение F111) выделяли в виде белого твердого вещества (0,150 г, 89%).
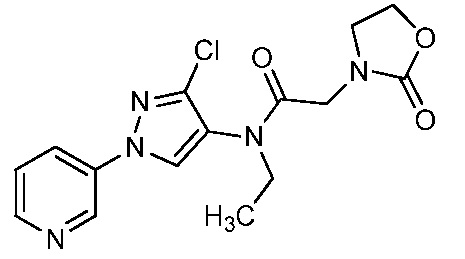
F48
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-2-(2-оксооксазилидин-3-ил)ацетамид (соединение F48) выделяли в виде белого твердого вещества (0,119 г, 68%).
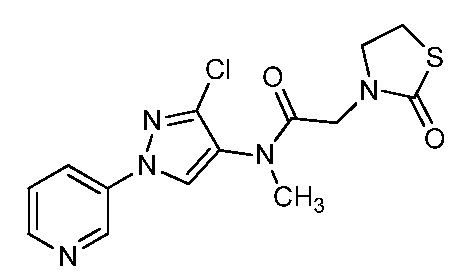
F7
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-метил-2-(2-оксотиазолидин-3-ил)ацетамид (соединение F7) выделяли в виде белого твердого вещества (0,166 г, 94%).
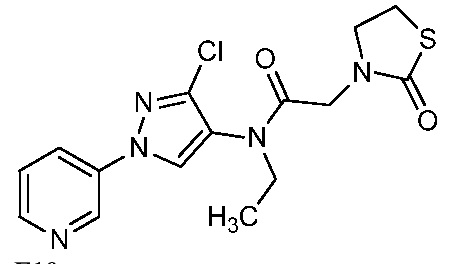
F10
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-2-(2-оксотиазолидин-3-ил)ацетамид (соединение F10) выделяли в виде белого твердого вещества (0,146 г, 80%).
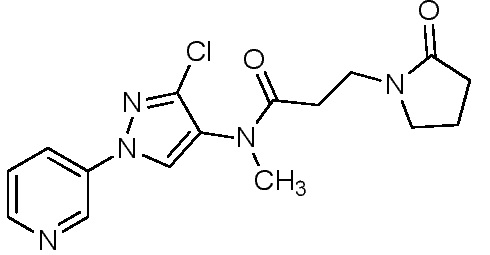
F107
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-метил-3-(2-оксопирролидин-1-ил)пропанамид (соединение F107) выделяли в виде бесцветного полужидкого вещества (0,167 г, 96%).
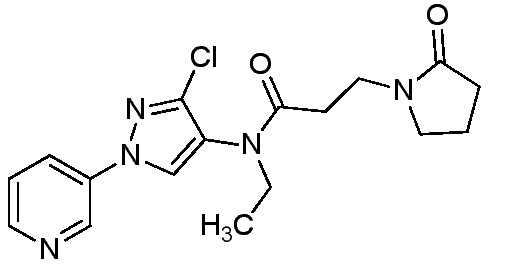
F39
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-3-(2-оксопирролидин-1-ил)пропанамид (соединение F39) выделяли в виде бесцветного масла (0,147 г, 81%).
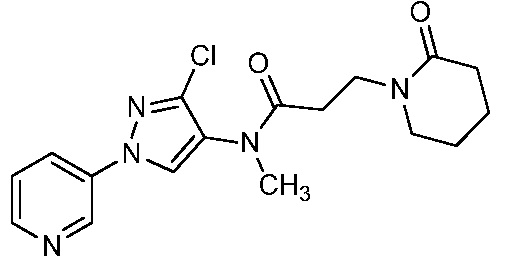
F49
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-метил-3-(2-оксопиперидин-1-ил)пропанамид (соединение F49) выделяли в виде бесцветного масла (0,193 г, 96%).
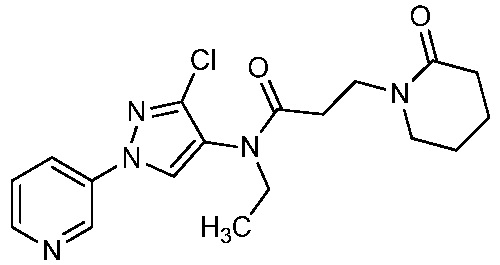
F8
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-3-(2-оксопиперидин-1-ил)пропанамид (соединение F8) выделяли в виде белого твердого вещества (0,155 г, 82%).
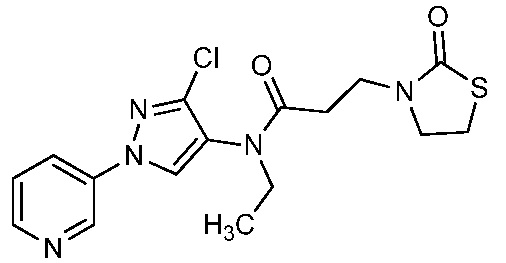
F88
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-3-(2-оксотиазолидин-3-ил)пропанамид (соединение F88) выделяли в виде бесцветного масла (0,091 г, 48%).
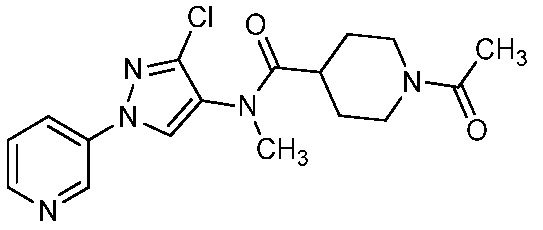
F29
1-Ацетил-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-метилпиперидин-4-карбоксамид (соединение F29) выделяли в виде белого полужидкого вещества (0,206 г, 85%).
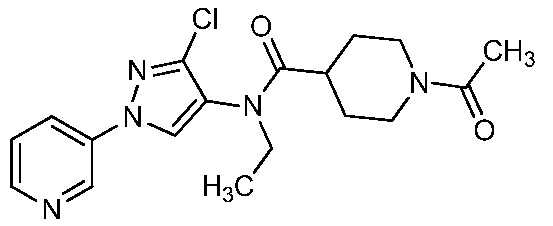
F61
1-Ацетил-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этилпиперидин-4-карбоксамид (соединение F61) выделяли в виде белого полужидкого вещества (0,217 г, 87%).
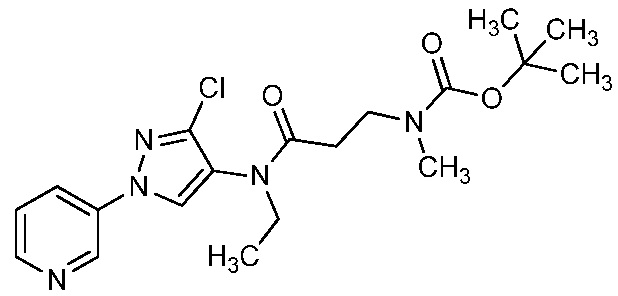
F52
трет-Бутил-(3-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-3-оксопропил)(метил)карбамат (соединение F52) выделяли в виде бесцветного масла (0,192 г, 75%).
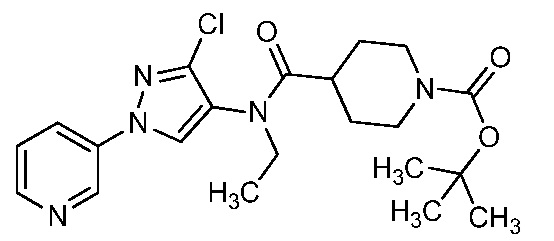
F110
трет-Бутил-4-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этилкарбамоил)пиперидин-1-карбоксилат (соединение F110) выделяли в виде белого полужидкого вещества (2 г, 77%).
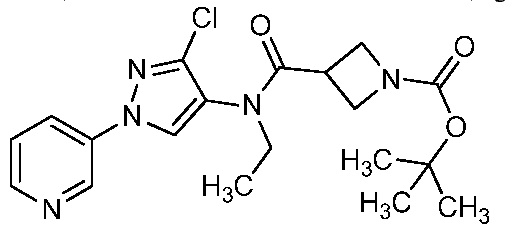
F26
трет-Бутил-3-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)карбамоилазетидин-1-карбоксилат (соединение F26) выделяли в виде белого полужидкого вещества (2 г, 82%).
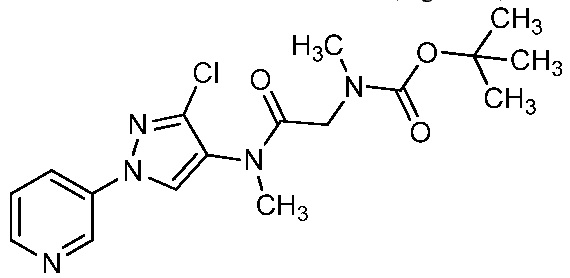
F90
трет-Бутил-(2-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(метил)амино)-2-оксоэтил)(метил)карбамат (соединение F90) выделяли в виде бесцветного масла (2 г, 73%).
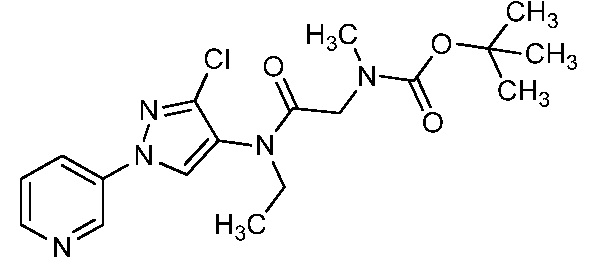
F4
трет-Бутил-(2-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-2-оксоэтил)(метил)карбамат (соединение F4) выделяли в виде бесцветного масла (0,616 г, 87%).
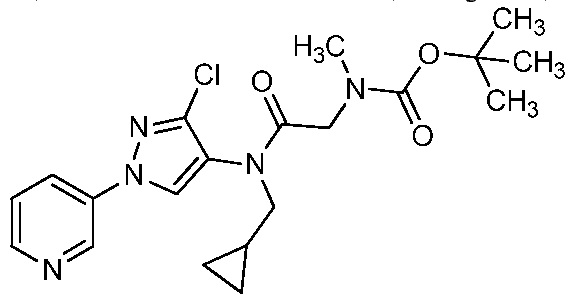
F76
трет-Бутил-(2-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(циклопропилметил)амино)-2-оксоэтил)(метил)карбамат (соединение F76) выделяли в виде белого полужидкого вещества (0,642 г, 95%).
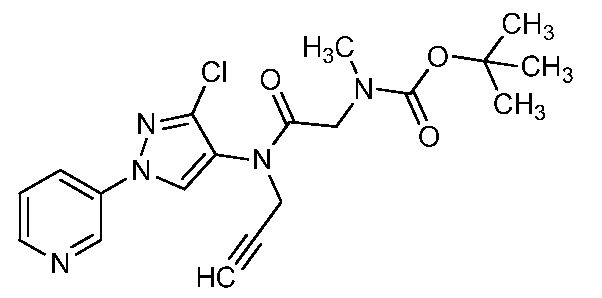
F23
трет-Бутил-(2-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(проп-2-ин-1-ил)амино)-2-оксоэтил)(метил)карбамат (соединение F23) выделяли в виде белого твердого вещества (0,513 г, 74%).
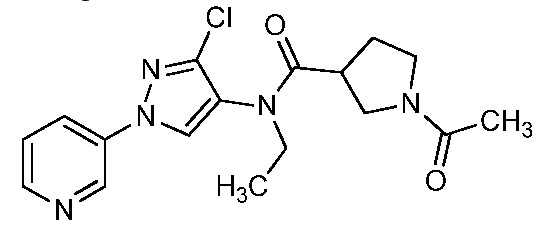
P20
1-Ацетил-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этилпирролидин-3-карбоксамид (соединение P20) выделяли в виде белого твердого вещества (0,202 г, 88%).
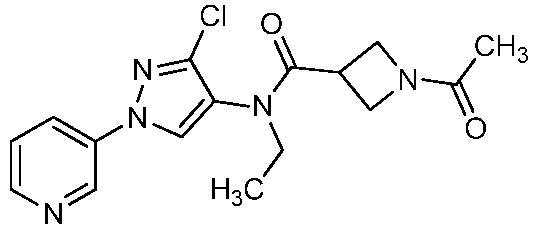
P23
1-Ацетил-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этилазетидин-3-карбоксамид (соединение P23) выделяли в виде белого твердого вещества (0,162 г, 74%).
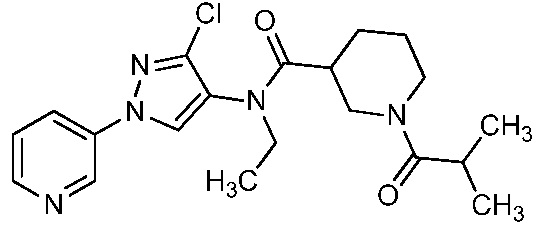
FA3
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-1-изобутирилпиперидин-3-карбоксамид (соединение FA3) выделяли в виде белого полужидкого вещества (0,216 г, 80%).
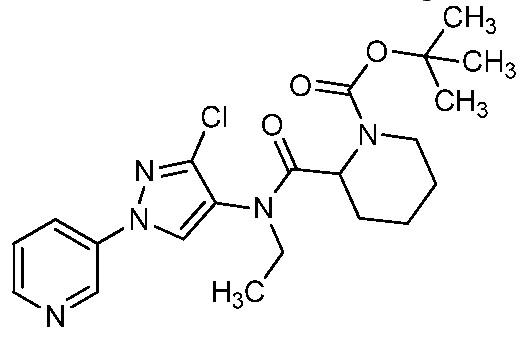
FA13
трет-Бутил 2-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)карбамоил)пиперидин-1-карбоксилат (соединение FA13) выделяли в виде белого полужидкого вещества (0,123 г, 28%).
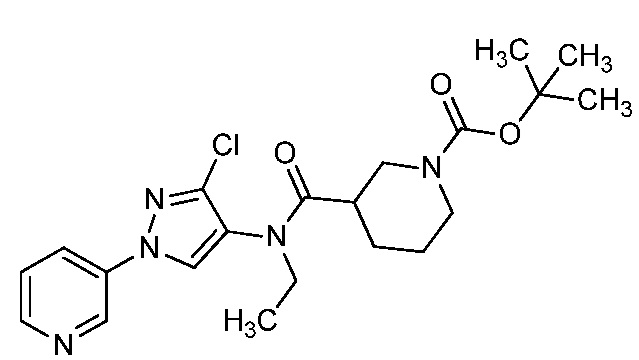
FA18
трет-Бутил-3-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)карбамоил)пиперидин-1-карбоксилат (соединение FA18) выделяли в виде желтого полужидкого вещества (1,08 г, 45%).
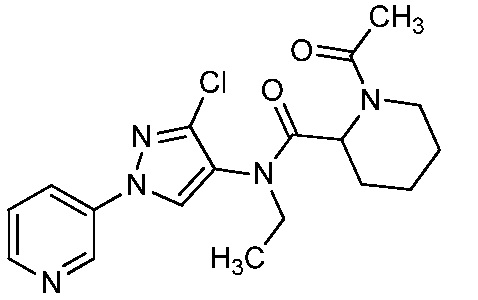
FA32
1-Ацетил-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этилпиперидин-2-карбоксамид (соединение FA32) выделяли в виде желтого масла (0,121 г, 61%).
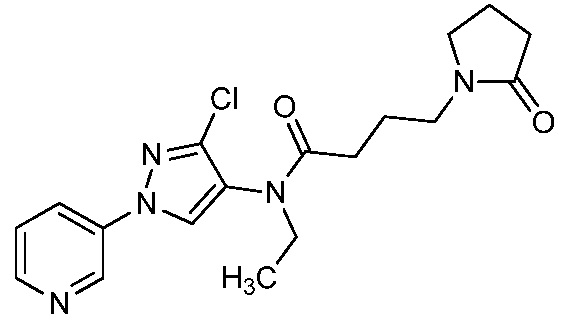
FA33
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(2-оксопирролидин-1-ил)бутанамид (соединение FA33) выделяли в виде желтого масла (0,151 г, 72%).

FA34
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(2-оксооксазилидин-3-ил)бутанамид (соединение FA34) выделяли в виде желтого масла (0,148 г, 71%).
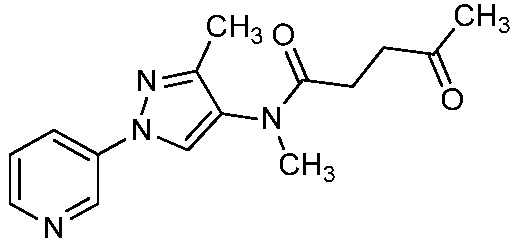
FA69
N-метил-N-(3-метил-1-(пиридин-3-ил)-1H-пиразол-4-ил)-4-оксопентанамид (соединение FA69) выделяли в виде бесцветного масла (0,114 г, 75%).
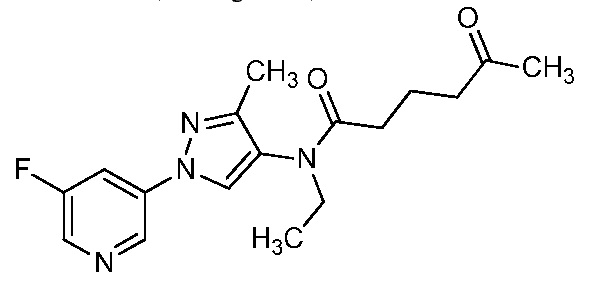
FA70
N-Этил-N-(1-(5-фторпиридин-3-ил)-3-метил-1H-пиразол-4-ил)-5-оксогексанамид (соединение FA70) выделяли в виде бесцветного масла (0,119 г, 79%).
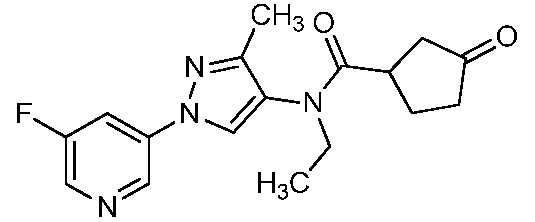
FA71
N-Этил-N-(1-(5-фторпиридин-3-ил)-3-метил-1H-пиразол-4-ил)-3-оксоциклопентанкарбоксамид (соединение FA71) выделяли в виде желтовато-коричневого твердого вещества (0,1 г, 62%).
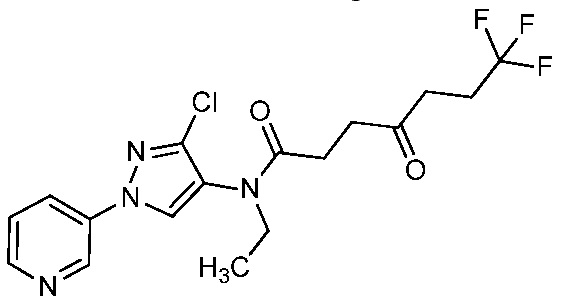
FA76
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-7,7,7-трифтор-4-оксогептанамид (соединение FA76) выделяли в виде коричневого вязкого масла (0,059 г, 50%).
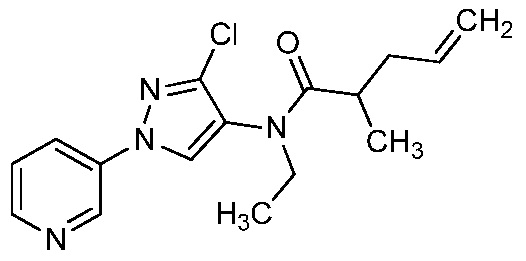
CA1
N-[3-Хлор-1-(3-пиридил)пиразол-4-ил]-N-этил-2-метилпент-4-енамид (соединение CA1) выделяли в виде прозрачного бесцветного масла (0,502 г, 75%): 1H ЯМР (400 МГц, CDCl3) δ 8,94 (дд, J=2,7, 0,8 Гц, 1H), 8,63 (дд, J=4,8, 1,5 Гц, 1H), 8,05 (ддд, J=8,3, 2,8, 1,5 Гц, 1H), 7,91 (c, 1H), 7,46 (ддд, J=8,4, 4,8, 0,8 Гц, 1H), 5,75 5,59 (м, 1H), 5,07 4,97 (м, 2H), 3,69 (д, J=47,8 Гц, 2H), 2,44 (ддт, J=28,2, 14,3, 7,2 Гц, 2H), 2,07 (тдд, J=7,5, 6,2, 5,0 Гц, 1H), 1,15 (т, J=7,2 Гц, 3H), 1,09 (д, J=6,6 Гц, 3H); ИЭРМС (масс-спектроскопия с ионизацией электрораспылением) m/z 319 ([M+H]+).
Пример 2: Получение N1,N1,N4-триметил-N4-(3-метил-1-(пиридин-3-ил)-1H-пиразол-4-ил)сукцинамида (соединение F62)
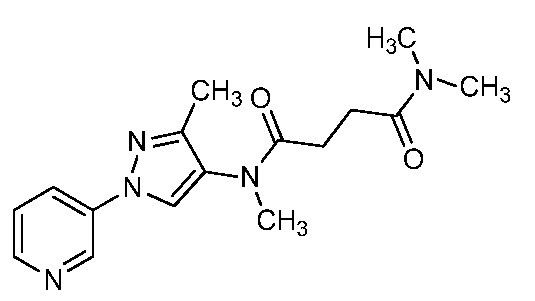
К охлажденному льдом раствору 4-(диметиламино)-4-оксобутановой кислоты (0,174 г, 1,20 ммоля) в CH2Cl2 (2 мл) добавляли ДИПЭА (0,208 мл, 1,120 ммоля), затем изобутилхлорформиат (0,138 мл, 1,06 ммоля). Смесь перемешивали в течение 10 мин и полученный смешанный ангидрид добавляли к раствору N,3-диметил-1-(пиридин-3-ил)-1H-пиразол-4-амина (0,100 г, 0,531 ммоля) в CH2Cl2 (0,66 мл). Реакционную смесь перемешивали при комнатной температуре (примерно 22°C) в течение 1 ч. Неочищенную реакционную смесь концентрировали и очищали с помощью колоночной хроматографии с обращенной фазой (0%-100% ацетонитрил (MeCN)/вода) и получали искомый продукт F62 в виде белого твердого вещества (0,155 г, 83%).
Указанные ниже молекулы получали по методикам, раскрытым в примере 2:
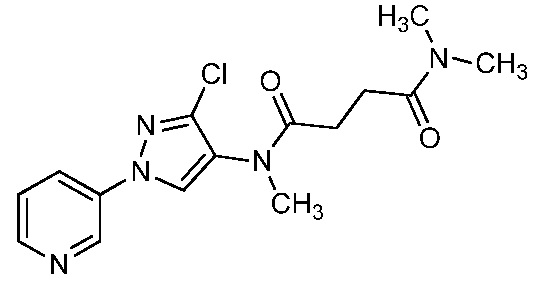
F25
N1-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N1,N4,N4-триметилсукцинамид (соединение F25) выделяли в виде белого твердого вещества (0,122 г, 68%).
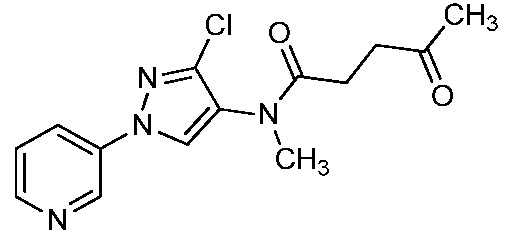
FA75
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-метил-4-оксопентанамид (FA75) выделяли в виде коричневого твердого вещества (1,26 г, 58%).
Пример 3: Получение 4-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-4-оксобутановой кислоты (соединение C1)
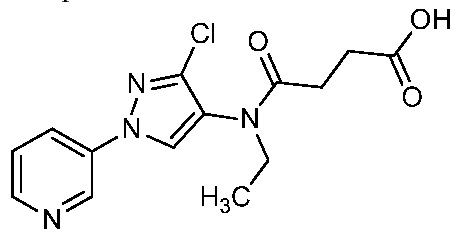
В круглодонную колбу объемом 100 мл, снабженную стержнем для магнитной мешалки, добавляли 3-хлор-N-этил-1-(пиридин-3-ил)-1H-пиразол-4-амин (0,500 г, 2,25 ммоля), ДМАП (0,0274 г, 0,225 ммоля), триэтиламин (0,469 мл, 3,37 ммоля) и дигидрофуран-2,5-дион (0,449 г, 4,49 ммоля) с ДХЭ (22,5 мл). После нагревания при температуре, равной примерно 60°C, в атмосфере азота (N2) в течение ночи реакционную смесь концентрировали и очищали с помощью колоночной флэш-хроматографии на силикагеле при элюировании с помощью 0%-15% MeOH/CH2Cl2 и получали искомое соединение C1 в виде почти белого твердого вещества (0,635 г, 86%): ИК (тонкая пленка) 3097, 1661 см-1; 1H ЯМР (400 МГц, CDCl3) δ 9,00 (c, 1H), 8,59 (д, J=4,8 Гц, 1H), 8,15 (ддд, J=8,4, 2,6, 1,4 Гц, 1H), 8,12 (c, 1H), 7,49 (дд, J=8,4, 4,8 Гц, 1H), 3,72 (кв., J=7,2 Гц, 2H), 3,49 (c, 1H), 2,72 (д, J=10,6 Гц, 2H), 2,47 (т, J=6,4 Гц, 2H), 1,16 (т, J=7,2 Гц, 3H); ИЭРМС m/z 323 ([M+H]+).
Пример 4: Получение N1-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N1-этил-N4-метил-N4-(3,3,3-трифторпропил)сукцинамида (соединение F108)
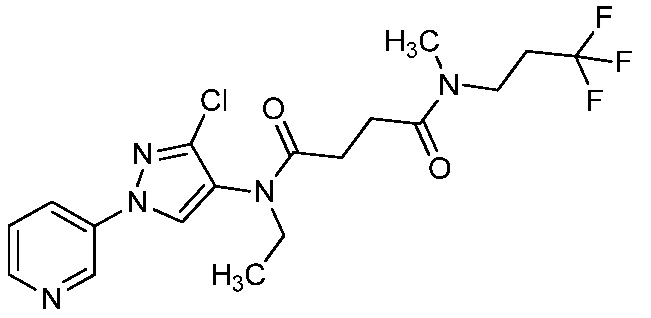
Раствор 4-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-4-оксобутановой кислоты (0,100 г, 0,310 ммоля), ДМАП (0,129 г, 1,05 ммоля) и 3,3,3-трифтор-N-метилпропан-1-амина (0,0394 г, 0,310 ммоля) в сухом CH2Cl2 (1,0 мл) охлаждали до температуры, равной примерно 0°C в атмосфере N2. Добавляли N,N'-метандиилидендициклогексанамин (0,153 мг, 0,744 ммоля) и реакционную смесь медленно нагревали до комнатной температуры в атмосфере N2, затем перемешивали при комнатной температуре в течение ночи. Реакционную смесь фильтровали с использованием дополнительного количества CH2Cl2 (0,5 мл) для удаления твердых веществ и концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле при элюировании с помощью 0%-5% MeOH/CH2Cl2 и получали искомое соединение F108 в виде прозрачного вязкого масла (0,078 г, 57%).
Указанные ниже молекулы получали по методикам, раскрытым в примере 4:
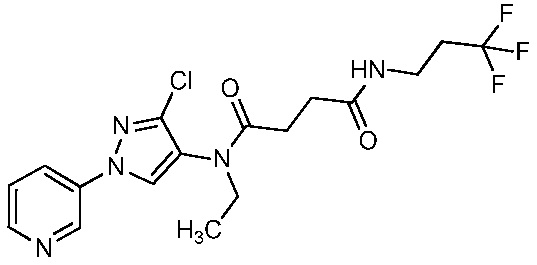
F73
N1-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N1-этил-N4-(3,3,3-трифторпропил)сукцинамид (соединение F73) выделяли в виде прозрачного вспененного вещества (0,389 г, 76%).
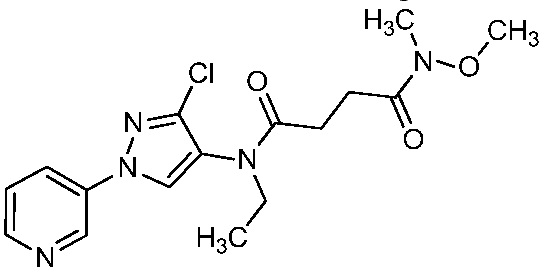
F78
N1-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N1-этил-N4-метокси-N4-метилсукцинамид (соединение F78) выделяли в виде белого полужидкого вещества (0,307 г, 65%).
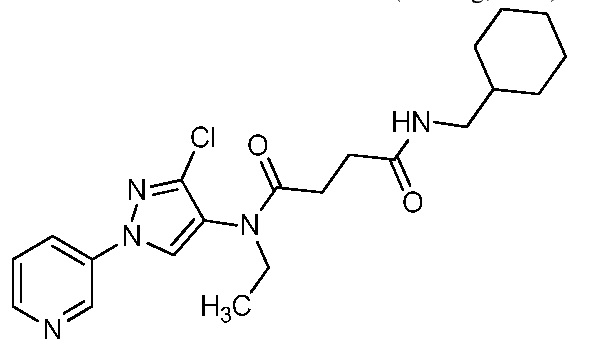
F15
N1-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N4-(циклогексилметил)-N1-этилсукцинамид (соединение F15) выделяли в виде светло-желтого твердого вещества (0,048 г, 52%).
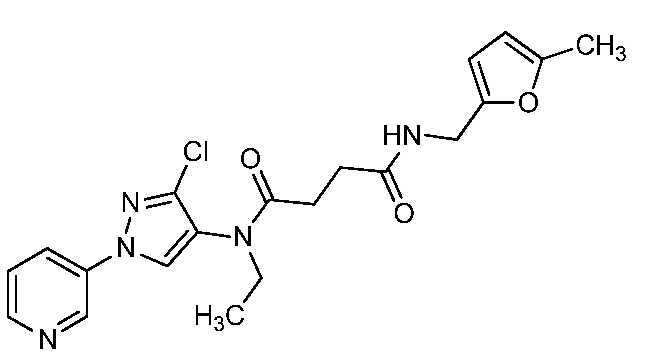
F13
N1-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N1-этил-N4-((5-метилфуран -2-ил)метил)сукцинамид (соединение F13) выделяли в виде желтоватого твердого вещества (0,072 г, 64%).
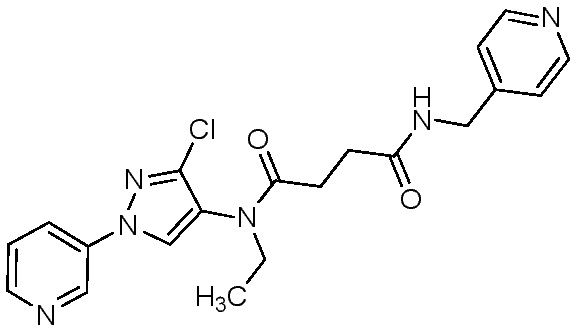
F115
N1-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N1-этил-N4-(пиридин-4-илметил)сукцинамид (соединение F115) выделяли в виде светло-желтого твердого вещества (0,076 г, 64%).
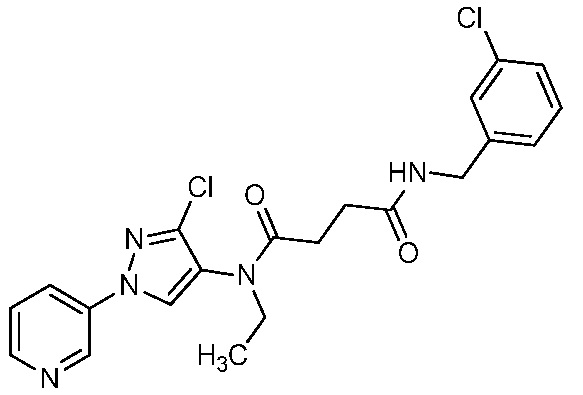
F68
N1-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N4-(3-хлорбензил)-N1-этилсукцинамид (соединение F68) выделяли в виде вязкого немного мутного масла (0,083 г, 71%).
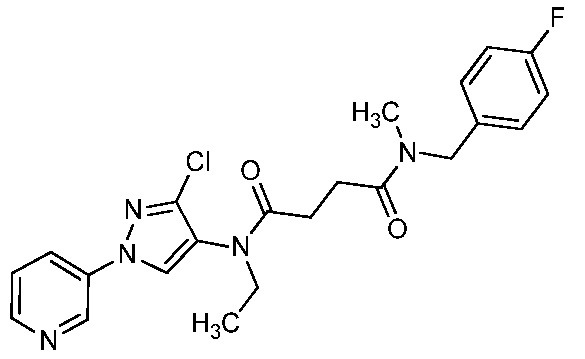
F118
N1-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N1-этил-N4-(4-фторбензил) -N4-метилсукцинамид (соединение F118) выделяли в виде мутного белого вязкого полужидкого вещества (0,041 г, 36%).
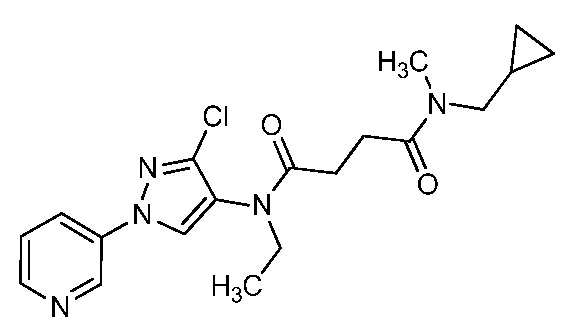
F30
N1-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N4-(циклопропилметил)-N1-этил-N4-метилсукцинамид (соединение F30) выделяли в виде светло-желтого прозрачного вязкого масла (0,069 г, 70%).
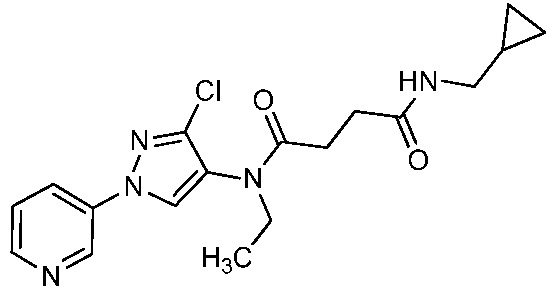
F70
N1-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N4-(циклопропилметил)-N1-этилсукцинамид (соединение F70) выделяли в виде белого полужидкого вещества (0,037 г, 38%).
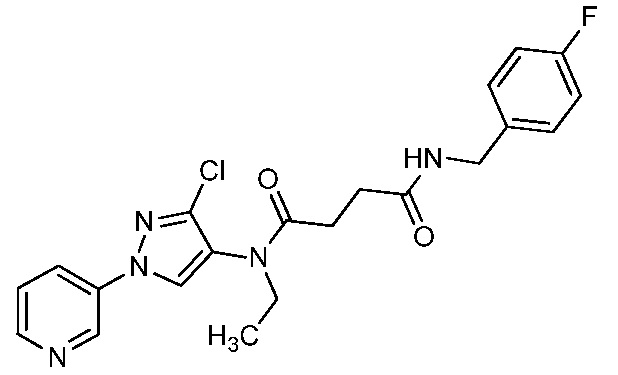
F80
N1-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N1-этил-N4-(4-фторбензил)сукцинамид (соединение F80) выделяли в виде белого твердого вещества (0,087 г, 79%).
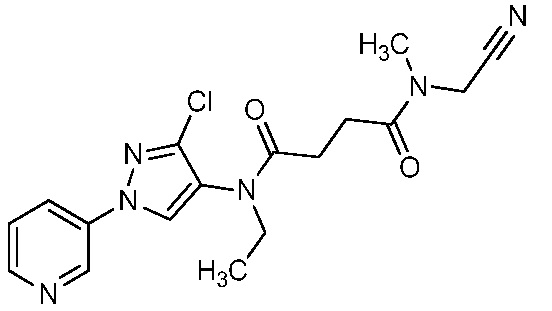
F55
N1-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N4-(цианометил)-N1-этил-N4-метилсукцинамид (соединение F55) выделяли в виде коричневого вязкого полужидкого вещества (0,066 г, 67%).
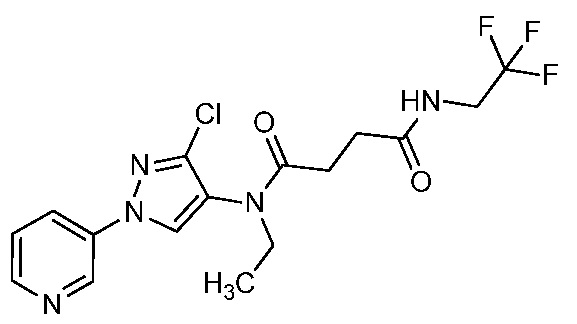
F67
N1-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N1-этил-N4-(2,2,2-трифторэтил)сукцинамид (соединение F67) выделяли в виде белого твердого вещества (0,064 г, 61%).
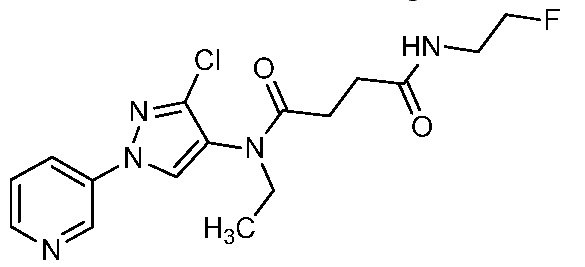
F43
N1-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N1-этил-N4-(2-фторэтил)сукцинамид (соединение F43) выделяли в виде прозрачного полужидкого вещества (0,070 г, 74%).
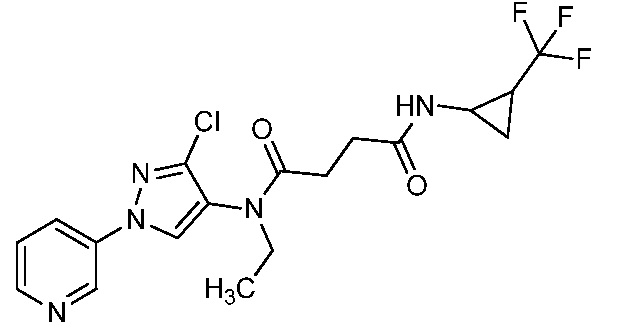
F54
N1-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N1-этил-N4-(2-(трифторметил)циклопропил)сукцинамид (соединение F54) выделяли в виде белого полужидкого вещества (0,036 г, 31%).
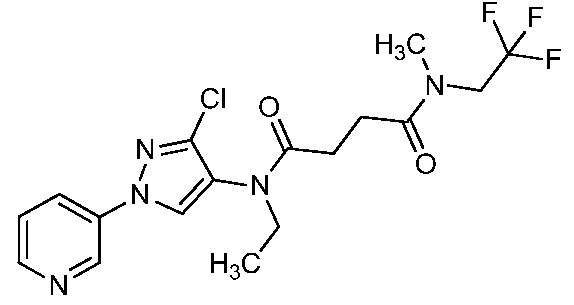
F85
N1-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N1-этил-N4-метил-N4-(2,2,2-трифторэтил)сукцинамид (соединение F85) выделяли в виде светло-коричневого вязкого полужидкого вещества (0,086 г, 80%).
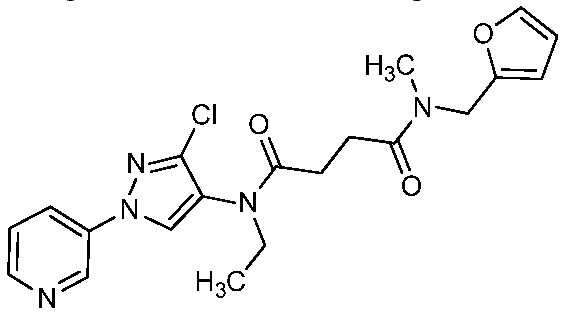
FA77
N1-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N1-этил-N4-(фуран-2-илметил)-N4-метилсукцинамид (соединение FA77) выделяли в виде оранжевого масла (0,074 г, 69%).
Пример 5: Получение N-(2-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-2-оксоэтил)-N-метилбензамида (соединение F83)
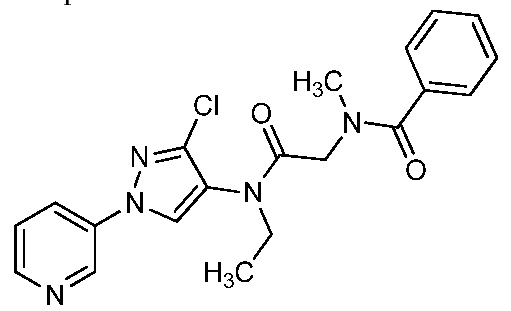
Раствор 3-хлор-N-этил-1-(пиридин-3-ил)-1H-пиразол-4-амина (0,075 г, 0,34 ммоля), 2-(N-метилбензамидо)уксусной кислоты (0,098 г, 0,51 ммоля) и ДМАП (0,062 г, 0,51 ммоля) в сухом диэтиловом эфире (1,0 мл) и сухом CH2Cl2 (1,1 мл) охлаждали до температуры, равной примерно 0°C, в атмосфере N2. Добавляли ДЦК (0,17 г, 0,81 ммоля) и реакционную смесь медленно нагревали до комнатной температуры в атмосфере N2, затем перемешивали при комнатной температуре в течение ночи. Реакционную смесь фильтровали с использованием дополнительного количества CH2Cl2 (0,5 мл) для удаления твердых веществ и концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле при элюировании с помощью 0%-10% MeOH/CH2Cl2 и получали искомое соединение F83 в виде белого твердого вещества (0,12 г, 87%).
Указанные ниже молекулы получали по методикам, раскрытым в примере 5:
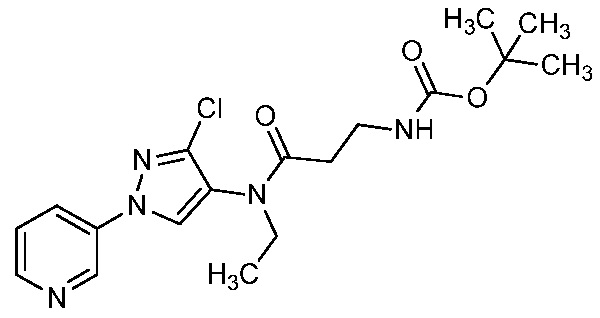
F19
трет-Бутил-(3-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-3-оксопропил)карбамат (соединение F19) выделяли в виде белого твердого вещества (1,506 г, 83%).
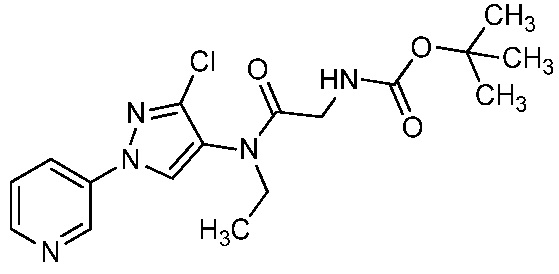
F2
трет-Бутил-(2-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-2-оксоэтил)карбамат (соединение F2) выделяли в виде розового твердого вещества (1,256 г, 71%).
Пример 6: Получение 3-амино-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этилпропанамида (соединение C2)
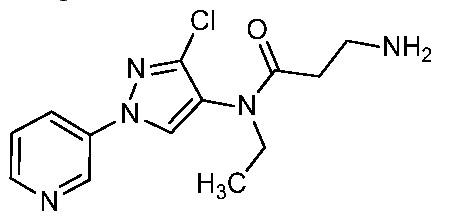
К раствору трет-бутил-(3-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-3-оксопропил)карбамата (0,100 г, 0,254 ммоля) в сухом CH2Cl2 (0,254 мл, 0,254 ммоля) добавляли ТФК (0,254 мл, 0,254 ммоля) при комнатной температуре в атмосфере N2. Реакционную смесь перемешивали при комнатной температуре в течение примерно 2 ч. Осторожно добавляли насыщенный водный раствор бикарбоната натрия (NaHCO3) (примерно 5 мл), пока реакционная смесь не становилась щелочной. Продукт реакции экстрагировали с помощью CH2Cl2 (3×5 мл), сушили и концентрировали. Неочищенный продукт в большинстве случаев обычно использовали без очистки. Продукт можно очистить с помощью хроматографии с обращенной фазой на силикагеле при элюировании с помощью 10%-100% MeCN/вода и получить искомое соединение C2 в виде вязкого светло-желтого масла (0,0160 г, 22%): ИК (тонкая пленка) 3368, 3091, 1657 см-1; 1H ЯМР (400 МГц, CDCl3) δ 8,95 (дд, J=2,8, 0,8 Гц, 1H), 8,62 (дд, J=4,7, 1,5 Гц, 1H), 8,04 (ддд, J=8,3, 2,7, 1,4 Гц, 1H), 7,98 (c, 1H), 7,46 (ддд, J=8,3, 4,7, 0,8 Гц, 1H), 3,71 (кв., J=7,2 Гц, 2H), 2,97 (т, J=6,1 Гц, 2H), 2,32 (т, J=6,1 Гц, 2H), 1,72 (c, 2H), 1,16 (т, J=7,2 Гц, 3H); МСВР-ББА (масс-спектроскопия высокого разрешения - бомбардировка быстрыми атомами) (m/z) ([M+H]+) рассчитано для C13H17ClN5O, 294,1116; найдено, 294,1117.
Пример 7: Получение N-(3-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-3-оксопропил)-2,2-дифтор-1-метилциклопропанкарбоксамида (соединение F113)
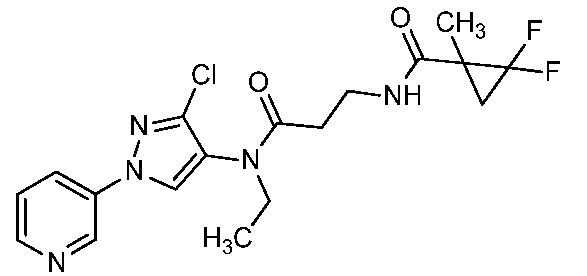
Раствор 3-амино-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этилпропанамида (0,074 мг, 0,25 ммоля), ДМАП (0,047 мг, 0,38 ммоля), 2,2-дифтор-1-метилциклопропанкарбоновой кислоты (0,052 мг, 0,38 ммоля) в сухом CH2Cl2 (1,69 мл) охлаждали до температуры, равной примерно 0°C, в атмосфере N2. Добавляли ДЦК (0,13 г, 0,61 ммоля) и реакционную смесь медленно нагревали до комнатной температуры в атмосфере N2, затем перемешивали при комнатной температуре в течение ночи. Реакционную смесь фильтровали с использованием дополнительного количества CH2Cl2 (0,5 мл) для удаления твердых веществ и концентрировали при пониженном давлении. Продукт очищали с помощью хроматографии на силикагеле при элюировании с помощью 0%-10% MeOH/CH2Cl2 и получали искомое соединение F113 в виде желтого вязкого масла (0,029 г, 26% за 2 стадии из соединения C2).
Указанные ниже молекулы получали по методикам, раскрытым в примере 7:
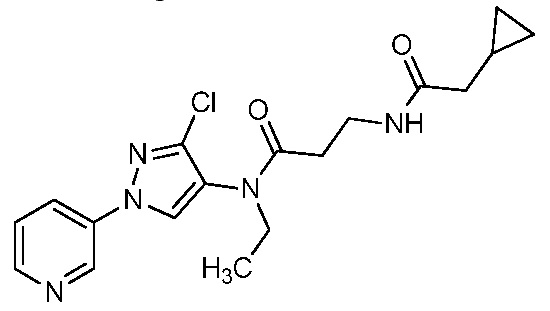
F75
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-3-(2-циклопропилацетамидо)-N-этилпропанамид (соединение F75) выделяли в виде белого очень липкого вспененного вещества (0,090 г, 84%).
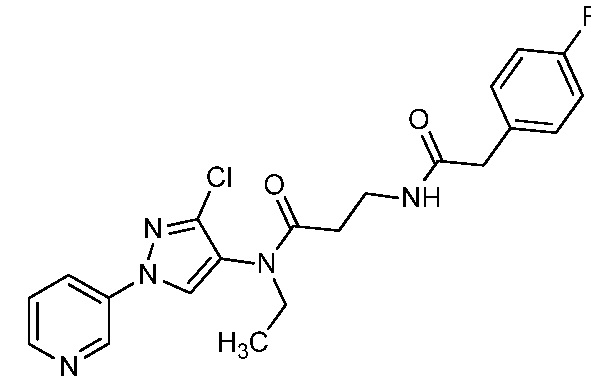
F46
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-3-(2-(4-фторфенил) ацетамидо)пропанамид (соединение F46) выделяли в виде белого твердого вещества (0,066 г, 83%).
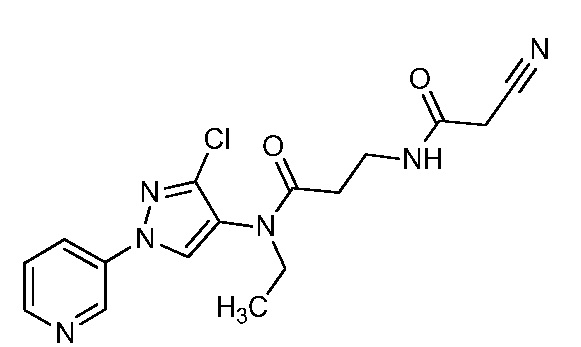
F101
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-3-(2-цианоацетамидо)-N-этилпропанамид (соединение F101) выделяли в виде светло-желтого твердого вещества (0,075 г, 83%).
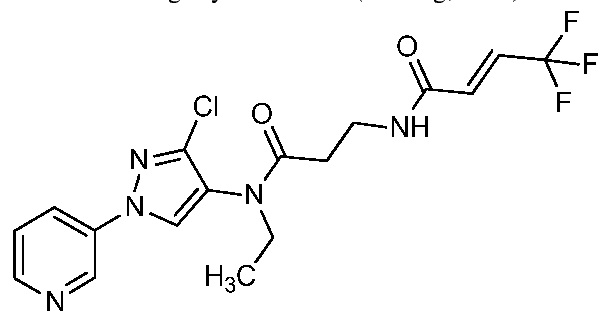
F65
(E)-N-(3-((3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-3-оксопропил)-4,4,4-трифторбут-2-енамид (соединение F65) выделяли в виде коричневого твердого вещества (0,026 г, 24% за две стадии из соединения C2).
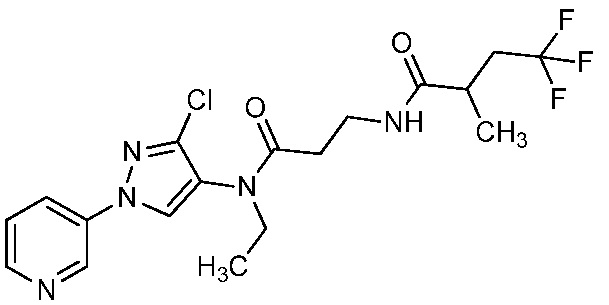
F44
N-(3-((3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-3-оксопропил)-4,4,4-трифтор-2-метилбутанамид (соединение F44) выделяли в виде почти белого вспененного вещества (0,050 г, 37% за две стадии из соединения C2).
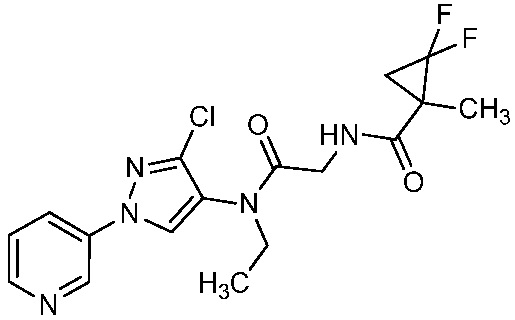
F1
N-(2-((3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-2-оксоэтил)-2,2-дифтор-1-метилциклопропанкарбоксамид (соединение F1) выделяли в виде белого твердого вещества (0,055 г, 41% за две стадии из соединения C2).
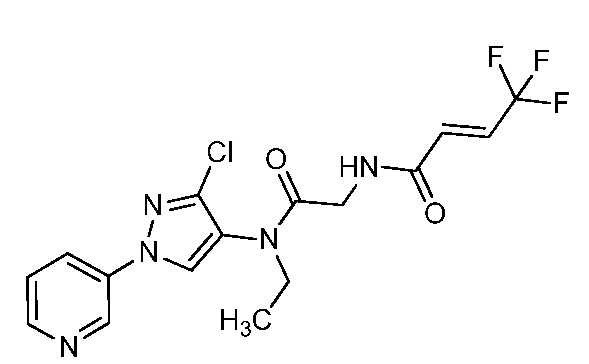
F99
(E)-N-(2-((3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-2-оксоэтил)-4,4,4-трифторбут-2-енамид (соединение F99) выделяли в виде оранжевого масла (0,061 г, 46% за две стадии из соединения C2).
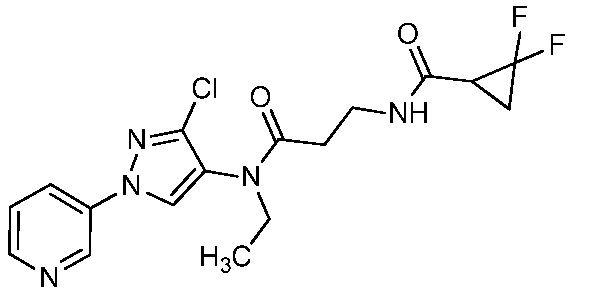
F56
N-(3-((3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-3-оксопропил)-2,2-дифторциклопропанкарбоксамид (соединение F56) выделяли в виде светло-коричневого твердого вещества (0,045 г, 35% за две стадии из соединения C2).
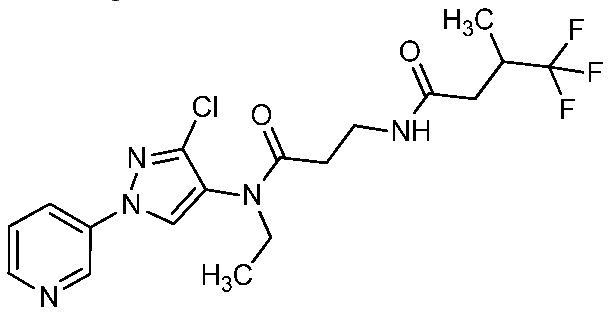
F28
N-(3-((3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-3-оксопропил)-4,4,4-трифтор-3-метилбутанамид (соединение F28) выделяли в виде почти белого вспененного вещества (0,044 г, 33% за две стадии из соединения C2).
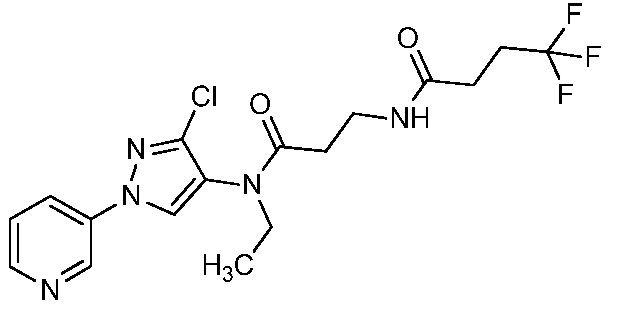
F12
N-(3-((3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-3-оксопропил)-4,4,4-трифторбутанамид (соединение F12) выделяли в виде почти белого полужидкого вещества (0,044 г, 33% за две стадии из соединения C2).
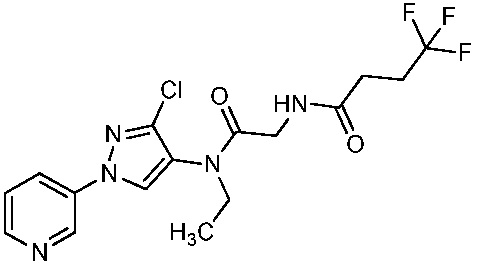
F97
N-(2-((3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-2-оксоэтил)-4,4,4-трифторбутанамид (соединение F97) выделяли в виде почти белого твердого вещества (0,080 г, 61% за две стадии из соединения C2).
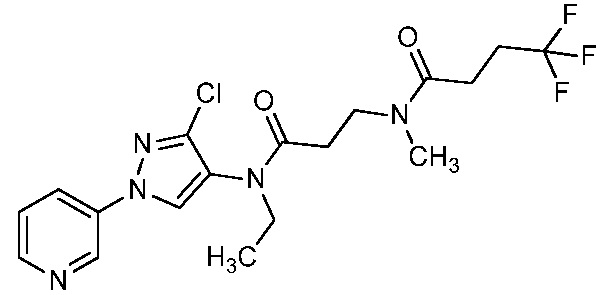
F94
N-(3-((3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-3-оксопропил)-4,4,4-трифтор-N-метилбутанамид (соединение F94) выделяли в виде вязкого прозрачного масла (0,083 г, 81%).
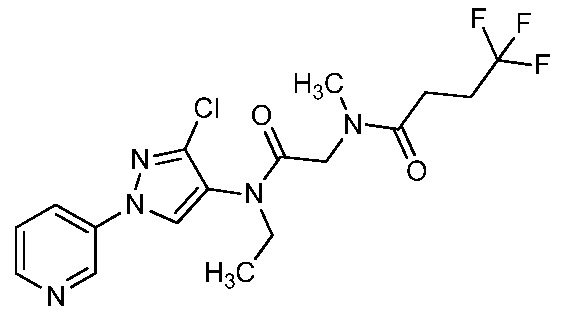
F5
N-(2-((3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-2-оксоэтил)-4,4,4-трифтор-N-метилбутанамид (соединение F5) выделяли в виде светло-желтого вспененного вещества (0,076 г, 75%).
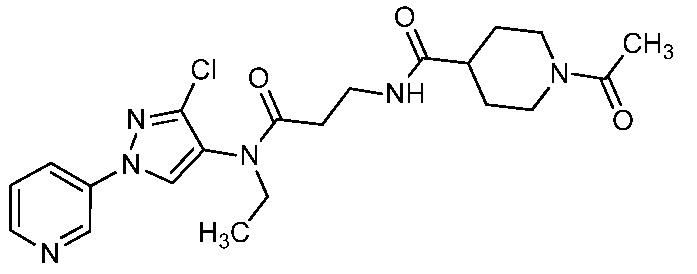
F112
1-Ацетил-N-(3-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-3-оксопропил)пиперидин-4-карбоксамид (соединение F112) выделяли в виде белого вспененного вещества (35 мг, 19% за две стадии из соединения C11).
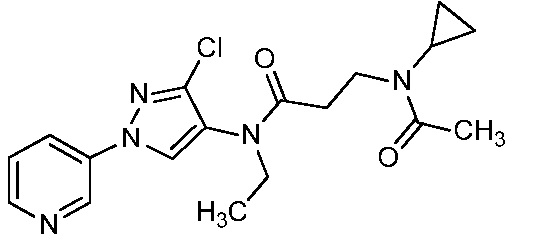
F9
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-3-(N-циклопропилацетамидо)-N-этилпропанамид (соединение F9) выделяли в виде желтого масла (0,074 г, 59%).
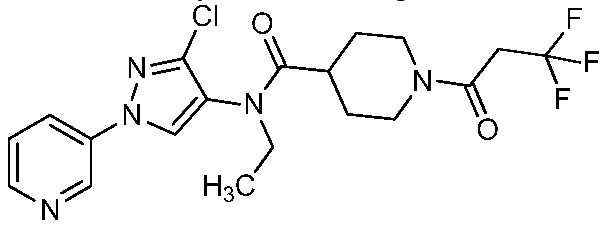
P16
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-1-(3,3,3-трифторпропаноил)пиперидин-4-карбоксамид (соединение P16) выделяли в виде белого полужидкого вещества (0,154 г, 81%).
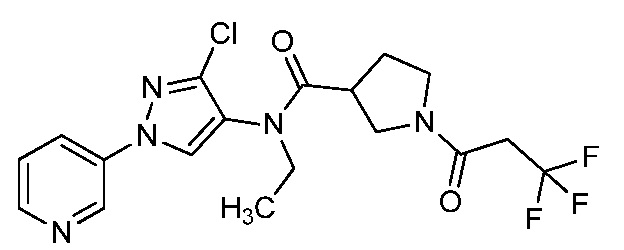
P21
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-1-(3,3,3-трифторпропаноил)пирролидин-3-карбоксамид (соединение P21) выделяли в виде белого полужидкого вещества (0,13 г, 58%).
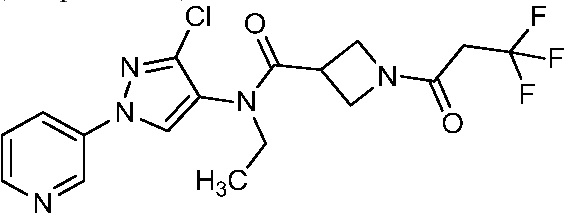
P24
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-1-(3,3,3-трифторпропаноил)азетидин-3-карбоксамид (соединение P24) выделяли в виде бесцветного масла (0,11 г, 50%).
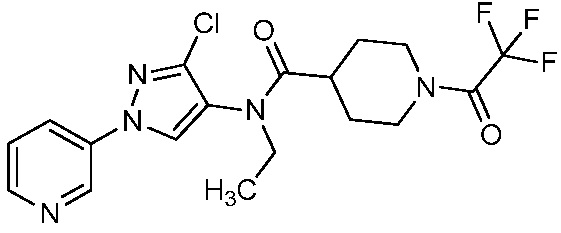
FA5
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-1-(2,2,2-трифторацетил)пиперидин-4-карбоксамид (соединение FA5) выделяли в виде белого твердого вещества (0,069 г, 31%).
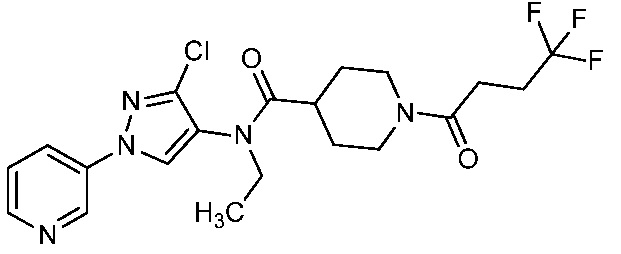
FA6
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-1-(4,4,4-трифторбутаноил)пиперидин-4-карбоксамид (соединение FA6) выделяли в виде желтого твердого вещества (0,158 г, 66%).
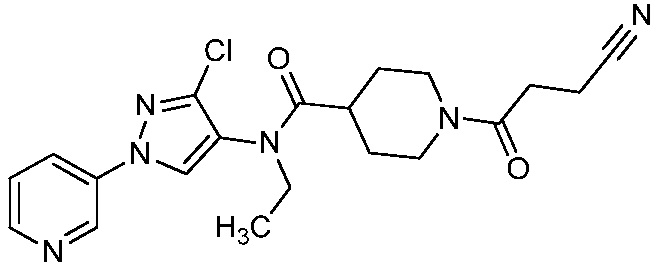
FA7
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-1-(3-цианопропаноил)-N-этилпиперидин-4-карбоксамид (соединение FA7) выделяли в виде желтого твердого вещества (0,199 г, 55%).
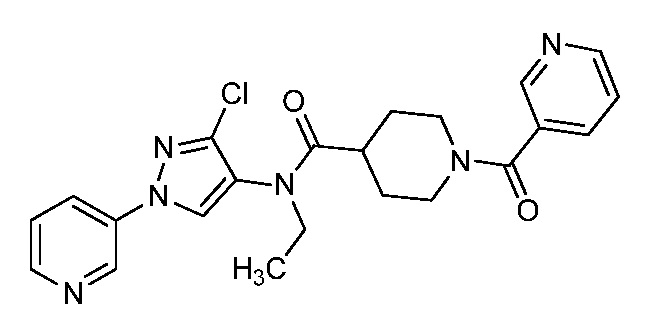
FA8
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-1-никотиноилпиперидин-4-карбоксамид (соединение FA8) выделяли в виде белого полужидкого вещества (0,138 г, 60%).

FA9
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-1-(2,2,2-трифторацетил)пирролидин-3-карбоксамид (соединение FA9) выделяли в виде бесцветного масла (0,074 г, 34%).
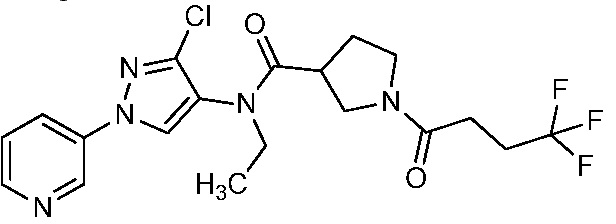
FA10
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-1-(4,4,4-трифторбутаноил)пирролидин-3-карбоксамид (соединение FA10) выделяли в виде белого полужидкого вещества (0,138 г, 59%).
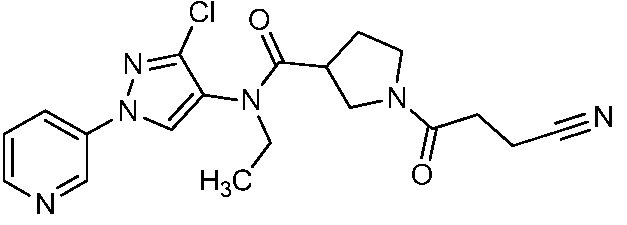
FA11
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-1-(3-цианопропаноил)-N-этилпирролидин-3-карбоксамид (соединение FA11) выделяли в виде желтого полужидкого вещества (0,113 г, 51%).
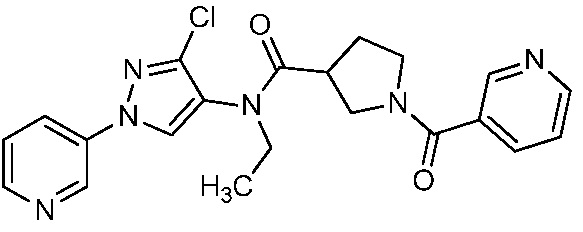
FA12
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-1-никотиноилпирролидин-3-карбоксамид (соединение FA12) выделяли в виде бесцветного масла (0,14 г, 59%).
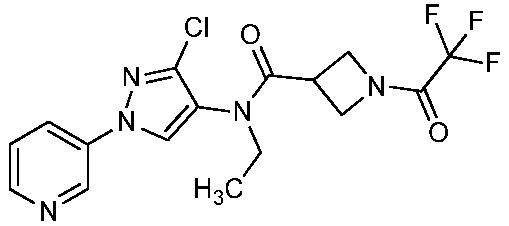
FA14
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-1-(2,2,2-трифторацетил)азетидин-3-карбоксамид (FA14) выделяли в виде бесцветного масла (0,122 г, 58%).
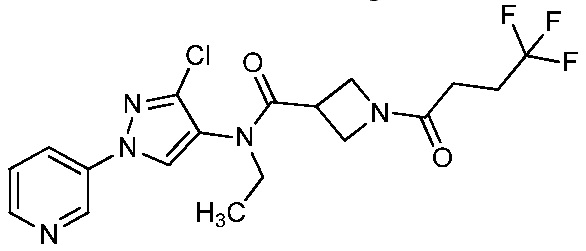
FA15
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-1-(4,4,4-трифторбутаноил)азетидин-3-карбоксамид (FA15) выделяли в виде бесцветного масла (0,135 г, 60%).
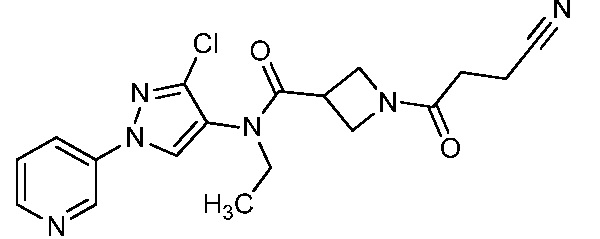
FA16
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-1-(3-цианопропаноил)-N-этилазетидин-3-карбоксамид (FA16) выделяли в виде белого твердого вещества (0,097 г, 48%).
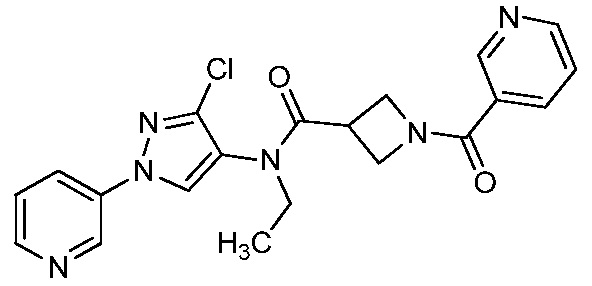
FA17
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-1-никотиноилазетидин-3-карбоксамид (FA17) выделяли в виде бесцветного масла (0,136 г, 63%).
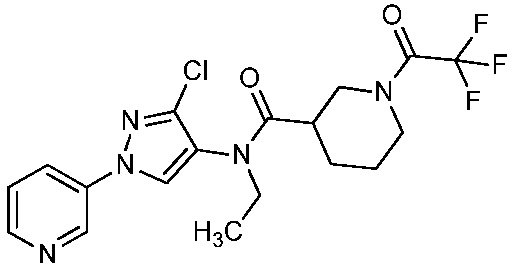
FA41
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-1-(2,2,2-трифторацетил)пиперидин-3-карбоксамид (соединение FA41) выделяли в виде белого полужидкого вещества (0,057 г, 25%).
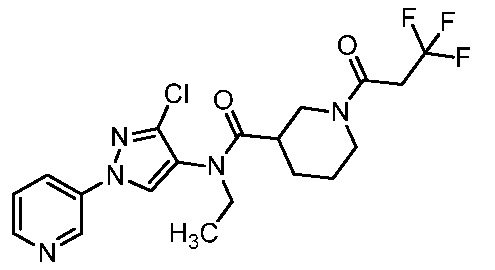
FA42
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-1-(3,3,3-трифторпропаноил)пиперидин-3-карбоксамид (соединение FA42) выделяли в виде белого полужидкого вещества (0,13 г, 56%).
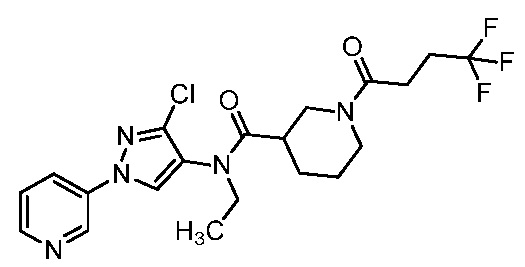
FA43
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-1-(4,4,4-трифторбутаноил)пиперидин-3-карбоксамид (соединение FA43) выделяли в виде желтого полужидкого вещества (0,178 г, 74%).
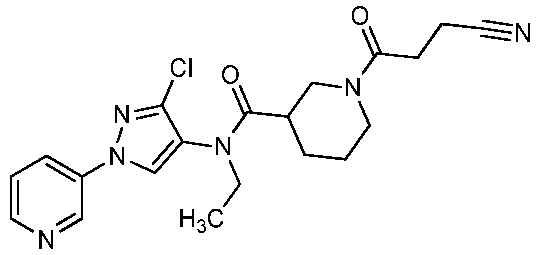
FA44
N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-1-(3-цианопропаноил)-N-этилпиперидин-3-карбоксамид (соединение FA44) выделяли в виде белого полужидкого вещества (0,148 г, 68%).
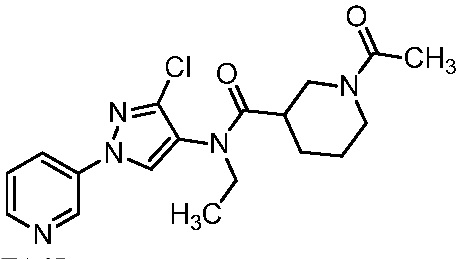
FA45
1-Ацетил-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этилпиперидин-3-карбоксамид (соединение FA45) выделяли в виде желтого твердого вещества (0,087 г, 44%).
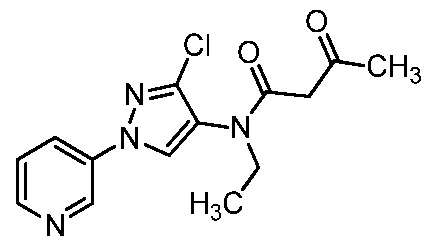
FA66
N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-3-оксобутанамид (соединение FA66) выделяли в виде желтого масла (0,151 г, 44%).
Пример 8: Получение N-(3-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-3-оксопропил)-3,3,3-трифтор-N-метилпропанамид (соединение F102)
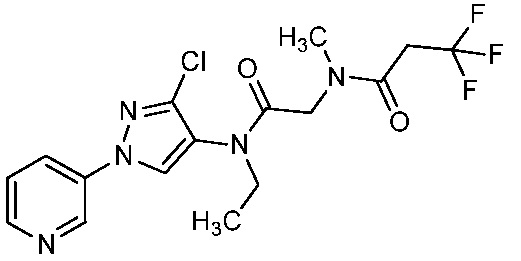
Раствор N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-3-(метиламино)пропанамида (0,070 г, 0,23 ммоля) в сухом CH2Cl2 (0,76 мл) охлаждали до температуры, равной примерно 0°C, в атмосфере N2. К раствору последовательно добавляли ДМАП (0,014 г, 0,11 ммоля), пиридин (0,028 мл, 0,34 ммоля) и 3,3,3-трифторпропаноилхлорид (0,026 мл, 0,25 ммоля). Реакционную смесь медленно нагревали до комнатной температуры в атмосфере N2, затем перемешивали при комнатной температуре в течение ночи. Реакционную смесь разбавляли водой (2 мл) и перемешивали в течение 5 мин. Слои разделяли и водный слой экстрагировали с помощью CH2Cl2 (2×2 мл). Объединенные органические экстракты сушили и концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле при элюировании с помощью 0%-5% MeOH/CH2Cl2 и получали искомое соединение F102 в виде белого полужидкого вещества (0,062 г, 63%).
Указанные ниже молекулы получали по методикам, раскрытым в примере 8:
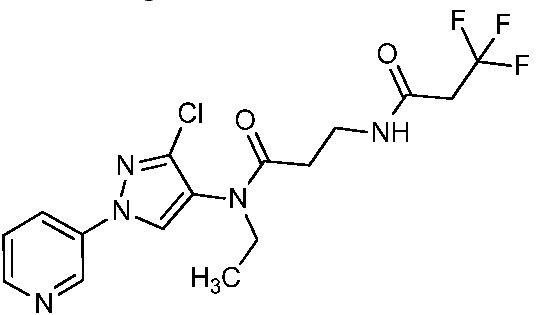
F63
N-(3-((3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-3-оксопропил)-3,3,3-трифторпропанамид (соединение F63) выделяли в виде белого твердого вещества (0,039 г, 31% за 2 стадии из соединения C2).
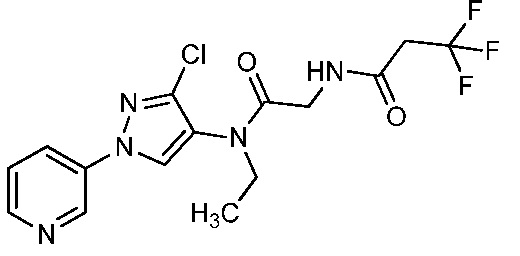
F57
N-(2-((3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-2-оксоэтил)-3,3,3-трифторпропанамид (соединение F57) выделяли в виде белого твердого вещества (66 мг, 52% за 2 стадии из соединения C2).
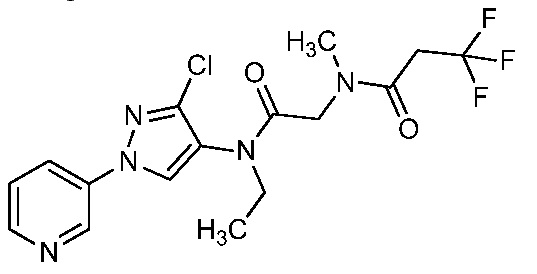
F120
N-(2-((3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-2-оксоэтил)-3,3,3-трифтор-N-метилпропанамид (соединение F120) выделяли в виде белого твердого вещества (0,057 г, 54%).
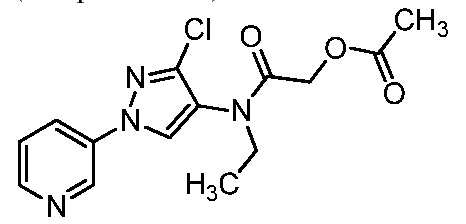
FA72
2-((3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-2-оксоэтилацетат (соединение FA72) выделяли в виде белого твердого вещества (0,068 г, 27%).
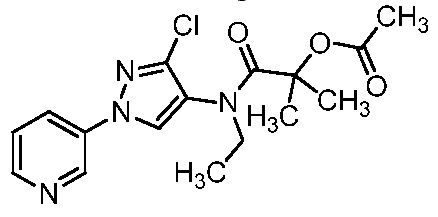
FA73
1-((3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-2-метил-1-оксопропан-2-илацетат (соединение FA73) выделяли в виде почти белого твердого вещества (0,173 г, 73%).
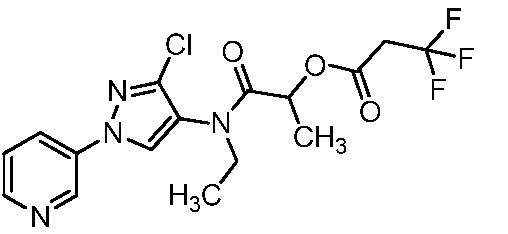
FA74
1-((3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-1-оксопропан-2-ил-3,3,3-трифторпропаноат (соединение FA74) выделяли в виде желтого масла (0,087 г, 63%).
Пример 9: Получение трет-бутил-3-(3-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-3-оксопропил)-2-оксопирролидин-1-карбоксилата (соединение F128)
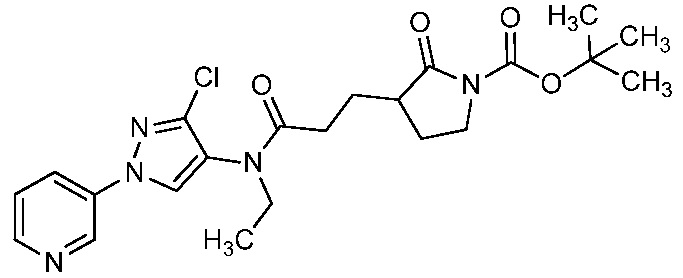
Раствор трет-бутил 2-оксопирролидин-1-карбоксилата (1,24 мл, 1,35 ммоля) в сухом ТГФ (3,86 мл) охлаждали до температуры, равной примерно -78°C в атмосфере N2 с использованием бани ацетон/твердый диоксид углерода. Добавляли 1M раствор LiHMDS в ТГФ (1,62 мл, 1,62 ммоля) и реакционную смесь перемешивали при температуре, равной примерно -78°C, в течение 45 мин. К смеси по каплям добавляли раствор 3-хлор-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этилпропанамида (0,465 г, 1,49 ммоля) в ТГФ (3,86 мл) и перемешивали при температуре, равной примерно -78°C, в течение 1 ч. Реакционной смеси давали медленно нагреться до комнатной температуры и перемешивали в течение ночи. Реакцию останавливали насыщенным водным раствором хлорида аммония (NH4Cl, 5 мл) и продукт экстрагировали с помощью CH2Cl2 (3×5 мл), сушили и концентрировали. Остаток очищали с помощью хроматографии на силикагеле при элюировании с помощью 20%-100% EtOAc/гексаны и получали искомое соединение F128 в виде белого вспененного вещества (0,0770 г, 12%).
Пример 10: Получение N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-3-(2-оксопирролидин-3-ил)пропанамида (соединение F131)
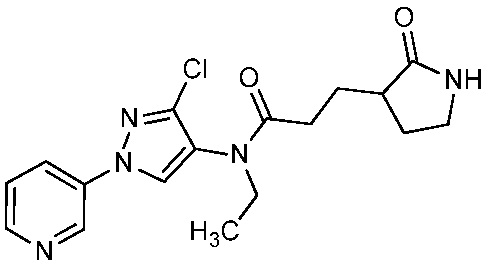
К раствору трет-бутил-3-(3-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-3-оксопропил)-2-оксопирролидин-1-карбоксилата (0,076 г, 0,17 ммоля) в сухом CH2Cl2 (0,33 мл) при комнатной температуре в атмосфере N2 добавляли ТФК (0,33 мл). Реакционную смесь перемешивали при комнатной температуре в течение примерно 90 мин. Осторожно добавляли насыщенный водный раствор NaHCO3 (примерно 10 мл), пока реакционная смесь не становилась щелочной. Продукт экстрагировали с помощью CH2Cl2 (3×10 мл), сушили и концентрировали. Остаток очищали с помощью хроматографии на силикагеле при элюировании с помощью 0%-15% MeOH/CH2Cl2 и получали искомое соединение F131 в виде белого вспененного вещества (0,041 г, 66%).
Пример 11: Получение трет-бутил-(3-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-3-оксопропил)(метил)карбамата (соединение F52)
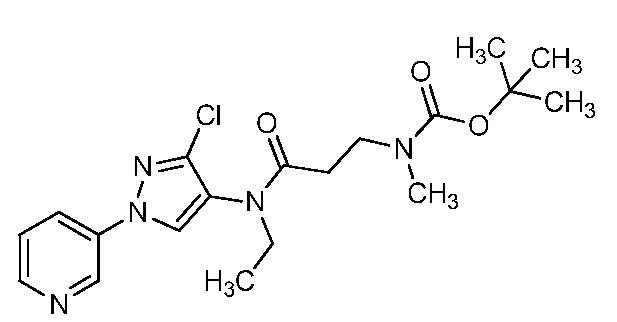
В чистый сосуд, снабженный стержнем для магнитной мешалки, добавляли трет-бутил-(3-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-3-оксопропил)карбамат (1,5 г, 3,8 ммоля) и герметизировали крышкой с диафрагмой. Пространство над раствором продували с помощью N2, шприцем добавляли сухой ДМФ (5,4 мл) и реакционную смесь охлаждали до температуры, равной примерно 0°C, в бане со льдом в атмосфере N2. Осторожно добавляли NaH (60% дисперсия в масле, 0,21 г, 5,3 ммоля) и перемешивали при температуре, равной 0°C, в течение 30 мин. Затем добавляли метилйодид (0,29 мл, 4,6 ммоля) и перемешивали в течение 30 мин при температуре, равной 0°C. После добавления метилйодида реакционная смесь превращалась в светло-желтую суспензию. Реакционную смесь нагревали до комнатной температуры и перемешивали в течение 2 ч. После того, как реакционную смесь нагрели, она приобретала ярко-оранжевый цвет. Реакцию останавливали путем медленного добавления воды (100 мл). Суспензию энергично перемешивали при комнатной температуре в течение 2 ч. Воду отфильтровывали и оставшуюся суспензию промывали гексанами. Затем суспензию растворяли в метаноле и пропускали через фильтр. Полученный раствор концентрировали, сушили в высоком вакууме и получали коричневое вязкое масло (1,6 г, 78%).
Пример 12: Получение 2-(1-(трет-бутилдиметилсилил)-2-оксоацетидин-3-ил)уксусной кислоты (соединение C3)
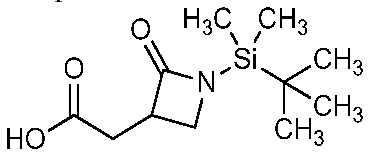
При перемешивании в раствор 3-аллил-1-(трет-бутилдиметилсилил)азетидин-2-она (4,90 г, 22,2 ммоля) в смеси тетрахлорид углерода(CCl4)/MeCN/вода (50 мл/50 мл/100 мл) при комнатной температуре помещали перйодат натрия (18,9 г, 88,7 ммоля), затем тригидрат хлорида рутения(III) (0,114 г, 0,440 ммоля) и перемешивали в течение 3 ч. Реакционную смесь разбавляли водой (100 мл) и экстрагировали с помощью CH2Cl2 (3×100 мл). Объединенные органические слои сушили над сульфатом натрия (Na2SO4), фильтровали и концентрировали при пониженном давлении и получали искомое соединение C3 в виде черного полужидкого вещества (4,58 г, 85%): ИК (KBr) 2956, 2929, 2351, 1732, 1681, 1361, 1215 см-1; 1H ЯМР (400 МГц, CDCl3) δ 3,62-3,59 (м, 1H), 3,46 (т, J=6,0 Гц, 1H), 3,05 (дд, J=6,4 Гц, 2,8 Гц, 1H), 2,88 (дд, J=17,2 Гц, 5,6 Гц, 1H), 2,67 (дд, J=17,2 Гц, 10,0 Гц, 1H), 0,96 (c, 9H), 0,25 (c, 3H), 0,23 (c, 3H); ИЭРМС m/z 244 ([M+H]+).
Указанные ниже молекулы получали по методикам, раскрытым в примере 12:
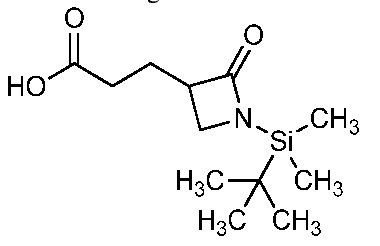
C4
3-(1-(трет-Бутилдиметилсилил)-2-оксоазетидин-3-ил)пропановую кислоту (соединение C4) выделяли в виде черного полужидкого вещества (5,07 г, 89%): ИК (KBr) 2929, 2858, 2376, 1718, 1695, 1345, 1219 см-1; 1H ЯМР (400 МГц, CDCl3) δ 3,37-3,32 (м, 2H), 2,93-2,91 (м, 1H), 2,56-2,48 (м, 2H), 2,10-1,97 (м, 2H), 0,95 (c, 9H), 0,25 (c, 3H), 0,23 (c, 3H); ИЭРМС m/z 258 ([M+H]+).
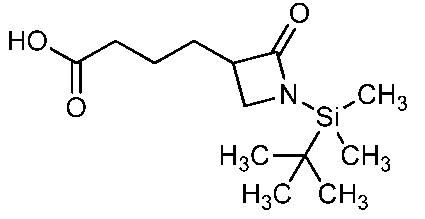
C5
4-(1-(трет-Бутилдиметилсилил)-2-оксоазетидин-3-ил)бутановую кислоту (соединение C5) выделяли в виде черного полужидкого вещества (5,17 г, 86%): ИК (KBr): 2954, 2858, 2358, 1728, 1467, 1350, 1199 см-1; 1H ЯМР (400 МГц, CDCl3) δ 3,37-3,28 (м, 2H), 2,93 (дд, J=2,8 Гц, 6,0 Гц, 1H), 2,43 (т, J=6,8 Гц, 2H), 1,89-1,66 (м, 4H), 0,97 (c, 9H), 0,25 (c, 3H), 0,23 (c, 3H); ИЭРМС m/z 272 ([M+H]+).
Пример 13: Получение N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-2-(2-оксоазетидин-3-ил)ацетамида (соединение F71)
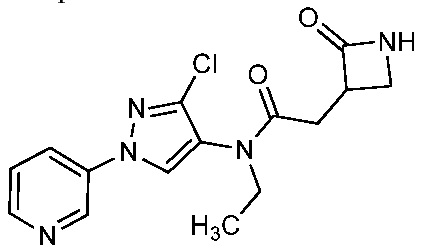
При перемешивании в раствор 2-(1-(трет-бутилдиметилсилил)-2-оксоацетидин-3-ил)уксусной кислоты (4,10 г, 16,9 ммоля) и 3-хлор-N-этил-1-(пиридин-3-ил)-1H-пиразол-4-амина (2,48 г, 11,2 ммоля) в EtOAc (50 мл) при комнатной температуре помещали триэтиламин (6,24 мл, 44,8 ммоля), затем ангидрид н-пропанфосфоновой кислоты (T3P®) (50% в ДМФ, 22,5 ммоля). Полученную реакционную смесь кипятили с обратным холодильником в течение 3 ч. Реакционную смесь разбавляли водой (50 мл) и экстрагировали с помощью EtOAc (3×100 мл). Объединенные органические слои промывали рассолом (100 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали с помощью флэш-хроматографии при элюировании с помощью 1%-10% MeOH/CH2Cl2 и получали искомое соединение F71 в виде почти белого твердого вещества (1,60 г, 43%).
Указанные ниже молекулы получали по методикам, раскрытым в примере 13:
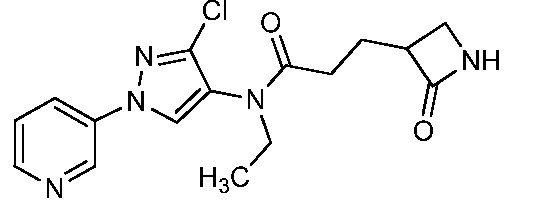
F50
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-3-(2-оксоазетидин-3-ил)ацетамид (соединение F50) выделяли в виде светло-желтого смолообразного вещества (1,7 г, 45%).
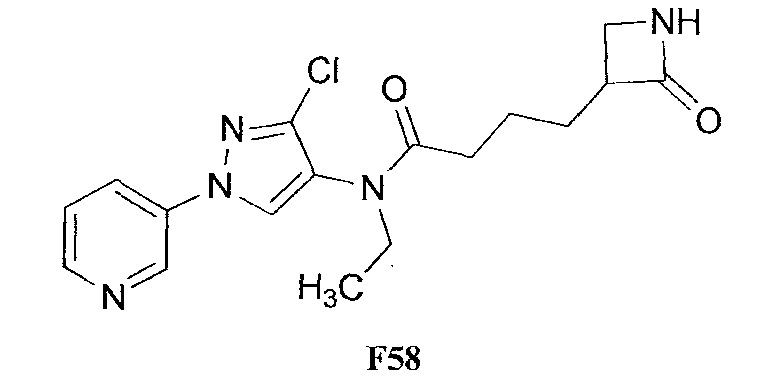
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(2-оксоазетидин-3-ил)ацетамид (соединение F58) выделяли в виде светло-желтого смолообразного вещества (2,5 г, 63%).
Пример 14: Получение N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-2-(1-метил-2-оксоазетидин-3-ил)ацетамида
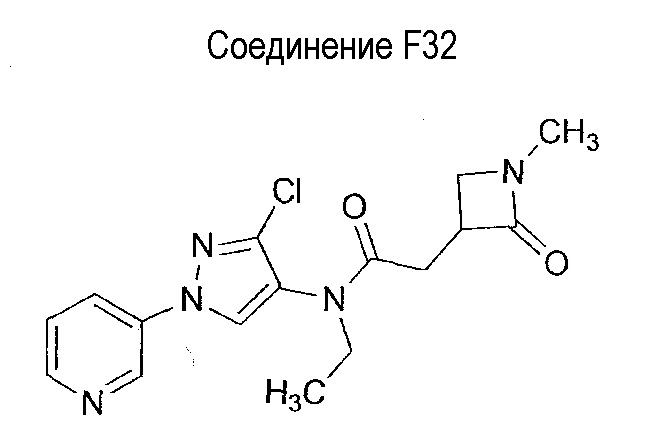
К суспензии NaH (60% дисперсия в масле, 0,029 г, 0,72 ммоля) в ДМФ (2 мл) при температуре, равной примерно -10°C, в течение 1 мин по каплям добавляли N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-2-(2-оксоазетидин-3-ил)ацетамид (0,20 г, 0,60 ммоля) в ДМФ (0,5 мл). В реакционную смесь по каплям добавляли метилйодид (0,093 г, 0,66 ммоля) в ДМФ (0,5 мл) и перемешивали в течение 5 мин. Реакцию останавливали водой со льдом (10 мл) и экстрагировали с помощью EtOAc (3×15 мл). Органические слои объединяли и промывали водой (3×10 мл) и рассолом (10 мл), сушили над Na2SO4 и концентрировали при пониженном давлении. Остаток очищали с помощью флэш-хроматографии при элюировании с помощью 1%-8% MeOH/CH2Cl2 и получали искомое соединение F32 в виде смолообразного вещества (0,065 г, 31%).
Указанные ниже молекулы получали по методикам, раскрытым в примере 14:
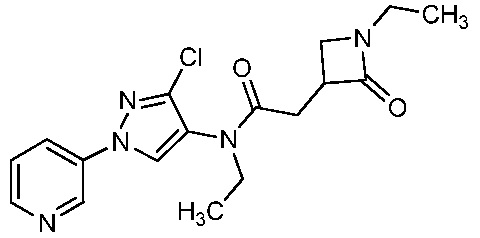
F84
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-2-(1-этил-2-оксоазетидин-3-ил)ацетамид (соединение F84) выделяли в виде смолообразного вещества (0,033 г, 15%).
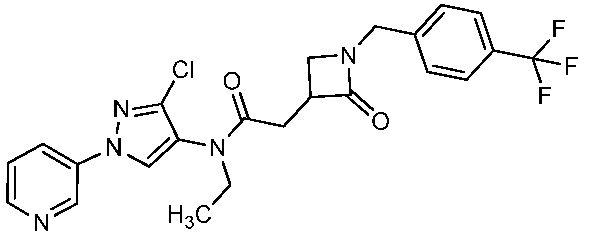
F14
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-2-(2-оксо-1-(4-трифторметил)бензил)азетидин-3-ил)ацетамид (соединение F14) выделяли в виде смолообразного вещества (0,080 г, 27%).
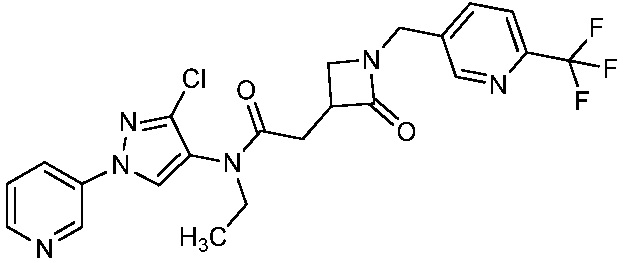
F117
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-2-(2-оксо-1-((6-трифторметил)пиридин-3-ил)метил)азетидин-3-ил)ацетамид) (соединение F117) выделяли в виде смолообразного вещества (0,050 г, 17%).
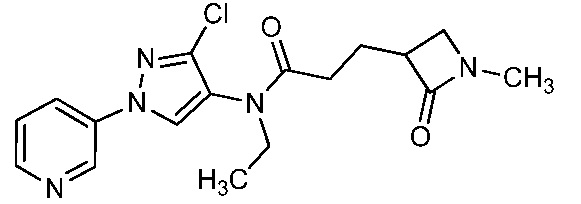
F119
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-3-(1-метил-2-оксоазетидин-3-ил)пропанамид (соединение F119) выделяли в виде смолообразного вещества (0,054 г, 25%).
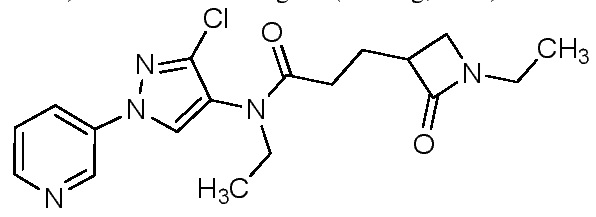
F103
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-3-(1-этил-2-оксоазетидин-3-ил)пропанамид (соединение F103) выделяли в виде смолообразного вещества (0,076 г, 34%).
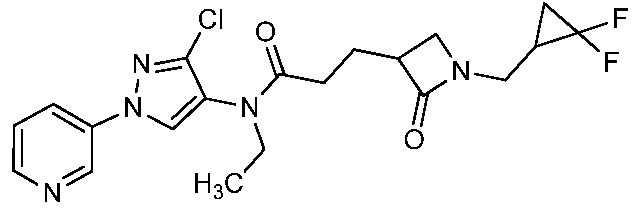
F74
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-3-1(1-((2,2-дифторциклопропил)метил)-2-оксоазетидин-3-ил)-N-этилпропанамид (соединение F74) выделяли в виде смолообразного вещества (0,0098 г, 8%).
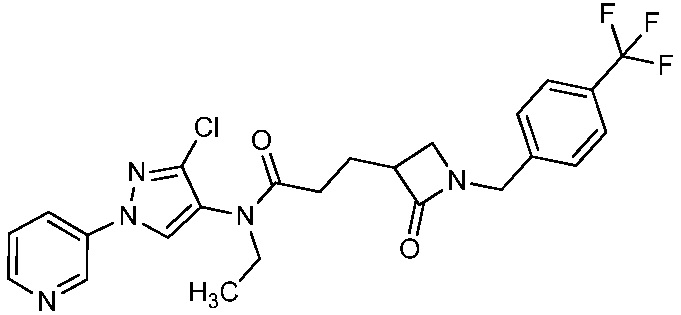
F129
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-3-(2-оксо-1-(4-трифторметил)бензил)азетидин-3-ил)пропанамид (соединение F129) выделяли в виде смолообразного вещества (0,166 г, 55%).
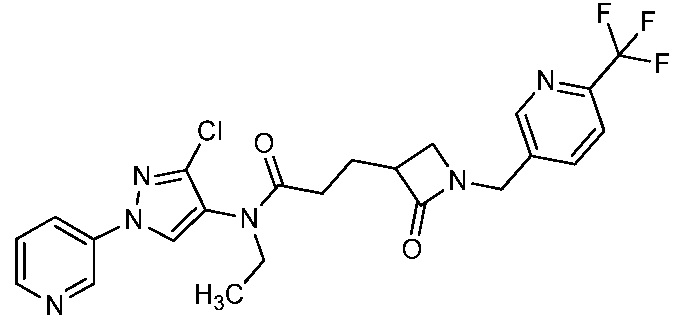
F91
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-3-(2-оксо-1-((6-(трифторметил)пиридин-3-ил)метил)азетидин-3-ил)пропанамид (соединение F91) выделяли в виде смолообразного вещества (0,057 г, 19%).
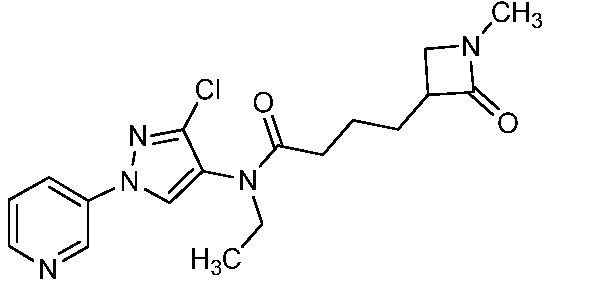
F53
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(1-метил-2-оксоазетидин-3-ил)бутанамид (соединение F53) выделяли в виде смолообразного вещества (0,112 г, 50%).
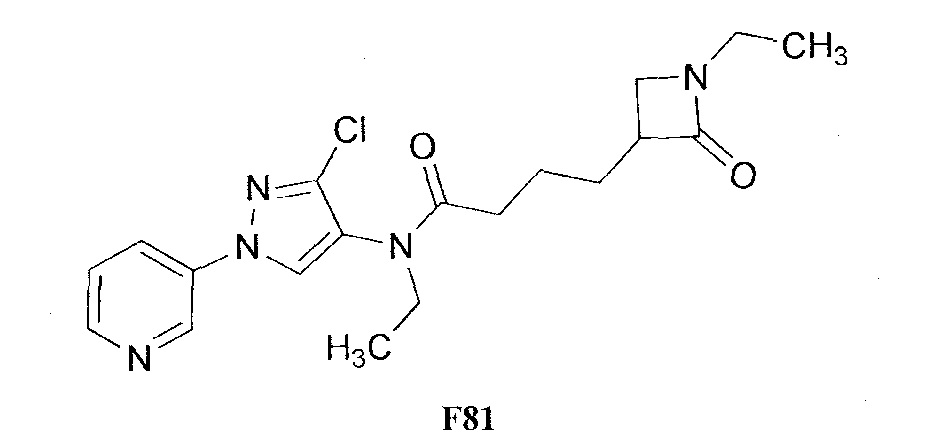
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(1-этил-2-оксоазетидин-3-ил)бутанамид (соединение F81) выделяли в виде смолообразного вещества (0,112 г, 48%).

F104
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-4-(1-((2,2-дифторциклопропил)метил)-2-оксоазетидин-3-ил)-N-этилбутанамид (соединение F104) выделяли в виде смолообразного вещества (0,010 г, 8%).
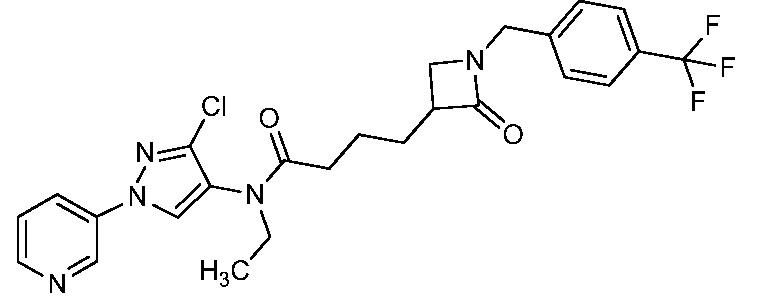
F127
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(2-оксо-1-(4-(трифторметил)бензил)азетидин-3-ил)бутанамид (соединение F127) выделяли в виде смолообразного вещества (0,121 г, 39%).
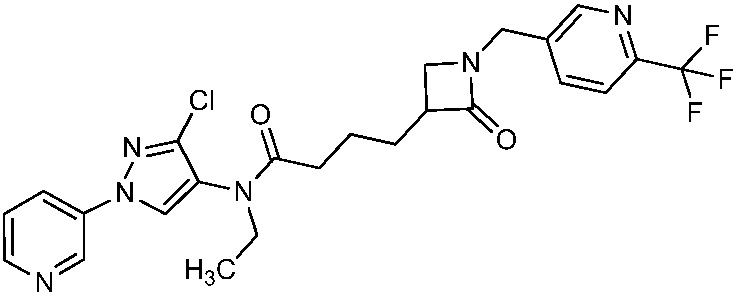
F87
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(2-оксо-1-((6-(трифторметил)пиридин-3-ил)метил)азетидин-3-ил)бутанамид (соединение F87) выделяли в виде смолообразного вещества (0,125 г, 40%).
Пример 15: Получение трет-бутил-((1R,4S)-4-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(метил)карбамоил)циклопент-2-ен-1-ил)карбамата (соединение F109)
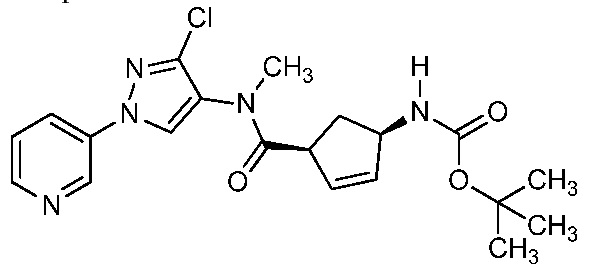
Раствор 3-хлор-N-метил-1-(пиридин-3-ил)-1H-пиразол-4-амина (0,20 г, 0,96 ммоля) в ТГФ (10 мл) охлаждали до температуры, равной примерно -78°C. Добавляли LHMDS (1 M раствор в гексанах, 1,0 мл, 1,00 ммоля) и раствор перемешивали при температуре, равной примерно -78°C, в течение 15 мин. При температуре, равной примерно -78°C, к раствору одной порцией добавляли раствор (1R,4S)-трет-бутил-3-оксо-2-азабицикло[2,2,1]гепт-5-ен-2-карбоксилата (0,20 г, 0,96 ммоля) в ТГФ (3 мл). После перемешивания в течение 1 ч при температуре, равной примерно -78°C, охлаждающую баню удаляли и реакционную смесь нагревали при температуре, равной примерно 20°C. После перемешивания в течение еще 5 мин к раствору добавляли уксусную кислоту (AcOH, 0,1 мл). Реакционную смесь концентрировали и очищали с помощью хроматографии на силикагеле при элюировании с помощью EtOAc/гексаны и получали искомое соединение F109 в виде белого твердого вещества (0,25 г, 59%).
Указанные ниже молекулы получали по методикам, раскрытым в примере 15:
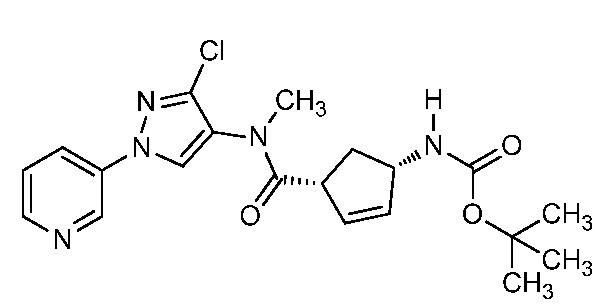
F116
трет-Бутил-((1S,4R)-4-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(метил)карбамоил)циклопент-2-ен-1-ил)карбамат (соединение F116) выделяли в виде розового вспененного вещества (3,46 г, 60%).
Пример 16: Получение (1S,4R)-4-амино-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-метилциклопент-2-енкарбоксамид-2,2,2-трифторацетата (соединение C6)
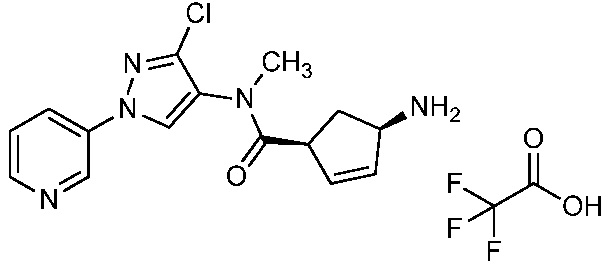
К раствору трет-бутил-((1R,4S)-4-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(метил)карбамоил)циклопент-2-ен-1-ил)карбамата (0,13 г, 0,31 ммоля) в CH2Cl2 (4 мл) добавляли ТФК (4 мл). Реакционную смесь выдерживали в течение 20 мин при периодическом взбалтывании. Реакционную смесь концентрировали в вакууме при температуре, равной примерно 40°C, что приводило к выделению искомого соединения C6 в виде прозрачного масла (0,13 г, 94%): 1H ЯМР (400 МГц, CD3OD) δ 9,02 (дд, J=2,7, 0,7 Гц, 1H), 8,70(c, 1H), 8,54 (дд, J=5,0, 1,4 Гц, 1H), 8,30 (ддд, J=8,4, 2,7, 1,4 Гц, 1H), 7,63 (ддд, J=8,4, 5,0, 0,7 Гц, 1H), 6,09 (ддд, J=5,6, 2,7, 1,0 Гц, 1H), 5,92 (дт, J=5,6, 2,1 Гц, 1H), 4,16 (д, J=7,7 Гц, 1H), 3,80-3,72 (м, 1H), 2,98 (c, 3H), 2,29 (дт, J=14,3, 7,9 Гц, 1H), 2,01 (дт, J=14,3, 2,5 Гц, 1H); 13C ЯМР (101 МГц, CDCl3) δ 179,16, 164,09, 163,71, 163,33, 162,94, 145,04, 142,05, 141,15, 137,81, 136,71, 134,11, 134,06, 132,73, 131,26, 129,77, 123,78, 120,92, 118,06, 115,21, 59,80, 51,85, 40,50, 36,87; ИЭРМС m/z 318 ([M+H]+).
Пример 17: Получение (1S,4R)-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-метил-4-(2,2,2-трифторацетамидо)циклопент-2-енкарбоксамида (соединение F126) и (1S,4R)-4-ацетамидо-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-метилциклопент-2-енкарбоксамида (соединение F24)
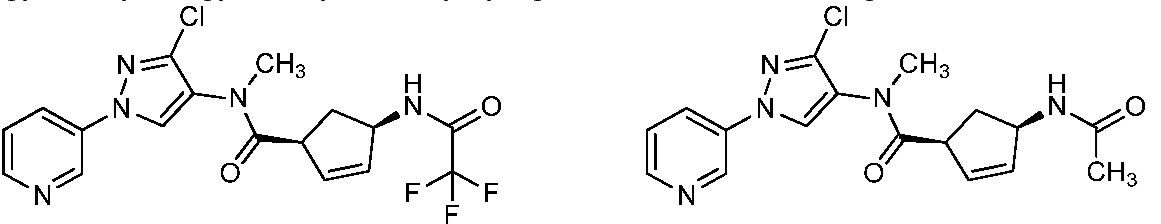
К раствору (1S,4R)-4-амино-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-метилциклопент-2-енкарбоксамид-2,2,2-трифторацетата (0,906 мг, 2,10 ммоля) в CH2Cl2 (25 мл), добавляли триэтиламин (0,637 мг, 6,29 ммоля) и ацетилхлорид (1 M в CH2Cl2, 3,15 мл, 3,15 ммоля). После перемешивания в течение 24 ч реакционную смесь разбавляли насыщенным водным раствором NaHCO3 (15 мл) и фазы разделяли. Органический слой сушили над безводным Na2SO4, фильтровали и концентрировали. Полученный остаток очищали с помощью хроматографии на силикагеле, сначала при элюировании с помощью EtOAC/гексаны и получали F126 в виде белого вспененного вещества (0,417 г, 48%), затем при элюировании с помощью MeOH/CH2Cl2 и получали соединение F24 в виде белого вспененного вещества (0,364 г, 48%).
Пример 18: Получение (1R,4S)-4-амино-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-метилциклопент-2-енкарбоксамиддигидрохлорида (соединение C7)
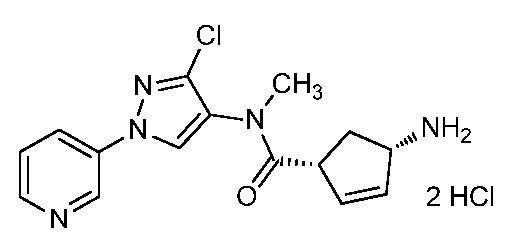
Твердый трет-бутил-((1S,4R)-4-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(метил)карбамоил)циклопент-2-ен-1-ил)карбамат (0,10 г, 0,25 ммоля) объединяли с хлористоводородной кислотой (HCl, 4 M в 1,4-диоксане, 2,0 мл, 8,0 ммоля) и MeOH (1 мл). После перемешивания в течение 3,5 ч реакционную смесь концентрировали и получали искомое соединение C7 в виде зеленовато-желтого твердого вещества (0,095 г, 99%): 1H ЯМР (400 МГц, CD3OD) δ 9,51 (д, J=2,3 Гц, 1H), 9,15-9,09 (м, 2H), 8,90 (д, J=5,5 Гц, 1H), 8,30 (дд, J=8,7, 5,6 Гц, 1H), 6,26 - 6,19 (м, 1H), 6,06 (дт, J=5,5, 1,7 Гц, 1H), 4,30 (д, J=7,4 Гц, 1H), 3,89 (д, J=7,5 Гц, 1H), 3,30 (c, 3H), 2,43 (дт, J=15,0, 7,7 Гц, 1H), 2,13 (дт, J=14,4, 2,5 Гц, 1H); 13C ЯМР (101 МГц, CD3OD) δ 176,53, 142,82, 141,12, 139,99, 138,74, 136,06, 134,13, 131,51, 130,90, 129,52, 127,40, 68,16, 57,35, 37,99, 34,44; ИЭРМС m/z 318 ([M+H]+).
Пример 19: Получение (1R,4S)-4-ацетамидо-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-метилциклопент-2-енкарбоксамида (соединение F86)
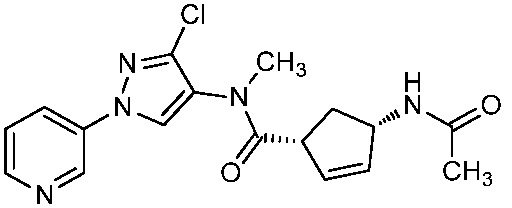
К суспензии (1R,4S)-4-амино-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-метилциклопент-2-енкарбоксамиддигидрохлорида (0,065 г, 0,17 ммоля) в CH2Cl2 (2 мл) добавляли триэтиламин (0,084 г, 0,83 ммоля), затем ацетилхлорид (1 M в CH2Cl2, 0,25 мл, 0,25 ммоля). После перемешивания в течение 24 ч, продукт реакции очищали путем прямого использования хроматографии на силикагеле при элюировании с помощью MeOH/CH2Cl2 и получали искомое соединение F86 в виде желтого вспененного вещества (0,040 г, 67%).
Пример 20: Получение (R)-4-ацетамидо-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-метилциклопент-1-енкарбоксамида (соединение F41)
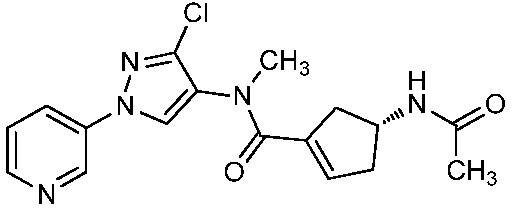
К раствору (1R,4S)-4-ацетамидо-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-метилциклопент-2-енкарбоксамида (0,230 г, 0,639 ммоля) в диметилсульфоксиде (ДМСО, 10 мл) добавляли 1,8-диазабицикло[5.4.0]ундец-7-ен (ДБУ, 4,00 мл, 26,7 ммоля). После перемешивания в течение 4 ч при температуре, равной 100°C, реакционную смесь охлаждали и разбавляли насыщенным водным раствором NH4Cl (200 мл) и экстрагировали с помощью EtOAc. Органический слой сушили над безводным Na2SO4, фильтровали и концентрировали. Полученный остаток очищали с помощью хроматографии на силикагеле при элюировании с помощью MeOH/CH2Cl2 и получали искомое соединение F41 в виде желтого масла (0,120 г, 44%).
Пример 21: Получение трет-бутил-((1S,4R)-4-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(метил)карбамоил)циклопентан-1-ил)карбамата (соединение F45)
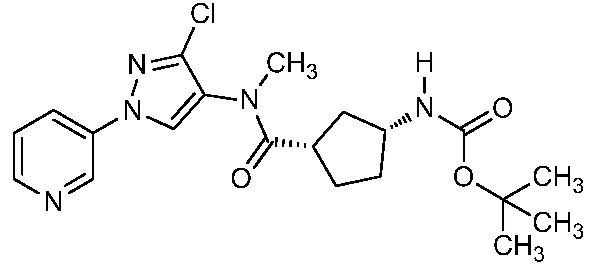
К раствору 3-хлор-N-метил-1-(пиридин-3-ил)-1H-пиразол-4-амин (0,109 г, 0,523 ммоля) и (1S,3R)-3-((трет-бутоксикарбонил)амино)циклопентанкарбоновой кислоты (0,120 г, 0,523 ммоля) в ДМФ (2,09 мл) добавляли O-(7-азабензотриазол-1-ил)-N,N,N′,N′-тетраметилуронийгексафторфосфат (HATU, 0,219 г, 0,576 ммоля) и получали коричневый раствор. К этому раствору добавляли 4-метилморфолин (0,115 мл, 1,05 ммоля). Реакционную смесь перемешивали при комнатной температуре в течение ночи. Вещество разбавляли с помощью EtOAc и водой. Органический слой сушили над MgSO4, фильтровали и концентрировали и получали масло апельсинового цвета, которое очищали с помощью хроматографии на силикагеле при элюировании с помощью EtOAc/гексаны и получали искомое соединение F45 в виде оранжевого масла (0,100 г, 39%).
Пример 22: Получение N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-оксопентанамида (соединение C8)
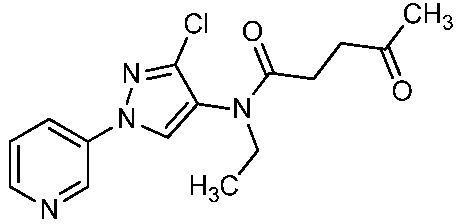
К смеси 3-хлор-N-этил-1-(пиридин-3-ил)-1H-пиразол-4-амина (1,00 г, 4,49 ммоля), 4-оксопентановой кислоты (0,626 г, 5,39 ммоля) и ДМАП (0,658 г, 5,39 ммоля) в диэтиловом эфире (10 мл) добавляли N,N'-метандиилиденбис(пропан-2-амин) (0,680 г, 5,39 ммоля) при температуре, равной примерно 0°C, и смесь перемешивали в течение 30 мин. Смесь нагревали до комнатной температуры и перемешивали при комнатной температуре в течение 1 ч. К смеси добавляли еще 1,2 экв. диизопропилкарбодиимида (0,820 г, 6,47 ммоля) и перемешивали при комнатной температуре в течение 16 ч. Реакцию останавливали насыщенным водным раствором NH4Cl и разбавляли с помощью EtOAc. Органическую фазу отделяли и водную фазу экстрагировали с помощью EtOAc. Объединенную органическую фазу промывали рассолом, сушили над MgSO4 и фильтровали. Удаление летучих веществ при пониженном давлении давало светло-коричневую смолу, которую очищали на силикагеле при элюировании с помощью MeOH/CH2Cl2 и получали искомое соединение C8 в виде бесцветного смолообразного вещества (1,41 г, 93 %): 1H ЯМР (400 МГц, CDCl3) δ 9,03 (дд, J=4,9, 2,6 Гц, 2H), 8,61 (м, 2H), 8,16 (д, J=3,2 Гц, 1H), 8,11 (дддд, J=8,4, 4,1, 2,6, 1,3 Гц, 2H), 7,50 (дт, J=8,5, 4,4 Гц, 2H), 3,66 (кв., J=7,0 Гц, 2H), 2,76 (т, J=6,2 Гц, 2H), 2,37 (т, J=6,1 Гц, 3H), 1,12 (тд, J=7,1, 1,3 Гц, 3H); ИЭРМС m/z 321 ([M+H]+).
Пример 23: Получение (E/Z)-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(метоксиимино)пентанамида (соединение F92)
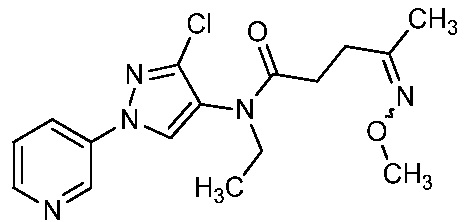
При перемешивании к раствору N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-оксопентанамида (0,142 г, 0,443 ммоля) в смеси пиридина (0,44 мл) и этанола (0,44 мл) добавляли O-метилгидроксиламингидрохлорид (0,129 мг, 1,50 ммоля). Реакционную смесь нагревали при температуре, равной 60°C, в течение 16 ч. Реакционную смесь охлаждали до комнатной температуры, разбавляли с помощью CH2Cl2 и затем промывали водой. Фазы разделяли, объединенные органические слои сушили над MgSO4, фильтровали, концентрировали и очищали с помощью хроматографии на силикагеле при элюировании с помощью 0%-50% ацетон/гексаны и получали искомое соединение F92 в виде бесцветного масла (0,116 г, 75%).
Указанные ниже молекулы получали по методикам, раскрытым в примере 23:
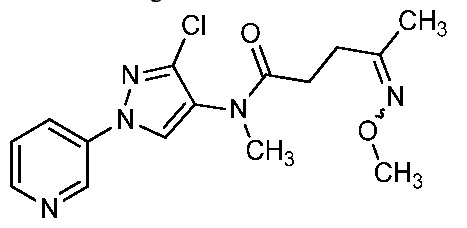
F60
(E/Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-4-(метоксиимино)-N-метилпентанамид (соединение F60) выделяли в виде бесцветного масла (0,188 г, 75%).
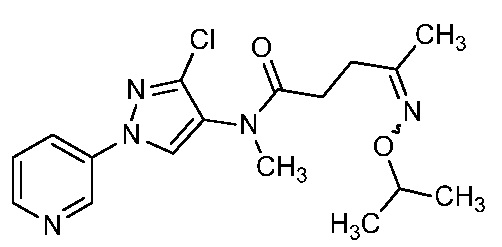
F130
(E/Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-4-(изопропоксиимино)-N-метилпентанамид (соединение F130) выделяли в виде бесцветного масла (0,135 г, 68%).
Пример 24: Получение 3-хлор-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этилпропанамида (соединение C9)
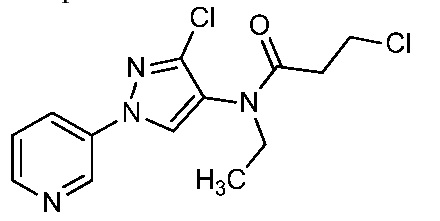
При перемешивании к раствору 3-хлор-N-этил-1-(пиридин-3-ил)-1H-пиразол-4-аминдигидрохлорида (1,00 г, 3,38 ммоля) в CH2Cl2 (7 мл) добавляли пропиленоксид (1,00 мл, 13,5 ммоля), затем 3-хлорпропаноилхлорид (0,360 мл, 3,72 ммоля). Смесь перемешивали при комнатной температуре в течение 16 ч и затем реакционную смесь разбавляли с помощью CH2Cl2 и промывали водой. Фазы разделяли, органическую фазу сушили, концентрировали и очищали с помощью хроматографии на силикагеле при элюировании с помощью 0%-50% ацетон/гексаны и получали белое твердое вещество (0,850 г, 80%): температура плавления 85-86°C; 1H ЯМР (400 МГц, CDCl3) δ 8,96 (д, J=2,6 Гц, 1H), 8,64 (дд, J=4,7, 1,4 Гц, 1H), 8,05 (ддд, J=8,3, 2,7, 1,4 Гц, 1H), 7,98 (c, 1H), 7,47 (ддд, J=8,4, 4,8, 0,6 Гц, 1H), 3,80 (т, J=6,7 Гц, 2H), 3,74 (кв., J=7,1 Гц, 2H), 2,64 (т, J=6,7 Гц, 2H), 1,18 (т, J=7,2 Гц, 3H); ИЭРМС m/z 313 ([M+H]+).
Указанные ниже молекулы получали по методикам, раскрытым в примере 24:
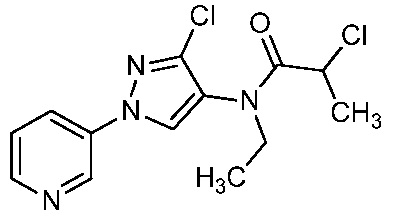
C10
2-Хлор-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этилпропанамид (соединение C10) выделяли в виде белого твердого вещества (1,25 г, 59%).
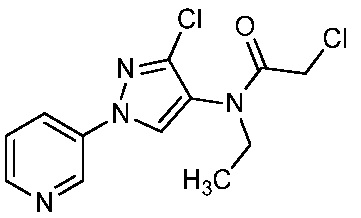
CA2
2-Хлор-N-[3-хлор-1-(3-пиридил)пиразол-4-ил]-N-этилацетамид (соединение CA2) выделяли в виде оранжевого масла (0,579 г, 86%): 1H ЯМР (400 МГц, CDCl3) δ 9,21 (c, 1H), 8,97 (д, J=2,6 Гц, 1H), 8,70-8,61 (м, 1H), 8,07 (c, 1H), 7,53-7,41 (м, 1H), 4,07-3,90 (м, 21H), 3,73 (c, 2H), 1,22-1,11 (м, 3H).
Пример 25: Получение N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-3-(метиламино)пропанамида (соединение C11)
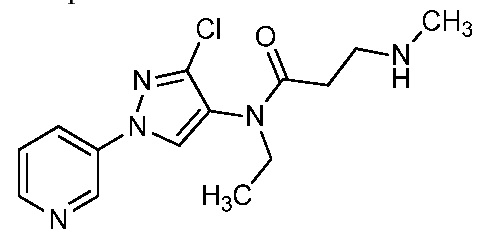
Монометиламин (33% раствор в EtOH, 11 мл, 90 ммоля) и 3-хлор-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этилпропанамид (1,9 г, 6,0 ммоля) закрывали в сосуде объемом 10-20 мл и нагревали в микроволновом реакторе BIOTAGE INITIATOR® в течение 1 ч при температуре, равной примерно 100°C, с наружным ИК-датчиком, наблюдая за температурой сбоку от сосуда. Затем реакционную смесь концентрировали и очищали с помощью хроматографии на силикагеле при элюировании с помощью 0%-10% MeOH/CH2Cl2 и получали желтое масло (1,7 г, 93 %): ИК (KBr, тонкая пленка) 3055, 2971, 2773, 1656 см-1; 1H ЯМР (400 МГц, ацетон-d6) δ 9,12 (дд, J=6,7, 2,6 Гц, 1H), 8,90 (c, 1H), 8,58 (дд, J=4,7, 1,4 Гц, 1H), 8,25 (м, 1H), 7,56 (м, 1H), 3,67 (кв., J=7,1 Гц, 2H), 3,01 (т, J=6,5 Гц, 2H), 2,66 (т, J=6,4 Гц, 2H), 2,50 (c, 3H), 1,12 (т, J=7,2 Гц, 3H); ИЭРМС m/z 308 ([M+H]+).
Пример 26: Получение N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-3-(N-метилацетамидо)пропанамида (соединение F64)
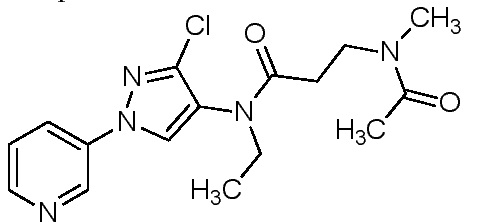
При перемешивании к раствору N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-3-(метиламино)пропанамиддигидрохлорида (0,060 г, 0,16 ммоля) в CH2Cl2 (0,5 мл) добавляли ДИПЭА (0,081 г, 0,60 ммоля), затем ацетилхлорид (0,019 мг, 0,24 ммоля). Реакционную смесь перемешивали в течение 16 ч. Затем реакционную смесь разбавляли с помощью CH2Cl2 и промывали водой. Органическую фазу отделяли, сушили, концентрировали и затем очищали с помощью хроматографии на силикагеле при элюировании с помощью 0%-10% MeOH/CH2Cl2 и получали искомое соединение F64 в виде бесцветного масла (0,025 г, 45%).
Указанные ниже молекулы получали по методикам, раскрытым в примере 26:
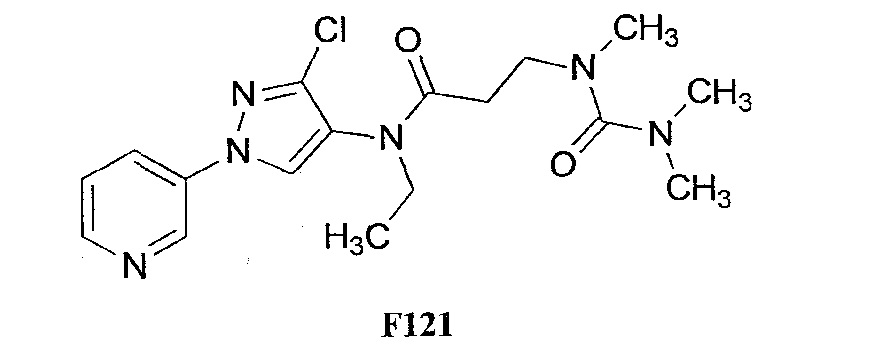
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-3-(1,3,3-триметилуреидо)пропанамид (соединение F121) выделяли в виде светло-желтого масла (0,071 г, 66%).
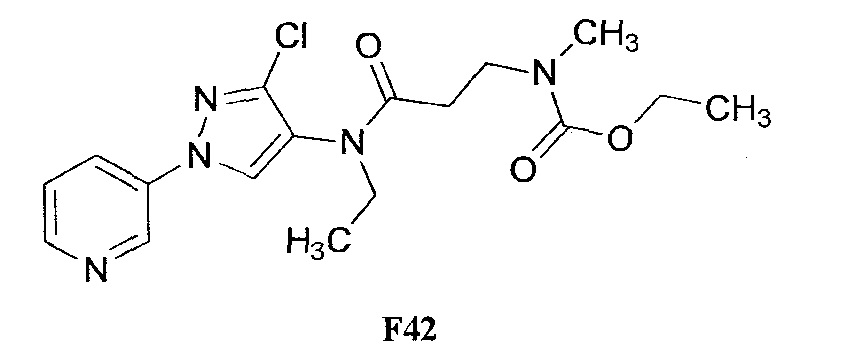
Этил-(3-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-3-оксопропил)(метил)карбамат (соединение F42) выделяли в виде бесцветного масла (0,065 г, 71%).
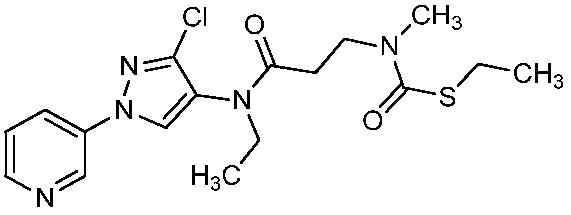
F40
S-Этил-(3-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-3-оксопропил)(метил)карбамотиоат (соединение F40) выделяли в виде бесцветного масла (0,065 г, 68%).
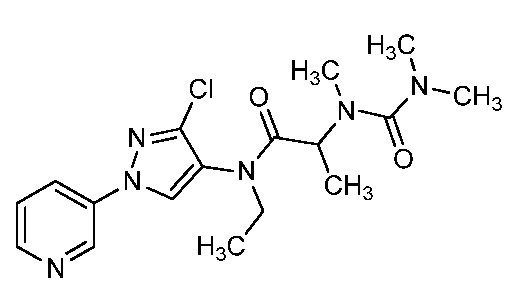
F114
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-2-(1,3,3-триметилуреидо)пропанамид (соединение F114) выделяли в виде оранжевого твердого вещества (0,147 г, 96%).
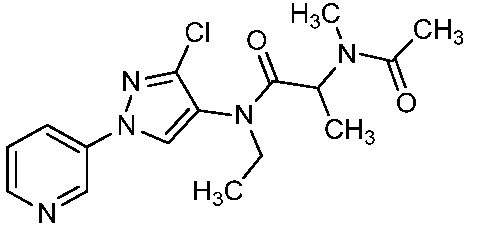
F96
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-2-(N-метилацетамидо)пропанамид (соединение F96) выделяли в виде масла (0,096 г, 68%).
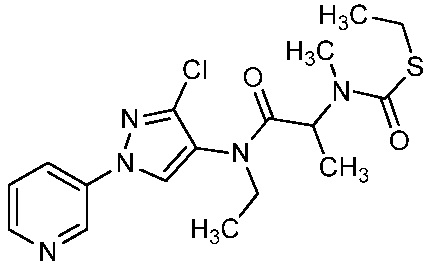
F79
S-Этил-(1-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-1-оксопропан-2-ил)(метил)карбамотиоат (соединение F79) выделяли в виде желтого масла (0,060 г, 41%).
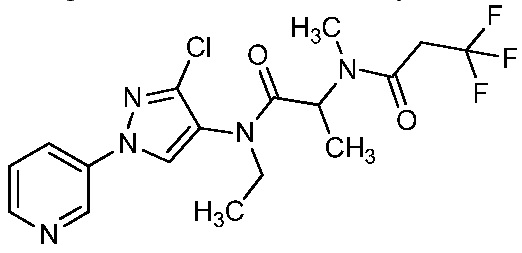
F66
N-(1-((3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-1-оксопропан-2-ил)-3,3,3-трифтор-N-метилпропанамид (соединение F66) выделяли в виде бесцветного масла (0,096 г, 57%).
Пример 27: Получение 1-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-1-оксопропан-2-илацетата (соединение C12)
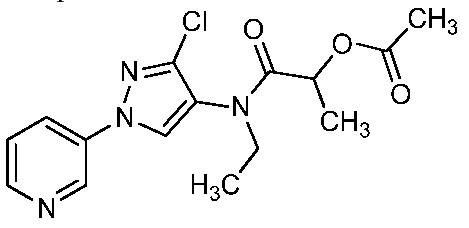
При перемешивании к раствору 3-хлор-N-этил-1-(пиридин-3-ил)-1H-пиразол-4-аминдигидрохлорида (3,00 г, 10,2 ммоля) в CH2Cl2 (20 мл), охлажденном в бане со льдом, добавляли триэтиламин (5,7 мл, 40,6 ммоля), затем по каплям добавляли 1-хлор-1-оксопропан-2-илацетат (1,3 мл, 10,2 ммоля). Реакционную смесь перемешивали в течение ночи, нагревая до комнатной температуры. Затем реакционную смесь разбавляли с помощью CH2Cl2 и промывали водой. Фазы разделяли и органические вещества сушили над MgSO4, фильтровали и концентрировали. Остаток очищали с помощью хроматографии на силикагеле при элюировании с помощью 0%-70% ацетон/гексаны и получали искомое соединение C12 в виде желтовато-коричневого карамелеобразного твердого вещества (3,2 г, 93%): 1H ЯМР (400 МГц, CDCl3) δ 8,99 (д, J=2,5 Гц, 1H), 8,62 (дд, J=4,8, 1,3 Гц, 1H), 8,18 (c, 1H), 8,04 (ддд, J=8,3, 2,7, 1,4 Гц, 1H), 7,46 (ддд, J=8,4, 4,8, 0,5 Гц, 1H), 5,01 (д, J=6,5 Гц, 1H), 3,54 (м, 2H), 2,09 (c, 3H), 1,39 (д, J=6,8 Гц, 3H), 1,17 (т, J=7,2 Гц, 3H); 13C ЯМР (101 МГц, CDCl3) δ 171,01, 148,62, 140,57, 140,24, 135,63, 127,56, 126,33, 124,06, 122,58, 67,49, 43,74, 20,61, 16,80, 12,57 (один сигнал углерода не локализован); ИЭРМС m/z 336,4 ([M+H]+), 335,0 ([M-H]-).
Пример 28: Получение N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-2-гидроксипропанамида (соединение C13)
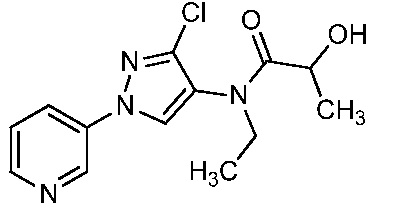
При перемешивании к раствору 1-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-1-оксопропан-2-илацетата (2,4 г, 7,1 ммоля) в MeOH (9 мл) и ТГФ (9 мл) добавляли гидроксид лития (LiOH, 2 M, 7,0 мл, 14 ммоля). Реакционную смесь перемешивали в течение 2 ч при комнатной температуре, и затем реакционную смесь нейтрализовывали путем добавления 2M водного раствора HCl. После того, как смесь экстрагировали с помощью EtOAc, органические фазы объединяли, сушили над MgSO4, фильтровали и концентрировали в вакууме и получали искомое соединение C13 в виде белого твердого вещества (1,9 г, 88%): температура плавления 137-138°C; 1H ЯМР (400 МГц, ДМСО) δ 9,08 (д, J=2,5 Гц, 1H), 8,98 (c, 1H), 8,58 (дд, J=4,7, 1,1 Гц, 1H), 8,23 (ддд, J=8,4, 2,6, 1,3 Гц, 1H), 7,59 (дд, J=8,3, 4,7 Гц, 1H), 4,97 (д, J=7,6 Гц, 1H), 4,08 (м, 1H), 3,57 (д, J=50,6 Гц, 2H), 1,10 (д, J=6,5 Гц, 3H), 1,07 (т, J=7,1 Гц, 3H); ИЭРМС m/z 295,6 ([M+H]+).
Пример 29: Получение 1-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-1-оксопропан-2-илдиметилкарбамата (соединение F93)
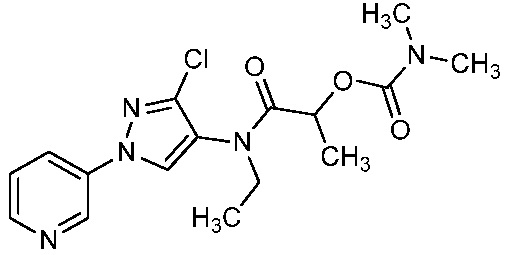
При перемешивании к раствору N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-2-гидроксипропанамида (0,10 г, 0,34 ммоля) в CH2Cl2 (1,1 мл) добавляли диметилкарбамилхлорид (0,073 г, 0,68 ммоля). Реакционную смесь перемешивали при комнатной температуре в течение 16 ч и затем разбавляли с помощью CH2Cl2, промывали водой. Фазы разделяли, сушили и концентрировали. Остаток очищали с помощью хроматографии на основном геле оксида алюминия при элюировании с помощью 0%-70% ацетон/гексаны и получали искомое соединение F93 в виде светло-желтого масла (0,11 г, 87%).
Указанные ниже молекулы получали по методикам, раскрытым в примере 29:
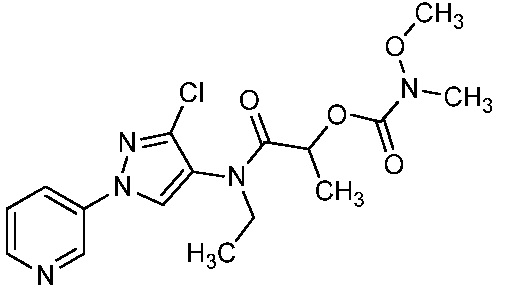
F16
1-((3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-1-оксопропан-2-илметокси(метил)карбамат (соединение F16) выделяли в виде бесцветного масла (0,127 г, 82%).
Пример 30: Получение трет-бутил-3-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)карбамоил)пирролидин-1-карбоксилата (соединение F11)
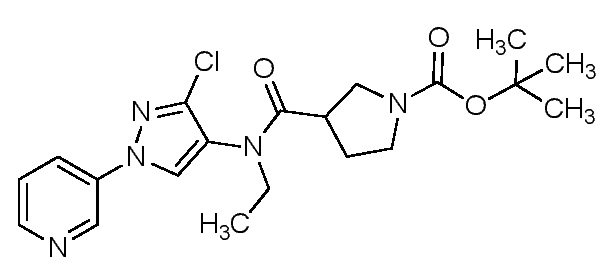
При перемешивании к раствору 3-хлор-N-этил-1-(пиридин-3-ил)-1H-пиразол-4-аминдигидрохлорида (0,20 г, 0,68 ммоля) в CH2Cl2 (1,4 мл) добавляли ДИПЭА (0,35 г, 2,7 ммоля), затем 1-(трет-бутоксикарбонил)пирролидин-3-карбоновую кислоту (0,22 г, 1,0 ммоля) и EDCI (0,20 г, 1,0 ммоля). Реакционную смесь перемешивали при комнатной температуре в течение 16 ч, затем концентрировали. Остаток очищали с помощью хроматографии на силикагеле при элюировании с помощью 0%-50% ацетон/гексаны и получали бесцветное масло (0,14 г, 49%).
Пример 31: Получение N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-метил-3-(2-оксооксазилидин-3-ил)пропанамида (соединение F31)
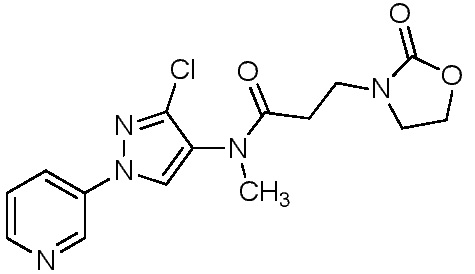
К раствору оксазолидин-2-она (0,038 г, 0,44 ммоля) в ДМФ (3 мл) добавляли NaH (60% дисперсия в масле, 0,011 г, 0,44 ммоля). Смесь перемешивали при температуре, равной примерно 0°C в течение 10 мин и добавляли 3-хлор-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-метилпропанамид (0,12 г, 0,40 ммоля). Полученную коричнево-желтую смесь перемешивали при комнатной температуре в течение 2 ч и разбавляли насыщенным водным раствором NH4Cl. Смесь разбавляли с помощью EtOAc и насыщенным водным раствором NaCl. Органическую фазу отделяли и водную фазу экстрагировали с помощью EtOAc (2×50 мл). Объединенные экстракты в EtOAc сушили над MgSO4, фильтровали и концентрировали при пониженном давлении и получали светло-коричневую смолу. Смолу очищали на силикагеле при элюировании с помощью MeOH/CH2Cl2 и получали искомое соединение F31 в виде бесцветного масла (0,13 г, 94 %).
Указанные ниже молекулы получали по методикам, раскрытым в примере 31:
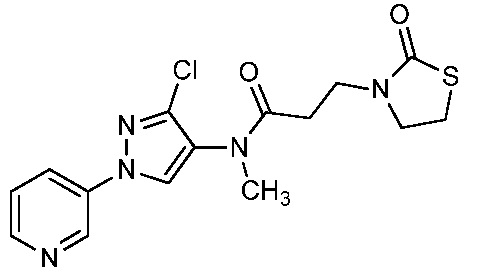
F38
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-метил-3-(2-оксотиазолидин-3-ил)пропанамид (соединение F38) выделяли в виде светло-коричневой смолы (0,029 г, 19%).
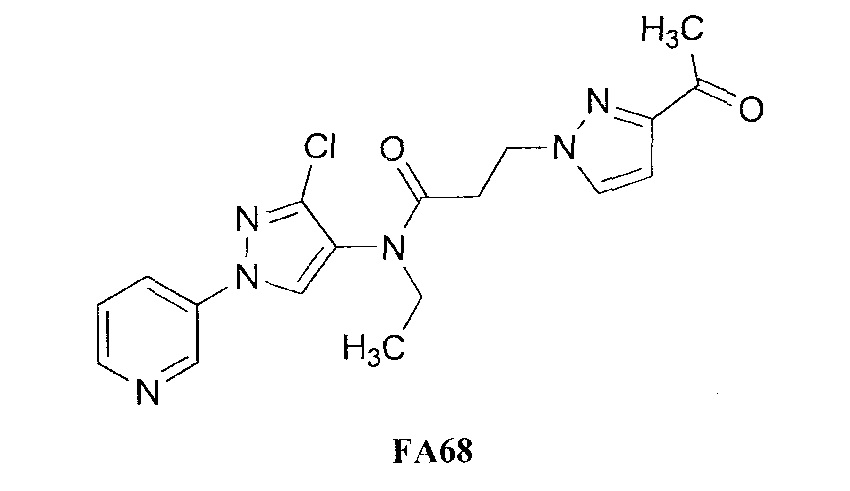
3-(3-Ацетил-1H-пиразол-1-ил)-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этилпропанамид (соединение FA68) выделяли в виде светло-коричневого масла (0,221 г, 59% выход).
Пример 32: Получение N-(3-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-3-оксопропил)-N-(2,2-дифторэтил)-2,2-дифторциклопропанкарбоксамида (соединение F34)
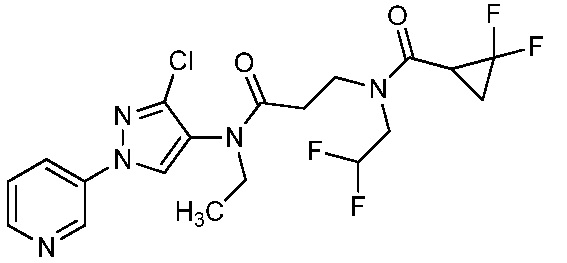
К раствору N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-3-((2,2-дифторэтил)амино)-N-этилпропанамида (0,10 г, 0,28 ммоля) в CH2Cl2 (2 мл) добавляли 2,2-дифторциклопропанкарбоновую кислоту (0,041 г, 0,34 ммоля), ДМАП (0,034 г, 0,28 ммоля) и N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-3-((2,2-дифторэтил)амино)-N-этилпропанамид (0,10 г, 0,28 ммоля) и смесь перемешивали при комнатной температуре в течение 2 ч. Смесь разбавляли с помощью CH2Cl2 и промывали насыщенным водным раствором NH4Cl и рассолом, сушили над MgSO4 и концентрировали при пониженном давлении и получали розовое масло. Остаток масла очищали на силикагеле при элюировании с помощью MeOH/CH2Cl2 и получали искомое соединение F34 в виде бесцветного масла (0,079 г, 58%).
Указанные ниже молекулы получали по методикам, раскрытым в примере 32:
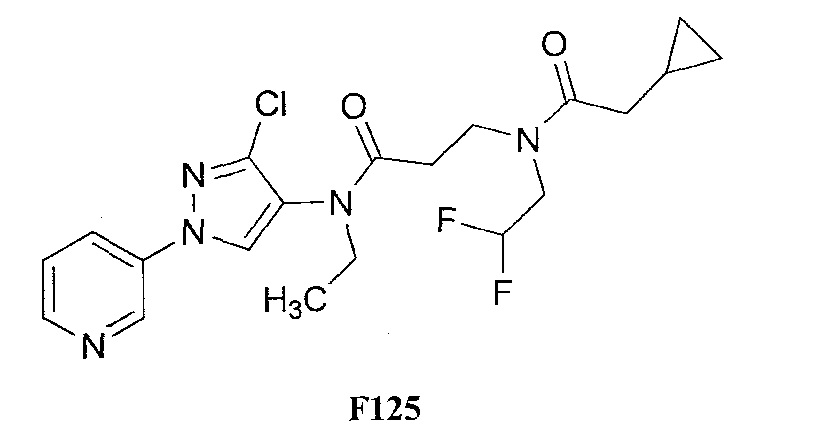
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-3-(2-циклопропил-N-(2,2-дифторэтил)ацетамидо)-N-этилпропанамид (соединение F125) выделяли в виде бесцветного масла (0,092 г, 75%).
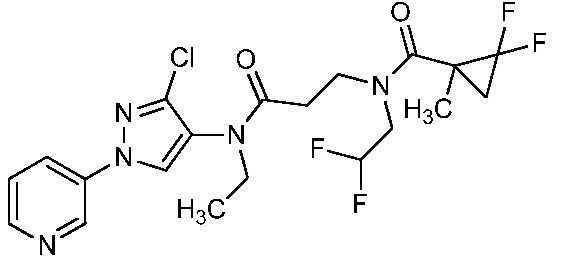
F35
N-(3-((3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-3-оксопропил)-N-(2,2-дифторэтил)-2,2-дифтор-1-метилциклопропан карбоксамид (соединение F35) выделяли в виде светло-коричневого масла (0,068 г, 51% выход).
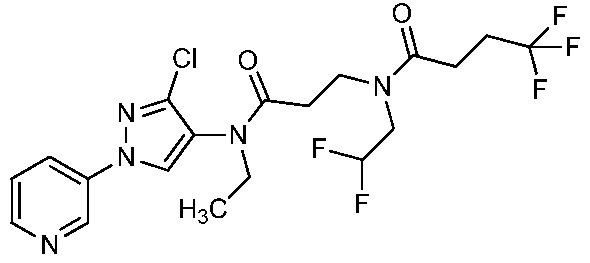
F89
N-(3-((3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-3-оксопропил)-N-(2,2-дифторэтил)-4,4,4-трифторбутанамид (соединение F89) выделяли в виде бесцветного масла (0,079 г, 56%).
Пример 33: Получение N-(3-((3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)(этил)амино)-3-оксопропил)-N-(2,2-дифторэтил)-1H-имидазол-1-карбоксамида (соединение F17)
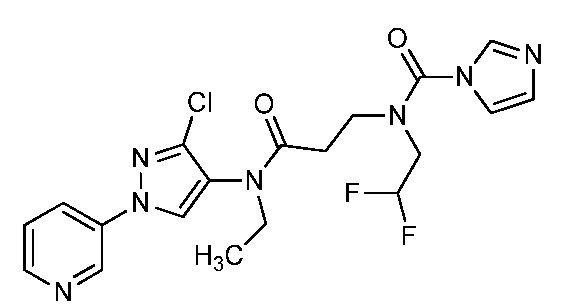
К раствору N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-3-((2,2-дифторэтил)амино)-N-этилпропанамида (0,10 г, 0,28 ммоля) в ДМФ (1 мл) добавляли карбонилдиимидазол (0,045 г, 0,28 ммоля) и смесь перемешивали при комнатной температуре в течение 3 ч. К смеси добавляли (2,2-дифторциклопропил)метанол (0,030 г, 0,28 ммоля) и перемешивали при комнатной температуре в течение 12 ч. Смесь разбавляли с помощью CH2Cl2 и промывали насыщенным водным раствором NH4Cl и рассолом, сушили над MgSO4 и концентрировали при пониженном давлении и получали коричневое масло. Остаток масла очищали на силикагеле при элюировании с помощью MeOH/CH2Cl2 и получали искомое соединение F17 в виде бесцветного смолообразного вещества (0,069 г, 55%).
Пример 34: Получение (E)-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(гидроксимино)пентанамида (соединение F105)
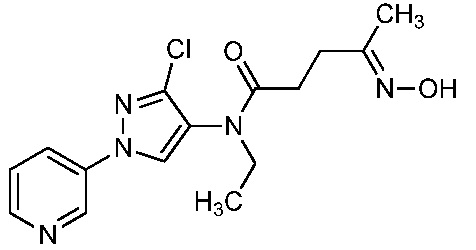
К раствору N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-оксопентанамида (0,10 г, 0,31 ммоля) в ТГФ (3,0 мл) добавляли раствор ацетата натрия (0,064 г, 0,78 ммоля) и гидроксиламин·HCl (0,033 г, 0,47 ммоля) в воде (0,5 мл) и смесь перемешивали в течение 1 ч. Смесь разбавляли с помощью EtOAc и водой. Органическую фазу отделяли и водную фазу экстрагировали с помощью EtOAc. Объединенную органическую фазу промывали рассолом, сушили над MgSO4 и фильтровали. Удаление летучих веществ при пониженном давлении давало бесцветную смолу, которую очищали на силикагеле при элюировании с помощью MeOH/CH2Cl2 и получали искомое соединение F105 в виде бесцветного смолообразного вещества (0,088 г, 80%).
Указанные ниже молекулы получали по методикам, раскрытым в примере 34:
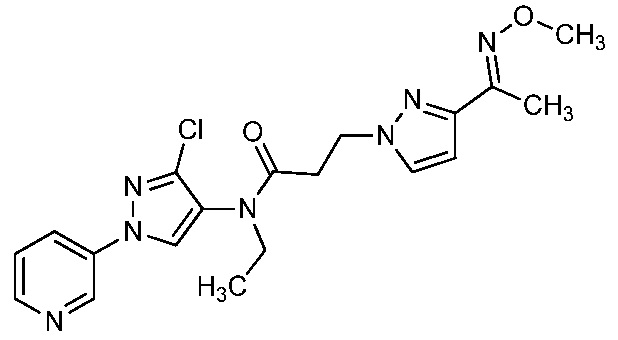
FA1
(E/Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-3-(3-(1-(метоксиимино)этил)-1H-пиразол-1-ил)пропанамид (соединение FA1) выделяли в виде светло-желтого масла (0,043 г, 80%).
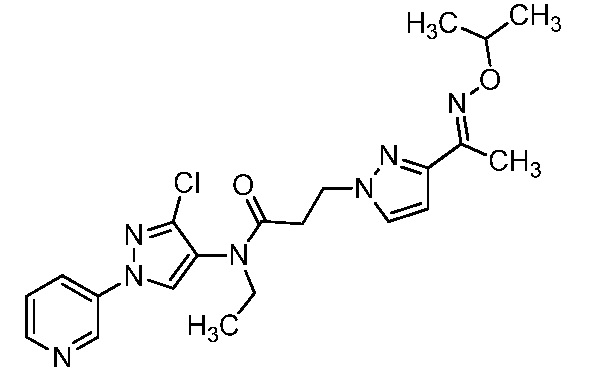
FA2
(E/Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-3-(3-(1-(изопропоксиимино)этил)-1H-пиразол-1-ил)пропанамид (соединение FA2) выделяли в виде бесцветного смолообразного вещества (0,048 г, 84%).
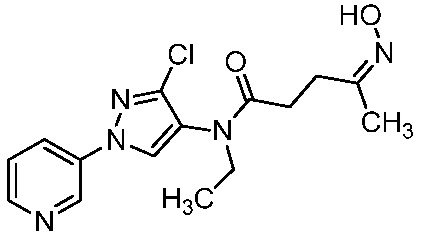
FA46
(Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(гидроксимино)пентанамид (соединение FA46) выделяли в виде бесцветного масла (0,158 г, 62%).
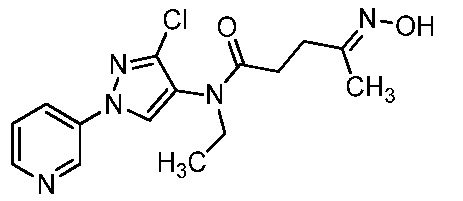
FA47
(E)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(гидроксимино)пентанамид (соединение FA47) выделяли в виде бесцветного масла (0,065 г, 26%).
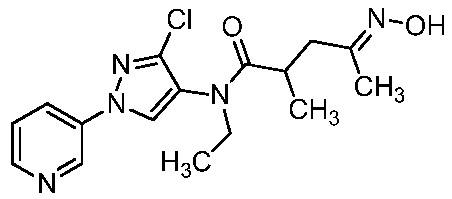
FA52
(E)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(гидроксимино)-2-метилпентанамид (соединение FA52) выделяли в виде бесцветного масла (0,015 г, 16%).
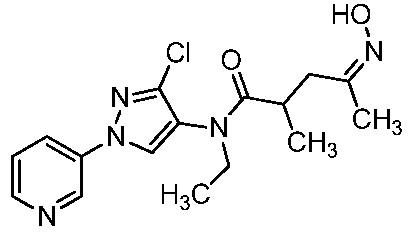
FA53
(Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(гидроксимино)-2-метилпентанамид (соединение FA53) выделяли в виде бесцветного масла (0,051 г, 54%).
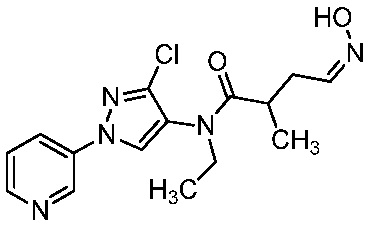
FA54
(Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(гидроксимино)-2-метилбутанамид (соединение FA54) выделяли в виде бесцветного масла (0,098 г, 17%).
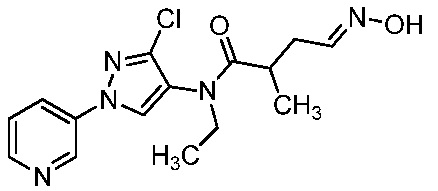
FA55
(E)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(гидроксимино)-2-метилбутанамид (соединение FA55) выделяли в виде бесцветного масла (0,148 г, 26%).
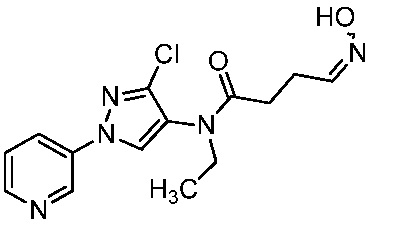
FA56
(E/Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(гидроксимино)бутанамид (соединение FA56) выделяли в виде бесцветного масла (0,204 г, 68%).
Пример 35: Получение (E/Z)-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-4-(((2,2-дифторциклопропил) метокси)имино)-N-этилпентанамида (соединение F72)
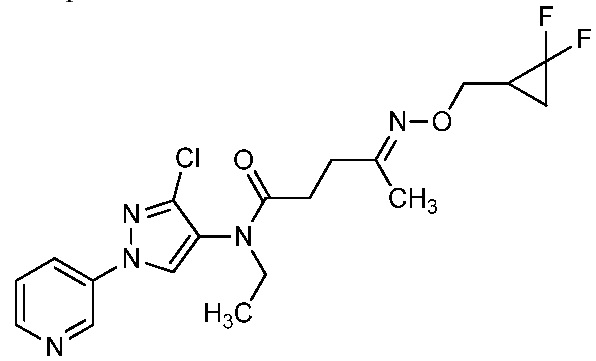
К раствору (E/Z)-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(гидроксимино)пентанамида (0,10 г, 0,30 ммоля) в сухом ТГФ (1 мл) при температуре, равной примерно 0°C, в атмосфере N2 добавляли NaH (60% дисперсия в масле, 0,013 г, 0,31 ммоля), затем 2-(бромметил)-1,1-дифторциклопропан (0,056 г, 0,33 ммоля). Смесь перемешивали в течение 1 ч и нагревали до комнатной температуры. После перемешивания в течение еще 1 ч реакцию останавливали насыщенным водным раствором NH4Cl и разбавляли с помощью EtOAc. Органическую фазу отделяли и водную фазу экстрагировали с помощью EtOAc. Объединенную органическую фазу промывали рассолом, сушили над MgSO4 и фильтровали. Удаление летучих веществ при пониженном давлении давало бесцветную смолу, которую очищали на силикагеле при элюировании с помощью MeOH/CH2Cl2 и получали искомое соединение F72 в виде коричневого масла (0,062 г, 46%).
Указанные ниже молекулы получали по методикам, раскрытым в примере 35:
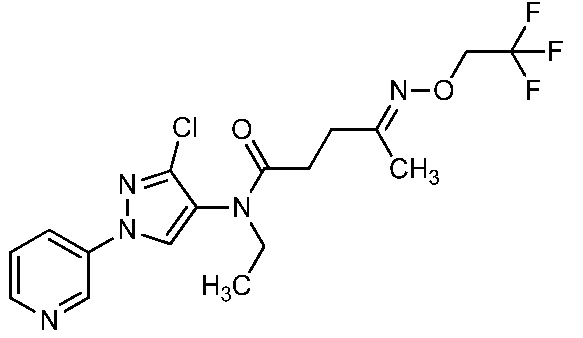
F51
(E/Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-((2,2,2-трифторэтокси)имино)пентанамид (соединение F51) выделяли в виде бесцветного масла (0,071 г, 54%).
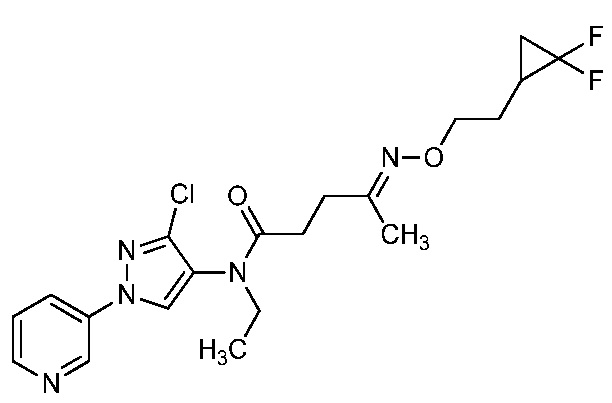
F20
(E/Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-4-((2-(2,2-дифторциклопропил)этокси)имино)-N-этилпентанамид (соединение F20) выделяли в виде бесцветного масла (0,059 г, 43%).
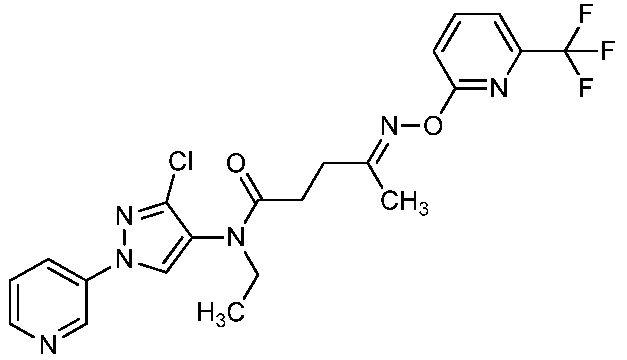
F59
(E/Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(((6-(трифторметил)пиридин-2-ил)окси)имино)пентанамид (соединение F59) выделяли в виде бесцветного масла (0,095 г, 75%).
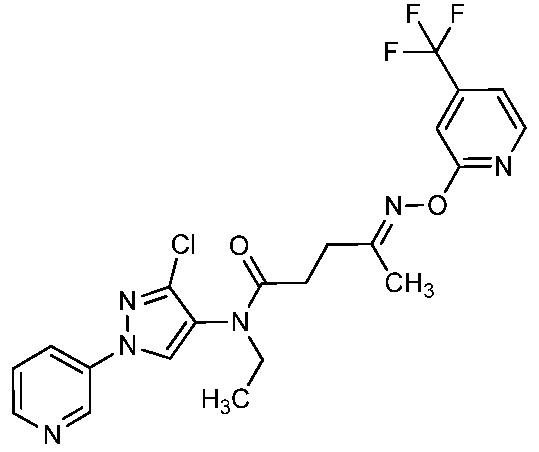
F36
(E/Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(((4-(трифторметил)пиридин-2-ил)окси)имино)пентанамид (соединение F36) выделяли в виде бесцветного масла (0,095 г, 82%).
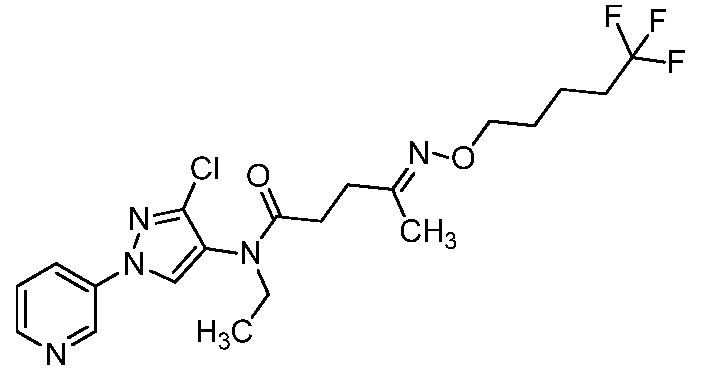
FA4
(E/Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(((5,5,5-трифторпентил)окси)имино)пентанамид (соединение FA4) выделяли в виде бесцветного смолообразного вещества (0,071 г, 52%).
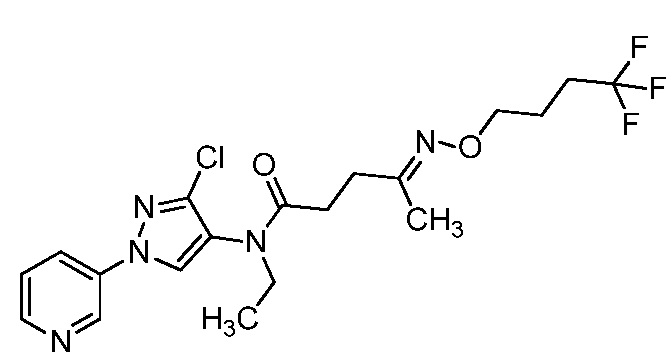
FA19
(E/Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-((4,4,4-трифторбутокси)имино)пентанамид (соединение FA19) выделяли в виде светло-желтого смолообразного вещества (0,098 г, 74%).
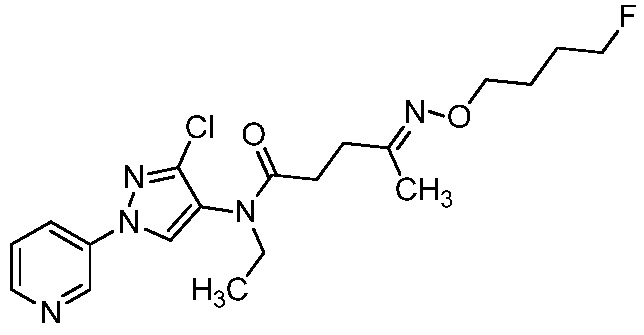
FA20
(E/Z)-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-((4-фторбутокси)имино)пентанамид (соединение FA20) выделяли в виде светло-желтого смолообразного вещества (0,063 г, 73%).
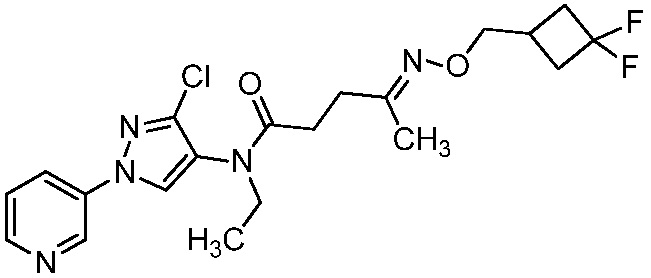
FA21
(E/Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-4-(((3,3-дифторциклобутил)метокси)имино)-N-этилпентанамид (соединение FA21) выделяли в виде бесцветной смолы (0,045 г, 34%).
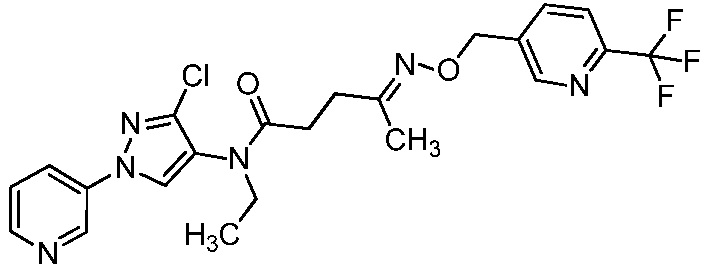
FA22
(E/Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(((6-(трифторметил)пиридин-3-ил)метокси)имино)пентанамид (соединение FA22) выделяли в виде светло-коричневой смолы (0,135 г, 87%).
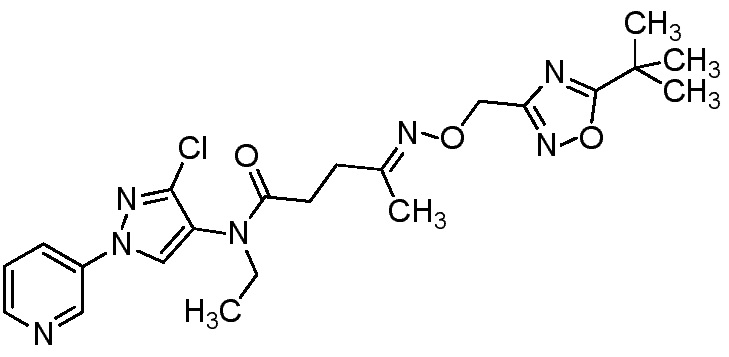
FA23
(E/Z)-4-(((5-(трет-Бутил)-1,2,4-оксадиазол-3-ил)метокси)имино)-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этилпентанамид (соединение FA23) выделяли в виде светло-коричневой смолы (0,124 г, 83%).
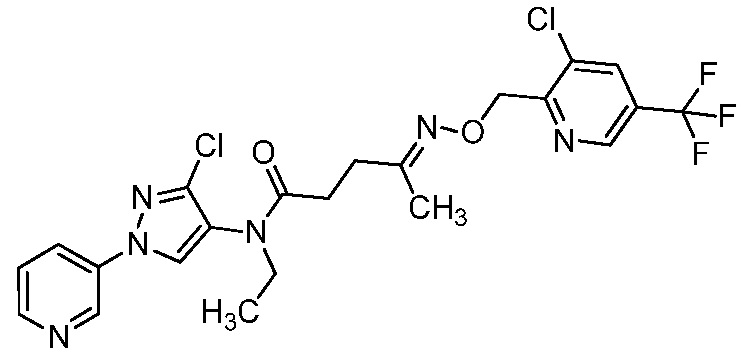
FA24
(E/Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-4-(((3-хлор-5-(трифторметил)пиридин-2-ил)метокси)имино)-N-этилпентанамид (соединение FA24) выделяли в виде светло-коричневой смолы (0,102 г, 61%).
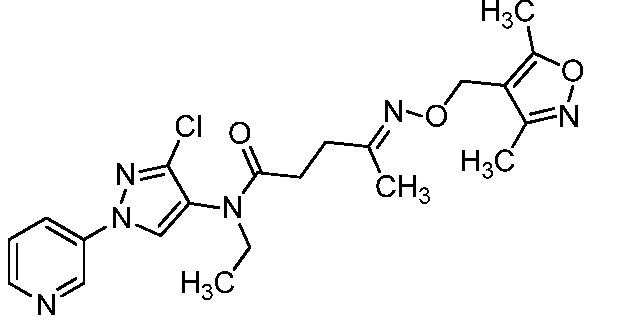
FA25
(E/Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-4-(((3,5-диметилизоксазол-4-ил)метокси)имино)-N-этилпентанамид (соединение FA25) выделяли в виде светло-коричневой смолы (0,099 г, 71%).
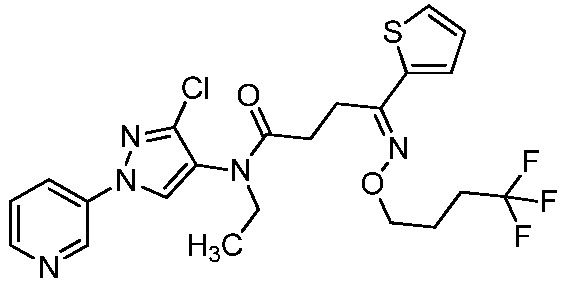
FA26
(E)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(тиофен-2-ил)-4-((4,4,4-трифторбутокси)имино)бутанамид (соединение FA26) выделяли в виде светло-желтой смолы (0,051 г, 38%).
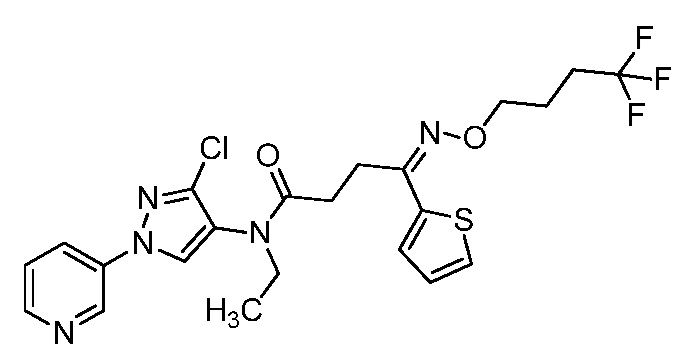
FA27
(Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(тиофен-2-ил)-4-((4,4,4-трифторбутокси)имино)бутанамид (соединение FA27) выделяли в виде светло-желтого смолообразного вещества (0,018 г, 13%).
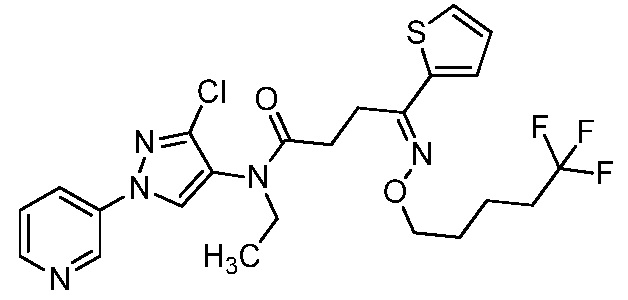
FA28
(E)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(тиофен-2-ил)-4-(((5,5,5-трифторпентил)окси)имино)бутанамид (соединение FA28) выделяли в виде светло-коричневой смолы (0,055 г, 40%).
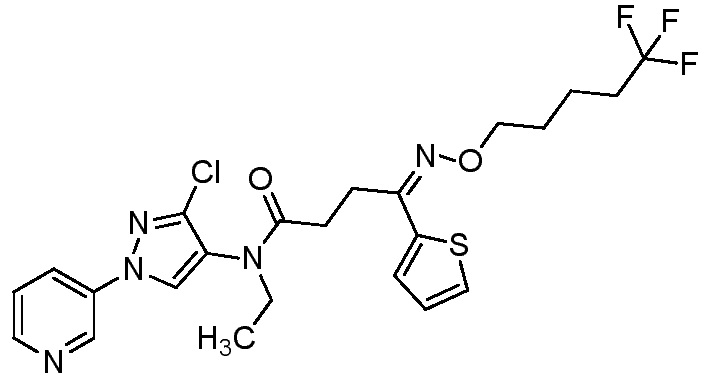
FA29
(Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(тиофен-2-ил)-4-(((5,5,5-трифторпентил)окси)имино)бутанамид (соединение FA29) выделяли в виде светло-коричневой смолы (0,021 г, 14%).
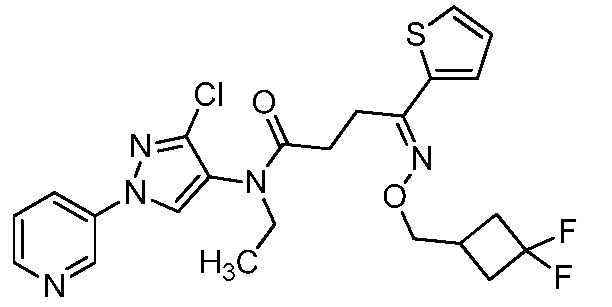
FA30
(E)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-4-(((3,3-дифторциклобутил)метокси)имино)-N-этил-4-(тиофен-2-ил)бутанамид (соединение FA30) выделяли в виде светло-коричневой смолы (0,053 г, 42%).
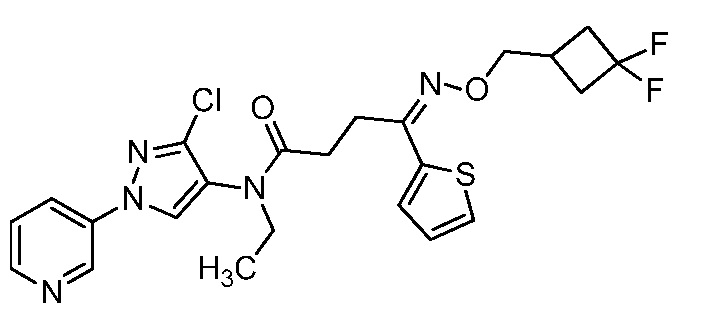
FA31
(Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-4-(((3,3-дифторциклобутил)метокси)имино)-N-этил-4-(тиофен-2-ил)бутанамид (соединение FA31) выделяли в виде светло-коричневой смолы (0,022 г, 17%).
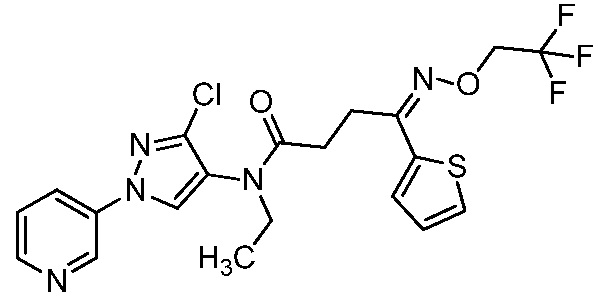
FA35
(E/Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(тиофен-2-ил)-4-((2,2,2-трифторэтокси)имино)бутанамид (соединение FA35) выделяли в виде светло-коричневой смолы (0,088 г, 69%).
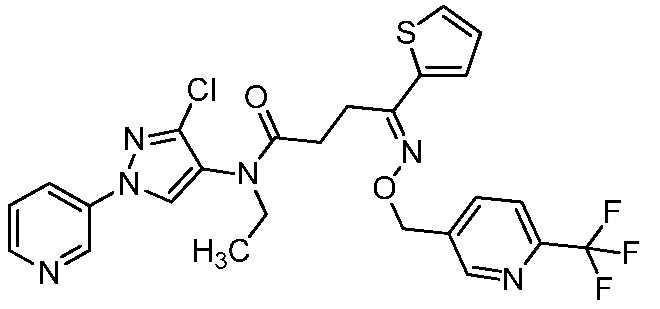
FA36
(E)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(тиофен-2-ил)-4-(((6-(трифторметил)пиридин-3-ил)метокси)имино)бутанамид (соединение FA36) выделяли в виде светло-коричневой смолы (0,058 г, 39%).
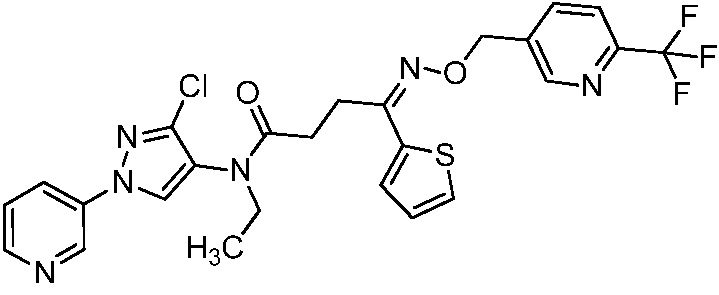
FA37
(Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(тиофен-2-ил)-4-(((6-(трифторметил)пиридин-3-ил)метокси)имино)бутанамид (соединение FA37) выделяли в виде светло-коричневой смолы (0,030 г, 20%).
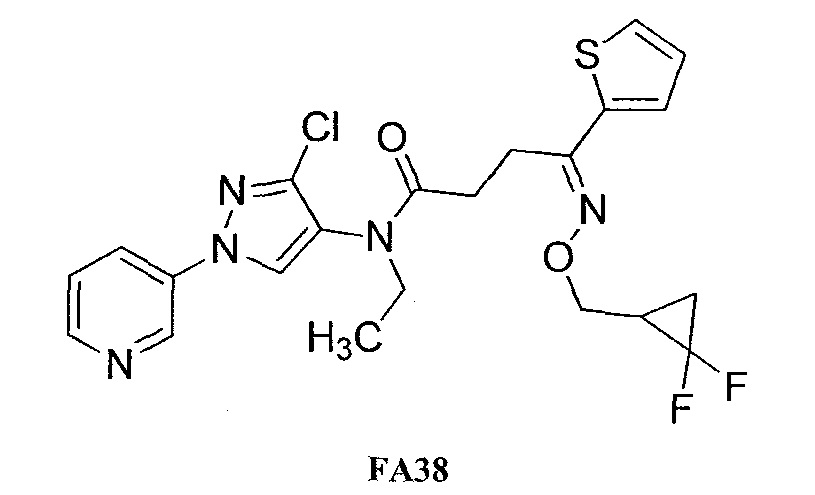
(E)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-4-(((2,2-дифторциклопропил)метокси)имино)-N-этил-4-(тиофен-2-ил)бутанамид (соединение FA38) выделяли в виде светло-коричневой смолы (0,040 г, 31%).
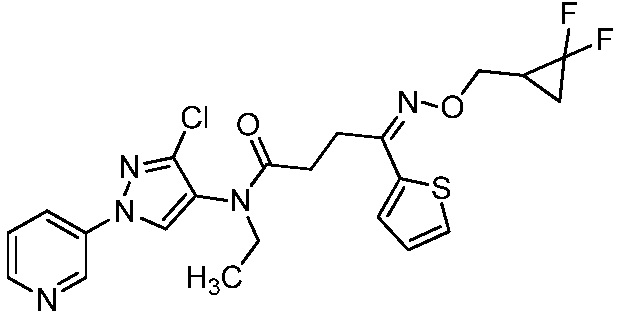
FA39
(Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-4-(((2,2-дифторциклопропил)метокси)имино)-N-этил-4-(тиофен-2-ил)бутанамид (соединение FA39) выделяли в виде светло-коричневой смолы (0,018 г, 14%).
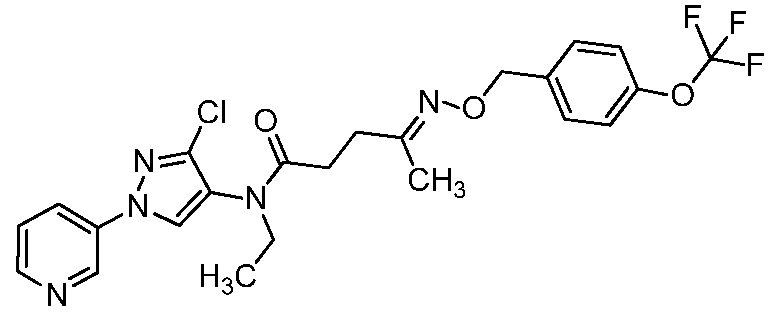
FA40
(E/Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-4-(((4-(трифторметокси)бензил)окси)имино)пентанамид (соединение FA40) выделяли в виде светло-коричневой смолы (0,044 г, 27%).
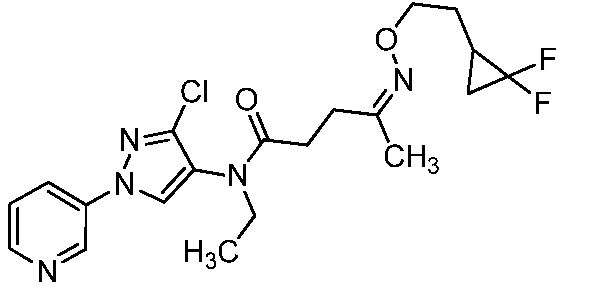
FA49
(Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-4-((2-(2,2-дифторциклопропил)этокси)имино)-N-этилпентанамид (соединение FA49) выделяли в виде бесцветного масла (0,55 г, 56%).
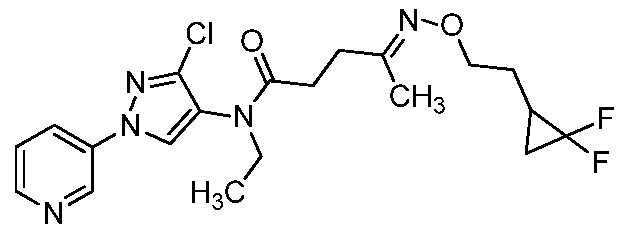
FA50
(E)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-4-((2-(2,2-дифторциклопропил)этокси)имино)-N-этилпентанамид (соединение FA50) выделяли в виде бесцветного масла (0,57 г, 67%).
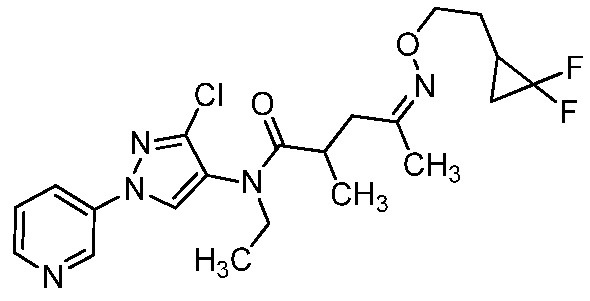
FA57
(Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-4-((2-(2,2-дифторциклопропил)этокси)имино)-N-этил-2-метилпентанамид (соединение FA57) выделяли в виде бесцветного масла (0,026 г, 41%).
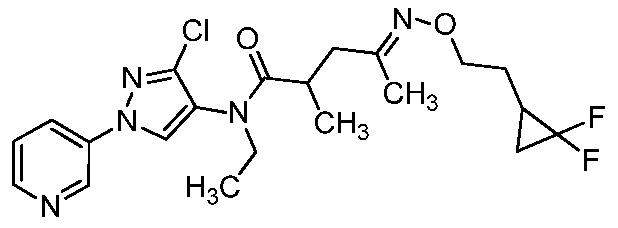
FA58
(E)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-4-((2-(2,2-дифторциклопропил)этокси)имино)-N-этил-2-метилпентанамид (соединение FA58) выделяли в виде бесцветного масла (0,011 г, 57%).
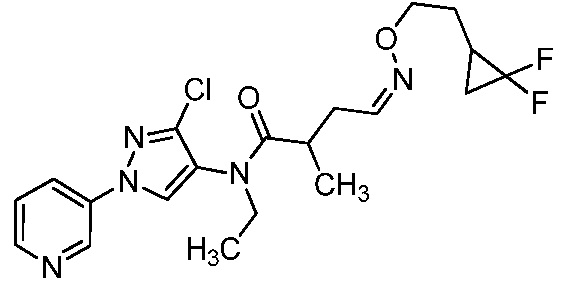
FA59
(Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-4-((2-(2,2-дифторциклопропил)этокси)имино)-N-этил-2-метилбутанамид (соединение FA59) выделяли в виде бесцветного масла (0,096 г, 47%).
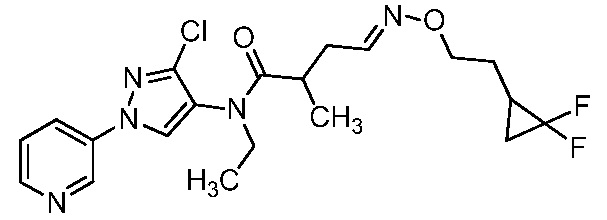
FA60
(E)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-4-((2-(2,2-дифторциклопропил)этокси)имино)-N-этил-2-метилбутанамид (соединение FA60) выделяли в виде бесцветного масла (0,059 г, 47%).
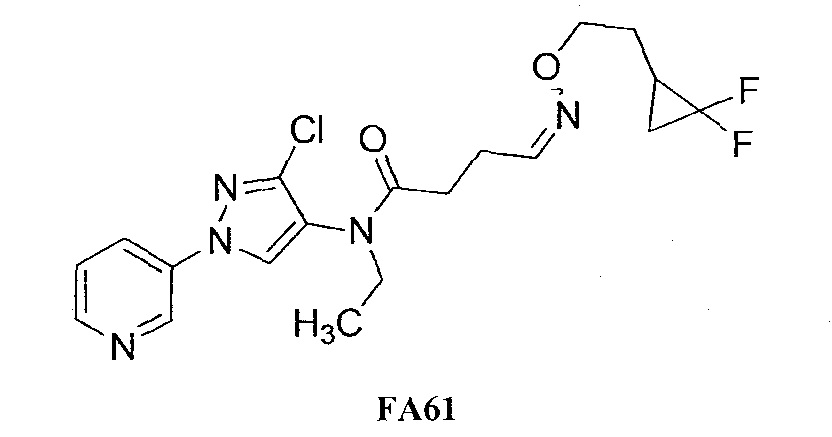
(E/Z)-N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-4-((2-(2,2-дифторциклопропил)этокси)имино)-N-этилбутанамид (соединение FA61) выделяли в виде бесцветного масла (0,208 г, 79%).
Пример 36: Получение N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-3-((2,2-дифторэтил)амино)-N-этилпропанамида (соединение C14)
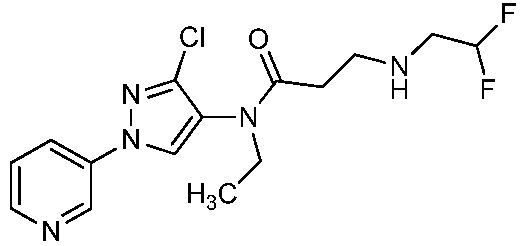
К раствору 3-хлор-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этилпропанамида (1,30 г, 4,15 ммоля) в 1,4-диоксане (15 мл) добавляли ДИПЭА (1,13 г, 8,72 ммоля) и 2,2-дифторэтанамин (0,67 г, 8,30 ммоля) и закрывали в сосуде объемом 10-20 мл и нагревали в микроволновом реакторе BIOTAGE INITIATOR® в течение 16 ч при температуре, равной 140°C, с наружным ИК-датчиком, наблюдая за температурой сбоку от сосуда. Смесь фильтровали и твердые вещества промывали с помощью EtOAc. Фильтрат концентрировали при пониженном давлении и получали коричневую смолу, которую очищали на силикагеле при элюировании с помощью MeOH/CH2Cl2 и получали искомое соединение C14 в виде коричневой смолы (1,22 г, 73,9 %).
Пример PE1: Получение N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-2-(2-оксо-3-(3,3,3-трифторпропил)пирролидин-1-ил)ацетамида (соединение P3)
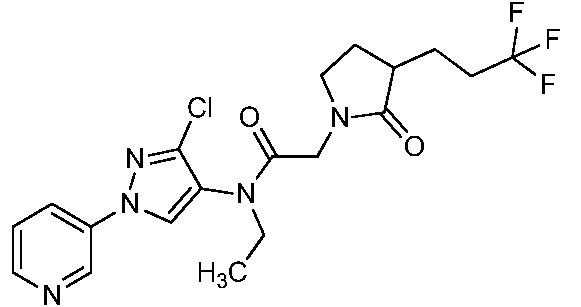
К 3-(3,3,3-трифторпропил)пирролидин-2-ону в подходящем реакционном сосуде можно добавить NaH (от примерно 1,0 экв. до примерно 2,0 экв.) в растворителе, таком как ТГФ (при концентрации, равной от примерно 0,01 M до примерно 1 M), затем 2-хлор-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этилацетамид (от примерно 0,5 экв. до примерно 1,5 экв.). Реакционную смесь можно перемешивать при температуре, равной от примерно 0°C до примерно 25°C, до установления завершения реакции. После завершения реакции продукт можно получить по стандартным методикам обработки и очистки, использующимся в органической химии.
Следующие соединения, указанные в таблице 5, можно получить в соответствии с процедурами, раскрытыми в примере PE1: P1, P2, P3, P4, P5, P6, P7.
Пример PE2: Получение N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-2-(2-оксо-1-(3,3,3-трифторпропил)пирролидин-3-ил)ацетамида (соединение P6)
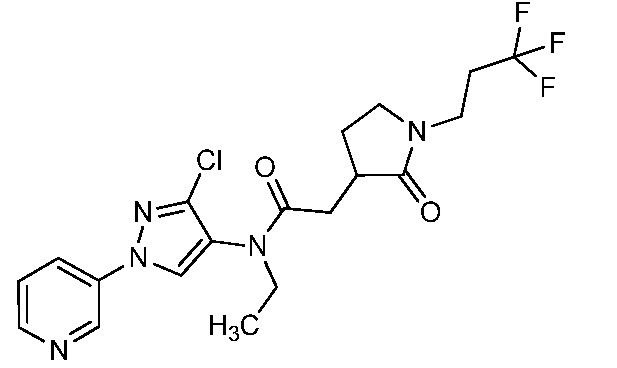
К N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-2-(2-оксопирролидин-3-ил)ацетамиду в подходящем реакционном сосуде можно добавить NaH (от примерно 1,0 экв. до примерно 2,0 экв.) в растворителе, таком как ТГФ (при концентрации, равной от примерно 0,01 M до примерно 1 M), затем 2-хлор-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этилацетамид (от примерно 1,0 экв. до примерно 2,0 экв.). Реакционную смесь можно перемешивать при температуре, равной от примерно 0°C до примерно 25°C, до установления завершения реакции. После завершения реакции продукт можно получить по стандартным методикам обработки и очистки, использующимся в органической химии.
Следующие соединения, указанные в таблице 5, можно получить в соответствии с процедурами, раскрытыми в примере PE2: P8, P9, P10, P11, P12, P13, P14, P15, P18, P19.
Пример PE3: Получение N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-1-(3,3,3-трифторпропаноил)пиперидин-4-карбоксамида (соединение P16)
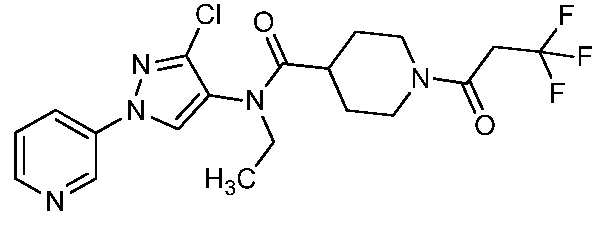
В подходящем реакционном сосуде к N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этилпиперидин-4-карбоксамиду можно добавить 3,3,3-трифторпропановую кислоту (от примерно 1,0 до примерно 2,0 экв.), ДМАП (от примерно 2,0 до примерно 3,0 экв.) и EDCI (от примерно 1,5 до примерно 3,0 экв.) в растворителе, таком как CH2Cl2 (при концентрации, равной от примерно 0,01 M до примерно 1 M). Реакционную смесь можно перемешивать при температуре, равной от примерно 0°C до примерно 50°C, до установления завершения реакции. После завершения реакции продукт можно получить по стандартным методикам обработки и очистки, использующимся в органической химии.
Следующие соединения, указанные в таблице 5, можно получить в соответствии с процедурами, раскрытыми в примере PE3: P16, P17, P20, P21, P22, P23, P24, P25, P28, P29, P30, P31, P32, P33.
Пример PE4: Получение (E/Z)-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-7,7,7-трифтор-3-(метоксиимино)гептанамида (соединение P26)
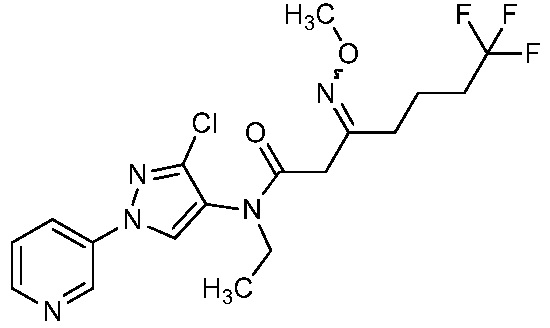
В подходящем реакционном сосуде к N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-7,7,7-трифтор-3-оксогептанамиду можно добавить систему растворителей, такую как пиридин и этанол (при концентрации, равной от примерно 0,01 M до примерно 1 M) и O-метилгидроксиламин·гидрохлорид (от примерно 2,0 до примерно 3,0 экв.). Реакционную смесь можно перемешивать при температуре, равной от примерно 25°C до примерно 80°C, до установления завершения реакции. После завершения реакции продукт можно получить по стандартным методикам обработки и очистки, использующимся в органической химии.
Следующие соединения, указанные в таблице 5, можно получить в соответствии с процедурами, раскрытыми в примере PE4: P26, P27.
Пример PE5: Получение (1S,3R)-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-3-(N-метилацетамидо)циклопентанкарбоксамида (соединение P36)
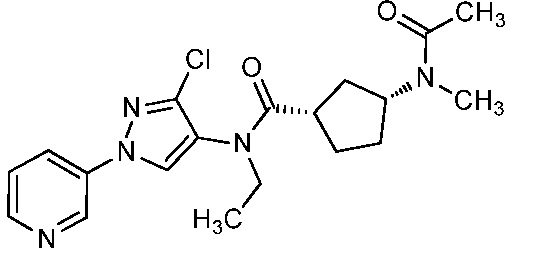
В подходящем реакционном сосуде к (1S,3R)-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-3-(метиламино)циклопентанкарбоксамиду можно добавить ацетилхлорид (от примерно 1,0 до примерно 2,0 экв.) и ДМАП (от примерно 2,0 до примерно 3,0 экв.) в растворителе, таком как CH2Cl2 (при концентрации, равной от примерно 0,01 M до примерно 1 M). Реакционную смесь можно перемешивать при температуре, равной от примерно 0°C до примерно 50°C, до установления завершения реакции. После завершения реакции продукт можно получить по стандартным методикам обработки и очистки, использующимся в органической химии.
Следующие соединения, указанные в таблице 5, можно получить в соответствии с процедурами, раскрытыми в примере PE5: P34, P35, P36, P37.
Пример PE6: Получение N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-1-(3,3,3-трифторпропаноил)пиперидин-4-карбоксамида (соединение P39)
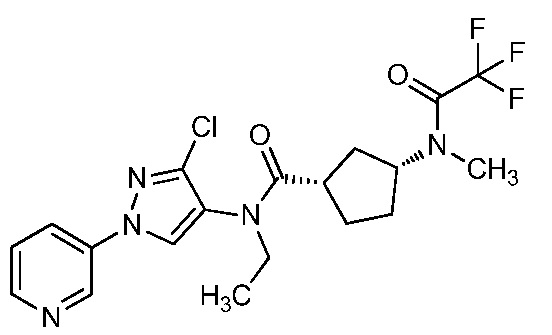
В подходящем реакционном сосуде к (1S,3R)-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-3-(метиламино)циклопентанкарбоксамиду можно добавить трифторуксусный ангидрид (от примерно 1,0 до примерно 2,0 экв.) и N-метилморфолин (от примерно 2,0 до примерно 3,0 экв.) в растворителе, таком как CH2Cl2 (при концентрации, равной от примерно 0,01 M до примерно 1 M). Реакционную смесь можно перемешивать при температуре, равной от примерно 0°C до примерно 50°C, до установления завершения реакции. После завершения реакции продукт можно получить по стандартным методикам обработки и очистки, использующимся в органической химии.
Следующие соединения, указанные в таблице 5, можно получить в соответствии с процедурами, раскрытыми в примере PE6: P38, P39.
Пример 37: Получение N-[3-хлор-1-(3-пиридил)пиразол-4-ил]-N-этил-3-[2-оксо-1-(2,2,2-трифторэтил)пирролидин-3-ил]пропанамид (соединение P1)
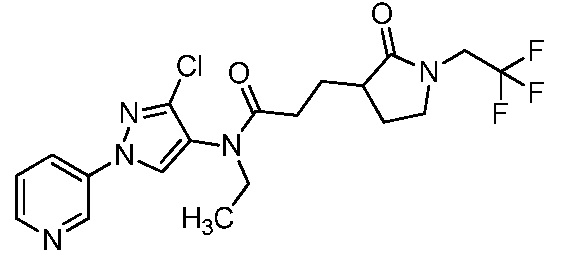
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-3-(2-оксопирролидин-3-ил)пропанамид (0,037 г, 0,10 ммоля) добавляли в сосуд, снабженный стержнем для магнитной мешалки, затем гидрид натрия (60% в минеральном масле, 0,010 г, 0,26 ммоля). В сосуде создавали атмосферу N2 и охлаждали до 0°C. Затем добавляли ТГФ (1 мл) и реакционную смесь перемешивали в течение 30 мин. По каплям добавляли неразбавленный 2,2,2-трифторэтилтрифторметансульфонат (0,037 мл, 0,26 ммоля). Реакционную смесь перемешивали в течение ночи. Реакционную смесь адсорбировали на целите®. Очистка с помощью колоночной флэш-хроматографии с использованием MeOH/CH2Cl2 в качестве элюента давала искомое соединение в виде бесцветного масла (0,011 г, 24%).
Указанные ниже молекулы получали по методикам, раскрытым в примере 37:
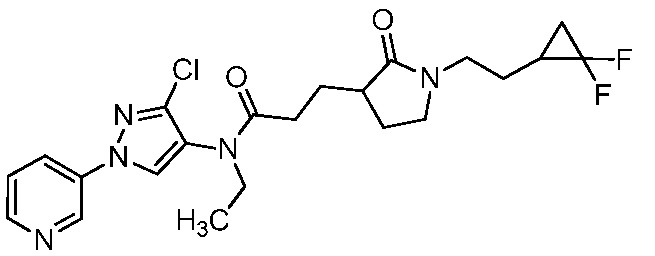
FA62
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-3-(1-(2-(2,2-дифторциклопропил)этил)-2-оксопирролидин-3-ил)-N-этилпропанамид (соединение FA62) выделяли в виде бесцветного масла (0,026 г, 40%).
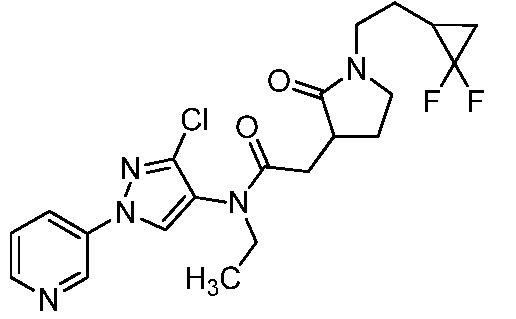
FA64
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-2-(1-(2-(2,2-дифторциклопропил)этил)-2-оксопирролидин-3-ил)-N-этилацетамид (соединение FA64) выделяли в виде бесцветного масла (0,027 г, 35%).
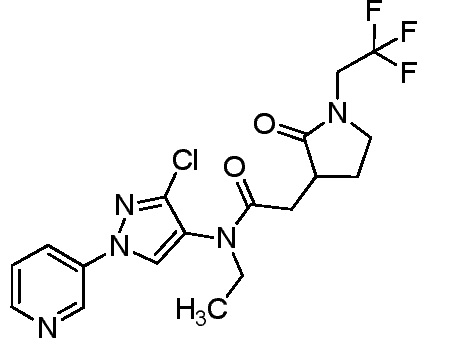
FA65
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-2-(2-оксо-1-(2,2,2-трифторэтил)пирролидин-3-ил)ацетамид (соединение FA65) выделяли в виде бесцветного масла (0,047 г, 63%).
Пример 38: Получение N-[3-хлор-1-(3-пиридил)пиразол-4-ил]-N-этил-2-метил-4-оксобутанамида (соединение FA48)
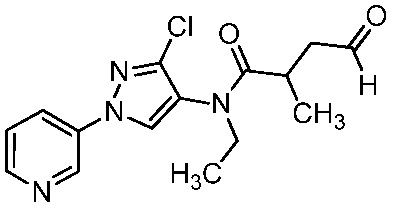
К N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-2-метилпент-4-енамиду (0,450 г, 1,41 ммоля) в колбе, снабженной стержнем для магнитной мешалки, растворенному в CH2Cl2 (13 мл) и MeOH (1,3 мл), добавляли раствор индикатора судан III (0,01 M, 0,060 мл). Колбу присоединяли к генератору озона и при перемешивании начинали пропускать поток кислорода. Реакционную смесь охлаждали до -78°C и образовавшийся озон пропускали через раствор в течение примерно 6 мин, после чего розовая окраска исчезала и желтый раствор начинал становиться зелено-синим. Выработку озона прекращали и через реакционную смесь в течение примерно 5 мин пропускали чистый кислород, затем темная окраска бледнела и проявлялась желтая окраска. Все еще при -78°C добавляли трифенилфосфин (0,555 г, 2,12 ммоля) в виде твердого вещества и охлаждающую баню удаляли. К колбе присоединяли патрубок для подачи азота и реакционной смеси давали медленно нагреться до комнатной температуры. Затем продукт концентрировали и загружали в целит®. Очистка с помощью колоночной флэш-хроматографии с использованием 0-40% ацетон/гексаны давала искомое соединение в виде прозрачного желтого масла, которое при выдерживании кристаллизовалось (0,390 г, 73%).
Пример 39: Получение N-[3-хлор-1-(3-пиридил)пиразол-4-ил]-N-этил-2-метил-4-оксопентанамида (соединение FA51)
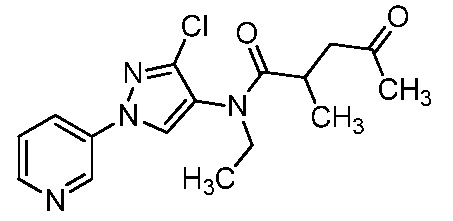
N-(3-Хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-2-метил-4-оксобутанамид (0,390 г, 1,22 ммоля) растворяли в ТГФ (12 мл) при -78°C. К этому раствору при перемешивании по каплям добавляли метилмагнийбромид (0,446 мл, 1,34 ммоля). Реакционную смесь перемешивали при -78°C в течение 30 мин и нагревали при 0°C, затем реакцию останавливали насыщенным водным раствором NH4Cl. Продукт реакции экстрагировали диэтиловым эфиром и объединенные органические вещества промывали рассолом, затем сушили над Na2SO4 и концентрировали в вакууме и получали желтое масло. Масло загружали в целит® и очищали с помощью колоночной флэш-хроматографии с использованием 0-50% ацетон/гексаны в качестве элюента. Вторичный спирт извлекали в виде неочищенного масла и сразу использовали. Оставшееся масло переносили в CH2Cl2 (10 мл) и вводили буфер, NaHCO3 (0,153 г, 1,82 ммоля). Полученную смесь охлаждали до 0°C и одной порцией добавляли перйодинан Десса-Мартина (0,516 г, 1,22 ммоля). Реакционную смесь перемешивали при 0°C в течение 1 ч, затем нагревали до комнатной температуры. Реакцию останавливали путем медленного добавления насыщенного водного раствора бисульфита натрия и экстрагировали с помощью CH2Cl2. Органический слой промывали рассолом, сушили над Na2SO4 и концентрировали с получением масла, которое загружали прямо в целит®. Очистка с помощью колоночной флэш-хроматографии с использованием 0-40% ацетон/гексаны в качестве элюента давала искомое соединение в виде прозрачного бесцветного масла. (0,0900 г, 20% за 2 стадии).
Пример 40: Получение N-[3-хлор-1-(3-пиридил)пиразол-4-ил]-N-этил-2-(2-оксопирролидин-3-ил)ацетамида (соединение FA63)
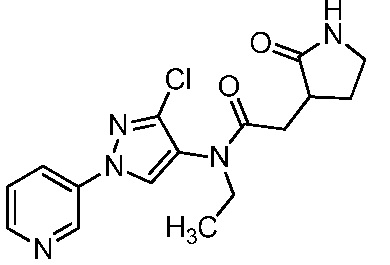
ДИПЭА (0,629 мл, 4,41 ммоля) растворяли в ТГФ (20 мл) и охлаждали примерно до -78°C. Затем добавляли н-бутиллитий (1,77 мл, 4,41 ммоля) и реакционную смесь нагревали примерно до 0°C в течение 10 мин, затем повторно охлаждали примерно до -78°C. Затем добавляли 1-(трет-бутилдиметилсилил)пирролидин-2-он (0,800 г, 4,01 ммоля) и реакционную смесь нагревали при 23°C и перемешивали в течение 1 ч. Затем реакционную смесь повторно охлаждали до -78°C и затем по каплям добавляли 2-хлор-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этилацетамид (0,600 г, 2,01 ммоля) в виде раствора в ТГФ (3 мл). Реакционную смесь перемешивали в холодном виде в течение 30 мин, затем ей давали медленно нагреваться до комнатной температуры. Через 1 ч реакцию останавливали раствором NH4Cl и экстрагировали диэтиловым эфиром. Органические вещества промывали рассолом, сушили над Na2SO4 и концентрировали. Полученное масло очищали с помощью колоночной флэш-хроматографии с использованием 0-40% ацетон/гексаны в качестве элюента и получали промежуточный продукт, 2-(1-(трет-бутилдиметилсилил)-2-оксопирролидин-3-ил)-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этилацетамид (0,604 г, 1,31 ммоля). Анализ с помощью 1H ЯМР показывал наличие смеси молекул, причем отношение количества искомого продукта к основному побочному продукту составляло примерно 5:1. Смесь направляли на стадию удаления защитной группы без дополнительной очистки. 2-(1-(трет-Бутилдиметилсилил)-2-оксопирролидин-3-ил)-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этилацетамид (0,604 г, 1,31 ммоля) растворяли в ТГФ (13 мл) и добавляли тетрабутиламмонийфторид (ТБАФ, 1,96 мл, 1,96 ммоля). Реакционную смесь перемешивали в течение 30 мин. Продукт реакции концентрировали на целите® и очищали с помощью колоночной флэш-хроматографии с использованием 40-100% ацетон/гексаны в качестве элюента и получали искомое соединение (0,204 г, 30% за 2 стадии).
Пример 41: Получение 3-(бут-3-ен-1-ил)пирролидин-2-она (соединение CA3)
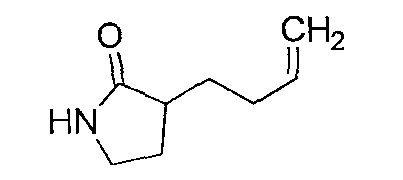
ДИПЭА (0,393 мл, 2,76 ммоля) растворяли в ТГФ (25 мл) и охлаждали до -78°C. н-бутиллитий (1,10 мл, 2,76 ммоля) затем добавляли, и реакционную смесь нагревали при 0°C и повторно охлаждали до -78°C. Затем добавляли 1-(трет-бутилдиметилсилил)пирролидин-2-он (0,500 г, 2,51 ммоля) в виде раствора в ТГФ (1 мл) и реакционную смесь нагревали до комнатной температуры в течение 1 ч. Затем реакционную смесь повторно охлаждали до -78°C и по каплям добавляли 4-бромбут-1-ен (0,305 мл, 3,01 ммоля) в ТГФ (1 мл). Реакционную смесь медленно нагревали до комнатной температуры в течение ночи. Реакционную смесь концентрировали с получением масла, которое загружали прямо в целит®. Очистка с помощью колоночной флэш-хроматографии с использованием 0-30% ацетон/гексаны давала искомое соединение (0,218 г, 62%): 1H ЯМР (400 МГц, CDCl3) δ 6,15 (c, 1H), 5,82 (ддт, J=17,0, 10,2, 6,6 Гц, 1H), 5,09 4,87 (м, 2H), 3,42 3,24 (м, 2H), 2,44 2,25 (м, 2H), 2,24 2,05 (м, 2H), 1,99 (дддд, J=13,6, 9,4, 6,9, 4,1 Гц, 1H), 1,78 (д кв., J=12,1, 8,4 Гц, 1H), 1,45 (дтд, J=13,7, 9,1, 5,5 Гц, 1H); 13C ЯМР (101 МГц, CDCl3) δ 180,44, 137,92, 115,13, 40,29, 40,16, 31,45, 30,05, 27,60; ИЭРМС m/z 138 ([M-H]-).
Пример 42: Получение 3-(3-бут-3-енил-2-оксопирролидин-1-ил)-N-[3-хлор-1-(3-пиридил)пиразол-4-ил]-N-этилпропанамида (соединение FA67)
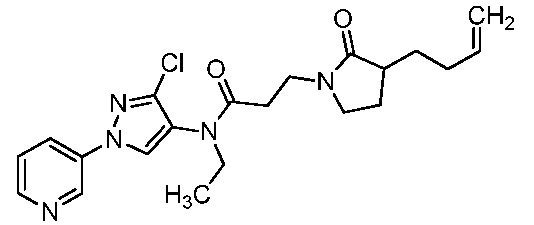
К 3-хлор-N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этилпропанамиду (0,500 г, 1,60 ммоля) в ацетоне (8 мл) добавляли йодид натрия (0,359 г, 2,40 ммоля). Реакционную смесь кипятили с обратным холодильником в течение 24 ч. Продукт реакции фильтровали и концентрировали и получали N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-3-йодпропанамид (0,363 г, 0,898 ммоля), который использовали сразу без дополнительной очистки. К 3-(бут-3-ен-1-ил)пирролидин-2-ону (0,125 г, 0,898 ммоля), растворенному в ДМФ (4,49 мл), добавляли гидрид натрия (60% в минеральном масле, 0,0360 г, 0,898 ммоля). Реакционную смесь перемешивали в течение 45 мин. Затем добавляли N-(3-хлор-1-(пиридин-3-ил)-1H-пиразол-4-ил)-N-этил-3-йодпропанамид (0,363 г, 0,898 ммоля) в виде раствора в ДМФ (2 мл). Реакционную смесь перемешивали при комнатной температуре в течение ночи. Продукт реакции выливали в воду, экстрагировали диэтиловым эфиром и промывали рассолом. Органические вещества сушили и концентрировали и получали масло, которое очищали с помощью колоночной флэш-хроматографии с использованием 0-60% ацетон/гексаны в качестве элюента и получали искомое соединение в виде прозрачного бесцветного масла. (0,257 г, 69%).
В таблице 3, таблице 4 и таблице 5 приведены неограничивающие примеры соединений формулы I.
Соединения F1, F5, F9, F12, F28, F44, F46, F56, F65, F65, F75, F94, F97, F99, F101, F112, F113, P16, P21, P24, FA5, FA6, FA7, FA8, FA9, FA10, FA11, FA12, FA14, FA15, FA16, FA17, FA41, FA42, FA43, FA44, FA45 и FA66 получали в соответствии с примером 7.
Соединения F2, F19 и F83 получали в соответствии с примером 5.
Соединения F3, F4, F6, F7, F8, F10, F18, F21, F22, F23, F26, F27, F29, F33, F37, F39, F47, F48, F49, F52, F61, F69, F76, F77, F82, F88, F90, F95, F98, F100, F106, F107, F110, F111, F122, F123, F124, P20, P23, FA3, FA13, FA18, FA32, FA33, FA34, FA69, FA70, FA71 и FA76 получали в соответствии с примером 1.
Соединение F11 получали в соответствии с примером 30.
Соединения F13, F15, F30, F43, F54, F55, F67, F68, F70, F73, F78, F80, F85, F108, F115, F118 и FA77 получали в соответствии с примером 4.
Соединения F14, F32, F53, F74, F81, F84, F87, F91, F103, F104, F117, F119, F127 и F129 получали в соответствии с примером 14.
Соединения F16 и F93 получали в соответствии с примером 29.
Соединение F17 получали в соответствии с примером 33.
Соединения F20, F36, F51, F59, F72, FA4, FA19, FA20, FA21, FA22, FA23, FA24, FA25, FA26, FA27, FA28, FA29, FA30, FA31, FA35, FA36, FA37, FA38, FA39, FA40, FA49, FA50, FA57, FA58, FA59, FA60 и FA61 получали в соответствии с примером 35.
Соединения F24 и F126 получали в соответствии с примером 17.
Соединения F25, F62 и FA75 получали в соответствии с примером 2.
Соединения F31, F38 и FA68 получали в соответствии с примером 31.
Соединения F34, F35, F89 и F125 получали в соответствии с примером 32.
Соединения F40, F42, F64, F66, F79, F96, F114 и F121 получали в соответствии с примером 26.
Соединение F41 получали в соответствии с примером 20.
Соединение F45 получали в соответствии с примером 21.
Соединения F50, F58 и F71 получали в соответствии с примером 13.
Соединение F52 получали в соответствии с примером 11.
Соединения F57, F63, F102, F120, FA72, FA73 и FA74 получали в соответствии с примером 8.
Соединения F60, F92 и F130 получали в соответствии с примером 23.
Соединение F86 получали в соответствии с примером 19.
Соединения F105, FA1, FA2, FA46, FA47, FA52, FA53, FA54, FA55 и FA56 получали в соответствии с примером 34.
Соединения F109 и F116 получали в соответствии с примером 15.
Соединение F128 получали в соответствии с примером 9.
Соединение F131 получали в соответствии с примером 10.
соединения P1, FA62, FA64 и FA65 получали в соответствии с примером 37.
Соединение FA48 получали в соответствии с примером 38.
Соединение FA51 получали в соответствии с примером 39.
Соединение FA40 получали в соответствии с примером 40.
Соединение FA67 получали в соответствии с примером 42.
Хотя в настоящее изобретение можно внести различные изменения и возможны альтернативные формы, в настоящем изобретении в качестве примера подробно описаны конкретные варианты осуществления. Однако следует понимать, что не предполагается, что настоящее изобретение ограничено конкретными раскрытыми формами. Напротив, настоящее изобретение включает все модификации, эквиваленты и альтернативы, входящие в объем настоящего изобретения, определяемый прилагаемой формулой изобретения и ее допустимыми эквивалентами.
ТАБЛИЦА 3. (см. в конце описания в графической части).
|
|