Результат интеллектуальной деятельности: ПЕПТИД, ОБЛАДАЮЩИЙ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ
Вид РИД
Изобретение
Изобретение относится к области биотехнологии и может быть использовано в медицине. Онкологические заболевания являются одной из основных причин человеческой смертности в современном мире. Классические методы лечения рака - хирургия, химиотерапия, лучевая и гормональная терапия - не приводят к ремиссии в более чем половине случаев. Кроме того, серьезную угрозу для тех, кто успешно прошел курс лечения, представляют рецидивы опухолеобразования. Существенными недостатками химиотерапевтического подхода являются развитие резистентности опухолевых клеток, а также токсичность многих антираковых препаратов для здоровых клеток. Действие традиционных препаратов-цитостатиков направлено на подавление роста быстро делящихся клеток. Однако вследствие того, что высокая скорость деления характерна не только для клеток опухолей, но и для некоторых нормальных клеток, например, клеток эпителиальных тканей и красного костного мозга, цитостатическая терапия сопровождается такими побочными эффектами, как иммуносупрессия, анемия, алопеция, воспаление слизистых оболочек желудочно-кишечного тракта, а также создает риск малигнизации здоровых клеток. В свете вышесказанного актуальной является проблема разработки противоопухолевых препаратов селективного действия, не вызывающих формирования резистентности со стороны клеток-мишеней.
Среди кандидатов на роль противоопухолевых средств нового поколения рассматриваются белки и пептиды системы врожденного иммунитета человека и животных [Zasloff М. Antimicrobial peptides of multicellular organisms // Nature. 2002. Vol. 415, №6870. P. 389-395]. Антимикробные пептиды (АМП) -природные соединения, обладающие широким спектром биологической активности. Для целого ряда АМП в экспериментах in vitro и in vivo показано наличие выраженного противоопухолевого действия за счет способности селективно воздействовать на цитоплазматическую мембрану и мембрану митохондрий раковых клеток, вызывая некротическую или апоптотическую гибель клетки.
Селективность действия катионных АМП определяется рядом физиологических особенностей раковых клеток. В норме внешняя поверхность мембран клеток млекопитающих образована цвиттерионными фосфолипидами - фосфатидилэланоламином, фосфатидилхолином и сфингомиелином, однако для опухолевых клеток характерен иной состав мембран. Цитоплазматическая мембрана трансформированных клеток приобретает выраженный отрицательный заряд из-за высокого содержания фосфатидилсерина, гликопротеинов и гликолипидов, обогащенных сиаловыми кислотами, а также протеогликанов, обогащенных сульфатом гепарина [Hoskin D.W., Ramamoorthy A. Studies on anticancer activities of antimicrobial peptides // Biochim. Biophys. Acta. 2008. Vol. 1778, №2. P. 357-375.]. Потеря асимметрии в распределении липидов была продемонстрирована на примере многих типов опухолевых линий клеток, что позволяет рассматривать данное явление как ключевой маркер онкогенеза. Для многих АМП показана цитотоксическая активность в отношении различных типов опухолевых клеток, однако, при этом лишь некоторые пептиды имеют выраженное избирательное токсическое действие в отношении клеток рака, в то время как другие повреждают как опухолевые, так и нормальные клетки.
Наиболее близкими аналогами заявляемого изобретения являются ранее открытые антимикробные пептиды из гемоцитов мечехвоста, представители семейства бета-шпилечных АМП [Nakamura Т. et al. Tachyplesin, a class of antimicrobial peptide from the hemocytes of the horseshoe crab (Tachypleus tridentatus). Isolation and chemical structure // J. Biol. Chem. 1988. Vol.263, №32. P. 16709-16713], в частности тахиплезин-1 (SEQ ID No. 4). Пептиды этой группы обладают стабилизированной дисульфидными связями β-шпилечной структурой, что обуславливает их высокую устойчивость к гидролизу под действием протеолитических ферментов. Несмотря на выраженную мембранотропную активность, в том числе в отношении нормальных клеток млекопитающих, противоопухолевые свойства тахиплезинов связаны не только с вызываемыми ими процессами апоптоза раковых клеток. Тахиплезин способен выступать в качестве связующего звена между гиалуроновыми кислотами на поверхности клеток карциномы простаты и Clq компонентом системы комплемента. Такое взаимодействие приводит к активации классического каскада системы комплемента [Chen J. Tachyplesin activates the classic complement pathway to kill tumor cells // Cancer Res. 2005. Vol. 65, №11. P. 4614-4622]. Благодаря способности одновременно подавлять неоваскуляризацию при развитии опухоли и вызывать апоптоз раковых клеток, тахиплезин показал высокую эффективность при лечении меланомы у мышей [Hoskin D.W., Ramamoorthy A. Studies on anticancer activities of antimicrobial peptides // Biochim. Biophys. Acta. 2008. Vol. 1778, №2. P. 357-375.]. Способность пептида подавлять пролиферацию опухолевых клеток была показана на примере гепатомы и аденокарциномы человека [Shi S.-L. et al. Effects of tachyplesin and n-sodium butyrate on proliferation and gene expression of human gastric adenocarcinoma cell line BGC-823 // World J. Gastroenterol. WJG. 2006. Vol. 12, №11. P. 1694-1698]. Недостатком природных тахиплезинов как химиотерапевтических агентов является низкая селективность противоопухолевого действия вследствие высокой токсичности в отношении нормальных клеточных линий [Kuzmin D.V. et al. Comparative in vitro study on cytotoxicity of recombinant β-hairpin peptides // Chem Biol Drug Des. 2017. DOI: 10.1111/cbdd.13081]. Так, тахиплезин-1 вызывает лизис 50% эритроцитов (НС50) и гибель 50% астроцитов (IC50) в концентрации менее 100 мкМ (см. Таблицу).
Изобретение решает задачу расширения ассортимента химических веществ, обладающих селективным противоопухолевым действием. Заявляемый пептид имеет аминокислотную последовательность SEQ ID No. 1. Заявляемый пептид состоит из 17 аминокислотных остатков, содержит две дисульфидные связи и не имеет иных посттрансляционных модификаций. Заявляемый пептид проявляет выраженную активность в отношении опухолевых клеточных линий (IC50<30 мкМ). Заявляемый пептид характеризуется низкими показателями гемолитического эффекта (НС50>400 мкМ) и цитотоксичности в отношении нормальных клеток человека, например, астроцитов (IC50>100 мкМ). Техническим результатом изобретения является выраженная противоопухолевая активность заявляемого пептида. Биосинтез заявляемого пептида не требует осуществления ферментативных посттрансляционных модификаций, что делает предпочтительным его биотехнологическое получение в бактериальной системе. Заявляемый пептид может быть получен путем гетерологической экспрессии в клетках Escherichia coli, а также с помощью химического синтеза.
Изобретение иллюстрируют графические материалы:
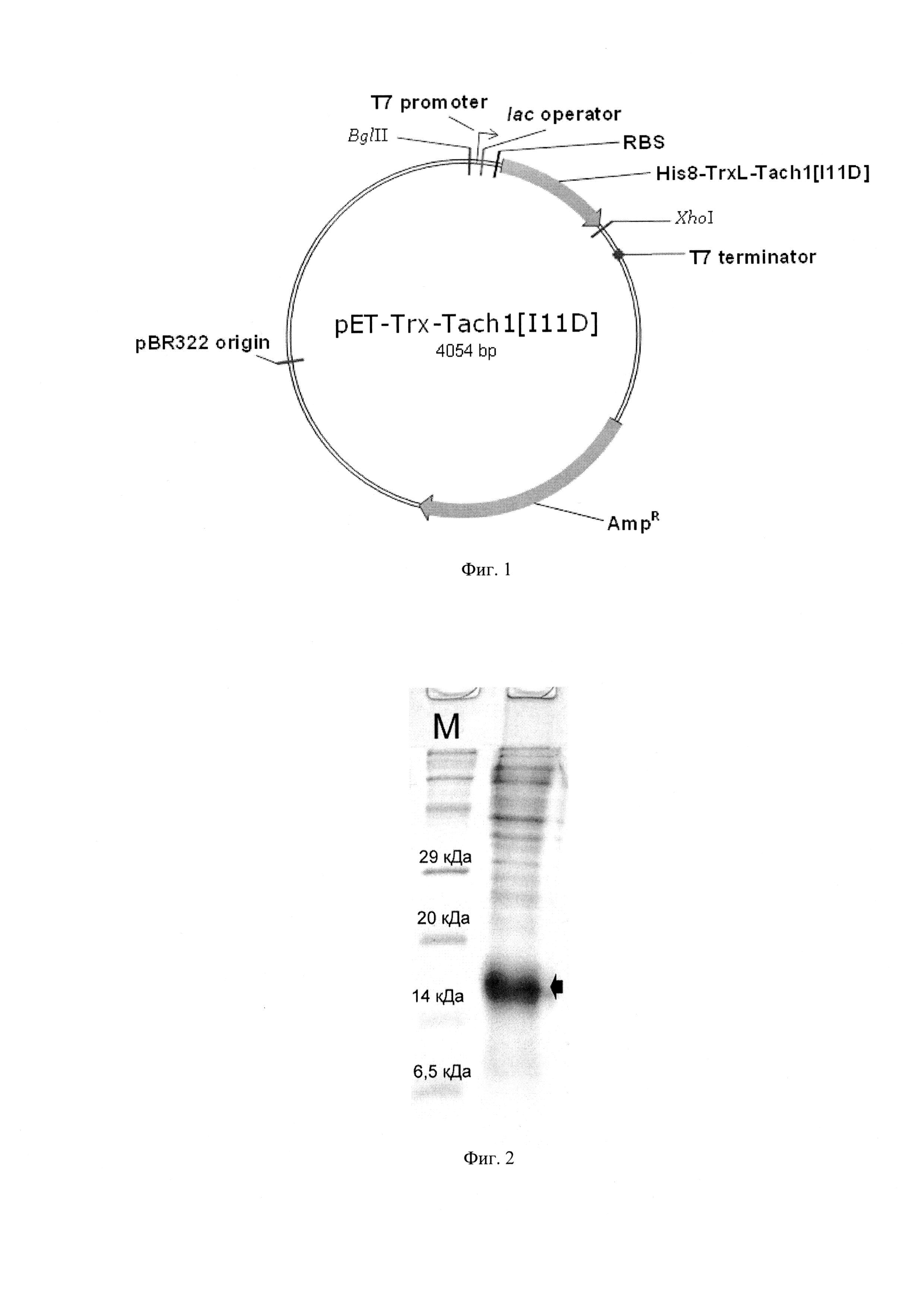
Фиг. 1. Физическая карта плазмидного вектора для экспрессии пептида Tach1[Ile11Asp]: Bg1ll, XhoI - сайты рестрикции с указанием координат; pBR322 origin - участок инициации репликации плазмиды; AmpR - ген устойчивости к β-лактамным антибиотикам; Т7 promoter - промотор транскрипции; Т7 terminator - терминатор транскрипции; 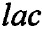 operator - сайт связывания
operator - сайт связывания 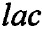 -репрессора; RBS -сайт связывания рибосомы; His8-TrxL-Tach1[Ile11Asp] - последовательность, кодирующая гибридный белок, содержащий целевой пептид.
-репрессора; RBS -сайт связывания рибосомы; His8-TrxL-Tach1[Ile11Asp] - последовательность, кодирующая гибридный белок, содержащий целевой пептид.
Фиг. 2. Электрофоретический анализ продукта экспрессии рекомбинантного гена, кодирующего Tach1[Ile11Asp] Tach1[Ile11Asp]. 1 - стандарт М.м.; 2 - суммарный клеточный лизат, содержащий гибридный белок His8-TrxL-Tach1[Ile11Asp] (молекулярная масса гибридного белка - 15,7 кДа - отмечена стрелкой).
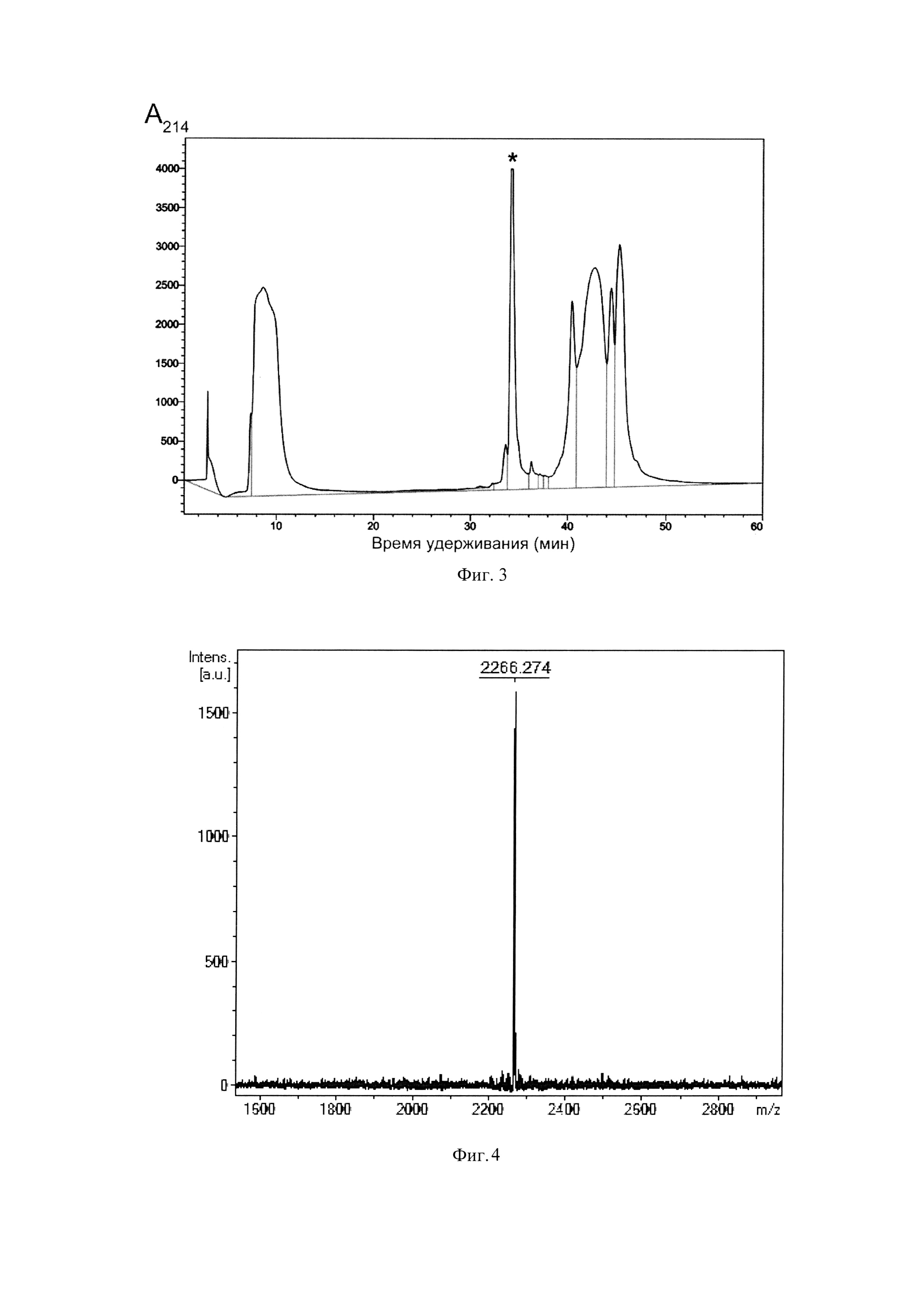
Фиг. 3. Хроматограмма очистки рекомбинантного пептида Tach1[Ile11Asp] (SEQ ID No. 1) методом обращенно-фазовой ВЭЖХ. Пик, соответствующий целевому пептиду, отмечен звездочкой.
Фиг. 4. МАЛДИ масс-спектр пептида Tach1[Ile11Asp] (SEQ ID No. 1), полученного генно-инженерным способом.
Таблица. Цитотоксическое действие рекомбинантных пептидов Tach1 и Tach1 [Hell Asp].
Изобретение иллюстрируют примеры.
Пример 1.
Конструирование плазмидного вектора pET-Trx-Tach1[Ile11Asp]
Нуклеотидную последовательность SEQ ID No. 2, содержащую промотор транскрипции T7 РНК-полимеразы, 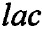 оператор, участок связывания рибосомы и участок, кодирующий гибридный полипептид (последовательно связанные гистидиновый октамер, тиоредоксин с заменой M37L, сайт расщепления бромцианом и Tach1[Ile11Asp]), получают химико-ферментативным синтезом с помощью ПЦР. Олигонуклеотиды, используемые в ПЦР, синтезируют твердофазным фосфорамидитным методом с наращиванием олигонуклеотидной цепи в направлении от 3'-конца к 5'-концу с помощью защищенных фосфорамидитов - 5'-диметокситритил-N-ацил-2'-дезоксинуклеозид-3'-О-(β-цианэтилдиизопропиламино)-фосфитов, активированных тетразолом.
оператор, участок связывания рибосомы и участок, кодирующий гибридный полипептид (последовательно связанные гистидиновый октамер, тиоредоксин с заменой M37L, сайт расщепления бромцианом и Tach1[Ile11Asp]), получают химико-ферментативным синтезом с помощью ПЦР. Олигонуклеотиды, используемые в ПЦР, синтезируют твердофазным фосфорамидитным методом с наращиванием олигонуклеотидной цепи в направлении от 3'-конца к 5'-концу с помощью защищенных фосфорамидитов - 5'-диметокситритил-N-ацил-2'-дезоксинуклеозид-3'-О-(β-цианэтилдиизопропиламино)-фосфитов, активированных тетразолом.
Фрагмент ДНК, кодирующий белок-носитель тиоредоксин (M37L), получают методом ПЦР-амплификации и направленного мутагенеза с помощью ген-специфических праймеров, используя в качестве исходной матрицы плазмиду рЕТ32а(+), содержащую ген тиоредоксина. Фрагмент ДНК, кодирующий пептид Tach1[Ile11Asp], получают путем медленного отжига 3'-концов двух праймеров (прямой праймер: GCA GAT СТС ATA TGA ААТ GGT GCT ТТС GTG TGT GTT АСС GCG GTG AT; обратный праймер: GCG ААТ ТСТ ТАА CGA CAG CGA CGA TAG САА ТСА CCG CGG ТАА САС АС), кодирующих, соответственно, N- и С-концевые области пептида, с последующей достройкой до двухцепочечной структуры с помощью фрагмента Кленова ДНК-полимеразы I Е. coli. В ходе дизайна праймеров используют кодоны, предпочтительные для экспрессии в Е. coli. Остальные, участки последовательности pET-Trx-Tach1[Ile11Asp] получают путем последовательного отжига и элонгации взаимно перекрывающихся олигонуклеотидов, а также отжига, элонгации и амплификации промежуточных продуктов синтеза. На завершающей стадии синтеза последовательность амплифицируют с помощью праймеров, несущих на 5'-концах сайты узнавания рестриктаз Bg1II и XhoI. Продукт амплификации гидролизуют указанными рестриктазами, очищают электрофорезом в 1% агарозном геле, полосу ДНК величиной -550 п.н. выделяют из геля с помощью колонки с силикагелем и лигируют с фрагментом ДНК размером 3,5 тыс.п.н., полученным в результате обработки плазмиды рЕТ-20b(+) рестриктазами Bg1II и XhoI. В результате лигазной реакции получают кольцевую ковалентно замкнутую ДНК размером 4054 п.н. (Фиг. 1). Продуктами лигазной реакции трансформируют компетентные клетки Е. coli DH10B, приготовленные с помощью 0,1 М хлорида кальция. После трансформации суспензию бактерий смешивают с питательной средой LB, растят 1 ч при 37°С и высевают на чашки Петри с LB-агаром, содержащим 100 мкг/мл ампициллина.
Первичный отбор клонов, содержащих нужную плазмиду, осуществляют методом «ПЦР с клонов» с использованием праймеров на плазмидный остов и вставку. Отобранные клоны подращивают в жидкой питательной среде и выделяют плазмидную ДНК, которую анализируют на наличие вставки с помощью рестрикционного анализа. Окончательное строение плазмид, содержащих требуемый фрагмент, подтверждают определением нуклеотидной последовательности с помощью секвенирования по Сэнгеру. По данным секвенирования отбирают плазмиду со вставкой, нуклеотидная последовательность которой полностью соответствует запланированной (SEQ ID No. 2).
Пример 2.
Получение рекомбинантного пептида
Проводят трансформацию компетентных клеток Е. coli BL21(DE3), приготовленных с помощью 0,1 М хлорида кальция, плазмидным вектором, сборка которого описана в примере 1. После трансформации суспензию бактерий смешивают с питательной средой LB, растят 1 ч при 37°С и высевают на чашки Петри с LB-агаром, содержащим 100 мкг/мл ампициллина и 0,02 М глюкозы. Чашки инкубируют при 37°С в течение 18 ч.
Бактериологической петлей переносят выросшие колонии в 10 мл жидкой среды LB, содержащей 100 мкг/мл ампициллина, растят в течение 18 ч на термостатируемой качалке со скоростью вращения 220 об⋅мин-1 при температуре 37°С. Полученную культуру засевают в жидкую питательную среду LB, содержащую 0,02 М глюкозы, 100 мкг/мл ампициллина, 1 мМ MgSO4, при этом начальная OD600 составляет 0,05. Индукцию биосинтеза гибридного белка осуществляют путем добавления изопропилтио-β-D-галактопиранозида (IPTG) к культуре клеток с оптической плотностью 1,0 до конечной концентрации 0,2 мМ. Культуру растят в течение 6 ч при температуре 32°С на термостатируемой качалке со скоростью вращения 220 об⋅мин-1. Контроль уровня экспрессии гибридного белка осуществляют методом денатурирующего SDS-электрофореза в полиакриламидном геле. Уровень экспрессии гибридного белка His8-TrxL-Tach1[Ile11Asp] при постановке эксперимента по приведенной методике составляет не менее 30%. Расчетная молекулярная масса гибридного белка (SEQ ID No. 3) составляет 15,7 кДа (Фиг. 2).
После экспрессии клетки осаждают центрифугированием, ресуспендируют в фосфатном буфере (рН 7.8) с добавлением 6М гуанидин гидрохлорида и 20 мМ имидазола при помощи стеклянного гомогенизатора Поттера и разрушают путем ультразвуковой обработки. Лизат клеток центрифугируют при 25000 g в течение 40 мин. Все работы по получению осветленного лизата проводят при температуре 4°С. Очистку гибридного белка, содержащего в качестве аффинной метки октагистидиновую последовательность, осуществляют с помощью металлохелатной хроматографии на препаративной колонке с Ni-NTA агарозой в денатурирующих условиях. Элюцию проводят повышением концентрации имидазола в буфере до 0,5 М. Собранную после очистки с помощью металлохелатной хроматографии фракцию, содержащую гибридный белок, титруют концентрированной соляной кислотой до значения рН 1,0, после чего добавляют равную массу бромциана (1 г бромциана на 1 г белка) и выдерживают при температуре 25°С в защищенном от света месте в течение 18 ч. Реакцию останавливают добавлением пятикратного объема деионизированной воды, после чего упаривают образцы на вакуумной центрифуге до исходного объема раствора и титруют до нейтральных значений рН. Финальную стадию очистки пептида проводят методом обращенно-фазовой ВЭЖХ (ОФ-ВЭЖХ) на колонке Reprosil-Pur C18-AQ в системе водных буферов, содержащих ацетонитрил и 0,1% ТФУ. Разделение происходит в линейном градиенте ацетонитрила от 5% до 80% за 60 мин. Выход полипептидов детектируют по изменению оптического поглощения при длине волны 214 нм (Фиг. 3). Концентрацию водного раствора очищенного пептида Tach1[Ile11Asp] определяют методом спектрофотометрии по поглощению при 280 нм и расчета на основе коэффициентов экстинкции.
Пример 3.
Определение молекулярной массы пептида
Соответствие относительной молекулярной массы полученного рекомбинантного пептида расчетному значению, а также его химическую чистоту оценивают с помощью масс-спектрометрического анализа на приборе Reflex III (Bruker Daltonics), оснащенном УФ-лазером с длиной волны 336 нм, с регистрацией положительных ионов в рефлекторном режиме. В качестве матрицы используют 2,5-дигидроксибензойную кислоту в смеси, содержащей 20% ацетонитрил и 0,1% трифторуксусную кислоту. Пик с m/z 2266,3 (Фиг. 4) соответствует молекулярному иону пептида Tach1[Ile11Asp] (SEQ ID No. 1) (расчетная средняя молекулярная масса 2266,7), что свидетельствует об образовании двух дисульфидных связей. По аналогичной схеме анализируют пептид Tach1.
Пример 4.
Тестирование гемолитической активности пептида
Для тестирования гемолитической активности пептида используют свежевыделенные человеческие эритроциты. Для предотвращения свертывания к цельной крови добавляют цитратный буфер. Кровь центрифугируют в растворе фиколла и урографина плотностью 1,077 г/мл в течение 15 мин при 1500 об⋅мин-1. Фракцию эритроцитов отбирают со дна и трижды промывают двадцатью объемами изотонического натрий-фосфатного буфера (рН 7,4), последовательно осаждая эритроциты путем центрифугирования при 2000 об⋅мин-1 в течение 10 мин. После отмывки готовят 8% суспензию эритроцитов в изотоническом натрий-фосфатном буфере.
Для теста в 96-луночном планшете готовят серии двойных разведений исследуемого пептида от 400 до 6,25 мкМ (в пересчете на конечную концентрацию) объемом 50 мкл. После этого к раствору пептида добавляют по 50 мкл 8% суспензии эритроцитов. Планшет инкубируют в течение 1,5 ч при 37°С и перемешивании 1000 об⋅мин-1. После инкубации планшеты центрифугируют в течение 15 мин при 3000 об⋅мин-1 для осаждения интактных эритроцитов. Далее аликвоты супернатанта переносят в другой планшет для измерения количества свободного гемоглобина. Определение количества гемоглобина в растворе осуществляют по поглощению раствора при 405 нм. В качестве отрицательного контроля (K-) используют супернатант, полученный после центрифугирования эритроцитов, инкубировавшихся в растворе натрий-фосфатного буфера без добавления пептидов. В качестве положительного контроля (K+) используют супернатант, полученный после центрифугирования эритроцитов, инкубировавшихся в 0,1% водном растворе неионогенного детергента Triton X-100, вызывающего их полный лизис. Эксперименты проводят дважды с кровью одного и того же человека в трехкратной повторности. Процент гемолиза рассчитывают по формуле:
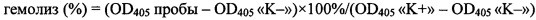
Полученные данные о гемолитической активности представлены в Таблице. В отличие от пептида дикого типа Tach1 (SEQ ID No. 4), пептид Tach1[Ile11Asp] (SEQ ID No. 1) не обладает выраженной гемолитической активностью при концентрациях до 400 мкМ, используемых при тестировании.
Пример 5.
Тестирование цитотоксического действия пептида
Тестирование цитотоксического действия пептида в отношении астроцитов и опухолевых клеточных линий проводят с помощью МТТ-теста. Методика основана на способности дегидрогеназ живых клеток восстанавливать 3-(4,5-диметилтиазол-2-ил)-2,5-дифенил-2Н-тетразолий бромид (МТТ-реагент) до нерастворимого в воде фиолетового кристаллического формазана. Клеточные линии (нормальные астроциты человека (NHA), эпидермоидная карцинома кожи человека (А431), трансформированные клетки эмбриональной почки человека (НЕК293Т)) высаживают в 96-луночные планшеты (по 10000 клеток в каждую лунку) и растят в среде DMEM/F-12 в течение 24 ч при 37°С в СО2-инкубаторе (5% СО2 в воздухе). Далее культуральную жидкость заменяют свежей средой, в которой предварительно растворяют тестируемый пептид. После инкубации в течение 48 ч в приведенных выше условиях в каждую лунку добавляют по 20 мкл раствора МТТ в забуференном физиологическом растворе (5 г/л), после чего продолжают инкубацию в течение 4 ч. Аккуратно удаляют среду, добавляют в лунки по 100 мкл смеси диметилсульфоксида и этилового спирта (1:1) для растворения кристаллов формазана и измеряют оптическую плотность растворов при 570 нм с помощью планшетного спектрофотометра. Долю живых клеток определяют по формуле:
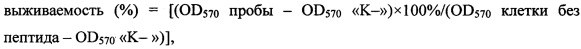 ,
,
где «K-» - фоновое поглощение лунки с растворителем. Эксперименты проводят дважды в трехкратной повторности. С помощью математической модели нелинейной регрессии строят графики сглаживающих кривых для экспериментальных значений выживаемости клеток. С использованием уравнений полученных кривых и программного обеспечения GraphPad PRISM 6.0 рассчитывают значения IC50. Полученные данные о цитотоксической активности представлены в Таблице. Пептид Tach1[Ile11Asp] (SEQ ID No. 1) обладает выраженной селективностью в отношении опухолевых клеточных линий по сравнению с пептидом Tach1 (SEQ ID No. 4).
Перечень аминокислотных и нуклеотидных последовательностей
SEQ ID No. 1
SEQ ID No. 2

SEQ ID No. 3


SEQ ID No. 4
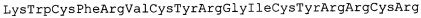
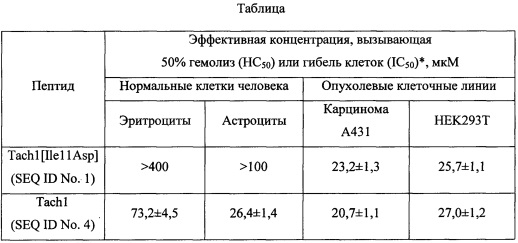
* - данные НС50 и IC50 приведены как средние значения с учетом стандартного отклонения
Пептид, обладающий противоопухолевой активностью, имеющий аминокислотную последовательность SEQ ID No. 1.