Результат интеллектуальной деятельности: Средство, обладающее ингибирующей активностью в отношении ингибитора активатора плазминогена 1-го типа
Вид РИД
Изобретение
Изобретения относятся к области фармации и медицины, а именно к новым лекарственным средствам, обладающим способностью снижать активность ингибитора активатора плазминогена 1-го типа (PAI-1), а также его композициям, способам их применения и получения. Это соединение и его композиции являются ингибиторами PAI-1 и могут использоваться при лечении PAI-1 ассоциированных заболеваний, включая, например, болезнь Альцгеймера.
Ингибитор активатора плазминогена 1-го типа (PAI-1), относится к группе ингибиторов сериновых протеаз (SERPIN). Ингибирование активности PAI-1 приводит к увеличению активности тканевого (tPA) и урокиназного (uPA) активаторов плазминогена. В результате увеличения активности tPA и uPA ускоряется переход профермента плазминогена в активную форму – плазмин. Одной из главных функций плазмина в головном мозге, в отличие от периферических тканей, является катаболизм амилоидов типа Aβ40 и Aβ42. Установлено, что концентрация плазмина прямо пропорциональна скорости деградации Aβ40 и Aβ42 в отделах головного мозга (например, в гиппокампе, гипоталамусе, мозжечке). Болезнь Альцгеймера представляет собой наиболее простую форму амилоидоза, являющегося причиной снижения когнитивных способностей и старческой деменции. Для данного заболевания характерно образование в головном мозге больных внеклеточных сенильных бляшек, состоящих преимущественно из β-амилоидных пептидов (в основном, Aβ40 и Aβ42), которые локализуются главным образом в тканях и сосудах головного мозга. Aβ40 и Aβ42 образуются путем ферментативного нарезания крупной белковой молекулы предшественника амилоида (APP). Избыточная продукция или замедленная деградация Aβ40 и Aβ42 приводит к увеличению их накоплений как внутри, так и вне нейронов в виде неправильно упакованных отложений, имеющих характерную β-структуру амилоида и обуславливающих нарушение нормальной функции нейронов и развитие симптомов болезни Альцгеймера. Катаболизм Aβ40 и Aβ42 регулируется несколькими протеазами, в том числе плазмином. Считается, что именно плазмин играет критическую роль в деградации Aβ40 и Aβ42 (Melchor J.P., Pawlak R., Chen Z., Strickland S. The possible role of tissue-type plasminogen activator (tPA) and tPA blockers in the pathogenesis and treatment of Alzheimer's disease // Journal of Molecular Neuroscience. 2003. Vol.20. P. 287-289). Увеличение содержания активного плазмина ускоряет распад Aβ40 и Aβ42 и уменьшает их количество в тканях мозга. Таким образом, фармакологически индуцированное торможение активности PAI-1 в структурах головного мозга приводит к ускорению распада Aβ40 и Aβ42 за счет увеличения количества активного плазмина и торможению патогенетического развития болезни Альгеймера.
Известен ингибитор активатора плазминогена 1-го типа (PAI-1), ZK4044. В исследованиях на животных показано, что торможение активности PAI-1 предотвращает артериальный и венозный тромбоз, вследствие чего, это соединение предназначено для лечения тромбозов. Соединение находится на стадии клинических испытаний (найдено в Интернете 15.11.2016 http://www.thrombosisresearch.com/article/S0049-3848(04)00532-8/abstract).
Ингибирующие свойства в отношении ингибитора активатора плазминогена 1-го типа обнаружены еще у двух соединений: T 1776Na (найдено в Интернете 15.11.2016 https://www.axonmedchem.com/product/1769) и Tiplaxtinin - PAI-039 (найдено в Интернете 15.11.2016 https://www.axonmedchem.com/product/1383). Эти соединения только синтезированы и для них проведены лишь первичные исследования.
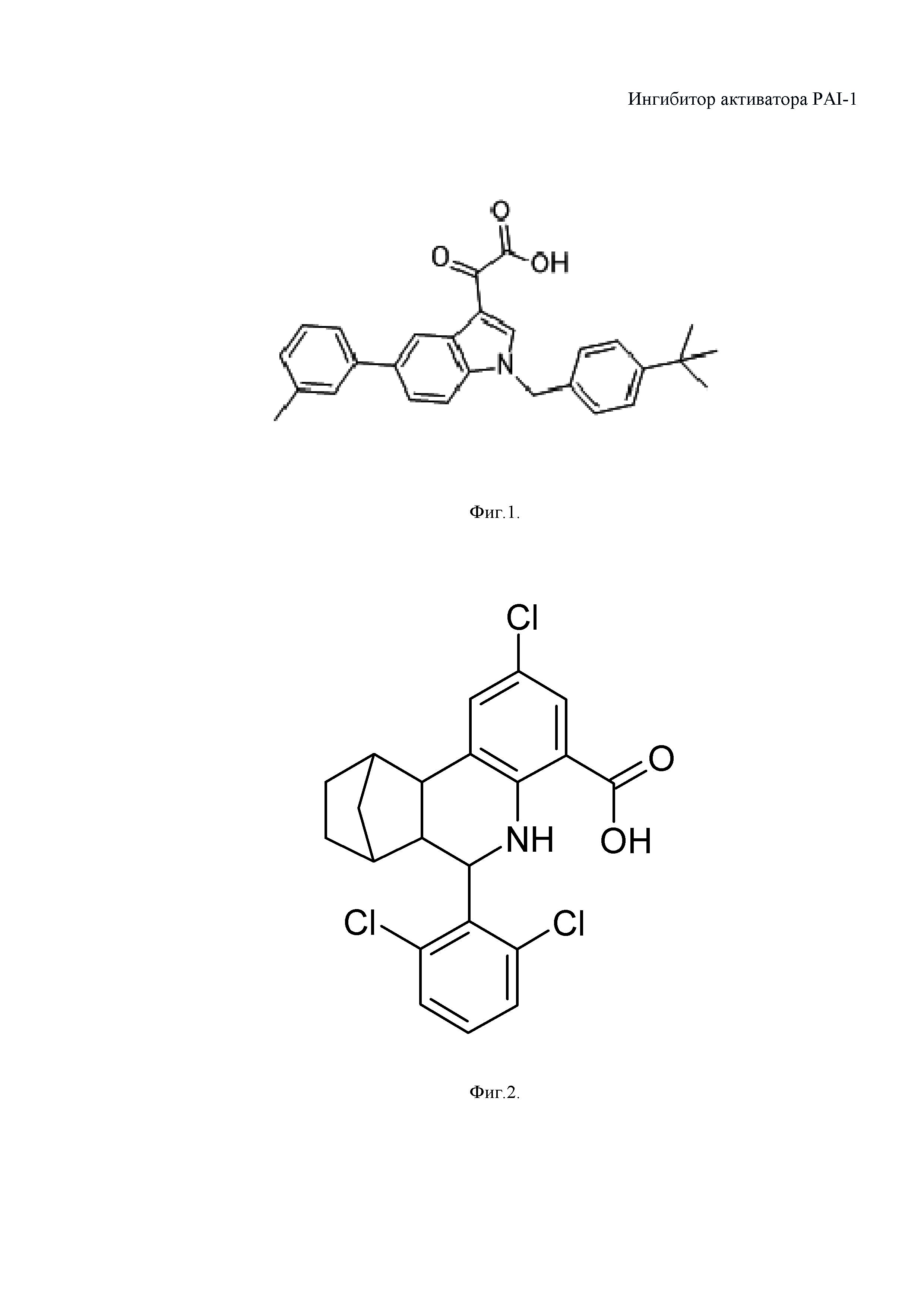
В этой серии соединений алеплазинин (PAZ-417), разработанный компанией Wyeth (дочерняя компания Pfizer), является перспективным лекарственным кандидатом. Алеплазинин показал достоверную и устойчивую эффективность на модели болезни Альцгеймера у лабораторных животных при проведении доклинических испытаний и в ходе фазы I клинических исследований (найдено в Интернете 15.11.2016 г. http://www.medkoo.com/products/8147). Структурная формула алеплазинина (PAZ-417) приведена на Фиг. 1.
Поиск новых улучшенных ингибиторов PAI-1 является одним из основных направлений в фармакологии для разработки новых, более эффективных лекарственных препаратов, предназначенных для лечения болезни Альцгеймера и заболеваний сердечно-сосудистой системы, сопровождающихся повышенным тромбообразованием. Соединения и способы, описанные в заявленной группе изобретений, направлены на удовлетворение этих потребностей.
|
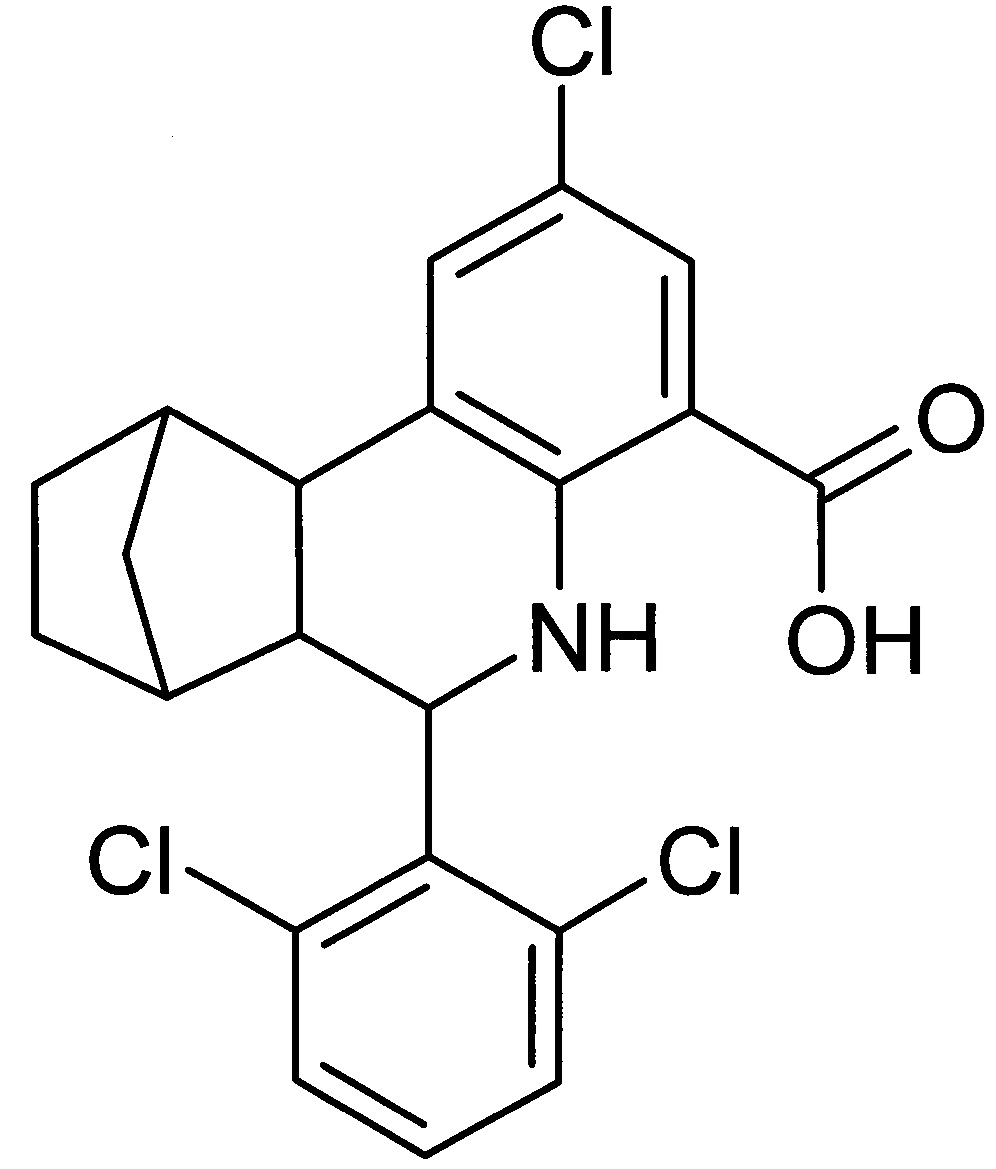
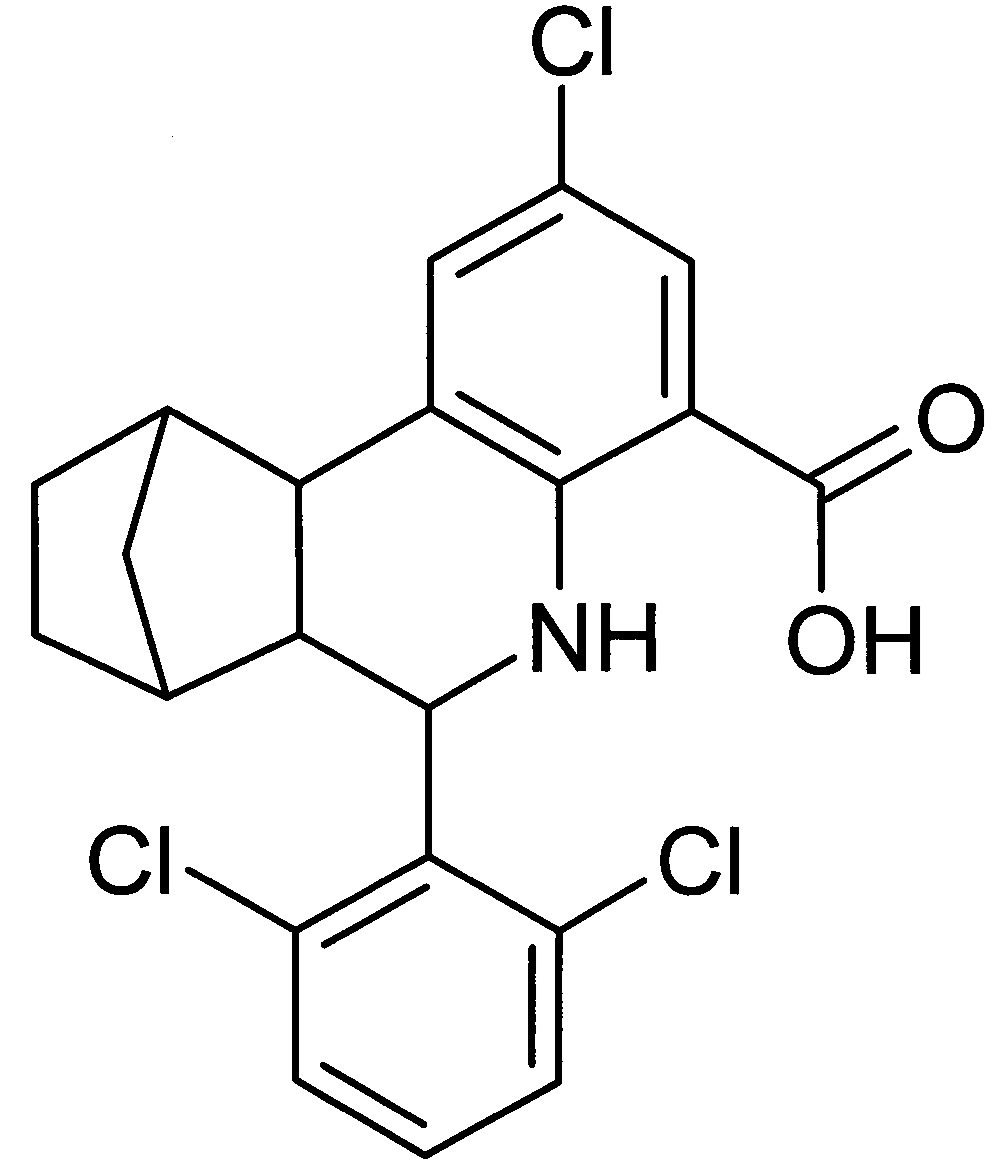
Поставленная задача решается за счет использования соединения 6-(2,6-дихлорфенил)-2-хлор-5,6,6a,7,8,9,10,10a-октагидро-7,10-метанофенантридин-4-карбоновой кислоты, проявляющего ингибирующую активность в отношении ингибитора активатора плазминогена 1-го типа
PAI-1), структурная формула которого (формула 1) представлена на фиг. 2.
Соединения по настоящему изобретению могут также включать все изотопы атомов, присутствующих в промежуточных или конечных соединениях.
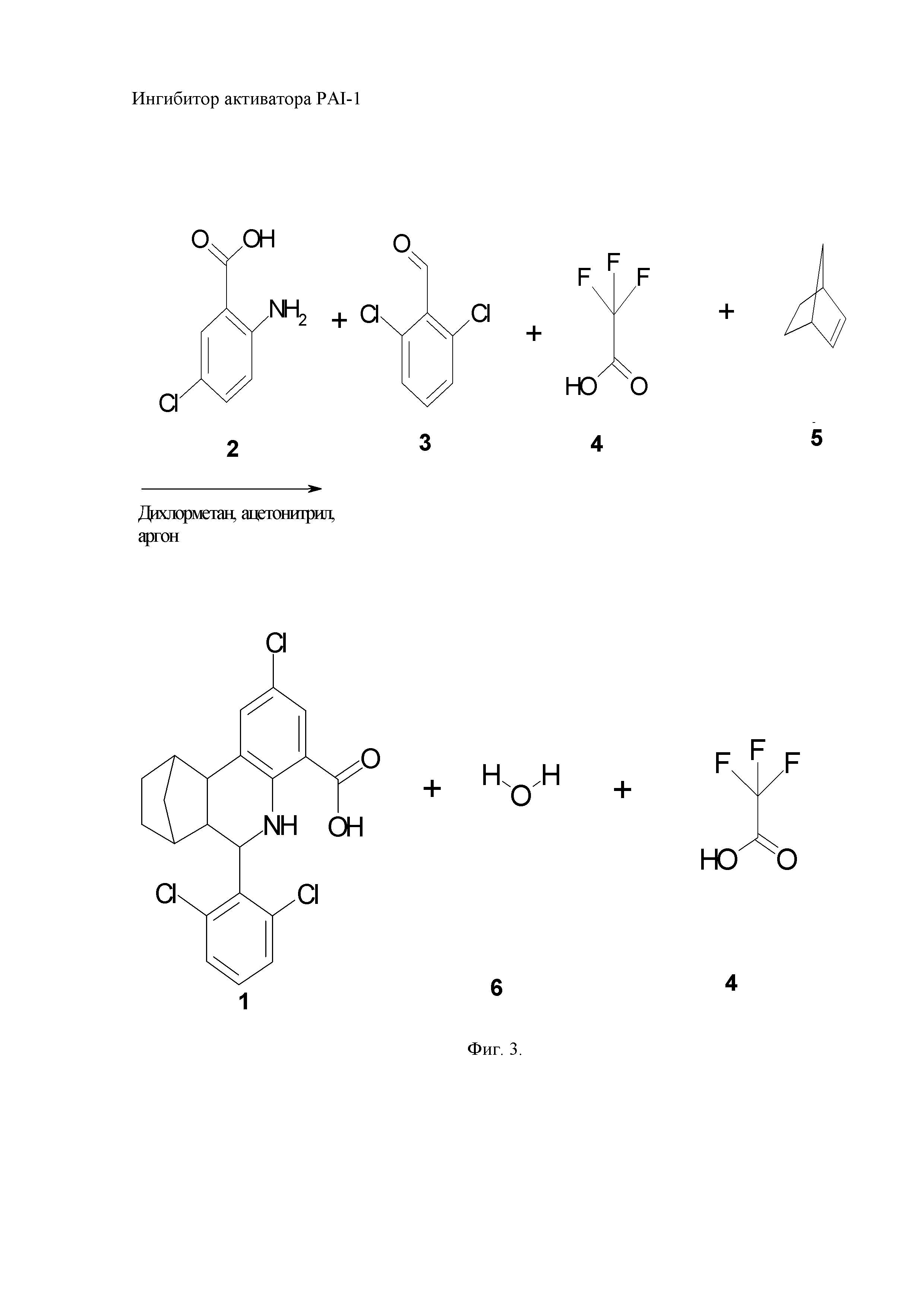
Поставленная задача решается также новым способом получения заявленного соединения, включающим взаимодействие в аргоне 2-амино-5-хлорбензойной кислоты с 2,6-дихлорбензальдегидом в смеси дихлорметан : ацетонитрил (1:1) с перемешиванием около 20-30 мин при комнатной температуре до полного растворения ингредиентов, с последующим добавлением к смеси по каплям трифторуксусной кислоты в количестве 1/100 общего объема смеси. После добавления трифторуксусной кислоты смесь перемешивают около 30-40 мин и добавляют норборнен, для получения целевого продукта (формулы (1), полученную смесь перемешивают для образования целевого продукта, который выпадает в осадок в виде порошка желтого цвета около 16-30 часов.
Для повышения чистоты целевого продукта формулы (1) выпавший желтый осадок отфильтровывают, промывают хлороформом, затем к осадку добавляют новую порцию хлороформ и кипятят при перемешивании, после чего смесь фильтруют горячей.
Именно заявленные параметры способа позволяют получить новое соединение формулы (1).
Схема способа получения целевого продукта - 6-(2,6-дихлорфенил)-2-хлор-5,6,6а,7,8,9,10,10а-октагидро-7,10-метанофенантридин-4-карбоновой кислоты (формула (1), приведена на фиг. 3.
Пример 1.
В токе аргона (100 мл\мин) в колбу помешают 2-амино-5-хлорбензойную кислоту (2) (20.0 г, 116 ммоль), 2,6-дихлорбензальдегид (3) (23.5 г, 134 ммоль), 300 мл смеси хлористый метилен : ацетонитрил (1:1) и перемешивают смесь при температуре 22°С в течение 2 0 мин, затем к смеси по каплям добавляют трифторуксусную кислоту (4) (3,4 г, 117 ммоль), полученную смесь перемешивают при комнатной температуре 30 мин, добавляют норборнен (5) (20 г, 210 ммоль) и оставляют перемешиваться при комнатной температуре на 30 ч для образования целевого продукта формулы (1), который выпадает в осадок в виде порошка желтого цвета.
Для повышения чистоты целевого продукта формулы (1) выпавший желтый осадок отфильтровывают, промывают хлороформом (3×100 мл), затем осадок переносят в колбу и кипятят при перемешивании в хлороформе 350 мл и фильтруют горячим. Получают целевой продукт формулы (1) в виде порошка светло-желтого цвета. Выход 49 г (84%).
Пример 2.
В токе аргона (100 мл\мин) в колбу помешают 2-амино-5-хлорбензойную кислоту (2) (20.0 г, 116 ммоль), 2,6-дихлорбензальдегид (3) (23.5 г, 134 ммоль), 300 мл смеси хлористый метилен : ацетонитрил (1:1) и перемешивают смесь при температуре 23°С в течение 30 мин, затем к смеси по каплям добавляют трифторуксусную кислоту (4) (3,4 г, 117 ммоль), полученную смесь перемешивают при комнатной температуре 40 мин, добавляют норборнен (5) (20 г, 210 ммоль) и оставляют перемешиваться при комнатной температуре на 16 ч для образования целевого продукта формулы (1), который выпадает в осадок в виде порошка желтого цвета.
Для повышения чистоты целевого продукта формулы (1) выпавший желтый осадок отфильтровывают, промывают хлороформом (3х100 мл), затем осадок переносят в колбу и кипятят при перемешивании в хлороформе 350 мл и фильтруют горячим. Получают целевой продукт формулы (1) в виде порошка светло-желтого цвета. Выход – 92,7%.
Вещество, полученное по примерам 1 и 2, представляет собой порошок желтого цвета, эмпирическая формула – С21Н18Cl3NO2, молекулярная масса 422,74.
Для подтверждения истинности формулы целевого продукта определяют его растворимость и снимают УФ спектры.
Определение термодинамической растворимости соединения формулы (1).
Пример 3.
Смешивают 5 мг исследуемого соединения формулы (1) c 1 мл универсального буфера (pION) с pH 2.0 в течение 15 мин при 25˚C. Дополнительные количества веществ добавляют до тех пор, пока раствор не становился мутным. Виалы с раствором инкубируют при перемешивании в течение 24 ч при 25˚C для достижения равновесия между раствором и осадком при насыщении. После уравновешивания 200 мкл раствора (в 2-х повторах) фильтруют через 96-луночный фильтровальный планшет (Millipore) для отделения осадка. Концентрацию соединений в фильтрате определяют спектрофотометрически с помощью стандартной калибровочной кривой. Проводят измерение спектра оптического поглощения вещества и построение калибровочной кривой при выбранной длине волны (обычно, соответствующей максимуму поглощения вещества, λmax), определяют концентрацию вещества и вычисляют растворимость.
Пример 4.
Смешивают 5 мг исследуемого соединения формулы (1) c 1 мл универсального буфера (pION) с pH 7.0 в течение 15 мин при 25˚C. Дополнительные количества веществ добавляют до тех пор, пока раствор не становился мутным. Виалы с раствором инкубируют при перемешивании в течение 24 ч при 25˚C для достижения равновесия между раствором и осадком при насыщении. После уравновешивания 200 мкл раствора (в 2-х повторах) фильтруют через 96-луночный фильтровальный планшет (Millipore) для отделения осадка. Концентрацию соединений в фильтрате определяют спектрофотометрически с помощью стандартной калибровочной кривой. Проводят измерение спектра оптического поглощения вещества и построение калибровочной кривой при выбранной длине волны (обычно, соответствующей максимуму поглощения вещества λmax), определяют концентрацию вещества и вычисляют растворимость.
На основании полученных данных по примерам 3,4 установлено, что соединение хорошо растворимо в диметилсульфоксиде и тетрагидрофуране, мало растворимо или практически нерастворимо в метаноле, практически нерастворимо в воде.
Подлинность соединения формулы (1) определяли методом УФ-спектрофотометрии и методом ядерного магнитного резонанса на ядрах 1Н.
Пример 5.
Подлинность соединения формулы (1) проводят методом УФ-спектрофотометрии в соответствии с требованиями Государственной фармакопеи (ГФ) XII, ч. 1, с. 56. Около 0,01 г субстанции соединения формулы (1) помещают в мерную колбу вместимостью 100 мл, растворяют в метаноле, доводят объем раствора тем же растворителем до метки и перемешивают. 1,0 мл полученного раствора помещают в мерную колбу вместимостью 10 мл, доводят до метки метанолом и перемешивают. В качестве раствора сравнения используют метанол. УФ-спектр поглощения 0,001% раствора субстанции соединения формулы (1) в области от 200 до 450 нм должен иметь максимумы при 204 ± 3 нм, 225 ± 3 нм и 264 ± 3 нм; минимум – при 214 ± 3 нм, 247 ± 3 и 302 ± 3.
Пример 6.
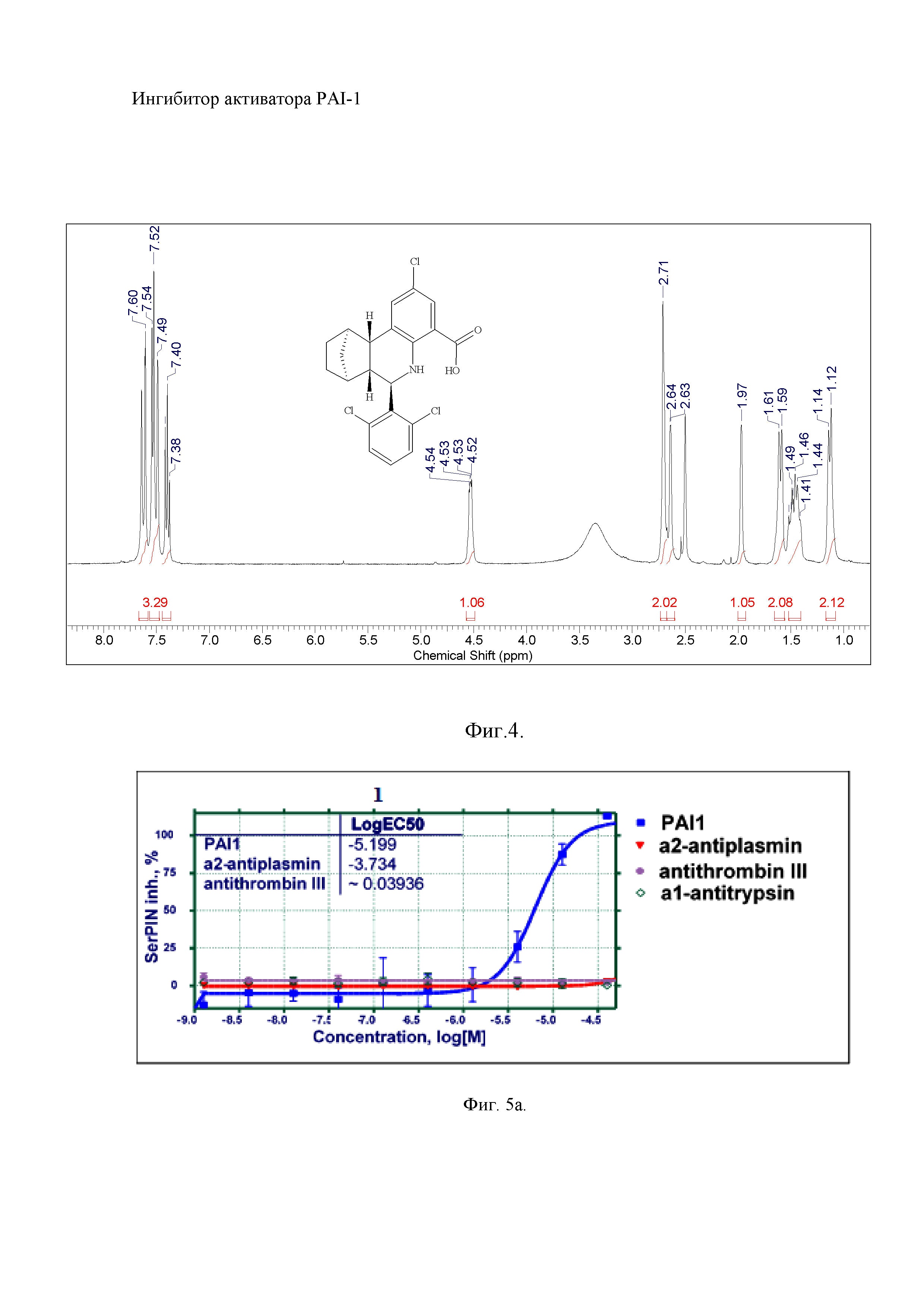
Процедуру снятия спектров ЯМР проводили по следующим параметрам: 1Н ЯМР (400 МГц, ДМСО-d6): 1.13 (д, J=9.76 Гц, 2 H) 1.47 (м, 2 H) 1.60 (д, J=11.07 Гц, 2 H) 1.97 (с, 1 H) 2.64 (д, J=2.19 Гц, 1 H) 2.71 (с, 2 H) 4.53 (дд, J=6.03, 3.51 Гц, 1 H) 7.40 (т, J=8.06 Гц 1 H), 7.51 (м, 3 H), 7.60 (с, 2 H).
где с – синглет, д – дублет, т – триплет.
Приведенный на фиг. 4 1H-NMR спектр целевого продукта формулы (1) -(6R,6aR,7S,10R,10aS)-2-хлоро-6-(2,6-дихлорфенил)-5,6,6a,7,8,9,10,10a-октагидро-7,10-метанофенантридин-4-карбоновой кислоты подтверждает представленную структуру соединения формулы (1).
Новое соединение формулы (1) проявляет ингибирующую активность в отношении ингибитора активатора плазминогена 1-го типа.
Пример 7. Определение ингибирующей активности соединения формулы (1).
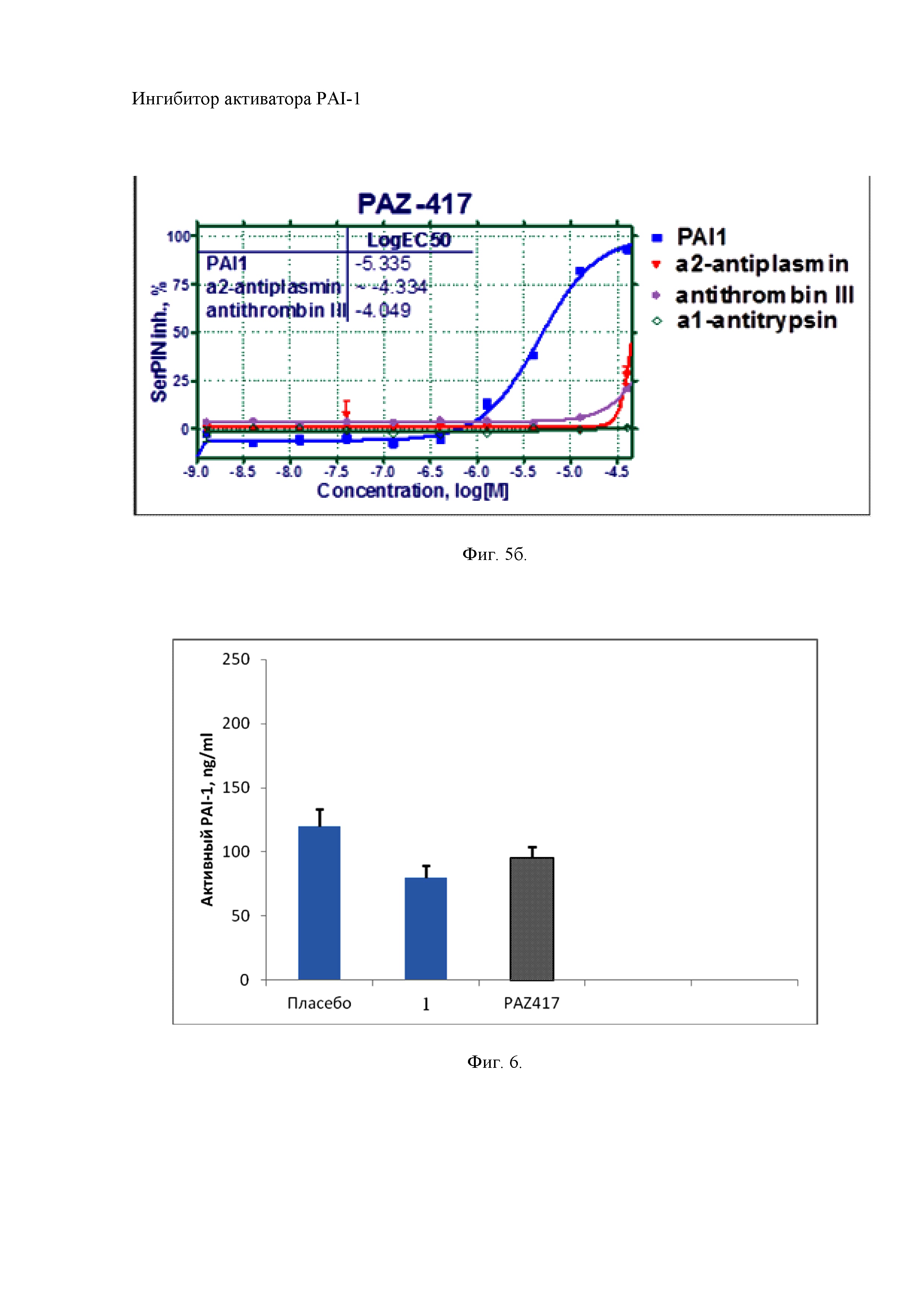
Белых мышей линии С57/В6 рандомизировали на три группы по 10 животных в каждой, после чего всем животным вводили внутрибрюшинно при помощи инъекции липополисахарид в дозе 2 мг/кг. Спустя 1 ч после введения липополсахрида двум группам опытных животных вводили в желудок через металлический зонд, соответственно, соединение формулы 1 и препарат сравнения алеплазинин (PAZ-417) в дозе 30 мг/кг в объеме 1 мл. Животным группы «плацебо» вводили физиологический раствор в объеме 1 мл. Оценку активности PAI-1 в крови лабораторных животных проводили через 3 ч после введения препаратов. Результаты эксперимента представлены в табл. 1, в которой приведена активность соединения формулы (1) и аналога алеплазинина in vitro в сравнении с тремя ферментами группы SERPIN: α2 antiplazmin (альфа2-антиплазмин), antithbromin III (антитромбин III) и α1-antitrypsin (альфа1-антитрипсин) и на фиг. 5, где а) ингибирующая активность соединения формулы (1); б) ингибирующая активность алеплазинина (PAZ-417). Ингибирующая активность соединений определялась в результате параллельного исследования в идентичных условиях.
Как видно из полученных результатов, новое соединение формулы (1) по сравнению с алеплазинином имеет достоверно большую активность в отношении ингибирования фермента PAI-1 в условиях in vitro. Одновременно, ингибирующая активность соединения формулы (1) в отношении других трех ферментов группы SERPIN достоверно ниже, чем таковая алеплазинина.
Пример 8. Определение ингибирующей активности соединения формулы (1) по отношению к PAI-1 в крови лабораторных животных мышей линии С57/В6 на фоне липополисахарид-индуцированного нейровоспаления при введении веществ в одинаковых дозах.
Белых мышей линии С57/В6 рандомизировали на три группы по 10 животных в каждой, после чего всем животным вводили внутрибрюшинно при помощи инъекции липополисахарид в дозе 2 мг/кг. Спустя 1 ч после введения липополисахрида двум группам подопытных животных вводили в желудок через зонд, соответственно, соединение формулы (1) и препарат сравнения алеплазинин (PAZ-417) в дозе 30 мг/кг в объее 1 мл. Животным группы «плацебо» вводили физиологический раствор в объеме 1 мл. Оценку активности PAI-1 в крови лабораторных животных проводили через 3 ч после введения препаратов. Результаты эксперимента по влиянию тестируемых ингибиторов PAI-1 на активность PAI-1 на фоне индуцированного воспаления представлены на Фиг. 6.
Полученные данные указывают на достоверное снижение активности фермента PAI-1 у животных, которым было введено соединение формулы (1), по сравнению с животными, получавшими плацебо. Эти данные демонстрируют наличие PAI-1 ингибирующей активности соединения формулы (1) при пероральном введении лабораторным животным, что подтверждает также проникновение соединения 1 из кишечника в системный кровоток и взаимодействие с эндогенным ферментом PAI-1
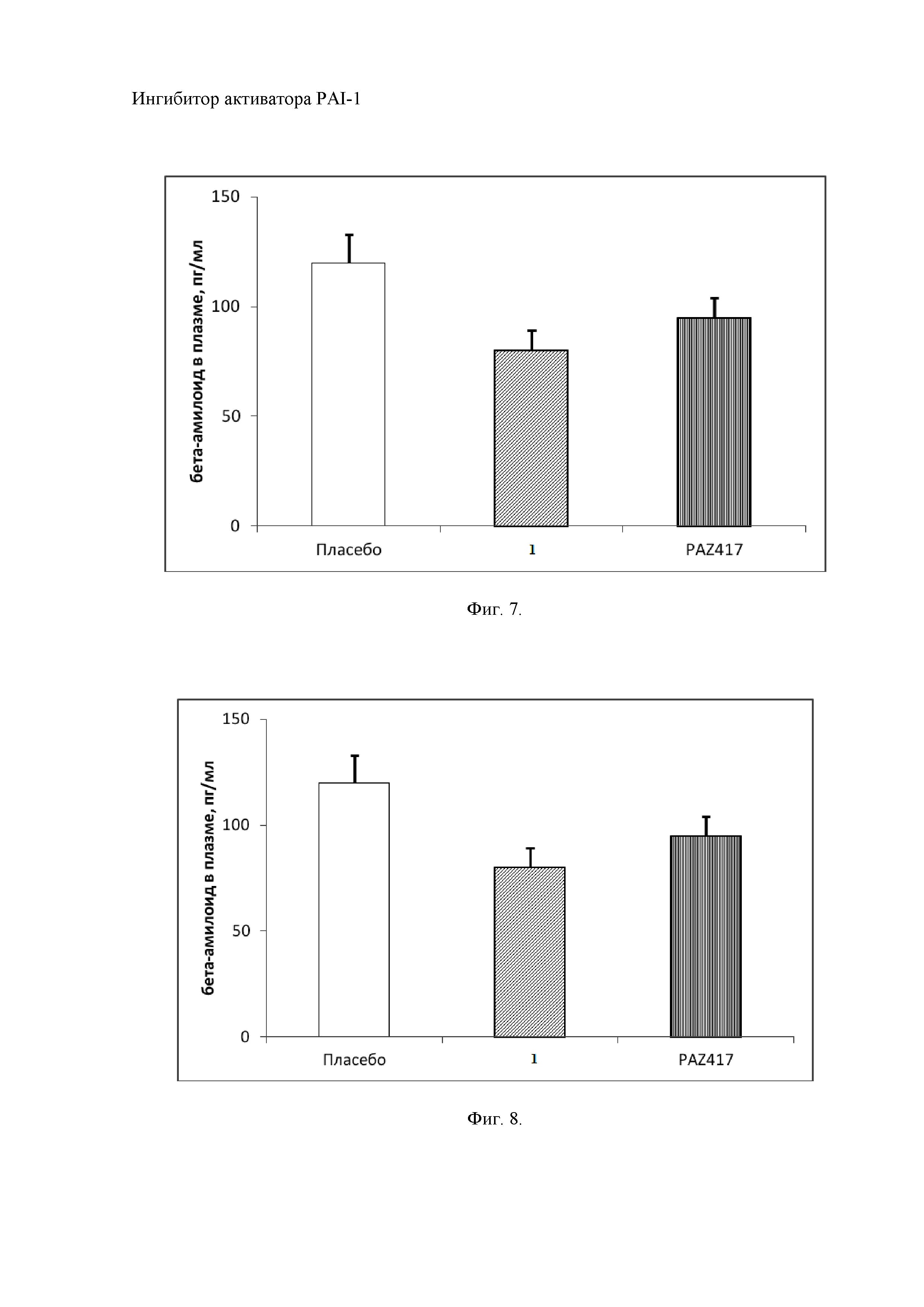
Пример 9. Определение концентрации амилоидного пептида Aβ в плазме и в ткани головного мозга лабораторных морских свинок.
Самцы морских свинок были разделены на три группы. Группе «плацебо» ежедневно в течение недели вводили 1 мл физиологического раствора через желудочный зонд. Группе «1» вводили вещество формулы (1) внутрижелудочно через зонд в течение одной недели в дозе 30 мг/кг в объеме 1 мл. Группе «PAZ-417» в течение недели вводили 30 мг/кг препарата алеплазинин. Анализ содержания β-амилода проводили по окончании введения препаратов в плазме крови и ткани головного мозга.
На фиг. 7 представлена концентрация амилоидного пептида Aβ в плазме лабораторных морских свинок, а на фиг. 8 – концентрация амилоидного пептида Aβ в ткани головного мозга морских свинок.
Как следует из результатов, представленных на фиг. 7. и фиг. 8, снижение концентрации амилоидного пептида Aβ в плазме крови морских свинок (фиг. 7.), а также в ткани головного мозга (фиг. 8.) после введения в течение одной недели соединения формулы 1 в дозе 30 мг/кг выражено достоверно больше, чем после введения алеплазинина в равной дозе. Эксперименты были проведены на морских свинках, поскольку эти животные характеризуются высоким уровнем Аβ в норме и используются в качестве модели для оценки антиамилоидного действия фармакологических веществ. При этом у животных не наблюдается других морфологических изменений, характерных для болезни Альцгеймера, а также отсутствуют клинические проявления, связанные с нарушением когнитивных функций и поведенческих реакций.
Заявленный технический результат достигается также использованием соединения формулы (1) в качестве лекарственного средства, обладающего ингибирующей активностью в отношении ингибитора активатора плазминогена 1-го типа (PAI-1), что достоверно подтверждают эксперименты, проведенные по примерам 8 и 9. Было установлено, что при введении больным животным заявляемого соединения формулы (1) у животных не наблюдается других морфологических изменений, характерных для болезни Альцгеймера, а также отсутствуют клинические проявления, связанные с нарушением когнитивных функций и поведенческих реакций.
Фармакологическую эффективность заявленного соединения формулы (1) на трансгенных мышах линии B6C3-(APP695)85DboTg (PSEN1) оценивали методом условной реакции пассивного избегания (УРПИ).
Пример 10.
Оборудование. Для обучения и тестирования УРПИ использовали челночную камеру (Ugo Basile, Италия), которая состояла из двух отсеков с непрозрачными стенками: темного и светлого. У темного отсека были черные стенки и крышка, у светлого отсека стенки были белыми, а крышка – прозрачной. Отсеки были разделены непрозрачной перегородкой, в которой было отверстие с раздвижными дверцами. Пол в камере представлял собой ряд поперечных металлических прутьев, на которые мог подаваться постоянный электрический ток.
Обучение (выработку) УРПИ проводили в 1-й день исследования. Тестирование сохранности памяти мышей проводили через 24 ч (2-й день) и 48 ч (3-й день) после обучения. Каждое животное помещали в светлый отсек головой к стене, противоположной отверстию, ведущему в темный отсек. Дверцы между отсеками были открыты. В течение 5 мин регистрировали время до захода в темный отсек – латентный период (сек). Как только животное оказывалось в темном отсеке, дверцы закрывали, и в течение 3 секунд на пол подавали ток 0,6 мА. После этого животное возвращали в жилую клетку.
Тестирование состояния памяти мышей. Каждое животное помещали в светлый отсек челночной камеры. Дверцы между отсеками были открыты. Электрический ток на пол установки не подавали. В течение 5 мин регистрировали латентный период (сек) до захода в темную камеру. Результаты обучения и тестирования УРПИ мышей линии B6C3-(APP695)85DboTg (PSEN1) после введения ингибиторов PAI-1 в дозе 30 мг/кг представлены в таблице 2. Достоверное увеличение длительности латентного периода по сравнению с контролем указывает на улучшение функции долговременной памяти у лабораторных животных. Эффект соединения формулы (1) достоверно, в среднем на 25-29%, превышал эффект алеплазинина Различия между измеряемыми показателями в группах «1» и «алеплазинин» были признаны достоверными (таблица 2).
Таким образом, на модели трансгенных мышей линии B6C3-(APP695)85DboTg (PSEN1), являющейся одной из животных моделей болезни Альгеймера, результаты оценки действия соединения формулы (1) показали достоверное наличие фармакологической эффективности, которая провалялась в достоверном увеличении латентного периода при проведении тестировании методом условной реакции пассивного избегания. Следовательно, соединение формулы (1) может использоваться в качестве лекарственного средства для лечения заболеваний, обусловленных повышенным уровнем активатора PAI-1.
Соединение формулы (1) - 6-(2,6-дихлорфенил)-2-хлор-5,6,6a,7,8,9,10,10a-октагидро-7,10-метанофенантридин-4-карбоновая кислота по настоящему изобретению ингибирует активность PAI-1. Термин "ингибировать" означает способность уменьшать активность одного или нескольких членов семьи PAI-1. Соответственно, соединение формулы (1) может быть использовано в способах ингибирования активности PAI-1.
В соответствии с настоящим изобретением соединение формулы (1) может действовать в качестве ингибитора одной или нескольких PAI-1.
В соответствии с настоящим изобретением соединение формулы (1) может быть использовано для ингибирования активности PAI-1 у пациентов, которые нуждаются в такой модуляции рецептора, путем введения ингибирующего количества соединения формулы (1).
Заявленный технический результат настоящего изобретения достигается также способом лечения заболеваний или расстройств у пациентов, связанных с PAI-1, путем введения пациенту, нуждающемуся в таком лечении, терапевтически эффективного количества соединения по настоящему изобретению или его фармацевтической композиции.
PAI-1-связанное заболевание может включать в себя любое заболевание, расстройство или состояние, непосредственно или косвенно связанные с экспрессией или активностью PAI-1, в том числе гиперэкспрессией и/или аномальным уровнем активности. PAI-1-сопутствующее заболевание может также включать любое заболевание, расстройство или состояние, которое может быть предотвращено, облегчено или вылечено путем модуляции PAI-1 активности.
Фармацевтическая композиция для лечения PAI-1 связанных заболеваний у млекопитающих, включающая в качестве активного ингредиента органическое соединение формулы (1) по п.1 в терапевтически эффективном количестве и, по меньшей мере, один из компонентов, выбранных из группы, состоящей из фармацевтически приемлемых и фармакологически совместимых наполнителей и/или растворителей.
Активный ингредиент означает физиологически активное вещество синтетического или иного (биотехнологического, растительного, животного, микробного и прочего) происхождения, обладающее фармакологической активностью и являющееся активным началом фармацевтической композиции, используемой для производства и изготовления лекарственного препарата (средства). В рамках заявленного изобретения активным ингредиентом является – соединение формулы (1).
Единичная доза фармацевтической композиции содержит от примерно 5 мг до примерно 1000 мг, обычно примерно от 100 мг до примерно 500 мг, активного ингредиента, сокединения формулы (1). Термин "единичные дозы" относится к физически дискретным единицам, пригодным в качестве единичных доз для человека и других млекопитающих, причем каждая единица содержит заданное количество активного материала, рассчитанное на получение желаемого терапевтического эффекта, в сочетании с подходящим фармацевтическим наполнителем или растворителем.
В качестве фармацевтического растворителя могут использоваться, в частности, являются вода, этанол, полиспирты, хлорбутанол, пропиленгликоль, а также их смеси, растительные масла (такие, как оливковое масло) и инъекционные органические сложные эфиры (такие, как этилолеат).
В качестве фармацевтического наполнителя могут использоваться, в частности, лактоза, молочный сахар, цитрат натрия, карбонат кальция, фосфат кальция, лактоза, крахмал, тальк.
Список выше перечисленных наполнителей, никоим образом, не ограничивается этими соединения, в зависимости от системного лечения они могут быть другими.
Для приготовления лекарственного препарата в виде суспензии применяют суспендирующие агенты, например, этоксилированный изостеариловый спирт, полиоксиэтилен, сорбитол и сорбитовый эфир, микрокристаллическая целлюлоза, метагидроксид алюминия, бентонит, агар-агар, трагакант, а также смеси этих веществ. Защита от действия микроорганизмов может быть обеспечена с помощью разнообразных антибактериальных и противогрибковых агентов, например, таких как, парабены, хлорбутанол, сорбиновая кислота и подобные им соединения. Композиция может включать также изотонические агенты, например сахара, хлористый натрий и им подобные. Пролонгированное действие композиции может быть обеспечено с помощью агентов, замедляющих абсорбцию активного начала, например моностеарат алюминия и желатин.
Фармацевтические композиции могут быть изготовлены в форме таблеток, пилюль, порошков, лепешек, облаток, эликсиров, суспензий, эмульсий, растворов, сиропов, аэрозолей (как твердое вещество или в жидкой среде), мазей, содержащих, например, до 10% по весу активного соединения, мягких и твердых желатиновых капсул, суппозиториев, стерильных инъекционных растворов и стерильно упакованных порошков.
Ниже изобретение будет описано более подробно с помощью конкретных примеров, которые представлены с целью иллюстрации и не предназначены для ограничения изобретения каким-либо образом. Специалисты в данной области техники легко поймут различие некритических параметров, которые могут быть изменены или модифицированы, чтобы получить те же результаты. Указанное вещество является новым соединением, синтез которого по результатам обзорного поиска не описан в литературе.
Способ получения фармацевтических композиций и лекарственных форм иллюстрируется следующими примерами.
Пример 11. Получение лекарственного средства в форме таблеток. Смешивают 1600 мг крахмала, 1600 мг измельченной лактозы, 400 мг талька и 1000 мг соединения формулы (1) и спрессовывают в брусок. Полученный брусок измельчают в гранулы и просеивают через сита, собирая гранулы размером 14-16 меш. Полученные гранулы прессуют в таблетки пригодной формы весом 500 мг каждая.
Пример 12. Получение лекарственного средства в форме капсул.
Соединение формулы (1) тщательно смешивают с лактозой в соотношении 2:1. Полученную порошкообразную смесь упаковывают по 600 мг в желатиновые капсулы подходящего размера.
Пример 13. Получение лекарственного средства в форме композиций для внутримышечных, внутрибрюшинных или подкожных инъекций.
Смешивают 500 мг соединения формулы (1), 300 мг хлорбутанола, 2 мл пропиленгликоля и 100 мл воды для инъекций. Раствор фильтруют и помещают в 1 мл в ампулы, которые укупоривают.
Из приведенного выше описания специалистам в данной области техники очевидны различные модификации изобретения в дополнение к описанным здесь.
Таким образом, в заявленной группе изобретений представлено новое, ранее неописанное в литературе соединение, обладающее ингибирующей активностью в отношении ингибитора активатора плазминогена 1-го типа, раскрыт способ его получения и предложено использование нового ингибитора и фармацевтических композиций, включающих заявленное соединение в качестве активного ингредиента, для лечения и профилактики связанных с болезнью Альцгеймера заболеваний сердечно-сосудистой системы, сопровождающихся повышенным тромбообразованием.