Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ СТАНДАРТНОГО ОБРАЗЦА МАГНИТНОГО СОРБЕНТА ДЛЯ КОНСТРУИРОВАНИЯ МЕДИЦИНСКИХ ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ
Вид РИД
Изобретение
Изобретение относится к биотехнологии, иммунологии и микробиологии и может быть использовано при конструировании медицинских иммунобиологических препаратов (МИБП) для диагностики особо опасных и других инфекций, а также в опытно-конструкторской экспериментальной работе.
Известен метод получения магнитных сорбентов на основе растворов сульфата железа - FeSO4×7Н2О (II), водного раствора аммиака - NH4OH и сернокислого железа, при котором оксид железа приобретает переменную валентность и магнитные свойства в завершение химических реакций. Мелкодисперсные магнитные частицы с размером 0,5 мкм имеют кристаллическую структуру шпинели с довольно высоким уровнем гидрофильности, инертны и могут включаться в гранулы полиакриламида [1].
Недостатком вышеприведенного метода получения магнитных частиц является необходимость использования химических реактивов и возможность их нестабильного включения в полиакриламидные гранулы, а также необходимость дополнительной обработки агаром, агарозой или желатином для повышения эффективности их включения в гранулы. Кроме того, магнитные частицы оксида железа перед включением в микрогранулы с целью предотвращения образования конгломератов требуют размагничивания.
Известен также способ получения магноиммуносорбента (МИС) для обнаружения бактериальных антигенов, включающий синтез магнитных латексов в присутствии коллоидно-дисперсных ферромагнитных частиц оксида железа. При этом оксид железа вводят в микросферы полиакролеиновых сорбентов путем их последовательной обработки 25-35%-ными растворами сульфата железа (II) в течение 48±2 часов и 20-25%-ными водными растворами аммиака в течение 48±2 часов, при этом объемы суспензии латексов и обрабатывающих жидкостей составляют 1:4-1:5 [2].
Недостатком приведенного способа получения МИС, включающего придание магнитных свойств микросферам латексов за счет оксида железа, является необходимость использования более 4-5-ти кратных объемов растворов реагентов сульфата железа (II) и водного раствора аммиака в сравнении с объемами суспензии латексов. Кроме того, вышеприведенный способ придания магнитных свойств латексам является длительным и требует около 96±4 часов, а также в значительной степени ингибирует иммунобиологические свойства конструируемых диагностикумов, а относительно мелкие размеры использованных микросфер пролонгируют этапы их магнитной сепарации при выполнении исследований.
Известен «Магнитный композиционный сорбент» [3], который содержит полимерное связующее в виде гуминовых кислот и магнитный наполнитель - магнетит с частицами размером 7-30 нм. Массовое отношение магнетита к гуминовым кислотам составляет от 1:4 до 4:1. Эффективность очистки природных водных сред от загрязнений этим сорбентом составляет 97-100% по отношению к экотоксикантам - ионов тяжелых металлов и радионуклидов. Кроме того, авторы вышеуказанного патента отмечают, что размеры частиц синтезированного композита зависят от условий его получения, типа мельницы, времени диспергирования, числа оборотов, количества шаров, соотношения веса шаров к весу образца и содержания компонентов.
Недостатком вышеприведенного способа является использование наноразмерных частиц магнетита и основное его предназначение для очистки природных водных сред от загрязнений. А стандартизация механохимического воздействия в шаровой мельнице при получения сорбента направлена на сохранение размеров магнетита и увеличение эффективности сорбционной емкости в отношении загрязнений. По сути, эта технология полностью не подходит для получения стандартного образца магнитного сорбента.
Известен «Наноразмерный сорбент для сорбции штаммов аэробных микроорганизмов Microccus albus и Pseudomonas putida» [4], который представляет собой суспендированные в воде наноразмерные частицы нестехиометрических кубических феррошпинелей с размерами 3-15 нм повышающие сорбционную способность по отношению к указанным микроорганизмам до 100%. Однако для клеток Pseudomonas putida при исходной их концентрации 124 млн/мл эффективность сорбции составляет 99,99%, т.е. не сорбированными остаются еще 12,4 тыс.микробных клеток. Только в одном примере таблицы 3 авторы показали 100% сорбцию микробных клеток.
Недостатком наноразмерного сорбента является его изначальное предназначение для высокоэффективной сорбции клеток вышеуказанных штаммов из суспензий с концентрацией клеток в пределах 64-124 млн/мл. При этом следует отметить, что предлагаемое изобретение предназначено для обнаружения клеток патогенных микроорганизмов в пределах их концентрации 102-103 м.к./мл, биотехнологическая система диагностической реакции включает в качестве основного природного сенсора биоспецифические молекулы - антитела с размерами около 20 нм, иммобилизованные на гигантских частицах магнитного сорбента в сравнении с последними.
Известна методика получения аффинных композиционных микрогранулированных сорбентов, представленная в работе Е.В. Алиевой с соавт. [5]. На основе кремнезема-алюмосиликата, 3% водного раствора полиглюкина и магнитного порошка авторы получали аффинные композиционные микрогранулированные магнитные сорбенты (МС) с высокой адсорбционной активностью за счет развитой поверхности и привитого специфического лиганда, что в совокупности приводило к относительной стандартности структурных характеристик, достаточной механической прочности, химической и микробиологической устойчивости; магнитная метка обеспечивала упрощение и удобства манипуляций с сорбентами при проведении анализов.
Недостатками описанного метода приготовления аффинного композиционного микрогранулированного сорбента с магнитными свойствами являются отсутствие жесткого контроля при измельчении высушенного исходного МС и выделение методом рассева фракций с размером частиц 80-120 мкм. Кроме того, не представлены сравнительные результаты адсорбционной активности довольно крупных частиц МС в отношении лиганда, а также не определены уровни удельной намагниченности фракции с вышеуказанными размерами частиц.
Наиболее близким к предлагаемому изобретению является методика сухого размола частиц для оптимизации воспроизведения физико-химических и иммунобиологических параметров при конструировании диагностических препаратов за счет метрологической аттестации удельной намагниченности композиционного органокремнеземного микрогранулированного МС. При измельчении МС планетарной микромельницей методом сухого размола в течение от 1-й до 5-ти минут распределение частиц по размерам, соответственно, составило 6,8±0,5; 4,8±0,5; 3,8±0,5; 3,0±0,3; 2,5±0,3 мкм. Удельную намагниченность каждого размерного пула МС измеряли в таблетках диаметром 4,5 и высотой 4 мм с массой в пределах 55-60 мг, было установлено, что уровни удельной намагниченности не существенно отличались в зависимости от размеров их частиц [6].
Недостатками известной методики являются отсутствие параметров процесса размола микромельницы, связанных с соотношением длины трека качения шаров с диаметром шара, величины центробежного ускорения, а также отсутствие соотношений: объема размольного стакана с объемом исходного образца МС, объема исходной массы измельчаемого МС с объемом шаров, поверхности шаров и поверхности размольного стакана, объема размольного стакана с объемом шаров.
Применение МИС позволяет на этапе подготовки пробы путем многократных промываний сорбента с фиксированным на нем инфекционным агентом освобождаться от всевозможных примесей, тем самым исключая их отрицательное влияние на реакцию, максимально концентрируя искомый патоген, что повышает специфичность и чувствительность методов экспресс-анализа, при этом значительно сокращается время проведения анализов - в 1,5-2 раза (до 1-3 часов).
Целью изобретения является разработка стандартного образца магнитного сорбента (СО МС) путем оптимизации воспроизведения физико-химических и иммунобиологических параметров, установленных в результате метрологической аттестации ингредиентов композиционного органокремнеземного микрогранулированного МС, используемого для конструирования МИБП.
Технический результат изобретения заключается в том, что процесс измельчения исходного МС, который обеспечивали путем его сухого размола с помощью планетарной шаровой микромельницы при длине трека качения шаров диаметром 0,01 м, равной 4,2×102 м, то есть при длине трека качения шаров, превышающей диаметр шара в 4,2×104 раза, и центробежном ускорении 42,3-46,8 «g». При этом соблюдается выдерживание утоняющих параметров размола, выраженных в виде относительных величин соотношений: объема размольного стакана с объемом исходного образца МС 13:1, объема исходной массы измельчаемого МС с объемом шаров не более 2/3, поверхности шаров и поверхности размольного стакана 1:2, объема размольного стакана с объемом шаров 1:8.
Указанный технический результат достигается тем, что физико-химические свойства МС, используемого в реакциях и, в первую очередь, размер частиц играют ведущую роль в скорости реакции, ее точности, воспроизводимости, чувствительности и специфичности.
В связи с чем, именно применение для измельчения исходного магнитного сорбента планетарной шаровой микромельницы «Fritsch Р-7» (Германия) позволило оптимально подобрать параметры размола и сгруппировать пулы А, В, С, D, Е размельченного МС по размерам, в зависимости от длины трека качения шаров. Кроме того, магнитные свойства носителя в соответствии с размерами его частиц неодинаково проявляются в реакциях, с неравнозначной эффективностью управляются постоянным магнитным полем и по-разному влияют на конечные результаты иммунологических реакций.
Одним из основных этапов при получении МС является получение однородной фракции частиц с оптимальными размерами. Распределение частиц МС по размерам, полученным в пулах А, В, С, D, Е при измельчении исходного образца МС на планетарной микромельнице в зависимости от длины трека качения шаров 1,4×102 - 7,0×102 м, составило, соответственно, 6,8±0,5 (А); 4,8±0,5 (В); 3,8±0,5 (С); 3,0±0,3 (D); 2,5±0,3 (Е) мкм. Из частиц вышеотмеченных пулов в специальной матрице с помощью разведенного ацетоном полимерного клея (стандарт ZN-10U-UNR) были изготовлены цилиндрические таблетки диаметром 4,5 и высотой 4 мм с массой 55-60 мг. Для определения удельной намагниченности А/м2/кг использовали вибрационный магнетометр «VSM Lake Shove 7400» (USA) с эталоном «NIST» (USA).
Некоторые отличия пулов частиц МС по массе приводили к снижению управления постоянным магнитным полем более мелких частиц пулов D и Е и значительной пролонгации в манипуляциях, а также более выраженному снижению адсорбционной активности у частиц пулов А, В и Е.
Одним из основных показателей эффективности МС является их адсорбционная емкость. Решение по выбору оптимальной длины трека качения шаров при измельчении и размера частиц МС было сделано после определения их адсорбционных свойств. Результаты приведены в таблице 1.
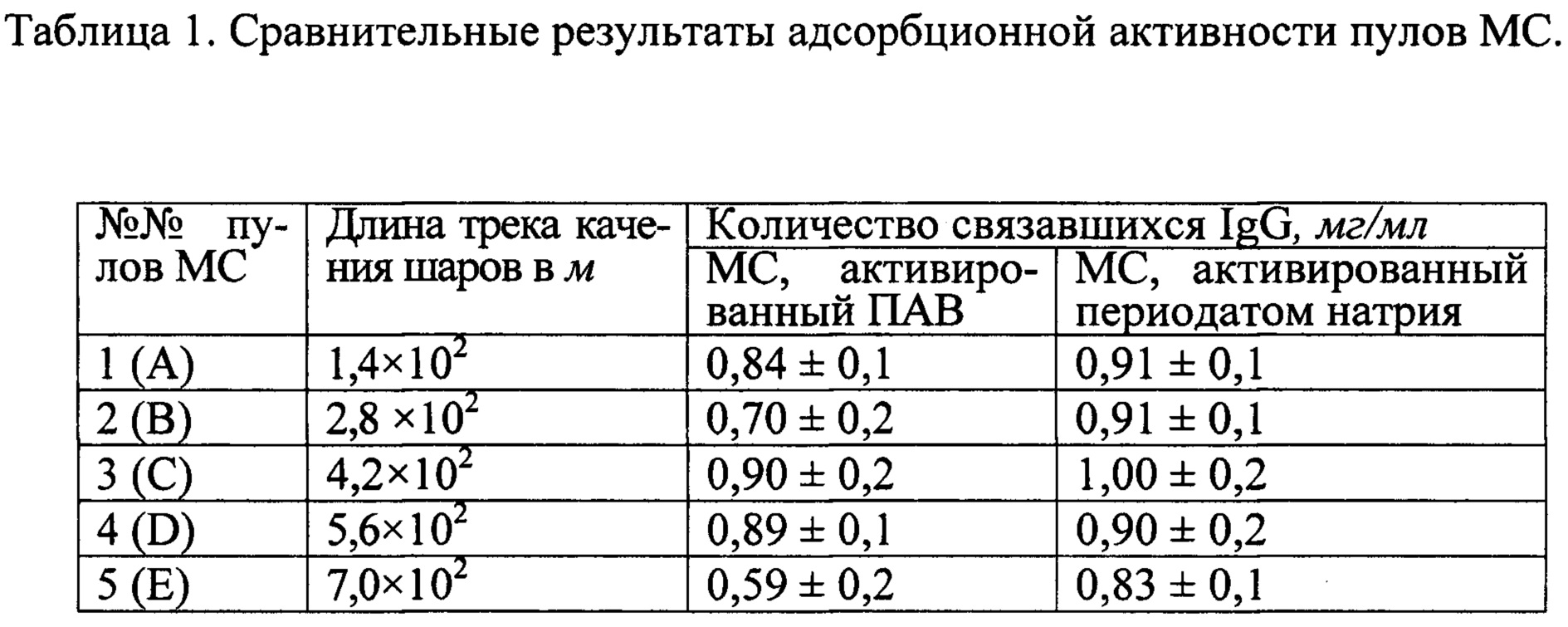
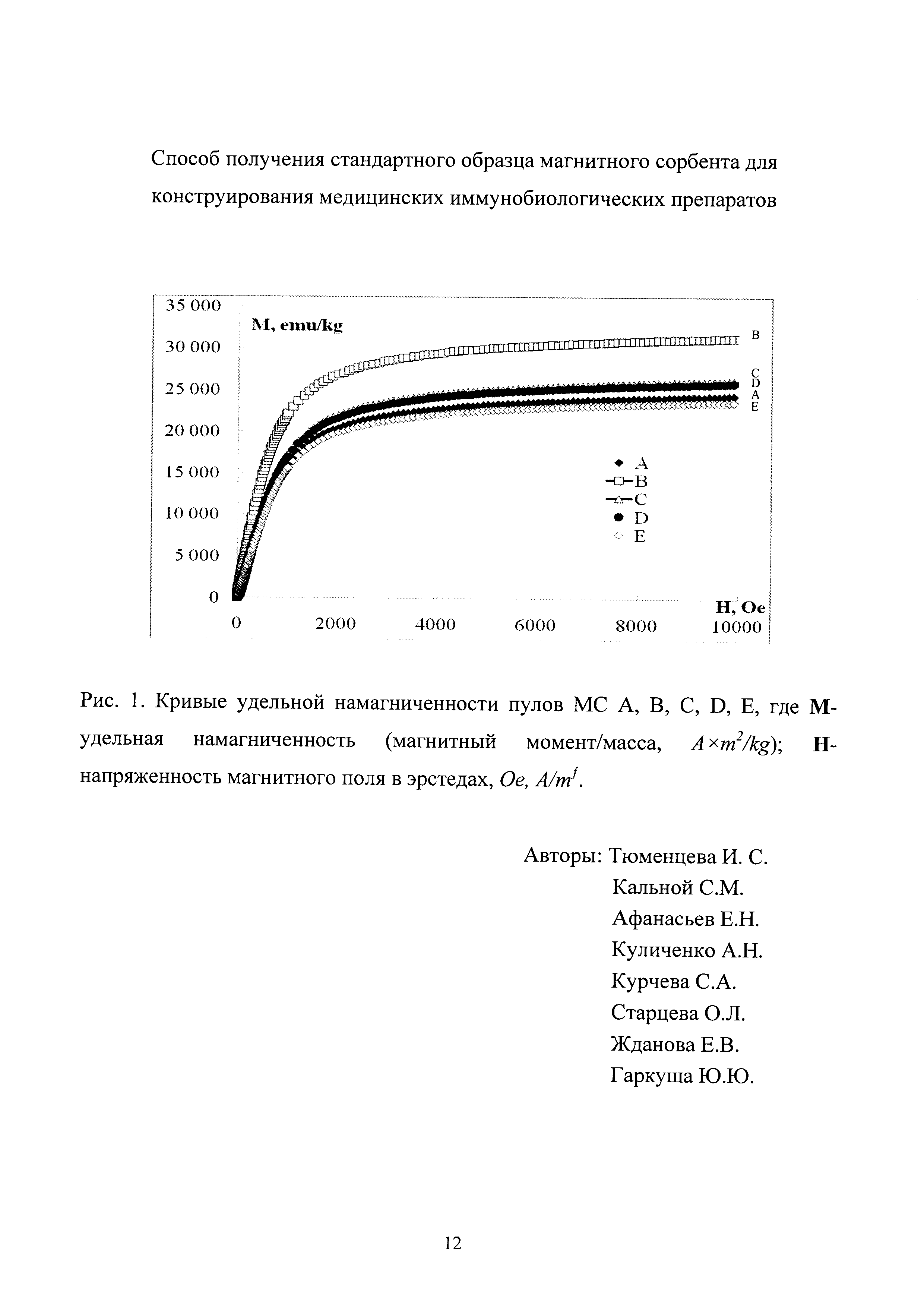
Оптимальными адсорбционными свойствами обладали образцы МС пула С (№3), адсорбировавшие до 1,00±0,2 мг/мл IgG на 1 мл 10% взвеси МС, при иммобилизации в течение 2-х часов с сохранением хорошей магнитоуправляемости. Адсорбционная активность зависит от уровня развитости поверхности МС, аффинности IgG и определяется эффективностью взаимодействия их активных центров с активированной поверхностью частиц. Уровни удельной намагниченности МС показаны на рисунке 1. При этом уровни удельной намагниченности частиц пулов МС А, В, С, D, Е, соответственно, с размерами 6,8±0,5; 4,8±0,5; 3,8±0,5; 3,0±0,3; 2,5±0,3 мкм не существенно отличаются в зависимости от размеров их частиц. Максимальная величина удельной намагниченности частиц пула С (№3) при напряженности поля 104 эрстед составила 26139,189 emu/kg, сопоставима с таковыми у других пулов, однако за счет откалиброванных размеров частиц сохраняется хорошая магнитная управляемость, наряду с адсорбционной активностью. Использование частиц пула С в качестве матрицы позволит получать точные и сопоставимые результаты при производстве диагностических препаратов, что значительно повысит качество разрабатываемых и выпускаемых диагностикумов.
По отношению к прототипу, в качестве которого выбрана методика воспроизведения физико-химических и иммунобиологических параметров при конструировании диагностических препаратов за счет метрологической аттестации удельной намагниченности композиционного органокремнеземного микрогранулированного МС [6], предлагаемый способ отличается:
- позволяет стандартно и конститутивно воспроизводить методику получения твердофазного носителя - СО МС с оптимальными размерами частиц, равными 3,8±0,5 за счет длины трека качения шаров и ее соотношения с диаметром шара 1:4,2×104;
- проводится при центробежном ускорении 42,3-46,8 «g»;
Уточняющие параметры размола выражены в виде относительных соотношений:
- объема размольного стакана с объемом исходного образца МС 13:1;
- объема исходной массы измельчаемого МС с объемом шаров не более 2/3;
- поверхности шаров и поверхности размольного стакана 1:2, объема размольного стакана с объемом шаров 1:8.
При этом уровни удельной намагниченности пулов А, В, С, D, Е частиц МС, определенные вибрационным магнетометром относительно эталона «NIST» (USA), разнились несущественно.
Предлагаемый способ способствует получению стандартных пулов частиц МС с их откалиброванными размерами при производстве МИБП, а также предоставляет возможности научного обоснования взаимодействия иммунобиологических и неорганических носителей (МС) с позиций их размеров и других особенностей реагирующих биологических систем в сравнении с физико-химическими.
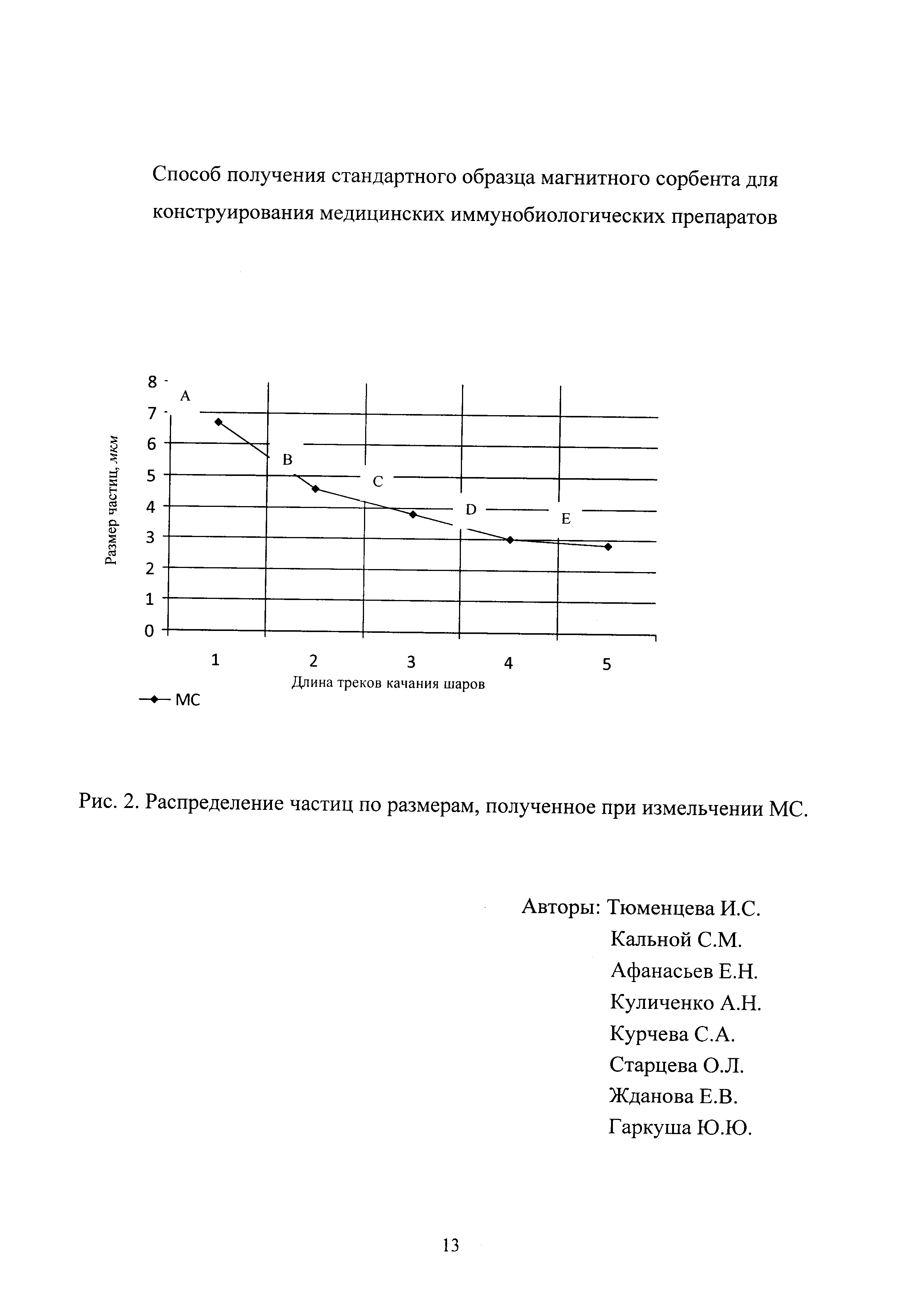
Распределение частиц МС по размерам, полученное в пулах А, В, С, D, Е показано на рисунке 2.
Длины треков качения шаров 1-5 составили 1,4×102 (1); 2, ×102 (2); 4,2×102 (3); 5,6×102 (4); 7,0×102 (5) м, что, соответственно, определило размеры частиц пулов: 6,8±0,5; 4,8±0,5; 3,8±0,5; 3,0±0,3; 2,5±0,3 мкм.
Отличия линейных размеров частиц пулов А, В, С, D и Е соответствуют их отличиям по площади - в квадрате, а по массе или объему - в кубе, то есть, кратность массовых (объемных) отличий пулов возрастает примерно в 20 раз. Эти отличия способствуют негативным проявлениям магнитной управляемости частиц пулов Е и D. Преимущество эффективности использования частиц МС каждого из пулов А, В, С, D, Е, активированных ПАВ или периодатом натрия, определяли на основании специфической сорбции белковых молекул. Лучшие результаты среди вышеуказанных МС продемонстрировал пул С (№3), активированный периодатом натрия с активностью 1,00±0,2 мг/мл.
Системы физических взаимодействий и химических реакций, обладающие новизной, соответствующие изобретательскому уровню и промышленной применимости, при введении их в биологические реакции, утрачивают свои преимущества точности и конкретности. Отмеченные системы в последующих манипуляциях, дезавуируются более сложной и неопределенной динамикой молекулярных белок-белковых взаимодействий, по результатам которой проводится биомедицинская оценка сконструированных частиц СО МС.
Возможность практического использования заявляемого способа подтверждается примерами конкретной иммобилизации туляремийных IgG на частицах полученных пулов МС для их испытания и пригодности конструирования МИБП.
Пример 1. Для конструирования МС использовали алюминий кремнекислый мета, декстран, магнитный компонент - оксид железа FeO, представляющий собой мелкокристаллическое соединение, с выраженными магнитными свойствами. Соотношение ингредиентов синтеза составляло, соответственно, 1:1:2 при времени гелеобразования в течение 2-х часов и рН 7,0. Исходный МС высушивали при 100°С в течение 30 мин. Для получения частиц контролируемого размера измельчение исходной массы МС производили планетарной микромельницей «Fritsch Р-7» (Германия) методом сухого размола при длине трека качения 10-ти шаров диаметром 0,01 м, равной 1,4×102 м, в соотношении МС, составившего 1/13-ю объема размольного стакана объемом 45 мл, диаметром 40 и высотой 40 мм. Размер частиц МС составил 6,8±0,5 мкм. Модифицирование поверхности МС осуществляли алкилсульфатом натрия (ПАВ) путем внесения 7,5 мл дистиллированной воды, содержащей 0,25 мл ПАВ, с экспозицией 2 часа при температуре 37,0±1,0°С. МС отмывали в 100 мл дистиллированной воды и 100 мл забуференного физиологического раствора. Адсорбционную активность МС определяли путем внесения его 10%-ной взвеси в раствор с белковыми молекулами лиганда с концентрацией 2,5 мг/мл в течение 2-х часов в объеме 0,4 мл 10%-ной суспензии МС. Адсорбционная активность частиц МС пула А составила 0,84±0,1 мг/мл IgG.
Пример 2. Отличается от примера 1 тем, что измельчение исходной массы МС производили планетарной микромельницей при длине трека качения шаров, равной 2,8×102 м, размер частиц МС пула В составил 4,8±0,5 мкм. Адсорбционная активность частиц МС пула В составила 0,70±0,2 мг/мл IgG.
Пример 3. Отличается от примера 1 тем, что измельчение исходной массы МС производили планетарной микромельницей при длине трека качения шаров, равной 4,2×102 м, размер частиц МС пула С составил 3,8±0,5 мкм. Адсорбционная активность частиц МС пула С составила 0,90±0,2 мг/мл IgG.
Пример 4. Отличается от примера 1 тем, что измельчение исходной массы МС производили планетарной микромельницей при длине трека качения шаров, равной 5,6×102 м, в течение 4-х минут, размер частиц МС пула D составил 3,0±0,3 мкм. Адсорбционная активность частиц МС пула D составила 0,89±0,1 мг/мл IgG.
Пример 5. Отличается от примера 1 тем, что измельчение исходной массы МС производили планетарной микромельницей при длине трека качения шаров, равной 7,0×102 м, в течение 5-ти минут, размер частиц МС пула Е составил 2,5±0,3 мкм. Адсорбционная активность частиц МС пула Е составила 0,59±0,2 мг/мл IgG.
Пример 6. Отличается от примера 1 тем, что модифицирование поверхности МС осуществляли периодатом натрия, а адсорбционная активность частиц МС размером 6,8±0,5 мкм пула А составила 0,91±0,1 мг/мл IgG.
Пример 7. Отличается от примера 1 тем, что измельчение исходной массы МС производили планетарной микромельницей при длине трека качения шаров, равной 2,8×102 м, модифицирование поверхности МС осуществляли периодатом натрия, а адсорбционная активность частиц МС размером 4,8±0,5 мкм пула В составила 0,91±0,1 мг/мл IgG.
Пример 8. Отличается от примера 1 тем, что измельчение исходной массы МС производили планетарной микромельницей при длине трека качения шаров, равной 4,2×102 м, модифицирование поверхности МС осуществляли периодатом натрия, а адсорбционная активность частиц МС размером 3,8±0,5 мкм пула С составила 1,0±0,2 мг/мл IgG.
Пример 9. Отличается от примера 1 тем, что измельчение исходной массы МС производили планетарной микромельницей при длине трека качения шаров, равной 5,6×102 м, модифицирование поверхности МС осуществляли периодатом натрия, а адсорбционная активность частиц МС размером 3,0±0,3 мкм пула D составила 0,90±0,2 мг/мл IgG.
Пример 10. Отличается от примера 1 тем, что измельчение исходной массы МС производили планетарной микромельницей при длине трека качения шаров, равной 7,0×102 м, модифицирование поверхности МС осуществляли периодатом натрия, а адсорбционная активность частиц МС размером 2,5±0,3 мкм пула Е составила 0,83±0,1 мг/мл IgG.
Таким образом, заявляемый способ практически осуществим, и имеет преимущество, так как обеспечивает получение МС с высокой стандартностью, чувствительностью, воспроизводимостью, стабильностью, демонстративностью регистрируемых результатов реакций, применение которого при разработке новых или выпуске коммерческих препаратов МИБП значительно повысит их биологические характеристики и, как следствие, достоверность результатов проводимых лабораторных исследований.
Список использованной литературы
1. Ефременко В.И. Магносорбенты в микробиологических исследованиях. - Ставрополь:, 1996. - 131 с.
2. Пат. RU №2246968. Опубл. 27.02.2005. Бюл. №6.
3. Пат. RU №2547496. Опубл. 10.04.2015. Бюл. №10.
4. Пат. RU №2545393. Опубл. 27.03.2015. Бюл. №9.
5. Алиева Е.В., Тюменцева И.С, Афанасьев Е.Н., Афанасьев Н.Е., Лаврешин М.П., Афанасьева Е.Е., Орлова Т.Н., Миронов А.Ю. Аффинные сорбенты для экспресс-диагностики заболеваний // Курский научно-практический вестник «Человек и его здоровье», 2008, №1, С. 5-9.
6. Кальной С.М., Куникин С.А., Газиева А.Ю. Физико-химические и иммунобиологические параметры магносорбентов для конструирования диагностических препаратов. Международный научный журнал «Символ науки». 2. 2016. С. 33-35.