Результат интеллектуальной деятельности: СРЕДА ДЛЯ КУЛЬТИВИРОВАНИЯ КЛЕТОК
Вид РИД
Изобретение
Область техники
Это изобретение относится к широкой области биотехнологии, в частности к культивированию клеток и их применению для продукции полипептидов в промышленном масштабе.
Настоящим изобретением обеспечиваются среды для культивирования клеток, которые подходят для культивирования клеток с высокими жизнеспособностями клеток, предпочтительно клеток млекопитающих, подобных клеткам CHO, и которые характеризуются молярным отношением ионов натрия к ионам калия в них. Среды для культивирования клеток в соответствии с настоящим изобретением позволяют достичь высоких продуктивностей полипептидов при использовании для продукции полипептида, в частности, посредством рекомбинантной экспрессии полипептидов в системах культивирования клеток млекопитающих, в частности, в промышленном масштабе.
Предпосылки создания изобретения
Приготовление полипептидов с использованием рекомбинантной технологии превратилось в стандартную процедуру за последние два десятилетия. Обращение к рекомбинантным полипептидам посредством клонирования генов, кодирующих соответствующий полипептид, с последующей трансформацией подходящих для экспрессии хозяев геном, который должен быть экспрессирован, и конечной продукцией и очисткой полученного продукта в виде рекомбинантного полипептида обеспечило доступ к целому новому классу биологически создаваемых и продуцируемых терапевтических средств.
Фармацевтически активные соединения готовились все в большем количестве в фармацевтической промышленности, используя технологию рекомбинантных ДНК, а затем процессы продуцирования, разработанные в области биотехнологии.
Такие биологические продукты включают моноклональные антитела, которые превратились в важные варианты лечения в различных областях медицины, включающих аутоиммунные заболевания, воспалительные нарушения, иммуносупрессию, онкологию или т.п.
Для разработки таких терапевтических средств биологического происхождения необходима продукция в промышленном масштабе, обеспечивающая таким образом доступ к большим количествам рекомбинантного пептида. Предпочтительными системами для экспрессии являются культуры клеток млекопитающих, которые лучше большинства эукариотических систем на основе клеток насекомых, дрожжей или т.п., или даже традиционных прокариотических экспрессионных систем.
Однако культивирование клеток млекопитающих, особенно в промышленном масштабе, присоединяет огромные проблемы. Для производственного оборудования для культивирования клеток млекопитающих требуется тщательная оптимизация многих условий процесса.
Одним из самых важных параметров процесса для контролирования всего процесса продуцирования является среда, в которой выращивают клетки и происходит продукция полипептидов. Подходящие среды для культивирования клеток должны обеспечить культуры клеток всеми необходимыми питательными веществами, что является особенно трудным, если в среды не добавлены компоненты животного происхождения, подобные сыворотке или белкам, например факторы роста.
В результате было разработано огромное множество различных сред для культивирования клеток. В некоторых случаях сосредоточились на общем составе, и были предложены среды с огромным множеством различных веществ (патент США № 5122469, EP 0481791, EP 0283942). В других случаях были предложены конкретные ингредиенты для улучшения культивирования клеток. Основными целями были улучшение или роста, или выживания клеток, или количества и качества рекомбинантно экспрессируемых полипептидов.
Характерными аспектами, рассматриваемыми в документах известного уровня техники, являются, среди прочего, вклад конкретных ионов, содержащихся в следовых количествах (например, WO 02/066603, EP 0872487, EP 1360314 A2), витаминов, таких как аскорбиновая кислота (например, патент США № 6838284), углеводов (EP 1543106) или содержания определенных аминокислот в сочетании с дополнительными особенностями (например, EP 0501435, патент США № 5830761, патент США № 7294484).
Основные ионы и их концентрации в средах для культивирования клеток в основном сохраняют постоянными и остаются не рассматриваемыми и неизменными. Во всех классических типах сред, таких как, например, DMEM, DMEM/F12, BME или RPMI 1640, используются относительно узкие и постоянные диапазоны концентраций основных ионов, в общем, и одновалентных катионов Na+ и K+, в частности. Это находится в соответствии с тем фактом, что ионный баланс основных ионов, в общем, и одновалентных катионов Na+ и K+, в частности, является довольно универсальным свойством почти всех клеток млекопитающих.
Более подробно, основным свойством клеток млекопитающих является трансмембранный градиент ионов натрия и калия с высокой концентрацией ионов калия внутри клетки и высокой концентрацией ионов натрия вне клетки. Натрий-калиевый насос является одним из основных ионных насосов клеточной мембраны, который является электрогенным и вносит вклад в установление и сохранение соответствующего трансмембранного градиента ионов натрия и калия (Kaplan, Membrane cation transport and the control of proliferation of mammalian cells. Annu Rev Physiol.; 40: 19-41 (1978)). Насос использует приблизительно 30% энергии клеток и является одним из основных процессов потребления энергии клеток. С электрохимическим градиентом ионов натрия сопряжены многие основные биохимические процессы, такие как, например, Na+/Ca+ обмен или перенос аминокислот в клетки. Поэтому концентрации ионов натрия и калия вне клетки являются параметрами первостепенной важности, которые влияют на трансмембранный градиент этих ионов и базисное состояние клетки.
В соответствии с типичной концентрацией ионов натрия внутри и вне характерной клетки млекопитающего (Alberts et al., Molecular Biology of the Cell (1994)) обычно выбирают концентрации натрия, составляющие приблизительно 145 мМ, вместе с концентрациями ионов калия, составляющими приблизительно 5 мМ. Для большинства типов сред это приводит к отношению ионов натрия к ионам калия, которое находится в диапазоне приблизительно 20-30 (см. таблицу 1 ниже и, например, патент США № 5135866).
Лишь в немногих документах известного уровня техники описываются среды для культивирования клеток, подходящие для культивирования клеток млекопитающих или продукции рекомбинантных белков, с упоминанием конкретных отношений ионов натрия к ионам калия. В этих документах предлагаются составы сред с удельно высокими отношениями в высокой области - приблизительно 30,7 в патенте США с № 5232848 или в диапазоне от приблизительно 25 до 35, достигая таким образом даже более высоких значений (EP 0283942, EP 0389786). В случае других сред, таких как HAM F12 или среды для культивирования клеток животных с определенным составом, предложенные в заявке на патент США № 2008/0261259, также рекомендуются, в частности, более высокие значения (например, от 27,9 до 57,5 в заявке на патент США № 2008/0261259). Лишь в очень незначительном числе документов описываются среды с отношением ионов натрия к ионам калия, составляющим меньше 20, например 11,5-30 (патент США № 7294484), или отношением, составляющим приблизительно 15 (патент США № 6180401). В этих документах, тем не менее, используются отношения, превышающие 10, а также не приписано особое преимущество изменению этого параметра на значения, упоминаемые здесь.
Помимо эффектов, связанных с ионным балансом между конкретными ионами, также должен учитываться вклад основных ионов в общую осмотическую концентрацию среды. Большинство общепринятых сред, таких как, например, DMEM, MEM альфа или среда Фишера, характеризуется большим количеством хлорида натрия.
В WO 02/101019 рассматривается высокое содержание глюкозы в среде в сочетании с использованием высокой осмотической концентрации. Высокая концентрация глюкозы, составляющая приблизительно 2-40 г/л, была достигнута посредством уменьшения или даже полного исключения таких реагентов, как хлорид натрия, с сохранением таким образом осмотической концентрации на установленном уровне.
Принимая во внимание вышеуказанные проблемы и существующие недостатки, продолжает существовать потребность в области промышленной биотехнологии в улучшенных средах для культивирования клеток, которые позволяют продуцировать рекомбинантные полипептиды в промышленном масштабе.
Краткое изложение сущности настоящего изобретения
Настоящим изобретением обеспечиваются среды для культивирования клеток с уменьшенным отношением Na+/K+, т.е. отношением Na+/K+, меньшим значения, равного приблизительно 10. Этого достигают посредством уменьшения количества суммарных ионов натрия и увеличения общего содержания ионов калия. Было установлено, что при таком низком отношении проявляется несколько положительных эффектов, в частности увеличенная жизнеспособность, рост и продуктивность клеток млекопитающих.
Таким образом, настоящим изобретением обеспечивается среда для культивирования клеток, оптимизированная для выращивания клеток млекопитающих, а также для продуцирования полипептидов, которая характеризуется отношением ионов натрия к ионам калия, которые измеряют как молярное содержание, составляющим от приблизительно 10 к 1 до приблизительно 1 к 1, альтернативно от приблизительно 8 к 1 до приблизительно 6 к 1. Воплощение этого признака может включать концентрации ионов натрия в диапазоне от приблизительно 50 до приблизительно 90 мМ, а ионов калия в диапазоне от приблизительно 8 до приблизительно 12 мМ.
В другом аспекте оптимизация среды для культивирования включает выбор общего содержания аминокислот, находящегося между приблизительно 40 мМ и приблизительно 100 мМ, альтернативно между приблизительно 50 мМ и приблизительно 100 мМ. Этот признак может сочетаться с очень низким молярным отношением общей концентрации ионов к общей концентрации аминокислот, составляющим от приблизительно 1,9 до приблизительно 4.
В дальнейшем аспекте настоящим изобретением обеспечивается способ, в котором среду для культивирования клеток в соответствии с настоящим изобретением используют для культивирования клеток млекопитающих для продуцирования желаемого рекомбинантного полипептида. Способ включает культивирование клеток млекопитающих в среде в соответствии с настоящим изобретением и экспрессию рекомбинантного полипептида.
Некоторые воплощения этого способа включают условия культивирования, при которых температуру и/или pH среды меняют по крайней один раз во время культивирования. В качестве дополнительного варианта осуществляют подпитку с использованием периодического процесса подпитки.
Желаемые, являющиеся полипептидами продукты включают гликозилированные полипептиды и, в частности, антитела и фрагменты антител.
Клетки млекопитающих, используемые в способе настоящего изобретения, предпочтительно выбирают из группы, состоящей из клеток CHO, клеток HEK и клеток SP2/0.
В дальнейшем аспекте настоящее изобретение относится к способу получения среды для культивирования клеток в соответствии с настоящим изобретением, в котором различные компоненты смешивают друг с другом. В частности, концентрация хлорида натрия, добавляемого в состав среды, может находиться в диапазоне от приблизительно 7 до приблизительно 15 мМ. Концентрация хлорида калия, добавляемого в состав среды, может находиться в диапазоне от приблизительно 8 до приблизительно 12 мМ.
Краткое описание чертежей
Настоящее изобретение будет лучше понято, исходя из следующих примеров и фигур. Однако эти примеры не предназначены для ограничения объема настоящего изобретения.
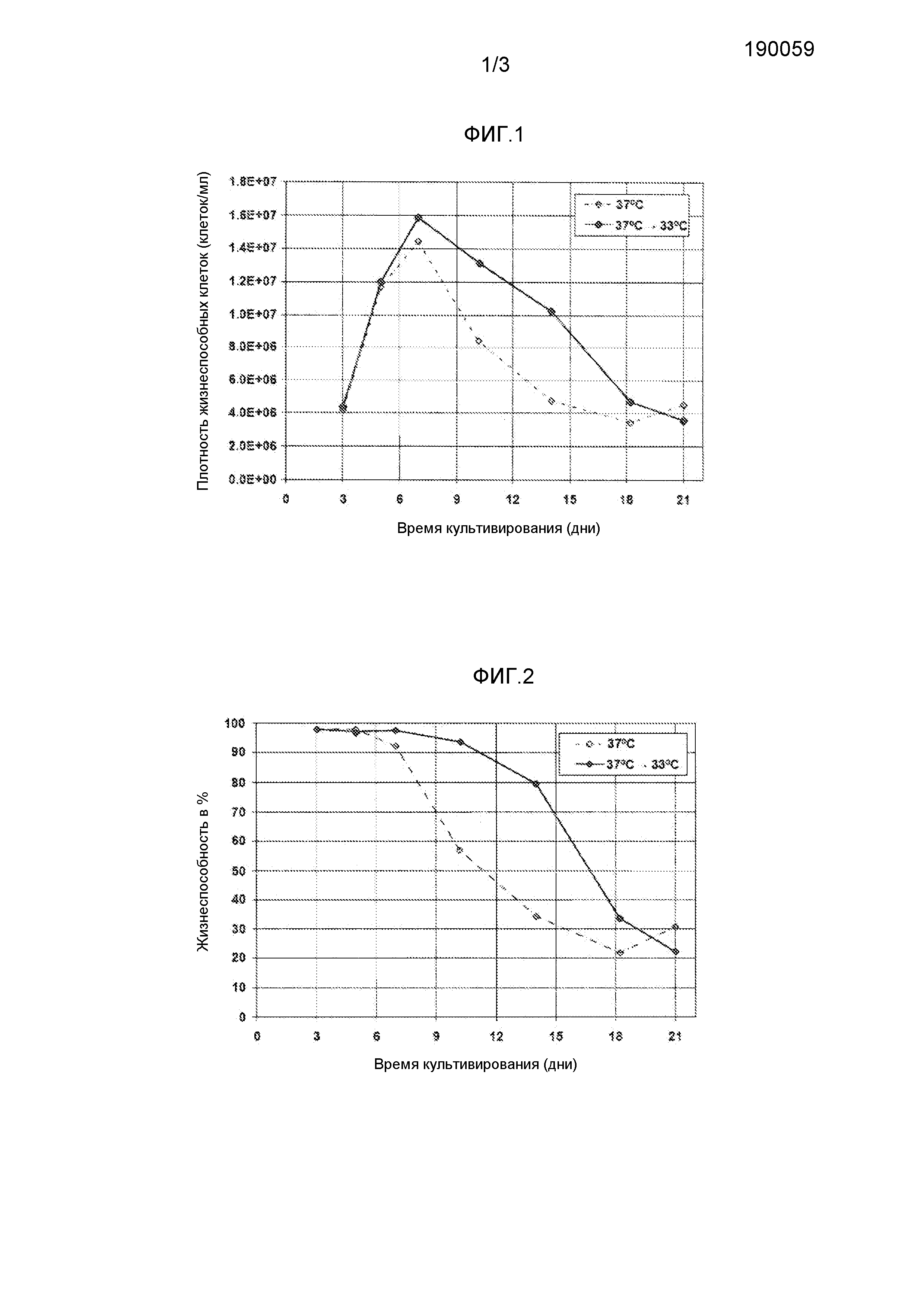
На фиг.1 показана плотность жизнеспособных клеток mAb1-продуцирующего клона клеток CHO в зависимости от времени культивирования в культурах во встряхиваемых колбах (см. пример 1), используя среды с уменьшенным отношением Na+/K+, как описано в настоящем изобретении. Кроме того, отображен эффект постоянной температуры в сравнении с изменением температуры.
На фиг.2 показаны жизнеспособность mAb1-продуцирующего клона клеток CHO (см. пример 1) при использовании среды с уменьшенным отношением Na+/K+ и эффект постоянной температуры в сравнении с изменением температуры в день 3.
На фиг.3 показан титр продукта в зависимости от времени культивирования для культур во встряхиваемых колбах mAb1-продуцирующего клона клеток CHO с изменением температуры и без такого изменения (см. пример 1). Клетки культивировали в среде с уменьшенным отношением Na+/K+ в соответствии с настоящим изобретением.
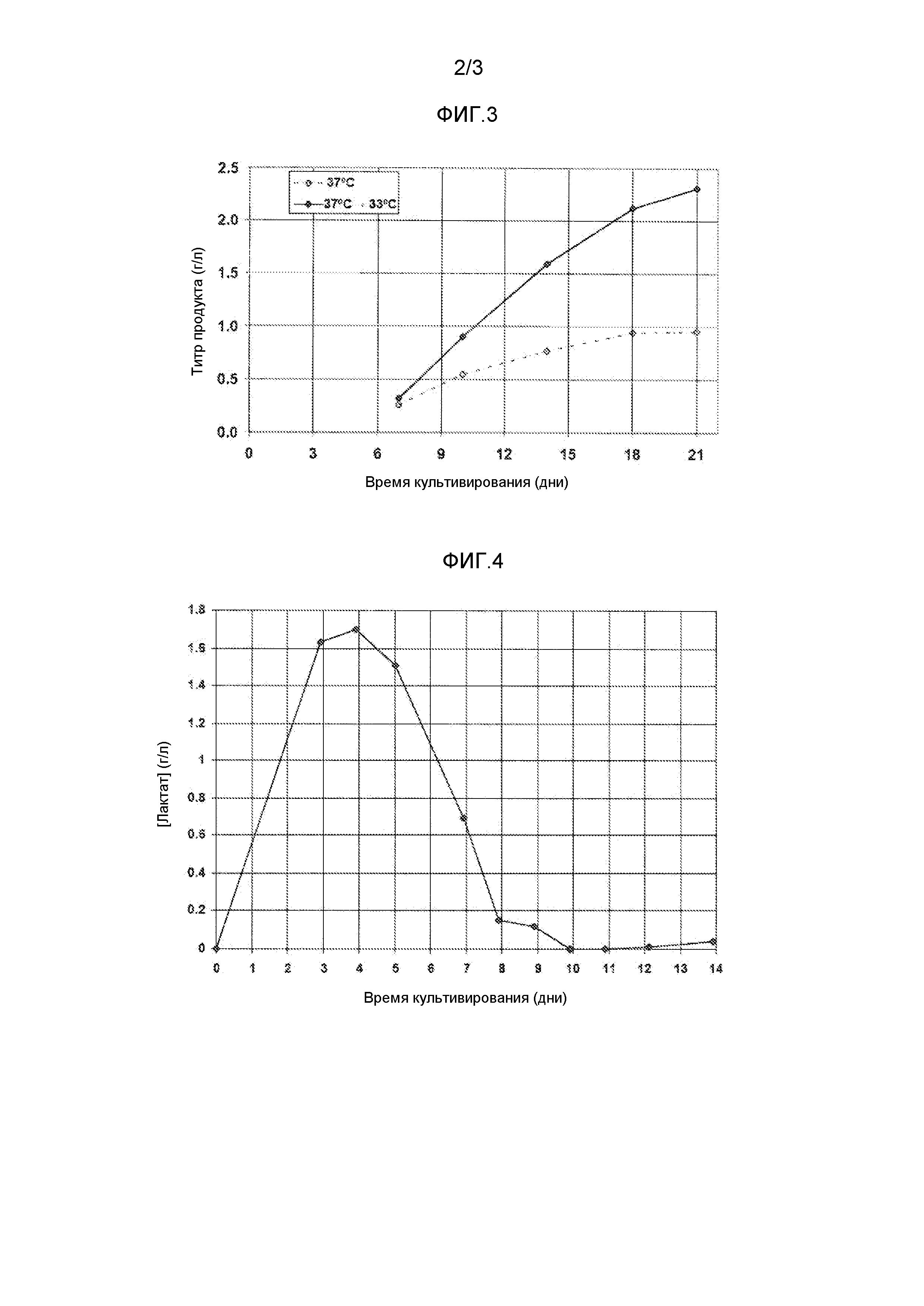
На фиг.4 показана концентрация лактата во время культивирования в mAb2-продуцирующем клоне (см. пример 2). Клетки культивировали в среде с уменьшенным отношением Na+/K+ в соответствии с настоящим изобретением.
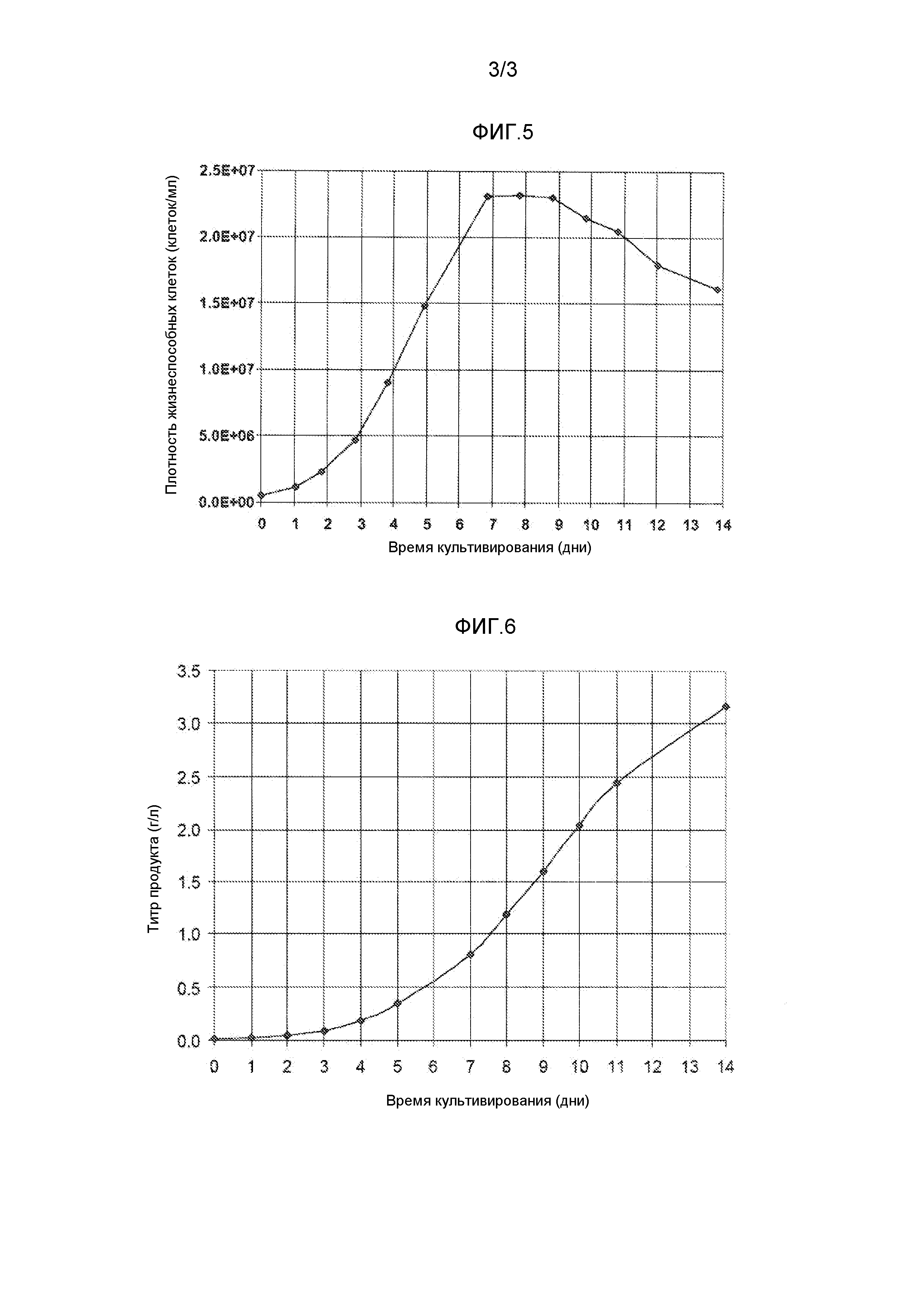
На фиг.5 показана плотность жизнеспособных клеток в зависимости от времени культивирования в биореакторе на 300 л с клоном клеток CHO. Условия культивирования включали стадию изменения температуры (в день 5) и два изменения pH вследствие регуляции pH в зависимости от заданного значения и мертвой зоны (см. также пример 2). Клетки культивировали в среде с уменьшенным отношением Na+/K+ в соответствии с настоящим изобретением.
На фиг.6 показан титр продукта в зависимости от времени культивирования в биореакторе на 300 л с клоном клеток CHO. В способе сочетаются изменение температуры с двумя изменениями pH (см. также фиг.5 и пример 2). Клетки культивировали в среде с уменьшенным отношением Na+/K+ в соответствии с настоящим изобретением.
Подробное описание настоящего изобретения
Среды для культивирования клеток в соответствии с настоящим изобретением используют для выращивания клеток млекопитающих, предпочтительно клеток CHO, клеток HEK и клеток SP2/0, и для продуцирования рекомбинантных полипептидов, используя такие клетки. Клетки CHO являются особенно предпочтительными. Термин «среда для культивирования клеток» относится к водному раствору питательных веществ, который может использоваться для выращивания клеток в течение длительного периода времени. Как правило, среды для культивирования клеток включают следующие компоненты: источник энергии, которым будет обычно углеводное соединение, предпочтительно глюкоза, аминокислоты, предпочтительно базисное множество аминокислот, включающее все незаменимые аминокислоты, витамины и/или другие органические соединения, которые требуются в низких концентрациях, свободные жирные кислоты и неорганические соединения, включающие микроэлементы, неорганические соли, буферные соединения и нуклеозиды и основания.
Среда для культивирования клеток в соответствии с настоящим изобретением может использоваться в различных способах культивирования клеток. Культивирование клеток может осуществляться в адгезионной культуре, например в монослойной культуре, или предпочтительно в суспензионной культуре.
Использование сред для культивирования клеток в области фармацевтической промышленности, например, для продуцирования терапевтически активных рекомбинантных полипептидов не дает, как правило, возможность использовать какой-либо материал биологического происхождения вследствие проблем, связанных с безопасностью и загрязнением. Поэтому средой для культивирования клеток в соответствии с настоящим изобретением является предпочтительно среда, не содержащая сыворотку и/или белки. Термин «среда, не содержащая сыворотку и/или белки» означает среду с полностью определенным химическим составом, не содержащую добавок из являющего животным источника, вроде гидролизатов тканей, например, фетальной бычьей сыворотки или т.п. Кроме того, в культуру клеток в соответствии с настоящим изобретением также предпочтительно не добавляют белки, особенно факторы роста, вроде инсулина, трансферрина или т.п. Предпочтительно среду для культивирования клеток в соответствии с настоящим изобретением также не дополняют источником гидролизованного белка, вроде соевого, пшеничного или рисового пептона или дрожжевого гидролизата или т.п.
Осмотическую концентрацию и pH сред доводят до значений, которые делают возможным рост клеток, например, при значениях, находящихся между приблизительно pH 6,8 и приблизительно pH 7,2. Осмотическая концентрация сред в начале культивирования, как правило, находится между приблизительно 280 и приблизительно 365 миллиосмоль, но она может постепенно увеличиваться во время культивирования и добавления подаваемых растворов до значений, составляющих менее чем или приблизительно 600 миллиосмоль/кг. Предпочтительно, когда среды в соответствии с настоящим изобретением имеют исходную осмотическую концентрацию, находящуюся между приблизительно 285 и приблизительно 365 миллиосмоль/кг.
Температуру культуры клеток выбирают в диапазоне, в котором клетки являются жизнеспособными и растут. Типичная температура для культивирования клеток находится в диапазоне от приблизительно 30°С до приблизительно 38°С. Например, клетки вначале выращивают при температурах, составляющих от приблизительно 36 до приблизительно 37°С, которые являются оптимальными для клеток CHO. Однако точное значение температуры можно подогнать к потребностям клеток, а также изменять во время культивирования для допуска оптимальной жизнеспособности, роста или продукции.
Первый аспект настоящего изобретения связан с ионным балансом между ионами натрия и калия в культуре клеток. В настоящем изобретении описывается молярное отношение ионов натрия к ионам калия, которое находится между приблизительно 10 к 1 и приблизительно 1 к 1. В дальнейших воплощениях настоящего изобретения отношение выбирают между приблизительно 9 к 1 и приблизительно 5 к 1. Альтернативно, отношение находится между приблизительно 8 к 1 и приблизительно 6 к 1.
Концентрацию ионов натрия и калия и соответствующее отношение определяют здесь через их молярное содержание. Концентрацию ионов натрия и калия определяют посредством расчета общего количества этих ионов в среде для роста, после добавления и растворения соответствующих солей в растворе среды.
Для достижения необходимой концентрации натрия обычно в среду добавляют различные соли. Обычно используемыми натриевыми солями являются, например, NaCl, соли одно- или двухосновного фосфата натрия, карбонат натрия, цитрат натрия, ионы в следовых количествах, такие как, например, селенит натрия, но без ограничения этими примерами. Также основание гидроксид натрия (NaOH), которое добавляют в среды для доведения pH, вносит вклад в общее содержание ионов натрия. Термин «ион» в связи с этим относится к диссоциированному состоянию. Расчет молярного содержания ионов, таким образом, означает учет валентности ионов. 1 мМ хлорид натрия (NaCl), добавленный в среду, будет, следовательно, давать концентрацию ионов натрия, равную 1 мМ, в то время как 1 мМ двухосновный фосфат натрия (Na2HPO4) будет соответственно давать концентрацию ионов натрия, равную 2 мМ. В соответствии с настоящим изобретением концентрация ионов натрия, используемая в средах, находится между приблизительно 50 и 90 мМ. Альтернативно, выбирают концентрацию ионов натрия, которая составляет от приблизительно 65 до приблизительно 85 мМ.
Калиевой солью, которую используют для сред, является, как правило, KCl, но она также включает, например, K2SO4 или первичный кислый фосфат калия (KH2PO4). Калиевая соль не ограничивается этими конкретными примерами. Альтернативно, концентрация ионов калия, используемая в средах, находится между приблизительно 8 и приблизительно 12 мМ или составляет приблизительно 10,7 мМ.
В таблице 1 представлены примеры сред, которые традиционно используются для выращивания клеток млекопитающих. Эти классические среды, такие как DMEM, DMEM/F12, BGJ и другие, характеризуются очень высоким отношением ионов Na/K. Среды в соответствии с настоящим изобретением характеризуются очень низким отношением Na/K, составляющим менее чем приблизительно 10 к 1 (см. таблицу 2). Среды в соответствии с настоящим изобретением подходят для культивирования CHO и других клеток млекопитающих и демонстрируют увеличенный рост клеток и/или делают возможной улучшенную продукцию полипептидов. Два примера таких сред представлены в таблице 3, в которой отражен состав двух сред в качестве примеров, и каким образом можно достичь низкого отношения Na/K. Синергетические эффекты между низким отношением ионов натрия к ионам калия и другими особенностями сред оказывают как раз дополнительный положительный эффект на рост клеток и продукцию рекомбинантных полипептидов.
Помимо специфической концентрации ионов натрия и калия и их специфического отношения, среды настоящего изобретения также характеризуются очень низкой концентрацией хлорида натрия (NaCl), который добавляют в смесь компонентов сред. Предпочтительно, когда используют концентрации, составляющие от приблизительно 7 до приблизительно 15 мМ. Такое низкое количество хлорида натрия является необычным. В некоторых воплощениях настоящего изобретения концентрация хлорида натрия (в мМ) даже ниже концентрации (в мМ) соответствующей калиевой соли, которую добавляют. Кроме того, в средах в соответствии с настоящим изобретением часто выявляется низкое общее содержание хлорид-иона. Как показано при помощи примеров таблицы 2, это приводит к исходным концентрациям хлорида, находящимся между приблизительно 36 и 46 мМ. Обычно неорганические соли, такие как NaCl или CaCl2, вносят вклад в это значение, но также компоненты сред, такие как хлорид холина, или аминокислоты, такие как, например, гидрохлорид L-гистидина или гидрохлорид L-лизина, могут прибавлять к общей концентрации.
Дальнейшим преимуществом составов сред в соответствии с настоящим изобретением является сочетание низкого молярного отношения Na/K с исходной концентрацией аминокислот, находящейся в диапазоне от приблизительно 40 мМ, альтернативно приблизительно 50 мМ, до приблизительно 100 мМ. В классических средах используются относительно низкие концентрации аминокислот и/или высокие отношения Na/K. Сочетание обоих признаков может дать дополнительные эффекты, которые являются положительными для роста клеток и продукции полипептидов.
В таблице 2 представлены различные воплощения этих параметров в соответствии с настоящим изобретением. Помимо общего содержания аминокислот в подходящих средах в соответствии с настоящим изобретением, оптимизированных для выращивания клеток, они предпочтительно содержат исходные концентрации аминокислот в соответствии со следующими диапазонами в них.
|
Среды настоящего изобретения, дополнительно определенные аминокислотами, как описано в вышеприведенной таблице, могут с выгодой использоваться в улучшенных способах культивирования клеток в соответствии с настоящим изобретением.
В особенно предпочтительном варианте осуществления среды в соответствии с настоящим изобретением оптимизированы в отношении продукции и предпочтительно содержат исходные концентрации аминокислот в соответствии со следующими диапазонами.
|
Среды для продукции, содержащие аминокислоты, как описано в вышеприведенной таблице, могут с выгодой использоваться в улучшенных способах культивирования клеток в соответствии с настоящим изобретением.
В дальнейшем аспекте настоящего изобретения, помимо специфического отношения ионов натрия к ионам калия, важным также является общий баланс между общими концентрациями ионов (вносящих вклад в общую ионную силу среды) и аминокислот в среде. На соотношение между общей концентрацией ионов и концентрацией аминокислот в питательной среде для роста влияют, главным образом, основные неорганические соли, такие как, например, хлорид натрия, хлорид калия, двууглекислый натрий и другие, которые являются основными ингредиентами большинства типов сред для культивирования клеток животных. Также соли ионов в следовых количествах, аминокислоты или витамины (например, сернокислая медь, L-аргинина гидрохлорид, L-гистидина гидрохлорид, хлорид холина, пантотенат D-кальция и другие) вносят вклад в это значение. Для клеток может быть полезным также регулирование концентраций этих ионов. Поэтому общая концентрация ионов здесь определяется как сумма всех основных органических и неорганических солей, добавляемых в среду, которые являются ионизируемыми в водном растворе среды, плюс основание NaOH и кислота HCl. Элементы в следовых количествах не включаются. Таким образом, 1 мМ каждого из NaCl, NaOH или органических солей, таких как лизина-HCl или хлорид холина, даст концентрацию ионов, составляющую 2 мМ. 1 мМ MgCl2 добавит, соответственно, 3 мМ ионов, в то время как 1 мМ органической соли тринатрия цитрата добавит 4 мМ.
В соответствии с настоящим изобретением молярное соотношение между ионами и аминокислотами выбирают так, чтобы оно находилось между приблизительно 1,9 и 4. В некоторых воплощениях выбирают соотношение, находящееся в диапазоне от приблизительно 2,0 до 3,9. Эти очень низкие соотношения не только достигаются за счет относительно высокого содержания аминокислот, но также за счет относительно низкого молярного содержания ионов в среде. Содержание ионов в среде, как правило, составляет менее 250 мМ. Например, выбирают значения, находящиеся между приблизительно 150 и 220 мМ или альтернативно между приблизительно 170 и 200 мМ.
Таким образом, описанные конкретные особенности сред оказывают значительные эффекты на клеточный метаболизм и физиологию, хотя в то же самое время они также оказывают влияние на общие параметры, такие как осмотическая концентрация, или, например, доступность питательных веществ. Баланс различных особенностей сред приводит, таким образом, к уникальным свойствам, которые приводят к неожиданным синергетическим эффектам по отношению к клеткам.
Среды с низким отношением Na/K, как правило, подходят для выращивания различных клеток млекопитающих и производства рекомбинантных полипептидов/белков при продукции в большом масштабе. Как здесь используются, полипептиды и белки относятся к рекомбинантным полипептидам, которые экспрессируются соответствующей клеткой млекопитающего после трансфекции клеткой ДНК-конструкцией или конструкциями, кодирующей представляющий интерес продукт. Любой полипептид, который может экспрессироваться в клетке-хозяине, можно продуцировать в соответствии с настоящим изобретением. После продукции полипептида(ов) с помощью способа настоящего изобретения он является либо экстраклеточно секретированным, связанным с клетками, либо остается в клетках, в зависимости от конкретного продукта и используемой линии клеток. Являющийся полипептидом продукт можно извлечь из супернатанта культуры сразу же или после лизиса клеток с помощью стандартных процедур. Также осуществляют дальнейшее выделение и очистку с помощью стандартных методов, известных квалифицированному специалисту. Полипептид настоящего изобретения можно также включить в фармацевтическую композицию.
Другой аспект настоящего изобретения относится к способу продуцирования рекомбинантного полипептида, включающему культивирование клеток млекопитающих в среде в соответствии с настоящим изобретением, причем условия культивирования включают по крайней мере одно изменение температуры и/или по крайней мере одно изменение pH.
Соответственно, в другом аспекте настоящего изобретения полезным может быть изменение температуры в ходе культивирования, и оно включает одно или более изменений температуры, которые инициируют в определенные моменты времени. Изменение/сдвиг температуры не относится к спонтанным флуктуациям температуры, а относится к изменениям температуры, составляющим по крайней мере 1°С или альтернативно на по крайней мере 2°С, которые являются умышленными, и при этом вторую температуру сохраняют в течение по крайней мере одного дня. Изменение/сдвиг можно обеспечить посредством изменения заданного значения температуры культуры. Выбор времени зависит от либо состояния наращивания культуры, заранее заданного числа дней после начала культивирования, либо метаболических потребностей клеток. Таким образом, температуру можно изменить в период от приблизительно 1 до 10 дней после начала культивирования. Предпочтительно изменение температуры осуществляют во время фазы роста клетки или к концу этой фазы. В зависимости от объема сосуда для культивирования изменение может происходить быстро или более медленно и длиться несколько часов. В одном примере такое изменение температуры осуществляют во время фазы роста культуры, когда плотность достигает приблизительно 40% - приблизительно 90% от максимальной плотности. В одном примере первая температура находится между приблизительно 33 и приблизительно 38°С, тогда как в других примерах первая температура находится между приблизительно 36 и приблизительно 38°С. Вторая температура находится между приблизительно 30 и приблизительно 37°С или альтернативно между приблизительно 32 и приблизительно 34°С.
В другом аспекте настоящего изобретения полезным может быть изменение pH в ходе культивирования в результате включения одного или более изменений pH. В дальнейших аспектах настоящего изобретения изменения температуры могут также сочетаться с одним или более изменениями pH. Несмотря на то что первый pH (например, pH, равный 7,0) выбирают так, что он был подходящим для быстрого наращивания клеток, полезным является изменение pH культуры после достижения определенной плотности клеток. Это изменение или сдвиг pH осуществляют посредством изменения заданного значения pH в биореакторе/сосуде для культивирования или определения заданного значения pH в сочетании с мертвой зоной. Изменение pH не относится к небольшим флуктуациям pH, а скорее оно относится к умышленному изменению. Второе значение pH (например, 6,8) выбирают для уменьшения гибели клеток и допуска высоких клеточноспецифических скоростей продукции полипептидов соответствующего качества. Второй pH может сохраняться до конца культивирования, или могут быть введены дополнительные изменения pH. В одном воплощении полезным может быть изменение pH на по крайней мере 0,2. В одном варианте осуществления выбирают первый pH, который находится в диапазоне от 6,8 до 7,5. В другом варианте осуществления выбирают первый pH, который находится в диапазоне от 6,8 до 7,2. Второе значение pH, которое достигается после изменения pH, может находиться в диапазоне от 6,0 до 7,5 или альтернативно от 6,5 до 6,8.
Среда для культивирования клеток в соответствии с настоящим изобретением может использоваться в различных способах культивирования клеток. Культивирование клеток может осуществляться в адгезионной культуре, например в монослойной культуре, или предпочтительно в суспензионной культуре.
Культивирование клеток в большом масштабе может использоваться, например, в различных ферментационных способах, широко известных в промышленной биотехнологии. Способы непрерывного или периодического культивирования клеток могут использоваться с использованием сред для культивирования клеток в соответствии с настоящим изобретением. Могут также использоваться другие известные технологии с использованием реакторов, например, перфузионные технологии. Способы периодического культивирования являются одним предпочтительным вариантом.
Культура клеток одного производственного цикла включает подпитываемую культуру или простую периодическую культуру. Термин «подпитываемая культура» относится к культуре клеток, в случае которой вначале в сосуд для культивирования подаются клетки млекопитающих и среда для культивирования клеток, и в культуру непрерывно или по отдельности подаются дополнительные культуральные питательные вещества во время процесса культивирования с периодическим сбором клеток и/или продукта или без него до завершения культивирования. Термин «простое периодическое культивирование» относится к процедуре, в которой все компоненты для культивирования клеток, включающие клетки млекопитающих и среду для культивирования клеток, подаются в сосуд для культивирования в начале процесса культивирования.
В соответствии с одним предпочтительным вариантом осуществления настоящего изобретения подпитку культур осуществляют в способе периодического культивирования с подпиткой. Такая подпитка для восстановления компонентов и питательных веществ сред, истощенных в средах во время процесса культивирования, полезна клеткам. Обычно подаваемые растворы включают аминокислоты, по крайней мере один углевод в качестве источника энергии, микроэлементы, витамины или специфические ионы. Подаваемые растворы добавляют в зависимости от потребностей клеток, что либо основывается на заранее заданном графике, который был определен для конкретной линии клеток или клона клеток и продукта, либо определяется во время процесса культивирования. Особенно предпочтительным является использование концентрированных подаваемых растворов во избежание большого увеличения объема и разведения сред. В некоторых вариантах осуществления полезным может быть также наличие по крайней мере двух различных подаваемых растворов. Это позволяет независимо вводить дозы двух или более различных групп питательных веществ и компонентов в клетки, а следовательно, лучше регулировать условия подпитки, касающиеся оптимальной подачи определенных питательных веществ.
В дальнейшем варианте осуществления настоящего изобретения одним из двух подаваемых растворов, добавляемых в среду для культивирования клеток, является подпитка, включающая дипептид цистин и аминокислоту тирозин. Предпочтительно подпитка содержит дипептид цистин и аминокислоту тирозин в соответствующих концентрациях, находящихся в диапазоне от приблизительно 6,5 г/л до приблизительно 8,0 г/л и в диапазоне от приблизительно 9 г/л до приблизительно 11 г/л, в водном растворе при основном pH, превышающем 10. В конкретном варианте осуществления концентрированная подпитка включает дипептид цистин и аминокислоту тирозин в соответствующих концентрациях, составляющих 10,06 г/л L-тирозина и 7,25 г/л цистина, при pH, превышающем 10.
Подаваемую среду, включающую цистин и тирозин, описанную выше, можно добавлять либо на основе определенного потребления соответствующих аминокислот, либо в соответствии с заданным графиком, например, в количестве приблизительно 0,2 - приблизительно 0,8 вес.% от исходного веса среды для культивирования клеток в день, предпочтительно приблизительно 0,4 вес.% от исходного веса среды для культивирования клеток в день.
В некоторых примерах другой подаваемый раствор содержит все остальные кислоты, которые также присутствуют в основной среде, за исключением тирозина и цистина. В некоторых примерах этот дополнительный подаваемый раствор может состоять из конкретных выбранных компонентов, таких как, например, аминокислоты или углеводы. В дальнейшем предпочтительном варианте осуществления настоящего изобретения эта концентрированная подаваемая среда предпочтительно содержит выбранные аминокислоты в соответствии со следующими диапазонами концентраций.
|
Предпочтительно в эту концентрированную подаваемую среду добавляют также углеводы, такие как глюкоза, при этом предпочтительные концентрации находятся между приблизительно 1200 и приблизительно 1400 ммоль/л или альтернативно между приблизительно 1300 и приблизительно 1395 ммоль/л.
Подаваемую среду, только что описанную, предпочтительно включающую углевод, такой как глюкоза, можно добавлять либо на основе определенного потребления соответствующих аминокислот, либо в соответствии с заданным графиком, например в количестве приблизительно 1 - приблизительно 4 вес.% от исходного веса среды для культивирования клеток в день, предпочтительно приблизительно 2 вес.% от исходного веса среды для культивирования клеток в день.
Клетки, культивируемые в среде для культивирования клеток в соответствии с настоящим изобретением, включают клетки млекопитающих и не млекопитающих. Клетки не млекопитающих включают клетки насекомых или т.п. Однако предпочтительными являются клетки млекопитающих. Термины «клетка», «линия клеток» и «культура клеток» могут использоваться здесь взаимозаменяемо.
Примеры клеток млекопитающих включают ретинобласты человека; клетки карциномы шейки матки человека, линию клеток почки человеческого эмбриона, клетки легкого человека, клетки печени человека, клетки PER.C6 (линию клеток, происходящих из ретинобластов человека), линию клеток гепатомы человека и линии клеток человека, такие как AGE1.HN; линию CV1 клеток почки обезьяны, трансформированную SV40; клетки почки обезьяны, клетки почки африканской зеленой мартышки, клетки яичника китайского хомячка/-DHFR, клетки почки детеныша хомячка; клетки Сертоли мыши; клетки опухоли молочной железы мыши, клетки почки собак; клетки печени крыс линии Буффало; клетки TRI; клетки MRC 5; клетки FS4; клетки CHO являются предпочтительной линией клеток для осуществления на практике настоящего изобретения.
В одном предпочтительном варианте осуществления настоящего изобретения эти клетки могут быть различными линиями клеток CHO, такими как CHO K1 дикого типа, CHO dhfr- (Dux1) или CHO dhfr- (DG44), а также клетками HEK, клетками Sp2/0. Эти клетки, как правило, трансфецируют одной или несколькими ДНК-конструкциями, которые кодируют представляющий интерес полипептид(ы). Любой полипептид, который может экспрессироваться в этих клетках-хозяевах, можно продуцировать в соответствии с настоящим изобретением.
Другой класс клеток, которые могут использоваться со средами для культивирования клеток в соответствии с настоящим изобретением, включает гибридомные клетки, которые обычно используются для продуцирования моноклональных или поликлональных антител.
Полипептиды, которые можно продуцировать благодаря культурам клеток и средам для культивирования клеток в соответствии с настоящим изобретением, не ограничиваются. Полипептиды могут быть рекомбинантными или не рекомбинантными. Используемый здесь термин «полипептид» включает молекулы, составленные из цепи более чем двух аминокислот, соединенных пептидными связями; молекулы, содержащие две или более такие цепи; молекулы, включающие одну или более таких цепей, которая(ые) является дополнительно модифицированной, например, в результате гликозилирования. Термин «полипептид», как предполагается, включает белки.
Предпочтительным классом полипептидов, продуцируемых с использованием культур клеток и сред для культивирования клеток в соответствии с настоящим изобретением, являются рекомбинантные антитела.
Термин «антитело» используется в самом широком значении и, в частности, охватывает моноклональные антитела (в том числе полноразмерные моноклональные антитела), поликлональные антитела, полиспецифические антитела (например, биспецифические антитела), нанотела, модифицированные антитела, субъединицы антител, производные антител, искусственные антитела, комбинации антител с белками и фрагменты антител, достаточно длинные, чтобы проявлять желаемую биологическую активность. Моноклональные антитела, как здесь используются, могут быть антителами человека.
Однако, используя культуры клеток и среды для культивирования клеток в соответствии с настоящим изобретением, можно также продуцировать полипептиды, отличные от антител, например полипептиды вроде трансмембранных белков, рецепторов, гормонов, факторов роста, протеаз, белков коагуляции и препятствующих коагуляции белков, ингибиторных белков, интерлейкинов, факторов переноса, гибридных белков и т.п.
Продукты, полученные благодаря таким способам культивирования клеток, могут использоваться для приготовления фармацевтических препаратов. Термин «фармацевтический препарат» означает композицию, подходящую для введения млекопитающему, особенно человеку, или адаптированную к нему. Кроме того, белок(и) в соответствии с настоящим изобретением можно вводить вместе с другими компонентами биологически активных агентов, такими как фармацевтически приемлемые поверхностно-активные вещества, накопители, носители, разбавители и наполнители.
В таблице 1 суммированы составы имеющихся в продаже сред и дополнительных сред для культивирования клеток известного уровня техники: значения основываются на опубликованных значениях; добавки, такие как NaOH, не включены, таким образом, в эти значения. Таким образом, концентрация натрия или отношение натрия к калию является довольно заниженной и даже более того, кроме значений настоящего изобретения.
|
В таблице 2 приведены составы сред для культивирования клеток в соответствии с настоящим изобретением, характеризующиеся очень низким отношением ионов натрия к ионам калия.
|
В таблице 3 приведены составы примеров для сред с определенным химическим составом для культивирования клеток в соответствии с настоящим изобретением. Отдельные компоненты этих сред для культивирования клеток доступны из стандартных коммерческих источников.
|
Примеры
В описываемых ниже примерах используются среды 1 и 2 с определенным химическим составом для культивирования клеток, имеющие состав, детализированный в таблице 3 выше. Отдельные компоненты этих сред для культивирования клеток доступны из стандартных коммерческих источников.
В таблице 4 ниже представлен состав концентрированной подаваемой среды, содержащей L-тирозин и цистин. Подаваемую среду можно добавлять либо на основе определенного потребления соответствующих аминокислот, либо в соответствии с заданным графиком, например, в количестве приблизительно 0,4 вес.% в день.
|
В таблице 5 ниже представлен состав приведенной в качестве примера, концентрированной подаваемой среды. Подаваемую среду можно добавлять либо на основе определенного потребления аминокислот, либо в соответствии с заданным графиком, например, в количестве приблизительно 2 вес.% в день.
|
В случае экспериментов примеров используют родительскую линию клеток CHO, полученную из линии dhfr (+) CHO-K1 клеток ATCC CCL-61 (Kao et. al., Genetics, 1967, 55, 513-524; Kao et. al., PNAS, 1968, 60, 1275-1281; Puck et al., J. Exp. Med., 1958, 108, 945-959) в результате адаптации к условиям не содержащих сыворотку, не содержащих белков сред. Трансфицировали две аликвоты этой родительской линии клеток для экспрессии двух различных моноклональных антител mAB1 и mAB2 соответственно.
Пример 1
В примере 1 в содержащие среду 1 культуры в двух встряхиваемых колбах инокулируют параллельно mAb1-продуцирующий клон CHO. Культуры во встряхиваемых колбах инкубируют в термостате с углекислым газом при 37°С. В день 3 одну колбу переносят в термостат с углекислым газом с установкой на 33°С. В обе встряхиваемые колбы сходным образом подают два раствора в качестве подпитки. Подпитку добавляют в соответствии с заданным графиком, с добавлением 0,4% первого подаваемого раствора (таблица 2) и 2% второго подаваемого раствора (таблица 3) в день, начиная со дня 5 и продолжая до конца культивирования.
Изменение температуры до 33°С позволяет дольше сохранить плотность жизнеспособных клеток и жизнеспособность культуры с течением времени (фиг.1 и 2) и достичь более высокого титра продукта (фиг.3) по сравнению с культурой, которую сохраняют при 37°С в течение всего эксперимента. Этот пример демонстрирует пользу осуществления сдвига температуры до 33°С во время процесса продуцирования с использованием культуры клеток на основе линии клеток CHO.
Пример 2
В этом эксперименте в биореактор на 300 л, содержащий среду 2, инокулируют mAb2-продуцирующий клон CHO. В день 5 температуру биореактора сдвигают с 36,5°С на 33°С. Заданное значение pH равно 6,90, а мертвая зона составляет 0,10. В результате культивирование начинают при pH 7,00, pH снижается до 6,80 между днями 2 и 4, а затем он постепенно возвращается к 7,00 вследствие потребления молочной кислоты клетками (фиг.4). Изменение до pH 6,80 позволяет уменьшить добавление основания по сравнению со сценарием с постоянным pH 7,00. Возвращение к pH 7,00 позволяет уменьшить концентрацию CO2 в среде по сравнению со сценарием, в котором pH остается на значении, равном 6,80, после первого изменения. В этом способе, в котором сочетаются изменения температуры и pH, достигают высокой плотности жизнеспособных клеток, и минимизируется уменьшение плотности жизнеспособных клеток с течением времени (фиг.5), позволяя достичь в день 14 высокого титра (фиг.6) продукта соответствующего качества. Подпитку применяют так же, как в примере 1.